Эрадикация хеликобактер пилори у детей схема лечения
Открытие Helicobacter pylori (HР) вошло в десятку ведущих достижений ХХ столетия в гастроэнтерологии наряду с эндоскопией желудочно-кишечного тракта (ЖКТ), компьютерной томографией, открытием НВsА, созданием вакцин против гепатита, трансплантацией печени
Открытие Helicobacter pylori (HР) вошло в десятку ведущих достижений ХХ столетия в гастроэнтерологии наряду с эндоскопией желудочно-кишечного тракта (ЖКТ), компьютерной томографией, открытием НВsА, созданием вакцин против гепатита, трансплантацией печени, применением Н2-гистаминоблокаторов и ингибиторов протонной помпы (ИПП).
H. pylori на сегодняшний день — одна из распространенных инфекций на земле. Получены неопровержимые доказательства, указывающие на связь H. pylori с различной патологией ЖКТ (хроническим гастритом, язвенной болезнью, мальтомой и раком желудка). В последнее время обсуждается роль H. pylori в развитии заболеваний печени, болезни Крона, идиопатической хронической крапивницы.
Хронические воспалительные заболевания верхних отделов пищеварительного тракта (ВОПТ) — это наиболее часто встречающаяся как среди взрослых, так и у детей патология, возбудителем которой в 93,7% случаев является H. pylori [1].
В настоящее время важнейшим направлением детской гастроэнтерологии можно считать поиск лекарственных средств, способствующих эффективному разрешению воспалительных заболеваний гастродуоденальной зоны, ассоциированных с H. pylori. В нашей клинике накоплен 14-летний опыт использования различных антихеликобактерных препаратов и разработаны наиболее эффективные схемы их применения.
В 80-е годы считалось, что для лечения HР-инфекции достаточно включения в схему терапии одного или двух препаратов антихеликобактерной направленности. С этой целью чаще всего применялся коллоидный субцитрат висмута в сочетании с метронидазолом (трихополом) или полусинтетическими антибиотиками пенициллинового ряда в возрастных дозировках курсом лечения 14-28 дней. Подобная схема приводила к эрадикации от H. pylori у 70-80% больных.
Коллоидный субцитрат висмута является основным препаратом для лечения HР-инфекции, который приводит к изменению структуры микроба, его разрушению и ослаблению действия ферментов H. pylori. Трихопол повреждает ДНК бактерии, ингибируя их репликацию. На его активность не влияет рН среды желудка.
В наших исследованиях была показана эффективность применения трихопола в сочетании с коллоидным субцитратом висмута, препятствующим образованию штаммов, устойчивых к трихополу, что подтверждалось и данными других авторов.
Однако уже к 1991 году эффективность эрадикации при использовании моно- и двойной терапии снизилась, чему способствовало бесконтрольное и далеко не всегда оправданное назначение трихопола при лечении гастродуоденальной патологии как у детей, так и у взрослых.
В связи с этим в лечении HР-инфекции стали применять тройную терапию с включением антибиотика. Следует отметить, что коллоидный субцитрат висмута замедляет процессы всасывания некоторых антибиотиков (тетрациклина, амоксициллина), способствуя повышению их концентрации в желудочном содержимом — месте приложения при лечении хеликобактериоза.
В 1992-1994 годах наиболее эффективной схемой лечения, по нашим данным, считалась 10-14-дневная тройная терапия с трехкратным приемом коллоидного субцитрата висмута — 120 мг, метронидазола — 20 мг/кг и флемоксина — 30 мг/кг, которая приводила к эрадикации у 78,3% детей.
Однако и данная схема лечения к концу 1994 года перестала удовлетворять, так как степень эрадикации от ее применения постепенно снижалась и составила всего 46,4%.
С середины 90-х годов в клиническую практику стали широко внедряться высокоэффективные препараты — антибиотики из группы макролидов и ИПП, которые успешно зарекомендовали себя в новых схемах лечения инфекции H. pylori. В 1996 году наиболее эффективной схемой на основе омепразола, применявшейся у взрослых, была признана тройная терапия с трихополом и кларитромицином. Было установлено, что сочетание метронидазола и кларитромицина (500 мг/сутки) уже исходно обладает довольно высокой эрадикационной стойкостью, а добавление в схему лечения омепразола повышает ее на 20%. Это дало основание Маастрихскому консенсусу 2-2000 ввести данную схему в терапию первой линии при лечении H. pylori-инфекции.
Но достижение эффективной эрадикации становится все более трудной задачей. При назначении самых мощных на настоящий момент препаратов для эрадикации уже подразумевается 20% терапевтических неудач, что на практике в наших условиях приводит к еще более низкому результату даже на фоне квадротерапии [2, 5].
Общепризнанной причиной неудачи антихеликобактерного лечения является резистентность H. pylori к антибактериальным препаратам. Многочисленные исследования in vitro показали, что у H. pylori имеется природная резистентность к ряду препаратов, которые с успехом применяются для создания транспортных сред (триметоприм, ванкомицин, полимиксин В, налидиксовая кислота, сульфаниламиды) [3].
Помимо природной резистентности у H. pylori описаны случаи приобретенной резистентности. Она может быть первичной, появляющейся в результате приспособительных реакций этого возбудителя к неблагоприятным воздействиям внешней среды и возникающей в случае приема антибактериальных препаратов, не связанных с инфекцией H. pylori. Вторичная резистентность развивается непосредственно в процессе лечения HР-инфекции.
Среди причин, приводящих к возникновению у H. pylori приобретенной резистентности, необходимо отметить увеличение количества пациентов, которым применяется противохеликобактерная терапия, неадекватность ее проведения (низкие дозы, короткие курсы терапии) и бесконтрольное использование антибактериальных препаратов в популяции.
Из препаратов, применяемых в схемах антихеликобактерного лечения, H. pylori имеет резистентность к метронидазолу, кларитромицину, амоксициллину и тетрациклину.
По данным Л. В. Кудрявцевой и др. (1999) [4], первичная резистентность к метронидазолу обнаружена более чем у 55% изученных штаммов H. pylori, резистентность к макролидам составляет около 14%, но имеет четкую тенденцию к росту.
По нашим данным, у детей резистентность к метронидазолу за последние 2 года стабилизировалась и составляет 27%, а к кларитромицину — 7%. Однако в настоящее время появились штаммы с комбинированной резистентностью к метронидазолу и кларитромицину.
Каков же путь преодоления приобретенной резистентности: исключение этих препаратов из схем лечения или увеличение доз и длительности применения препаратов?
Во-первых, лекарственных средств, обладающих антихеликобактерной направленностью, не так уж и много, чтобы так категорично отказываться от их использования; во-вторых, назначение коротких (3-4 дня) курсов комбинаций антибиотиков в пределах максимально разрешенных доз или удлиненных курсов (до 14 дней), способствующих преодолению резистентности у взрослых, неприемлемо в педиатрии. Определить чувствительность H. pylori к различным препаратам на сегодняшний день в широкой практике сложно из-за технических и экономических трудностей.
Расширить и улучшить возможности эрадикационной терапии возможно двумя путями: первый — это создание схем лечения с использованием новых комбинаций препаратов с антихеликобактерной направленностью; второй — определение зависимости структуры и резистентности патогенов от анамнеза антибиотикотерапии.
Так, опубликованы данные об успешном использовании у детей тройной 7-дневной терапии де-нолом по 120 мг, метронидазолом по 250 мг и фуразолидоном 50 мг в 2 приема за сутки с эрадикацией H. pylori в 94,6% [6].
В нашей клинике проведен анализ эффективности использования у детей тройной терапии трихополом — 20-30 мг/кг в сутки, кларитромицином — 7,5-15 мг/кг в сутки и омепразолом 20 мг в сутки. При 7-дневном курсе лечения по такой схеме частота эрадикации от H. pylori составила 94,4% [7]. Мы предприняли также попытку преодолеть резистентность к метронидазолу и кларитромицину, используя данные препараты в сочетании с де-нолом в общепринятых дозировках у 12 детей с первично выявленной язвенной болезнью двенадцатиперстной кишки. Отбор пациентов в данную группу проводился на основании тщательно собранного анамнеза (отсутствие данных об использовании трихопола в лечении каких-либо инфекций у ребенка). В результате проведенного исследования было выявлено, что эрадикация H. pylori составила 83,35% при 100-процентной репарации язвенного дефекта.
Еще полвека назад существовало несколько теорий, предлагающих свой вариант причин появления язвенной болезни желудка и кишечника. Переломным моментом стал 1979 год, когда в результате научного исследования было доказано, что первоисточник этой проблемы – бактерия хеликобактер пилори (Helicobacter pylori), в норме благополучно существующая в ЖКТ более половины всех представителей человечества. Любое снижение иммунной защиты – благополучный повод для размножения колоний хеликобактер пилори. Для лечения хелиобактериоза созданы схемы эрадикции патогенной бактерии из организма человека.
Схема эрадикционной терапии хеликобактер пилори

При выборе врачом схемы эрадикционной терапии в каждом конкретном случае приходится учитывать следующие факторы:
Прогнозируемая длительность лечения;
Клиническая картина данного случая хелиобактериоза;
Стоимость препаратов, входящих в схему лечения.
Российская Гастроэнтерологическая ассоциация и Российская группа по изучению Helicobacter pylori рекомендует принять за основу комбинированную трехкомпонентную схему терапии, удовлетворяющую следующим принципам:
Способность провести эрадикцию бактерии не менее чем в 80% случаев;
Отсутствие побочных эффектов, вынуждающих лечащего врача отменить схему лечения, или провоцирующих больного на прекращение приема препаратов (допускается до 5% таких случаев);
эффективность даже при коротком курсе не дольше 1-2 недель.
В основе методики назначения эрадикционной терапии лежат рекомендации, выработанные мировым сообществом гастроэнтерологов в Маастрихте в 1996 г., и обновленные в 2000 г.
Рекомендации Второго Маастрихтского соглашения по проведению антихеликобактерной терапии:
При неосложненных случаях язвенной болезни после курса эрадикционной терапии не требуется использование антисекреторных препаратов.
Показания для эрадикционной терапии кроме язвенной болезни: MALT-лимфома, атрофический гастрит, близкие родственные связи с больным раком желудка, состояние после резекции по поводу рака желудка, желание пациента.
Лечение инфекции Helicobacter pylori должно предусматривать возможность неудачи первой линии эрадикционной терапии и необходимость использования второй линии в случае сохранения бактерии в организме. В схему первой линии эрадикции (тройную терапию) предлагается включить 2 антибиотика: Кларитромицин + Амоксициллин (или Метронидазол) и ингибитор протонной помпы (или Ранитидин). Она длится не более 7 дней. При неудаче рекомендуется применять схему второй линии (квадротерапию), включающую в себя 2 антибиотика: Тетрациклин + Метронидазол, препараты висмута и ингибитор протонной помпы. Длительность использования квадротерапии – 7 дней.
В настоящее время в практике не применяются специфические антибактериальные препараты, пробиотики и вакцины, направленные исключительно против Helicobacter pylori, они пока находятся в стадии разработки.
Разработчики Маастрихтских рекомендаций исключили из схемы лечения привычную для России комбинацию: Амоксициллин + Метронидазол + блокатор протонной помпы из-за повышения резистентности Helicobacter pylori к производным нитроимидазолов. Исследования российских ученых подтвердили низкую эффективность этой комбинации (всего 30%). Российские гастроэнтерологи в эрадикционной терапии первой линии часто используют доступную и эффективную тройную терапию, включающую в себя препараты висмута + Амоксициллин + Фуразолидон. Совершенствование антихеликобактерной терапии продолжается, В 2005 году в Нидерландах были разработаны современные схемы эрадикционной терапии первой, второй, третьей линии.
Первая линия эрадикции хеликобактер пилори
Трехкомпонентная схема первой линии получила свое название за то, что она состоит из трех препаратов:
ингибитор протонной помпы на основе Омепразола, регулирующий активность кислой среды желудочного сока.
Ингибиторы протонной помпы позволяют избавиться от множества негативных проявлений язвы и гастрита, вызванных повышенной кислотностью среды желудка, а так же избежать чрезмерно строгих ограничений, вносимых в рацион питания больного язвенной болезнью. Тем не менее, ограничения все-таки сохраняются, хотя и не такие строгие.
Допускается замена Амоксициллина на антибиотик Нифурател или на Метронидазол. По показаниям гастроэнтеролог может назначить в схему 4 препарат, имеющий в основе производные висмута. В норме такие лекарства включают в эрадикционную схему второй линии, но их свойства положительно влияют на течение процесса купирования воспалительного процесса. На поверхности желудка образуется защитное покрытие, снимающее симптомы воспаления и боль.
Облегченная схема для больных пожилого возраста:
Ингибитор протонной помпы;
Для увеличения эффективности стандартной терапии первой линии предлагается удвоить срок ее применения – с 7 до 14 дней. Ожидаемая эффективность – до 95%. При неэффективности лечения врач рекомендует перейти на вторую линию эрадикционной терапии.
Вторая линия эрадикции хеликобактер пилори
Четыре компонента эрадикционной схемы второй линии:
2 антибиотика: Тетрациклин + Метронидазол, или Амоксициллин + препарат из группы нитрофуранов;
Ингибитор протонной помпы;
Препараты на основе висмута – отличные цитопротекторы, восстанавливающие структуру клеток слизистой желудка и кишечника и их устойчивость к агрессивному воздействию кислоты и продуктов жизнедеятельности Helicobacter pylori. Кроме того, они обладают бактерицидным действием, до минимума снижают риск рецидивов хелиобактериоза. При планировании схемы эрадикции второй линии не рекомендуется использовать уже применяемые ранее антибиотики. Эффективная, доступная и дешевая схема квадротерапия с висмутом тоже не лишена недостатков:
Большое количество принимаемых таблеток (18 штук в сутки);
Частые побочные эффекты;
4-х кратный режим дозирования.
Для усиления эффективности терапии препаратами висмута на время лечения из рациона исключают фрукты, соки, молоко. Длительность терапии второй линии – 10-14 дней.
Третья линия эрадикции хеликобактер пилори
Исключительно редко приходится переходить на третью линию эрадикционной терапии, но такая возможность все-таки существует. Перед началом реализации третьей схемы пациента тестируют на чувствительность штамма Helicobacter pylori к антибиотикам.
Препараты 3 линии:
Два антибиотика, не использовавшихся ранее и показавших при лабораторной диагностике наивысшую степень эффективности;
Ингибиторы протонной помпы.
Лекарственные средства на основе висмута (трикалий дицитрат висмута) обладают комплексным действием:
Снимают проявления диспепсии (вздутие живота, изжогу, гастралгию);действуют в отношении Helicobacter pylori, как эффективное бактерицидное средство;
Стимулируют регенерацию повреждений более глубоких слоев стенок желудка.
Терапия третьей линии по Маастрихтским рекомендациям третьего созыва включает препараты из группы рифамицинов (Рифабутин) и хинолонов (Левофлоксацин). Такое сочетание стало эффективным в 91% случаев. Резистентность Helicobacter pylori к Рифабутину очень мала, поэтому его включение в протокол лечения совместно и Амоксициллином и ингибитором протонной помпы позволяет повысить эффективность терапии и даже игнорировать резистентность бактерии к Метронидазолу и Кларитромицину.
Выбор препаратов при необходимости проведения повторного курса эрадикционной терапии
И первая, и вторая, и даже третья схема терапии Helicobacter pylori может быть неэффективной, когда процент эрадикции составляет 80% или менее случаев целевого достижения цели лечения. Эффективность лечения снижается по причине резистентности бактерии к антибиотикам, поэтому исследователи проблемы не прекращают поиск лучших схем.
Не вызывает опасения резистентность Helicobacter pylori к Амоксициллину (менее 1%), к Тетрациклину (близка к 0).
Количество резистентных штаммов бактерии к другим антибактериальным препаратам:
К Кларитромицину – в Европе от 9,9 до 18%, в Москве – 19,3% у взрослых, 28,5% - у детей;
К Метронидазолу – в Европе от 20 до 40%, в Москве - 54,8% у взрослых, 23,8% – у детей
Это объясняется частым назначением антибиотиков из группы макролидов в педиатрической и терапевтической практике. Немаловажное значение в успешности эрадикционной терапии имеют ингибиторы протонной помпы, создающие в ЖКТ благоприятную среду для применения антибиотиков. При низком качестве препаратов этой группы эффективность антибактериальных средств тоже снижается.
Проводятся исследования о добавлении к стандартной терапии пробиотика, позволяющего уменьшить частоту стула и проявления метеоризма.
Появилась новая схема эрадикции бактерии – последовательная терапия, занимающая 10 дней. Ее используют при неудаче использования схемы первой линии.
В первые 5 дней принимают:
Ингибитор протонной помпы – 2 раза в сутки;
Амоксициллин – 2000 мг/сутки.
В следующие 5 дней:
Ингибитор протонной помпы – 2 раза в сутки;
Кларитромицин – 1000 мг/сутки;
Тинидазол – 1000 мг/сутки.
По данным исследования, даже у пациентов, зараженных Helicobacter pylori с высокой резистентностью к Кларитромицину, эрадикция повысилась с 29% до 89%. У остальных больных с неудачной эрадикцией первой линии показатель повысился с 78% до 91%.
Протокол лечения хеликобактер пилори у взрослых
Основные протоколы эрадикции Helicobacter pylori у взрослых, рекомендованные Торонтским и Маастрихтским консенсусом 2016 года:
Открытая в 1982-м австралийцами Б. Маршаллом и Р. Уорреном инфекция Helicobacter pylori является виновницей язвенных болезней различных участков желудка и кишечника. Для борьбы с ней международным медицинским сообществом разработаны различные схемы эрадикационной терапии.
Опасный сосед
В настоящее время не подлежит сомнению высокая степень ассоциации пептических язв с жизнедеятельностью хеликобактер пилори в слизистой желудка. Для лечения используется комплексная эрадикационная терапия – это действия, направленные на полное освобождение от инфекции, которые сводят к минимуму вероятность рецидивирования язв.
В последующие за открытием Н. pylori годы появились сообщения о том, что эта бактерия является этиологическим фактором целого ряда других заболеваний: хронического активного антрального гастрита (типа В), атрофического гастрита (типа А), некардиального рака, MALT-лимфомы, идиопатической железодефицитной анемии, идиопатической тромбоцитопенической пурпуры и анемии, обусловленной дефицитом витамина В12. Продолжается изучение взаимосвязи спиралевидной бактерии с аллергическими, респираторными и другими внежелудочными заболеваниями.
Эрадикационная терапия у детей
Необходимость эрадикации инфекции H. pylori у детей показана в многочисленных клинических исследованиях и их метаанализах, которые послужили основой для составления и регулярного обновления международного согласительного документа, хорошо известного практикующим гастроэнтерологам как Маастрихтский консенсус. В настоящее время вопросы диагностики и лечения хеликобактер-ассоциированных заболеваний регламентируются уже четвертым Маастрихтским консенсусом, принятым в 2010 году.
В развитых странах Европы, Америки и в Австралии, где с момента открытия этиологической роли Н. pylori систематически разрабатывались и внедрялись в практику методы диагностики и лечения данной инфекции, отмечен спад заболеваемости язвенной болезнью и хроническим гастритом. Кроме того, в этих государствах впервые за десятилетия наметилась тенденция к снижению заболеваемости раком желудка, чему также способствует эрадикационная терапия.
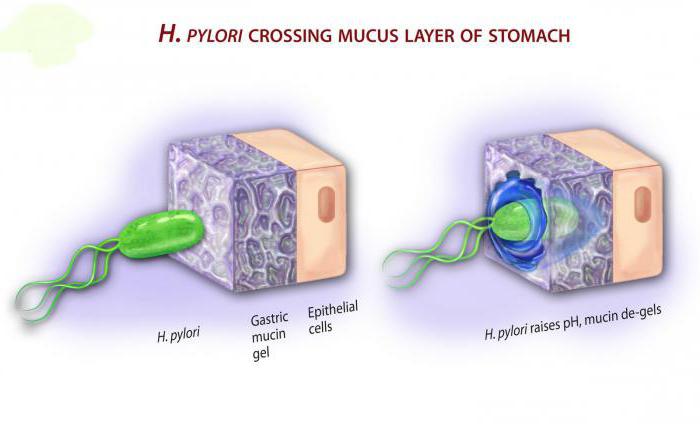
Загадочная бактерия
На основании результатов многочисленных рандомизированных плацебо и сравнительных исследований определена эффективность пробиотических средств при различных клинических ситуациях, в том числе и при хеликобактерной инфекции у детей. Однако, несмотря на некоторые достижения в понимании действия пробиотиков на бактерию H. pylori, ее тонкие механизмы остаются малоизученными.
Основным ингибирующим и бактерицидным фактором Lactobacillus является молочная кислота, которую они производят в больших количествах. Молочная кислота ингибирует активность уреазы H. pylori и, как предполагают, оказывает свое антимикробное действие за счет снижения рН в пространстве люмена желудка. Однако было установлено, что молочная кислота, которая производится клетками слизистой желудка (СОШ), способствует росту колонии H. pylori. Кроме молочной кислоты лактобактерии и некоторые другие пробиотические штаммы продуцируют антибактериальные пептиды.
Комплексная терапия
Эрадикационная терапия при язвенной болезни у детей (как и при гастрите) часто предполагает использование нитроимидазолов, макролидов, лактамов, тетрациклина и нитрофуранов. Хеликобактер вырабатывает устойчивость именно к антибактериальным компонентам, что снижает эффективность эрадикационной терапии. И актуальность этой проблемы растет с каждым десятилетием.
Резистентность к антибиотикам
Выработка устойчивости к антибиотикам – общая черта, присущая всем патогенным микроорганизмам. Это эволюционный механизм, который обеспечивает их выживание в изменяющихся условиях. Резистентность Н. pylori подразделяют на:
Причины устойчивости к лечению
В числе главных причин формирования приобретенной резистентности H. pylori ученые называют:
- Рост назначений антибактериальных препаратов этих же групп по другим показаниям.
- Бесконтрольное самолечение антибиотиками в странах, где они продаются без рецепта.
- Неадекватно назначенная эрадикационная терапия гастрита или язвы (назначение низких доз антибиотиков, сокращение курсов лечения, неправильная комбинация в схеме препаратов).
- Несоблюдение предписаний врача пациентами.
- Появление на фармацевтических рынках препаратов низкого качества.
В результате всего перечисленного рост резистентности H. pylori сокращает и без того ограниченное количество антибиотиков, активных в отношении данного микроорганизма.
Проблема антибиотикорезистентности особенно актуальна для детей, которым показана эрадикационная терапия язвенной болезни. Чаще всего они инфицируются первично резистентными микроорганизмами от родителей и близких родственников.
Кроме того, в детской популяции особенно распространено необоснованное применение антибиотиков для лечения других заболеваний, чаще всего респираторных инфекций, что также способствует селекции первично устойчивых штаммов. Нарушение режима эрадикационной терапии, как и у взрослых, приводит к формированию вторичной резистентности. Развитие устойчивости патогенна также связано с мутациями разных генов хеликобактерии.

Диагностика
Эрадикационная терапия у подростков начинается после всеобъемлющей диагностики. Первичной целью обследования ребенка, у которого наблюдаются гастроинтестинальные симптомы, является определение причины возникновения этих симптомов, а не только наличия H. pylori. При этом проведение тестов на выявление хеликобактера не рекомендуется у детей с функциональной абдоминальной болью. Можно рассмотреть целесообразность проведения тестов на выявление патогена:
- у пациентов, в семейном анамнезе которых есть рак желудка у родственника первой степени родства;
- при рефрактерной железодефицитной анемии (если исключены другие причины заболевания).
Не хватает достаточных практических доказательств причастности H. pylori к среднему отиту, инфекциям ВДП, пародонтиту, пищевой аллергии, синдрому внезапной детской смерти, идиопатической тромбоцитопенической пурпуре, низкому росту. Но подозрения есть.
Диагностические тесты
Эрадикационная терапия при язвенной болезни и гастрите определяется диагностическими тестами. Методика тестирования зависит от многих факторов:
- Для диагностики хеликобактера при проведении эзофагогастродуоденоскопии рекомендуется провести биопсию антрального отдела желудка для дальнейшего гистологического анализа.
- Рекомендуется, чтобы первоначальный диагноз H. pylori был основан на следующих данных: положительное гистологическое исследование и положительный тест на уреазу (как альтернатива – положительные результаты культурального исследования).
- C-уреазный дыхательный тест является надежным неинвазивным методом для определения того, состоялась ли эрадикация H. pylori.
- Иммуноферментный анализ кала также является надежным неинвазивным тестом для определения того, состоялась ли эрадикация бактерии.
- Тесты, основанные на выявлении антител к хеликобактерии в сыворотке, цельной крови, мочи и слюне, наоборот, надежными не являются.

Показания
Какие нужны показания к эрадикационной терапии:
- При наличии язвенной болезни и инфицировании хеликобактером.
- Если язвенной болезни нет, а инфекцию H. pylori выявили по результатам исследования образцов, взятых с помощью биопсии, эрадикация возбудителя необязательна, но возможна.
Эпидемиология
Препарат нового поколения
Схемы эрадикационной терапии
Примеры терапии первой линии. Однонедельные тройные схемы с препаратом висмута:
Однонедельные тройные схемы с ингибиторами протонной помпы:
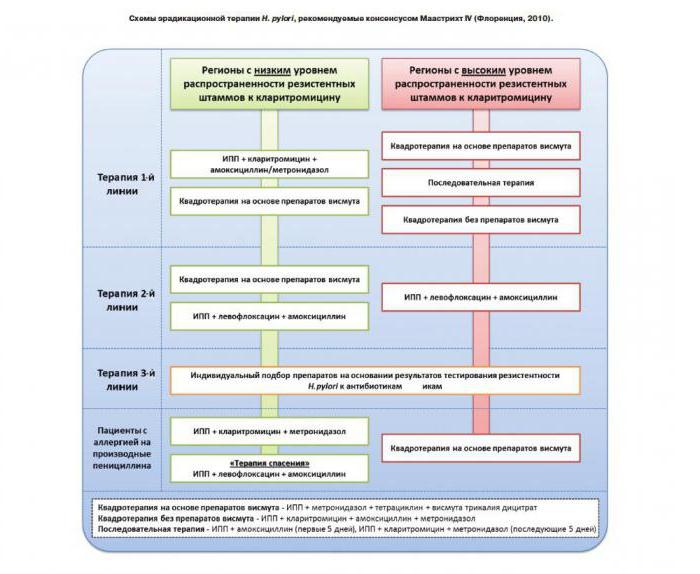
Протоколами также регламентируются дозы препаратов, которые следует использовать в эрадикационных схемах у детей (ежесуточно на килограмм веса):
Особенности лечения
Какое лечение следует применять в той или иной ситуации:
Если не помогло
В случае неэффективности лечения рекомендуется следующие подходы:
Вывод
Эрадикационная терапия – это действенное (порой единственное) средство борьбы с опаснейшей бактерией Helicobacter pylori, способной спровоцировать язвы, гастриты, колиты и прочие болезни ЖКТ.

Хеликобактер пилори — микроорганизм, обитающий в ЖКТ животных и человека. Выделяется у 20-90% жителей Земного шара. Среди российских детишек, носителей хеликобактера в 3-6 раз больше, чем среди Европейских детей, что ставит нас в один ряд со слаборазвитыми странами по этому показателю.
Хеликобактер пилори часто ассоциируется с хроническим гастритом и гастродуоденитом, считается главной причиной развития хронического гастрита (гастродуоденита) типа В.
Гастрит типа В — наиболее распрстраненный вид гастрита, занимает примерно 80% среди всех случаев гастрита.
Хеликобактер пилори впервые попадает в человеческий организм в детстве, если лечение не проводится, микроб может жить в желудке и двенадцатиперстной кишке длительное время, провоцируя развитие заболеваний желудка и 12-ти перстной кишки.
Пути заражения
Источники инфицирования: люди и животные, носители микроорганизма (собаки, кошки, кролики и др). Путь передачи пищевой (с инфицированными пищевыми продуктами), питьевой (хеликобактер пилори может жить в холодной воде на протяжении 2-4 суток) и контактно-бытовой через (грязные руки, мед. инструменты, поцелуи). Хеликобактер пилори может быть высеян из кала, промывных вод желудка, рвотных масс, зубного налета.
Хеликобактер пилори Особенности инфекции у деток до 3х лет
Детки до 1,5-2 лет практически не инфицируются, что объясняется трансплацентарным иммунитетом. Единственным проявлением хеликобактерной инфекции в 1-ые месяцы жизни бывает лишь недостаток массы тела ребенка.
У деток 1-3 лет клинические проявления хеликобактерной инфекции разнообразны: боль в животе, диспепсические симптомы, отрыжка, рвота.
До 5-8 лет антихеликобактерная терапия не проводится.
Особенности гастрита (гастродуоденита) вызванного хеликобактер пилори
- Нет сезонности обострений.
- Нет периодичности болезни (проявления гастрита отмечаются непрерывно).
- Частые проявления симтомов диспепсии: тошноты, рвоты.
- Возможны проявления признаков инфекции: субфебрильная температура, слабые проявления интоксикации, в анализах крови небольшое увеличение числа лейкоцитов, увеличение скорости оседания эритроцитов (СОЭ).
- Неприятный запах изо рта — халитоз.
Гастрит вызванный хеликобактером пилори Эндоскопические признаки
- Многочисленные язвы и эрозии в районе луковицы двенадцатиперстной кишки.
- Мутный желудочный секрет.
- Гиперплазия эпителия, лимфоидная гиперплазия,
- Типичный вид слизистой оболочки, называемый булыжная мостовая.
![]()
Хеликобактер пилори Методы подтверждения инфицирования
- Определение в крови антител к хеликобактеру пилори.
- Определение в кале антигенов хеликобактера пилори.
- Уреазный дыхательный тест.
- Биопсия ткани слизистой пилорического отдела желудка или ткани слизистой двенадцатиперстной кишки. В тканях исследуют наличие уреазы, исследуют их на наличие антигенов хеликобактера пилори + делают посев на специальные среды для выделения культур бактерии.
Точность разных методов выявления инфицированности хеликобактером пилори 50-85%. Для подтверждения или исключения инфицированности используют сразу несколько методов диагностики, комбинируя инвазивные и неинвазивные методы, т. к при каждом их методов возможны неверные результаты.
![]()
Лечение
При подтверждении хеликобактерной инфекции, чаще при эрозивном гастродуодените, проводят терапию первой линии — эрадикации хеликобактер пилори (тритерапию). Используют препараты висмута или омепрозола в комбинации с 1-м или 2-мя антибиотиками (всего три препарата).
Назначается Де-нол (разрешен детям с 4х лет) + 2 антибиотика или Омепрозол + 2 антибиотика.
В качестве антибактериальных препаратов назначают амоксициллин (разрешен детям с рождения) и кларитромицин (разрешен детям с 6 месяцев) в возрастных дозах курсом 10 дней. Один из антибиотиков может заменяться на метронидазол.
- Эзомепразол — с 1 года в суспензии, доза на прием — 10 мг при весе ребенка до 20 кг и 20 мг при весе ребенка больше 20 кг 1 р/д за полчаса до еды, продолжительность приема — 3-4 нед.
- Рабепразол — с 12-ти лет внтрь по 20 мг 1 р/д, утром, длительность курса — 4-6 нед. Таблетки нужно глотать, не жуя.
- Омепразол применяют с 16 лет по 1 капcуле (20 мг) 1 р/д натощак. Для пациента с массой тела 34 кг — по 10 мг 2 р/д или 20 мг 1 р/д. Длительность курса при эрозивном гастродуодените — 2-3 нед, возможно назначаение поддерживающего лечения еще 2-3 нед.
Эффект тритерапии отмечается в 70-90% случаев, но на успешность лечения влияют осложнения, побочные эффекты и устойчивость (резистентность) к ингибиторам протонной помпы, антибиотикам и другим препаратам.
Терапию 2-ой линии (квадротерапию) назначают для эрадикации штаммов хеликобактер пилори устойчивых к антибактериальным препаратам, при неудачах терапии первой линии.
Как правило выбирают: висмута трикалия дицитрат (де-нол) + амоксициллин + кларитромицин + нифурател (макмиррор); у детишек после 8 лет — тетрациклин + нифурател или фуразолидон + ингибитор протонной помпы.
В последние годы используют ступенчатый вариант эрадикации с назначением препаратов по 5 дней, что позволяет уменьшить побочные эффекты антибиотиков. К примеру, первые 5 дней амоксициллин + висмута трикалия дицитрат и следующие 5 дней кларитромицин + нифурател.
Антихеликобактерную терапию назначают 2 р/д, длительностью 10 дней.
Обязательна вторичная диагностика — контроль эрадикации инфекции, которую выполняют не раньше чем через 6 нед от начала терапии, чаще уреазными дыхательными методами.
Уменьшить число побочных эффектов и повысить переносимость лечения хеликобактера пилори помогает добавление к терапии пробиотиков, содержащих лактобактерии и др. м/организмами, относящиеся к антагонистам хеликобактер пилори (линекс, энтерол, рела-лайф).
Это всё про хеликобактер пилори и его лечение у детей. Желаю Вам здоровья!
Читайте также:




