Французские ученые о мутации бактерии коклюша
Замечено, что созданный с помощью бесклеточной вакцины (содержащей некоторые белки с поверхности бактерии коклюша) искусственный иммунитет ослабевает быстрее, чем когда прививали старой (цельноклеточной).
Изучение генов, отвечающих за поверхностные белки бактерии коклюша, продемонстрировало: белки, против которых работает вакцина, эволюционируют с повышенной скоростью. Это может свидетельствовать об усилении защиты микроба. Необходимо определить, насколько данный процесс влияет на поведение бактерии в реальном мире (например, на ее вирулентность).
Если такое воздействие будет доказано, встанет вопрос: целесообразно переделать вакцину, добавив в нее новые белки или адъюванты (вещества, повышающие иммуногенность антител), либо вернуться к прежней (цельноклеточной) версии? Вспышки коклюша носят циклический характер, и уже осенью текущего года станет понятно, увеличивается ли размах эпидемии.
По материалам интернет-источников.
ПРИЧИН ВОЗРОЖДЕНИЯ КОКЛЮШНОЙ ИНФЕКЦИИ НЕСКОЛЬКО, И ПОКА О НИХ ТОЛЬКО ДИСКУТИРУЮТ
Валентина Колодкина, ведущий научный сотрудник лаборатории вакциноуправляемых инфекций РНПЦ эпидемиологии и микробиологии, кандидат мед. наук:
— Коклюш относится к вакциноуправляемым инфекциям. Несмотря на успехи массовой иммунизации, патология остается актуальной и среди детей, и среди взрослых. Эндемичная заболеваемость коклюшем регистрируется во многих странах, а в последние годы отмечается ее рост (особенно в США, Австралии, Новой Зеландии и некоторых европейских государствах).
Ведущие специалисты сходятся во мнении: возрождения коклюшной инфекции происходят по ряду причин, которые следует изучать и анализировать. Среди них — утрата поствакцинального иммунитета, антигенная дивергенция возбудителя с вакцинными штаммами, переход на бесклеточные вакцины, снижение охвата прививками. Необходимо повышать осведомленность врачей о заболевании, улучшать диагностику.
С введением вакцинопрофилактики детей уменьшилась циркуляция возбудителя коклюша. Но при отсутствии естественного подстегивания иммунитета, без ревакцинаций невосприимчивость со временем утрачивается. Подростки и взрослые становятся источником инфицирования для младенцев, которым еще нельзя делать прививки против коклюша. Когда появились бесклеточные вакцины, начали проводить ревакцинацию. Сразу снизились риск передачи инфекции младенцам и уровень заболевания у подростков и взрослых. Инфекцию стало легче контролировать. Однако эрадикация возбудителя коклюша как биологического вида с помощью существующих средств невозможна из-за его адаптации к вакциноиндуцированному иммунитету. Изменчивость антигенных и вирулентных свойств коклюшной патологии изучается во многих странах, где поднимается вопрос об эффективности используемых вакцин.
Обнаружено, что защита против коклюша, обусловленная В. pertussis нейтрализующими антителами, быстро ослабевает и утрачивается в результате применения любой вакцины. По силе и длительности протективный иммунный ответ на клеточную и бесклеточную вакцины имеет разные пути стимулирования клеток памяти и продукции антител. Эксперименты на животных подтверждают: бесклеточные вакцины индуцируют иммунный ответ, который не предотвращает колонизацию и трансмиссию возбудителя коклюша. С учетом утраты протективного иммунитета это правдоподобно объясняет возрождения коклюшной инфекции.
В 2012 году в Беларуси зарегистрировано 576 случаев коклюша, лабораторно подтвержденных — 87,7%. В 2013 году — 188 случаев, лабораторно подтверждены 85,1%. В 2014 году — 378 и 98,3% соответственно. Высокий (98,7%) охват детей иммунизацией обеспечивает стабильную эпидситуацию.
В настоящее время РНПЦ ЭМ проводит исследования по выявлению особенностей генотипической изменчивости (по 7 генам вирулентности) штаммов В. pertussis, возбудителей коклюша на современном этапе эпидемического процесса (2009–2014 гг.), а также их сравнительный анализ со штаммами, входящими в используемую в стране вакцину АКДС.
Предстоит оценить эффективность применяемых в Беларуси целлюлярных и ацеллюлярных противококлюшных вакцин, чтобы усовершенствовать тактику иммунизации против этого заболевания.`
"Коклюш" (именно так, с ударением на последнем слоге) - слово французское, означает оно "петушиный крик". Откуда такое название? Обо всем по порядку.
Палочка идет на прорыв
КОКЛЮШ - это детская инфекция. Основная его "мишень" - дети от 1 года до 5 лет. Больше шансов подхватить заразу у детей ослабленных, плохо питающихся, склонных к простудным заболеваниям. Ученые установили, что, если в коллектив не привитых от коклюша детсадовцев попадет один-единственный подхвативший эту инфекцию ребенок, семеро из десяти его товарищей заболеют. Более старших от коклюша спасает уже достаточно крепкий иммунитет, а младенцы просто реже попадают в места, где могут оказаться заразные больные. Но и подросток может подхватить эту заразу. Причина в том, что благодаря массовой иммунизации младших детей дошколята и младшие школьники хорошо защищены от коклюша, вот он и пытается "прорваться" там, где его не ждут: к подростковому возрасту эффект от прививок может несколько снизиться. Но зато дважды переболеть коклюшем невозможно - после этой инфекции останется стойкий пожизненный иммунитет.
Коклюш вызывается бактерией, получившей по имени открывших ее в 1906 году ученых название палочки Борде - Жангу. Эти палочки поселяются на слизистых оболочках дыхательных путей ребенка: гортани, бронхов и их мелких разветвлений - бронхиол, а также на поверхности мельчайших функциональных единичек легких, которыми мы, собственно, и дышим, - альвеол. Попадают коклюшные микробы туда через верхние дыхательные пути - нос и рот. Чтобы ребенок заразился, нужно, чтобы на него попросту накашляли: палочки коклюша на посторонних предметах и просто в воздухе живут недолго, поэтому через вещи и третьих лиц заразиться практически невозможно. Особенно заразны дети в первые дни заболевания, но и спустя месяц после его начала к ним не стоит допускать неболевших друзей.
Опаснее тот, кто сильнее кашляет: мокрота от него летит дальше, а болезнетворных микробов в ней больше. Наверное, коклюш уже победили бы, если бы не больные стертыми формами этой инфекции. Не всегда ясно, что у них именно коклюш: признаки не такие четкие, и врачам подчас кажется, что это обычная простуда. Но и такие больные-"партизаны" могут, выделяя палочки Борде - Жангу, заразить других детей. Правда, они опасны менее всего - потому что реже кашляют. А вот заразен ли тот, у кого коклюшные микробы всего лишь живут, но болезни не вызывают, пока неясно. Известно только, что таких много среди привитых детей. Интересно, что время года практически не важно в заболевании коклюшем. Большее значение имеют скученность и неблагоприятные жилищные условия, повышающие риск заразиться.
Попав в дыхательные пути, возбудитель коклюша прочно обосновывается на их стенках. На это нужно некоторое время - микроб словно бы окапывается. Этот период "устройства быта" длится от трех до пятнадцати дней (в среднем пять - восемь суток). Во время этого инкубационного периода ребенок чувствует себя ничуть не хуже, чем его здоровые сверстники. Так продолжается, пока вслед за первым периодом болезни не наступит второй - катаральный (воспалительный) период. Тут уж малыш почувствует себя неважно, а столбик термометра доползет до тридцати семи, тридцати восьми, а то и до тридцати девяти градусов. Так случается из-за того, что, хотя сами палочки Борде - Жангу в кровь проникнуть не могут, в нее в больших количествах всасываются токсические вещества, в обилии производимые этим микробом. Токсины вызывают отравление организма, на которое тот отвечает повышением температуры тела. Но прежде чем с кровью разнестись по всему организму, коклюшные токсины раздражают нервные окончания, в обилии расположенные в толще стенок бронхов, бронхиол и альвеол. Нервы "беспокоят" мозг, а тот отвечает командами на сухой, не приносящий облегчения кашель.
Неукротимый кашель
КАТАРАЛЬНЫЙ период развития коклюша продолжается от трех дней до двух недель. Когда кашель становится не просто сухим, а приступообразным, неукротимым, говорят о следующем периоде развития болезни - спазматическом, когда токсины коклюшной палочки добираются до головного мозга ребенка и вызывают образование там очага стойкого возбуждения. Именно этот постоянно действующий очаг возбуждения и виноват, что кашель у ребенка становится мучительным и навязчивым: откашляться практически невозможно, а сам кашель возникает при всяком внешнем раздражающем факторе - шуме, ярком свете, при виде врача.
Кашель становится главным фактором, определяющим состояние ребенка, и, хотя температура тела в спазматическом периоде может снизиться и до нормальной, состояние ухудшается. Кашель возникает или внезапно, или после коротких предвестников: чувства першения в горле, давления в груди, беспокойства. Приступ состоит из серии коротких кашлевых толчков, следующих непосредственно друг за другом. Естественно, полностью откашляться во время столь неглубокого кашля дети не могут. Затем, без паузы, следует свистящий вдох. Свист получается потому, что из-за токсического действия продуктов коклюшных микробов голосовая щель гортани сужается и воздух врывается сквозь нее как через свисток. Из-за этого приступ коклюшного кашля напоминает петушиный крик. Заканчивается приступ откашливанием вязкой прозрачной мокроты и часто - рвотой.
По частоте приступов и наличию рвоты можно установить, насколько тяжело протекает болезнь. Если приступы случаются от пяти до пятнадцати раз в сутки, а рвота бывает редко - это легкая форма болезни. При пятнадцати - двадцати четырех приступах в день, частой рвоте говорят о средней тяжести заболевания. Ну а коли приступы бывают чаще, чем один раз в час, они продолжительные (иногда по пятнадцать минут и более), тяжелые, после них всегда бывает рвота, наблюдаются расстройства сна, аппетита, вялость, похудание, лихорадка - это тяжелая форма коклюша. Но бывает и стертая форма, при которой болезнь протекает совсем легко - настолько, что ее не всегда и принимают за коклюш и часто лечат, как обыкновенную простуду.
В типичных случаях во время приступа внешний вид больного ребенка весьма характерен: лицо краснеет, шейные вены набухают, глаза наливаются кровью, появляется слезотечение, язык до предела вываливается наружу, а кончик его загибается кверху. Из-за того, что высунутый язык трется о зубы, на его уздечке часто образуется небольшая язвочка. Вместе с характерным "петушиным криком" она служит важнейшим признаком коклюша. Во время тяжелого приступа может случиться конфуз - непроизвольно отойти кал и моча. В течение приступа повышаются давление и частота пульса, учащается дыхание. Нервная система реагирует вялостью, раздражительностью, могут быть судороги, эпизоды затемнения сознания. В анализе крови врач найдет повышение числа клеток воспаления - лейкоцитов, повышение СОЭ.
Длится период спазматического кашля от двух до восьми недель. Вслед за ним наступает период разрешения, когда организм постепенно освобождается от болезни. Кашель теряет свой характерный "петушиный" характер и становится реже. Мокрота из прозрачной превращается в слизисто-гнойную. Затем пропадают и остальные симптомы болезни - ребенок выздоравливает. На это требуется от двух до четырех недель. Так бывает, если не случается осложнений. Возникают они, как правило, в самый разгар болезни - в периоде спазматического кашля. Наиболее подвержены осложнениям те дети, что помладше, - до трех лет. Чаще всего встречаются осложнения со стороны органов дыхания - бронхиты и воспаления легких (пневмонии). В тяжелых случаях пневмония может послужить причиной смерти. Другое осложнение - судороги. Судорожные припадки, в том числе и с потерей сознания, возникают в разгар приступа кашля. У детей до 2 лет судорожный припадок может привести к смерти. Из-за токсического действия продуктов палочки Борде - Жангу на стенки сосудов редко, но случаются кровоизлияния в мозг. Они могут стать причиной параличей конечностей. Токсическое отравление сердца способно привести к сердечной недостаточности, присоединение другой бактериальной и вирусной инфекции - к отитам, а из-за натужного кашля у младших детей могут возникнуть пупочные грыжи.
Помогите "отключить" мозги
К СЧАСТЬЮ, в наше время лечится коклюш гораздо успешнее, чем раньше, да и частота тяжелых форм и осложнений значительно уменьшилась. Гибель же от коклюша в последние десятилетия и вовсе стала единичными случаями. Переломить ситуацию помогли антибиотики, уничтожающие палочки Борде - Жангу в организме ребенка.
Антибиотики назначает врач. Но многое могут сделать и родители заболевшего малыша, особенно если он лечится дома (в больницу кладут лишь детей до 2 лет, а также больных с тяжелыми и осложненными формами заболевания). Очень важны режим и уход. В постели нужно лежать лишь при лихорадке и осложнениях, но физических и эмоциональных перегрузок следует избегать. В то же время ребенок должен быть занят увлекательным делом: замечено, что во время интересного занятия частота и сила приступов кашля уменьшаются. Так происходит потому, что в коклюшном кашле "виноват" очаг возбуждения в коре головного мозга. Если малыш чем-то сильно увлекся, у него возникает другой очаг возбуждения, а коклюшный временно отключается. Полезен свежий прохладный воздух: пребывание на улице улучшает вентиляцию легких, облегчает кислородный обмен. Если на дворе тепло, ребенок может проводить на дворе большую часть дня, а зимой гулять следует по полтора-два часа два-три раза в день в укрытых от ветра местах при температуре воздуха не ниже минус десяти градусов.
В питании ребенка нужно учитывать, что рвота затрудняет усвоение принятой пищи. Еда должна быть диетической, не раздражающей стенки желудка. Рекомендуется высококалорийная, полноценная, богатая витаминами пища: вареное мясо, вареный картофель и другие овощи, каши, фрукты. Кормить ребенка нужно пять-шесть раз в день, не перекармливать за один раз.
Лучше предупредить болезнь, чем ее лечить. Поэтому не следует пускать своего малыша к тому, кто заболел. При возникновении в детском коллективе коклюша устанавливают карантин. На детей до семилетнего возраста, бывших в контакте с больными, но не заболевшими и не привитыми от коклюша, накладывают карантин сроком четырнадцать дней с момента выявления и изоляции больного.

Public Health Image Library
Французские и американские ученые сообщили о первом случае излечения человека от серповидноклеточной анемии с помощью генной терапии. Пациентом стал подросток из Франции. Описание случая приводится в New England Journal of Medicine.
Серповидноклеточная анемия — это наследственное заболевание, обусловленное одиночной мутацией в гене бета-субъединицы гемоглобина (белковая часть гемоглобина состоит из двух альфа- и двух бета-субъединиц). Дефектный гемоглобин (HbS), отдавая тканям кислород, полимеризуется с образованием волокон, которые деформируют эритроциты, придавая им серповидную форму. Такие эритроциты хуже проходят через мелкие сосуды, что приводит к образованию тромбов, а также быстрее разрушаются, из-за чего возникает анемия.
Для лечения серповидноклеточной анемии в настоящее время одобрено только одно лекарство — гидроксимочевина. Она способствует синтезу младенческой (фетальной) формы гемоглобина, которая снижает концентрацию HbS и замедляет его полимеризацию. Однако препарат действует не на все клетки и обладает множеством побочных эффектов. Небольшому числу пациентов (примерно 18 процентам) можно помочь пересадкой донорского костного мозга. Подобные виды лечения не могут покрыть потребности всех больных, и ученые на протяжении десятков лет занимались разработкой генной терапии заболевания. После успешных ее испытаний на животных в 2014 году начались клинические испытания этого метода лечения.
Одним из участников испытаний, которые продолжаются до сих пор на базе Детской больнице Неккер в Париже, стал мальчик, болевший серповидноклеточной анемией с рождения и наблюдавшийся в этом медучреждении. В возрасте от двух до девяти лет пациент получал гидроксимочевину без выраженного эффекта: у него наблюдались повторные тромбозы мелких сосудов (в том числе дважды — легочных) и двусторонний очаговый некроз бедренных костей. С 2010 года ему проводили профилактические переливания эритроцитарной массы.
В октябре 2014 года, когда мальчику было 13 лет, ему провели генную терапию в соответствии с протоколом, разработанным французскими учеными и американской компанией Bluebird Bio. На первом этапе лечения у пациента дважды забрали ткань костного мозга (для проведения терапии и создания резервного запаса) и выделили из нее мультипотентные кроветворные клетки (CD34+). В эти клетки с помощью обезвреженного лентивируса ввели ген здорового варианта бета-глобина β A-T87Q . Средняя доза геннотерапевтического препарата LentiGlobin BB305 составила 1,0 и 1,2 копии вирусного вектора на клетку.
После этого мальчику провели миелоабляцию (уничтожение кроветворных клеток) бусульфаном. Через два дня ему ввели модифицированные клетки. На всем протяжении лечения пациенту переливали кровь, пока уровень β A-T87Q не достиг от 25 до 30 процентов от всего гемоглобина на 88 день терапии.
На шестой месяц уровень общего гемоглобина в крови мальчика стабилизировался на показателях от 106 до 120 граммов на литр (около нижней границы нормы). К девятому месяцу после введения модифицированных клеток β A-T87Q составлял 46 процентов, а к 15 месяцу — 48 процентов от всего гемоглобина.
В течении более чем 15 месяцев наблюдения у пациента не наблюдалось никаких клинических событий, связанных с серповидноклеточной анемией, показатели анализа крови нормализовались. По итогам наблюдения всю медикаментозную терапию отменили за ненадобностью. Основные побочные эффекты были связаны с миелоабляцией и устранены в процессе лечения.
Помимо описываемого пациента к настоящему времени терапию препаратом LentiGlobin BB305 получили еще несколько десятков французских и американских участников испытаний с серповидноклеточной анемией и другим наследственным дефектом бета-глобина — бета-талассемией. Предварительные результаты лечения признаны обнадеживающими, однако окончательные выводы делать пока рано, пишут авторы работы.
Недавно были разработаны несколько других экспериментальных подходов к терапии серповидноклеточной анемии и других гемоглобинопатий. В частности, ученые успешно испытали на мышах и клетках человека редактирование дефектного гена с помощью системы CRISPR/Cas9, убедились, что вещества, увеличивающие объем эритроцитов, препятствуют их деформации, и разработали метод генетической коррекции мутаций гемоглобина, основанный на пептидонуклеиновых кислотах.
Первые исторические справки о заболеваемости коклюшем относятся к эпохе средневековья, когда были описаны эпидемии заболевания в Голландии, Франции, Англии.
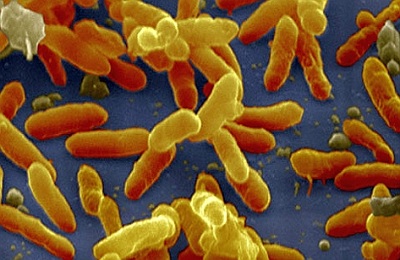
Бельгийским бактериологом Жюлем Борде и французским ученым Октавом Жангу в 1906 году впервые в мире был выделен и описан возбудитель заболевания, который впоследствии был назван палочкой Борде-Жангу. Позднее, в честь Ж. Борде был назван род бактерий Bordetella. Массовую вакцинацию против коклюша начали проводить в середине 20-го века.
Коклюш представляет собой острый инфекционный процесс в дыхательной системе человека, поражающий слизистую оболочку бронхов, бронхиол, а также гортани, трахеи, сопровождающееся судорожным приступообразным кашлем. Возбудителем коклюша является бактерия Bordetella pertussis.
Микробиологическая характеристика возбудителя коклюша
Род Bordetella включает несколько возбудителей респираторных болезней человека, из которых первостепенное значение имеют Bordetella pertussis – возбудитель коклюша, и Bordetella parapertussis – возбудитель паракоклюша (клинически схожее заболевание, но протекающее в легкой форме).
Бактерии данного рода грамотрицательны (не удерживают краситель при окрашивании), имеют палочковидную форму и небольшие размеры, неподвижны.
Палочка коклюша – Bordetella pertussis – характеризуется маленькими размерами (не превышают 1 мкм), способна образовывать защитную микрокапсулу, покрыта микроворсинками. Бактерия способна размножаться только в присутствии кислорода (аэроб), достаточно требовательна к питательным средам. Колонии коклюшной палочки напоминают жемчуг или капельки ртути: серебристые, мелкие, сферические и конусообразные.
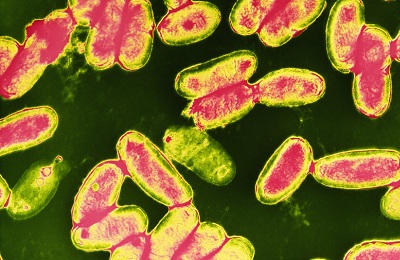
Основные структурные элементы коклюшной палочки – защитная микрокапсула, микроворсинки, клеточная стенка (наружная и внутренняя мембраны) – несут антигенную нагрузку микроорганизма и продуцируют токсины, обеспечивая иммунный ответ и клинику заболевания.
В отличие от истинного возбудителя коклюша, В.parapertussis имеет большие размеры, на питательных средах растет иными колониями и самое главное, отличается структурой антигенов.
Антигенная структура у бактерий рода Бордетелла очень сложна. В капсуле расположено 14 агглютиногенов (капсульные антигены), называющихся факторами. Так, фактор 1, 2, 3 специфичен для B.pertussis, антигенный фактор 14 свойственен B.parapertussis, а фактор 7 считается общим для всего рода Bordetella.
Всего у коклюшной палочки 8 агглютиногенов, но ведущими являются 1,2 и 3. В зависимости от сочетания этих антигенов в одной бактериальной клетке, выделяют 4 серотипа: 1,2,0, 1,0,3, 1,2,3, 1,0,0. Первые два серотипа чаще выделяют у привитых заболевших и больных легкими формами, последние – у пациентов с тяжелыми формами.
Факторы патогенности коклюшной палочки:
В реализации действия бактериальной клетки на организм человека факторы патогенности коклюшной палочки играют первостепенную роль.
Среди них можно выделить:
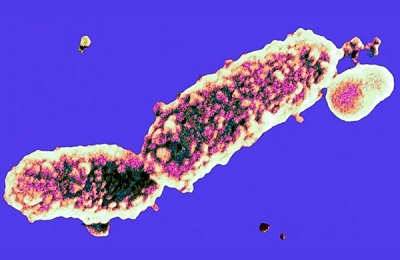
Микроворсинки, белок пертактин, расположенный в наружной мембране клеточной стенки, капсульные агглютиногены, филаментозный гемагглютинин, реализуют прикрепление палочки коклюша к эпителиальным клеткам дыхательных путей. Филаментозный гемагглютинин запускает выработку антител IgA и IgG в организме больного. Пертактин отвечает за индукцию иммунного ответа.
Ряд токсинов, которые выделяет палочка:
- коклюшный токсин – основной виновник тяжелой симптоматики болезни – является ферментом, состоящим из двух частей. Одна часть реализует токсичность, а вторая – прикрепление к клеткам эпителиальной ткани бронхов и трахеи. Токсин вызывает повышенную чувствительность клеток респираторных путей к гистамину (медиатор аллергии, который продуцируется в организме человека в ответ на поступление чужеродных веществ, приводит к спазму гладкой мускулатуры, повышению проницаемости сосудов, отеку, застою венозного кровотока), повышение выработки инсулина поджелудочной железой, повышение уровня лейкоцитов. К коклюшному экзотоксину вырабатывается стойкий пожизненный антитоксический иммунитет,
- трахеальный цитотоксин – вызывает прямое повреждающее действие на эпителиальные клетки дыхательных путей, вызывая приступообразный кашель,
![]()
дерматонекротический термолабильный токсин – вызывает некроз (разрушение) эпителия и повреждающее действие на сосуды (кровоизлияния в коже), токсически действует на печень, селезенку и лимфоузлы,- термостабильный эндотоксин – запускает выраженное воспаление в дыхательных путях,
- внеклеточная аденилатциклаза – угнетает движение лейкоцитов (фагоцитов) к бактериальным клеткам.
Эпидемиология коклюша
Источником инфекции является больной человек (антропонозная инфекция). В настоящее время бактерионосительство бордетеллы не доказано. Период заразительности длится с 1 по 25 день заболевания.
Наибольшее количество случаев заболевания регистрируется в возрастной группе до 1 года. Это связано с незавершенным курсом вакцинации у младенцев этого возраста и высокой их восприимчивостью. Младшие школьники также являются группой риска: поствакцинальный иммунитет к 5-7 годам значительно ослабевает, поэтому среди детей этой возрастной группы накапливается много не иммунных, поддерживающих циркуляцию возбудителя.
Механизм передачи коклюша – аэрозольный, путь передачи – воздушно-капельный.
Контагиозность (заразительность) очень высокая и индекс контагиозности равен 70-100%. При отсутствии иммунитета к коклюшу (если не сделана прививка или человек не болел), восприимчивость приближается к 90%.
Возбудитель коклюша массивно выделяется в окружающую среду при кашле. При судорожном коклюшном кашле образуется крупнодисперсная аэрозоль, которая быстро оседает в радиусе 2 метра. Способность к проникновению в дыхательные пути мала: частицы слюны и мокроты задерживаются в верхних дыхательных путях, где не может реализоваться инфекционный процесс. Поэтому для заражения коклюшем необходим очень длительный и тесный контакт.

Устойчивость в окружающей среде низкая. Палочка коклюша быстро погибает под воздействием ультрафиолетовых лучей и нагревания (при температуре 50 градусов погибает в течение 30 минут), быстро инактивируется действующими дезинфицирующими растворами. В высохшей мокроте на предметах обихода погибает довольно быстро, а во влажной может сохранять жизнедеятельность несколько дней. Сезонность: осенне-зимняя с пиком в ноябре-декабре.
Иммунитет после болезни напряженный и стойкий. Возможно повторное инфицирование при иммунодефиците, но такие случаи требуют лабораторного разбирательства.
Коклюш является вакциноуправляемой инфекцией. В конце 90-х гг. 20 века начался постепенный рост заболеваемости коклюшем, а в настоящее время рост уровня заболеваемости неуклонен. Так, показатель заболеваемости в Российской Федерации в 2015 году составил 4,42 случая на 100000 населения, в 2014 г. – 3,23 на 100000, в 2012 г. – 3,15 на 100000. В 2014 году зарегистрирован 1 случай летального исхода.
В структуре по возрастам доля детей до года в 2015 году составила 82%, в 2014 году – 54%.
Причины роста заболеваемости коклюшем:
Следует также отметить, что истинные цифры числа заболеваний могут значительно превышать статистические, т.к. в реальности диагностировать коклюш удается не всегда: болезнь может протекать атипично, симптоматика может быть схожа с паракоклюшем, в небольших городах отсутствуют современные способы диагностики.
Патогенез коклюша
Время от попадания коклюшной палочки в дыхательные пути до первых появлений симптомов (инкубационный период) составляет от 3 до 14 дней.
Эпителий является местом прикрепления и размножения бактерий в дыхательных путях. Менее выражен процесс в трахее, гортани, более , в бронхах и бронхиолах.
В крови возбудитель не появляется. Процесс размножения длится 2-3 недели и сопровождается активной выработкой экзотоксинов – внеклеточной аденилатциклазы и коклюшного токсина. Коклюшный токсин крайне негативно влияет на дыхательную, сердечную, иммунную и нервную системы. Возникает появление выраженного бронхоспазма, сужения сосудов, которое приводит к увеличению артериального давления, значительно угнетается клеточное звено иммунитета.
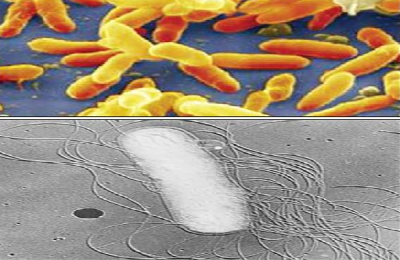
После окончания цикла размножения бордетеллы разрушаются и из клеток выходит большое количество факторов патогенности. Наступает предсудорожный катаральный период, длящийся 10-13 дней (чем он короче, тем хуже прогноз). Слизистая оболочка некротизируется, разрушается, могут появиться язвы. Формируются пробки гнойной мокроты, закупоривающие просвет бронхов и альвеол, что может способствовать их спадению.
Непрекращающееся воздействие на рецепторный аппарат дыхательных путей токсинов бактерий приводит к повышенной возбудимости блуждающего нерва. Нервные импульсы постоянно поступают в продолговатый мозг, в результате чего появляется очаг возбуждения дыхательного центра – доминанта.
Вследствие этого кашлевой рефлекс становится самоподдерживающимся и не требует участия бактерий. Кашель становится спастическим и судорожным, характерным именно для коклюша. Он может появляться от любых раздражителей: боль, прикосновение и др. Наступает период судорожного спазматического кашля, который длится у привитых 1-1,5 недели, а у непривитых до 6 недель.
Так как рядом с дыхательным центром находятся многие другие важные центры регуляции жизнедеятельности, возбуждение, распространяясь на них, вызывает и рвоту, и скачки артериального давления, и спазмы мышц лица и тела.

После судорожного кашля постепенно наступает период выздоровления, который длится от 2 недель до 6 месяцев, в зависимости от иммунного статуса и осложнений.
Токсины коклюшной палочки оказывают негативное влияние на кишечную флору и перистальтику кишечника, что приводит к дисбактериозу и диарее. Известно, что вторичное иммунодефицитное состояние при коклюше обусловлено апоптозом иммунных клеток. Это объясняет частое присоединение хламидийных, микоплазменных пневмоний и бронхитов, развитие обструкции бронхов.
Коклюш — острая инфекционная болезнь, характеризующаяся поражением верхних дыхательных путей, приступами спазматического кашля; наблюдается преимущественно у детей. Возбудитель коклюша Bordetella pertussis
Таксономия. B.pertussis относится к отделу Gracilicutes, роду Bordetella.
Морфологические и тинкториальные свойства. В.pertussis — мелкая овоидная грамотрицательная палочка с закругленными концами. Спор и жгутиков не имеет, образует микрокапсулу, пили.
Культуральные и биохимические свойства. Строгий аэроб. Оптимальная температура культивирования 37С. B.pertussis очень медленно растет только на специальных питательных средах, например на среде Борде — Жангу (картофельно-глицериновый агар с добавлением крови), образуя колонии, похожие на капельки ртути. Характерна R-S-трансформация. Расщепляют глк. и лактозу до кислоты без газа.
Антигенная структура. О-антиген термостабильный продоспецифический. 14 поверхностных термолабильных капсульных К-антигенов. В.pertussis имеет 6 сероваров. Фактор 7 является общим для всех бордетелл. Для В.parapertussis специфический фактор 14. К – антигены выявляют в реакции агглютинации.
Факторы патогенности. Термостабильный эндотоксин, вызывающий лихорадку; белковый токсин, обладающий антифагоцитарной активностью и стимулирующий лимфоцитоз; ферменты агрессии, повышающие сосудистую проницаемость, обладающие гистаминсенсибилизирующим действием, адгезивными свойствами и вызывающие гибель эпителиальных клеток. В адгезии бактерий также участвуют гемагглютинин, пили и белки наружной мембраны.
Резистентность. Очень неустойчив во внешней среде, быстро разрушается под действием дезинфектантов и других факторов.
Эпидемиология. Коклюш — антропонозная инфекция: источником заболевания являются больные люди и в очень незначительной степени бактерионосители. Заражение происходит через дыхательный тракт, путь передачи воздушно-капельный. Коклюш встречается повсеместно, очень контагиозен. Паракоклюш реже, эпиходический характер. Протекает легче.
Патогенез. Неинвазивные микробы (не проникают внутрь клетки-мишени). Входными воротами инфекции являются верхние дыхательные пути. Здесь благодаря адгезивным факторам бордетеллы адсорбируются на ресничках эпителия, размножаются, выделяют токсины и ферменты агрессии. Развиваются воспаление, отек слизистой оболочки, при этом часть эпителиальных клеток погибает. В результате постоянного раздражения токсинами рецепторов дыхательных путей появляется кашель. В возникновении приступов кашля имеет значение и сенсибилизация организма к токсинам B.pertussis.
Клиника. Инкубационный период составляет 2—14 дней. В начале болезни появляются недомогание, невысокая температура тела, небольшой кашель, насморк. Позже начинаются приступы спазматического кашля, заканчивающиеся выделением мокроты. Таких приступов может быть 5—50 в сутки. Болезнь продолжается до 2 мес.
Иммунитет. После перенесенной болезни иммунитет стойкий, сохраняется на протяжении всей жизни. Видоспецифический (антитела против В.pertussis не защищают от заболеваний, вызванных В.parapertussis.
Лечение. Антимикробные препараты – эритромицин, ампициллин (кроме пенициллина). При тяжелых формах коклюша применяют нормальный человеческий иммуноглобулин. Рекомендуются антигистаминные препараты, холодный свежий воздух. При легких формах заболевания достаточно пребывания на воздухе.
Профилактика. Адсорбированная коклюшно-дифтерийно-столбнячная вакцина (АКДС). В ее состав входит убитая культура В. pertussis I фазы, коклюшный токсин, агглютиногены, капсульный антиген. Нормальный человеческий иммуноглобулин вводят неиммунизированным детям при контакте с больными для экстренной профилактики. Разрабатывается неклеточная вакцина с меньшими побочными эффектами, содержащая анатоксин, гемагглютинин, пертактин и антиген микроворсинок.
Паракоклюш вызывает Bordetella parapertussis. Паракоклюш сходен с коклюшем, но протекает легче. Паракоклюш распространен повсеместно и составляет примерно 15 % от числа заболеваний с диагнозом коклюш. Перекрестный иммунитет при этих болезнях не возникает. Возбудитель паракоклюша можно отличить от B.pertussis по культуральным, биохимическим и антигенным свойствам. Иммунопрофилактика паракоклюша не разработана.
113. Осложнения антибиотикотерапии, их предупреждение.
Читайте также:



