Гемодинамические изменения при сепсисе
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ СЕПСИСА
Определение сепсиса охватывает клинический синдром системной воспалительной реакции, причиной которой является инфекция. Поэтому клиническое проявление сепсиса включает в себя признаки и симптомы ССВО, и эти два понятия неразрывны (см. критерии ССВО). Дисфункция наиболее важных органов, сопутствующая сепсису — острая лёгочная недостаточность с лёгочным дистресс-синдромом взрослых (ЛДСВ), сердечно-сосудистый коллапс (сердечая недостаточность, гипотензия и шок), почечная недостаточность, делирий или кома, и диссеминированное внутрисосудистое свёртывание.
Острая лёгочная недостаточность (ОЛН) встречается приблизительно в 35% всех случаев сепсиса. Приблизительно в 25% этих случаев развивается острый лёгочный дистресс-синдром. Нарушение функции лёгких является результатом панэндотелиального повреждения, вызванного воспалительным фактором. Эндотелиальное повреждение приводит к увеличению проницаемости легочных сосудов, что вносит вклад в формирование отека и последующую рефрактерную гипоксемию с дыхательной недостаточностью. Патогенез, клинические проявления, течение и исход ЛДСВ настолько обширны, что их освещение требует специальной главы.
Влияние сепсиса на сердечно-сосудистую систему весьма значимо. Дисфункция миокарда возникает в результате выброса NO, которая вызывает его депрессию. Это выражается в снижении сократимости и диастолического расслабления желудочков, приводящее к желудочковой дилатации. В результате возникает уменьшение абсолютного сердечного выброса. Несмотря на уменьшение абсолютного сердечного выброса, имеется повышение минутного сердечного выброса за счёт тахикардии. Системная гипотензия является конечным результатом гипервоздействия сосудорасширяющих веществ типа NO и продуктов циклооксигеназ на микроциркуляторное русло, вызывающего заметное снижение резистентности сосудов. В результате вазодилятации возникает уменьшение эффективного внутрисосудистого объема из-за перераспределения жидкости в интерстиции и секвестрации её в венозных сосудах, в дальнейшем способствующее гипотензии. Недостаточная перфузия ведет к гипоксии ткани и последующему анаэробному метаболизму с выработкой лактата (см. выше).
Острая почечная недостаточность — частое явление при сепсисе. Изменения в микроциркуляции, вызванные системным воспалением и септическим шоком, приводят к изменениям в интраренальном кровотоке, выражающемся в дисбалансе кровоснабжения кортикального и медулярного слоя. Снижение среднего артериального давления может привести к уменьшению давления гломерулярной фильтрации и ишемии трубочек. Следствием этого является уменьшение выработки мочи и острый некроз канальцев. В результате возникает снижение степени очистки крови от азотистых метаболитов с развитием азотемии.
ЖКТ вносит вклад в системное воспаление и также сильно подвержен его влиянию. Слизистая оболочка желудочно-кишечного тракта, как было упомянуто выше, особенно восприимчива к недостаточной перфузии и ишемии. В результате этого у больных сепсисом очень часто возникают желудочно-кишечные кровотечения. К другим осложнениям сепсиса относятся адинамическая непроходимость кишечника; развитие ишемического колита с потенциальной угрозой микроперфорации; холестаз с или без желтухи; бескаменный холецистит с потенциальной ишемией и перфорацией желчного пузыря; и возникновение цитопатического гепатита.
Лейкоцитоз, лейкопения, тромбоцитопения, тромбоцитоз, диссеминированное внутрисосудистое свёртывание, тромбоз — всё это гематологические проявления сепсиса.
Схема различных ответов на воспаление представлена на рис. 28-3.
ЛЕЧЕНИЕ СЕПСИСА
Как было установлено в исследованях на животных и у человека, чтобы улучшить выживаемость, должны преследоваться 2 цели. В исследованиях на собаках, которым вводили живую культуру Е. coli, показана 100 % смертность в нелеченных случаях. В случаях только антибиотикотерапии, выживаемость была 13 %. В группе собак, которые получали только поддерживающую гемодинамическую терапию, выживаемость была такой же. А сочетание антибиотикотерапии с поддерживающей гемодинамической терапией, повысило выживаемость до 45 %. Поэтому в лечение сепсиса должна входить как надлежащая и ранняя антибиотикотерапия, так и эффективная поддерживающая гемодинамическая терапия. Кроме того, может потребоваться хирургическое вмешательство, для осуществления дренирования гноя из абсцесса, разрешения холестаза, механической анурии или кишечной непроходимости. Эти манипуляции необходимы, потому что недостаточно только антибиотико и гемодинамической терапии. Кроме того, всегда необходима общая поддерживающая терапия. Например, раннее энтеральное кормление важно для сохранения целостности кишечного тракта и предотвращения транслокации бактерий. Питание важно ещё и для покрытия необходимых энергетических затрат, которые значительно возрастают при сепсисе в результате лихорадки.
Наиболее часто встречающимися при тяжёлом сепсисе и септическом шоке гемодинамическими изменениями являются: тахикардия, гипотензия, пониженный возврат крови к сердцу, проявляющийся низким центральным венозным давлением и низким давлением окклюзии легочных капилляров, низкое системное сосудистое сопротивление, повышенный сердечный выброс, незначительная или умеренная легочная артериальная гипертензия и сниженный индекс выброса левого желудочка. Гемодинамическая поддержка должна быть направлена на коррекцию вышеупомянутых нарушений инфузией жидкости (кристаллоиды, коллоиды или кровь) при низком возврате крови к сердцу — применением вазопрессоров для поддержания адекватного перфузионного давления, и время от времени, использование инотропной поддержки типа допамина или добутамина. Если гемодинамические нарушения скоррегированы, доставка кислорода может улучшиться, в результате возрастает утилизация кислорода, уменьшается лактоацидоз. Сегодня только с трудом можно поверить, что достижение супранормального уровня доставки кислорода тканям, привносит положительный вклад в лечение этих пациентов.
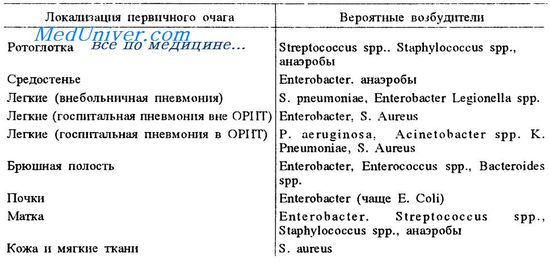
У всех пациентов с сепсисом, должны быть выполнены надлежащие микробиологические посевы, с особым акцентом на получение культур посевов крови. Немедленно должен быть назначен эмпирически выбранный, с учётом чувствительности бактериальной флоры, типичной для внутри-больничной инфекции антибиотик. Выбор должен быть осуществлён с учётом локализации очага инфекции и состояния пациента. Правильный выбор типа и дозы антибиотика на первых этапах лечения дает пациенту больше шансов, по сравнению с ситуацией назначения антибиотика по результатам посевов (хорошее предположение лучше, чем стандартный подход).
ОСОБЕННОСТИ ИНФЕКЦИОННЫХ ОСЛОЖНЕНИЙ В НЕЙРОХИРУРГИЧЕСКОЙ ПРАКТИКЕ
достигает, по некоторым сообщениям, 16.5 % или 22.1 на 1000 койко-дней. Наиболее частым осложнением является пневмония с частотой встречаемости до 9%. Пневмония, связанная с ИВЛ встречается приблизительно в 15.1 из 1000 койко-дней. Второе наиболее общее осложнение — уроинфекция (7.3 % или 8.5 на 1000 дней койко-дней вследствие катетеризации мочевого пузыря. Бактеремия встречается в 1 % и связана с катетеризацией центральных вен. Частота инфекционных осложнений в связи с хирургической активностью (нагноение раны), по некоторым сообщениям, достигала 3.5—4 %. Нагноение в глубине раны (менингит, абсцесс, нагноение костного лоскута и остеомиелит) встречаются в 2.5—4.3 %.
Наиболее часто встречающиеся микроорганизмы, вызывающие инфекционно-гнойные осложнения в послеоперационном периоде, являются грамм-положительными кокками, сопровождаемые энтеральными грамм-отрицательными палочками. По некоторым данным, Staph. aureus не окрашивались по грамму, а в 46 % случаев инфекции, вызванной энтеральными микроорганизмами, выделены лекарственно устойчивые штаммы. К факторам риска возникновения инфекционных осложнений, сопутствующих нейрохирургическим манипуляциям, относятся произведенное оперативное вмешательство, продолжительность операции более 4 часов, экстренная хирургия, ликворея и сложный характер хирургической раны. Бритье головы незадолго до операции, согласно последним исследованиям, не является самостоятельным фактором риска возникновения инфекции.
В Соединенных Штатах, антибиотикопрофилак-тика в периоперативном периоде является рутинной в нейрохирургической практике. В литературе имеется статистическая обоснованность подобного ведения пациентов только в случае ревматических заболеваний сердца. Чаще всего в целях антибиоти-копрофилактики используется цефалоспорин первого поколения — цефазолин. Имеется несколько предпосылок к предположению, что обильное орошение раны в процессе операции в сочетании с системным применением антибиотиков уменьшает уровень послеоперационных инфекционных осложнений. Лечение инфицированных хирургических ран чаще носит эмпирический характер — антибиотиками, воздействующими на Staph. Aureus, энтерококки, стрептококки.. В случае возникновения назокоминально индуцированного воспаления раны мягких тканей и интракраниального воспаления, эмпирическая терапия должна включать антибиотики, действующие на метициллин-резистентные стафилококки и энтеральные грамм-негативные микроорганизмы. Интратекальное введение антибиотиков для лечения внутричерепной инфекции носит противоречивый характер. Установка временных и хронических устройств в головной мозг и позвоночник (например вентрикулостомия, эпидуральные катетеры, вентрикулоперитонеостомия и трансплантанты) вызывает возрастание уровня инфекционных осложнений. В этих случаях необходимо их удаление с хирургической обработкой раны и началом антибиотикотерапии.

Исторически сепсис рассматривается как инфекционный процесс в ответ на внедрение микроорганизмов с существенным изменением типичного компенсаторного характера воспаления. Именно формирование реакции системного (генерализованного) воспаления, инициированного инфекционным агентом, знаменует развитие сепсиса. Клиническая интерпретация подобного взгляда легла в основу определения синдрома системного воспалительного ответа, а также критериев диагностики и классификации сепсиса, предложенных в 1991 г. согласительной конференцией Американского колледжа пульмонологов и Общества специалистов критической медицины (ACCP/SCCM) [1]. Соответственно в 2004 г. в Калуге состоялась отечественная согласительная конференция по сепсису, итогом которой явилось издание практического руководства [2].
Дальнейшее активное выяснение факторов риска и причин развития, особенностей изменения лабораторных показателей и клинической картины при сепсисе явилось основанием для регулярного обсуждения и выработки консенсуса по проблемам сепсиса как среди зарубежных исследователей [3], так и в нашей стране [4, 5]. В настоящее время общепринятыми считаются положения, предложенные в 2016 г. специальной комиссией SCCM/ESICM (Sepsis-3) [6], согласно которым сепсис характеризуется дисрегуляцией системного воспалительного ответа при микробной инвазии с развитием органной дисфункции (полиорганной недостаточности).
Среди основных органов-мишеней, поражаемых при сепсисе, особое место занимает сердце, обеспечивающее адекватное кровоснабжение органов и тканей, поражение которого считается важным звеном формирования синдрома полиорганной недостаточности и развития септического шока [7, 8].
Цель работы: анализ данных литературы о клинико-морфологических проявлениях поражения сердца при сепсисе.
Согласно положениям консенсуса Sepsis-3 [6], наличие и степень органной дисфункции рекомендуется оценивать по шкале SOFA (Sepsis-related (sequential) Organ Failure Assessment), где ноль баллов указывает на отсутствие органной дисфункции, а два и более баллов при наличии очага инфекции соответствуют сепсису. Степень поражения сердечно-сосудистой системы по шкале SOFA оценивается по наличию артериальной гипотензии и дозе вазопрессорных препаратов для ее коррекции.
По данным K.W. McConnell и M.K. Coopersmith [9] поражение сердечно-сосудистой системы отмечается примерно у половины пациентов с сепсисом. Считается, что дисфункция сердца при сепсисе может проявляться в виде левожелудочковых и/или правожелудочковых нарушений во время систолы или диастолы, неадекватного сердечного выброса и, соответственно, доставки кислорода, развития аритмий, а также прямого повреждения кардиомиоцитов [10].
Примечательно, что при сепсисе примерно 90 % осложнений со стороны сердца, включая инфаркт, аритмии и сердечную недостаточность, происходит в первые семь дней, из которых более половины развивалось в первые 24 часа заболевания [13]. Более 60 % больных сепсисом, поступавших в отделения интенсивной терапии, имели клинические признаки сердечной дисфункции, летальность для них составляла 70–90 % в отличие от 20 % у пациентов без поражения сердца [14].
– дилатация левого желудочка с нормальным или низким давлением наполнения,
– снижение сократимости желудочков,
– дисфункция (систолическая или диастолическая) правого и/или левого желудочка со сниженным ответом на инфузионную терапию.
Действительно, у 29–67 % пациентов, страдающих сепсисом или септическим шоком, при эхокардиографии выявляются признаки систолической дисфункции левого желудочка в виде снижения фракции выброса менее 45–55 %, а около 15 % больных имеют выраженную систолическую дисфункцию левого желудочка (фракция выброса менее 30 %) [16].
При изучении гемодинамики или при радиоизотопном исследовании до 56 % пациентов с сепсисом имеют признаки систолической дисфункции левого желудочка. Диастолическая дисфункция левого желудочка выявляется примерно с той же частотой: по данным B.J. Anderson и M.E. Mikkelsen [16] – в 57 % наблюдений сепсиса. При этом развитие диастолической дисфункции левого желудочка при сепсисе коррелирует с неблагоприятным исходом [16].
Изучению систолической дисфункции правого желудочка при сепсисе посвящено меньшее количество исследований, хотя развивается она обычно в сочетании с дисфункцией левого желудочка и может характеризоваться как увеличением, так и уменьшением фракции выброса. Частота развития систолической дисфункции правого желудочка составляет 32–52 % [17]. У ряда пациентов отмечается развитие диастолической дисфункции правого желудочка. Примечательно, что у трети больных, страдающих сепсисом, наблюдаются признаки систолической дисфункции обоих желудочков сердца [16]. Следует также отметить интересную особенность дисфункции сердца у больных с сепсисом: степень уменьшения фракции выброса выражена в большей степени у выживших больных по сравнению с погибшими [16].
Другим грозным осложнением со стороны сердца при сепсисе считается развитие нарушений ритма, частота которых достигает 12 % у пациентов в критическом состоянии [18]. Наиболее часто, примерно у 6–8 % больных с сепсисом, определяется фибрилляция предсердий. Развивается она, как правило, в течение первых трех дней заболевания [16]. При этом роль фибрилляции предсердий в развитии летального исхода при септическом шоке сопоставима с таковой от полиорганной недостаточности. Желудочковые аритмии встречаются реже (примерно в 2 % наблюдений) [18].
В основе развития поражения сердца и формирования его дисфункции (сердечно-сосудистой недостаточности) лежит сложный комплекс различных взаимно усугубляющих реакций и механизмов. К первоначальным повреждающим агентам следует отнести циркулирующие микроорганизмы и продукты их распада, в частности липополисахарид, взаимодействующие с клетками различных органов и тканей, включая кардиомиоциты, и вызывающие активацию транскрипционного ядерного фактора-kB (NF-kB) с последующей продукцией провоспалительных цитокинов [19]. Еще 30 лет назад A.F. Suffredini с соавт. [20] показали, что у здоровых добровольцев через 3 ч после внутривенного введения липополисахарида в дозе 4 нг/кг наблюдалось повышение частоты сердечных сокращений, а также снижение фракции выброса и увеличение конечного диастолического объема в левом желудочке. Повышение продукции провоспалительных цитокинов также сопровождается нарушением функций сердца. Более того, введение фактора некроза опухоли (TNF) вызывало дозозависимый эффект угнетения функции левого желудочка [21].
Важно, что под действием липолисахарида происходит высвобождение из кардиомиоцитов и других клеток амфотерина (HMGB1) – белка группы ядерных негистоновых белков HMG, вызывающего выход кальция из эндоплазматического ретикулюма и соответственно снижение сократимости кардиомиоцитов [22]. Помимо липополисахаридов другие компоненты клеточной стенки патогенных микроорганизмов, в частности липопротеины, также способны реагировать с различными толл-подобными рецепторами (–2, –5, –9) клеток сердца, приводя к развитию воспаления и дисфункции кардиомиоцитов [23].
Наряду с прямым и опосредованным эффектом патоген-ассоциированных молекулярных паттернов (PAMP) происходит высвобождение различных эндогенных лигандов / медиаторов, в частности опасность-ассоциированных молекул (DAMP), усугубляющих повреждение клеток и тканей. В свою очередь опасность-ассоциированные молекулы (DAMP) вызывают высвобождение гепаран сульфата из гликокаликса эндотелоцитов, индуцирующего развитие воспалительного ответа и повреждение митохондрий в кардиомиоцитах [24].
Существенная роль в повреждении сердца при сепсисе принадлежит также оксиду азота (NO) и его синтазам (NOS). В кардиомиоцитах идентифицировано три изоформы синтазы оксида азота. Две из них, нейрональная и эндотелиальная синтазы оксиды азота, постоянно генерируют небольшое количество оксида азота, Индуцибельная же изоформа характеризуется выраженным повышением своей экспрессии и значительной продукцией оксида азота при воспалении. Именно поэтому индуцибельной синтазе оксида азота отводится важная роль в развитии поздней дисфункции сердца при сепсисе [21].
Основными звеньями такого поражения считаются угнетение регуляции β-адренергических рецепторов, снижение реакции миофиламентов на изменения ионов Ca, повышение проницаемости мембран митохондрий с нарушением их функций. Следует также отметить, что введение липополисахарида приводит к подавлению транскрипции гена белков митохондрий и соответственно к повреждению самих митохондрий, что в свою очередь сопровождается снижением продукции АТФ и в дальнейшем к активации процессов апоптоза клеток [21].
Важным моментом при изучении патогенеза сепсиса, механизмов развития органной дисфункции и недостаточности, а также эффективности проводимого лечения и танатогенеза больных, несомненно, является проведение полноценных клинико-патологоанатомических сопоставлений.
В этой связи заслуживает внимание работа австрийских исследователей [25], посвященная ретроспективному анализу макроскопических изменений органов больных, погибших от сепсиса. В исследованный период времени (1997–2006 гг.) в отделении интенсивной терапии клиники Университета Инсбрука находилось на лечении 415 больных с сепсисом и 442 – с септическим шоком. Общая смертность составила 32,3 % (n = 277), в том числе 11,8 % (49) от сепсиса и 51,5 % (228) от септического шока. Аутопсийное исследование было проведено в 92,4 % (256) случаев. В результате вскрытия тел умерших в 76,6 % (180) наблюдений были выявлены септические очаги: 34 % (80) пациентов имели по одному очагу, 30,6 % (72) – по два, 8,9 % (21) – три и 3 % (7) – четыре очага. Чаще всего (в 41,3 % наблюдений) определялась пневмония, в 28,9 % – трахеобронхит, в 23,4 % – перитонит, в 9,1 % – внутрибрюшные абсцессы и в 6 % – пиелонефрит. При этом авторы указывают на отсутствие различий по частоте и характеру септических очагов у больных с рефрактерной полиорганной недостаточностью и септическим шоком. В качестве наиболее частой причины смерти, по данным C. Torgersen с соавт. [25], фигурировала патология сердечно-сосудистой системы, в том числе в трети наблюдений указана неокклюзионная ишемия миокарда. Авторы также указывают на более частое выявление при аутопсийном исследовании острой дилатации правого желудочка сердца по сравнению с дилатацией левого желудочка, что свидетельствует о преобладании правожелудочковой недостаточности в танатогенезе от сепсиса и септического шока. К сожалению, и на это указывают сами авторы, в работе были проанализированы только макроскопические характеристики.
Гистологическому изучению поражений сердца при сепсисе была посвящена другая работа этих же авторов [26]. Для анализа были взяты образцы ткани из левого и правого предсердия, межжелудочковой перегородки, передней стенки левого и правого желудочка, задней стенки левого и правого желудочка, верхушки и левой сосочковой мышцы 20 больных, погибших от сепсиса и септического шока. Гистологические препараты окрашивали гематоксилином и эозином и трехцветной окраской по Массону. В результате проведенного исследования авторы представили распределение частоты различных микроскопических признаков поражения сердца при сепсисе [26]:
– миоцитолиз – в 100 % наблюдений,
– интерстициальный фиброз – 100 %,
– участки контрактурного некроза – 95 %,
– участки мононуклеарной инфильтрации – 90 %,
– интерстициальный отек – 90 %,
– участки кровоизлияний – 30 %.
В наблюдениях же септикопиемии гнойные очаги значительно чаще отмечались в субэндокардиальных отделах правого желудочка.
Необходимо добавить, что выявляемые при гистологическом исследовании поражения миокарда характеризуются большой вариабельностью по степени выраженности и преимущественной локализации, что, видимо, отражает особенности клинических проявлений дисфункции сердца.
В результате анализа данных литературы о морфологическом изучении сердец экспериментальных животных после моделирования сепсиса M.R.N. Celes с соавт. [27] указывают на следующие изменения: некроз и повреждения кардиомиоцитов, нейтрофильная инфильтрация, субэндокардиальные кровоизлияния, отложения фибрина в микрососудах, интерстициальный и внутриклеточный отек, отек и набухание митохондрий, уменьшение содержания гликогена в клетках,
Наиболее перспективным, по нашему мнению, является проведение иммуногистохимических и молекулярно-биологических исследований. С одной стороны, использование люминесцирующих противомикробных сывороток позволяет не только выявлять на гистологических препаратах органов и тканей различные микроорганизмы (возбудители сепсиса), но и установить их вид. С другой стороны, иммуногистохимическое исследование способствует объективному выяснению звеньев патогенеза дисфункции сердца. Так, при иммуногистохимическом исследовании препаратов миокарда больных, погибших от сепсиса, в 56 % наблюдений была выявлена положительная реакция с маркерами нейтрофилов (лактоферрином и CD15), преимущественно в периваскулярных участках, в контрольной группе реакция отсутствовала [28]. Примечательно, что на препаратах, окрашенных гематоксилином и эозином, признаки воспалительной клеточной реакции отмечались лишь в 32 % случаев. Использование маркера макрофагов – CD68 позволило показать увеличение почти в 15 раз количества и в 2,5 раза размеров макрофагов преимущественно в периваскулярных участках миокарда.
По данным M.A. Rossi c соавт. [29], при сепсисе практически во всех кардиомиоцитах, макрофагах и гладко-мышечных клетках интрамуральных сосудов сердца определяется выраженная положительная экспрессия индуцируемой синтазы оксида азота (iNOS), что вызывает увеличение продукции оксида азота, обладающего отрицательным инотропным эффектом и вызывающего развитие цитолизиса кардиомиоцитов.
В экспериментах по моделированию сепсиса у мышей M.A. Makara с соавт. [30] установили диффузные повреждения кардиомиоцитов межжелудочковой перегородки, левого и правого желудочков сердца. При этом в межжелудочковой перегородке практически отсутствовали CD45-положительные клетки (лейкоциты), но отмечалось увеличение экспрессии генов интерлейкина-1β (IL-1β), интерлейкина-8 (IL-8) и фактора некроза опухолей (TNF), что свидетельствует о прямом повреждающем эффекте провоспалительных цитокинов. Одновременно с этим авторы выявили увеличение апоптоза кардиомиоцитов, выраженное в большей степени в участках с воспалительной инфильтрацией [30]. Иммуногистохимическими методами также было показано увеличение количества клеток (макрофагов, кардиомиоцитов, гладкомышечных клеток и эндотелиоцитов) с положительной экспрессией фактора некроза опухоли (TNF) на препаратах сердца больных, погибших от сепсиса и септического шока [27].
Таким образом, на основании проведенного анализа литературных данных, можно заключить, что сердце занимает важную роль в патогенезе полиорганной недостаточности при сепсисе. Основными клиническими проявлениями сердечной дисфункции считаются левожелудочковая и/или правожелудочковая недостаточность, неадекватный сердечный выброс и развитие аритмий. В основе развития поражения сердца и формирования сердечно-сосудистой недостаточности лежит сложный комплекс различных взаимно усугубляющих реакций и механизмов: непосредственное действие микроорганизмов, активация провоспалительных и противовоспалительных цитокинов с развитием системной воспалительной реакции, нарушения структуры и функции кардиомиоцитов. Перспективным методом изучения звеньев патогенеза сердечной недостаточности и танатогенеза больных с сепсисом является проведение клинико-морфологических сопоставлений.
Активация при сепсисе системы гемостаза обусловлена эндото-ксемией и бактериальными липополисахаридами. Центральным медиатором сепсиса является фактор некроза опухоли (TNF—tumor necrosis factor), который вырабатывается в ответ на поступление эндотоксина. Вторичный медиатор — интерлейкин-1, концентрация которого резко возрастает после поступления в сосудистое русло TNF. Вслед за выработкой этих провоспалительных медиаторов происходит повышение уровня интерлейкина-6, который активизирует синтез в печени белков острой фазы.
Полисахариды грампозитивных бактерий также могут посредством цитокинов активизировать систему гемостаза, что резко увеличивает риск ДВС.
Иногда ДВС индуцируется фулминантной вирусной инфекцией. Тяжело протекающие инфекции сопровождаются обычно лейкоцитозом. Нейтрофильные лейкоциты вырабатывают ряд субстанций (в том числе нейтрофильную эластазу), которые вызывают дефицит AT III, а гепаринотерапия усугубляет этот процесс.
Следует иметь в виду, что применение бактерицидных антибиотиков увеличивает риск возникновения септического шока вследствие массивного поступления в русло эндотоксинов из разрушенных бактерий. Молниеносные формы сепсиса возникают на фоне иммуносупрессивнои терапии. Смертность при септическом шоке достигает 40 %. Септический шок, рефракторный к терапии, быстро, в течение нескольких часов приводит к полиорганной недостаточности и ДВС-синдрому.
В ряде случаев не удается установить возбудителя инфекции в гемокультуре больных сепсисом. Концепция системного воспалительного ответа предполагает наличие сепсиса при отсутствии (невозможности определения) возбудителя в крови в случаях выраженной характерной клиники:
• фебрильная температура (> 38 °С) или гипотермия (> 35,5 °С встречается у 10 % больных);
• тахикардия;
• тахипноэ, гипервентиляция с респираторным алкалозом. Для лабораторных показателей характерно:
• лейкоцитоз > 15 000 /мм3 или лейкопения > 3500 /мм3;
• сдвиг лейкоцитарной формулы влево, токсическая зернистость;
• изменения коагуляции — снижение числа тромбоцитов более чем на 30 % за 24 ч, снижение AT III;
• метаболические сдвиги — гиперлактатемия, гипергликемия, гипофосфатемия.
Для сепсиса характерен дефицит системы естественных антикоагулянтов, причем снижение AT III происходит ранее основных клинических проявлений сепсиса. При снижении содержания AT III ниже 60 % смертность резко возрастает.
Количество тромбоцитов при сепсисе снижается вследствие тромбоцитопении потребления — тромбоциты связываются с фибрином, адгезируют к поврежденному эндотелию, секвестрируются в легких и печени. Тромбоцитопатия — снижение агрегирующих свойств тромбоцитов — может быть вызвана длительным применением антибиотиков.
Лечение сепсиса, септического шока и ДВС-синдрома должно носить комплексный характер и основываться на следующих принципах:
1. Хирургическое лечение очага инфекции (санация и дренирование).
2. Антибиотикотерапия, основанная на идентификации возбудителя и определении его чувствительности к соответствующей группе антибиотиков.
3. Адекватная оксигенация — необходима ранняя ИВЛ в различных режимах.
4. Инфузионная терапия — высока опасность гипергидратации, особенно в условиях тканевой гипоксии и повышения капиллярной проницаемости. Трансфузия эритроцитов не только повышает кислородтранспортную функцию крови, но и обеспечивает эффективность трансфузионной терапии. Критическим для септических больных считается содержание гемоглобина менее 70—80 г/л. Предпочтительна трансфузия свежезаготовленной эритроцитной массы.
5. Применение катехоламинов. Содержание фактора некроза опухоли (TNF) при сепсисе значительно возрастает (TNF — медиатор, обладающий выраженным кардиодепрессйвным действием).
6. Препараты AT III.
В 1985 году В. Blauhut опубликовал результат клинических исследований по применению препарата AT III (кубернина HS). У пациентов с клиникой септического шока и ДВС, которым был назначен кубернин HS, отмечено ускоренное восстановление показателей коагуляции, хотя и не было отмечено снижение смертности.
Некоторые исследователи рекомендуют поддерживать содержание AT III на уровне 140 %, это возможно при введении препарата в суммарной дозе 18 000 ЕД. Содержание AT III не должно снижаться менее 80 %.
9. Поливалентные иммуноглобулины используются для нейтрализации эндотоксинов. Отмечено снижение смертности при их применении у кардиохирургических больных.
10. Методы экстракорпоральной детоксикации: гемофильтрация, плазмаферез.
- Вернуться в оглавление раздела "Хирургия"
Определение
Определение сепсиса показывает эволюцию взглядов на этиологию и патогенез данного состояния. Само определение неоднократно менялось, ранее считалось, что главенствующую роль в патогенезе играет системный воспалительный ответ, однако на данный момент центральную роль отводят нарушению действий воспалительной и противовоспалительной систем. Решение о необходимости изменения дефиниции было принято в 2017 году European Society of Intensive Care Medicine и Society of Critical Care Medicine.
Сепсис ― угрожающая жизни органная дисфункция, вызванная дезрегулирующим ответом организма хозяина на инфекцию.
Септический шок ― подвид сепсиса, в основе которого лежит нарушение циркуляции, а патологические изменения в клетках и метаболизме достаточно глубоки, чтобы в значительной степени увеличить летальность.
Диагностика
Исходя из определения и патогенеза, для скрининга сепсиса было предложено использовать шкалу qSOFA (quick Sepsis-related Organ Failure Assessment).
- Системное артериальное давление ≤ 100 мм рт. ст.;
- Частота дыхания ≥ 22 в минуту;
- Любое нарушение сознания ( Таблица 1 | Критерии SOFA
После выставления диагноза проводится начальная интенсивная терапия, важной частью которой является проведение массивной инфузии, далее определяется среднее артериальное давление (СрАД), а также уровень лактата. Среднее артериальное давление определяется по формуле: СрАД = САД – ДАД + ⅓ ДАД, где САД ― систолическое артериальное давление, а ДАД ― диастолическое артериальное давление. При необходимости применения вазопрессоров для поддержания адекватного среднего артериального давления ( ≥ 65 мм рт. ст.), а также при высоком уровне лактата ( > 2 ммоль/л) выставляется диагноз септический шок.
Начальная терапия
Интенсивная терапия сепсиса должна начинаться сразу же после постановки диагноза. Рекомендации по ведению сепсиса 2012 года предлагали использовать цели, которые необходимо было достигнуть за определенное время. К сожалению, после проведения крупных испытаний данная стратегия не показала преимуществ по сравнению со стандартной терапией, а также оказалась более затратной.
После выявления сепсиса для коррекции сепсис-индуцированной гипоперфузии в начальном периоде используются кристаллоиды в объеме 30 мл/кг внутривенно в первые 3 часа. Последующая инфузия должна проводиться на основании имеющихся в наличии данных о физиологии пациента (частота сердечных сокращений, артериальное давление, артериальная сатурация кислорода, частота дыхания, температура и другие данные), полученных с помощью неинвазивных и инвазивных методов. Предпочтение желательно отдавать динамическим методам измерения.
У пациентов с септическим шоком, требующим применения вазопрессоров, необходимо поддерживать среднее артериальное давление на уровне не менее 65 мм рт. ст. Пациентам с повышенными уровнями лактата (маркер тканевой гипоперфузии) необходимо проводить интенсивную инфузионную терапию с целью его снижения до нормальных уровней.
Всем организациям здравоохранения рекомендуется разрабатывать собственные или усовершенствовать имеющиеся программы по ведению сепсиса и септического шока, методам скрининга у тяжелобольных пациентов, а также оценке риска развития сепсиса. Допустимо применение других шкал для скрининга состояния тяжелобольных пациентов: привычная шкала ССВО, LODS (Logistic Organ Disfunction System), NODS (National Organ Disfunction System).
Интенсивная терапия сепсиса
Антибактериальная терапия
До начала антибактериальной терапии необходимо взять посевы (кровь, спинномозговую жидкость, мочу, секрет из дыхательных путей, раневое отделяемое или другие жидкости организма) для определения чувствительности микроорганизмов к антибиотикам с использованием как минимум двух наборов культур: анаэробной и аэробной. Однако взятие посевов не должно существенно затягивать начало антибактериальной терапии сепсиса. Антибиотикотерапия должна начинаться в максимально ранние сроки, до 1 часа после постановки диагноза сепсиса или септического шока. Любое промедление в назначении антибактериальных средств значительно повышает смертность пациентов. Эмпирическую антимикробную терапию рекомендуется начинать с одного или нескольких антибиотиков (АБ) из двух разных классов, с широким спектром активности, действующих на предполагаемую флору (бактериальную и/или грибковую).
При выборе АБ необходимо учитывать: анатомический источник и типичную его флору, преобладающую флору в госпитале или вне его, резистентность преобладающего патогена, иммунные нарушения у пациента (нейтропения, спленэктомия, плохо контролируемая ВИЧ-инфекция, приобретенные или врожденные дефекты иммуноглобулина, системы комплемента или функции лейкоцитов), а также возраст пациента и наличие сопутствующей патологии, хронических заболеваний. Дозу и время введения необходимо оптимизировать на основании фармакодинамики/фармакокинетики и специфических свойств препаратов. Необходимо помнить о том, что у пациентов зачастую есть нарушение функции почек и/или печени, а также о возможной резистентности микроорганизмов. При применении бета-лактамных АБ важно достигнуть концентраций выше минимальной ингибирующей в течение как можно более длительного времени, в то время как для аминогликозидов и фторхинолонов главную роль играет достижение пиковой концентрации.
Деэскалацию (замена АБ широкого спектра действия на АБ более узкого спектра действия) антибактериальной терапии проводят в течение нескольких последующих дней после того, как определены микроорганизмы, вызвавшие сепсис и септический шок, и их спектр чувствительности к антибиотикам, либо наступает значительное клиническое улучшение/ухудшение. По возможности каждый день оцениваются клинические данные, и на их основании проводится решение об деэскалации. Рекомендуемая длительность антибактериальной терапии составляет 7–10 дней, что зачастую достаточно для большинства серьезных инфекций, ассоциированных с развитием сепсиса и септического шока.
При проведении антибиотикотерапии необходимо руководствоваться уровнем прокальцитонина (ПКТ), это позволяет сократить продолжительность курса, а также отменить АБ у пациентов, у которых имелись подозрение на сепсис и слабые доказательства наличия инфекции. При снижении уровня прокальцитонина более, чем на 80 % от пикового значения или снижении ПКТ менее 0,5 мкг/л необходимо прекратить введение АБ.
Контроль очага
Необходимо как можно быстрее (не позже 6‒12 часов после постановки диагноза) выявить или исключить наличие очага инфекции в организме и провести вмешательство по его удалению. Следует обратить особое внимание на внутрисосудистые девайсы (центральные венозные катетеры), так как они могут быть источниками инфекции.
Инфузионная терапия
Препаратами выбора для инфузионной терапии при развитии сепсиса и септического шока являются кристаллоиды. Предпочтительней применять сбалансированные растворы, так как они не вызывают развитие гиперхлоремического метаболического ацидоза (раствор Хартмана или Рингер-лактат), при их отсутствии допустимо применение несбалансированных растворов (Рингер или физиологический раствор NaCl 0,9 %). Недостаточно данных об использовании препаратов желатина для восстановления объема внутрисосудистого русла при сепсисе.
При необходимости инфузии значительных объемов кристаллоидов допускается добавление инфузии коллоидов (альбумина 20 %) с целью достижения плазменного уровня альбумина > 30 г/л. На основании данных проведенных исследований не рекомендуется использование при сепсисе и септическом шоке растворов гидроксиэтилкрахмала.
Вазоактивные препараты
Добутамин может назначаться пациентам, имеющим признаки тканевой гипоперфузии, на фоне адекватной инфузии и использовании других вазопрессоров. Дозу данного препарата необходимо тщательно титровать для достижения желаемого эффекта (восстановление тканевой перфузии), а при развитии аритмий или усугублении гипотензии незамедлительно прекратить его введение. Всем пациентам с септическим шоком желательно установить артериальный катетер для контроля показателей гемодинамики.
Кортикостероиды
Нет необходимости использовать глюкокортикоиды, когда на фоне инфузионной терапии и применения вазопрессоров достигнута гемодинамическая стабильность. Если же невозможно поддерживать гемодинамику на должном уровне на фоне приведенной выше терапии (инфузия + прессоры), допускается применение гидрокортизона внутривенно в дозе 200 мг/сутки.
Препараты крови
Трансфузия эритроцитов проводится при снижении уровня гемоглобина менее 70 г/л у взрослых без признаков тяжелой гипоксемии, ишемии миокарда или острого кровотечения. Эритропоэтин у пациентов с сепсисом не применяется. Свежезамороженная плазма может использоваться при нарушениях свертываемости крови перед планированием инвазивных процедур или при наличии активного кровотечения.
Трансфузия тромбоцитов проводится в зависимости от клинической необходимости при уровне:
- 9 , если отсутствует риск кровотечения;
- 9 при наличии значительного риска развития кровотечения;
- ≤ 50 х 10 9 при наличии активного кровотечения, проведении хирургического вмешательства или инвазивной процедуры.
Иммуноглобулины
Эксперты не рекомендуют использовать иммуноглобулины у пациентов с сепсисом и септическим шоком.
Очистка крови
Эффект применения различных технологий очистки крови не доказан. Необходимо провести дополнительные исследования.
Искусственная вентиляция легких (ИВЛ)
На фоне сепсиса у пациентов часто развивается сепсис-индуцированный острый респираторный дистресс синдром (ОРДС). При развитии ОРДС проводится ИВЛ со следующими параметрами:
- Целевой дыхательный объем 6 мл/кг на прогнозируемую массу тела (ПМТ). ПМТ у мужчин = 50 + 0,91 * (рост в см – 152,4), ПМТ у женщин = 45,5 + 0,91 * (рост в см –152,4);
- Верхний предел давления плато (Рplat) = 30 см вод. ст.;
- Высокий PEEP — около 10‒12 см вод. ст., для подбора оптимального PEEP можно использовать таблицы, основанные на значениях FiO2;
- Использование рекрутмент маневра и прон-позиции при отношении PaO2/FiO2 Седация и анальгезия
Необходимо избегать продолжительной или интермиттирующей седации пациентов, которым проводится ИВЛ. Если же все-таки необходима седация, то предпочтительнее использовать короткодействующие препараты (пропофол или дексмедетомидин).
Контроль гликемии
Рекомендуется поддержание уровня глюкозы ≤ 10 ммоль/л. При наличии двух последовательных проб крови с превышением данного уровня глюкозы необходимо незамедлительно начать введение инсулина. Мониторинг гликемии проводится каждые 1–2 часа до момента, когда уровни глюкозы и инфузия инсулина не стабилизируются; после стабилизации контроль проводится каждые 4 часа. Для измерения уровней глюкозы предпочтительнее использовать артериальную кровь. Допустимо использование портативных глюкометров, однако нужно критически относиться к результатам данных исследований.
Почечно-заместительная терапия (ПЗТ)
При развитии у пациентов с сепсисом острого повреждения почек и наличии показаний к диализу может применятся длительная или перемежающаяся почечно-заместительная терапия. Во время ПЗТ возможен контроль и изменение баланса жидкости у гемодинамически нестабильных пациентов.
Применение бикарбоната натрия
Не рекомендуется раннее применение бикарбоната натрия при индуцированном гипоперфузией лактат-ацидозе с pH ≥ 7,15.
Профилактика венозной тромбоэмболии (ВТЭ)
Рекомендуется проводить профилактику ВТЭ у пациентов с сепсисом и септическим шоком, предпочтительнее низкомолекулярными гепаринами (НМГ) либо с помощью нефракционированного гепарина (НФГ). Возможно использование механических методов профилактики (компрессионные чулки или устройства для перемежающейся пневматической компрессии) как дополнение к основной терапии или как самостоятельный метод при наличии противопоказаний к применению НМГ и НФГ .
Не рекомендуется применение антитромбина III.
Профилактика язв
У пациентов с сепсисом и септическим шоком, имеющих факторы риска желудочно-кишечного кровотечения (проведение ИВЛ > 48 часов, заболевания печени, коагулопатии, проведение ПЗТ), необходимо проводить профилактику стрессовых язв с помощью блокаторов протонной помпы или антагонистов Н2-гистаминовых рецепторов.
Питание
Рекомендуется раннее начало энтерального питания у пациентов с сепсисом. В зависимости от переносимости могут использоваться трофические/гипокалорические смеси или полное раннее энтеральное питание. Начинать парентеральное питание следует не ранее 8 суток при невозможности обеспечить раннее энтеральное питание. При непереносимости энтерального питания или наличии высокого риска аспирации может проводиться измерение остаточного объема желудка, а также использоваться пост-пилорические зонды для кормления. Пациентам с гастропарезом, диабетом или получающим седативные и вазоактивные препараты может потребоваться применение прокинетиков (метоклопрамид, домперидон). При применении прокинетиков необходим ЭКГ мониторинг для ранней детекции синдрома удлиненного QT и снижения риска внезапной смерти.
Отсутствуют данные о положительном эффекте применения омега-3-жирных кислот, внутривенного введения селена, аргинина, глютамина и карнитина.
Источники:
- Singer M. et al. The third international consensus definitions for sepsis and septic shock (Sepsis-3) //Jama. – 2016. – Т. 315. – №. 8. – С. 801-810.
- Rhodes A. et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock: 2016 //Intensive care medicine. – 2017. – Т. 43. – №. 3. – С. 304-377.
Читайте также:


