Геморрагический синдром при сепсисе
Активация при сепсисе системы гемостаза обусловлена эндото-ксемией и бактериальными липополисахаридами. Центральным медиатором сепсиса является фактор некроза опухоли (TNF—tumor necrosis factor), который вырабатывается в ответ на поступление эндотоксина. Вторичный медиатор — интерлейкин-1, концентрация которого резко возрастает после поступления в сосудистое русло TNF. Вслед за выработкой этих провоспалительных медиаторов происходит повышение уровня интерлейкина-6, который активизирует синтез в печени белков острой фазы.
Полисахариды грампозитивных бактерий также могут посредством цитокинов активизировать систему гемостаза, что резко увеличивает риск ДВС.
Иногда ДВС индуцируется фулминантной вирусной инфекцией. Тяжело протекающие инфекции сопровождаются обычно лейкоцитозом. Нейтрофильные лейкоциты вырабатывают ряд субстанций (в том числе нейтрофильную эластазу), которые вызывают дефицит AT III, а гепаринотерапия усугубляет этот процесс.
Следует иметь в виду, что применение бактерицидных антибиотиков увеличивает риск возникновения септического шока вследствие массивного поступления в русло эндотоксинов из разрушенных бактерий. Молниеносные формы сепсиса возникают на фоне иммуносупрессивнои терапии. Смертность при септическом шоке достигает 40 %. Септический шок, рефракторный к терапии, быстро, в течение нескольких часов приводит к полиорганной недостаточности и ДВС-синдрому.
В ряде случаев не удается установить возбудителя инфекции в гемокультуре больных сепсисом. Концепция системного воспалительного ответа предполагает наличие сепсиса при отсутствии (невозможности определения) возбудителя в крови в случаях выраженной характерной клиники:
• фебрильная температура (> 38 °С) или гипотермия (> 35,5 °С встречается у 10 % больных);
• тахикардия;
• тахипноэ, гипервентиляция с респираторным алкалозом. Для лабораторных показателей характерно:
• лейкоцитоз > 15 000 /мм3 или лейкопения > 3500 /мм3;
• сдвиг лейкоцитарной формулы влево, токсическая зернистость;
• изменения коагуляции — снижение числа тромбоцитов более чем на 30 % за 24 ч, снижение AT III;
• метаболические сдвиги — гиперлактатемия, гипергликемия, гипофосфатемия.
Для сепсиса характерен дефицит системы естественных антикоагулянтов, причем снижение AT III происходит ранее основных клинических проявлений сепсиса. При снижении содержания AT III ниже 60 % смертность резко возрастает.
Количество тромбоцитов при сепсисе снижается вследствие тромбоцитопении потребления — тромбоциты связываются с фибрином, адгезируют к поврежденному эндотелию, секвестрируются в легких и печени. Тромбоцитопатия — снижение агрегирующих свойств тромбоцитов — может быть вызвана длительным применением антибиотиков.
Лечение сепсиса, септического шока и ДВС-синдрома должно носить комплексный характер и основываться на следующих принципах:
1. Хирургическое лечение очага инфекции (санация и дренирование).
2. Антибиотикотерапия, основанная на идентификации возбудителя и определении его чувствительности к соответствующей группе антибиотиков.
3. Адекватная оксигенация — необходима ранняя ИВЛ в различных режимах.
4. Инфузионная терапия — высока опасность гипергидратации, особенно в условиях тканевой гипоксии и повышения капиллярной проницаемости. Трансфузия эритроцитов не только повышает кислородтранспортную функцию крови, но и обеспечивает эффективность трансфузионной терапии. Критическим для септических больных считается содержание гемоглобина менее 70—80 г/л. Предпочтительна трансфузия свежезаготовленной эритроцитной массы.
5. Применение катехоламинов. Содержание фактора некроза опухоли (TNF) при сепсисе значительно возрастает (TNF — медиатор, обладающий выраженным кардиодепрессйвным действием).
6. Препараты AT III.
В 1985 году В. Blauhut опубликовал результат клинических исследований по применению препарата AT III (кубернина HS). У пациентов с клиникой септического шока и ДВС, которым был назначен кубернин HS, отмечено ускоренное восстановление показателей коагуляции, хотя и не было отмечено снижение смертности.
Некоторые исследователи рекомендуют поддерживать содержание AT III на уровне 140 %, это возможно при введении препарата в суммарной дозе 18 000 ЕД. Содержание AT III не должно снижаться менее 80 %.
9. Поливалентные иммуноглобулины используются для нейтрализации эндотоксинов. Отмечено снижение смертности при их применении у кардиохирургических больных.
10. Методы экстракорпоральной детоксикации: гемофильтрация, плазмаферез.
- Вернуться в оглавление раздела "Хирургия"

Лёгкие превращаются в кровавую губку. А почки отказывают. Таков результат разрушительной работы коронавируса в организме.
Известно, что самый точный диагноз ставят не врачи, а патологоанатомы после вскрытия пациента. Увы, коронавирус уже оставил после себя немало жертв. Как именно он выводит из строя жизненно важные функции, теперь точно известно.
Могут ли восстановиться лёгкие?
Лев Кактурский: На вскрытии лёгкие умерших от коронавирусной пневмонии увеличены в объёме, уплотнены, как при любой другой пневмонии. Но есть и отличие – резко выраженный отёк со скоплением в лёгочной ткани геморрагической жидкости (то есть жидкости с примесью крови). Именно отёк, причём гораздо более масштабный, чем при тяжёлом осложнённом гриппе, и последующие изменения в лёгких вызывают острую дыхательную недостаточность. Внешне поверхность разреза лёгочной ткани имеет вишнёво-красный цвет, часто пористый вид, с поверхности разреза при надавливании стекает тёмно-красная жидкость (геморрагический экссудат). Ясно, что при такой ситуации лёгкое неспособно осуществлять нормальный газообмен между кровью и воздухом, на пути создаётся преграда из воспалительной жидкости. Вот почему у больного коронавирусом возникает острая дыхательная недостаточность, он синеет, начинает хватать ртом воздух. Здесь необходима срочная искусственная вентиляция лёгких (ИВЛ).

– Это спасает?
– Не всегда. Но если больной переживёт острый период, то примерно через неделю в лёгочной ткани начинают развиваться склеротические изменения, при которых лёгочная ткань замещается плотной соединительной тканью, по типу рубцовой. Участки рубцовой ткани полностью выключены из газообмена. У больных развивается хроническая дыхательная недостаточность. У молодых эти склеротические изменения не так сильно выражены, и функция лёгких после болезни может полностью восстановиться. Есть основание полагать, что лица мужского пола более подвержены коронавирусной пневмонии, но это ещё требует подтверждения.
Откуда берутся тромбы и сепсис?
– Были предположения, что коронавирус вызывает повреждения не только лёгких, но и мочеполовой системы, других органов.
– Наиболее опасны изменения функции почек. Из-за нарушения кровообращения может развиться острая почечная недостаточность вследствие сброса крови из артерий непосредственно в вены, минуя почечный фильтр. Как это возникает? В почках происходит фильтрация крови через клубочковые капилляры. За счёт этого формируется моча, и все шлаки с ней выводятся наружу. При коронавирусной пневмонии эта фильтрация может быть нарушена, кровь минует почечный фильтр, в результате чего не происходит её очистки, возникает задержка мочи и отравление организма вредными продуктами клеточного распада.

– Говорили, что COVID-19 может приводить к тромбоэмболии, когда сосуды перекрывают тромбы. Это так?
– Тромбоэмболия крупных сосудов может быть, но нехарактерна. При тяжёлом течении пневмонии может развиться грозное осложнение – сепсис. А при сепсисе возникает так называемый тромбогеморрагический синдром. При этом в мельчайших кровеносных сосудах (капиллярах) формируются мелкие тромбы (микротромбы), они закупоривают просвет сосуда, и органы не получают нужного кровоснабжения. Развивается полиорганная недостаточность, когда нарушается функция многих органов.
– Насколько часто возникают описанные смертельные осложнения?
– 80% больных и более переносят коронавирусную инфекцию, как обычную ОРВИ (острую респираторно-вирусную инфекцию) или как обычный сезонный грипп, без таких тяжёлых осложнений. Некоторые переносят вообще на ногах, как лёгкое недомогание. А часть заражённых вообще не подозревают об этом, считая себя здоровыми. Но такие носители инфекции опасны тем, что могут заразить других людей. Вот почему лица из групп риска (вернувшиеся из эпидемических очагов, из заражённых стран) должны обязательно пройти диагностический тест, чтобы не подвергать близких опасности.

Сепсис — это самая тяжелая, генерализованная форма инфекционного процесса, которая развивается либо при высокой патогенности возбудителя, либо при недостаточном ответе защитных систем организма. Международным консенсусом рекомендовано использовать следующее определение: сепсис — это опасная для жизни дисфункция внутренних органов, вызванная нарушением регуляции ответа организма на инфекцию. При сепсисе наблюдается общий интоксикационный синдром, тромбогеморрагический синдром (кровоизлияния) и поражение внутренних органов.
Причины возникновения сепсиса
Сепсис может быть вызван большинством известных в эпидемиологии микроорганизмов, среди которых бактерии, вирусы (в том числе сезонные вирусы гриппа), грибы, паразиты. Обычно возбудитель инфекции попадает в организм из внешней среды. При определенных условиях, например, при иммунодефицитах, заболевание может развиться от естественной, условно-патогенной флоры организма, которая в норме присутствует у каждого человека.
Само по себе наличие инфекции еще не является гарантией развития сепсиса. Необходимы дополнительные условия, которые приведут к генерализации процесса и патологическому ответу организма. Вероятность таких событий увеличивается в следующих случаях:
- Возраст больного старше 75 лет.
- Выполнение операций или инвазивных процедур.
- Наличие травм и ожогов.
- Нарушения иммунной системы — СПИД, онкологические заболевания, проведение химиотерапии, необходимость применения иммуносупрессивной терапии (например, после трансплантации органов), необходимость приема высоких доз глюкокортикостероидов.
- Долгое лечение в условиях стационара.
- Наличие катетеров, канюль, зондов и других инвазивных устройств.
- Беременность и роды.
- Наличие химической зависимости — алкоголизм, наркомания.
- Наличие хронических заболеваний — хроническая почечная недостаточность, дыхательная недостаточность, сахарный диабет и многое другое.
Виды сепсиса
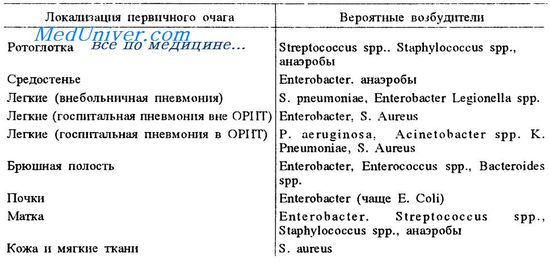
В зависимости от расположения первичного очага инфекции, выделяют первичный (криптогенный) и вторичный сепсис. При первичном, очаг инфекции установить не удается. При вторичном сепсисе таковой очаг имеется. В зависимости от его локализации, выделяют:
- Чрескожный сепсис. Первичный очаг находится на коже, это могут быть раны, ожоги, гнойные заболевания кожи (гнойные абсцессы, фурункулы и др).
- Одонтогенный сепсис. Причиной его развития может стать кариес, пульпит, периодонтит, челюстной остеомиелит и другие заболевания зубочелюстной системы.
- Отогенный сепсис. Первичным очагом является воспалительный процесс в ухе. Как правило, это гнойные отиты среднего уха.
- Гинекологический сепсис — первичный очаг располагается в половых органах женщины.
- Хирургический сепсис — развивается в результате инфицирования хирургической раны или при инфицировании во время проведения инвазивных процедур.
Первые признаки и симптомы сепсиса
Определить первые признаки сепсиса бывает непросто, даже для специалистов. Это связано с тем, что, во-первых, этот синдром развивается уже на фоне существующей патологии, которая может иметь самую разнообразную симптоматику, а во-вторых, при наличии иммунодефицита, клиническая картина может быть стертой. Тем не менее, есть некоторые симптомы, которые позволяют заподозрить начало сепсиса:
- Повышение или понижение температуры тела — выше 38 и ниже 36 градусов.
- Снижение давления ниже рабочего значения.
- Увеличение частоты пульса.
- Увеличение частоты дыхательных движений (одышка).
- Снижение количества выделенной мочи.
- Общая слабость, изможденность.
- Нарушение сознания или поведения.
Особое внимание возникновению этих признаков уделяют у хронических больных, при наличии лейкопении, онкологических заболеваний и у пациентов, перенесших травмы или хирургические вмешательства. При возникновении хотя бы 2-3 таких симптомов, следует немедленно связаться с врачом.
Диагностика сепсиса
Своевременная диагностика сепсиса имеет решающее значение для выздоровления больного. Чем раньше начато лечение, тем больше шансов на успех. Диагноз выставляется на основании данных клинического осмотра и лабораторно-инструментального обследования.

- Температура тела более 38 градусов или менее 36 градусов.
- Частота сердечных сокращений более 90 или превышает возрастную норму.
- Частота дыхания более 20 раз в минуту.
- Наличие отеков.
- Спутанность сознания.
- Повышение уровня глюкозы в крови более 7,7 мкмоль/л при отсутствии диабета.
- Нарушение гемодинамических процессов — снижение систолического артериального давления менее 90 мм.рт.ст, либо его снижение более чем на 40 мм.рт.ст. от привычного значения.
Проводят общий анализ крови с подсчетом лейкоцитарной формулы и определением количества тромбоцитов. При сепсисе определяется лейкоцитоз более 12*109/л или лейкопения, когда количество лейкоцитов ниже 4*109/л. Также отмечается выход в кровяное русло незрелых форм гранулоцитов и уменьшение количества тромбоцитов.
В биохимическом анализе крови отмечается увеличение С-реактивного белка, креатинина, билирубина. Но это неспецифичные признаки, которые могут наблюдаться и при других заболеваниях. Поэтому продолжается поиск более информативных методов диагностики.
На сегодняшний день главными таким маркерами являются прокальцитонин, пресепсин, СРБ. По данным этого лабораторного показателя устанавливают диагноз и отслеживают динамику заболевания.
Обнаружение в крови микроорганизмов является важным, но не обязательным проявлением сепсиса. Даже при использовании самых современных диагностических систем и при тщательном соблюдении техники забора материала, выделить возбудитель из крови удается менее, чем в половине случаев. Поэтому отрицательный результат бакпосева при наличии клинической симптоматики не должен расцениваться как отсутствие сепсиса, и, наоборот, выделение микроорганизмов из крови при отсутствии симптоматики, должно расцениваться как транзиторная бактериемия или вирусемия, но не как сепсис.
Тем не менее, биологические исследования в любом случае должны присутствовать, как один из этапов диагностики сепсиса по следующим причинам:
- Возможность определения этиологии возбудителя.
- Подбор или смена режимов антибиотикотерапии.
- Контроль эффективности лечения.
- В некоторых случаях позволяет определить источник инфекции, например, катетер-связанная инфекция, эндокардиты и др.
Стадии развития сепсиса
Развитие и течение септического процесса индивидуально и зависит как от свойств возбудителя, так и от особенностей организма больного. Тем не менее, можно выделить несколько фаз течения данного заболевания:
Что касается продолжительности заболевания, то здесь все опять же индивидуально. У одних, более сильных пациентов, сепсис купируется в течение 3-4 недель, у других он может протекать годами, периодически стихая и вспыхивая.
Кроме того, при диагностике сепсиса выделяют следующие состояния.
Токсико-резорбтивная лихорадка — состояние, которое развивается при всасывании бактериальных токсинов или продуктов тканевого распада из первичного патологического очага. Как правило, это характерно для бактериальных инфекций ран, катетеров и др. Характерны общие типовые синдромы, которые сопровождают инфекционные процессы — лихорадка, изменения в общем анализе крови и мочи (лейкоцитоз, протеинурия). При ликвидации первичного очага, состояние пациента стабилизируется.
Септицемия — форма сепсиса, при которой наблюдается выраженный интоксикационный синдром, гиперэргия (повышенная реакционность организма) и быстрое течение. Септические очаги либо выражены минимально, либо отсутствуют. Такая форма сепсиса больше характерна для детей первых лет жизни. Для клинической картины больше характерны общие проявления:
- Гемолитическая желтуха, сопровождающаяся пожелтением кожных покровов и склер.
- Сыпь. Сначала она проявляется в виде мелких розовых точек, которые разрастаются и сливаются между собой, образуя бледно-розовые или пурпурные пятна.
- У некоторых пациентов элементы сыпи могут покрываться пузырями или язвами. При глубоких поражениях может затрагиваться подкожная жировая клетчатка с развитием флегмонозного воспаления.
- Геморрагический синдром — кровоизлияния во внутренние органы.
Септикопиемия — это форма сепсиса, при которой в организме, помимо общей интоксикации, начинают возникать метастатические абсцессы в органах и тканях, которые являются результатом бактериальной эмболии. Чаще всего первые абсцессы обнаруживаются в легких, а затем процесс распространяется на другие органы: печень, печень, сердце, менингиальные оболочки, синовиальные оболочки. Абсцессы могут прорваться и вызвать развитие эмпиемы плевры, флегмоны, перитонита и др.
Лечение сепсиса
Лечение сепсиса базируется на трех принципах:
Санация первичного очага. Это может быть достигнуто с помощью хирургического вмешательства и/или адекватной антибактериальной терапии. При обнаружении первичного очага, который можно санировать хирургически, необходимо провести это как можно скорее. Это может быть вскрытие и дренирование абсцессов, удаление инфицированных инвазивных устройств (катетеры, имплантаты и др.), дренирование и лаваж брюшной полости, и др.
Антимикробная терапия является еще одним краеугольным камнем лечения сепсиса, при этом важна ее своевременность и адекватность. Например, при развитии септического шока, препараты должны быть введены в течение часа от начала симптомов. При этом препарат должен охватывать весь спектр предполагаемых возбудителей и, что немаловажно, проникать в первичный инфекционный очаг. При необходимости назначения комбинированной терапии из нескольких препаратов, их применяют не более 5 дней, после чего должны быть получены данные биологических методов исследования и произведена коррекция схемы лечения.
Обеспечение транспорта кислорода — все клинические проявления сепсиса усугубляются в условиях недостатка кислорода, поэтому очень важно контролировать этот процесс. Для этого проводят:
- Гемодинамическую поддержку — вливание растворов, которые обеспечивают восполнение водно-электролитного баланса, назначаются препараты, поддерживающие артериальное давление и др.
- Респираторную поддержку — искусственную вентиляцию легких, кислородные маски и др.
Коррекция метаболических нарушений
- Обеспечение поступления необходимых питательных веществ (белков, жиров, углеводов). Если пациент не в состоянии сам принимать пищу или питательные смеси, рассматривается вариант заместительной терапии.
- Контроль уровня глюкозы.
- Детоксикационные мероприятия.
Одним из эффективных способов лечения сепсиса является селективная сорбция на колонках TORAYMYXIN. Данная методика успешно применяется во многих странах мира. В настоящее время такое лечение прошли более 200 тысяч пациентов с септическим шоком и тяжелыми формами сепсиса. Эффективность и безопасность технологии подтверждена в ходе клинических исследований.
Осложнения при сепсисе
- Осложнения со стороны дыхательной системы. Нарушение вентиляции легких приводит к повышению аэрогематического барьера и, как следствие, пропотеванию жидкости в альвеолы. Это еще больше нарушает газообмен и приводит к развитию шокового легкого и респираторного дистресс-синдрома, который усугубляется усталостью дыхательных мышц.
- Осложнения со стороны почек. Наблюдается снижение фильтрационной функции почек из-за повреждения канальцев, развившееся в результате снижения давления. Сопровождается резким уменьшением выделяемой мочи, протеинурией, азотемией.
- Нарушение свертывания крови из-за падения уровня тромбоцитов и развития ДВС-синдрома — грозного состояния, при котором сначала происходит массовое образование тромбов в кровеносном русле, а затем массивные кровотечения из-за недостаточности кровесвертывающих факторов.
- Неврологические осложнения. Длительно протекающий сепсис может привести к развитию полинейропатии, которая, в частности, приводит к ослаблению дыхательной мускулатуры и невозможности самостоятельного дыхания.
- Септический шок — самое тяжелое проявление сепсиса, сопровождающееся стойким снижением кровяного давления, которое сложно восстановить даже с применением инфузионной терапии и вазопрессоров. Он развивается из-за выхода жидкости из кровеносных сосудов и из-за общего обезвоживания. При этом, нарушения настолько тяжелые, что могут привести к гибели пациента от полиорганной недостаточности.
Прогноз при сепсисе
Прогноз при сепсисе очень осторожный. На возможность выздоровления оказывают влияние особенности этиологической микрофлоры, общее состояние пациента в начале заболевания, а также своевременность и адекватность проводимого лечения. Наиболее неблагоприятно сепсис протекает у людей старческого возраста и у ослабленных пациентов, имеющих сопутствующие заболевания.
В целом в крупных клиниках летальность при данном состоянии составляет 30-40%. При развитии септического шока, ситуация усугубляется и согласно некоторым данным, в таком случае от него погибает до 90% больных.
При сепсисе различают местные и общце изме-нения. Местные изменения развиваются в очаге внедрения инфекции (входные ворота) или в отдалении от него. Образуется септический очаг, который представляет собой фокус гнойного воспаления (в некоторых случаях септический очаг отсутствует). Из септического очага инфекция быстро распространяется по лимфатическим и кровеносным сосудам. Распространение инфекции по лимфатической системе ведет к развитию лимфангита, лимфотромбоза и лимфаденита, а распространение ее по кровеноснойсистеме (по венам) – к развитию флебита и тромбофлебита. Нередко возникает гнойный тромбофлебит, что ведет к расплавлению тромбов и тромбобактериальной эмболии.
Общие изменения при сепсисе имеют характер дистрофических, воспалительных и гиперпластических. Дистрофические изменения развиваются в паренхиматозных органах (печень, почки, миокард, мышцы, ЦНС) и проявляются различными видами дистрофии и некробиозом, которые нередко завершаются некрозом.
Воспалительные изменения представлены межуточными процессами (межуточный септический нефрит, гепатит, миокардит – рис. 281). На клапанах сердца может возникать острый полипозно-язвенный эндокардит (рис. 282) с расплавлением ткани и отрывом клапанов. Воспалительные изменения возникают в сосудах (васкулиты), что обусловливает появление множественных геморрагий. Однако геморрагический синдром связан при сепсисе не только с васкулитами, но и с интоксикацией, повышенной сосудисто-тканевой проницаемостью, анемией и т. д.
Гиперпластические процессы при сепсисе наблюдаются главным образом в кроветворной и лимфатической (иммунокомпетентной) тканях. Происходит гиперплазия костного мозга плоских костей. Желтый костный мозг трубчатых костей становится красным, в крови увеличивается количество лейкоцитов, иногда появляются молодые формы лейкоцитов, развивается так называемая лейкемоидная реакция. Гиперплазия лимфатической ткани приводит к увеличению размеров лимфатических узлов, селезенки, которая становится не только резко увеличенной, но и дряблой, на разрезе имеет красный цвет и дает обильный соскоб пульпы (септическая селезенка). Гиперпластичекие процессы в гистиоцитарно-макрофагальной системе объясняют увеличение печени. В связи с гемолитическим действием некоторых бактериальных токсинов при сепсисе может возникнуть гемолитическая желтуха.
Классификация.
При классификации сепсиса необходимо учитывать ряд признаков:
2. характер входных ворот инфекции (локализация септического очага);
По этиологическому признаку выделяют следующие виды сепсиса: стрептококковый, стафилококковый, пневмококковый, гонококковый, синегнойный, колибациллярный, брюшнотифозный, сибиреязвенный, туберкулезный, сифилитический, грибковый и др. Особенно большое значение в развитии сепсиса имеют стафилококк и синегнойная палочка, а также ассоциация этих микробов. Это связано с широким и недостаточно рациональным применением в клинике антибиотиков, причем в больших дозах, а также цитостатических препаратов.
В зависимости от характера входных ворот инфекции (локализации септического очага) различают терапевтический (параинфекционный), тонзиллогенный, хирургический, маточный, отогенный, одонтогенный, пупочный, криптогенный сепсис. Криптогенным (от греч. kryptos – тайный, скрытый) называют сепсис при отсутствии септического очага. Следует иметь в виду, что септический очаг не всегда локализуется в воротах инфекции и может находиться в отдалении от них (например, случаи сепсиса, развивающегося из абсцессов печени после бывшего ранее гнойного аппендицита или язвенного колита).
По клинико-морфологическим признакам выделяют 4 клинико-анатомические формы сепсиса: септицемию, септикопиемию, септический (бактериальный) эндокардит и хрониосепсис.
Септицемия
Септицемия – форма сепсиса, для которой характерны выраженный токсикоз (высокая температура, затемненное сознание), повышенная реактивность организма (гиперергия), отсутствие гнойных метастазов и быстрое течение. Развитие септицемии часто связано со стрептококком.
При вскрытии умерших от септицемии септический очаг, как правило, отсутствует или выражен слабо (входные ворота инфекции не обнаруживаются). Кожа и склеры нередко желтушны (гемолитическая желтуха), отчетливо выражены признаки геморрагического синдрома в виде петехиальной сыпи на коже, кровоизлияний в серозных и слизистых оболочках, во внутренних органах. Характерна гиперплазия лимфоидной и кроветворной тканей. В связи с этим резко увеличиваются селезенка, которая дает обильный соскоб пульпы (септическая селезенка), и лимфатические узлы. В селезенке и лимфатических узлах находят не только пролиферацию лимфоидных и ретикулярных клеток, но и скопления зрелых и незрелых форм клеток гемопоэза. В костном мозге плоских костей и диафизах трубчатых костей отмечается усиленное кроветворение с образованием большого числа юных форм. Появляются также очаги внекостномозгового кроветворения. В паренхиматозных органах – сердце, печени, почках – развивается межуточное воспаление (см. рис. 281). Строма этих органов отечна и инфильтрирована нейтрофилами, лимфоцитами, гистиоцитами. Для септицемии характерны повышение сосудисто-тканевой проницаемости, развитие фибриноидных изменений стенок сосудов, аллергических васкулитов, с чем в значительной мере связаны проявления геморрагического синдрома.
Септикопиемия
При вскрытии умерших от септикопиемии, как правило, находят септический очаг,, обычно расположенный в воротах инфекции, с гнойным лимфангитом и лимфаденитом, причем ткань лимфатического узла нередко подвергается гнойному расплавлению. В области септического очага обнаруживается также гнойный тромбофлебит, который является источником тромбобактериальной эмболии. В связи с тем что источники последней появляются чаще в венах большого круга кровообращения, первые метастатические гнойники появляются в легких (рис. 283). Затем при вовлечении в процесс легочных вен (тромбофлебит легочных вен) гнойники появляются в органах системы большого круга кровообращения-в печени (абсцессы печени), почках (гнойничковый нефрит), подкожной клетчатке, костном мозге (гнойный остеомиелит), в синовиальных оболочках (гнойный артрит), клапанах сердца (острый септический полипозно-язвенный эндокардит, см. рис. 282). Гнойники могут распространяться на соседние ткани. Например, при абсцессе легкого развиваются гнойный плеврит и перикардит, при метастатическом абсцессе печени – гнойный перитонит; гнойники почки осложняются перии паранефритом, гнойники кожи – флегмоной и т. д. Гиперпластические процессы в лимфатической (иммунокомпетентной) и кроветворной тканях выражены слабее, чем при септицемии. Поэтому лимфатические узлы резко не увеличиваются, однако селезенка может быть типично септической, причем в пульпе ее обнаруживается большое число лейкоцитов (септический лейкоцитоз селезенки). В костном мозге омоложение его клеточного состава встречается редко. Межуточные воспалительные реакции в паренхиматозных органах весьма умеренны или отсутствуют.
Сепсис (от греч. sepsis - гниение) - общее инфекционное заболевание, возникающее в связи с существованием в организме очага инфекции и имеющее ряд отличий от других инфекционных болезней. Сепсис отличают этиологические, эпидемиологические, клинические, иммунологические и патолого-анатомические особенности.
Этиологические особенности сепсиса ааключаются в том, что его могут вызывать самые разнообразные возбудители: стафилококк, стрептококк, пневмококк, менингококк, синегнойная палочка, микобактерия туберкулеза, брюшнотифозная палочка, грибы и другие инфекты (кроме вирусов). Таким образом, сепсис полиэтиологичен.
В эпидемиологическом отношении сепсис не является заразной болезнью.
Клиническое своеобразие сепсиса как инфекции состоит в том, что независимо от характера возбудителя проявления болезни остаются трафаретными, они обусловлены генерализацией инфекции и неадекватной реакцией организма на инфект. Сепсис не имеет определенных сроков инкубации. Ему свойственны разные сроки течения – от нескольких дней до нескольких месяцев и даже лет, в связи с чем выделяют острейший, острый, подострый и хронический сепсис.
Иммунологическая особенность сепсиса состоит в том, что иммунитет при нем не вырабатывается, организм в условиях повышенной реактивной готовности реагирует на инфекционный возбудитель неадекватно, преобладают гиперергические реакции.
Патологоанатомические особенности сепсиса сводятся к тому, что местные и общие изменения при нем не имеют каких-либо специфических особенностей.
Патогенез. Для возникновения заболевания необходима бактериемия, что, однако, является только одной из предпосылок для развития сепсиса. Доказано, что при сепсисе велика роль не только меняющейся реактивности макроорганизма, но и самого инфекта. Сепсис рассматривается как особая форма взаимодействия макро- и микроорганизма, при этом воздействию инфекта и реакции на него организма придается равное значение. Гиперергическая реакция организма на инфект и отсутствие иммунитета объясняют генерализацию инфекции, ациклическое течение сепсиса, преобладание реакций общего плана и утрату способности локализовать инфекцию.
Патологическая анатомия. При сепсисе различают местные и общие изменения. Местные изменения развиваются в очаге внедрения инфекции (входные ворота) или в отдалении от него. Образуется септический очаг, который представляет собой фокус гнойного воспаления. Из септического очага инфекция быстро распространяется по лимфатическим и кровеносным сосудам. Распространение инфекции по лимфатической системе ведет к развитию лимфангита, лимфотромбоза и лимфаденита, а распространение ее по кровеносной системе (по венам) - к развитию флебита и тромбофлебита. Нередко возникает гнойный тромбофлебит, что ведет к расплавлению тромбов и тромбобактериальной эмболии. Общие изменения при сепсисе имеют характер дистрофических, воспалительных и гиперпластических. Дистрофические изменения развиваются в паренхиматозных органах (печень, почки, миокард, мышцы, ЦНС) и проявляются различными видами дистрофии и некробиозом, которые нередко завершаются некрозом.
Воспалительные изменения представлены межуточными процессами (межуточный септический нефрит, гепатит, миокардит). На клапанах сердца может возникать острый полипозно-язвенный эндокардит с расплавлением ткани и отрывом клапанов. Воспалительные изменения возникают в сосудах (васкулиты), что обусловливает появление множественных геморрагий. Однако геморрагический синдром связан при сепсисе не только с васкулитами, но и с интоксикацией, повышенной сосудисто-тканевой проницаемостью, анемией и т. д.
Гиперпластические процессы при сепсисе наблюдаются главным образом в кроветворной и лимфатической (иммунокомпетентной) тканях. Происходит гиперплазия костного мозга плоских костей. Желтый костный мозг трубчатых костей становится красным, в крови увеличивается количество лейкоцитов, иногда появляются молодые формы лейкоцитов, развивается так называемая лейкемоидная реакция. Гиперплазия лимфатической ткани приводит к увеличению размеров лимфатических узлов, селезенки, которая становится не только резко увеличенной, но и дряблой, на разрезе имеет красный цвет и дает обильный соскоб пульпы (септическая селезенка). Гиперпластичекие процессы в гистиоцитарно-макрофагальной системе объясняют увеличение печени. В связи с гемолитическим действием некоторых бактериальных токсинов при сепсисе может возникнуть гемолитическая желтуха.
Классификация. При классификации сепсиса необходимо учитывать ряд признаков:
2) характер входных ворот инфекции (локализация септического очага);
По этиологическому признаку выделяют следующие виды сепсиса: стрептококковый, стафилококковый, пневмококковый, гонококковый, синегнойный, колибациллярный, брюшнотифозный, сибиреязвенный, туберкулезный, сифилитический, грибковый и др.
В зависимости от характера входных ворот инфекции различают терапевтический (параинфекционный), тонзиллогенный, хирургический, маточный, отогенный, одонтогенный, пупочный, криптогенный сепсис. Криптогенным называют сепсис при отсутствии септического очага. Следует иметь в виду, что септический очаг не всегда локализуется в воротах инфекции и может находиться в отдалении от них (например, случаи сепсиса, развивающегося из абсцессов печени после бывшего ранее гнойного аппендицита или язвенного колита).
По клинико-морфологическим признакам выделяют 4 клинико-анатомические формы сепсиса: септицемию, септикопиемию, септический (бактериальный) эндокардит и хрониосепсис.
Пупочный сепсис - самый частый вид сепсиса у детей, при котором входными воротами инфекции являются пупочные сосуды или раневая поверхность пупочной области, всегда имеющаяся после отторжения культи пуповины. Септическим очагом могут быть флебит и артериит пупочных сосудов, реже - омфалит (воспаление пупочной ямки).
Этиология и патогенез. До применения антибиотиков и сульфаниламидных препаратов самым частым возбудителем был стрептококк. В настоящее время его сменили стафилококк, грамотрицательная флора, устойчивая к многим антибиотикам, и даже грибы (дрожжеподобные и плесневые).
Патогенез связан с попаданием бактериальной флоры при обработке культи пуповины и уходе за пупочной ранкой в детской комнате родильного дома или при введении в нестерильных условиях лекарственных растворов в пупочную вену в родильной комнате. Изменился срок развития пупочного сепсиса. Если раньше дети умирали от него чаще на 3-й неделе жизни, что указывало на заражение в детской комнате, то теперь чаще всего на первой неделе жизни, что свидетельствует об инфицировании в родильной комнате, где проводят инъекции и катетеризацию.
Патологическая анатомия. Преобладающей формой пупочного сепсиса раньше являлась септицемия, особенно у недоношенных детей. До применения инфузионной терапии новорожденным и грудным детям септическим очагом чаще всего является артериит одной или обеих пупочных артерий, причем очаг располагается непосредственно под пупочной ямкой, реже - в отдалении от нее. Чистый омфалит как септический очаг встречается так же редко, как и раньше, чаще наблюдается сочетание его с флебитом или артериитом. Отмечается также сочетание артериита и флебита. Пораженный пупочный сосуд утолщен, что особенно хорошо заметно на поперечном разрезе. В просвете сосуда обнаруживается тромб, иногда с явлениями гнойного расплавления. Если гной макроскопически не обнаруживается, помогает мазок из просвета сосуда или микроскопическое исследование.
При артериите в просвете сосуда встречаются тромб, пронизанный нейтрофилами, колонии микробов. Стенка сосуда часто местами расплавлена, инфильтрирована нейгрофилами - гнойный тромбартериит пупочной артерии. Сходные изменения наблюдаются в пупочной вене при гнойном тромбофлебите. При артериите и флебите может иметь место продуктивный компонент воспаления в виде лимфогистиоцитарных инфильтратов, пролиферации фибробластов, наличия гранулем с гигантскими клетками инородных тел - продуктивный или продуктивно-гнойный артериит и флебит. Омфалит может быть яэвенно-некротическим, гнойно-некротическим, вплоть до развития флегмоны передней брюшной стенки.
При септицемии кожные покровы сероватые, иногда слегка желтушные, характерна геморрагическая сыпь. Подкожный жировой слой истощен. Выражены дистрофические изменения в паренхиматозных органах. Микроскопически в них могут быть обнаружены мелкие некрозы. Селезенка может быть увеличена незначительно, в ней и лимфатических узлах повсеместно наблюдается миелоидная метаплазия. Вилочковая железа истощена, с явлениями акцидентальной трансформации и скоплением миелоидных клеток в дольках и перегородках. Миелоидные инфильтраты обнаруживаются также в интерстиции легкого, печени, почек и других органов. В головном мозге обнаруживаются отек или острое набухание, полнокровие, стазы, в надпочечниках - часто некрозы, кровоизлияния, делипидизация.
При септикопиемии - метастатические очаги в настоящее время чаще всего наблюдаются в виде гнойного менингита, метастатических абсцессов в легких, почках, миокарде, печени (при флебите пупочной вены), реже - в суставах, костном мозге в виде гнойного остеомиелита и др.
Осложнения. Довольно частым осложнением пупочного сепсиса является ДВС-синдром с развитием геморрагического диатеза (мелена, кровоизлияния в мозг, надпочечники, серозные листки и слизистые оболочки, в кожу и мягкие ткани). Часто присоединяются вирусно-бактериальная пневмония, язвенный энтероколит, гнойный отит.
Смерть наступает от основного заболевания, осложнения ухудшают прогноз. В случаях выздоровления в пупочной вене наблюдаются облитерация просвета, гемосидероз, в пупочных артериях - выраженная деформация стенок с массивным кальцинозом.
Бактериальный шок –тяжелый токсический синдром, осложняющий течение некоторых микробных заболеваний и терапевтических вмешательств. Наблюдается при активации хронической очаговой инфекции мочеполовой системы, заболеваниях кишечника (прободение, непроходимость, инфаркт), менингите, септицемии, хирургическом вмешательстве на инфицированных органах, переливании крови и жидкостей, загрязненных бактериями, принятии больших доз антибиотиков. Возникает внезапно при поступлении в кровь больших количеств бактерий и токсинов. Токсическое действие бактерий (кишечной палочки, протея, клебсиелл, псевдомонад, бактероидов, менингококков) обусловливается эндотоксинами. Оно проявляется в высвобождении протеолитических энзимов, активации комплемента, снижении концентрации прекалликреина и резком увеличении гистамина, серотонина, что сопровождается сужением и стазом капиллярной сети, ДВС-синдромом, уменьшением объема циркулирующей крови, гипоксией, ацидозом. Исход неблагоприятный.
Читайте также:


