Лепра этиология патогенез морфологическая характеристика осложнения
Большая медицинская энциклопедия
Авторы: Ф. Е. Вишневецкий, В. А. Евстратова, А. А. Ющенко.
Возбудитель лепры человека был описан в 1874 году норвежским врачом Г. Гансеном. Он выявил его в соскобе с поверхности разреза узла у больного узловатой лепрой. В 1879 году немецкий микробиолог А. Нейссер предложил методы окраски бактерий лепры. Именно поэтому в литературе иногда возбудитель лепры описывается как микобактерия Гансена-Нейссера. В 1882 году была установлена кислото и спирто-устойчивость возбудителя лепры. В первые годы после открытия возбудителя лепры его называли Bacillus leprae, Coccothrix leprae, Streptothrix leprae, дифтероид, затем он был включён как самостоятельный вид в род Mycobacterium Lehmann et Neumann, 1896.
Электронно-микроскопическими исследованиями установлено, что ультраструктура возбудителя лепры принципиально не отличается от строения других видов грамположительных бактерий:
- На поверхности микобактерий лепры выявляется равномерный электроннопроницаемый (осмиофобный) слой толщиной 5-10 нанометров (наружный диффузный слой клеточной стенки).
- За ним следует осмиофильный слой клеточной стенки толщиной от 3 до 10 нанометров, состоящий из двух очень тонких слоёв, плотно прилегающих друг к другу.
- Непосредственно к внутренней поверхности клеточной стенки примыкает наружный слой цитоплазматической мембраны, представляющей собой, как и у других бактерий, трёхслойную мембрану толщиной 7,5-9 нанометров.
В бактериальной клетке встречаются 1-2 мезосомы с выраженным полиморфизмом (петлеобразные, пластинчатые, трубчатые, везикулярные, гроздевидные). В цитоплазме выявляется сравнительно небольшое количество рибосом, сферические электронно-плотные включения волютина диаметром 20-50 нанометров, включения, имеющие вид ограниченных мембраной вакуолей (предположительно липоиды), и гомогенные тельца, природа которых остаётся неизвестной. Ядро не имеет определённой формы, расположено в центре клетки вдоль её длинной оси, не ограничено мембраной. Иногда в лизирующихся под воздействием химиотерапии клетках микобактерий лепры выявляются спороподобные образования.
Основным способом размножения микобактерий лепры является деление материнской клетки и врастания поперечной перегородки. Микобактерия лепры является облигатным внутриклеточным паразитом тканевых макрофагов или клеток ретикулоэндотелиальной системы, проявляет выраженный тропизм к коже и периферическим нервам, но на поздних стадиях развития процесса встречается также во многих других клетках и тканях организма. В тканевой клетке микобактерии лепры размножаются только в цитоплазме; внутриядерный паразитизм для них нехарактерен. Микобактерии в лепрозных клетках иногда отграничены от цитоплазмы клетки-хозяина фагосомной мембраной. На поздних стадиях инфекции паразитирование возбудителей лепры человека сопровождается нарушением строения эндоплазматического ретикулума и митохондрий клетки-хозяина.
Попавший в организм возбудитель лепры, пройдя кожно-слизистые барьеры, проникает в нервные окончания, лимфатическую и кровеносную системы и медленно диссеминирует, не вызывая обычно на месте внедрения видимых изменений.
Многочисленные попытки разработать метод культивирования микобактерий лепры in vitro не дали положительного результата. Этим объясняется малочисленность и разноречивость опубликованных данных о биологических свойствах микобактерий лепры, а также трудности в решении важнейших задач практической лепрологии (получение вакцины, испытание in vitro новых лекарственных средств, определение лекарственной устойчивости возбудителя лепры, получение диагностикумов и т. д.). Ещё Г. Гансен предпринимал попытки заразить лепрой различных лабораторных животных, включая обезьян. Однако ни ему, ни его последователям в течение 80 лет не удавалось найти восприимчивое к лепре экспериментальное животное. С 1902-1903 годы в качестве приближенной экспериментальной модели лепры человека использовалась лепра крыс (лепра Стефанского), являющаяся самостоятельным заболеванием грызунов. В 1960 году американский исследователь C. C. Shepard разработал метод получения локального размножения микобактерий лепры их введением в мякоть подошвы лапки мышей.
Несмотря на недостатки (длительность опыта, трудоёмкость подсчёта микобактерий лепры в суспензии тканей, сравнительно небольшой выход размножившихся микобактерий лепры), метод Шепарда сыграл значительную роль в изучении лепры и широко применяется для экспериментальной проверки активности лечебных и профилактических средств.
В 1971 году американские исследователи W. F. Kirchheimer и E. Storrs сообщили об успешном заражении лепрой девятипоясных броненосцев (Dasypus novemcucinctus). В последующие годы эта модель усиленно изучалась и совершенствовалась. Подтверждено, что при внутривенном заражении большими дозами (до 108) микобактерий лепры у 60% броненосцев через 18-35 мес. развивается генерализованный специфический инфекционный процесс с наличием громадного количества микобактерий лепры – до 6 × 10 12-13 в поражённых тканях (печень, селезёнка, лимфатические узлы). Это открывает возможности для более широкого изучения биологии микобактерий лепры и получения диагностических и вакцинных препаратов в условиях отсутствия методов культивирования возбудителя лепры. Гистологическая картина поражений органов у броненосца соответствует лепроматозному типу лепры у человека, однако у броненосца в патологический процесс рано вовлекаются ткани лёгкого, что нехарактерно для лепры человека.
M. Abe (в 1970 году), проводя иммунохимические исследования экстракта лепромы, выделил два бактериальных антигена лепры, один из которых является термостабильным полисахаридом. а другой – термолабильным белком, высокоспецифичным для микобактерий лепры. При иммунизации кроликов большими количествами микобактерий лепры, выделенных из тканей заражённых броненосцев, выявлено более 20 антигенных компонентов микобактерий, только один из которых, по мнению G. Kronvall (в 1977 году), является специфичным. Уникальной особенностью антигенных свойств возбудителя лепры, по сравнению с другими микобактериями, является способность убитых микобактерий усиливать клеточные иммунные реакции без добавления адъювантов.
K. Prabhakaran (в работах 1967 и 1973 годов) описал специфический для микобактерий лепры фермент Одифенолоксидазу, который, по-видимому, играет важную роль в размножении микобактерий лепры. Выявление дыхательных ферментов – пероксидазы, цитохром-с-оксидазы, сукцинатдегидрогеназы, дегидрогеназы и других подтвердило наличие у микобактерий лепры автономных систем аэробного дыхания.
Большая медицинская энциклопедия 1979 г.
 |
Последнее обновление страницы: 17.11.2014 Обратная связь Карта сайта

Классификация. Современные методы коррекции морщин, применяемые в косметологии.
ЛЕКЦИЯ № 12. Лепра
Лепра (синонимы: проказа, болезнь Ганзена) – хроническая болезнь, которая обычно поражает кожу, слизистые оболочки верхних дыхательных путей и периферическую нервную систему. В настоящее время лепра наиболее распространена в странах Африки, Азии и Южной Америки. В России отмечаются спорадические случаи заболевания.
Этиология. Возбудитель представляет собой кислотоустойчивую палочковидную бактерию, относящуюся к семейству микобактерий. Микроорганизм устойчив во внешней среде. До сих пор нет возможности культивировать возбудителя на искусственной среде. Интенсивно размножаются микобактерии лепры только при лабораторном заражении в тканях броненосца. Возбудитель лепры – это внутриклеточные паразиты макрофагов. Длительный инкубационный период связан с низкой скоростью роста микроорганизмов.
Патогенез. Лепра – слабоконтагиозное низкопатогенное заболевание. Часто встречается субклиническая инфекция. К лепре восприимчивы не более трети людей. Чаще заболевают родственники больных, что подтверждает генетическую предрасположенность к болезни.
Основным путем передачи считается воздушно-капельный. Входные ворота – слизистая верхних дыхательных путей. Возможно и трансэпителиальное проникновение возбудителей. Случайное заражение может быть при татуировке, вакцинации против оспы, хирургической операции. Мужчины заболевают в 2 – 3 раза чаще, чем женщины.
Резистентность инфицированного организма и вирулентность возбудителя определяют форму заболевания. Имеет значение гормональный фон: первое проявление может быть вскоре после полового созревания, во время беременности или после родов. В эти периоды могут появляться новые и активизироваться старые очаги поражения.
Иммунитет при лепре носит клеточный характер, он минимален при лепроматозной и диморфной лепре и максимален у больных туберкулоидной лепрой.
Клиника. Различают несколько клинических форм заболевания. Это лепроматозная лепра, туберкулоидная лепра, пограничная, или диморфная, лепра и недифференцированная лепра.
Лепроматозный тип. Наиболее тяжелая форма. Для нее характерен полиморфизм клинических проявлений, особенно в коже. Кроме кожи, поражаются слизистая носа, полости рта, носоглотки, гортани, иногда трахеи, лимфатические узлы, периферические нервные стволы, органы зрения, слуха, мочеполовые, иногда внутренние органы.
Первые проявления заболевания – обычно округлые или неправильных очертаний эритематозные пятна с блестящей поверхностью, могут быть ржавой окраски. Наиболее характерная локализация – лицо, разгибательные поверхности кистей, предплечий, голеней.
Характерна симметричность высыпаний. В дальнейшем появляется инфильтрация, образуются бляшки с нормальной чувствительностью или гиперестезией. Из-за усиления функции сальных желез поверхность бляшек жирная, блестящая. Потоотделение снижено (в дальнейшем оно исчезает совсем).
Через 3 – 5 лет выпадают брови и пушковые волосы на бляшках. Возможно выпадение усов, бороды. При диффузной инфильтрации кожи лица углубляются естественные морщины и складки, надбровные дуги резко выступают, нос утолщен, щеки и губы имеют дольчатый вид. Обычно не поражаются волосистая часть головы, локтевые и подколенные ямки, подмышечные впадины.
В области инфильтратов формируются одиночные или множественные бугорки и узлы (лепромы), резко отграниченные, безболезненные. Они могут быть дермальными и гиподермальными (вначале выявляются лишь при пальпации), их консистенция плотноэластическая. В дальнейшем узлы и бугорки вяло, без выраженных воспалительных явлений, изъязвляются. Подобные высыпания могут появляться и на неизмененной коже.
На слизистых, как и на коже, процесс может начаться с развития отдельных лепром или диффузной лепроматозной инфильтрации. Все это приводит к образованию рубцов и деформаций.
Нередко увеличивается селезенка, может быть поражение печени, почек, легких, у мужчин часто проявляется орхоэпидидимит, возможно поражение предстательной железы, семенных канатиков. Характерны лимфадениты, периоститы (особенно большеберцовых, локтевых костей, ребер), приводящие к надломам, переломам, деформациям суставов, укорочению и деформации фаланг.
Течение заболевания хроническое, с обострениями, которые провоцируются гормональными сдвигами, оперативными вмешательствами, погрешностями в терапии. При обострениях наблюдаются подъем температуры тела, увеличение и болезненность лимфатических узлов, яркость, распад инфильтратов, новые высыпания.
Нервная система поражается сравнительно поздно – в виде симметричного полиневрита. Постепенно происходит инфильтрация всего нервного ствола, по мере развития которого теряется чувствительность до полной анестезии. На поздних стадиях могут быть трофические и двигательные нарушения.
Туберкулоидная форма. Поражаются кожа, периферическая нервная система, редко – внутренние органы. Возбудитель выявляется при гистологическом исследовании органов, в кожных соскобах. В слизистой носа возбудитель отсутствует.
Пограничная лепра. Иммунная реактивность при этой форме болезни широко варьируется и изменяется под действием стрессов, инфекций, истощения. Все это отражается в клинических проявлениях со стороны тканей-мишеней.
Недифференцированная лепра – это неустойчивая клиническая форма, при которой поражается кожа, пятна (гипо– и гиперпигментированные) не чувствительны к боли и температуре. Главная особенность – множественные поражения нервов. Через несколько лет эта форма переходит или в туберкулоидную, или в лепроматозную.
Диагностика. Основные признаки – это клинические изменения со стороны кожи. Настороженность должна быть и при снижении и исчезновении чувствительности на отдельных участках кожного покрова, парастезиях, нерезко выраженных контрактурах V, IV и III пальцев рук, начинающейся атрофии мышц, пастозности кистей и стоп, стойких поражениях слизистой носа.
Подтверждающими методами считаются бактериоскопический и гистологический. Для бактериоскопического исследования при лепроматозном типе берутся соскобы со слизистой носа. Дополнительно проводят функциональные пробы с гистамином на потоотделение (выражены слабо), никотиновой кислотой (воспламенение), горчичником (нет реакции) и выявление диссоциации чувствительности в очаге поражения.
Лепроминовая проба (внутрикожное введение суспензии микобактерий лепры, полученной при гомогенизации лепромы) не является диагностической. Она проводится для оценки иммунного ответа и дифференциальной диагностики различных типов лепры: проба положительна при туберкулоидном варианте и отрицательна при лепроматозном (при диморфной лепре возможны как положительные, так и отрицательные результаты).
Лечение. В зависимости от типа болезни лечение проводится в лепрозории либо по месту жительства (при незначительных кожных проявлениях абациллярной лепры). Лечение комбинированное, курсовое с использованием противолепрозных препаратов (диафенилсульфона, солюсульфона, диуцифона и других производных сульфонового ряда): курсы по 6 месяцев с перерывами в 1 месяц.
При мультибактериальной лепре начинают с рифампицина или клофазимина, а затем переходят к сульфонам. Кроме того, могут быть использованы солюсульфон, бенемицин, этионамид, лампрен.
Эффективность лечения оценивается по результатам бактериоскопического контроля и гистологического исследования. Средняя продолжительность терапии 3 – 3,5 года.
Профилактика. Общая профилактика заключается в повышении жизненного уровня населения, раннем выявлении, изоляции и лечении больных. Контактные лица обследуются и наблюдаются не менее 7 лет. Проводится превентивная химиотерапия сульфонами. Мужчины, находившиеся в контакте с больными лепрой, не подлежат призыву в армию.
Проказа или лепра?

Несколько исторических фактов

Лепра в наши дни

Портрет возбудителя
Патогенез проказы начинается с проникновения в тело человека палочки Хансена. Это микроскопическая бактерия длиной до 8 мкм, а диаметром всего до 0,5 мкм. Палочки имеют заостренные либо утолщенные края и покрыты четырьмя слоями очень плотных оболочек, защищающими их от внешних раздражителей. Они неподвижны, не образуют споры, размножаются невероятно медленно. Деление одной бактерии длится примерно 14 дней. Держатся палочки группами, тогда они напоминают рассыпанные сигареты. Иногда паразитов можно встретить и по одному. Живут они исключительно в клетках жертв, поэтому, попав во внешнюю среду, быстро погибают. Палочки Хансена паразитируют только в человеке, но есть мнение, что они могут заражать мышей, броненосцев, бурундуков и некоторые виды обезьян. Этиология и патогенез проказы (лепры) изучаются трудно, потому что колонии палочек Хансена на питательной среде в лабораториях растут необыкновенно плохо и медленно - от 6 недель, против нескольких часов у других бактерий. Еще одна трудность – вне клетки они становятся непатогенными, а в подопытных животных практически не приживаются. И все-таки удалось узнать, что палочки Хансена и Коха (вызывают туберкулез) произошли от одной бактерии, но в процессе эволюции несколько видоизменили свои структуры. А в 2009 году открыли еще один вид этой бактерии, который вызывает диффузную лепроматозную проказу.

Пути заражения
Источником микроба лепры может быть только страдающий этим недугом в активной форме человек. Но по некоторым сведениям иногда причиной инфицирования становится работа без перчаток с животными, которых поражает бактерия Хансена. Как происходит патогенез лепры? Инфекции, передающиеся воздушно-капельным путем, всегда самые вирулентные и способны заразить многих. Но в случае с лепрой этого не происходит по пока невыясненным причинам. Известно лишь, что палочки Хансена активно размножаются на участках тела, которые может охлаждать воздух, а именно на слизистых ротовой полости. От больного здоровому они передаются при чихании, поцелуе, кашле, эмоциональном разговоре. Кроме того, микроб может передаться с кровью больного или при попадании его экссудатов, насыщенных паразитами, непосредственно на травмированную кожу новой жертвы.
Группы риска
Высокая вероятность заразиться у тех, в чьих семьях есть больной проказой. Во-первых, из-за того, что между членами семьи трудно избежать длительных контактов, а во-вторых, потому что существует генетическая предрасположенность к данному заболеванию. Семейным парам запрещено иметь наследников. Но у больных матерей дети рождаются здоровыми. Если таких малышей сразу изолировать, их совершенно не поражает лепра (проказа). Этиология заболевания пока не выяснена и в отношении других категорий риска среди населения. Пока точно установлено, что недуг активно развивается у лиц с ослабленным иммунитетом. Есть случаи, когда люди, ухаживающие за прокаженными, оставались здоровыми, но заболевали их родственники, не принимавшие участия в уходе. Врач Даниэль Даниэльсон долгие годы вводил себе кровь прокаженных, помещал в свои раны экссудат из бугорков на их теле, но так и не был инфицирован. А вообще, болезнь наиболее вероятна там, где низкий уровень жизни.

Патогенез проказы
Предположительно, из-за медленного размножения бактерий Хансена слишком долго развивается и вызываемая ими проказа. Этиология, патогенез болезни таковы: возбудитель, попав на слизистые либо в рану, просачивается в кровь и лимфу, а с этими жидкостями в нервную систему и другие внутренние органы. Там бактерии образуют гранулемы, содержащие множество макрофагов. Заразившись, человек может десятилетия жить и не подозревать о своем недуге. Инкубационный период у некоторых длится полгода, чаще около 5 лет, а в отдельных случаях 20 и даже 40 лет. Помимо инкубационного, существует латентный период (время, с которого инфицированный способен заражать окружающих). Для лепры он несколько меньше инкубационного. У пациента в это время может вообще не быть симптомов либо наблюдаться легкое недомогание, потеря аппетита, необъяснимо быстрая утомляемость, но о серьезном заболевании он не предполагает, хотя уже является заразным.
Симптомы
Микроб поражает не только слизистые во рту, но и в легких, а также клетки в нервных окончаниях (швановские). При прогрессировании заболевания бактерии находят в глазах, в печени, даже в головном мозге. Первый признак недуга – это тяжело переносимые боли в конечностях, в спине. Тогда же больные могут жаловаться на слабость, сонливость, потерю аппетита, расстройства кишечника. В дальнейшем боли сменяются ощущением покалывания, а потом человек вообще утрачивает чувствительность в пораженных местах. Это часто становится причиной травм, заражения другой инфекцией и в конечном итоге потерей пальцев, необратимыми дефектами рук и ног. Палочки Хансена сами по себе больного конечностей не лишают. У лепры выделяют два основных вида – туберкулоидную лепру и лепроматозную. Их симптомы отличаются, поэтому рассмотрим каждую подробнее.
Туберкулоидная проказа, этиология, симптомы, лечение
Этот вид заболевания диагностируется в трех формах:
- полярная;
- пограничная;
- недифференцированная.
Основным симптомом туберкулоидной лепры является появление на коже четкого гипопигментированного (светлого) пятна. Недифференцированная форма способна самостоятельно исцелиться, либо перейти к более тяжелым. Вначале кожа на месте пигментации очень чувствительна, но вскоре пятно начинает увеличиваться, его края выпячиваются, а центральная часть, наоборот, западает. Здесь отсутствуют потовые железы, исчезают волосы, кожа теряет чувствительность. За пределами пятна нервы утолщаются, так как палочки Хансена, разрастаясь, раздувают пораженные клетки. Инфицирование нервов вызывает атрофию мышц, контрактуру ступней и кистей рук. Когда бактерии поражают лицевой нерв, у больных развиваются заболевания глаз, в конечном итоге приводящие к слепоте.

Лепроматозная проказа
Этот вид заболевания протекает тяжелее и более опасен для людей в окружении больного. Здесь различают две формы:
- проблемы с носом (заложенность, затруднено дыхание, иногда из носа идет кровь);
- изменение голоса (становится хриплым);
- проблемы со зрением (кератит, иридоциклит);
- увеличение лимфоузлов в паху;
- инфильтрация ткани в яичках;
- образование на месте распавшихся лепром обезображивающих язв;
- слабость конечностей, атрофия, а в дальнейшем некроз.
Существует смешанная форма проказы, при которой одновременно наблюдаются симптомы туберкулоидной и лепроматозной форм.

Диагностика
Заболевание лепра, этиология и патогенез которого еще изучаются, диагностируется несколькими методами.
- Клинический. Состоит в визуальном осмотре кожи больного, выявлении нечувствительных слизистой и участков кожи.
- Микроскопический. В носоглотке делают довольно интенсивный (до крови) соскоб, берут материал из лимфоузлов. Микроскоп показывает у больного наличие характерных овальных или круглых лепрозных клеток. Мазки окрашивают по методу Циля - Нильсена, в результате старые палочки Хансена становятся красными, а молодые в основном синими.
- Аллергический тест (Мит-суда). Под кожу вводят лепромин (готовят из тканей, взятых у больных лепрой). Если испытуемый заражен, у него менее чем за сутки кожа в месте пробы напухает и краснеет.
- Серологический метод.
Лечение
Прогноз
Если лечение начато вовремя, исход достаточно благоприятный. У больных даже может не остаться на коже никаких следов. В запущенных стадиях вернуть здоровье уже не удается, человек остается инвалидом пожизненно, но у него возможно восстановление работы внутренних органов, что позволяет продлить ему жизнь.
Профилактика заболевания включает:
- гигиену, особенно при нахождении в регионах, где лепра процветает;
- раннюю диагностику и лечение;
- профилактический контроль всех, кто длительно контактирует с больными лепрой (медики, семья).
Лепра (лат. lepra, болезнь Хансена, хансениаз, проказа, болезнь святого Лазаря, elephantiasis graecorum, lepra arabum, leontiasis, satyriasis, ленивая смерть, чёрная немочь, скорбная болезнь) — хроническая антропонозная инфекционная болезнь из группы микобактериозов с аэрозольным механизмом заражения, при которой происходит первичное поражение производных эктодермы (кожа, периферическая нервная система, слизистые оболочки верхних дыхательных путей, передний отдел глазного яблока).
Коды по МКБ -10
А30. Лепра (болезнь Хансена).
А30.0. Недифференцированная лепра.
А30.1. Туберкулоидная лепра.
А30.2. Пограничная туберкулоидная лепра.
А30.3. Пограничная лепра.
А30.4. Пограничная лепроматозная лепра.
А30.5. Лепроматозная лепра.
А30.8. Другие формы лепры.
А30.9. Лепра неуточнённая.
Этиология (причины) лепры
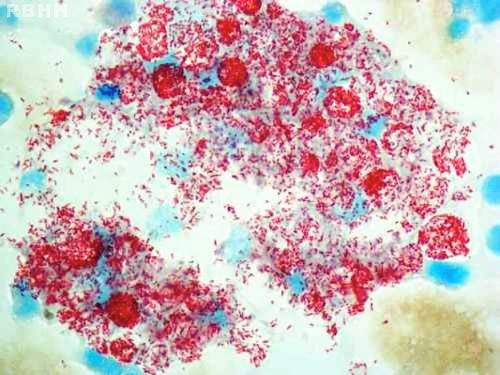
Микобактерии лепры. 1000 × увеличение
Для возбудителя характерен необычайно медленный рост, не свойственный бактериям: время одного деления составляет 12 сут.
Из антигенных детерминант наиболее значим специфический фенольный гликолипид (ФГЛ-1). В его состав входит уникальный трисахарид, на основе которого предпринимаются попытки создать специфический искусственный антиген.
Клеточная стенка микобактерии лепры на 50% состоит из липидов, среди которых преобладают высокомолекулярные миколовые кислоты. Описан также безуглеводный липид (фтиоцерол димикоцерозат), отличающийся от таковых других микобактерий. Установлена способность M. leprae секретировать липиды.
Факторы патогенности M. leprae не изучены.
M. leprae длительно выживают при низких температурах и при хранении, например, в 40% растворе глицерола; сохраняют жизнеспособность в течение нескольких недель при высушивании различными способами в условиях затенения. Прямое ультрафиолетовое облучение действует на них губительно.
Эпидемиология лепры
Единственный доказанный источник инфекции при лепре — больной человек. Большинство специалистов допускают как воздушно-капельный, так и контактный (перкутанный) путь передачи лепры. Данные эпидемиологических исследований свидетельствуют о преобладающем значении воздушно-капельного пути передачи: обычно больной может служить источником инфекции при развитии у него обширных поражений слизистой оболочки носоглотки, т.е. в период массивного выделения возбудителя в окружающую среду респираторным путём. В то же время зарегистрированные случаи заражения при хирургических вмешательствах, а также при татуировке подтверждают, что возможны заражение лепрой и проникновение возбудителя через повреждённую кожу.
Большинство людей относительно невосприимчивы к лепре. Какой-либо расовой предрасположенности или особой резистентности к лепре не существует.
Однако, если учитывать данные иммуногенетики, нельзя отрицать роль факторов генетически обусловленной предрасположенности к лепре внутри отдельных этносов и популяций, о чём свидетельствует в 3–6 раз более частое заражение лепрой кровных родственников, чем супругов друг от друга, поскольку между последними генетические различия более выражены. Известно, что конкордантность по лепре у монозиготных близнецов почти в три раза выше, чем у дизиготных близнецов.
Сезонность и климатические условия имеют некоторое значение в заражении лепрой лишь в отношении усиления миграционных процессов, степени профессиональных контактов с источниками инфекции, снижения неспецифической резистентности, общей гигиены. Основной показатель иммунореактивности к M. leprae — внутрикожная проба на лепромин, предложенная в 1919 г. K. Митсуда.
Лепромин — суспензия растёртой и автоклавированной лепромы больного, содержащая огромное количество M. leprae (1 мл стандартизированного лепромина содержит от 40 до 160 млн бактериальных тел). При введении внутрикожно во внутреннюю поверхность предплечья 0,1 мл этого антигена у больных лепроматозным типом заболевания и у незначительной части (до 10–12%) здоровых лиц проба всегда отрицательная (анергия, толерантность к M. leprae). В то же время у больных с туберкулоидным типом лепры и большинства здоровых людей она положительная, т.е. относительный естественный иммунитет к лепре у них характеризуется довольно высокой напряжённостью. Следовательно, лепроминовая проба диагностического значения не имеет, но помогает установить тип заболевания, а также важна для прогноза. Лепроминоотрицательные лица из числа контактных составляют группу повышенного риска заболевания, а трансформация отрицательной лепроминовой пробы у больного в положительную свидетельствует о нарастании напряжённости специфического клеточного иммунитета к антигенам M. leprae. Реакция на лепромин Митсуда развивается через 3–4 нед после его введения (возникает бугорок, узел, иногда — с некрозом).
Во второй половине ХХ в. больных лепрой регистрировали практически во всех странах мира. В 1980 г. их численность, по оценке ВОЗ, составила около 13 млн человек. Однако после того, как ВОЗ приняла решение обеспечить комбинированную терапию тремя препаратами (дапсон, рифампицин, клофазимин) всех больных и снять с учёта пациентов, прошедших полный курс этого лечения, к 2000 г. число состоящих на учёте уменьшилось до 600–700 тыс. человек. В то же время уже в XXI в. ежегодно регистрируют от 500 тыс. до 800 тыс. новых случаев лепры, всё более насущной становится проблема рецидивов, и, как считают большинство специалистов, проблема элиминации лепры до единичных случаев продлится ещё на десятилетия. В настоящее время наиболее поражены лепрой страны Юго-Восточной Азии (Индия, Индонезия, Мьянма), некоторые страны Африки и Бразилия.
В России лепра никогда не имела широкого распространения. Максимум зарегистрированных больных (около 2500 человек) отмечался в начале 60-х гг.
В начале 2007 г. на учёте состояли 580 человек, а за предыдущие десять лет зарегистрировано всего 14 новых больных.
В отсутствие специфической противолепрозной вакцины для профилактики лепры рекомендуется вакцина БЦЖ, но, по данным разных авторов, она защищает от лепры лишь на 20–70%. В ряде стран, в том числе и в России, проводят химиопрофилактику лепры. Превентивное лечение одним из препаратов сульфонового ряда в течение 6–12 мес назначают лицам, проживающим совместно с больным лепрой (бактериовыделителем).
Патогенез лепры
При туберкулоидном типе лепры чёткие фокусы эпителиоидных клеток окружены лимфоидным бордюром (туберкулоидный бугорок); гранулёма достигает непосредственно эпидермиса; отмечают признаки гиперчувствительности (глубокая эрозия эпидермиса, утолщение и центральный казеоз кожных нервов, фибриноидный некроз в дерме, наличие гигантских клеток Лангханса). Мелкие нервы обычно не определяются, так как они разрушены или сильно инфильтрированы. M. leprae обнаруживают с трудом в виде единичных клеток в ткани утолщённого нерва или они не выявляются.
При недифференцированной форме лепры гранулёма не развивается, а возникает инфильтрат простой воспалительной структуры с большим или меньшим содержанием M. leprae, расположенных внутриклеточно.
Клиническая картина (симптомы) лепры
Для лепры характерны крайне длительный и неопределённый инкубационный период (от нескольких месяцев до 20 лет и более; в среднем 3–7 лет), большое разнообразие клинических симптомов, отсутствие чётких признаков течения.
Современная классификация лепры Ридли–Джоплинга (1966) основана на зависимости клинических симптомов болезни и результатов гистопатологических, бактериоскопических и иммунобиологических исследований от состояния иммунологической реактивности больных к M. leprae. Лепрозный процесс рассматривают как непрерывный спектр иммунопатологических изменений между туберкулоидным и лепроматозным типами лепры, называемыми полярными типами, с выделением трёх пограничных групп: погранично-лепроматозной, пограничной, погранично-туберкулёзной и одной недифференцированной формы.
В качестве продромальных при лепре иногда выступают признаки периферической вегетативной недостаточности и симптомы рефлекторно-сосудистых расстройств (мраморность кожи, цианоз, отёки кистей и стоп, нарушения пото- и салоотделения), а также слабость, ломота, парестезии, кровотечения из носа.
В начале развития манифестных форм заболевания, как правило, отмечают диффузные изменения окраски кожного покрова, одиночные или множественные пятнистые высыпания, варьирующие по локализации, форме, размерам и окраске (эритематозные, гипопигментные, гиперпигментные, синюшные, с буроватым оттенком), усиливающиеся парестезии. В более поздних стадиях болезни возникают ограниченные или разлитые кожные инфильтраты, папулы, бугорки, узлы, ринит и высыпания на слизистых оболочках верхних дыхательных путей, лепрозный пемфигус, выпадение бровей и ресниц (мадароз), амиотрофия, ломкость ногтей, ихтиозиформные признаки, язвы и другие трофические расстройства, грубые нарушения поверхностных видов чувствительности.

Кожные проявления туберкулоидного типа лепры (ТТ-лепры), в зависимости от стадии болезни, имеют вид одиночных или множественных пятен с чёткими краями, а также папулёзных элементов, бляшек, саркоидных и кольцевидных бордюрных элементов с чётко очерченным приподнятым краем.
Характерный признак высыпаний туберкулоидного типа лепры на коже — рано обнаруживаемое уменьшение болевой, температурной и тактильной чувствительности на них, обычно выходящее на 0,5 см за видимые границы поражений, нарушение потоотделения и выпадение пушковых волос. При регрессе высыпаний туберкулоидного типа лепры на их месте остаются гипопигментные пятна, а в случае более глубокой инфильтрации — атрофия кожи.
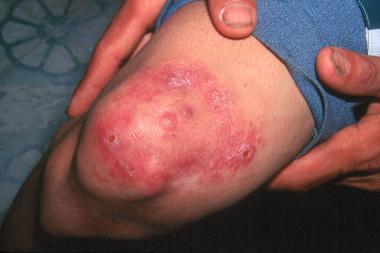
Начальные высыпания при лепроматозном типе лепры (ЛЛ-лепры) чаще всего имеют вид многочисленных эритематозных, эритематозно-пигментных или эритематозно-гипопигментных пятен, характерные признаки которых — небольшие размеры, симметричное расположение и отсутствие чётких границ. Чаще пятна возникают на лице, разгибательных поверхностях кистей и предплечий, голенях и ягодицах. Поверхность их обычно гладкая и блестящая.
Часто уже в ранних стадиях заболевания в области инфильтратов возникают одиночные или множественные бугорки и узлы (лепромы), размеры которых варьируют от просяного зерна до 2–3 см в диаметре. Лепромы резко отграничены от окружающей кожи, безболезненны. Наиболее частым исходом их развития, если не проводится противолепрозное лечение, бывает изъязвление.
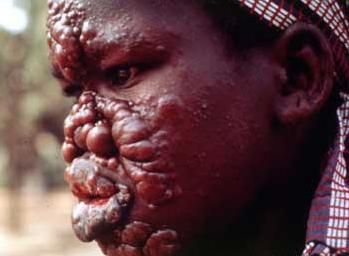
Во всех случаях лепроматозного типа лепры отмечают поражения слизистой оболочки носоглотки. Она выглядит гиперемированной, сочной, испещрена небольшими эрозиями.
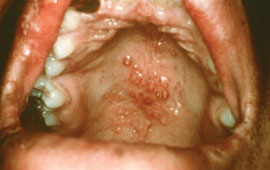

В очень запущенных случаях заболевания может наблюдаться изъязвление лепром на слизистой оболочке нёба. Поражение области голосовых связок может вызвать резкое сужение голосовой щели, афонию. Если генерализация лепроматозного типа лепры наступила до периода полового созревания, то нередко отмечают недоразвитие вторичных половых признаков, у мужчин — гинекомастию. Периферическая нервная система вовлекается в процесс в поздних стадиях развития лепроматозного типа лепры, поэтому в течение длительного времени нарушения кожных видов чувствительности могут отсутствовать.
В клинической картине других разновидностей лепры в различном соотношении выражены признаки обоих полярных типов заболевания (пограничные состояния).
Поражения периферической нервной системы раньше или позже обнаруживаются при всех формах лепры. Особенность лепрозных невритов — их восходящий характер и островковый (рамускулярный) тип расстройства чувствительности, что обусловлено разрушением нервных окончаний в очагах высыпаний, поражением кожных веточек нервов и отдельных нервных стволов. Чаще всего именно поражение периферической нервной системы приводит к инвалидности (отсутствие кожных видов чувствительности, амиотрофия, контрактуры, параличи, нейротрофические язвы, остеомиелит, мутиляции, лагофтальм).

После внедрения в практику эффективных противолепрозных препаратов заболевание перестало фигурировать в качестве причин смерти, а показатели средней продолжительности жизни у больных лепрой превышают таковые в остальной популяции.
Диагностика лепры
Диагностика лепры основывается на выявлении дерматологических и неврологических симптомов болезни и оценке результатов функциональных и лабораторных исследований. Большое значение придают анамнезу, проживанию в эндемической зоне, контакту с больными лепрой. Поскольку у больного человека длительно (годами) отсутствует субъективное ощущение болезни (отсутствие повышенной температуры, боли и зуда в области высыпаний), для своевременного её выявления обязательно осматривать пациента при хорошем освещении. Необходимо провести неврологическое обследование, чтобы обнаружить утолщённые нервные стволы и кожные нервные веточки (особенно в области высыпаний на коже).
Стандарт диагностики лепры включает:
· осмотр всего кожного покрова, а также слизистых оболочек верхних дыхательных путей;
· пальпацию нервных стволов и кожных веточек нервов;
· обследование конечностей для обнаружения амиотрофии и контрактур;
· постановку функциональных проб в очагах кожных поражений (выявление нарушений различных видов чувствительности кожи, проба на потоотделение, проба с никотиновой кислотой и др.);
· бактериоскопическое исследование, позволяющее обнаружить кислотоустойчивые микобактерии в мазках из скарификатов кожи;
· патогистологическое исследование кожи, взятой из края очага поражения, с окраской по Цилю–Нильсену для выявления M. leprae.
Дифференциальную диагностику проводят со многими заболеваниями кожи и периферической нервной системы: бугорковым сифилидом, сифилитическими гуммами, токсидермией, многоформной экссудативной эритемой, красным плоским лишаём, туберкулёзом кожи, саркоидозом, грибовидным микозом, ретикулёзом, лейшманиозом, узловатой эритемой, трофическими и прободными язвами стоп различной этиологии и др. О туберкулоидном типе лепры свидетельствуют характер высыпаний и нарушение в них поверхностных видов чувствительности (иногда — выявление единичных M. leprae при гистологическом исследовании).
Верифицирующий признак при лепроматозном типе лепры, помимо клинических симптомов, — обнаружение большого количества M. leprae.
Поскольку при лепре, помимо высыпаний на коже, можно обнаружить неврологические и амиотрофические поражения, трофические язвы и остеомиелиты, поражения глаз и органов дыхания, больным показаны консультации дерматолога, невропатолога, хирурга, офтальмолога, оториноларинголога.
Больных с лепроматозным типом лепры, а также пациентов с погранично-лепроматозной и пограничной формами лепры, относящихся к бактериовыделителям (открытые формы), необходимо по эпидемическим показаниям госпитализировать в противолепрозные учреждения. Показано, что после 3–6 мес активного лечения они перестают выделять бактерии в окружающую среду. Госпитализации также подлежат больные с любыми другими формами лепры в стадии обострения процесса (реактивные состояния). Больные с туберкулоидными формами лепры после установления диагноза могут проходить амбулаторное лечение (вопрос об этом и о переводе на диспансерное наблюдение решает комиссия врачей противолепрозного учреждения). Больные должны соблюдать предписанный им индивидуальный эпидемический режим; каких-либо других требований к режиму нет.
Рацион должен быть богат белками, содержать небольшое количество жира.
Лечение лепры
Для лечения бактериовыделителей ВОЗ рекомендует следующую помесячную схему комбинированной терапии. В первый день назначают три препарата: дапсон (100 мг), рифампицин (600 мг) и клофазимин (300 мг), а в последующие дни в течение месяца — по два препарата (100 мг дапсона и 50 мг клофазимина). Затем цикл повторяют (без перерыва). Длительность курса не менее двух лет (до исчезновения M. leprae в биоптатах кожи).
Больным туберкулоидной и погранично-туберкулоидной формой лепры с самого начала назначают по такой же схеме два препарата: в первый день — 100 мг дапсона и 600 мг рифампицина, а затем, в течение месяца, — дапсон по 100 мг.
В России из группы препаратов сульфонового ряда производят димоцифон. В качестве препаратов второго ряда для лечения больных лепрой применяют этионамид и протионамид. Для купирования острых лепрозных реакций назначают глюкокортикоиды, НПВС, анальгетики, витамины, средства, улучшающие нервную проводимость и предупреждающие развитие мышечных атрофий, десенсибилизирующие препараты и иммуномодуляторы. Из дополнительных методов лечения по показаниям применяют физиотерапевтические (лечение невритов) и хирургические (остеомиелиты).
Прогноз
При своевременно поставленном диагнозе прогноз благоприятный. При поздней диагностике и несвоевременно начатом лечении возможны инвалидизирующие последствия. При ранней диагностике и хорошей переносимости комбинированного лечения трудоспособность не страдает.
Диспансеризация
Пациентов, находящихся на диспансерном учёте, не реже двух раз в год должен осматривать врач-лепролог или дерматолог. Периодически по решению противолепрозного учреждения, наблюдающего больного, ему назначают противорецидивные курсы специфического лечения, проводят общеукрепляющие мероприятия. Отдых в бальнеологических санаториях больным, завершившим лечение, противопоказан.
Памятка для пациента
Пациенты, особенно с нарушением кожной чувствительности, должны ежедневно осматривать свои конечности, чтобы своевременно обнаружить травмы и ожоги и провести соответствующее лечение. Они должны регулярно принимать назначаемые им противорецидивные курсы химиотерапии, несмотря на субъективно хорошее самочувствие и отсутствующие признаки активации заболевания.

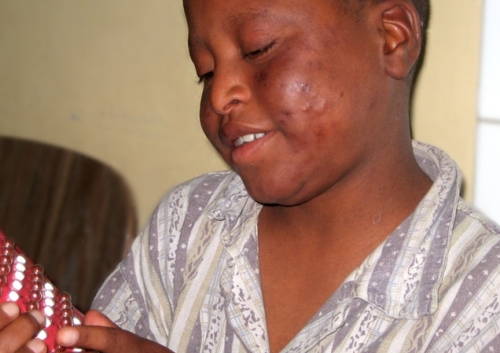
Gudiya из Непала, ему всего 7, болен лепрой, имеет поражения кожи, охватывающие все тело. Проказа все еще не искоренена.
Читайте также:


