Сепсис всего организма на фоне гнойного холангита
Воспалительный процесс желчевыводящих путей, вызванный неспецифическими возбудителями, называется холангит. Это довольно распространенный недуг, и в зависимости от патологических изменений, которые протекают в стенках желчных протоков, различают холангит: гнойный, некротический, катаральный и дифтерический. В этой статье речь пойдет о гнойной форме заболевания.
Общая информация
Ранее холангит в основном диагностировали в старшей возрастной категории, а в последние десятилетия все чаще его выявляют у сорокалетних индивидов. Страдают этой патологией в основном женщины. Болезнь обычно протекает на фоне иных аномалий ЖКТ – гастро- и дуоденита, желчнокаменной болезни, гастрита, гепатита, холецистита, панкреатита. В связи с этим течение недуга довольно тяжелое. Кроме того, сопутствующие болезни создают некое препятствие эффективному оперативному устранению причины заболевания. Острый гнойный процесс воспаления в желчевыводящих путях, который формируется на фоне плохого оттока желчи из-за полной или частичной блокировки, приводит к гнойной форме холангита.
Для болезни свойственна следующая клиника: желтушность, которая стремительно нарастает, боль в правом боку под ребрами, высокая температура, чувство холода. Одним из осложнений недуга является совокупность системных воспалительных реакций на процесс в желчевыводящих путях с нарушением сознания, гемодинамики, работы почек и иных органов. Выставление диагноза проводится на визуализации механического препятствия, выявленного при КТ или УЗИ органов брюшной полости. Декомпрессия желчных путей с устранением обструкции осуществляется путем хирургического вмешательства, после которого назначается антибиотикотерапия. Далее корректировке подлежат иные нарушения.
Причины развития патологии
Гнойный холангит имеет бактериальную природу. Для него характерно наличие на стенках желчных протоков ран, которые через какое-то время гноятся. Это тяжелая хирургическая патология, которая без лечения приводит к смерти индивида. Около половины всех пациентов с этим диагнозом имеют гнойный воспалительный процесс в протоковой системе.
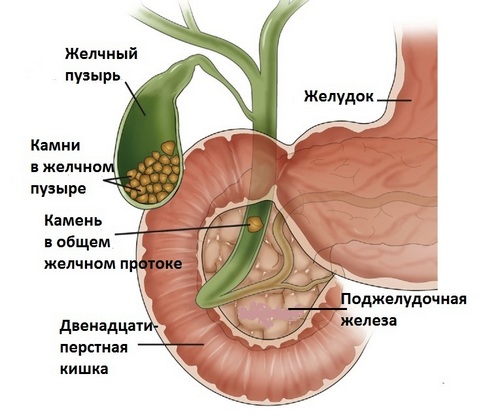
Закупорка желчных протоков камнями плотного образования – это основная причина гнойного холангита. К иным факторам, приводящим к сбою оттока желчи и вызывающим воспаление, относятся:
- сужения протоков после травмы;
- рубцовые изменения;
- паразитарная инвазия;
- новообразования в районе большого сосочка 12-перстной кишки.
В желчевыводящих путях активно размножаются патогенные бактерии в результате прекращения или неполного оттока желчи. В небольшом количестве микробы имеются в желчи, попав в нее из тощей кишки гематогенно или при дуоденобилиарном рефлюксе. При нормальном оттоке воспаление не развивается, а микрофлора поддерживает иммунную систему в тонусе. При сбое этого процесса количество микроорганизмов в желчи увеличивается. Провоцируют развитие гнойного холангита в основном грамотрицательные микробы, в редких случаях – стрептококки, стафилококки, псевдомонады.

Подъем внутреннего давления в протоковыводящих путях печени приводит к тому, что желчь, содержащаяся в них, ввиду изменения сопротивления попадет в русло крови. В итоге наблюдается бактериемия. Чаще всего выявляют клебсиеллу или кишечную палочку. Просачивание болезнетворных микроорганизмов в систему тока крови провоцирует возникновение билиарного септического шока. Кроме того, развитие сепсиса происходит и в результате эндотоксемии. Эндотоксины бактерий, наделенные пирогенным действием, стимулируют свертывающую систему крови, что провоцирует внутрисосудистое образование сгустков. В результате гуморального иммунного ответа работа почек претерпевает сбой. В развитии токсемии особую роль играет нарушение функционирования, как общего, так и местного кишечного иммунитета.
Другие причины развития болезни
После удаления желчного пузыря холангит развивается более чем в пятидесяти процентов случаев. При этом недугу сопутствует сильное воспаление протоков. Провоцируют патологию следующие факторы:
- поражения глистами желчных протоков;
- гепатит;
- постхолецистэктомический синдром;
- проникновение патогенных микроорганизмов из области кишечника в органы ЖКТ;
- не леченый холецистит;
- кисты на желчных протоках.
Клиническая картина
При частичной или полной обструкции желчных протоков развивается острый гнойный холангит. Происходит все внезапно и начинается с подъема температуры до сорока градусов, озноба, тошноты, ощущения распирания и тяжести в правом подреберье. Желтуха в этом случае проявляется довольно быстро. При необструктивной гнойной форме желтушность неба, дермы и склер отсутствует или проявляется позднее.
Классическая триада острого течения болезни, а именно болевой синдром, лихорадка, желтуха, при полной обтурации желчных протоков наблюдается у пятидесяти процентов индивидов. Всегда присутствует билиарный сепсис – этот термин используют как в гастроэнтерологии, так и в абдоминальной хирургии, чтобы описать весьма тяжелое состояние индивида. При острых признаках застоя желчи в течение нескольких часов развивается сепсис. Причем он может возникнуть молниеносно и сопровождаться полиорганной недостаточностью и множественными абсцессами печени. Основные признаки билиарного сепсиса – это олигурия, нарушения сознания и низкое давление.
Диагностические мероприятия
Первоначально медик оценивает анамнез и жалобы индивида. При подозрении на воспаление желчных протоков, пациента консультирует абдоминальный хирург. Он выставляет предварительный диагноз. На развитие билиарного сепсиса указывает следующая симптоматика: желтушность, повышение температуры и давления, нарастание синдрома боли, тахипноэ, нарушение ритма сердца. В этом случае организм больного не реагирует на введение внутривенно 500 мл физраствора, имеется подтвержденная бактеримия, в желчевыводящих путях присутствует гной густой консистенции. Признаки острого воспаления выявляются на основании лабораторных исследований:
- В общем клиническом анализе крови – увеличение скорости оседания красных кровяных телец, нейтрофильный лейкоцитоз.
- В пробах печени – гиперфосфатемия, гипербилирубинемия, повышенный холестерин. В некоторых случаях повышается активность трансаминаз.
Для диагностики гнойного холангита непременно проводят УЗИ органов брюшной полости. При помощи этого вида аппаратного исследования:
- выявляют основание, вызвавшее недуг;
- визуализируют механическую преграду и расширение желчных ходов выше уровня препятствия;
- обнаруживают модификации паренхимы в случае образования гнойно-воспалительного процесса в печени.
На КТ уточняют и подтверждают полученные результаты. Кроме того, проводится эзофагогастродуоденоскопия. При необходимости, т. е. если доктор не располагает полной информацией, то рекомендуется эндоскопическая ретроградная холангиопанкреатография. При отсутствии возможности ее сделать, используют чрескожную чреспеченочную холангиографию.
Полученное при исследовании содержимое путей желчевыведения направляют на бактериологический анализ, где определяется чувствительность патогенного микроорганизма к антибиотикам. Желчь оценивается лаборантом визуально. Гнойная форма болезни доказывается наличием в ней гноя.
Хирургические методы
Лечение холангита, симптомы гнойной формы которого были описаны выше, требует оказания немедленного вмешательства медиков. Когда развился билиарный сепсис, необходима экстренная декомпрессия желчных путей. Если причина патологии рубцовые изменения, то благодаря установке эндопротеза в холедохе достигается адекватная компрессия.
Ввиду того, что открытые операции травматичны для больных и имеют частые осложнения, в наше время доктора предпочитают малоинвазивные вмешательства:
- Чрескожная чреспеченочная холангиостомия – окончательный способ лечения при наличии тяжелой сопутствующей патологии. В иных случаях – это предоперационная подготовка, в ходе проведения которой проводится отведение желчи до оперативной ликвидации помех.
- Механическая литотрипсия.
- Эндоскопическая папиллосфинктеротомия – полностью убирает стаз желчи и механическую желтуху. Применяется при этиологии калькулезно-воспалительного характера.
- и некоторые другие.
В зависимости от признаков застоя желчи, стадии нарушения ее оттока, уровня нахождения механической преграды, назначается выбор метода. После неотложной декомпрессии проводят радикальное лечение – холецистэктомия, холангиодуоденостомия или реканализация, если гнойная форма вызвана рубцовым сужением билиодигестивного анастомоза.
Консервативное лечение
После выполнения срочной декомпрессии показана антибиотикотерапия, она играет вспомогательную роль. Трудности на этом этапе врачевания связаны с тем, что выявление патогенного микроорганизма занимает длительный период, а кроме того, после, проведенного внешнего дренирования, состав флоры изменяется.

Прогноз
Гнойный холангит или воспалительный процесс, поражающий желчевыводящие пути в связи со сбоем или полной блокировкой оттока желчи считается тяжелой хирургической аномалией. Прогноз при этом недуге определяется не только уровнем перекрытия желчевыводящих путей, но и своевременностью оказания особой специальной помощи. К сожалению, смертность при этой болезни довольно высокая. Опасность гнойной формы болезни в том, что клиника сходна с иными разновидностями этой патологии, а несвоевременное и неверное лечение приводит к очень тяжелым последствиям – гнойной интоксикации, печеночной недостаточности, образовании в печении абсцессов.
Профилактика
Не допустить тяжелые осложнения можно при эндоскопическом лечении желчнокаменного заболевания. Кроме того, этому способствует новейшая хирургическая аппаратура и высокая квалификация абдоминального хирурга. Индивиды, проходившие оперативное лечение гнойного холангита, а также пациенты, в анамнезе которых есть эпизоды механической желтухи, находятся на диспансерном наблюдении врача-гастроэнтеролога. Для них проводятся плановые обследования, которые направлены на выявление наличия конкрементов и рубцовых стриктур желчевыводящих путей. Они на протяжение всей жизни придерживаются диетического питания. Оно помогает избежать нарушений выведения желчи и желчеобразования. При необходимости принимают медикаменты, рекомендованные доктором.
Абдоминальный хирург: кто это и что лечит?
Это доктор, который проводит хирургические вмешательства, используя различные инновационные методики и диагностическую аппаратуру. Он оперирует:
- травмы производственного и бытового характера;
- воспаление червеобразного отростка слепой кишки;
- полипы, варикозное расширение вен органов брюшины;
- проникающие ранения;
- новообразования;
- наследственные и приобретенные недуги органов брюшной полости;
- забрюшинное пространство.
Кроме того, лечит панкреатит, желчнокаменную болезнь, язвенные поражения, а также занимается профилактикой осложнений и реабилитацией индивидов.
В современных условиях абдоминальные хирурги выполняют экстренно и планово сложнейшие операции:
- На расстоянии (видеохирургия) – когда больной находится в труднодоступном районе, доктор руководит действиями медиков по видеосвязи.
- По трансплантации органов и тканей.
- Малоинвазивные эндоскопические операции (лапароскопия). В этих случаях хирург находится вне операционного поля и с помощью 3D-изображения на экране монитора и робота оперирует с высочайшей точностью.
При всех оперативных вмешательствах медики используют роботизированную технику и сложнейшую диагностическую аппаратуру. В многопрофильных учреждениях здравоохранения существуют узкие специализации абдоминальных хирургов – детский, гепатолог, онколог, гастроэнтеролог, колопроктолог.
Теперь вы знаете, кто это абдоминальный хирург и что лечит.



Что такое сепсис?
Наиболее частые возбудители, которые приводят к заражению, это бактерии стафилококки, стрептококки, кишечная палочка, а также различные грибы.
Причины сепсиса у взрослых
Наиболее частая причина сепсиса – это попадание в кровь вредных микроорганизмов – бактерий, грибков и вирусов. И чем сильнее заражается организм, тем тяжелее протекает заболевание. Особенно это касается тех случаев, когда инфицирование происходит сразу несколькими видами возбудителей.
Сепсис часто может развиваться на фоне ослабленной иммунной системы. Это происходит при онкологических заболеваний, при ВИЧ, при приеме препаратов, ослабляющих иммунную систему, при лучевой терапии и других факторах.
В ряде случаев сепсис может развиваться при распространении бактерий, которые полезны для организма. Например, кишечных бактерий, которые помогают переваривать пищу. При ослабленном иммунитете эти бактерии становятся опасными. При их попадании в кровь развивается интоксикация.
Виды сепсиса у взрослых
Сепсис может развиваться на фоне различных инфекционных заболеваний. Например:
- Тяжелая ангина;
- Пневмония;
- Онкологические заболевания;
- СПИД;
- Перитонит;
- Воспаление среднего уха (отит);
- Другие тяжелые раны и инфекции.
Различают три фазы развития сепсиса:
-
Токсемия – начальная фаза заболевания, при которой возбудитель выходит из первичного очага инфекции. Сопровождается активизацией иммунной системы в ответ инфицирование;
-
Септицемия – ухудшение общего состояния пациента, в результате проникновения в кровь микроорганизмов или их токсинов;
Септикопиемия – при этой форме сепсиса вместе с общей интоксикацией в организме образуются метастатические абсцессы (гнойные очаги). Они могут находится в различных тканях и органах.
- Молниеносный сепсис с быстрым развитием септического шока и летальным исходом через 1-2 дня;
- Острый сепсис с острой воспалительной реакцией в течение 5-28 суток;
- Подострый – заболевание длится около 3-4 месяцев;
- Хронический – может продолжаться до нескольких лет.
Симптомы сепсиса у взрослых
Симптомы заболевания могут различаться в зависимости от расположения первичного очага инфекции. Однако имеются и общие симптомы, которые встречаются у всех типов заболевания. Обычно это резкое повышение температуры, жар может периодически сменяться ознобом.
Когда заболевание начинает прогрессировать, меняется внешний вид пациента, заостряются черты и меняется цвет лица, на коже появляются высыпания (гнойники). Если заболевание протекает остро у больного может развиться истощение, обезвоживание организма и пролежни. К другим симптомам сепсиса относят:
- Вялость, заторможенность сознания;
- Слабый пульс, аритмию;
- Дыхательную недостаточность;
- Чередующиеся запоры и понос;
- Нарушение мочеиспускания из-за развития токсического нефрита;
- Мутные выделения из ран.
Диагностика сепсиса у взрослых
Лечение сепсиса у взрослых
Возможен ли благополучный исход такой грозного заболевания как сепсис? Согласно статистике, около 50% случаев сепсиса заканчиваются летальным исходом. Однако вылечить заболевание все же можно, если вовремя поставить диагноз и начать лечение.
Обычно таких больных помещают в палату интенсивной терапии, где под контролем специалистов проводят антибактериальную, дезинтоксикационную, симптоматическую терапию. При необходимости поддерживают работу важных органов, назначают иммуностимулирующие средства.
Удалить очаг инфекции можно только хирургическим способом, полностью удалив гнойник. В наиболее тяжелых случаях приходится удалять целиком орган.
Для того, чтобы уничтожить возбудителя инфекции внутривенно вводят антибиотики, к которым наиболее чувствительны микроорганизмы, вызвавшие заболевание.
Длительность лечения сепсиса составляет около 2 недель. Больного можно считать выздоровевшим после полной нормализации температуры и отсутствии возбудителей в двух посевах крови.
Острый холангит и билиарный сепсис (научный обзор)
По данным литературы проанализированы современные сведения об этиологии, патогенезе, клинике, диагностике и профилактике острого холангита и билиарного сепсиса. В 8–42 % случаев причиной острого холангита является холедохолитиаз. Острый гнойный холангит и билиарный сепсис — это разные проявления инфекционно-воспалительного процесса, который протекает местно и системно. Послеоперационная летальность составляет от 13 до 60 %. Многие вопросы патогенеза, лечения и профилактики этих патологических процессов не решены окончательно и нуждаются в дальнейшем изучении.
За даними літератури проаналізовані сучасні данi про етіологію, патогенез, клініку, діагностику та профілактику гострого холангіту і біліарного сепсису. У 8–42 % випадків причиною гострого холангіту є холедохолітіаз. Гострий гнійний холангіт і біліарний сепсис — це різні прояви інфекційно-запального процесу, що перебігає місцево та системно. Післяопераційна летальність становить від 13 до 60 %. Багато питань патогенезу, лікування і профілактики цих патологічних процесів не вирішені остаточно і потребують подальшого вивчення.
According to the literature data, there had been analyzed the modern data on the etiology, pathogenesis, clinical picture, diagnosis and prevention of acute cholangitis and biliary sepsis. In 8–42 % of cases, the cause of acute cholangitis is choledocholithiasis. Acute purulent cholangitis and biliary sepsis are different manifestations of infectious and inflammatory process, which occurs locally and systemically. Postoperative mortality ranged from 13 to 60 %. Many questions about pathogenesis, treatment and prevention of these pathological processes are not completely resolved and need further study.
острый холангит, билиарный сепсис, обзор литературы.
гострий холангіт, біліарний сепсис, огляд літератури.
acute cholangitis, biliary sepsis, literature review.
Гнойный холангит (ГХ) в настоящее время приобрел статус самостоятельной проблемы. Считается, что от 11 до 60 % пациентов с нарушением проходимости желчевыводящих протоков больны гнойным холангитом. На данный момент существует более 30 причин, которые могут обусловить нарушение оттока желчи [1, 13, 14, 16, 17]. Однако основной причиной гнойного холангита считают холедохолитиаз, который, в свою очередь, занимает ведущее место среди осложнений желчнокаменной болезни (ЖКБ) и наблюдается у 8,1–26,8 % больных ЖКБ [7, 18–20].
Холангит, или острое воспаление желчных протоков, впервые был описан J.M. Charkot в 1877 г. в виде триады клинических признаков: озноба, лихорадки и желтухи. В 1903 г. Rogers отметил связь между гнойным холангитом, обструкцией желчных протоков и абсцессами печени у больного, умершего после неудачной попытки разрешить холестаз [2, 4].
Считается, что без хирургического разрешения острый гнойный холангит приводит к смерти в 100 % случаев. Послеоперационная летальность, по данным разных авторов, колеблется в широких пределах и составляет от 13 до 60 % [9–11, 17].
Объективизация оценки тяжести состояния и прогноза заболевания имеет особое значение для разработки перспективных направлений лечения билиарного сепсиса, для которого характерна гетерогенность клинических проявлений [1, 3, 5]. Проблема объективной оценки операционного риска является краеугольным камнем медицины [8, 9, 20]. Большое разнообразие методов прогнозирования и профилактики БС, небольшое количество публикаций по тактике хирургического лечения еще раз свидетельствуют о необходимости продолжения исследований, определения новых путей и возможностей решения проблемы.
В основе инфекции желчевыводящих путей, как правило, лежат два предрасполагающих анатомофизиологических условия: стаз желчи и возможность развития микробной атаки. Застойная желчь подвержена сгущению, сладжу и легко инфицируется восходящим путем из кишечника. Наиболее распространенной причиной обструкции путей желчеоттока является холедохолитиаз. Нередко причиной обструкции могут быть также доброкачественные стриктуры желчных протоков [7, 15, 18].
Кроме того, наблюдается заброс содержимого тонкой кишки в желчевыводящие пути, вследствие чего развиваются рефлюксные холангиты. Однако патологический рефлюкс не играет определенной роли, если отток желчи происходит нормально. Так, после папиллосфинктеротомии, и особенно установки билиарных стентов, у многих больных наблюдается свободный рефлюкс воздуха и дуоденального содержимого в холедох и выявляется бактериальная колонизация желчи, что обычно не сопровождается развитием холангита [6, 20]. Последний может выступать как осложнение реконструктивных операций на желчных протоках. Ярким примером может служить также синдром слепого мешка (синдром отстойника, синдром клоаки).
Как правило, возбудителями холангитов являются микроорганизмы кишечной микрофлоры, в большинстве случаев встречающиеся в ассоциациях, что установлено по результатам посева желчи, взятой у больных. К ним относятся представители семейства энтеробактерий, среди которых доминирующую роль играет E.coli (50–60 %), с меньшей частотой встречается Klebsiella spp. (8–20 %), Serratia spp., Proteus spp., Enterobacter spp., Acinetobacter spp.; грамположительные микроорганизмы Streptococcus, Enterococcus, выявляемые, по данным различных исследователей, в 2–30 % случаев; неспорообразующие анаэробы Bacteroides spp., Clostridium spp., фузобактерии, пептококки (до 20 %); Pseudomonas spp. (2–4 % случаев). Явное превалирование грамотрицательной кишечной флоры бесспорно, однако существенная разница среди серий наблюдений отмечается в определении частоты анаэробов, стафилококков, стрептококков, Pseudomonas aeruginosa. Следует отметить, что у 13–18 % больных с типичной клинической картиной острого холангита микробная флора из желчи не высевается [7–9].
В настоящее время гнойный холангит приобрел статус самостоятельной проблемы, от решения которой зависит дальнейший прогресс хирургии гепатобилиопанкреатодуоденальной зоны. В значительной степени это обусловлено увеличением числа больных с осложненной формой желчнокаменной болезни, высоким уровнем ятрогенных повреждений желчных протоков, широким внедрением операций, нарушающих автономность желчевыделительной системы, и методик прямого контрастирования желчных протоков (чрескожночреспеченочная холангиостомия (ЧЧХС), эндоскопическая ретроградная панкреатохолангиография (ЭРПХГ)), склонностью гнойного холангита к генерализации с образованием множественных абсцессов печени, развитием БС.
По клиническому течению, остроте процесса и его тяжести гнойный холангит отличается определенной вариабельностью. Соответственно этому выделяют три его формы: острый и острый рецидивирующий, которые возникают при внезапной и практически полной закупорке желчных путей, а также хронический, когда вследствие неполной блокады желчных протоков сохраняется частичный желчеток, препятствующий развитию восходящей инфекции [2, 5, 6, 19].
Клиническая симптоматика при остром ГХ (ОГХ) складывается из триады Шарко или пентады Рейнольдса, включающей в себя недомогание, боли в правом подреберье, желтуху, спутанность сознания и артериальную гипотензию.
Установлены различия в скорости возникновения гнойного холангита у больных механической желтухой, а также сроках его трансформации в билиарный сепсис. Так, у 39,1 % больных с острым холангитом сепсис развивается быстро (от нескольких часов до нескольких дней) и нередко носит молниеносный характер, характеризуется бурным течением с частым развитием милиарных абсцессов печени и симптомами полиорганной недостаточности. У 60,9 % больных с длительно текущим хроническим холангитом он имеет затяжной характер и развивается медленно (от нескольких недель до нескольких месяцев). При хроническом сепсисе абсцессы единичные и нередко сливные.
Причинноследственная связь острого гнойного холангита и билиарного сепсиса очевидна, однако острый гнойный холангит — это прежде всего морфологические изменения во вне и внутрипеченочных желчных протоках. А билиарный сепсис — это патологический процесс, в основе которого лежит реакция организма на инфекцию в виде генерализованного (системного) воспаления. Иначе говоря, острый гнойный холангит и билиарный сепсис — это разные проявления инфекционновоспалительного процесса, который протекает местно и системно [7, 10, 11, 13].
Программа обследования больных при наличии у них определенных клинических признаков ОГХ включает в себя лабораторные (клиникобиохимические) и инструментальные исследования. При поступлении большинство больных указывает на острое начало и быстрое развитие заболевания, проявляющееся болями в правом подреберье и повышением температуры на фоне желтухи. Постановке диагноза могут способствовать данные анамнеза: перенесенные ранее операции на желчных путях, приступы холангита в прошлом, а также возможные осложнения диагностических или лечебных эндоскопических вмешательств.
При наличии у больных указанной симптоматики диагноз острого холангита правомочен; наличие гипертермии, а также выявляемого лабораторного лейкоцитоза в пределах 6–9 ´ 10 9 /л следует расценивать как результат выброса эндотоксина и медиаторов воспаления из гнойного очага (желчные протоки) в общий кровоток. Эти симптомы полностью купируются при местном лечении холангита на фоне восстановленного желчеоттока [5, 9, 10, 18].
Часть больных поступает в больницы в более тяжелом состоянии, когда помимо триады Шарко у них обнаруживаются разной степени выраженности клинические критерии системной воспалительной реакции (тахикардия, тахипноэ, гипертермия с ознобами), что при наличии очага гнойной инфекции (желчные пути) позволяет считать, что у этих больных ОГХ трансформировался в билиарный сепсис.
БС обусловлен распространенной и вышедшей изпод контроля активацией мононуклеарных фагоцитов (макрофагов), нейтрофилов и эндотелия сосудов. В результате такой активации эти клетки осуществляют гиперпродукцию цитокинов, что ведет к развитию синдрома системной воспалительной реакции (ССВР). Основой его являются не функциональные, а гистоструктурные (морфологические) изменения в органах и системах организма, усиление которых обусловливает их дисфункцию [7, 10, 11, 17].
Однако следует иметь в виду, что обнаруживаемый в анализах крови лейкоцитоз со сдвигом формулы влево является общим признаком недренируемого гнойника; данные биохимических исследований подтверждают наличие холестаза (гипербилирубинемия, гиперфосфатемия, гиперхолестеринемия). Некоторое диагностическое значение имеет повышенная активность трансаминаз, которая возникает при остро развившейся обструкции желчных путей [2, 10, 17, 19].
В диагностике ОГХ важное значение имеет ультразвуковое исследование (УЗИ) органов брюшной полости. Метод практически в 100 % наблюдений позволяет определить характер желтухи: признаки билиарной гипертензии в виде расширения ходов над уровнем препятствия всегда достоверно свидетельствуют о механической природе холестаза. Но при преходящей гипертензии диаметр протоков может оставаться нормальным. В этих случаях более информативными являются данные компьютерной томографии печени.
При ОГХ на сонограммах характерны изменения печени, паренхима которой теряет свою однородность за счет формирования вдоль желчных ходов очаговых образований с нечеткими контурами повышенной (воспалительные инфильтраты) или сниженной (микроабсцессы) эхогенности [1, 4, 5, 16].
При малоинформативном УЗИ выполняют эндоскопическую ретроградную холангиопанкреатографию, а при ее невозможности — чрескожную чреспеченочную холангиографию (ЧЧХГ). Во время катетеризации протоков для проведения холангиографии осуществляется забор желчи для микробиологических исследований. Предварительно полученная желчь оценивается микроскопически: наличие в ней гноя и фибрина подтверждает диагноз ОГХ. Бактериологическое исследование желчи направлено на идентификацию возбудителя инфекции желчных путей с определением его чувствительности к антибактериальным препаратам [2, 7, 11, 14].
Развившийся билиарный сепсис — это принципиально новое патологическое состояние, требующее особых подходов к лечебной тактике. Лечение больных острым гнойным холангитом необходимо начинать сразу при их поступлении в стационар. Следует иметь в виду, что в условиях желчной гипертензии при холангите самостоятельное значение медикаментозной терапии относительно невелико.
При угрожающем состоянии интенсивную терапию необходимо сочетать с немедленной декомпрессией. Несмотря на высокий уровень хирургической техники, анестезиологической и реанимационной помощи, традиционные операции представляют серьезную травму для больных, обусловливают нарушение топографоанатомических взаимоотношений органов, что ведет к функциональным и органическим изменениям. Кроме того, они сопровождаются большим количеством осложнений и высокой летальностью, особенно у пациентов старших возрастных групп с тяжелой сопутствующей патологией.
В связи с этим все больший интерес вызывает использование малоинвазивных методов, и в первую очередь эндоскопических, таких как папиллосфинктеротомия (ЭПСТ), назобилиарное дренирование, литоэкстракция и механическая литотрипсия, транспапиллярное эндопротезирование холедоха. Большинству больных, которым выполняется ЭРПХГ, производится ЭПСТ, являющаяся методом выбора для многих пациентов с калькулезновоспалительными заболеваниями органов панкреатобилиарной зоны. Внедрение ЭПСТ в хирургию панкреатобилиарной зоны в полной мере разрешило вопросы декомпрессии желчевыводящей системы на фоне механической желтухи и острого холангита [6, 10, 13, 14].
Показания к применению того или иного метода декомпрессии необходимо устанавливать строго индивидуально, в зависимости от клинической ситуации, характера, уровня и протяженности препятствия оттоку желчи, с учетом результатов прямых рентгеноконтрастных исследований желчных путей. Введение эндопротеза в холедох при его посттравматических рубцовых стриктурах и опухолях обеспечивает адекватную декомпрессию и в 90 % случаев разрешает холангит [5, 6, 9, 13].
Чрескожная чреспеченочная холангиостомия впервые была описана К.С. Weichel в 1964 г. и с тех пор рассматривается как способ декомпрессии желчных путей перед хирургическим вмешательством. Однако следует помнить, что данная процедура может являться источником таких осложнений, как сепсис и эндотоксический шок. С помощью ЧЧХС возможно как наружное отведение желчи, так и наружновнутреннее дренирование при проведении дренажа ниже препятствия или транспапиллярно. При внутрипеченочном стенозе и литиазе, вызывающем билиарный сепсис, методом выбора является ЧЧХС. Через холангиостому возможно проведение баллонной дилатации стриктур, фиброхоледохоскопии с внутрипротоковыми манипуляциями [7, 10].
Нередко пациентам после срочной декомпрессии билиарного тракта с применением малоинвазивной технологии выполняется радикальная операция: холецистэктомия, холедоходуоденостомия и др. В отдельных случаях наружное дренирование билиарного тракта с применением малоинвазивной технологии или без нее является окончательным методом лечения. В основном оно применяется у пациентов с онкологическими и тяжелыми сопутствующими заболеваниями [13–15].
Часто больные поступают в клинику в тяжелом состоянии после ряда повторных операций с синдромом механической желтухи, явлениями холангита, вторичным билиарным циррозом печени, портальной гипертензией. При обследовании у таких пациентов выявляются высокие рубцовые стриктуры желчных протоков вследствие их травматического повреждения при неоднократных повторных операциях и стриктуры билиодигестивного анастомоза. В тех случаях, когда у больных происходит рубцовое сужение билиодигестивного анастомоза, выполняется реканализация последнего с последующим транспеченочным дренированием. При рубцовом сужении протоков операция завершается созданием билиодигестивного анастомоза с транспеченочным дренированием [5, 12, 13, 17].
Одной из важнейших проблем в лечении холангита является выбор адекватной антибиотикотерапии. После декомпрессии антибактериальная терапия играет вспомогательную роль. При этом полной стерильности желчи (при взятии посева из Тдренажа) достичь не удается. Установлено, что без антибиотикотерапии титр микробных тел в желчи после декомпрессии не уменьшается. Кроме того, определение количества микроорганизмов в желчи считается трудоемкой задачей [2, 9, 10, 17].
При билиарном септическом шоке лечение более сложное. Эффективная интенсивная терапия билиарного сепсиса возможна только при условии полноценной хирургической санации очага инфекции и адекватной антимикробной терапии. Неадекватная стартовая антимикробная терапия — независимый фактор риска летального исхода у больных с билиарным сепсисом. Вместе с тем поддержание жизни больного, предотвращение и устранение органной дисфункции невозможны без проведения целенаправленной интенсивной терапии.
Конкретными задачами лечения острого холангита и билиарного сепсиса являются: неотложная декомпрессия желчных протоков, которая устраняет источник инфекции, адекватная антибактериальная терапия, гемодинамическая и респираторная поддержка, иммунокоррекция, нутритивная поддержка, профилактика образования стрессязв желудочнокишечного тракта.
Больные с острым холангитом должны проходить предоперационную подготовку, включающую в себя инфузионнодетоксикационную терапию и антибактериальную терапию в условиях отделения. Препаратами выбора для антибактериальной терапии являются цефалоспорины III поколения. Пациенты с билиарным сепсисом и тяжелым билиарным сепсисом должны госпитализироваться в отделение хирургической реанимации для предоперационной подготовки. Препаратами выбора для антибактериальной терапии билиарного сепсиса являются цефалоспорины III поколения, для тяжелого билиарного сепсиса — цефалоспорины IV поколения или карбапенемы [7–9, 13].
При оперативном вмешательстве предпочтение следует отдавать малоинвазивным методам лечения, а именно — ЭПСТ, ЧЧХС, так как использование данных технологий сопровождается низким количеством осложнений и меньшей летальностью.
При сочетании острого холангита, билиарного сепсиса и тяжелого билиарного сепсиса с острым холециститом операцией выбора следует считать лапароскопическую холецистэктомию с дренированием желчных протоков по Холстеду и интраоперационной холангиографией. При одиночном конкременте и его диаметре до 1,5 см в послеоперационном периоде выполняется ЭПСТ с удалением конкремента. Если конкременты множественные или диаметром более 1,5 см, то выполняется конверсия, производятся традиционная холедохолитотомия и холедохостомия по Керу [3–5, 10].
При стриктурах гепатикохоледоха и билиодигестивных анастомозов операцией выбора следует считать терминолатеральный гепатикоеюноанастомоз на изолированной по Ру петле тощей кишки с транспеченочным дренированием по Groetz — Saypol — Kurian сменными перфорированными транспеченочными дренажами. На 7е сутки послеоперационного периода целесообразна замена перфорированного дренажа на неперфорированный каркасный транспеченочный стент в целях профилактики холангита в послеоперационном периоде [3, 5, 10].
Таким образом, острый гнойный холангит и билиарный сепсис — это разные проявления тяжелого инфекционновоспалительного процесса, который протекает местно и системно. До настоящего времени некоторые вопросы их патогенеза, диагностики, лечения и профилактики окончательно не решены и требуют дальнейшего изучения.
Читайте также:


