Термин сепсис впервые ввел
Большой вклад в учение о сепсисе был внесен Н.И. Пироговым, который считал, что пиемия есть миазматическое заболевание, отличающееся особой прилипчивостью, продукт общего заражения организма в обширнейшем значении этого слова. Заразное начало — гипотетические миазмы (роль микробов в развитии сепсиса еще не была известна) образуются в тканях раны, подвергшихся обширному разрушению, а затем, при скоплении больных в закрытых помещениях госпиталя, накапливаются в окружающей среде и начинают поражать всех, даже не раненых.
Дальнейшие исследования показали, что трактовать течение сепсиса только с микробиологических позиций нельзя. В первой половине XX века исследователи стали сосредоточивать свое внимание не только на изучении возбудителей, но и на состоянии макроорганизма.
Макробиологическая теория И.В. Давыдовского (1928) внесла существенный вклад в понимание вопросов патогенеза сепсиса; согласно ей, сепсис стал трактоваться как общее инфекционное заболевание, обусловленное неспецифической реакцией организма на попадание в кровоток различных микроорганизмов и их токсинов. В середине XX века в вопросе патогенеза сепсиса возник ряд разночтений, взгляды ученых разделились на две группы, одни были сторонниками бактериологической теории, другие — токсической. Согласно бактериологической концепции, бактериемия считалась постоянным или непостоянным специфическим симптомом сепсиса.
Аллергическая теория (Royx I.C., 1983) предполагала, что патогенетические сдвиги в организме обусловлены реакцией аллергического типа на бактериальные токсины.
Нейротрофическая теория (Сперанский Г.Н. и др., 1937) основывается на работах И.П. Павлова, в которых показано главенствующее значение центральной нервной системы (ЦНС) в развитии патологии вообще. Согласно данной теории основная роль в развитии сепсиса отводится состоянию ЦНС и периферической нервной системы.
Цитокиновая теория (Ertel W., 1991) в настоящее время занимает доминирующее положение. Согласно данной теории эндотоксины бактерий вызывают поступление в кровь большого количества цитокинов. Они являются веществами, которые регулируют иммунитет. В результате увеличения в крови цитокинов поражается эндотелий и развивается синдром системной воспалительной реакции и иммунодепрессия.
Важным шагом можно считать принятие в Чикаго в 1991 году решения согласительной конференции, посвященной унификации клинических представлений о сепсисе и связанных с ним состояний. Были определены основные понятия и термины, которыми рекомендуется пользоваться, предложена удобная классификация. Последний пересмотр состоялся в 2016 году (Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016), опубликован 18 января 2017 года в журнале Intensive Care Med.
Определения и понятия
Сепсис — генерализованное инфекционное заболевание, не имеет склонности к самоликвидации (самовыздоровлению).
В соответствии с решением согласительной конференции Американской ассоциации пульмонологов и Общества специалистов критической медицины (ACCP/SCCM, Чикаго, 1991): сепсис — это патологический процесс, в основе которого лежит реакция организма в виде генерализованного (системного) воспаления на инфекцию различной природы (бактериальную, вирусную, грибковую).
Сепсис — одна из форм такой реакции, при которой как минимум два симптома SIRS развиваются в ответ на локальный инфекционный процесс. Локальное воспаление, сепсис, тяжелый сепсис и септический шок — это различные формы выраженности воспалительной реакции организма на инфекционный процесс. Тяжелый сепсис и септический шок являются наиболее тяжелыми формами такой реакции и сопровождаются нарушениями функций, дистантных от основного инфекционно-воспалительного процесса систем и органов.
В 2014 году была образована группа из 19 экспертов в области интенсивной терапии, хирургии, инфекционных болезней и пульмонологии, которые после 2 лет исследовательской работы вышли с предложениями о введении в клиническую практику новых определений. Быстрая оценка SOFA (Sepsis organ failure assessment) (quickSOFA или qSOFA) была введена группой Sepsis-3 на 45-м конгрессе Society Critical Care Medicine (SCCM) в феврале 2016 года в качестве упрощенной версии показателя SOFA и первичного способа выявления пациентов с высоким риском неблагоприятного исхода при инфицировании.
Предложение исключения симптомов SIRS вызвало неоднозначную реакцию в медицинском сообществе, несмотря на одобрение 31 общественной организации. Это обусловлено тем, что базовыми для большинства национальных и международных рекомендаций являются определения ACCP/SCCM 1991 года. Таким образом, в настоящее время нет однозначного мнения о необходимости и целесообразности перехода на использование Sepsis-З.
Следует отметить, что в Международной классификации болезней 10-го пересмотра критерии SIRS включены в разделы R57.2 — септический шок, R65(0-5) — синдром системной воспалительной реакции с последующей детализацией.
Классификация сепсиса
По клиническому течению различают сепсис:
- молниеносный — характерно чрезвычайно бурное начало и быстро прогрессирующее течение, комплекс клинических симптомов появляется за несколько часов, максимум через 1-2 дня с момента внедрения инфекции, часто заканчивается смертью больного;
- острый — клинические симптомы проявляются в течение нескольких дней, протекает более благоприятно, длится 2—4 недели;
- подострый — процесс развивается медленно, в течение нескольких недель, симптомы менее выражены, длительность заболевания — от 6 до 12 недель;
- хронический — в случаях, когда не удалось ликвидировать острый сепсис, он переходит в хроническую форму (сроки — более 3 месяцев), протекает с мало выраженной клинической симптоматикой и нередкими ремиссиями, заболевание продолжается несколько лет;
- рецидивирующий сепсис характеризуется сменой периодов обострений и периодов ремиссий;
- как особая форма хронического воспаления выделяется sepsis lenta.
По времени развития:
- ранний (развился до 10-14 дней с момента повреждения);
- поздний (развился позднее 2 недель с момента повреждения или гнойно-септического заболевания).
При наличии на месте входных ворот возбудителя инфекции первичного септического (гнойного) очага, обусловливающего развитие сепсиса, говорят о вторичном сепсисе, при отсутствии видимого септического очага сепсис условно называют первичным или криптогенным.
По характеру входных ворот возбудителя заболевания различают сепсис раневой и возникший на почве гнойно-воспалительных заболеваний различных органов; своеобразным видом сепсиса является ожоговый сепсис.
В зависимости от локализации первичного очага инфекции различают сепсис:
- одонтогенный (первичный очаг локализуется в полости рта);
- отогенный (возникающий как осложнение острого или хронического гнойного отита);
- риногенный (первичный очаг локализуется в полости носа и придаточных пазухах);
- тонзиллогенный (первичный очаг в миндалинах, чаще — небных);
- уросепсис (первичный очаг в почках и мочевых путях);
- акушерско-гинекологический (первичный очаг в матке или ее придатках);
- пупочный (наиболее частый у детей первого года жизни; первичный очаг локализуется в месте отделения культи пуповины);
- эндокардиальный (очаг инфекции локализуется в эндокарде, главным образом в клапанах сердца);
- ангиогенный (первичный очаг инфекции расположен внутри сосудов; нередко возникает как результат внутрисосудистых инструментальных исследований и длительного стояния центрального венозного катетера и т.д.);
- кожный (первичный очаг формируется в коже в виде пиодермии, гнойного пустулеза, фурункулов);
- кишечный (первичным очагом являются язвенно-некротический энтерит, колит, энтероколит).
Помимо перечисленных выше локализаций, септический очаг может находиться и в других органах при различных гнойных процессах, например, гнойно-деструктивных поражениях легких, плевры, гнойном перитоните, гнойном тромбофлебите и др.
Особую группу составляет так называемый хирургический сепсис, который объединяет все случаи заболеваний сепсисом по признаку наличия первичного или метастатического гнойного очага, доступного оперативному вмешательству. Чаще всего сюда относятся раневой и послеоперационный сепсис, когда входными воротами является рана, а также сепсис, возникающий на фоне или вследствие гнойных заболеваний, например, абсцесс, карбункул, остеомиелит, перитонит, флегмона, фурункул, эмпиема плевры, некротизирующая инфекция и другие.
Некротизирующая инфекция имеет множество названий, таких как антонов огонь, некротическая рожа, злокачественный отек, гангрена Фурнье, прогрессирующая гангрена мягких тканей, flesh-eating bacteria (бактерия, поедающая плоть), неудержимое омертвение кожи, эпифасциальная прогрессивная гангрена, госпитальная гангрена, фагеденическая язва, гемолитическая стрептококковая гангрена, острая дермальная гангрена, язва Мелени (Meleney ulcer), гнойный фасциит, синергический некротический целлюлит. Летальность при некротизирующих формах инфекции (НФИ), согласно данным литературы, составляет от 20 до 80 % и выше.
Некротизирующая инфекция I типа. Возбудителем является смешанная флора, однако главенствующая роль в развитии НФИ I типа отводится анаэробным грамположительным коккам рода Peptostreptococcus в ассоциации с такими бактериями, как грамотрицательные палочки рода Bacteroides — Fusobacterium, Proteus, Klebsiella, Ps. aeruginosa, Acinetobacter, и грамположительными кокками Staphylococcus spp., Enterococcus spp.
Некротизирующая инфекция II типа. Возбудителем является бета-гемолитический стрептококк группы А, с возможной ассоциацией с St. aureus. Характеризуется фульминантным течением, развитием септического шока и полиорганной недостаточности, а также высокой летальностью до 80—100 %. НФИ II типа требует дифференциальной диагностики с тяжелыми формами рожистого воспаления.
Некротизирующая инфекция III типа. Возбудителем является Clostridium spp., чаще всего выделяют Cl.perfringens, а также Cl.oedematiens, с развитием классического клостридиального мионекроза.
Возбудитель, характерный для морской/пресной среды обитания, — Vibrio vulnificu/aeromonas hydrophila. Данный вид возбудителя отмечается у людей с хроническими заболеваниями печени.
По характеру реакции организма больного:
- гиперергическая форма;
- нормергическая форма;
- гипергическая форма.
По фазам клинического течения:
- Фаза напряжения — стимуляция гипофизарно-адреналовой системы.
- Катаболическая фаза — нарушение метаболизма, преобладает катаболизм, нарушение кислотно-основного состояния и водно-электролитного баланса.
- Анаболическая фаза — с 10-12-го дня — восстановление обменных процессов (особенно протеины).
- Фаза реабилитации — полное восстановление обменных процессов.
По клинико-анатомическим признакам:
- септицемия (сепсис без метастазов);
- септикопиемия (сепсис с метастазами).
Септицемию (сепсис без гнойных метастазов), пиемию (сепсис с метастазами) и септикопиемию (смешанная форма сепсиса) большинство современных исследователей, как и Н.И. Пирогов, не считают принципиально различными формами сепсиса, а рассматривают скорее как различные фазы единого септического процесса, нередко переходящие одна в другую.
По бактериологическому признаку различают стафилококковый, стрептококковый, колибациллярный, псевдомонозный, анаэробный, гнилостный, грибковый и другие виды сепсиса.
Критерии диагностики сепсиса
Заболеваемость сепсисом в мире составляет 18–20 млн случаев в год, становясь причиной летального исхода у 4–6 млн человек. В США сепсис является причиной 6 % от всех смертей и входит в десятку причин летальных исходов, а в некардиологических отделениях реанимации и интенсивной терапии занимает второе место.
Известно, что у каждого четвертого пациента с тяжелым сепсисом развивается септический шок, летальность при котором достигает 80 %. Сепсис как таковой чаще всего не является самостоятельным заболеванием, развивается как осложнение многих патологических состояний.
Вызванный сепсисом ответ организма в виде органной дисфункции может быть скрытым, не всегда видимым клинически, и это, в свою очередь, вызывает необходимость рассматривать возможность наличия органной дисфункции у каждого пациента при наличии инфекционного процесса. И наоборот, нераспознанная инфекция может быть причиной развития органной дисфункции.
Все это создает необходимость иметь действенные критерии для диагностики и верификации сепсиса, более полного понимания клинической ситуации: оценки тяжести состояния с целью определения прогноза, показаний для госпитализации в отделение реанимации и интенсивной терапии, выбора объема терапии и мониторинга.
На данный момент на основании проведенных клинических и экспериментальных исследований рассматривают сепсис как патологический процесс, в основе которого лежит ответ организма в виде системной генерализованной реакции воспаления на инфекцию различной природы (бактериальную, вирусную, грибковую).
Клинической интерпретацией такого взгляда на патогенез сепсиса явились критерии диагностики и классификация, предложенные согласительной конференцией Американского колледжа пульмонологов и Общества специалистов критической медицины. Согласно критериям ACCP/SCCM локальный воспалительный процесс, сепсис, тяжелый сепсис и полиорганная недостаточность — это звенья одной цепи в реакции организма на воспаление вследствие микробной инвазии. В свою очередь, тяжелый сепсис и септический шок являются следствием прогрессирования системного воспаления с развитием нарушения функций систем и органов.
Для оценки органной, системной дисфункции и общей тяжести состояния больных с сепсисом с 1991 года рекомендовалась шкала SOFA. Шкала SOFA позволяет определять в количественном выражении и тяжесть органно-системных нарушений. Нулевое значение по шкале SOFA указывает на отсутствие органной дисфункции.
Патогенез сепсиса сейчас известен лучше, чем в 1991 г. Если раньше в основе критериев диагностики был SIRS, то теперь признают, что при сепсисе активируется не только воспалительный, но и противовоспалительный ответ. Задействуются не только иммунологические, но и другие пути (кардиологические, неврологические, гормональные, метаболические, коагуляционные), имеющие также высокую прогностическую значимость. Выраженная биологическая и клиническая гетерогенность пострадавших: возраст, преморбидный фон, принимаемые препараты, разные источники инфекции — создают высокую вариабельность начала и течения патологического процесса.
Самая популярная шкала, SOFA, за пределами отделений реанимации известна мало. Сейчас расшифровывается как Sequential Organ Failure (последовательная шкала органной недостаточности), раньше была Sepsis Related (связана с сепсисом). Хорошая, но сложная вне отделений интенсивной терапии.
К сожалению, из-за необходимости в лабораторных данных (число тромбоцитов, билирубина и креатинина, РаО2) затрудняется быстрая скрининговая оценка пациента. Принятая группой Sepsis-3 qSOFA показала высокие сравнимые с SOFA возможности прогнозирования госпитальной смертности для пациентов с подозрением на генерализованную инфекцию.
Органная дисфункция определяется как острое изменение по шкале qSOFA как > 2 балла. qSOFA > 2 балла отражает общую летальность примерно в 10 % в общей популяции больных с подозрением на инфекцию. Даже при умеренной органной дисфункции ситуация может быстро ухудшиться, если не предпринять быстро и правильно необходимые лечебные действия.
Длительно пребывающие больные с подозрением на инфекцию с высокой вероятностью могут быть быстро идентифицированы по qSOFA как пациенты с риском сепсиса и высокой летальностью (нарушение сознания, систолическое АД 22 в 1 минуту). Возрастание балльности по qSOFA должно подтолкнуть клинициста на поиск инфекции, углубленное обследование больного, более тщательный мониторинг.
Критериями септического шока в современном представлении являются наличие клиники сепсиса с персистирующей гипотензией, требующей применения вазопрессоров для поддержания среднего АД >65 мм рт.ст. на фоне проводимой жидкостной ресусцитации, при уровне лактата крови > 2 ммоль/л. Такое сочетание критериев приводит к летальности 40 % и более.
Наиболее надежным образом диагноз сепсиса устанавливается на основании следующих признаков (Гельфанд Б.Р. и соавт.):
- Клинические проявления инфекции или выделение возбудителя.
- Наличие воспалительного ответа и органной дисфункции.
- Лабораторные маркеры системного воспаления (специфичным является повышение в крови уровня прокальцитонина, С-реактивного протеина, а также интерлейкинов (IL)-1, -6, -8, -10 и фактора некроза опухоли (TNF)).
Развитие органно-системных повреждений при сепсисе связано прежде всего с неконтролируемым распространением из первичного очага инфекционного воспаления провоспалительных медиаторов с последующей активацией под их влиянием макрофагов, нейтрофилов, лимфоцитов и ряда других клеток в органах и тканях, с повреждением эндотелия и снижением органной перфузии и доставки кислорода. Диссеминация микроорганизмов может вообще отсутствовать или быть кратковременной, трудноуловимой.
Развивающаяся острофазовая реакция контролируется провоспалительными медиаторами (IL-1, -6, -8, TNF и др.) и их эндогенными антагонистами, такими как IL-4, -10, -13 и др., получившими название антивоспалительных медиаторов. В генезе острой сосудистой недостаточности, лежащей в основе септического шокового синдрома, ведущая роль отводится оксиду азота (NО), концентрация которого увеличивается в десятки раз в результате стимуляции макрофагов TNF, IL-1, IFN.
Прокальцитониновый тест является одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции. При неочевидной бактериальной природе системного ответа проведение прокальцитонинового теста позволяет в ранние сроки определить бактериальную природу септического процесса.
Для постановки диагноза сепсиса рекомендовано выполнение количественного прокальцитонинового теста. У здоровых людей уровни прокальцитонина очень низкие. При системных инфекциях, включая сепсис, уровни обычно выше 0,5-2 нг/мл и часто превышают уровень >10 нг/мл, что коррелирует с тяжестью заболевания и плохим прогнозом.
В качестве диагностического лабораторного теста при грибковой инфекции рекомендовано использовать определение маннанового антигена и антиманнановых антител в качестве дополнительных диагностических тестов.
Заключение
Новые определения сепсиса перенастроили фокус на переосмысление клинических проявлений этого синдрома и подчеркнули важность органной дисфункции как ключевого диагностического признака. Необъяснимая органная недостаточность у пациента должна насторожить врача в отношении возможности развития сепсиса. И от того, насколько быстро мы сможем среагировать на изменения, рационально и адресно назначить терапию, будет зависеть конечный результат.
Ежегодно в странах Западной Европы регистрируется более чем 500 000 случаев сепсиса; с определенным постоянством регистрируются случаи с сепсисом среди женщин (акушерско-гинекологический), среди новорожденных в развивающихся странах; все чаще приходится иметь дело с ВИЧ-инфицированными больными с развитием сепсиса; отсутствие специфической профилактики сепсиса в силу различных возбудителей этого состояния.
Обращает на себя внимание:
Что же такое сепсис?
Сепсис – это общий инфекционный процесс, который возникает в результате проникновения и распространения возбудителя из первичного очага в кровь с генерализацией процесса на фоне сниженной иммунологической реактивности организма (иммунодефицита).
Каковы причины развития сепсиса?
Возбудителями сепсиса могут быть многие патогенные и условно-патогенные бактерии. Их представители: семейство энтеробактерий – сальмонеллы, эшерихии, протей, клебсиелла, иерсинии, цитробактер и др; Staphilococcus – aureus, epidermalis (в последние годы возрасла роль устоучивых к антибиотикам штаммов стафилококка); Streptococcus – pneumoniae, piogenes, faecalis; Bacillae perfringens; Синегнойная палочка;
Грибы рода Candida; М.б. простейшие.
В 6 до 13% случаев сепсис вызывается несколькими возбудителями. Это часто наблюдается на фоне выраженного иммунодефицита (лейкемия, иммуносупрессивная терапия), при чем летальность при этом в 2,5 раза выше, чем при наличии одного микроба.
Факторы риска развития сепсиса
Зная факторы риска можно прогнозировать возможность развития септического состояния у пациентов. Вот некоторые состояния и заболевания, предрасполагающие к развитию сепсиса:
Сепсис развивается при определенных условиях:
- наличие первичного воспалительного очага или входных ворот инфекции (рана, носоглотка, кишечник и прочее);
- многократное или постоянное поступление возбудителя из первичного очага в кровоток (т.е. бактериемия);
- распространение возбудителя через кровь и формирование 2-х и более очагов;
- ацикличное течение болезни на фоне выраженного иммунодефицита.
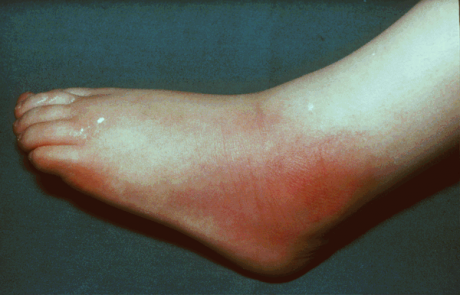
Септический артирит
Клинические симптомы и проявления сепсиса
Для большинства больных сепсисом характерно:
А. Септический синдром, который включает в себя:
- Инфекционно-токсический синдром (температура и симптомы интоксикации слабость, потеря аппетита, головная боль, сердцебиение).
- Спленомегалию – увеличение селезенки наблюдается у большинства больных.
- изменения периферической крови – нейтрофильный лейкоцитоз с воспалительным сдвигом влево, увеличение СОЭ, гипохромная анемия.
В тяжелых случаях острые воспалительные изменения в крови могут отсутствовать, что является плохим признаком в плане прогноза, также как и наличие абсолютной лимфопении.
Б. Симптомы поражения различных органов и систем:
- высыпания на коже и слизистых оболочках (пустулы, везикула, геморрагическая сыпь);
- опорно-двигательного аппарата (моноартриты, полиартриты инфекционно-аллергического характера, остеомиелит);
- развитие септической пневмонии, при которой преобладают деструктивные процессы при слабовыраженной воспалительной реакцией, и на первый план выступают явления ДН: одышка, участие вспомогательной мускулатуры в акте дыхания, цианоз;
- поражение сердечно-сосудистой системы (васкулиты, тромбофлебиты, эмболии, нарушение в системе гемостаза, нередко встречается эндокардит (при нем поражаются клапаны сердца как здоровые, так и измененные (склеротические изменения у пожилых, у лиц с ревматическими пороками);
- поражение органов пищеварения наблюдается крайне редко (возможно развитие энтероколитов, колитов с синдромом диареи в 60% случаев, возможно увеличение печени с нарушением ее функций;
- поражение почек – чаще токсический нефроз или диффузный нефрит с развитием ОПН, что сопровождается микробурией; ж) поражение ЦНС наблюдается не более чем в 2% случаев (гематоэнцефалический – серьезное препятствие для микроорганизмов).
Осложнения сепсиса: респираторный дистресс-синдром (дыхательная недостаточность), септический шок (гемодинамическая недостаточность), отек головного мозга.
Лабораторная диагностика сепсиса
- Изменения общего анализа крови: анемия, лейкоцитоз чаще нейтрофильный со сдвигом влево, увеличение СОЭ. Прогноз неблагоприятен: лейкопения с абсолютной лимфопенией (иммунный паралич).
- Экспресс-диагностика сепсиса по прокальцитонину (PCT-Q) — одному из воспалительных медиаторов. Исследуют сыворотку крови.
- 0,05 нг/мл. → норма;
- 2 нг/мл → повышенная вероятность наличия бактериального сепсиса;
- 10 нг/мл → тяжелый сепсис с развитием синдрома полиорганной недостаточности.
- Изоляция возбудителя из кровь, моча, кал, отпечатки – мазки, жидкости из полостей и т.п. методом посева на среды. Длительность – 6-10 дней.
Принципы терапии сепсиса. Лечение сепсиса
I. Организационно-режимные мероприятия (госпитализация больного в стационар, обеспечение тщательного ухода за больным (санация полости рта, поддержание гигиены, профилактика пролежней), обеспечение полноценного питания пациенту.
II. Этиотропная терапия (антибактериальная). Принципы: антибиотики назначается эмпирически (препараты широкого спектра действия) до прихода результатов антибиотикограммы выделенного возбудителя; далее назначаются к терапии препараты узкой направленности с учетом очага поражения и симптомов болезни.
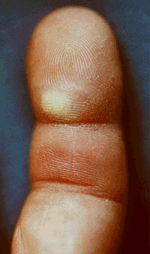
Стафилококковая септицемия
Для стартовой терапии используются цефалоспорины III-IV поколений, полусинтетические пенициллины, фторхинолоны, иногда карбапенемы. Для дополнительной комбинированной терапии назначаются аминогликозиды, цефалоспорины I-II поколений, макролиды, тетрациклины, При подозрении на анаэробный сепсис → метронидазол, при грибковом → амфотерицин, флюконазол, флуцитозин.
Санация первичного очага — удаление гнойный материал или дренирование местного очага инфекции (постоянный в/в или мочевой катетер, в брюшную полость, малый таз, паранефральное пространство).
Повышение иммунологической активности макроорганизма — это применение специфических и неспецифических иммунопрепаратов, иммунокорректоров (с большой осторожностью) — антистафилококковая плазма, антистафилококковый гамма-глобулин, человеческий гамма-глобулин, пентаглобин, антиэндотоксиновая плазма.
III. Патогенетическая терапия — направлена на детоксикацию организма, коррекцию нарушений гемостаза.
Профилактика сепсиса
Cвоевременное обращение за врачебной помощью при возникновении очагов воспаления, недопущения самолечения на дому антибактериальными препаратами, избегать переохлаждений, авитаминоза, трудоголизма с развитием синдрома усталости и, как следствие, иммунодефицита, диспансерное наблюдение больных с хроническими заболеваниями, своевременная терапия их обострений, соблюдение санитарно-эпидемиологического режима в отделениях во избежание внутрибольничных инфекций.
Протекает болезнь тяжело, быстро развивается, характеризуется отсутствием прогрессивной тенденции к скорейшему выздоровлению. В прошлом летальность при сепсисе крови доходила до 80%.
Благодаря современным возможностям медицины, антибактериальная и противогрибковая терапии снизили летальность в несколько раз, однако и в наше время при снижении общего иммунитета и защитных свойств местных барьеров эта болезнь нередко завершается серьезными осложнениями, такими как миокардит, септический эндокардит, нагноительные процессы в суставах, костях, брюшине, плевре и внутренних органах, которые, в свою очередь, сами становятся источниками распространения инфекции, что приводит к глубокой инвалидности и даже смерти.
Что это такое простыми словами?
Сепсис — это общее заражение организма, при котором инфекция распространяется с током крови. При сепсисе воспален не отдельный орган, а весь организм.
У 70% пациентов сепсис — осложнение местного воспаления: абсцесс, флегмона, фурункул, менингит, пневмония, плеврит, лимфаденит, пр., а также раневого процесса: травма, оперативное вмешательство, пр. Важно подчеркнуть, что сепсис развивается при истощении защитных сил организма (иммунитета) в результате затянувшегося первичного воспалительного процесса. Как правило, это происходит из-за запоздалого или неправильного лечения первичного воспалительного процесса.
Возбудители сепсиса — различные бактерии (стафилококки, стрептококки, менингококки, пневмококки, энтерококки, кишечная палочка, сальмонеллы, пр.) и грибы (Candida, Aspergillus, пр.).
Классификация
Формы сепсиса классифицируются в зависимости от локализации первичного инфекционного очага. На основании этого признака различают первичный (криптогенный, эссенциальный, идиопатический) и вторичный сепсис. При первичном сепсисе входные ворота обнаружить не удается. Вторичный септический процесс подразделяется на:
- плевро-легочный – развивается на фоне гнойных заболеваний легких (абсцедирующей пневмонии, эмпиемы плевры и др.)
- одонтогенный – обусловлен заболеваниями зубочелюстной системы (кариесом, корневыми гранулемами, апикальным периодонтитом, периоститом, околочелюстными флегмонами, остеомиелитом челюстей)
- тонзиллогенный – возникает на фоне тяжелых ангин, вызванных стрептококками или стафилококками
- хирургический – развивается при заносе инфекции в кровь из послеоперационной раны
- акушерско-гинекологический – возникает после осложненных абортов и родов
- уросепсис – характеризуется наличием входных ворот в отделах мочеполового аппарата (пиелонефрит, цистит, простатит)
- кожный – источником инфекции служат гнойные заболевания кожи и поврежденные кожные покровы (фурункулы, абсцессы, ожоги, инфицированные раны и др.)
- перитонеальный (в т. ч. билиарный, кишечный) – с локализацией первичных очагов в брюшной полости
- риногенный – развивается вследствие распространения инфекции из полости носа и придаточных пазух, обычно при синуситах
- отогенный — связан с воспалительными заболеваниями уха, чаще гнойным средним отитом.
- пупочный – встречается при омфалите новорожденных
По времени возникновения сепсис подразделяется на ранний (возникает в течение 2-х недель с момента появления первичного септического очага) и поздний (возникает позднее двухнедельного срока). По темпам развития сепсис может быть молниеносным (с быстрым развитием септического шока и наступлением летального исхода в течение 1-2 суток), острым (длительностью 4 недели), подострым (3-4 месяца), рецидивирующим (продолжительностью до 6 месяцев с чередованием затуханий и обострений) и хроническим (продолжительностью более года).
Сепсис в своем развитии проходит три фазы: токсемии, септицемии и септикопиемии. Фаза токсемии характеризуется развитием системного воспалительного ответа вследствие начала распространения микробных экзотоксинов из первичного очага инфекции; в этой фазе бактериемия отсутствует. Септицемия знаменуется диссеминацией возбудителей, развитием множественных вторичных септических очагов в виде микротромбов в микроциркуляторном русле; наблюдается стойкая бактериемия. Для фазы септикопиемии характерно образование вторичных метастатических гнойных очагов в органах и костной системе.
Причины развития сепсиса
Для развития сепсиса необходимо, чтобы в организм попали болезнетворные бактерии – возбудители инфекции (бактерии, вирусы, грибки). В результате массового инфицирования гнилостными продуктами разрушения патогенных микроорганизмов и токсинами возникает воспалительный процесс.
Воспалительная реакция организма, возникающая в ответ на внедрение инфекционных агентов, связано не столько с самими возбудителями, сколько с состоянием иммунных сил человека. Снижение защитных сил приводит к тому, что организм не может вовремя локализовать патогенные организмы и предотвратить их распространение внутрь различных органов.
Способствовать развитию сепсиса могут:
- Нарушение правил антисептики и асептики при обработке гнойных ран, а также при оперативных вмешательствах.
- Неправильный подбор антибактериальных средств при лечении внутренних воспалительных процессов.
- Расстройства иммунной системы.
Выше всего вероятность развития сепсиса у людей, имеющих длительные хронические заболевания, у которых на этом фоне наблюдается истощение иммунитета.
Какие болезни могут осложняться сепсисом:
- Остеомиелит;
- Ожоги, обширные травмы;
- Инфекционно-воспалительные заболевания;
- Раны и гнойники на коже;
- Пневмония, гнойные образования в легких;
- Тяжелые формы ангины;
- Инфекционно-воспалительные осложнения после перенесенной операции;
- Гнойный отит;
- Перитонит;
- Карбункул, фурункул;
- Врожденные патологии иммунной системы;
- Инфицирование после родов, выкидыщей, абортов;
- ВИЧ-инфекции;
- Онкологические заболевания.
Этот список достаточно условен, т.к. сепсис может осложнить любой инфекционно-воспалительный процесс в организме.
Для развития сепсиса необходимо соблюдение определенных условий:
- Наличие первичного очага (источника инфекции), из которого патогенные организмы попадают в кровь.
- Распространение возбудителей с системой кровотока по всему организму.
- Формирование вторичных очагов, из которых в дальнейшем возбудители также будут распространяться по организму.
- Ответ защитной системы, реагирующей на проникновение возбудителей воспалительным процессом.
- Неспособность организма выстроить необходимую иммунную защиту и своевременно реагировать на внедрение возбудителей.
Первые признаки
Жалобы больных весьма разнообразны, но основное внимание следует уделить следующим симптомам сепсиса:
- сильный озноб;
- повышение температуры тела;
- изменение психического состояния пациента (эйфория или, наоборот, апатия);
- усталый, безучастный взгляд;
- бледность кожных покровов;
- впалость щек;
- гиперемированость лица;
- обильное потоотделение;
- петехиальные кровоизлияния в виде полос и пятен на поверхности предплечий и голеней.
Кроме того, сепсис может проявляться герпесом на губах, кровоточивостью слизистых оболочек полости рта, затрудненным дыханием, появлением уплотнений и гнойничков на коже.
Симптомы сепсиса у взрослых
Клиническое течение сепсиса может быть молниеносным (бурное развитие проявлений в течение 1-2 суток), острым (до 5—7 суток), подострым и хроническим.
При диагностике различают:
- Синдром системной воспалительной реакции. Характеризуется изменением температуры тела (как в сторону повышения, более 38 °C, так и в сторону понижения — ниже 36 °C), учащенным сердцебиением (более 90 ударов в минуту) и дыханием (более 20 вдохов в минуту), изменением количества лейкоцитов в крови (менее 4×109 или более 12×109 клеток на литр крови).
- Сепсис. При тех же симптомах, что и в случае системного воспалительного синдрома, в одной из стерильных в норме тканей (в крови, цереброспинальной жидкости, в моче…) обнаруживают один из известных патогенов, выявляют признаки перитонита, пневмонии, пурпуры и других местных воспалительных процессов.
- Тяжелый сепсис. Характеризуется так же, как обычный сепсис, но с гипотензией, гипоперфузией или дисфункцией отдельных органов.
- Септический шок. Наиболее тяжелое состояние, после которого у каждого второго больного из-за нарушения кровоснабжения органов и тканей наступает смерть. Определяется теми же симптомами, что и сепсис, когда интенсивные реанимационные мероприятия не приводят к нормализации кровотока и уровня артериального давления. Другими признаками септического шока являются замедление образования мочи и спутанность сознания.
В феврале 2016 года понятия и диагностические критерии сепсиса были пересмотрены. Понятие синдрома системной воспалительной реакции и тяжелого сепсиса признаны неактуальными, понятиям сепсиса и септического шока даны новые определения.
Для выявления и диагностики сепсиса рекомендовано использовать шкалы SOFA и qSOFA.
Неонатальный сепсис
При развитии сепсиса у новорождённых (источник — гнойный процесс в тканях и сосудах пуповины — пупочный сепсис) характерны рвота, понос, полный отказ ребёнка от груди, быстрое похудение, обезвоживание; кожные покровы теряют эластичность, становятся сухими, иногда землистого цвета; нередко определяются местное нагноение в области пупка, глубокие флегмоны и абсцессы различной локализации.
К факторам сепсиса у новорождённых относятся:
Осложнения сепсиса
Наиболее тяжелое осложнение сепсиса. Нарушается работа всех органов, обмен веществ, кровоток.
Наиболее высок риск развития септического шока у пожилых лиц, больных с ослабленным иммунитетом. До половины всех пациентов с этим осложнением погибает.
Симптомы септического шока:
- повышение температуры тела более 39°C;
- либо снижение температуры тела менее 36°C;
- учащение пульса более 90 ударов в минуту;
- частое дыхание, одышка;
- тошнота, рвота, понос;
- уменьшение количества мочи;
- значительное ухудшение состояния больного;
- нарушение сознания: сначала больной становится возбужденным, утверждает, что с ним всё в порядке, а затем возникает вялость, заторможенность;
- жажда;
- падение артериального давления;
- сухость и бледность кожи;
- затем возникает холодный липкий пот;
- кровоизлияния на коже;
- синюшность кончиков пальцев, носа, губ, мочек ушей.
Если больному в состоянии септического шока не будет срочно оказана врачебная помощь – он погибнет.
Тромбофлебит – это воспаление венозной стенки с образованием на ней тромбов.
- боли в области пораженных вен;
- покраснение кожи, болезненные уплотнения;
- отек пораженной конечности.
Чаще всего является осложнением тромбофлебита. При тромбоэмболии кусок тромба отрывается, попадает с током крови в сердце, а затем в легочные сосуды. Достигая достаточно мелкого сосуда, тромб перекрывает его.
- одышка;
- кожа становится бледной, приобретает пепельно-серый оттенок;
- синюшность кончиков пальцев, носа, губ, мочек ушей;
- затруднение дыхания, слышны свистящие хрипы;
- кашель, во время которого с мокротой может отходить кровь;
- боль в половине грудной клетки;
- падение артериального давления;
- повышение частоты пульса до 100 ударов в минуту;
- сильные боли за грудиной;
- нарушение сердечного ритма;
- головокружение, шум в ушах;
- потеря сознания, обмороки;
- кома;
- боль под правым ребром;
- отрыжка, тошнота, рвота.
Течение тромбоэмболии легочной артерии может быть разным. Иногда она не сопровождается практически никакими симптомами, а иногда быстро приводит к гибели пациента.
Является, как правило, осложнением тромбофлебита. Часто происходит по ночам.
- нарушение сознания, состояние оглушенности;
- повышенная сонливость;
- нарушение ориентации во времени и пространстве;
- головные боли, симптомы, напоминающие менингит;
- нарушения движений и чувствительности, рефлексов, в зависимости от того, в каком сосуде застрял тромб, и какая часть мозга вследствие этого была лишена поступления кислорода.
Статистика показывает, что каждый четвертый больной сепсисом теряет около 20% массы.
В результате поражения сосудов при сепсисе могут развиваться внутренние кровотечения в разных органах, например, в желудке. Состояние больного ухудшается, появляется бледность, слабость.
Диагностика
Диагностика сепсиса проводится с использованием лабораторных и клинических методов:
- общий анализ крови позволяет выявить воспалительную картину в целом;
- посев крови. Для точного диагноза рекомендуется делать многократный посев, что позволяет учесть жизненный цикл возбудителя на разных этапах терапии. Кровь берется из вены пациента и подвергается лабораторному анализу;
- бакпосев содержащегося в гнойном очаге;
- биохимический анализ крови (берется из вены, анализ проводится натощак);
- метод ПЦР позволяет выделить ДНК возбудителя;
- для поиска первичных очагов используется рентген, УЗИ, компьютерная томография, МРТ.
Все эти методики позволяют диагностировать заражение крови, в том числе и криптогенный сепсис, и определить, как его лечить.
Лечение сепсиса
Сепсис лечится только в инфекционном или терапевтическом стационаре, в отделении реанимации и интенсивной терапии. Принципы лечения аналогичны лечению других очагов инфекции, но учитываются общее тяжелое состояние и риск летального исхода.
Для лечения сепсиса у взрослых применяют:
- антибиотики в максимальных дозах с учетом чувствительности, внутривенно.
- проводят активную борьбу с токсикозом,
- активизируют собственную иммунную систему, корректируют нарушенные процессы жизнедеятельности.
Необходимо создание покоя и изоляции, назначается особая диета, в случае тяжелого состояния – искусственное внутривенное питание.
Важно удаление инфекции из первичного очага, применение двух и более антибиотиков иногда в сочетании с гормонами.
При необходимости больным производят вливание плазмы крови, гамма-глобулина и глюкозы.
При формировании вторичных гнойных очагов необходимо их хирургическое лечение – вскрытие абсцессов, удаление гноя и промывание ран, иссечение пораженных участков.
Профилактика
Профилактика сепсиса основывается на правильном и своевременном лечении местных гнойных процессов и соблюдении асептических условий во время проведения операций и других медицинских манипуляций.
Читайте также:


