Доброкачественные опухоли и вич
Некоторые виды онкологических заболеваний так часто встречаются у больных СПИДом, что считаются СПИД-определяющими болезнями – это означает, что их присутствие у ВИЧ-инфицированного является признаком развития у такого больного СПИДа. Эти онкологические заболевания также называют СПИД-ассоциированными онкологическими заболеваниями, к которым относится:
- Саркома Капоши
- Лимфома (особенно неходжкинская лимфома и лимфома центральной нервной системы)
- Инвазивный рак шейки матки
К другим видам рака, которые с большей вероятностью могут развиться у ВИЧ-инфицированных, относятся: инвазивный рак анального канала, болезнь Ходжкина, рак лёгких, рак ротовой полости, рак яичек, рак кожи, включая базальный эпидермоцит и плоскоклеточную карциному, а также злокачественная меланома. Конечно, ВИЧ-отрицательные люди тоже могут болеть этими заболеваниями, даже теми, которые считаются СПИД-ассоциированными. Но таковыми они называются только тогда, когда возникают у ВИЧ-позитивных больных.
В развивающихся странах у 4 из 10 больных СПИДом в тот или иной момент болезни развивается рак. Тем не менее, общая картина раковых опухолей у ВИЧ-инфицированных изменяется. С распространением антиретровирусного лечения снизилось число случаев саркомы Капоши и неходжкинской лимфомы. Большинство других онкозаболеваний не замедлились благодаря анти-ВИЧ лечению, а их факторы риска остаются такими же, как у здоровых людей. Например, ВИЧ-позитивные курильщики имеют больше шансов получить рак губ, ротовой полости, горла и лёгких, чем здоровые некурящие люди.
Взаимосвязь между ВИЧ и другими онкологическими заболеваниями до сих пор не до конца установлена. Тем не менее, существует мнение, что рак развивается быстрее у людей с иммунной системой, ослабленной ВИЧ. К сожалению, рак у ВИЧ-инфицированных труднее поддается лечению, отчасти из-за ослабленной ВИЧ иммунной системы и сниженного количества белых кровяных телец, что является прямым результатом ВИЧ-инфекции. Прохождение химиотерапии может быть сложным для больных СПИДом, поскольку костный мозг, который должен производить новые клетки крови, иногда оказывается уже пораженным ВИЧ-инфекцией. Больные с подобной проблемой часто не могут пройти полный курс химиотерапии, не нанеся себе при этом серьезного вреда. Внедрение высокоактивной антиретровирусной терапии (ВААРТ) в конце 1990х привела к снижению частоты некоторых видов рака у ВИЧ-инфицированных и увеличило продолжительность жизни больных СПИДом. Это также позволило ВИЧ-позитивным больным проходить полные курсы химиотерапии в случае онкологических заболеваний. На данный момент для ВИЧ-инфицированных разрабатываются альтернативные методы лечения рака на основе моноклональных антител и трансплантации стволовых клеток.
Саркома Капоши (СК) когда-то была редкой болезнью, поражающей преимущественно пожилых мужчин средиземноморского или еврейского происхождения, больных, которым произвели пересадку органов, или молодых людей из Африки. Эта форма называется классической СК. Однако в 1970-х и 80-х годах число людей с СК стремительно возросло
За последние 25 лет большинство случаев СК в США было связано с ВИЧ-инфекцией у мужчин, практикующих секс с мужчинами. Эти случаи относятся кэпидемической СК. Сейчас известно, что СК у ВИЧ-инфицированных связана с другой вирусной инфекцией. Ее вызывает вирус под названием герпес-вирус человека 8-го типа (ГВЧ-8), также известный как герпес вирус, ассоциированный с саркомой Капоши. ГВЧ-8 не вызывает болезни у большинства ВИЧ-отрицательных людей. Инфицирование этим вирусов распространено в Соединенных Штатах среди мужчин, вступающих в половые отношения с мужчинами, хотя он также может передаваться во время секса между мужчиной и женщиной. Вирус был обнаружен в слюне, а значит, может передаваться во время глубоких поцелуев.
В большинстве случаев эпидемическая СК вызывает темно-фиолетовые или коричневатые злокачественные образования дермы (называемые лезиями), которые могут появляться в разных местах на теле. Такие образования могут возникнуть на коже или в полости рта, и повредить лимфатические узлы и другие органы, такие как пищеварительный тракт, лёгкие, печень и селезёнку.
Во время первичной диагностики у некоторых людей с эпидемической СК не обнаруживают никаких других симптомов, особенно если лезии возникают на коже. Однако у многих, даже при отсутствии образований на коже, бывают увеличенные лимфатические узлы, необъяснимое повышение температуры или потеря веса. Со временем симптомы эпидемической СК распространяются по всему телу. Если СК поражает значительную поверхность лёгкого или кишечника, это может приводить к фатальным последствиям.
Обычно больным, у которых диагностируют эпидемическую СК, назначают антиретровирусные препараты и противораковое лечение.
Неходжкинская лимфома (НХЛ) поражает 4-10% больных СПИДом. Это онкологическое заболевание, которое начинается в лимфоидной ткани и может распространяться на другие органы. С момента внедрения антиретровирусной терапии число ВИЧ-инфицированных, у которых развивается лимфома, значительно снизилось, хотя не настолько, как число больных с саркомой Капоши.
Неходжкинские лимфомы, которые обычно возникают у больных СПИДом, часто являются первичными лимфомами центральной нервной системы (ЦНС). Первичная лимфома ЦНС начинается в центральном или спинном мозге. Среди симптомов первичной лимфомы ЦНС могут быть: судороги, паралич лицевого нерва, замешательство, потеря памяти и сонливость (усталость). СПИД-ассоциированная неходжкинская лимфома также может провоцировать развитие других лимфом средней и высокой степени злокачественности, включая лимфому Беркитта.
Прогноз или итог для больных со СПИД-ассоциированной неходжкинской лимфомой частично зависит от типа лимфомы, а частично от функции иммунной системы пациента. Больные с генерализованной стадией неходжкинской лимфомы, количество CD4 Т-лимфоцитов которых составляет менее 200 на микролитр крови и/или те больные, которые не принимают антиретровирусной терапии, обычно чувствуют себя хуже, чем те, у которых эти факторы присутствуют.
По-видимому, наилучшим лечением для СПИД-ассоциированной неходжкинской лимфомы является использование препаратов, которые применяются для ВИЧ-отрицательных пациентов. Одно время лечение состояло из малых доз химиотерапии. Но с появлением ВААРТ многие пациенты могут получать стандартные комбинации лекарств, применяемые для химиотерапии у людей, которые не больны СПИДом. Использование кроветворных (гемопоэтических) факторов в комбинации с химиотерапией также показало многообещающие результаты при лечении ВИЧ-инфицированных пациентов.
Для больных с первичной лимфомой ЦНС, могут использоваться химиотерапия или облучение всего головного мозга. ВААРТ используется для улучшения функции иммунной системы и продления жизни.
ВИЧ-инфицированные женщины имеют повышенный риск развития внутриэпителиальной неоплазии шейки матки (ВНШМ). ВНШМ – это рост аномальных, предраковых клеток в шейке матки или нижней части матки. Со временем ВНШМ может перерасти в инвазивный рак шейки матки, при котором раковые клетки будут поражать более глубокие слои шейки матки (и, в конце концов, могут распространиться по всему организму).
ВНШМ должна своевременно лечиться (путем удаления или уничтожения внешних слоев клеток шейки матки), чтобы не дать ей перерасти в инвазивный рак. Исследования показали, что нелеченная неоплазия шейки матки с большей вероятностью переходит в инвазивный рак у ВИЧ-инфицированных женщин, чем у здоровых. Стандартное лечение ВНШЛ хуже действует на ВИЧ-инфицированных женщин. Шансы на возобновление болезни (рецидив) после прохождения лечения довольно высоки, что связывают с функцией женской иммунной системы. Женщины, имеющие число CD4 клеток меньше 50 на микролитр крови имеют высокие шансы рецидива ВНШМ.
ВИЧ-инфицированные женщины с инвазивным раком шейки матки и хорошей иммунной функцией обычно нормально переносят хирургическое вмешательство и проходят то же лечение, что и ВИЧ-отрицательные женщины. Больным с запущенной формой заболевания само облучение помогает плохо. Женщинам с запущенной формой рака шейки матки или его рецидивом проводят химиотерапию. После прохождения курса лечения больные должны постоянно находиться под наблюдением врача, чтобы убедиться, что болезнь не возобновится. Во время лечения рака иммунный статус больной должен постоянно проверяться, она должна принимать антиретровирусные препараты. Эти лекарства обычно прописываются для улучшения результатов лечения инвазивного рака шейки матки у ВИЧ-инфицированных женщин, невзирая на число CD4 клеток.
Женщины больные СПИДом и раком шейки матки одновременно, вылечиваются от рака не так успешно, как ВИЧ-отрицательные пациентки. Женщины с количеством CD4 клеток больше 500 склонны к более скорому выздоровлению.
Наряду с широким распространением антиретровирусного лечения, СПИД-ассоциированные онкологические заболевания случаются все реже. Однако, поскольку ВИЧ-инфицированные стали жить дольше, у них начали развиваться раковые опухоли, которые не всегда вызваны напрямую ВИЧ, например, рак лёгких, гортани, печени, кишечника и анального канала, а также болезнь Ходжкина и множественная миелома. В большинстве случаев курс лечения включает антиретровирусные препараты и обычное лечение против рака, применяемое для людей без ВИЧ. Одновременно используются любые необходимые лекарства от ВИЧ (например, антибиотики для предотвращения инфекция)
ВИЧ-инфекция — один из факторов, который во много раз повышает вероятность развития рака. Выяснили, какие именно онкозаболевания чаще всего могут возникать при положительном ВИЧ-статусе, как их вовремя обнаружить, и на какие факторы риска еще нужно обратить внимание людям, живущим с ВИЧ.
Главная мишень вируса — CD4-Т-лимфоциты. Они передают сигнал другим клеткам, которые защищают организм от рака. В результате вмешательства вируса количество CD4-T-лимфоцитов постепенно уменьшается. Критически низкий уровень этих клеток - одна из причин отсутствия согласованной работы между звеньями иммунитета и главный механизм, приводящий к развитию СПИДа.
Иммунитет человека с ВИЧ-инфекцией перестает контролировать процессы избыточного клеточного деления и злокачественной трансформации клеток. Вместе с уменьшением количества CD4-T-лимфоцитов происходит накопление раковых клеток. В результате у человека развиваются несколько видов опухолей, которые называют СПИД-индикаторными: появление такого вида рака с очень большой вероятностью означает наличие у человека СПИДа.
Однако повышается риск появления не только СПИД-индикаторных опухолей, но и тех видов рака, которые развиваются из-за потери иммунного контроля над несколькими онкогенными инфекциями: вирусом герпеса человека 8 типа (ВГЧ-8), вирусом папилломы человека (ВПЧ), вирусами гепатита В и С (ВГВ, ВГС), вирусом Эпштейна-Барр (ВЭБ) и другими.
Все эти состояния развиваются у людей с ВИЧ-инфекцией преимущественно на фоне снижения количества CD4-T-лимфоцитов до уровня менее 200 клеток/мкл (при разбросе в норме от 500 до 1100 клеток), но также могут возникать при нормальном или близком к нормальному уровню CD4-T-лимфоцитов.
Саркома Капоши (СК) — СПИД-индикаторная опухоль, при которой происходит злокачественная трансформация клеток лимфатических и кровеносных сосудов. Риск развития СК у пациентов с ВИЧ-инфекцией увеличивается в несколько сотен раз. Различные белки ВИЧ-1 способны усиливать воспаление и нарушать регуляцию в эндотелиальных клетках. Это приводит к тому, что саркома Капоши может развиться до того, как уровень CD4-T-лимфоцитов упадет ниже 200 клеток/мкл. Еще одно обязательное условие для возникновения СК — наличие в организме вируса герпеса человека 8 типа.
Саркома Капоши развивается в виде папулы, пятна, узелка, бляшки коричневого, розового, красного или темно-красного цвета от нескольких миллиметров до нескольких сантиметров в диаметре. Обычно высыпания концентрируются на ногах, голове, шее, на слизистой оболочке — в области неба, десен, конъюнктивы.
До эры внедрения лекарств от ВИЧ — антиретровирусной терапии (АРТ) 5-летняя выживаемость (с момента диагностики опухоли) пациентов с саркомой Капоши составляла менее 10%. Применение АРТ значительно улучшило ситуацию — сейчас речь идет о 74%, — а также позволило снизить риск развития СК.
Более половины случаев СК (56%) диагностируются сейчас в локальной форме — до того, как опухоль распространится на лимфатические узлы, слизистую ЖКТ, печень, селезенку и другие органы. Прием антиретровирусной терапии помогает значительно замедлить прогрессию болезни и предотвратить распространение СК по всему организму.
К сожалению, обнаружить саркому Капоши до появления симптомов не получится
Однако, человеку с ВИЧ и его амбулаторному врачу-инфекционисту необходимо учитывать несколько факторов риска развития этой опухоли:
- Этническая принадлежность: люди еврейского или средиземноморского происхождения, а также экваториальные африканцы;
- Мужской пол;
- Иммунодефицит: Люди с уровнем CD4-клеток менее 200 кл/мкл, те, кто перенес трансплантацию органов или костного мозга или постоянно принимает глюкокортикостероиды;
- Сексуальная ориентация: мужчины, имеющие секс с мужчинами(МСМ), подвержены более высокому риску развития СК.
К онкологическим заболеваниям, ассоциированным с вирусом папилломы человека, относятся инвазивный рак шейки матки (ИРШМ), сквамозный (чешуйчатый) рак головы/шеи, рак анального канала, вульвы и влагалища. СПИД-индикаторной из них является только ИРШМ.
Распространенность генитальной онкогенной инфекции ВПЧ среди женщин, живущих с ВИЧ, в целом выше, чем у остального населения.
Вирус папилломы человека способен к самопроизвольной элиминации — исчезновению из организма. У ВИЧ-положительных женщин этот процесс занимает больше времени, что увеличивает вероятность появления патологических изменений в шейке матки.
Продолжительный прием АРТ приводит к более низкой распространенности ВПЧ высокого риска и поражений шейки матки и даже предотвращает новые случаи ИРШМ.
Раннее начало антиретровирусной терапии, приверженность лечению обеспечивают снижение вирусной нагрузки — количества вируса в крови. Эти меры очень эффективны в отношении местного иммунитета слизистой оболочки и профилактики ИРШМ.
Скрининг ИРШМ заключается в проведении ПАП-теста и ВПЧ-теста (ПЦР). Женщины с ВИЧ-инфекцией в возрасте от 21 до 29 лет должны пройти ПАП-тест во время первичной диагностики ВИЧ, затем — через 12 месяцев, если анализ не показал патологии. Некоторые эксперты рекомендуют делать следующий ПАП-тест через 6 месяцев после первого. Если результаты трех последовательных мазков без отклонений, повторные тесты следует проводить каждые 3 года. ВПЧ-тест не рекомендуется подключать к ПАП-тесту до 30 лет — высока вероятность положительного результата, при этом оснований для активных действий нет. Лечения ВПЧ не существует, а для развития РШМ требуется, как правило, от 10 лет.
После 30 лет ПАП-тест и ВПЧ-тест проводятся совместно
У пациентов с ВИЧ-инфекцией повышается риск развития:
- гепатоцеллюлярной карциномы (ГЦК), связанной с вирусами гепатита С и В (ВГВ и ВГС) — в три раза;
- рака желудка, ассоциированного с инфекцией H.pylori;
- лимфомы Ходжкина — 8-13 раз. Риск связан с сопутствующей Эпштейн-Барр-инфекцией. Важно, что повсеместное внедрение АРТ не повлияло на показатели заболеваемости лимфомой Ходжкина в популяции людей с ВИЧ.
К факторам риска развития ГЦК у пациентов с ВИЧ относятся: цирроз печени, ожирение, диабет, возраст старше 60 лет, мужской пол.
Скрининг ГЦК проводится с помощью анализа крови на альфа-фетопротеин (АФП), который может продуцироваться раковыми клетками, или инструментальных методик диагностики — УЗИ, КТ, МРТ.
В последние годы всё чаще используется фиброскан для оценки стадии фиброза и близости к циррозу, независимому фактору риска ГЦК.
Предотвратить появление гепатоцеллюлярной карциномы можно с помощью своевременной вакцинации и ревакцинации от вирусного гепатита В и контроля вирусной нагрузки.
Несмотря на появление АРТ, НХЛ остаются актуальной проблемой для людей, длительное время живущих с ВИЧ. Хотя в большом количестве случаев неходжкинские лимфомы являются СПИД-индикаторными, они способны развиваться при нормальном уровне CD4-клеток и являются одной из наиболее частых причин смерти среди ВИЧ-положительных.
Общая выживаемость у пациентов с этим диагнозом низкая: более половины умирают в течение пяти лет от момента постановки диагноза
Отсюда возникают факторы риска развития НХЛ при ВИЧ-инфекции:
- наличие ко-инфекции вирусными гепатитами В, C, H.pylori;
- наличие вирусной нагрузки вируса Эпштейна-Барр или цитомегаловируса;
- наличие аутоиммунных заболеваний до постановки диагноза ВИЧ-инфекция;
- наличие специфических изменений в протеинограмме до или во время ВИЧ-инфекции;
- наличие минимальной вирусной нагрузки ВИЧ, несмотря на АРТ;
- снижение CD4-Т-лимфоцитов.
К скринингу неходжкинских лимфом относятся мониторинг вирусной нагрузки ВЭБ, ВГС, ВГВ и проведение инструментальной диагностики (КТ, МРТ, УЗИ, ФГДС).
С помощью контроля факторов риска и своевременного скрининга можно не только найти опухоль на ранней стадии, но и предотвратить заболевание.
Если рак все же обнаружили, ни в коем случае нельзя прерывать антиретровирусную терапию — она проводится по жизненным показаниям, что означает высокую вероятность неблагоприятного исхода противоопухолевой терапии без сопутствующего противовирусного лечения.
а) Определения:
• ВИЧ/СПИД-ассоциированные оппортунистические инфекции, новообразования
1. Общие характеристики манифестации ВИЧ/СПИД:
• Лучший диагностический критерий:
о Первичная лимфома ЦНС (ПЛЦНС): накапливающие контраст очаги поражения, часто имеющие геморрагический/некроти-ческий характер и локализующиеся в структуре базальных ганглиев, перивентрикулярного БВ
о Саркома Капоши (СК): объемное образование мягких тканей, локализующееся в коже волосистой части головы, интенсивно накапливающее контраст
о Бактериальные абсцессы (БА): образования с кольцевым характером накопления контрастного вещества и ↑ интенсивности сигнала на ДВИ
о Аспергиллез (Ас): множественные образования с кольцевым характером контрастирования
о Нейросифилис (НС): кортикальные/субкортикальные инфаркты, гранулемы, лептоменингеальное контрастирование
о Доброкачественные лимфоэпителиальные ВИЧ-ассоциированные образования (ДЛО-ВИЧ): множественные кистозные объемные образования обоих околоушных слюнных желез
• Локализация:
о ПЛЦНС: 90% локализованы супратенториально; часто поражаются глубокие ядра серого вещества, перивентрикулярное белое вещество
о СК: лицо, кожа головы и шеи
о БА: обычно в супратенториальных отделах, лобной и теменной областях больших полушарий
о Ас: бассейны кровоснабжения СМА, перфорантных артерий кортикальной/субкортикальной областей, базальных ганглив/таламуса
о НС: кортикальная/субкортикальная локализация, в оболочках мозга
о ДЛО-ВИЧ: околоушные слюнные железы
• Морфология:
о ПЛЦНС: одиночное объемное образование или множественные поражения
о СК: объемное образование мягких тканей с инфильтративным характером роста
о БА: гладкое образование с кольцевым характером накопления контрастного вещества
о Ас: множественные образования, часто расположенные в области бассейна кровоснабжения СМА
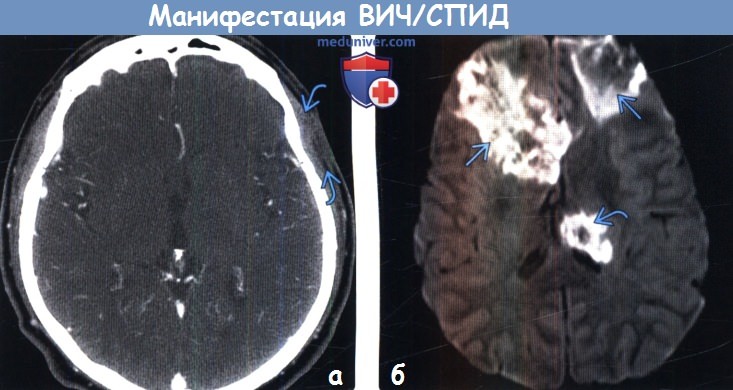
(а) КТ с контрастированием, аксиальный срез: у ВИЧ-положительного пациента с припухлостью кожи волосистой части головы определяется объемное образование мягких тканей с инфильтративным типом роста, вызывающее утолщение кожи волосистой части головы левой лобной области. При биопсии была обнаружена саркома Капоши. Саркома Капоши относится к группе СПИД-определяющих опухолей (СОО).
(б) МРТ, ДВИ, аксиальный срез: у ВИЧ-положительного пациента, поступившего в медицинское учреждение с изменениями чувствительности и судорожным синдромом в лобных долях и таламусе слева определяются крупные зоны ограничения диффузии.
2. КТ признаки манифестации ВИЧ/СПИД:
• Бесконтрастная КТ:
о ПЛЦНС: гиподенсная или гиперденсная зона, ± кровоизлияние, некроз
о СК: утолщение мягких тканей лица и волосистой части головы о БА: гиподенсное объемное образование с перифокальным отеком и масс-эффектом
о Ас: множественные кортикальные/субкортикальные образования низкой плотности; могут сочетаться с кровоизлиянием
о НС: образования изоинтенсивного по отношению к коре сигнала, имеющие периферическую локализацию
о ДЛО-ВИЧ: множественные двусторонние кистозные объемные образования, хорошо отграниченные от окружающих тканей, локализованные в структуре увеличенных околоушных слюнных желез
• КТ с контрастированием:
о ПЛЦНС: кольцевой характер накопления контрастного вещества у пациентов с ВИЧ
о СК: интенсивное накопление контраста объемным образованием в коже волосистой части головы
о БА: накопление контрастного вещества по типу тонкого кольца
о Ас: множественные образования с кольцевым характером контрастирования:
- Контрастное усиление может быть умеренным или интенсивным в зависимости от иммунного статуса
о НС: накапливающие контраст кортикальные очаги поражения ± утолщение твердой мозговой оболочки
о ДЛО-ВИЧ: кистозное образование с тонким ободком накопления контрастного вещества
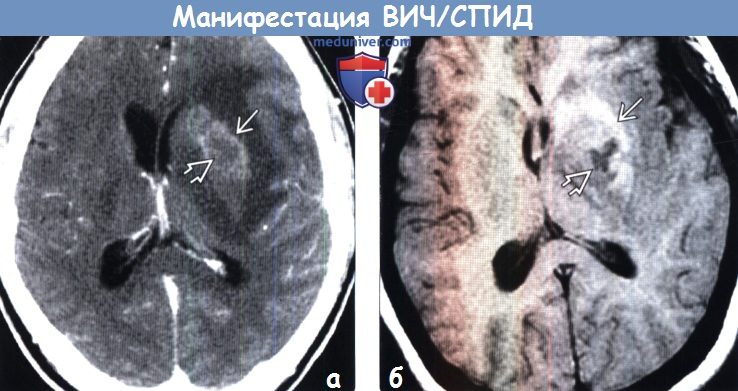
(а) КТ с контрастированием: у ВИЧ(+) пациента с одиночным объемным образованием, расположенным в области базальных ганглиев, вокруг зоны его центрального некроза определяется слабо заметное накопление контрастного вещества.
(б) МРТ, Т1-ВИ, аксиальный срез: у этого же пациента вокруг некротического ядра определяется повышение интенсивности сигнала вследствие подострого кровоизлияния. При лимфоме ЦНС редко наблюдаются кровоизлияния или некротические изменения, исключение составляют иммунокомпрометированные пациенты.
3. МРТ признаки манифестации ВИЧ/СПИД:
• Т1-ВИ:
о ПЛЦНС: изо-/гипоинтенсивный сигнал по отношению к коре головного мозга
о СК: локализованное утолщение волосистой части кожи головы, изоинтенсивное по отношению к мышечной ткани
о БА: на ранней стадии заболевания объемное образование, плохо отграниченное от окружающих тканей, имеет гипо-/изоин-тенсивный сигнал, на поздней стадии - гипоинтенсивные центральные отделы
о Ас: гипоинтенсивные объемные образования
- Кровоизлияние: ↑ интенсивности сигнала на Т1-ВИ
• Т2-ВИ:
о ПЛЦНС: изо-/гипоинтенсивный сигнал по отношению к коре, легкий перифокальный отек:
- Возможна неоднородность сигнала, что связано с кровоизлиянием и некрозом
о СК: объемное образование волосистой части кожи головы с сигналом, гипоинтенсивным по отношению к мышечным тканям о БА: капсула с характерным гипоинтенсивным на Т2-ВИ ободком
о Ас: неоднородный сигнал при наличии кровоизлияния о НС: гиперинтенсивные образования/инфаркты в кортикаль-ных/субкортикальных отделах
• ДВИ:
о ПЛЦНС: вариабельное ограничение диффузии
о БА: ↑ сигнала на ДВИ, низкий ИКД
о Ас: ограничение диффузии в стенке абсцесса
• Постконтрастное Т1-ВИ:
о ПЛЦНС: у пациентов с ВИЧ более часто наблюдается периферийный характер контрастирование образования с центральным некрозом, чем его гомогенный характер
о СК: интенсивное контрастирование объемного образования мягких тканей, локализованного в волосистой части кожи головы
о БА: на ранней стадии - фрагментарный характер контрастирования, на поздней - капсула в виде хорошо очерченной тонкой границы, накапливающей контрастное вещество
о Ас: множественные образования с кольцевым характером контрастирования
о НС: очаги поражения накапливают контрастное вещество; также наблюдается контрастирование вышележащих лептоменинкс/твердой мозговой оболочки
о ДЛО-ВИЧ: четко визуализируемые кистозные образования в околоушных слюнных железах с кольцевым характером накопления контраста
о Воспалительный синдром восстановления иммунитета (ВСВИ): образование(я) с атипичным характером контрастирования
• МР-спектроскопия
о ПЛЦНС: ↓ пика NAA, ↑ пика холина
о БА: в области центрального некроза могут наблюдаться пики ацетата, лактата, аланина, сукцината и аминокислот
4. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о Наиболее чувствительным методом является МРТ
• Советы по протоколу исследования:
о ПЛЦНС: МРТ с контрастным усилением
- ПЭТ или ОФЭКТ с Tl-201 полезны для дифференциальной диагностики стоксоплазмозом
о БА: МРТ с контрастным усилением, ДВИ, МР-спектроскопия
5. Радионуклидная диагностика:
• ПЛЦНС: гиперметаболизм при ПЭТ с ФДГ/ОФЭКТ с TI-201
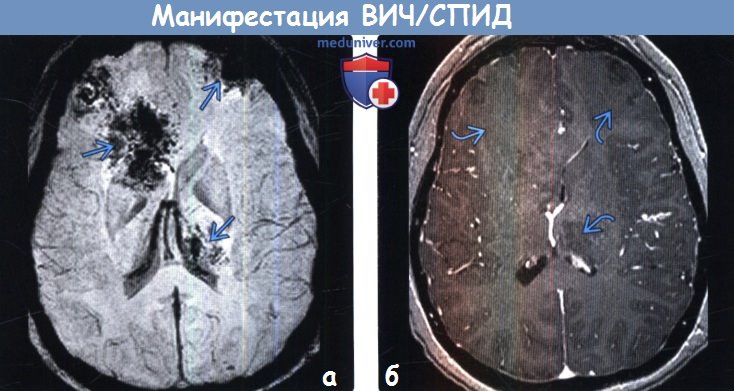
(а) MPT, SWI, аксиальный срез: у этого же пациента в выявленных на ДВИ зонах определяются участки кровоизлияния.
(б) МРТ, постконтрастное Т1 -ВИ, аксиальный срез: у этого же пациента не наблюдается патологического контрастирования мозговой ткани лобных долей или левой части таламуса. При биопсии зоны поражения правой лобной доли был обнаружен инвазивный аспергиллез. Аспергиллезная инфекция вызывает инфекционную васкулопатию, которая приводит к острому инфаркту, кровоизлиянию и церебриту/абсцессу.
1. Общие характеристики манифестации ВИЧ/СПИД:
• Этиология:
о ПЛЦНС: обычно диффузная В-крупноклеточная неходжкинская лимфома:
- Связана с количеством CD4(+) 3
- У пациентов с подавленным иммунитетом важную роль играет ВЭБ
о СК: вызывается герпесвирусом ВГЧ-8:
- Относится к группе СПИД-определяющих опухолей (СОО)
о БА: наиболее частыми возбудителями заболевания являются Staphylococcus и Streptococcus
о Ас: род Aspergillus = плесневые грибы с септированными гиалиновыми гифами:
- Наиболее частым возбудителем является Aspergillus fumigatus
- Гематогенное распространение из очага в легком или прямое распространение через пазухи
- Инфекционная васкулопатия: острый инфаркт, кровоизлияние, инфекционный церебрит/абсцесс
о НС: заболевание, передающееся половым путем, вызываемое спирохетой Treponema pallidum
о ВСВИ: восстановление иммунитета (спустя несколько недель после начала ВААРТ) → гиперактивный иммунный ответ
- Наиболее частый этиологический фактор - вирус JC (ПМЛ-ВСВИ)
2. Макроскопические и хирургические особенности:
• ПЛЦНС: одиночные, множественные объемные образования в больших полушариях головного мозга, центральный некроз/кровоизлияние при ВИЧ
• БА: зависит от стадии; очаги некроза, ободок из воспалительных клеток, грануляционной ткани, перифокальный вазогенный отек
• Ас: геморрагические инсульты с различными воспалительными изменениями
• НС: сифилитические гуммы; некротические объемные образования из грануляционной ткани (аваскулярные), хорошо отграниченные от окружающих тканей
д) Клиническая картина:
1. Проявления манифестации ВИЧ/СПИД:
• Наиболее частые признаки/симптомы:
о ПЛЦНС: летаргия, спутанность сознания, головная боль, судорожные приступы, очаговый двигательный дефицит
о СК: обычно протекает бессимптомно; симптомы могут появляться при изъязвлении образования или появлении локального масс-эффекта
о БА: наиболее частым симптомом является головная боль:
- Судорожные приступы, очаговая неврологическая симптоматика
о Ас: судорожные приступы, изменения психического состояния, очаговая симптоматика
о НС: часто протекает бессимптомно:
- Головные боли, судорожные приступы, изменения личности, спутанность сознания
о ДЛО-ВИЧ: двусторонние объемные образования в области околоушных слюнных желез
• Клинический профиль:
о ПЛЦНС: CD4(+) 3
- СМЖ: плеоцитоз, ↑ содержания белков; моноклональные лимфоциты с признаками злокачественности при цитологическом исследовании
- ПЦР: амплифкация ДНК ВЭБ в СМЖ
о СК: низкое число CD4 (например, 3 )
о НС: СМЖ - ↑ числа лейкоцитов, положительный VDRL-тест и/или положительный анализ на антитела к Т. pallidum
2. Демография:
• Эпидемиология:
о ПЛЦНС: второе по частоте объемное образование после токсоплазмоза у пациентов со СПИД:
- 2-6% пациентов со СПИД
о СК: ↓ распространенности СПИД-ассоциированной СК, что, возможно, обусловлено применением ВААРТ
о БА: у пациентов со СПИД встречается относительно нечасто
о НС: встречается примерно у 1,5% популяции со СПИД
о ДЛО-ВИЧ: 5% ВИЧ(+) пациентов
о ВСВИ: 25-35% ВИЧ(+) пациентов, у которых начинается ВААРТ
3. Лечение:
• ПЛЦНС: для постановки окончательного диагноза необходима стереотаксическая биопсия головного мозга:
о ВААРТ в сочетании с лучевой терапией
• СК: основным методом лечения является лучевая терапия
• БА: хирургическое дренирование, антибактериальная терапия
• Ас: хирургическое лечение, антимикотическая терапия
• НС: пенициллин ± стероидные препараты
• ДПЛ-ВИЧ: при использовании ВААРТ наблюдается тенденция к полному или частичному излечению
е) Диагностическая памятка:
1. Обратите внимание:
• Рассмотрите возможность проведения МРТ с ДВИ, МР-спектроскопии, ПЭТ/ОФЭКТ для того, чтобы дифференцировать оппортунистические инфекции от злокачественных образований
2. Советы по интерпретации изображений:
• У пациентов с ВИЧ дифференциальная диагностика между ПЛЦНС и токсоплазмозом представляет достаточную трудность
о Могут быть полезны ПЭТ/ОФЭКТ
• Для подтверждения бактериальных абсцессов, аспергиллеза, нейросифилиса может потребоваться хирургическая биопсия
ж) Список литературы:
1. Bilgrami М et al: Neurologic diseases in HIV-infected patients. Handb Clin Neurol. 121:1321-44, 2014
2. Gobert A et al: [HIV-related malignancies: state of art ] Bull Cancer. 101(1 0:1020-9, 2014
3. Rios A: HIV-related hematological malignancies: a concise review. Clin Lymphoma Myeloma Leuk. 14 Suppl: S96-103, 2014
Редактор: Искандер Милевски. Дата публикации: 18.4.2019
Читайте также:


