Новые подходы к лечению вич
Сегодня наиболее распространенные и опасные вирусные инфекции – это ВИЧ и гепатит. Эпидемиологическая ситуация последнего десятилетия в России характеризуется прогрессирующим увеличением числа больных СПИДом. На начало 2005 г. в нашей стране зарегистрировано более 300 тысяч ВИЧ-инфицированных. Однако есть все основания полагать, что их реальное число достигает одного миллиона.
Борьба с вирусными инфекциями в настоящее время становится одной из главных задач медицины. Для лечения вируса иммунодефицита человека в мире зарегистрировано около двадцати препаратов. По механизму действия и особенностям химического строения они разделяются на три группы: нуклеозидные ингибиторы обратной транскриптазы, ненуклеозидные ингибиторы обратной транскриптазы и ингибиторы протеазы. Для проведения терапии, как правило, используются комбинации из этих лекарств.
Несмотря на солидный перечень коммерческих препаратов, ученые всего мира продолжают разрабатывать все новые и новые противовирусные средства. Годовая стоимость лечения одного больного составляет $5000. При этом использование всех указанных лекарств и их комбинаций не позволяет полностью излечить человека, а только препятствует прогрессированию заболевания и предполагает проведение пожизненной терапии.
Принципиально новым и наиболее перспективным направлением лечения ВИЧ-инфекции сегодня является генотерапия. В результате реализации этого подхода возможно как полное излечение больных СПИДом, так и создание популяции, устойчивой к данному вирусу. Основа современной генотерапии – применение природных механизмов клетки, регулирующих экспрессию генов. На сегодняшний день наиболее изучены механизмы эпигенетического сайленсинга генов (от англ. silence – молчание). К ним относятся РНК-интерференция (защитный механизм, блокирующий работу строго определенных генов и не позволяющий им работать) и хромосомный сайленсинг.
Новые методы генотерапии
Этапы ВИЧ-инфекции, на которых ее возможно заблокировать с помощью siRNA (показаны красными крестами).
Преимущество данного подхода заключается в том, что он может быть использован для сайленсинга любых генов, вовлеченных в развитие патологии, а также позволяет разработать средство, пригодное как для лечения уже заболевших людей, так и для создания популяции, невосприимчивой к ВИЧ.
В отличие от зарубежных лабораторий, проводящих аналогичные исследования и применяющих для оценки противовирусного эффекта молекулярные клоны ВИЧ-1, в работе российских ученых по тестированию siРНК использовались лабораторные вирусные штаммы. Проведение таких исследований более трудоемко, так как предполагает работу с живым вирусом. Тем не менее, подобная модель эксперимента наиболее адекватна, если учитывать уникальное свойство вируса иммунодефицита человека – постоянное изменение его генетической структуры. Ученые уже доказали, что различные вирус-специфические siРНК обладают разной эффективностью подавления репродукции ВИЧ-1 на культуре клеток человека. Созданы две генетические конструкции, которые кодируют пока только две (отобранные из многих) siРНК, эффективно ингибирующие продукцию вируса.
Новые генетические конструкции
РНК-интерференция – природный механизм, обеспечивающий физиологическую регуляцию работы генов, а также защиту клеток от экспрессии чужеродной ДНК и РНК. Она отвечает за мощное и специфическое подавление экспрессии генов, транскрипты которых вовлечены в образование дуплексов РНК. Ключевым элементом в механизмах РНК-интерференции служат так называемые малые интерферирующие РНК (siРНК). Они обеспечивают узнавание молекул РНК, вовлеченных в образование дуплексов, а комплекс белков, в который входит siРНК, нарезает данные РНК до размеров siРНК (см. рисунок). В результате данный вид РНК практически полностью деградирует и экспрессия соответствующего гена блокируется.
Российские ученые планируют создать эффективно работающие генетические конструкции, так называемые кассеты. Они способны кодировать набор siРНК, подавляющих продукцию ВИЧ-1 в клетках человека, несмотря на появление нуклеотидных замен в каких-то отдельных мишенях вируса. Данные об эффективных siРНК позволяют также выбрать их последовательности для химического синтеза олигонуклеотидов ДНК и РНК.
Применяя такую систему, можно провести скрининг различных конструкций и получить количественные данные об эффективности РНК-интерференции. Несомненное достоинство подхода состоит в том, что он не требует работы с вирусом, а предполагает использование лишь разных коротких областей его генома, полученных с помощью ПЦР (полимеразной цепной реакции).
Для вируса иммунодефицита человека первого типа характерно быстрое возникновение и отбор мутантных вариантов, обладающих резистентностью к различным противовирусным препаратам. Для решения проблемы вирусной изменчивости ученые разработали и создали кассетные конструкции, стабильно экспрессирующие одновременно несколько siРНК. Затем, после оценки экспрессии сложных кассетных конструкций в безвирусной системе, разработчики использовали вирусную модель – культуру клеток человека, инфицированную различными штаммами ВИЧ-1, в частности, штаммами, репродуцирующимися по типу острой и хронической инфекции. Такой подход позволяет проводить исследования, приближенные к реальным процессам развития ВИЧ-инфекции в организме. Применение лабораторных штаммов ВИЧ-1 (в отличие от молекулярных клонов вируса) дает возможность оценивать влияние интерферирующих РНК на естественный пул вирусной популяции, заведомо обладающий генетическим разнообразием. Это также допускает проведение более объективной оценки противовирусной эффективности генетических конструкций.
Эффективность влияния различных конструкций ДНК и РНК оценивается по их способности подавлять репродукцию вируса в культуре клеток человека. Имея большой опыт работы по исследованию влияния различных противовирусных препаратов на репродукцию ВИЧ-1, российские ученые широко используют разработанную ими тест-систему для количественного определения вирусного антигена р24, которая позволяет достоверно оценивать интенсивность развития ВИЧ-инфекции в клетках.
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препара
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препарата. Препарат относится к ингибиторам обратной траскриптазы.
Препаратами второго поколения являются дидеоксииназин (ДДИ), дидеоксицитидин (ДДС). В настоящее время спектр препаратов этой группы значительно расширился (ставудин-ДДТ, хивид, фосфозид и другие).
Эта группа лекарственных средств (ЛС) имеет ряд существенных недостатков. Указанные ЛС не подавляют полностью репликацию вируса, который может быть выделен у большинства больных во время терапии.
Как показали исследования, к ЗДВ достаточно быстро развивается устойчивость, в особенности на поздних стадиях болезни с усиленной репликацией ВИЧ, когда, по-видимому, возникает резистентность и к другим аналогам нуклеозидов.
Обычный фактор, существенно ограничивающий применение ЛС этой группы, — их токсичность. Для ЗДВ характерно главным образом токсическое действие на костный мозг, тогда как ДДИ и ДДС обладают нейротоксическим действием. Кроме того, ДДИ может вызывать тяжелый острый геморрагический панкреатит.
Установлена тесная связь между клинической неэффективностью ЗДВ и резистентностью к нему in vitro.
Вторая группа препаратов, открытая сравнительно недавно и уже широко используемая, — это ингибиторы протеаз: индиновир (криксиван), инвираза (саквиновир), вирасепт (нельфиновир) и другие.
В настоящее время речь не идет уже о монотерапии антиретровирусными средствами, а только о ди-, три- и даже тетратерапии. Такие методики позволяют снижать концентрацию вируса до величин, не определяемых с помощью современных тест-систем ( В настоящее время практически не применяется монотерапия ВИЧ-инфекции, а применяется ди- , три- и даже тетратерапия. Такие методики позволяют снижать концентрацию вируса до величин, не определяемых с помощью современных тест-систем
- Использование многих этиотропных агентов более эффективно подавляет жизнедеятельность вируса, воздействуя на различные болевые точки или синергически воздействуя на одну из них.
- Это позволяет снизить дозы препаратов, что уменьшает частоту и выраженность побочных эффектов.
- Различные лекарства имеют различную способность проникать в ткани (головной мозг и т. д.).
- Комбинация лекарств затрудняет формирование устойчивости, или она появляется позднее.
Все описанные выше подходы к терапии ВИЧ-инфекции предполагали непосредственное воздействие на репликацию вируса. Другая возможная методика лечения ВИЧ-инфекции состоит в усилении защитных сил макроорганизма. Некоторые варианты такого подхода в большинстве случаев неспецифические, изредка специфические и могут воздействовать на защитные свойства клетки-хозяина.
Интерфероны, как природные, так и рекомбинантные, имеют ряд недостатков: антигенность, необходимость многократного введения для поддержания достаточной концентрации в организме, большое количество побочных эффектов и т. д.
Этих недостатков лишены многие индукторы эндогенного интерферона, некоторые из них способны включаться в синтез ИФН в некоторых популяциях клеток, что в ряде случаев имеет определенное преимущество перед поликлональной стимуляцией иммуноцитов интерфероном.
Специфическая активность циклоферона при ВИЧ-инфекции изучена в 1997 году в Институте гриппа РАМН
.
- Выявлена выраженная ингибирующая активность циклоферона на репродукцию ВИЧ в культуре клеток моноцитов.
- По показателям ингибирующей активности циклоферон значительно превосходит азидотимидин.
- Представленные экспериментальные данные обосновывают клиническое использование циклоферона для лечения больных ВИЧ-инфекцией.
Пятилетний опыт применения циклоферона у ВИЧ-инфицированных позволяет оценить результаты этой работы.
В период 1992 – 1997 годы в Санкт-петербургском городском центре по профилактике и борьбе со СПИД циклоферон получили 40 пациентов с разными стадиями ВИЧ-инфекции. Следует отметить, что 11 больных прошли два курса терапии циклофероном, в связи с чем общее число лиц, получивших один курс лечения циклофероном, составило 29 человек. В основном это были молодые люди в возрасте до 40 лет (20 человек), в том числе трое детей до 14 лет.
Курс циклоферона состоял из пяти внутримышечных инъекций 2 мл 12,5%-ного раствора в 1, 2, 4, 6, 8-й дни лечения. Препарат вводился как монотерапия у 29 ВИЧ-инфицированных и больных СПИД.
Все больные отмечали хорошую переносимость циклоферона, отсутствие пирогенных реакций после его введения.
Пациенты также констатировали улучшение общего состояния, сна и аппетита, повышение жизненного тонуса, работоспособности. 30% из числа получавших препарат и перенесших в осенне-зимний период грипп или ОРВИ отметили, что заболевание протекало непривычно легко и выздоровление наступило быстрее обычного.
Из клинической практики
После курса циклоферона отмечалось существенное снижение вирусной нагрузки (в 3,6 раза). Число CD4+ возросло на 62%. Монотерапия циклофероном оказала положительное стабильное влияние на изученные показатели у пациентов.
Определенный интерес представляют результаты многолетнего наблюдения больных ВИЧ-инфекцией, которые получали длительно циклоферон в своеобразном профилактическом режиме с целью стабилизации процесса и профилактики прогрессирования заболеваний.
В 1998 году на базе Российского научно-методического Центра по профилактике и борьбе со СПИД (руководитель член-корр. АМН В. В. Покровский) была изучена динамика суррогатных маркеров ВИЧ-инфекций (уровень CD4+) и вирусная нагрузка у больных ВИЧ-инфекцией при лечении циклофероном.
Оценка достоверности полученных результатов проводилась с помощью непараметрических критериев (критерий знаков, максимум-критерий, критерий Вилкоксона для сопряженных совокупностей).
2019. Второго человека в истории вылечили от ВИЧ

Врачи из Кембриджского университета (а именно, Равиндра Гупта - на фото) сообщили, что полностью вылечили некоего "Лондонского пациента" от ВИЧ-инфекции с помощью пересадки костного мозга. Три года назад ему пересадили клетки от человека с генетической мутацией CCR5 delta 32, дающей устойчивость к ВИЧ. И вот, после 3 лет БЕЗ антиретровирусной терапии в его крови вирус ВИЧ не обнаружили. Равиндра говорит, что это второй случай в истории после "Берлинского пациента", которого вылечили тем же способом в 2007 году. Правда, если б он читал наш сайт, то знал бы, что его коллеги из Британского Национального института в 2016 году тоже отрапортовали об излечении ВИЧ-пациента с помощью иммунотерапии.
2018. Коктейль из антител остановил ВИЧ на несколько месяцев
2018. Мозаичная вакцина против ВИЧ успешно прошла первый этап испытаний на людях
За последние 35 лет, прошедших с начала эпидемии ВИЧ-инфекции, только 4 вакцины добрались до стадии клинических испытаний на людях, и лишь одна из них более или менее успешно прошла эти испытания. Это вакцина RV144, тестировавшейся в Таиланде, которая снизила риск заражения на 31%. Неплохой результат, но недостаточный для выпуска нового профилактического препарата на рынок. Ученые из Гарвардской медицинской школы под руководством Дана Баруха недавно разработали пятую вакцину, которую уже успешно испытали на людях на предмет отсутствия побочных эффектов. Теперь начнется самое интересное - вторая стадия клинических испытаний - на эффективность. Ученые говорят, что у их вакцины больше шансов, т.к. фактически это не одна вакцина, а мозаика из 7 наиболее перспективных вакцин-кандидатов от различных штаммов вируса иммунодефицита.
2018. Разработана вакцина, защищающая от 30% штаммов ВИЧ
Американские вирусологи из Национального института по изучению аллергии и инфекций в Бетесде создали вакцину, эффективную против трети известных штаммов вируса ВИЧ. В ходе работ по изучению вируса ученые выявили в крови одного из носителей необычное антитело, которое довольно хорошо боролось с ВИЧ. Исследователи сделали копии этого антитела и заставили подействовать его на несколько копий вируса. Благодаря тому, что антитело проникало внутрь структуры, ученым удалось обнаружить ту часть белка, который сцепляется с клеткой перед ее заражением. Лишив вирус этой возможности, ученые смогли защитить здоровые клетки от заражения. Сейчас ученые занимаются модификацией вакцины с целью повышения ее эффективности, а полномасштабные клинические испытания на людях запланированы на вторую половину 2019 года.
2016. В России образовалась новая опасная модификация вируса ВИЧ
Хотя этот год ознаменован победой над вирусом ВИЧ, он (как и любой другой вирус) тоже не сидит на месте, а развивается, модифицируется. Новая опасная модификация образовалась в России из-за смешения ранее доминировавшего в РФ штамма A1 и нового агента A63, занесенного из Центральной Азии. Об сообщила лаборатория иммунохимии Института вирусологии имени Д.И. Ивановского. Таким образом, об окончательной победе можно будет говорить только с появлением технологий быстрого изготовления (обновляемых, а может и индивидуальных) вакцин с использованием искусственного интеллекта.
2016. Медики впервые вылечили взрослого человека от ВИЧ
Команда Британского Национального института медицинских исследований сообщила об успешном испытании новой терапии для борьбы с вирусом иммунодефицита человека (ВИЧ). Новый метод позволяет выявлять и уничтожать ВИЧ по всему организму, а не только в очагах его наивысшей активности. Сначала терапия ликвидирует пораженные клетки, а затем активирует T-лимфоциты, обеспечивающие иммунный ответ организма. Новая методика была испытана на 50 взрослых добровольцах. Успешный результат получили в первом же эксперименте. Исследователи заявили о том, что им удалось практически полностью вылечить 44-летнего пациента (на фото он улыбается). После терапии вирусов в его крови не обнаружили. Конечно, в случае с ВИЧ, нужно несколько лет, чтоб окончательно убедиться, что вирус покинул организм.
2016. Новая технология удаляет гены ВИЧ из клеток в живом организме

Исследователи из Темпльского университета (США) под руководством Камела Халили (на фото) впервые успешно вырезали сегмент ДНК, принадлежавший вирусу ВИЧ, из всех клеток в живом организме (мыши) с помощью технологии редактирования генов CRISPR/Cas9. В организмы животных вводили аденовирусный вектор — молекулу, которая содержала в себе необходимые нуклеотидные последовательности, а также гены белка Cas. Через две недели после начала эксперимента оказалось, что сегмент ВИЧ был вырезан из ДНК во всех тканях, в том числе в головном мозге, почках, печени, лёгких, селезёнке и клетках крови. Анализ вирусной РНК показал, что её количество сильно снизилось в клетках лимфоцитов, а также в лимфатических узлах.
2016. СПИД: врачи переходят в наступление
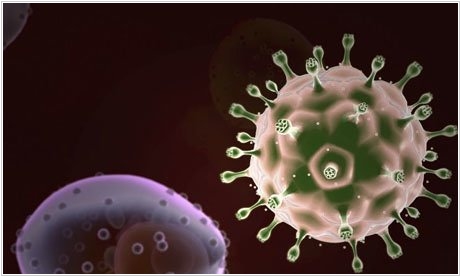
В прошлом году СПИД официально перестал считаться смертельным заболеванием. Современные антиретровирусные препараты могут подавить размножение вируса в организме. Однако, они не могут полностью удалить его из организма, поэтому пациентам с ВИЧ приходится принимать их всю оставшуюся жизнь. Поэтому теперь ученые и медики переходят в наступление: разрабатывают технологии для полного уничтожения вируса. Так, в Лёвенском университете (Бельгия) разработали препарат LEDGIN, который блокирует встраивание вируса ВИЧ в ДНК клеток и его размножение. Пока это все на уровне лабораторных испытаний и разработчики прогнозируют, что лечение, основанное на этом открытии, появится только через несколько лет.
2015. СПИД перестал быть смертельно опасным заболеванием
Сегодня во Всемирный день борьбы со СПИДом медики констатируют, что из смертельного заболевания СПИД уже превратился в хроническую болезнь. По последним данным статистики, средний возраст смерти ВИЧ-пациентов резко вырос по сравнению с 1987 годом. Для мужчин он вырос на 34 процента: с 37,9 (1987 год) до 50,8 года (2013). Среди женщин прогресс еще более разителен — с 35,2 года до 49,7 года. Таких результатов удалось добиться благодаря технологиям ранней диагностики и антиретровирусной терапии: даже у пациентов с ослабленной иммунной системой она повышает уровень жизни и резко снижает вероятность передачи вируса другим людям. Новейшие методы лечения СПИДа включают генотерапию и использование стволовых клеток.
2015. Медики разрабатывают прививку от СПИДа
2014. Hemopurifier - фильтр крови для лечения Гепатита, ВИЧ, Эболы и других вирусов
Американская компания Aethlon Medical разработала фильтр Hemopurifier, который может очищать кровь от вирусные инфекций, резистивных к медикаментам, в т.ч. Гепатита и ВИЧ. Как он работает - показано на видео. Стенки фильтра содержат антитела cyanovirin, которые притягивают к себе и выводят из крови вирусы. Фильтр используется на стандартном аппарате для гемодиализа. Aethlon Medical уже получила разрешение FDA на проведение клинических испытаний (на людях) по лечению Гепатита C, а также проводит клинические испытания по лечению ВИЧ в Индии. А вот на днях появилась информация, что в Университетской больнице Франкфурта Hemopurifier используется для лечения больных Эболой.
2014. Sangamo пробует лечить СПИД с помощью генотерапии

Вирус иммунодефицита (ВИЧ) уничтожает человеческие имунные Т-клетки, атакуя их белок, кодируемый геном CCR5, что и приводит к возникновению заболевания под названием СПИД. Американская биотехнологическая компания Sangamo использовала свою технологию молекулярных ножниц (ZFN-технологию), чтобы разрезать ДНК Т-клеток в определенных местах и отключить этот ген CCR5. В результате человеческие иммунные клетки становятся неуязвимыми к ВИЧ и распространение заболевания как минимум останавливается. А если учесть, что в организме постоянно появляются новые Т-клетки, а старые умирают, то потенциально с помощью генотерапии можно полностью излечить больного. Ученые не ограничились экспериментами в пробирке, а уже провели клиническое испытание на 12 пациентах. По окончании исследования у всех участников наблюдался повышенный уровень Т-клеток, а у одного из участников вирус не распространялся в организме в течение 12 недель после отмены антиретровирусной терапии.
2013. В США начали клинические испытания лечения СПИДа стволовыми клетками

Американская компания Calimmune объявила о начале официальных клинических испытаний своего препарата Cal-1, который изготавливается из собственных стволовых клеток пациента и применяется для лечения ВИЧ-инфекции. Учитывая то, как американский медицинский регулятор FDA подозрительно относится к стволовым клеткам, то, что он санкционировал эти испытания, означает, что надежда действительно есть. Первый ВИЧ-инфицированный пациент в Лос Анжелесе уже получил инъекцию нового лекарства. Результаты испытаний ожидают к 2015 году. Смысл технологии Calimmune примерно такой: гемопоэтические стволовые клетки пациента получают из его костного мозга и модифицируют с целью блокирования рецептора CCR5, что делает их невосприимчивыми к вирусу иммунодефицита человека. Затем их вводят вместе с собственными лимфоцитами пациента в кровеносную систему с целью развития резистентности организма к вирусу СПИДа.
2013. Наночастицы с пчелинным ядом могут убивать ВИЧ-вирусы
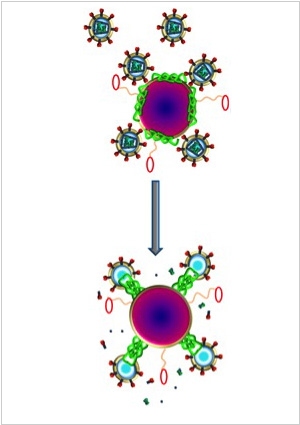
Команда ученых из Медицинской школы Университета Дж. Вашингтона разработала технологию уничтожения вируса иммунодефицита, вызывающего СПИД. Они использовали токсин Мелитин (пчелинный яд), обернув его в оболочку из наночастиц. Оболочка этих наноконтейнеров представляет собой множества бамперов, таким образом, они отталкиваются от здоровых клеток. А маленькие ВИЧ-вирусы застяют между бамперами и получают инъекцию мелитина, который разрушает их оболочку и делает их уязвимыми для антител организма. Такое нанолекарство может быть создано в виде интровагинального геля (для профилактики СПИДа) или в виде внутривенной инъекции для лечения уже зараженного организма. Ученые говорят, что теоретически, данная технология может быть использована и для уничтожения других вирусов, например Гепатита.
Блистая стильной бородой, на сцену конференции по ВИЧ и старению в Нью-Йорке вышел доктор Джованни Гуаральди и рассказал историю лиссабонского пациента — ВИЧ-положительного человека, которому в этом году исполнилось 100 лет. Гуаральди — не просто автор важнейших исследований по этой теме. Он также выступает за переосмысление и пересмотр помощи ВИЧ-позитивным людям по мере их старения, особенно сейчас, когда возраст более чем половины пациентов перевалил за 50, а к 2030-му около 40 % людей с ВИЧ будет 65.
Нынешних медицинских услуг для таких пациентов явно недостаточно — людям с ВИЧ требуется более тщательный подход к выявлению, диагностике и лечению заболеваний, вызванных старением.
Жуль Левин, активист Национального проекта по продвижению лечения СПИДа, пытается донести уже много лет мысль, что существующая система здравоохранения просто не готова предоставить необходимые услуги стареющим людям с ВИЧ. Он основывается на множестве исследований, подтверждающих более высокий уровень уязвимости, возрастных осложнений и инвалидности среди ВИЧ-положительных людей в сравнении с общей популяцией.

Его предостережения не были услышаны во многом из-за эйджизма — люди не любят слушать о проблемах, связанных со старением. Вероятно, проблему также усугубляет чувство вины выживших в эпидемии СПИДа 80-х. Более того, многие ВИЧ-позитивные люди, узнав о диагнозе, не могли представить, что доживут до 50. Еще одна грань этой проблемы — зачем жаловаться на естественный процесс старения, если чувствуешь себя хорошо?
Но на самом деле не похоже, что этот процесс вкупе с жизнью с вирусом иммунодефицита такой уж и естественный. Во-первых, вирус наносит почти всему организму огромный урон: мозгу, пищеварительной системе, сердцу, иммунной системе и другим органам.
Причем это происходит как и до начала лечения, так и после: из-за хронического воспаления, вызванного низким уровнем репликации вируса, из-за коинфекций (цитомегаловирус и гепатит), а также других факторов. Кроме того, люди с ВИЧ сталкиваются с отложенными последствиями лечения старыми, порой весьма токсичными, антиретровирусными препаратами. Хотя побочки есть даже и у современных лекарств — некоторые препараты могут изменять метаболизм и даже повреждать митохондрии — генераторы энергии для клеток. Вдобавок большинство живущих с ВИЧ-инфекцией подвергались серьезному эмоциональному стрессу: теряли близких людей, были стигматизированы, боролись со стереотипами и предвзятостью, страдали депрессией. Как следствие, вредные привычки и не самый здоровый образ жизни.
Поэтому неудивительно, что у многих людей с ВИЧ возрастные болячки проявляются раньше обычного. Несколько лет назад Гуаральди опубликовал исследование, которое подтвердило это и показывало: ряд возрастных осложнений у людей с ВИЧ встречался на 10–15 лет раньше среднего.

Но в то же время другие исследования наглядно демонстрируют: у тех, кто наблюдается у врачей и принимает современную антиретровирусную терапию, уровень здоровья как минимум сопоставим с людьми их возраста в краткосрочной перспективе. Это легко объясняется регулярными обследованиями, позволяющими ловить заболевания на ранних стадиях и относительно легко их пролечивать.
Лиссабонскому пациенту диагностировали ВИЧ в 84 года, на тот момент у него была запущенная стадия болезни и менее 100 CD4-лимфоцитов. Но после начала лечения он пошел на поправку. На конференции в Нью-Йорке, разбирая его историю, Гуаральди определил факторы, объясняющие, почему мужчина до сих пор в отличном состоянии: во-первых, он живет в здоровой среде. У него никогда не было финансовых проблем и сопутствующего с ними стресса, к тому же ему помогает 70-летняя дочь, живущая по соседству. Во-вторых, средиземноморская жизнь и диета — ежедневные походы по холмам Лиссабона в качестве кардионагрузки, а также оливки и рыба.

Другие подходы к лечению стареющих людей с ВИЧ
Именно сейчас необходимо повышать устойчивость к заболеваниям не только на индивидуальном уровне, но и в целом в обществе, а также в системе здравоохранения.
На индивидуальном уровне, главное, не зарывать голову в песок. Знание — сила. Многие помнят, как до появления эффективной антиретровирусной терапии, сделавшей ВИЧ хроническим контролируемым заболеванием, люди с диагнозом пытались найти всю доступную информацию об оппортунистических инфекциях, о фармацевтических разработках — кто-то даже начинал разбираться в теме лучше своих лечащих врачей. Проблема со старением может быть решена похожим образом: именно медики должны обращать внимание на то, какие шаги необходимо предпринять пациентам, чтобы стареть правильно.

Дата публикации: 05.05.2019 2019-05-05
Статья просмотрена: 653 раза
В настоящее время основой лечения пациентов с ВИЧ-инфекцией является антиретровирусная терапия (АРТ), позволяющая добиться контролируемого течения заболевания, основанная на одновременном использовании нескольких антиретровирусных препаратов, действующих на разные этапы жизненного цикла ВИЧ [3].Было доказано, что раннее начало АРТ позволяет достичь не только улучшения клинического прогноза заболевания, но и снижения уровня распространенности ВИЧ-инфекции в популяции. АРТ предполагает использование комбинации трех или более АРВ-препаратов для достижения адекватной вирусной супрессии [2].
Ключевые слова: антиретровирусная терапия, вирус иммунодефицита человека, побочные эффекты, рекомендации, ВОЗ, схемы лечения.
Число ВИЧ-инфицированных пациентов увеличивается с каждым годом. Количество инфицированных и больных ВИЧ- инфекцией в стране за период с 1987 по 2008 гг. превысило 400 тыс. человек [11]. По статистическим данным, на период начала 2017 года насчитывалось 36,7 миллионов заболевших, 2,1 миллиона детей. В России на 1 миллион граждан приходится 168 тысяч случаев ВИЧ-инфекции [8].
Наиболее распространенным и эффективным методом лечения ВИЧ- инфекции является антиретровирусная терапия (АРТ) [4]. Благодаря АРТ ВИЧ-инфекция из заболевания с неизбежным смертельным исходом превратилась в управляемое хроническое заболевание [7]. Основными задачами АРТ является максимальное снижение концентрации вирусной РНК в организме человека на длительный срок, а также сохранение или восстановление функций иммунной системы, сведение к минимуму числа осложнений и смертности от ВИЧ-инфекции, повышение качества жизни больного [2]. По рекомендациям ВОЗ антиретровирусную терапию рекомендовано предлагать на ранних стадиях, из-за доказанной большей ее эффективности [5].
По механизму действия выделяют следующие группы препаратов: ингибиторы проникновения, ингибиторы обратной транскриптазы, ингибиторы интегразы, ингибиторы протеазы [3]. В 1985 г. начались клинические испытания первого антиретровирусного препарата азидотимидин (зидовудин), в начале 90-х годов появились еще несколько препаратов, относящиеся группе нуклеозидных ингибиторов обратной транскриптазы (НИОТ)- диданозин (ddI), зальцитабин (ddC), ставудин (d4T), ламивудин (3ТС) [7]. Нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ) активны в инфицированных ВИЧ Т-клетках и макрофагах, ингибируют ранние стадии жизненного цикла вируса [5]. Главным прорывом стало появление во второй половине 90-х годов антиретровирусных препаратов других групп, в частности ингибиторов протеазы (ИП) [7]. Ингибиторы протеазы характеризуются высокой антиретровирусной активностью против ВИЧ-1 и ВИЧ-2 [5]. В последующие годы были введены в клиническую практику новые группы антиретровирусных препаратов: ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ), ингибиторы интегразы (ИИ), ингибиторы слияния (ИС) [7].
Учитывая задачи, механизм действия и нежелательное побочное действие, выделяют плюсы и минусы антиретровирусной терапии. К положительной стороне лечения относится: контроль за репродукцией вируса и его мутациями, замедление прогрессирования ВИЧ-инфекции, увеличение продолжительности жизни, снижение риска появлений новых устойчивых штаммов вируса, уменьшение риска побочных эффектов, возможно снижение риска передачи инфекции. Но положительную динамику можно увидеть только при условии регулярного применения препаратов и соблюдения схемы лечения. К сожалению, данные параметры не всегда соблюдаются пациентами. Минусами лечения являются: ухудшение качества жизни из-за побочных эффектов, неудобства схем лечения, раннее возникновение устойчивости к лекарственным средствам. Наличие побочные эффектов, которые представляют угрозу для жизни: цирроз печени (невирапин), токсический эпидермальный некролиз (невирапин, эфавиренц), лактатацидоз (ставудин), панкреатит (зидовудин), нефротоксическое действие (тенофовир), угнетение костного мозга (зидовудин) [5].
В развитии АРТ было несколько переломных моментов. Ранее основным приоритетом в лечении ВИЧ-инфекции было достижение эффективности, в том числе в ущерб безопасности и удобству режима терапии [2]. Постепенно требования к антиретровирусным препаратам увеличивались: приемлемая стоимость, хорошая переносимость и удобство приема, в последующем хорошая долгосрочная переносимость, удобство приема и высокий барьер к резистентности [4]. При этом, во всех случаях лечение должно быть комбинированным и соответствовать разработанным рекомендуемым схемам для предотвращения развития резистентности [4]. В настоящее время разработано большое разнообразие схем АРТ, поскольку используется более 20 препаратов 5 классов. Большинство комбинаций лекарственных препаратов для лечения ВИЧ-инфекции схожи по эффективности [6]. В 2000-х годах создавались новые препараты разных групп, отличавшиеся от ранее созданных препаратов меньшей токсичностью и более удобными для приема лекарственными формами. Все больше и больше становятся доступны комбинации антиретровирусных препаратов для приема одной или максимум двух таблеток в сутки.
Рекомендации EACS существенно изменились в вопросе выбора предпочтительных схем для начала терапии. В качестве предпочтительных стали указываться не возможные комбинации препаратов, а конкретные схемы.
1. RPV/TAF/FTC или RPV/TDF/FTC.
Оба сочетания принимаются в виде фиксированной комбинации доз (25/200/25 мг) или (300/200/25 мг), 1 таблетка в сутки.
1. DRV/c или DRV/r + TAF/FTC или TDF/FTC
Все препараты применяются 1 р/сут, TAF/FTC (25/200/25 мг), TDF/FTC (300/200/25 мг) и DRV/c (800/150 мг) применяются в виде ФКД, а DRV/r (800 + 100 мг) в виде отдельных препаратов дарунавира и ритонавира. Таким образом, данная комбинация может применяться в виде 2 или 3 таблеток 1 раз в день.
Принимается в виде фиксированной комбинации доз (600/300/50 мг), 1 таблетка в сутки.
2. DTG + TAF/FTC или TDF/FTC. Все препараты применяются 1 раз в сутки, TAF/FTC (25/200/25 мг) и TDF/FTC (300/200/25 мг) в виде ФКД, DTG (50 мг). Таким образом, эта схема включает в себя прием 2 таблеток 1 р/сут.
3. EVG/c/TAF/FTC или EVG/c/TDF/FTC
Оба варианта схемы принимаются в виде ФКД (300/200/150/150) или (10/200/150/150), 1 таблетка в сутки.
4. RAL + TAF/FTC или TDF/FTC
TAF/FTC (10/200 мг) и TDF/FTC (300/200 мг) применяются 1 раз в сутки в виде ФКД, RAL (400 мг) — 2 р/сут. Таким образом, пациент получает в сутки 3 таблетки — в один прием две, а в другой —одну.
С учетом новых рекомендаций ВОЗ в отношении лечения всех людей с ВИЧ, число людей, отвечающих критериям АРТ, увеличилось с 28 миллионов до 36,9 миллиона человек [9].
Рекомендации EACS регулярно обновляются. В процессе этих обновлений расширялись показания к назначению антиретровирусной терапии, включались новые препараты, выводились устаревшие. Менялись рекомендации по предпочтительности назначения отдельных препаратов и схем. Важнейшим положением, отраженным в рекомендациях EACS и DHHS, стала рекомендация по назначению АРТ практически всем пациентам с ВИЧ-инфекцией и как можно более раннее назначение этого лечения.
Второе направление предполагает генетическую модификацию цитотоксических лимфоцитов и/или В-лимфоцитов за счет введения генов, кодирующих специфические к ВИЧ рецепторы, цитокины или другие агенты, усиливающие противовирусный иммунный ответ хозяина. И, наконец, третье направление — это терапевтическая или профилактическая вакцинация, основанная на введении генов ВИЧ для экспрессии отдельных вирусных антигенов внутри клетки [13].
Несомненно, что появление новых препаратов для лечения ВИЧ-инфекции и новых научных и практических данных приведет к дальнейшему развитию рекомендаций по лечению ВИЧ-инфекции [7].
Читайте также:


