От ген или от генов вич
Кандидат биологических наук А. ЛУШНИКОВА. По материалам "Scientific American".
Иголка в стоге сена
Генетикам давно известны гены устойчивости к некоторым вирусам у мышей, например к вирусу лейкоза. Но существуют ли подобные гены у человека, и если да, то какова их роль в защите против СПИДа?
Стивен О'Брайн и Михаэль Дин со своими коллегами из Национального института рака США много лет вели поиск таких генов у человека.
В начале 80-х годов американские ученые исследовали множество людей, которые по тем или иным причинам могли заразиться вирусом иммунодефицита. Они проанализировали тысячи образцов крови и обнаружили, казалось бы, необъяснимое явление: у 10-25% обследованных вирус вообще не выявляется, а около 1% носителей ВИЧ - относительно здоровы, признаки СПИДа у них либо отсутствуют, либо выражены очень слабо, а иммунная система в полном порядке. Неужели существует какая-то устойчивость к вирусу у некоторых людей? И если да, то с чем она связана?
Опыты на лабораторных мышах, крысах, морских свинках и кроликах показали, что устойчивость к различным вирусным инфекциям часто определяется целым набором генов. Оказалось, что сходный механизм определяет и устойчивость к вирусу иммунодефицита человека.
Известно, что многие гены ответственны за выработку определенных белков. Часто бывает, что один и тот же ген существует в нескольких измененных вариантах. Такие "многоликие" гены называются полиморфными, а их варианты могут отвечать за выработку различных белков, которые по-разному ведут себя в клетке.
Сравнив восприимчивость к вирусам у мышей, несущих множество разнообразных наборов генов, и у мышей с небольшим числом генных вариантов, ученые пришли к выводу, что чем разнороднее генетически были животные, тем реже они заражались вирусом. В таком случае можно предположить, что в генетически разнообразных человеческих популяциях генные варианты, определяющие устойчивость к ВИЧ, должны встречаться достаточно часто. Анализ заболеваемости СПИДом среди американцев различных национальностей выявил еще одну особенность: более устойчивы американцы европейского происхождения, у африканцев и азиатов устойчивость близка к нулю. Чем объяснить такие различия?
Ответ на этот вопрос предложил в середине 80-х годов американский вирусолог Джей Леви из Калифорнийского университета в Сан-Франциско. Леви и его коллеги пытались выяснить, какие именно клетки в организме поражает вирус. Они обнаружили, что после того, как вирус заражает иммунные клетки, они легко узнаются иммунными клетками другого типа, так называемыми Т-киллерами (убийцами). Киллеры разрушают зараженные вирусом клетки, препятствуя дальнейшему размножению вируса. Клетки-убийцы несут на своей поверхности особую молекулу - рецептор CD8. Она, как принимающая антенна, "узнает" сигналы от клеток, зараженных вирусом, и клетки-убийцы уничтожают их. Если из крови удалить все клетки, несущие молекулу CD8, то вскоре в организме обнаруживаются многочисленные вирусные частицы, происходит быстрое размножение вируса и разрушение лимфоцитов. Не в этом ли ключ к разгадке?
В 1995 году группа американских ученых под руководством Р. Галло обнаружила вещества, которые вырабатываются в клетках-киллерах, несущих молекулы CD8, и подавляют размножение ВИЧ. Защитные вещества оказались гормоноподобными молекулами, называемыми хемокинами. Это небольшие белки, которые прикрепляются к молекулам-рецепторам на поверхности иммунных клеток, когда клетки направляются к месту воспаления или заражения. Оставалось найти "ворота", сквозь которые проникают в иммунные клетки вирусные частицы, то есть понять, с какими именно рецепторами взаимодействуют хемокины.
Ахиллесова пята иммунных клеток
Вскоре после открытия хемокинов Эдвард Бергер, биохимик из Национального института аллергических и инфекционных болезней в Бетезде, США, обнаружил в иммунных клетках, в первую очередь поражаемых вирусом (их называют клетки-мишени), сложный по строению белок. Этот белок как бы пронизывает мембраны клеток и содействует "посадке" и слиянию вирусных частиц с оболочкой иммунных клеток. Бергер назвал этот белок "фузин", от английского слова fusion - слияние. Оказалось, что фузин родствен белкам-рецепторам хемокинов. Не служит ли этот белок "входными воротами" иммунных клеток, через которые вирус проникает внутрь? В таком случае взаимодействие с фузином какого-нибудь другого вещества закроет доступ вирусным частицам в клетку: представьте, что в скважину замка вставляется ключ, и вирусная "лазейка" исчезает. Казалось бы, все встало на свои места, и взаимосвязь хемокины - фузин - ВИЧ уже не вызывала сомнений. Но верна ли эта схема для всех типов клеток, зараженных вирусом?
Пока молекулярные биологи распутывали сложный клубок событий, происходящих на поверхности клеток, генетики продолжали поиск генов устойчивости к вирусу иммунодефицита у людей. Американские исследователи из Национального института рака получили культуры клеток крови и различных тканей от сотен пациентов, зараженных ВИЧ. Из этих клеток выделили ДНК для поиска генов устойчивости.
Чтобы понять, насколько сложна эта задача, достаточно вспомнить, что в хромосомах человека содержится около 100 тысяч различных генов. Проверка хотя бы сотой доли этих генов потребовала бы нескольких лет напряженной работы. Круг генов-кандидатов заметно сузился, когда ученые сосредоточили свое внимание на клетках, которые прежде всего поражает вирус, - так называемых клетках-мишенях.
Уравнение со многими неизвестными
Одна из особенностей вируса иммунодефицита заключается в том, что его гены внедряются в наследственное вещество зараженной клетки и "затаиваются" там на время. Пока эта клетка растет и размножается, вирусные гены воспроизводятся вместе с собственными генами клетки. Затем они попадают в дочерние клетки и заражают их.
Из множества людей с высоким риском заражения ВИЧ отобрали зараженных вирусом и тех, кто не стал носителем ВИЧ, несмотря на постоянные контакты с больными. Среди зараженных выделили группы относительно здоровых и людей с быстро развивающимися признаками СПИДа, которые страдали сопутствующими заболеваниями: пневмонией, раком кожи и другими. Ученые изучили разные варианты взаимодействия вируса с организмом человека. Различный исход этого взаимодействия, по-видимому, зависел от набора генов у обследованных людей.
Выяснилось, что люди, устойчивые к СПИДу, имеют мутантные, измененные гены рецептора хемокинов - молекулы, к которой прикрепляется вирус, чтобы проникнуть в иммунную клетку. У них контакт иммунной клетки с вирусом невозможен, поскольку нет "принимающего устройства".
В это же время бельгийские ученые Михаэль Симпсон и Марк Парментье выделили ген другого рецептора. Им оказался белок, который также служит рецептором для связывания ВИЧ на поверхности иммунных клеток. Только взаимодействие этих двух молекул-рецепторов на поверхности иммунной клетки создает "посадочную площадку" для вируса.
Итак, основными "виновниками" заражения клеток вирусом иммунодефицита служат молекулы-рецепторы, названные CCR5 и CD4. Возник вопрос: что происходит с этими рецепторами при устойчивости к ВИЧ?
В июле 1996 года американская исследовательница Мэри Керингтон из Института рака сообщила, что нормальный ген рецептора ССR5 обнаруживается лишь у 1/5 обследованных ею пациентов. Дальнейший поиск вариантов этого гена среди двух тысяч больных дал удивительные результаты. Оказалось, что у 3% людей, не заразившихся вирусом, несмотря на контакты с больными, ген рецептора ССR5 измененный, мутантный. Например, при обследовании двух нью-йоркских гомосексуалистов - здоровых, несмотря на контакты с зараженными, выяснилось, что в их клетках образуется мутантный белок CCR5, не способный взаимодействовать с вирусными частицами. Подобные генетические варианты были найдены лишь у американцев европейского происхождения или у выходцев из западной Азии, у американцев же африканского и восточноазиатского происхождения не нашли "защитных" генов.
Оказалось также, что устойчивость некоторых пациентов к инфекции лишь временная, если они получили "спасительную" мутацию только от одного из своих родителей. Через несколько лет после заражения количество иммунных клеток в крови таких пациентов снижалось в 5 раз, и на этом фоне развивались сопутствующие СПИДу осложнения. Таким образом, неуязвимыми для ВИЧ были только носители сразу двух мутантных генов.
Но у обладателей одного мутантного гена признаки СПИДа все же развивались медленнее, чем у носителей двух нормальных генов, и такие больные лучше поддавались лечению.
Не так давно исследователи обнаружили разновидности чрезвычайно агрессивных вирусов. Людей, зараженных такими вирусами, не спасает даже присутствие двух мутантных генов, обеспечивающих устойчивость к ВИЧ.
Это заставляет продолжать поиск генов устойчивости к ВИЧ. Недавно американские исследователи О'Брайн и М. Дин с коллегами обнаружили ген, который, присутствуя у людей лишь в одной копии, задерживает развитие СПИДа на 2-3 года и более. Значит ли это, что появилось новое оружие в борьбе с вирусом, вызывающим СПИД? Скорее всего, ученые приоткрыли еще одну завесу над загадками ВИЧ, и это поможет медикам в поисках средств лечения "чумы ХХ века". В многочисленных популяциях американцев афро-азиатского происхождения мутантные гены так и не найдены, но тем не менее есть небольшие группы здоровых людей, контактировавших с зараженными. Это говорит о существовании других генов защиты иммунной системы от страшной инфекции. Пока можно лишь предполагать, что в различных популяциях человека сложились свои системы генетической защиты. По-видимому, и для других инфекционных заболеваний, включая вирусный гепатит, также имеются гены устойчивости к вирусам-возбудителям. Теперь уже никто из генетиков не сомневается в существовании таких генов для вируса иммунодефицита. Исследования последних лет дали надежду найти решение такой, казалось бы, неразрешимой проблемы, как борьба со СПИДом. Кто станет победителем в противоборстве ВИЧ - человек, покажет будущее.
КАК ЛЕЧИТЬ СПИД. ПОИСК СТРАТЕГИИ
Результаты исследований последних лет заставили задуматься не только ученых и практических врачей, занимающихся проблемами СПИДа, но и фармацевтов. Раньше основное внимание уделялось комбинированному лечению инфекции, направленному против вируса. Применялись препараты, препятствующие размножению вируса в клетке: невипарин и атевирдин. Это так называемая группа ингибиторов обратной транскриптазы ВИЧ, которые не дают наследственному материалу вируса внедряться в ДНК иммунных клеток. Их сочетают с аналогами нуклеозидов типа зидовудина, диданозина и ставудина, которые облегчают течение болезни. Однако эти средства токсичны и обладают побочными действиями на организм, поэтому их нельзя считать оптимальными. Им на смену все чаще приходят более совершенные средства воздействия на ВИЧ.
В последнее время появилась возможность препятствовать "посадке" вирусных частиц на поверхность клеток. Известно, что этот процесс происходит за счет связывания вирусного белка gр120 с клеточными рецепторами. Искусственное блокирование мест связывания ВИЧ с помощью хемокинов должно защищать клетки от вторжения ВИЧ. Для этого нужно разработать специальные препараты-блокаторы.
Другой путь - получение антител, которые будут связываться с рецепторами ССR5, создающими "посадочную площадку". Такие антитела будут препятствовать взаимодействию этих рецепторов с вирусом, не давая доступа ВИЧ в клетки. Кроме того, можно вводить в организм фрагменты молекул ССR5. В ответ на это иммунная система начнет вырабатывать антитела к данному белку, которые также перекроют доступ к нему вирусных частиц.
Наиболее дорогостоящий способ обезопасить вирусные частицы - ввести в иммунные клетки новые мутантные гены. В результате сборка рецептора для "посадки" вируса на поверхности "оперированных" клеток прекратится, и вирусные частицы не смогут заразить такие клетки. Подобная защищающая терапия, по-видимому, наиболее перспективна при лечении больных СПИДом, хотя и весьма дорого стоит.
При лечении сопровождающих СПИД раковых заболеваний врачи чаще всего прибегают к высоким дозам химических препаратов и к облучению опухолей, что нарушает кроветворение и требует пересадки больным здорового костного мозга. А что, если в качестве донорских кроветворных клеток пересадить больному костный мозг, взятый от людей, генетически устойчивых к инфекции ВИЧ? Можно предположить, что после такой пересадки распространение вируса в организме пациента будет остановлено: ведь донорские клетки устойчивы к инфекции, поскольку не имеют рецепторов, позволяющих вирусу проникнуть через клеточную мембрану. Однако эту привлекательную идею вряд ли удастся воплотить в практику полностью. Дело в том, что иммунологические различия между пациентом и донором, как правило, приводят к отторжению пересаженной ткани, а иногда и к более серьезным последствиям, когда донорские клетки атакуют чужеродные для них клетки реципиента, вызывая их массовую гибель.
Т-киллеры - иммунные клетки, которые уничтожают зараженные вирусом клетки.
Рецепторы клеток - особые молекулы на поверхности, которые служат "опознавательным знаком" для вирусных частиц и других клеток.
Ген рецептора - ген, ответственный за выработку соответствующего белка.
Хемокины - гормоноподобные вещества на поверхности иммунных клеток, которые подавляют размножение вируса в организме.
Культура клеток - клетки, развивающиеся вне организма, в питательной среде пробирки.
Мутантные гены - измененные гены, не способные контролировать выработку нужного белка.
Клетки-мишени - иммунные клетки, которые в первую очередь поражает вирус.
- Сегодня в мире 29 миллионов зараженных вирусом иммунодефицита. 1,5 миллиона человек уже умерли от вызванного этим заражением СПИДа.
- Самый неблагополучный по СПИДу регион - Африка. В Европе лидируют Испания, Италия, Франция, Германия. С 1997 года к этим странам присоединилась Россия. На территории бывшего СССР зараженность ВИЧ распределяется так: 70% - Украина, 18,2% - Россия, 5,4% - Беларусь, 1,9% - Молдова, 1,3% - Казахстан, остальные - менее 0,5%.
- К 1 декабря 1997 года в России официально зарегистрировано около 7000 зараженных вирусом иммунодефицита, в основном при передаче инфекции половым путем.
- В России и странах ближнего зарубежья существует более 80 центров по профилактике и борьбе со СПИДом.
Американская компания потребительской геномики 23andMe хочет проанализировать свою базу данных из миллионов клиентов, чтобы понять, почему одни люди страдают от коронавируса больше, чем другие. Возможно, что это связано с ДНК. Об этом пишет американский журнал Wired.
Коронавирус SARS-COV-2, впервые всплывший на поверхность в прошлом году в Китае, — это агрессор равных возможностей. Похоже, что вирус одинаково заражает людей вне зависимости от их возраста, расы и пола. Это логично, так как это совершенно новый болезнетворный микроорганизм, от которого ни у кого нет иммунитета, пишет автор статьи Меган Молтени.
Но вызываемая вирусом болезнь Covid-19 более непредсказуема в своих проявлениях, отмечает она. Очень немногие инфицированные люди реально заболевают. У заболевших очень разные симптомы. У кого-то высокая температура и кашель. У кого-то желудочные колики и диарея. Кто-то теряет аппетит. Кто-то перестает различать запахи. Кто-то способен преодолеть недуг, сидя дома, потребляя много жидкости и радуя себя сериалами. А кто-то попадает в реанимацию, где к нему подключают множество трубок, которые безуспешно качают воздух в его больные легкие. Пожилые люди с хроническими заболеваниями и мужчины составляют большинство летальных исходов. Но не всегда. В США большой процент госпитализированных с серьезными симптомами — это люди моложе 40 лет. Дети, особенно грудного возраста, тоже не защищены на сто процентов.
Чтобы понять, чем вызваны такие различия, ученые изучают обрывочные эпидемиологические данные, поступающие из очагов заражения, таких как Китай, Италия и США. Они ищут особенности и закономерности в возрасте пациентов, их расе, поле, социально-экономическом положении, поведении и в доступности для них медицинских услуг. А сейчас они стали копать глубже, стараясь отыскать отгадки в нашей ДНК.
6 апреля компания 23andMe начала новое исследование, имеющее целью выявить генетические различия, которыми можно объяснить, почему у заболевших Covid-19 людей такая разная реакция на инфекцию. Эта фирма потребительской геномики присоединилась к целой серии новых научных проектов, ищущих ответ на один и тот же вопрос. Проведенные ранее исследования показывают, что некоторые варианты генов при заболевании определенными инфекционными болезнями подвергают людей повышенной опасности. Другие же обеспечивают им защиту, скажем мутация гена CCR5, делающая носителя невосприимчивым к ВИЧ.
Если другие компании по изучению ДНК переоборудовали свои лаборатории и теперь проверяют людей на Covid, то 23andMe решила воспользоваться своим уникальным достоянием — базой данных на 10 с лишним миллионов клиентов, 80% которых дали согласие на использование в научно-исследовательских целях своей генетической информации и прочих данных, которые они сообщили сами. Компания несколько лет формировала эту базу данных, которая облегчает проведение массовых опросов среди потенциальных участников исследования. В результате каждый генетический профиль включает сотни фенотипических единиц информации, скажем, сколько сигарет клиент выкурил за свою жизнь и был ли диабет у кого-нибудь из его родственников. Огромный объем данных, которыми располагает компания, позволил ей начать поиски лекарства и сделал ее мощным источником информации из области генетических исследований.
Последний опрос, опубликованный на клиентском портале 23andMe, включает вопросы о том, где живет человек, какие меры социального дистанцирования он соблюдает, проверялся ли он на коронавирус, контактировал ли с инфицированными и ставили ли ему диагноз Covid-19 (в опросе могут участвовать только американские клиенты компании). 23andMe надеется привлечь к исследованию сотни тысяч своих клиентов, включая тех, кому поставлен диагноз Covid-19, у кого тест дал отрицательный результат, у кого есть похожие на грипп симптомы, но кто проверку пока не проходил, а также членов семей инфицированных.
Если компания соберет достаточно ответов у людей, заразившихся Covid-19, ее исследовательская команда проведет статистический анализ под названием полногеномный поиск ассоциаций (GWAS). Этот метод широко используется в генетических исследованиях. При проведении GWAS людей делят на разные группы, в нашем случае, скорее всего, на основании симптомов. После этого проводится сканирование данных их ДНК с тем, чтобы выяснить, проявляются ли определенные однобуквенные вариации в генетическом коде чаще среди людей с определенными симптомами. Если такое происходит достаточно часто, можно с определенной долей уверенности говорить о том, что такие вариации связаны с этими симптомами.
Ученым предстоит выяснить, почему чрезмерная защитная реакция, известная как гиперцитокинемия, вызвала немало смертей среди больных атипичной пневмонией. Есть подозрения, что гиперцитокинемия является также причиной некоторых летальных исходов среди молодых людей, заболевших Covid-19.
Ген на поверхности легких
Еще одним потенциальным кандидатом является ген, предназначенный для рецептора ACE2. Он находится на поверхности легких и других клеток человека и является тем молекулярным проходом, через который в организм проникает SARS-CoV-2. Небольшие изменения в этом гене могут привести к тому, что проникнуть через определенные рецепторы станет легче или труднее. Кроме того, свою роль могут сыграть и вариации на том участке генома, который включает или выключает рецептор ACE2. Если гены менее активны, клетки человека производят меньше рецепторов и вирусу труднее за них ухватиться.
Пока рано строить догадки о той роли, которую гены играют в определении исхода болезни Covid-19, говорит Снайдер. Но он готов поставить на то, что проекты типа тех, которые реализует 23andMe, вряд ли дадут единый генетический вариант, который решает, окажется человек в реанимации или нет.
Все дело в том, что полногеномный поиск ассоциаций — это игра в числа. С его помощью лучше всего выявляются мутации, вновь и вновь возникающие во всей популяции, причем каждая из них оказывает лишь очень небольшое воздействие на подверженность человека болезни. А поскольку полногеномный поиск ассоциаций обычно проводится на основе ограниченного набора генетических данных — типа того, что собрала 23andMе (статическое представление о 600 тыс. локациях генома), — эти общие варианты выявить проще, чем редкие.
Мутации
Однако именно очень редкие мутации, скорее всего, являются причиной крайней подверженности Covid-19, указал пульмонолог Стивен Чапман, работающий исследователем в Центре человеческой генетики Оксфордского университета и не участвующий в проекте 23andMe. В середине 2000-х годов он проводил первые генетические исследования предрасположенности к бактериальной пневмонии и обнаружил редкие мутации в отвечающих за иммунитет генах, которые делали здоровых в остальном детей и взрослых крайне восприимчивыми к проникновению в организм одной особой бактерии. Чапман подозревает, что столь же редкие мутации, участвующие в иммунной функции и в реакции на воспалительные процессы, укладывают в кровати реанимационных отделений молодых и здоровых людей, у которых нет других факторов риска.
Чтобы найти их, потребуется взять анализы крови у нестандартных пациентов и секвенировать их геномы целиком. Если расшифровать ДНК молодого взрослого человека, подключенного к искусственной вентиляции легких, не исключено, что удастся раскрыть уникальную генетическую предрасположенность к Covid-19. С другой стороны, ДНК пожилых людей, у которых обнаружен коронавирус и Covid-19, но нет симптомов, может содержать защитные мутации, предохраняющие от самых тяжелых форм болезни.
В научных лабораториях по всему миру реализуется уже свыше 90 таких проектов секвенирования, и ученые спешно пытаются понять болезнь, от которой в мире умерло уже более 76 000 человек. Некоторые проекты — это начатые уже давно генетические исследования на населении, в которых длительное время участвуют тысячи добровольцев. Исландская компания DeCODE Genetics, которая на протяжении десятилетий занимается сбором данных о геномах и состоянии здоровья 364 000 жителей этой островной страны, получила от правительства разрешение на публикацию результатов анализов на Covid-19.
Но вряд ли стоит ждать, что мы уже в ближайшее время получим генетический оценочный лист предрасположенности к Covid-19. Чапман говорит, что, скорее всего, в результате этих исследований мы не получим возможность выявлять восприимчивых к этой болезни людей на основе их ДНК. Скорее мы просто станем лучше понимать молекулярные пути, через которые появляются самые тяжелые формы Covid-19.
Возраст, прежние проблемы со здоровьем, раннее тестирование и качественный уход — все эти моменты будут иметь главное значение при определении того, кто выживет, а кто умрет от Covid-19. Но и ДНК тоже наверняка играет определенную роль, влияя на исход болезни. И здесь нам еще очень многое предстоит узнать и выяснить.
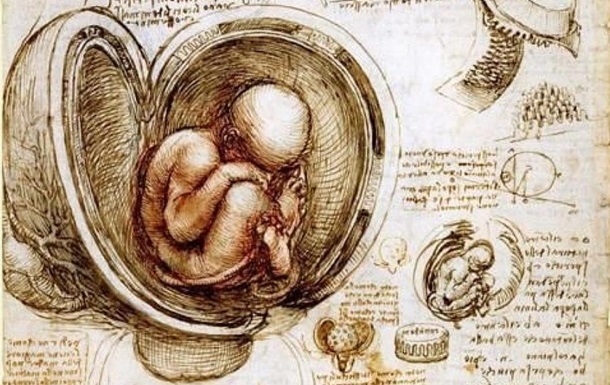
Исследователь из КНР при помощи метода CRISPR удалил у эмбрионов ген CCR5, который "открывает ВИЧ двери в клетки организма". Многие ученые его осудили.
Kитайский ученый Цзянькуй Хэ в начале недели заявил о рождении первых в мире детей с отредактированным геномом. 28 ноября на конференции в Гонконге Хэ рассказал о еще одной беременности в рамках этого проекта.
Власти начали расследование о законности действий ученого. А более ста китайских ученых написали открытое письмо, в котором обвинили Хэ в открытии ящика Пандоры.
Исследователь Хэ Цзянькуй из Шэньчжэня заявил, что изменил гены эмбрионов при помощи метода CRISPR, в результате чего родились первые в мире дети с модифицированным геномом. Ими стали девочки-близнецы Лулу и Нана.
В эксперименте приняли участие семь пар из программы лечения бесплодия. Все мужчины были ВИЧ-инфицированы, а женщины - здоровы. Всего ученому удалось отредактировать 16 из 22 эмбрионов, 11 из которых использовались в шести попытках - одна из которых уже закончилась беременностью и родами.
Его целью было не лечение или предотвращение наследственных заболеваний, а наделение организма способностью к невосприимчивости ВИЧ.
Хэ Цзянькуй утверждает, что удалил у девочек ген CCR5, который "открывает ВИЧ двери в клетки организма", чем обеспечил им иммунитет к вирусу. В видеообращении ученый назвал рождение двух здоровых детей с измененными генами "историческим прорывом Китая в профилактике заболеваний".
"Теперь они будут здоровы, а у отца появился смысл жить и работать, у него есть цель", - сказал ученый.
Пока результаты его работы не публиковалась в научных журналах и не проверялась другими генетиками. О своей работе ученый рассказал одному из организаторов международной конференции по редактированию генов в Гонконге, а позже дал агентству AP интервью.
"Суть модификации заключается в том, чтобы придать организму невосприимчивость к вирусу ВИЧ. Подобная мутация естественно встречается среди людей, но очень редка", - объяснил Хэ.
Редактирование происходило во время экстракорпорального оплодотворения. Он отметил, что хочет проложить путь таким исследованиям в дальнейшем.
"Общество решит, что будет делать дальше", - подчеркнул ученый.
28 ноября на конференции в Гонконге заявил, что в рамках этого проекта есть еще одна беременность.
Метод направленного редактирования генома, называемый CRISPR-Cas9, был обнаружен учеными совсем недавно. Активные лабораторные эксперименты, направленные на изучение возможностей метода, проводятся с 2012 года.
Это относительно простой способ, который на генетическом уровне может помочь в лечении смертельных заболеваний. Пока в США и Европе запрещено применение метода на человеческом организме и разрешено только в рамках лабораторных исследований.
Китай - одна из наиболее продвинутых в плане работы с человеческими генами стран. В законах КНР, в отличие от многих других стран, нет прямого запрета на работу с генами эмбрионов. С 2015 года ученые страны, по информации газеты Wall Street Journal, отредактировали гены 86 человек, больных ВИЧ и раковыми заболеваниями.
Тем не менее случаев рождения детей с измененными генами до случая с Хэ Цзянькуем зарегистрировано не было.
Цзянькуй учился в Америке, прежде чем открыть лабораторию и начать исследования на родине, в Южном научно-технологическом университете в Шэньчжэне. Также у него есть две собственные "генетические компании".
Китайский исследователь объяснил, что в течение нескольких лет проводил исследования на мышах и обезьянах, а затем на человеческих эмбрионах, и даже собирался запатентовать свой метод. Выбор редактирования генома для борьбы с ВИЧ он обосновал тем, что этот вирус представляет серьезную проблему для Китая.
Он также отметил, что его университет не знал о проекте, который Хэ финансировал из собственных средств.
На ученого обрушились с критикой
Президент университета Чэнь Шии созвал экстренное совещание, на котором собрал всех ученых, имевших хотя бы косвенное отношение к проекту, и объявил им, что ЮУНТ не имеет к этому никакого отношения.
Руководство университета объявило, что Хэ Цзянькуй серьезно нарушил стандарты академической этики и что университет собирается провести расследование.
Экспертный совет по медицинской этике города Шэньчжэня также сообщил, что начинает расследование в отношении Хэ Цзянькуя.
Национальная комиссия по здравоохранению Китая намерена тщательным образом проверить законность действий ученого.
Многие исследователи были поражены экспериментом Хэ. 122 китайских ученых написали открытое письмо, в котором осудили своего коллегу и призвали правительство резко ограничить работу с генами человека.
"Ящик Пандоры открыт, но мы можем еще закрыть его, пока не слишком поздно. Это просто нечестно по отношению к тем китайским исследователям, которые защищают трудолюбие и инновации, основанные на научной этике", - говорится в письме.
"Это бессовестный эксперимент над людьми, который нельзя оправдать ни с этической, ни с моральной точки зрения", - отметил доктор Киран Мусунуру, генетик из Университета Пенсильвании.
Против подобных экспериментов выступил и один из создателей технологии генетического инжиниринга CRISPR Фэн Чжан. Он заявил, что "при нынешнем состоянии технологий" считает разумным введение "моратория на подсадку модифицированных эмбрионов".
Он также указал на то, что, уменьшив риск заболевания ВИЧ, две новорожденные девочки получили повышенный риск заболевания лихорадкой Западного Нила.
Однако знаменитый генетик Джордж Черч из Гарвардского университета поддержал китайского ученого, назвав редактирование генов для противостояния ВИЧ оправданной попыткой, поскольку это заболевание несет "серьезную угрозу для здравоохранения".
Источник кореспондент нет
Если кто еще знает что - пишите в комменты плиз
![]()
два дня достаточно, это же пикабу
Тут, по видимому, принцип я не видел - значит не боян. А вообще что это за отсебятина про иммунитет к СПИДУ? ТС хоть знает что такое СПИД и почему бессмысленно писать об иммунитете к нему?
Эволюция живых организмов, происходящая прямо на глазах

У эволюции много доказательств:
морфологические, эмбриологические палеонтологические, биохимические, биогеографические, и генетические. Самые наглядные - это филогенетические ряды, на которых можно поэтапно пронаблюдать изменения в строении животных. Правильно расставить порядок скелетов позволяет радиоизотопный и другие виды анализов возраста окаменелостей.

Здесь, например, вы можете посмотреть, как исчезли пальцы, возникли копыта и изменилась форма черепа лошади. Но креационистам мало подобных филогенетических рядов. Они говорят, что пока эволюцию вживую никто не видел, она не может называться фактом. И мутации не бывают полезными. Чтобы это опровергнуть, вспомним историю австралийских кроликов

В Австралию завезли кроликов, и они быстро расплодились, нанося вред сельскому хозяйству. Тогда учёные использовали вирус миксоматоза. Вирус очень быстро выкашивал кроликов, добрался даже до домашних. Часть кроликов, пережившая эпидемию, сново расплодилась. Но у них было отличие от предыдущих поколений. Это мутация в гене, кодирующем интерферон IFN-α21A. Это влияет на иммунную систему и ее борьбу с вирусом. То есть несмотря на то, что мутации чаще редки и приводят к болезням, порой они приводят и к положительным изменениям. Это эволюция.

Ещё более интересна ситуация, произошедшая с итальянской стенной ящерицей. Тут речь идёт о более радикальных изменениях. Экспериментаторы перевезли их с острова Копиште в Адриатике на соседний остров Мрчару. Там было много травы и не было хищников. Через 36 лет у ящериц изменилось страница тела. Поскольку травы было много, насекомоядные рептилии стали травоядными, их челюсти стали более массивными и сильными для переживывания травы. В их пищеварительной системе появилось место для бактерий, которые помогают переварить траву. Поскольку им больше не надо было быть юркими, чтобы убегать от хищников, они стали большими и неповоротливыми.

Но креационистам этого не достаточно. Их ведь и селекция как доказательство не устраивает. Они хотят увидеть более серьезные изменения в строении организмов. Но полезным мутациям нужно накопиться, чтобы изменения было серьезны, поэтому такая эволюция длится миллионы лет. Неужели мы не можем посмотреть на эволюцию? Можем. Благодаря вирусам и бактериям, у которых смена поколений происходит гораздо быстрее. Учёные в лабораториях наблюдают, что кардинальные изменения в строении вирусов и бактерий происходят не мгновенно, по воле божьей, а засчет процесса накопления полезных мутаций. То есть строение вируса или бактерии продиктовано эволюцией.
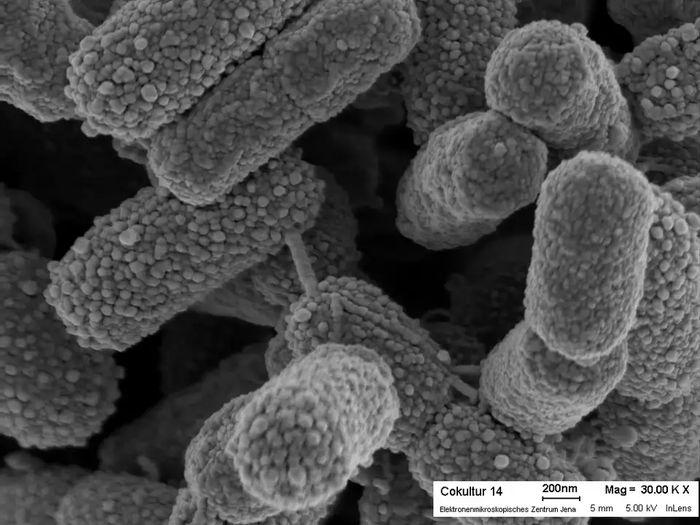
Когда смотришь на то, как совершенно устроены животные, кажется, что такое разумное строение мог обеспечить только разумный создатель. А у вирусов и бактерий, напомню, доказано, что строение обусловлено эволюцией. И они устроены не менее "разумно", чем животные. Порой они даже похожи на роботов.
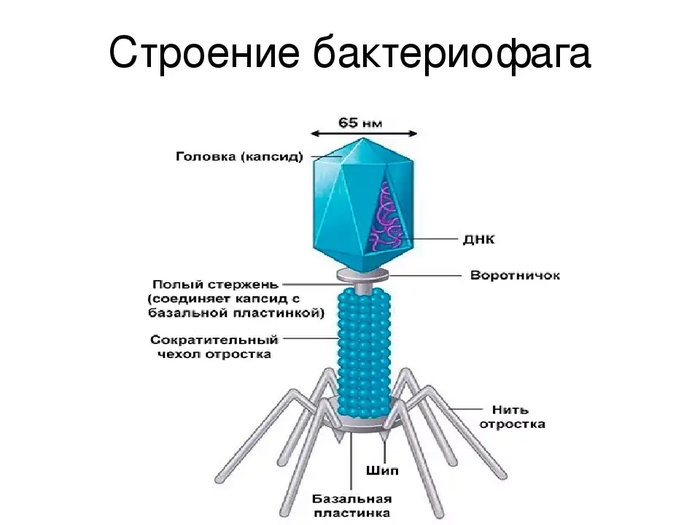
Рассмотрим, к примеру, вирус бешенства. Он поражает мозг заражённого животного именно таким образом, чтобы вызвать у него агрессию. Тогда жертва кусает других и переносит вирус. Разумно? Разумно.

Или вирус СПИДА. Он поражает именно своих главных врагов в теле человека - клетки иммунной системы. В результате организм не способен ему противостоять и выздороветь. Разве не гениально он устроен?
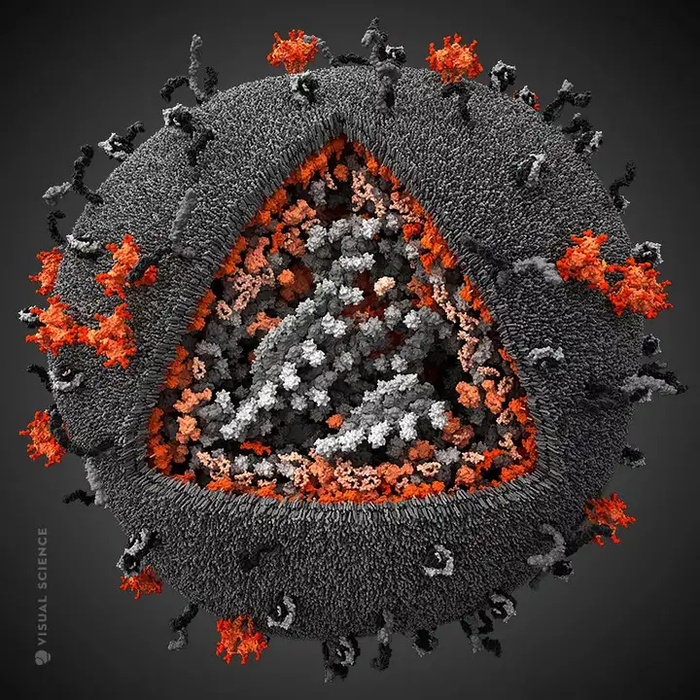
Или чума.. Бубонная чума размножается в глотке блохи и перекрывает ее. Блоха не может пить. В результате насекомое в порыве жажды мечется от жертвы к жертве, отчаянно пытаясь напиться,и заражает чумой больше жертв. Тоже разумно. Но это бактерия, а доказано, что они формируются в процессе эволюции.
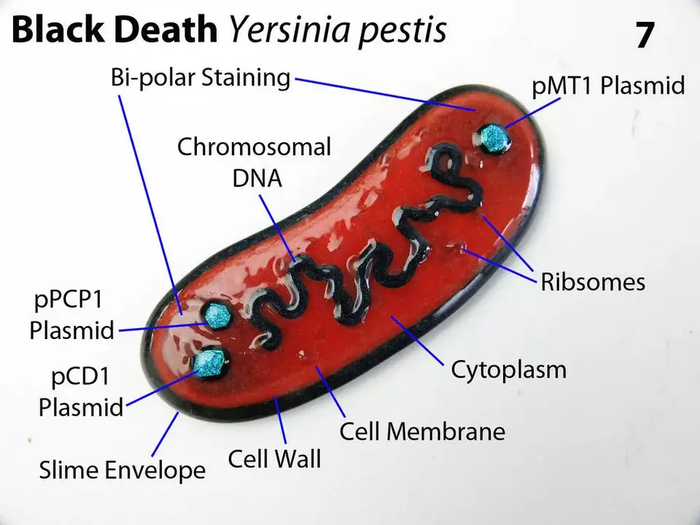
А напомню, что с животными происходят те же процессы, что и при эволюции бактерий, только медленные. Мы не можем увидеть в лаборатории эволюцию животных, но благодаря микроорганизмам мы всё же можем пронаблюдать ее вживую.

![]()
В Златоусте для медика, которой в глаза попала кровь ВИЧ-инфицированного, второй день ищут противовирусный препарат
По ее словам, накануне вечером фельдшер в темном подъезде оказывала помощь ВИЧ-инфицированному мужчине, у которого уже развился СПИД. Кровь пациента брызнула в глаза медику.
По словам депутата, главврач станции скорой помощи Златоуста заявила, что давала поручение закупить противовирусные средство еще прошлом году, но почему-то этого сделано не было.
В результате необходимое лекарство нашлось только в областном ВИЧ-центре в Челябинске. Сегодня его передадут в Златоуст.
В Минздраве региона оперативно прокомментировать ситуацию не смогли
![]()
Второй пациент вылечен от ВИЧ: новый рубеж в борьбе с глобальной эпидемией СПИДа
Учёные долго пытались повторить последовательность действий, которые привели к первой долгосрочной ремиссии 12 лет назад. С так называемым “Лондонским пациентом” у них, кажется, получилось.

Уже во второй раз с начала глобальной эпидемии пациент излечен от ВИЧ-инфекции – вируса, который вызывает СПИД.
Новость появилась почти через 12 лет после того, как стало известно об излечении первого пациента – о подвиге, который учёные долго и безуспешно пытались повторить.
Исследователи опубликовали свой доклад в журнале “Nature” и представили некоторые детали на конференции по ретровирусам и оппортунистическим инфекциям в Сиэтле. В данной публикации учёные описывают этот случай как долгосрочную ремиссию. В интервью же большинство экспертов называли это излечением, но с оговоркой, что очень сложно определить, какое слово стоит использовать, так как пока известно только два таких случая.
Оба выдающихся результата достигнуты благодаря пересадке заражённым пациентам костного мозга. Но в обоих случаях трансплантация предназначалась для лечения рака, а не ВИЧ.
Трансплантация костного мозга вряд ли станет предпочтительным вариантом лечения в ближайшем будущем. Сейчас для контроля ВИЧ-инфекции используются сильнодействующие препараты, пересадка же остается рискованным вмешательством из-за серьёзных побочных эффектов, которые могут длиться годами.
Однако, как говорят учёные, замена собственных иммунных клеток организма на специально модифицированные к сопротивлению ВИЧ-инфекции может успешно применяться на практике.
Доктор Венсинг соруководитель “IciStem” – консорциума европейских учёных, изучающих пересадку стволовых клеток в качестве лекарства от ВИЧ-инфекции. Консорциум поддерживается “amfAR” – американской организацией по изучению СПИДа.
Новый пациент предпочел сохранить анонимность, и учёные называют его исключительно “Лондонским пациентом”.
На той же конференции в 2007 году доктор из Германии описал первый случай излечения “Берлинского пациента”, позже идентифицированного как Тимоти Рэй Браун 52-х лет, сейчас проживающего в Палм Спрингс, Калифорния.
Эта новость, размещенная на плакате в задней части конференц-зала изначально не привлекла много внимания. Как только стало ясно, что мистер Браун вылечен, учёные начали попытки повторить этот результат с другими раковыми пациентами, зараженными ВИЧ.
Раз за разом вирус возвращался примерно через девять месяцев после того, как пациенты прекращали антиретровирусную терапию, или же пациент умирал от рака. Неудачи заставляли учёных гадать, останется ли излечение мистера Брауна счастливой случайностью.
У мистера Брауна была лейкемия, и после неудачной химиотерапии ему потребовалась пересадка костного мозга.
Трансплантация была от донора с мутацией белка CCR5, который находится на поверхности определенных иммунных клеток. ВИЧ использует этот белок, чтобы проникнуть внутрь клеток, но не может попасть в их мутированную версию.
Мистеру Брауну давали сильнейшие имуносупрессивные лекарства, которые больше не используются, он страдал от сильнейших побочных эффектов месяцами после трансплантации костного мозга. Его даже погрузили в искусственную кому, и он едва не умер.
У него была лимфома ходжкина, и он перенес трансплантацию костного мозга от донора с мутацией белка CCR5 в мае 2016 года. Ему также была назначена имуносупрессивная терапия, но лечение было менее интенсивным, согласно нынешним стандартам трансплантации.
Он перестал принимать лекарства от ВИЧ в сентябре 2017 года, что сделало его первым пациентом после Брауна, у которого не обнаружен вирус спустя более чем год после прекращения терапии.
Хотя “Лондонский пациент” после трансплантации не был болен так же сильно, как мистер Браун, вмешательство все равно сработало: трансплантация уничтожила рак без разрушительных побочных эффектов. Пересаженные иммунные клетки, устойчивые к ВИЧ, похоже, полностью заменили его собственные уязвимые клетки.
Большинство людей с мутацией устойчивости к ВИЧ, названной “Дельта 32”, североевропейского происхождения. В базе данных “IciStem” насчитывается около 22 тысяч таких доноров.
Пока учёные отслеживают 38 ВИЧ-инфицированных, перенесших пересадку костного мозга, включая шестерых с пересадкой от доноров без мутации. Лондонский пациент 36-й в этом списке. Другой, 19-й номер из списка, называемый также “Дюссельдорфским пациентом”, не принимает анти-ВИЧ терапию уже четыре месяца. Детали этого случая будут представлены на Сиэтльской конференции позже.
Консорциум учёных повторно проанализировал кровь “Лондонского пациента” на наличие вируса. Они увидели слабые признаки инфекции в одном из 24-х тестов, но говорят, что это может быть результатом загрязнения образца.
Большинство экспертов, которые знают подробности, согласны, что этот новый случай выглядит, как легитимное лечение, однако некоторые не уверены в его актуальности для терапии против СПИД в целом.
Несколько компаний стремятся разработать такие генные терапии, но еще не достигли успеха. Изменения должны быть нацелены на нужное количество клеток и в нужном месте – например, только в костном мозге, а не в головном мозге – и менять только гены, связанные с производством CCR5.
По словам доктора МакКьюна, сейчас над преодолением этих трудностей работает сразу несколько групп учёных.
В конце концов, у них может получиться вирусная система доставки, которая, после введения в организм, будет находить и удалять все рецепторы CCR5. А может быть, даже создадут стволовые клетки, устойчивые к ВИЧ, которые можно перенести любому пациенту.
Одним из важных предостережений для любого подхода является то, что пациент всё равно будет уязвим к форме ВИЧ X4, который использует другой белок, CXCR4, чтобы попасть в клетки.
Если у человека есть даже небольшое количество вируса X4, то его количество многократно увеличится в отсутствие конкуренции с его вирусными собратьями.
Существует как минимум один описанный случай пациента, которому пересадили “Дельта 32” от донора, но позже у него был найден вирус Х4. (В качестве предосторожности от вируса Х4 мистер Браун ежедневно принимает таблетки для предотвращения ВИЧ).
Читайте также:


