Что такое нозокомиального сальмонеллеза






ЭПИДЕМИОЛОГИЯ, КЛИНИКА, ДИАГНОСТИКА, ЛЕЧЕНИЕ И ПРОФИЛАКТИКА НОЗОКОМИАЛЬНОГО САЛЬМОНЕЛЛЕЗА
Профилактика и лечение внутрибольничных инфекций (ВБИ) важный раздел деятельности многопрофильных лечебных учреждений (ЛПУ). Среди большой группы ВБИ отдельной проблемой на современном этапе развития здравоохранения является нозокомиальный (внутрибольничный) сальмонеллез. Поражая наиболее ослабленные контингенты находящихся на лечении больных и персонал стационаров сальмонеллез значительно осложняет клиническое течение основного заболевания пациентов и является одним из значимых факторов внутригоспитальной летальности.
Настоящие методические рекомендации разработаны с использованием современных литературных данных, на основе большого личного клинико-эпидемиологического материала, новых приоритетных научно-практических разработок и методов лабораторно-инструментальных исследований. Данные методические рекомендации предназначены для широкого круга врачей: руководителей ЛПУ, госпитальных эпидемиологов, инфекционистов, микробиологов, хирургов, реаниматологов, гастроэнтерологов, и др.
В подготовке издания принимали участие:
- главный эпидемиолог ГВКГ им.Н.Н.Бурденко кандидат медицинских наук майор медицинской службы АКИМКИН В.Г. (научный руководитель),
- начальник инфекционного отделения ГВКГ им.Н.Н.Бурденко полковник медицинской службы КУБЕНСКИЙ Е.Н.,
- старший ординатор инфекционного отделения ГВКГ им.Н.Н.Бурденко кандидат медицинских наук подполковник медицинской службы ПОНОМАРЕВ
Данные методические рекомендации не могут быть тиражированы, копированы или опубликованы другим способом, как целиком, так и частями, без письменного разрешения автора и Главного военно-медицинского управления МО РФ. При использовании ссылка на источник информации обязательна.
ЭПИДЕМИОЛОГИЯ НОЗОКОМИАЛЬНОГО САЛЬМОНЕЛЛЕЗА
Термином "сальмонеллезы" обозначают большую группу инфекционных заболеваний, возбудителями которых являются многочисленные представители (серовары) рода Salmonella. Они характеризуются значительным полиморфизмом клинического течения с преимущественным поражением желудочно-кишечного тракта и различной степенью выраженности симптомов общей интоксикации и могут встречаться в виде как единичных случаев, так и групповых заболеваний. Основным источником инфекции являются различные животные, ведущий путь заражения - алиментарный, а возбудитель чаще передается через пищевые продукты.
За последние десятилетия накопилась обширная литература, касающаяся вопроса о нозокомиальных инфекциях и свидетельствующая о все возрастающем числе случаев внутрибольничного распространения заболеваний, вызываемых различными микроорганизмами. Все это в значительной мере относится и к сальмонеллезам как госпитальной инфекции.
Нозокомиальный (внутригоспитальный) сальмонеллез - кишечная инфекция, относящаяся к разряду внутрибольничных и характеризующаяся рядом важных принципиальных особенностей в клинике и эпидемиологии от классического варианта этого инфекционного заболевания.
Возбудитель инфекции (чаще всего - Salm.typhimurium) характеризуется относительной стабильностью его культуральных, серологических, биохимических и молекулярно-генетических свойств, а также значительной полиантибиотикорезистентностью. Большинству полирезистентных штаммов
S.typhimurium, выделяющихся на различных территориях страны у больных и из объектов окружающей среды в очагах внутрибольничной инфекции, свойственен сходный спектр резистентности (антибиотикограмма). Выделяемые штаммы сальмонелл, как правило, не чувствительны к известным антибиотикам широкого спектра действия, за исключением препаратов фторхинолонового ряда. Все они несут конъюгативную R-плазмиду, принадлежащую к группе несовместимости, F1mе, подобную той, которая широко распространена у S.typhimurium, выделяемых в странах Среднего Востока (Е.Аnderson et al.,1977). Молекулярно-генетические исследования показывают, что эпидемии нозокомиального сальмонеллеза в лечебных учреждениях чаще всего вызываются штаммами Salm.typhimurium с набором плазмид
128.7 kb, 17.4 kb и 2.4 kb. Штаммы сальмонелл с идентичным плазмидным профилем выделяются от медицинского персонала, с объектов внешней сре- ды палат, кишечника грызунов (крыс), отловленных в стационаре. Отмечаются случаи выявления сальмонелл у вновь поступивших больных с нетипичным плазмидным профилем, что позволяет предполагать факты заноса инфекции в стационар. Наличие плазмиды вирулентности размером 128.7 kb
- свидетельствует об антропонозном происхождении возбудителя сальмонеллеза, и что также характерно для плазмид такого размера в геном входит фактор антибиотикорезистентности (В.Г.Акимкин,1997).
В очагах инфекций, связанных одним источником и путями распространения возбудителя, выделяются S.typhimurium, принадлежащие к одному биохимическому варианту. Основная часть госпитальных штаммов S.typhimurium, имеет пониженное содержание фермента лизин-декарбоксилазы (С.Ш.Рожнова, 1977), разлагают инозит в первые сутки (Л.А.Кафтырева,
1984). Указанные культуры были обозначены II типом (в отличие от I-типичного классического варианта), а в последующем - IIR.
Сальмонеллы — возбудители внутрибольничных инфекций
Общая характеристика. Возбудителем внутрибольничного сальмонеллеза чаще всего является S. typhimurium. Однако нередки заболевания, вызываемые другими сероварами S. derby, S. heidel-berg, S. wien, S. haifa и др., которые относятся к группе В. Эти сальмонеллы по своим морфологическим, физиологическим, биохимическим и антигенным признакам не отличаются от бактерий — возбудителей пищевых токсикоинфекций. Идентифицированы биовары некоторых из перечисленных выше сальмонелл, которые, как правило, выделяются только при внутрибольничной инфекции. Так, среди S. typhimurium идентифицировано три биовара, одинаковых по своей антигенной структуре, но отличающихся друг от друга по патогенности для белых мышей при энтеральном заражении и по чувствительности к антибиотикам. Как правило, сальмонеллы, выделяемые при внутрибольничной инфекции, резистентны к 15-20 антибиотикам. Это связано с наличием у них конъюгативных R-плазмид, несущих множественную устойчивость к антибиотикам.
Патогенность и патогенез. Распространение внутрибольничных сальмонеллезов происходит тремя путями: контактно-бытовым, воздушно-пылевым и пищевым. Наиболее распространен контактно-бытовой путь передачи инфекции. Проявления болезни разнообразны и варьируют от бессимптомного бактерионосительства и легчайших субклинических форм до выраженных интестинальных расстройств с тяжелой интоксикацией, бактериемией, иногда с генерализацией процесса и развитием осложнений. Внутрибольничные сальмонеллезы у детей раннего возраста протекают более тяжело и длительно. Они сопровождаются значительной интоксикацией и более глубокими поражениями желудочно-кишечного тракта, а также бактериемией и развитием токсико-септических и даже септико-дистрофических состояний. У детей старше 3 лет часто отмечаются легко протекающие кишечные формы и бессимптомное бактерионосительство. Сальмонеллезная интоксикация нарушает функции гипоталамуса и обменные процессы. При этом дети грудного возраста теряют большое количество солей и воды, что приводит к возникновению токсикоза и обезвоживанию организма. У детей старше 1 года может наступить синдром нейротокси-коза. Особенно опасно для детей раннего возраста присоединение сальмонеллезов к стафилококковой инфекции, респираторной вирусной инфекции, пневмонии, эшерихиозу. Часто у таких больных развивается сепсис смешанной этиологии или менингит.
Лабораторная диагностика. Основное значение имеет выделение чистой культуры и определение ее серовара при инфекции S. typhimurium.
Профилактика. С целью специфической профилактики используют поливалентный сальмонеллезный фаг. Его вводят детям в стационарах, контактировавшим с больными сальмонеллезами и носителями. Получают фаг также матери, находящиеся в тесном контакте с больными детьми.
Что такое нозокомиального сальмонеллеза

— выделении от больных только условно-патогенной флоры в единичных случаях, без достоверно выявленного фактора передачи возбудителя;
— проведении детекции вирусных агентов в материалах из окружающей среды, продуктов питания или лиц — предполагаемых источников инфицирования;
По предложению Всемирной Гастроэнтерологической Организации (2008) микробиологическое исследование при инфекционных диареях показано:
− больным с тяжелыми и генерализованными (септическими) формами болезни (обезвоживанием, лихорадкой или с наличием крови в кале),
− при вспышках инфекции,
− при персистирующих диареях.
4.7.1 Методы диагностики
Для подтверждения сальмонеллеза используются бактериологические, молекулярногенетические, серологические методы. Материал для исследования при гастроинтестинальном сальмонеллезе: фекалии, рвотные массы, промывные воды желудка, моча (начиная со второй недели болезни); при генерализованных формах — кровь, ликвор, желчь, синовиальная жидкость.
Наиболее эффективными способами экспресс-диагностики сальмонеллеза являются методы, направленные на выявление нуклеиновых кислот или антигенов возбудителя — полимеразная цепная реакция (ПЦР), реакция иммунофлюоресценции (РИФ), реакция латекс агглютинации (РЛА), иммуноферментный анализ (ИФА) для определения в копрофильтрате антигенов сальмонелл:

Серологическая диагностика (РНГА, ИФА, РИФ) имеет значение только для эпидемиологических исследований и определения связи осложнений с перенесенной инфекцией.
Изменения гемограммы и копроцитограммы при сальмонеллезной инфекции не имеют специфических черт, характеризуются нейтрофильным лейкоцитозом у 60-80% больных, ускорением СОЭ до 15-40 мм/ч.
Сальмонеллез. План лекции Определение Характеристика возбудителя Характеристика эпидемического процесса Нозокомиальный сальмонеллез Механизм развития. — презентация
Презентация была опубликована 4 года назад пользователемЮрий Тишечкин
2 План лекции Определение Характеристика возбудителя Характеристика эпидемического процесса Нозокомиальный сальмонеллез Механизм развития заболевания Клиническая картина Методы диагностики Лечебная тактика Профилактика и диспансеризация
3 Сальмонеллез – острое инфекционное заболевание, вызываемое энтеробактериями рода Salmonella
4 МКБ-X А 01 – тиф и паратиф А 01.0 – брюшной тиф А 01.1 – паратиф А А 01.2 – паратиф В А 01.3 – паратиф С А 01.4 – паратиф неуточненный А 02 – другие сальмонеллезные инфекции А 02.0 – сальмонеллезный энтерит А 02.1 – сальмонеллезная септицемия А 02.2 – локализованная сальмонеллезная инфекция (артрит, менингит, остеомиелит и др.) А 02.8 – другая уточненная сальмонеллезная инфекция А 02.9 – сальмонеллезная инфекция неуточненная
5 В настоящее время извест- но более 2500 серовариан- тов, из которых около 700 патогенны для человека Наиболее часто регистрируются серовары групп В, С и D
6 Таксономия сальмонелл Подвид I – или название серовара для сероваров вида S.enterica подвида enterica. Для представителей других подвидов вида S.enterica введены следующие обозначения: Подвид II – для сероваров S.enterica subsp. salamae Подвид IIIa – для сероваров S.enterica subsp. arizonae Подвид IIIb — для сероваров S.enterica subsp. diarizonae Подвид IV — для сероваров S.enterica subsp. houtenae; Подвид VI — для сероваров S.enterica subsp. indica V – Вид S.bongori – для серовара S.bongori subsp. bongori. Все серовары вида S.bongori имеют символ V.
7 Звенья эпидпроцесса Источник инфекции – естественным резервуаром сальмонелл подвидов 1 и 2 служат теплокровные животные, а для представителей остальных подвидов (IIIa, IIIb, IV, VI и вида S.bongori (V) – хладнокровные животные и окружающая среда. Механизм передачи – фекально-оральный, воздушно-пылевой (нозокомиальный) Пути передачи – пищевой, контактный Восприимчивость — всеобщая
8 Этиологические агенты нозокомиального сальмонеллеза С конца 70 годов XX века до 60% всех заболеваний, связанных с внутрибольничным инфицированием, вызванны S. typhimurium, 80% заболевших – пациенты хирургических и реанимационных отделений, только 20% — больные терапевтического профиля и персонал лечебных учреждений
9 Факторы риска развития нозокомиального сальмонеллеза Оперативное вмешательство (преимущественно на органах брюшной полости) Лечение и пребывание в послеоперационном периоде в отделениях интенсивной терапии и реанимации Пожилой и старческий возраст пациентов Хроническая патология органов и систем с признаками функциональной недостаточности Нарушения иммунного статуса пациентов
10 Факторы, способствующие развитию сальмонеллеза Область фактораСостояние Желудок Кишечник Кровь Иммунная система Ахлоргидрия Операции на желудке Применение антибиотиков Операции на кишечнике Воспалительные заболевания кишечника Гемоглобинопатии Опухолевые заболевания, лейкоз, применение иммуносупрессантов, сахарный диабет, ВИЧ
11 Внедрение в организм Колонизация нижних отделов тонкой кишки Инвазия слизистой цитотоксин Острое воспаление ±язвеобразование Синтез простагландинов Синтез энтеротоксина Синтез цитокинов Активация аденилатциклазы цАМФ Продукция изотонической жидкости ДИАРЕЯ
12 Сальмонеллез, гастроинтестинальная форма, гастроэнтеритический вариант, средней тяжести, дегидратация II степени. Гастроинтестинальная форма гастрит гастроэнтерит гастроэнтероколит Генерализованная форма тифоподобный септический (септикопиемический) Бессимптомное бактериовыделение – острое (до 1 месяца), затяжное (до 3 месяцев), хроническое (свыше 3 месяцев) и транзиторное.
14 Атипичные формы Стертая форма — характеризуется слабо выраженной и быстропроходящей дисфункцией желудочно-кишечного тракта. Общее состояние не нарушается. Стул разжижен, но имеет каловый характер, без видимых патологических примесей, с частотой 23 раза в сутки в течение 12 дней. У отдельных больных возможны урчание и кратковременная боль в животе. Субклиническая форма — клинически не проявляется. Бактериовыделение
15 Осложнения сальмонеллеза Коллапс. Инфекционно-токсический шок, ОПН. Дегидратационный шок. Хирургические – токсическая дилатация кишки, перитонит, аппендицит и др. Реактивный полиартрит, инфекционно- аллергический артрит. Реактивный панкреатит. Обострения и рецидивы.
16 Методы диагностики Клинико-анамнестический Лабораторная -общеклинические исследования -бактериологический метод -серологический метод -иммунологические -молекулярно-генетические Инструментальная
17 Для исследования на наличие сальмонелл отбирают: испражнения, рвотные массы и промывные воды желудка, кровь, мочу, а при наличии специальных показаний — желчь, дуоденальное содержимое, спинномозговую жидкость и секционный материал. Патологический материал следует доставлять в лабораторию в возможно короткий срок, но не позднее 12 ч. после отбора, испражнения (фекалии) — не позднее 3-4 ч.; кровь высевают у постели больного
18 Лечебная тактика Промывание желудка Диета Регидратация Энтеросорбционная терапия Антидиарейные препараты Коррекция дисбиоза Иммунноориентированная терапия Посимптомная терапия Хирургическое лечение Этиотропная терапия
20 СП ПРОФИЛАКТИКА ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ КИШЕЧНЫЕ ИНФЕКЦИИ ПРОФИЛАКТИКА ОСТРЫХ КИШЕЧНЫХ ИНФЕКЦИЙ СП ПРОФИЛАКТИКА САЛЬМОНЕЛЛЕЗА
Внутрибольничный сальмонеллез — острая антропонозная инфекция, обусловленная полирезистентными к антибиотикам вариантами возбудителей и характеризующаяся преимущественным поражением кишечника с развитием синдрома интоксикации. Имеет место бактерионосительство — как форма проявления инфекции.
По мере накопления данных об эпидемическом процессе сальмонеллезов стало очевидным, что у некоторых возбудителей возможен антропонозныи цикл развития.
Биологические варианты S. typhimurium, дифференцируемые по степени патогенности для энтерально зараженных мышей, чувствительности к антибиотикам и содержанию плазмид 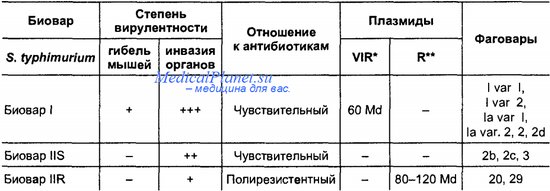
Анализ 52 вспышек внутрибольничного сальмонеллеза, зарегистрированных на территории России в 1976—1983 гг. (Кафтырева Л. А., 1999) показал, что возбудителями внутрибольничного сальмонеллеза являлись представители пяти сероваров сальмонелл: S. typhimurium (35 вспышек), S. haifa (6 вспышек), S. infantis (2 вспышки), S. рапата (2 вспышки), S. enteritidis (3 вспышки).
Возбудители внутрибольничного сальмонеллеза характеризуются гетерогенностью фенотипических и генотипических свойств, полирезистентностью к антибиотикам, неоднородностью по серологическим и ферментативным признакам, по фаготиповой принадлежности, спектрам устойчивости к антибиотикам и плазмидному профилю. Все эти свойства могут быть использованы в целях эпидемиологического маркирования штаммов и дифференциальной диагностики антропонозных и зоонозных вариантов.
В таблице представлены основные дифференциальные признаки, по которым возможно определить зоонозныи и антропонозныи вариант S. typhimurium.
Cравнительное изучение штаммов S. typhimurium, которые были выделены при эпизоотиях и при пищевых токсикоинфекциях — с одной стороны, и при ВБИ было осуществлено В. А. Арбузовой. Эти исследования с применением генетических приемов были продолжены Л. А. Кафтыре-вой. Дифференциация штаммов оказалась возможной по культуральным, некоторым биохимическим признакам, но главное различие — штаммы, выделенные при ВБИ, не обладали вирулентностью для белых мышей.
Эпидемиологические данные внутрибольничного сальмонеллеза свидетельствуют, что штаммы, потерявшие вирулентность для белых мышей, приобрели высокую вирулентность для человека. Эпидемиологические наблюдения показывают, что зоонозный сальмонеллез у человека возможен только при пищевых токсикоинфекциях, т. е. при очень высокой инфицирующей дозе. В отличие от этого антропонозный госпитальный сальмонеллез возникает при заражении через различные предметы при уходе за пациентами, через руки персонала, т. е. заражение происходит от заметно меньших доз.
Кроме того, госпитальные штаммы внутрибольничного сальмонеллеза имеют выраженную резистентность к различным антибиотикам. Поэтому и высказывалось мнение, что появление возбудителей ВБИ — результат широкого применения антибиотиков. Э. М. Новгородская, В. А. Арбузова и ряд зарубежных авторов обнаружили возбудителей ВБИ еще до активного использования антибиотиков. Кроме того, надо иметь в виду, что госпитальные штаммы, выделенные в различных стационарах ряда стран, обладали существенными отличиями между собой по плазмидному профилю (по R-плазмидам).
Обращает внимание также то, что госпитальные штаммы внутрибольничного сальмонеллеза не обладают чувствительностью ко всем сальмонеллезным фагам. Потребовались большие и кропотливые исследования, которые позволили найти фаг, обладающий активностью в отношении госпитальных штаммов (в частности фаг 20 Тбилисского ИВСа). Имеются все основания предполагать, что формирование госпитальных штаммов — это результат заражения не столько R-плазмидами, сколько умеренным фагом, ведущим к лизогенности бактерий (потере чувствительности к собственному фагу и множеству других).
Умеренные фаги, как известно, внедряют свой генетический материал в хромосому, в отличие от плазмид, которые находятся в цитоплазме (вне ядра). По-видимому, в этом объяснение обилия плазмидных профилей. R-плазмиды — это сопутствующий, влияющий на лечебные мероприятия фактор, но не ответственный за кардинальную трансформацию биологических свойств.
Важно отметить, что определение плазмидного профиля внутрибольничного сальмонеллеза служит эпидемиологическим целям, поскольку позволяет устанавливать эпидемические связи.
Большинство исследователей отмечают значительную устойчивость сальмонелл к воздействию физических и химических факторов. Они обладают высокой устойчивостью к высушиванию (сохраняют жизнеспособность в комнатной пыли до 80 дней), к низким температурам. Определенные штаммы микроорганизмов этого рода в условиях стационара обладают повышенной устойчивостью к дезинфектантам.
.jpg)
Внутрибольничные сальмонеллезы представляют серьезную проблему для стационаров различного профиля. В структуре внутрибольничных кишечных инфекций их доля может достигать половины, и они чаще других инфекций данной группы формируют внутрибольничные вспышки.
Согласно данным некоторых специалистов (Яфаев Р.Х., Зуев Л.П., 1989; Акимкин В.Г., 1998), сальмонеллез – единственная нозологическая форма (не считая некоторых гнойно-септических инфекций), для которой большое значение в сохранении возбудителя как биологического вида имеет его циркуляция в лечебных учреждениях. Эпидемическая характеристика внутригоспитального сальмонеллеза во многом отличается от эпидемиологии классического сальмонеллеза. Чаще сальмонеллез в стационарах возникает и распространяется за счет циркуляции госпитальных штаммов возбудителя, имеющих своеобразные параметры (хотя в стационаре бывают вспышки, связанные с нарушением технологии приготовления мяса животных).
Присоединение сальмонеллеза к уже имеющейся патологии у пациентов усугубляет тяжесть течения основного заболевания. До 6% внутрибольничных сальмонеллезов заканчиваются летальным исходом (Ковалева Е.П., Семина Н.А., 1993; Бухарин О.В. и соавт., 2000; Акимкина В.Г., Покровский В.И., 2002).
Е.А. Трунилина (2004) отмечает, что летальность при сальмонеллезе составляет более 7%, но в 96,7% эти случаи вызваны инфицированием Salmonella typhimurium. Летальный исход наступает вследствие сепсиса, перфорации кишечника после полостной операции с развитием перитонита, пневмонии, полиорганной недостаточности в результате интоксикационного синдрома и по другим причинам.
Способностью распространяться внутрибольнично обладают различные серовары сальмонелл, но лидирующая роль принадлежит S. typhimurium, на примере которой изучен эпидемический процесс внутрибольничных сальмонеллезов и разработаны принципы эпидемиологического надзора (Масалин Ю.М., Перепелкин В.С., 1995; Демин И.А., Брусина Е.Б., 2006).
На многих территориях второе место в структуре сальмонеллезов стойко удерживает Salmonella enteritidis, а третье – Salmonella infantis (Демин И.А., Брусина Е.Б., 2006). При определенных условиях каждый из этих двух сероваров может стать лидирующим и вызвать внутрибольничную вспышку.
Имеющиеся значительные отличия в эпидемиологии, этиологии, клинике классического (зоонозного) и нозокомиального сальмонеллеза позволяют выделить последний в особую группу инфекций, придав ей статус самостоятельной нозоформы инфекционной патологии человека.
Эпидемиологические закономерности госпитальных сальмонеллезов значительно отличаются от внегоспитальных, наблюдаемых при традиционном пищевом пути их распространения.
Госпитальные штаммы сальмонелл представляют собой особую биологическую разновидность, имеющую ряд свойств, позволяющих дифференцировать их от обычных сероваров, и обладают способностью формировать очаги инфекции, характеризующиеся значительным количеством принципиальных особенностей течения эпидемического процесса в отличие от классической сальмонеллезной инфекции.
В отличие от традиционного пищевого зоонозного сальмонеллеза, госпитальному сальмонеллезу присуще своеобразие всех звеньев эпидемического процесса: источника инфекции, путей передачи возбудителя и восприимчивого к заражению организма.
Принципиально важной особенностью сальмонеллеза как госпитальной инфекции является то, что источником возбудителя и основным резервуаром инфекции в этих условиях служит человек – дети и взрослые (больные или бактерионосители), поступающие в стационар или находящиеся в нем, а также медицинский персонал. Заболевшие могут находиться на лечении в различных по профилю отделениях (хирургических, реанимационных, детских, инфекционных, терапевтических и др.). Стойкие очаги инфекции в стационарах поддерживаются за счет вовлекающегося в эпидемический процесс медицинского персонала, составляющего в отдельных случаях до 5–9% от всех выявленных заболевших (носителей; Акимкин В.Г., Покровский В.И., 2002; Демин И.А., Брусина Е.Б., 2006). Перевод больных сальмонеллезом из одних отделений в другие ведет к возникновению случаев инфекции и способствует формированию стойких очагов нозокомиального сальмонеллеза.
В эпидемический процесс вовлекаются новорожденные, дети первого года жизни, лица пожилого и старческого возраста (Акимкин В.Г. и соавт., 2000; Трунилина Р.А., 2004), пациенты с тяжелой общесоматической патологией. Анализ вспышек внутрибольничного сальмонеллеза контактно-бытового характера (Акимкин В.Г., 1998, 2000; Демин М.А., Другина Е.Б., 2006;. Трухина Г.М., Наполова И.В., 2008) показывает, что своеобразие эпидемического процесса обусловлено совокупностью факторов риска:
• условиями замкнутого коллектива;
• концентрацией контингентов повышенного риска развития заболеваний (острая хирургическая патология пищеварительного тракта и мочевыводящих путей, обширные термические поражения кожи, онкологические заболевания, травматические повреждения и др.);
• условиями резервации госпитальных штаммов сальмонелл;
• особенностями содержания и ухода за пациентами;
• перемещениями по стационарам (отделениям);
• дисбактериозом;
• выраженной иммуносупрессией и др.
Вспышки внутрибольничного сальмонеллеза и спорадические случаи приводят к контаминации возбудителями воздуха, палат, предметов ухода за больными, постельного белья, лечебно-диагностической аппаратуры, мебели и т. д. со значительной их устойчивостью к антибактериальным препаратам и растворам дезинфектантов в обычных концентрациях (сальмонеллы погибают лишь при обработке дезинфицирующими растворами в высоких концентрациях или при воздействии дезинфектантов и антисептиков нового поколения). В связи с этим нозокомиальному сальмонеллезу, в отличие от классического, имеющего фекально-оральный механизм передачи инфекции с преимущественно пищевым путем, в наибольшей степени присущ контактно-бытовой путь. Заражение в этом случае чаще всего происходит через общие предметы (инструментарий, медицинский инвентарь, соски, игрушки и другие предметы обихода, обстановки и ухода в палатных секциях), грязные руки персонала, посуду, лекарственные средства (физиологический раствор, раствор глюкозы), контаминированные сальмонеллами. Указанный механизм передачи в большом количестве случаев подтверждается бактериологически.
Другой механизм передачи – воздушно-пылевой, хотя он является дискутабельным. В настоящее время накопленный практический опыт эпидемиологического обследования очагов нозокомиального сальмонеллеза позволяет не только убедительно говорить о его наличии, но и в ряде случаев считать такой механизм передачи ведущим (то есть наиболее активным; Беляков В.Д., Акимкин В.Г., 1997; Акимкин В.Г. и соавт., 2000). Воздушно-пылевой путь передачи может реализоваться двумя способами (Крыстева Т. и соавт., 1969): при непосредственном проникновении возбудителя с вдыхаемым воздухом, содержащим пылевые частицы (аэрозольный), и через пищевые продукты в результате попадания на них пылевых частиц, несущих сальмонеллы.
Описываются случаи выделения сальмонелл из раны в условиях стационара. При сформировавшемся хроническом очаге внутрибольничного сальмонеллеза в крупной многопрофильной больнице, обусловленном сероваром S. infantis, в течение более 10 лет выявляли большое количество пациентов, находившихся в тяжелом или терминальном состоянии, у которых из ран выделялся данный серовар (Демин И.А., 2003). Причем большинство штаммов высевались с типичными возбудителями раневых инфекций (от 1 до 4 патогенных бактерий – стафилококки, стрептококки, протей, кишечная палочка, клебсиелла и др.). Согласно наблюдениям, обсеменение раны S. infantis происходило в одних случаях эндогенным путем при генерализации сальмонеллезной инфекции, в других – экзогенным (при контактно-бытовом пути инфицирования) и не зависело напрямую от обсеменения кишечника, то есть являлось самостоятельным процессом.
Важной особенностью госпитального сальмонеллеза является также возможность заражения пациентов в стационарах малой инфицирующей дозой сальмонелл – 10 3 микробных тел (Blaser M.I., Newman I.S., 1982). Это связано с полирезистентностью нозокомиальных штаммов, сочетанием устойчивости их к воздействию факторов внешней среды, обусловливающих длительное (до 180–250 дней) выживание (Акимкин В.Г., 1998), и высокой степени контагиозности (Беляков В.Д., Акимкин В.Г., 1997) в отношении определенных категорий больных и персонала стационара. Заражающей дозой для иммунокомпетентного человека является доза 107 бактерий. Эстафетная передача возбудителя инфекции – характерная черта эпидемиологии внутригоспитального сальмонеллеза.
Инкубационный период составляет 3–8 дней. У более чем 90% заболевших нозокомиальным сальмонеллезом диарея появляется на 3-й день. Заболевание развивается постепенно, диарея может быть незначительной (Масалин Ю.М., Перепелкин В.С., 1995), во многих случаях наблюдается энтероколит. В то же время клиническая картина нозокомиального сальмонеллеза может характеризоваться бурным началом с высокой и продолжительной лихорадкой, диспепсическими явлениями на фоне выраженной интоксикации (Акимкин В.Г., 1998).
Поражение кишечника носит распространенный характер и более чем в 50% случаев сопровождается гастроэнтеритическим синдромом. Регистрируется жидкий водянистый стул с примесью слизи, иногда – крови. Часто в процесс вовлекается гепатобилиарная система. У большинства больных нарушается почечная гемодинамика. Практически у всех пациентов отмечаются выраженные изменения микрофлоры кишечника.
В структуре проявлений нозокомиального сальмонеллеза преобладают манифестные формы с типичным течением заболевания. Однако отмечается значительное количество случаев (1/4) с атипичными проявлениями инфекционного процесса, в том числе иногда на первый план выступает симптоматика сальмонеллеза как гнойно-септической инфекции. У отдельной группы пациентов (прооперированные онкобольные) госпитальный сальмонеллез в 80–97% случаев протекает более тяжело с одинаковой частотой развития локализованных и генерализованных форм (Беляков В.Д., Акимкин В.Г., 1997; Акимкин В.Г., 1998).
Заслуживает внимания тот факт, что в первые 7 мес вспышки в клинике преобладают более тяжелые формы (74,7%), и они практически отсутствуют в последние месяцы регистрации заболевания (Беляков В.Д., Акимкин В.Г., 1997). Инфицирование больных преимущественно (65%) происходит в послеоперационный период.
Возбудители нозокомиального сальмонеллеза отличаются значительной полирезистентностью к антибиотикам, которая развивается не только вследствие их интенсивного применения. В.Д. Беляков, В.Г. Акимкин еще в 1997 г. отметили, что выделенные штаммы от больных в лечебно-профилактических учреждениях в 81,7% случаев были абсолютно нечувствительны к 38 известным антибиотикам широкого спектра действия. Еще во второй половине ХХ ст. после курса антибактериальной терапии до 30–50% больных выделяли сальмонеллы повторно (Buchwald D.S., Blaser M.I., 1984; Ковалева Е.П., Семина Н.А., 1993). Поэтому выбор этиотропной терапии и профилактики заболевания, а также схемы применения препаратов должны быть научно обоснованными.
Наряду с антибиотикорезистентностью отмечается значительная устойчивость выделенных штаммов к растворам дезинфектантов в обычных концентрациях.
Таким образом, нозокомиальная сальмонеллезная инфекция характеризуется:
• образованием стойких очагов со сформировавшимися госпитальными штаммами возбудителя;
• существованием совокупности факторов риска внутрибольничной заболеваемости;
• длительным инкубационным периодом;
• острым или постепенным началом заболевания;
• гастроинтестинальным синдромом, реже – в виде гнойно-септической инфекции;
• вовлечением в процесс гепатобилиарной системы;
• преобладанием более тяжелых форм инфекции;
• усугублением тяжести основного заболевания;
• часто повторным выделением сальмонелл;
• полиантибиотикорезистентностью возбудителя инфекции.
Профилактические и противоэпидемические мероприятия довольно трудоемкие и сложные.
Эффективность ликвидации очагов сальмонеллеза в лечебно-профилактических учреждениях зависит от своевременности, качества проведения комплекса противоэпидемических мероприятий, ориентированных на все звенья эпидемического процесса: своевременная изоляция больного, адекватная терапия, наблюдение за контактными лицами, влажная уборка палат не менее 2 раз в день, текущая и заключительная дезинфекция в очаге, обработка и дезинфекция инструментария и аппаратуры, дезинфекция постельных принадлежностей и матрацев, контроль за пищеблоком. Всем восприимчивым, поступающим в отделения с высоким риском заражения (отделения реанимации, полостной хирургии) в эпидемиологически неблагоприятный период, профилактически целесообразно назначение сальмонеллезного бактериофага. Значительное снижение уровня заболеваемости и выраженный лечебный эффект получены только при использовании сальмонеллезного бактериофага, адаптированного к штаммам сальмонелл, выделенных из очага (Беляков В.Д., Акимкин В.Г., 1997). Необходимо проводить санацию и профилактику заражения среди медицинского персонала, бактериологическое обследование всех больных, в первую очередь, поступающих в отделения хирургического профиля.
Система профилактических мероприятий основывается на мониторинге диарейного синдрома, выявлении предвестников эпидемического неблагополучия, сокращении времени пребывания пациента в стационаре, обеспечении высокой степени антиинфекционной защиты медицинских технологий, сокращении числа пациентов в палате, систематическом обучении персонала.
Читайте также:


