Спиртовая дизентерийная вакцина флекснера зонне используется для
Содержит раствор очищенного Vi-капсульного полисахарида Salmonella typhi, консервант – фенол. Применяется для профилактики брюшного тифа у взрослых и детей старше3 лет по эпидпоказаниям.
Аналог: Тифим Ви (Россия)
Брюшнотифозная вакцина с секста(тетра)анатоксином (Россия)
Содержит О- и Vi-антигены брюшнотифозных бактерий и очищенные концентрированные анатоксины возбудителей столбняка, ботулизма. газовой гангрены, адсорбент – гидроксид алюминия. Применяется для профилактики брюшного тифа и клостридиальных инфекций по эпидпоказаниям.
Вакцина холерная корпускулярная инактивированная сухая (Россия)
Содержит взвесь равных количеств холерных вибрионов сероваров Огава и Инаба, классических или Эль-Тор биоваров. Применяется для активной иммунизации против холеры по эпидпоказаниям у лиц старше 7 лет.
Вакцина холерная (Холероген-анатоксин и О-антиген) жидкая и сухая (Россия)
Содержит 2400 ЕС холерогена-анатоксина и 90 усл. ЕД О-антигена. Применяются для профилактики холерыпо эпидпоказаниям.
Спиртовая дизентерийная вакцина сухая (Россия)
Содержит убитые спиртом палочки Флекснера и Зонне 2 : 1. Вводят после растворения изотоническим раствором подкожно. Применяют для лечения затянувшихся и хронических форм дизентерии у взрослых и детей.
СолкоТриховак (Ай Си Эн Фармасьютикал Швейцария ЛТД)
Содержит лизат инактивированных лактобацилл L. rhamnosus, L. vaginalis, L. fermentum, L. salivaris, консервант – фенол, стабилизатор – желатин, растворитель физиологический раствор. Применяется для профилактики и лечения рецидивирующего неспецифического бактериального вагиноза и трихомониаза у женщин. Препарат повышает титр неспецифических антител sIgA в секрете влагалища.
Сыворотки и иммуноглобулины
Лактоглобулин против условно-патогенных бактерий и сальмонелл коровий сухой для перорального применения сухой (Россия)
Содержит фракцию глобулинов молозива иммунизированных коров. Действующее начало препарата – иммунные глобулины молозива, содержащие антитела к сальмонеллам группы В (тифимуриум) и Д (энтеритидис, дублин), протею (мирабилис и вульгарис), клебсиелле, пневмонии, псевдомонас аэругиноза. Применяется для лечения диарейных заболеваний у детей, вызванных вышеперечисленными бактериями и гнойно-воспалительных заболеваний.
Лактоглобулин противоколиротейный коровий для перорального применения сухой (Россия)
Содержит фракцию глобулинов молока иммунизированных коров. Действующим началом являются антитела к патогенным Е. coli O26, O55, O111, O119; Proteus vulgaris O43 и Р. mirabilis O35. Применяют для лечения коли-инфекции, вызванной Е. coli O26, O55, O111, O119 и коррекци дисбиоза кишечника, сопровождающегося массивным выделением P .vulgaris и Р. mirabilis.
Бактериофаги
Бактериофаг дизентерийный поливалентный в таблетках с кислотоустойчивым покрытием и в свечах (Россия)
Содержит стерильный фильтрат фаголизатов возбудителей бактериальной дизентерии: шигелл Флекснера и Зонне. Применяется для экстренной профилактики и лечения острой дизентерии.
Бактериофаг сальмонеллезный групп А, В, С, D, Е в таблетках с кислотоустойчивым покрытием, в свечах, жидкий (Россия)
Содержит стерильный фильтрат фаголизатов наиболее распространенных серогрупп сальмонелл А, В, С, D, Е. Применяется для лечения и экстренной профилактики паратифов А, В и сальмонеллезных гастроэнтеритов.
Бактериофаг брюшнотифозный в таблетках с кислотоустойчивым покрытием (Россия)
Содержит стерильный фильтрат фаголизатов сальмонелл брюшного тифа. Применяется для лечения и экстренной профилактики.
Интести-бактериофаг жидкий (Россия)
Содержит смесь стерильных фильтратов фаголизатов: шигелл Флекснера 1, 2, 3, 4, 6-го серовариантов, шигелл Зонне, сальмонелл паратифа А и В, тифимуриум, инфантис, холнрасуис, ораниенбург, энтеритидис, протея, ЭПКП, энтерококков, стафилококков, синегнойной палочки. Применяется для лечения кишечных инфекций и коррекции дисбиозов кишечника.
Бактериофаг коли-протейный жидкий (Россия)
Содержит смесь стерильных фильтратов фаголизатов ЭПКП О111, О55, О 44, О 20, О145, О26, O124, O125 и протея (P.mirabilis, P. vulgaris). Применяют для лечения и профилактики дисбактериозов, инфекций коли-протейной этиологии.
Бактериофаг протейный жидкий (Россия)
Содержит смесь стерильных фаголизатов, активных в отношении Р. mirabilis, P. vulgaris. Применяют с лечебной и профилактической целью.
Вакцины и сыворотки
1. Живые вакцины
· Живая бактериальная вакцина, содержащая Ag
· Применяется с профилактической целью
· Получают путём культивирования ослабленного штамма – микобактерии туберкулёза бычьего типа
· Иммунитет искусственный приобретённый активный антибактериальный напряжённый
NB!История вопроса. Вакцина создана в 1921г. 13 лет ученые выращивали возбудитель на яично – картофельном глицериновом агаре с добавлением желчного бульона. Сделано 230 пассажей.
· Живая вирусная вакцина, содержащая Ag
· Применяется с профилактической целью
· Получают путём культивирования в культуре клеток эмбрионов японских перепелов
· Иммунитет искусственный приобретённый активный противовирусный напряжённый
· Вводят детям в возрасте 1 года. Ревакцинация в возрасте 6 лет.
· Инфекция – корь, паротит, краснуха
· Живая вирусная вакцина, содержащая Ag
· Применяется с профилактической целью
· Получают путём культивирования в культуре клеток куриного эмбриона (штамм вируса кори и паротита) и диплоидных клеток человека (штамм вируса краснухи)
· Иммунитет искусственный приобретённый активный противовирусный напряжённый
· Вводят детям в возрасте 1 года. Ревакцинация в 6 лет, девочкам, у которых не было вакцинации против краснухи, в 13 лет.
· Инфекция – корь, краснуха, паротит
· Живая вирусная вакцина, содержащая Ag
· Применяется с профилактической целью
· Получают путём культивирования раздельно в культуре клеток куриного эмбриона (штамм вируса кори и паротита) и диплоидных клеток человека (штамм вируса краснухи)
· Иммунитет искусственный приобретённый активный противовирусный напряжённый
· Вводят детям в возрасте 1 года. Ревакцинация в 6 лет, девочкам, у которых не было вакцинации против краснухи, в 13 лет.
2. Убитые вакцины (профилактические)
Коклюшная
· Убитая вакцина, содержащая Ag
· Применяется с профилактической целью
· Получают путём выращивания коклюшного компонента на питательных средах и затем инактивированных формалином или мертиолятом натрия?
· Иммунитет искусственный приобретённый активный антибактериальный напряжённый
· Вводят здоровым детям в 3-4,5-6 месяцев.
· Усиленная инактивированная вакцина, содержащая Ag
· Применяется с профилактической целью
· Получают путём культивирования в культуре клеток, с последующей инактивацией и очисткой
· Иммунитет искусственный приобретённый активный противовирусный напряжённый
· Вводят здоровым детям по схеме 3-4,5-6 месяцев. Ревакцинация в 18 мес., 20 мес. и 14 лет.
3. Убитые вакцины (Лечебные)
· Инфекция – гепатит А
· Инактивированная вакцина, содержащая Ag
· Применяется для плановой и экстренной профилактики гепатита А, в т.ч. для ликвидации эпидемических очагов
· Получают путём культивирования на диплоидных клетках человека, затем инактивируют формальдегидом
· Иммунитет искусственный приобретённый активный противовирусный напряжённый
· Применяется по эпид. показаниям
· Вводят детям с 2 лет и взрослым однократно в/м. Ревакцинация проводится через 6-18 месяцев однократно.
Стафилококковая
ü Вакцина стафилококковая лечебная жидкая (Антифагин стафилококковый)
· Применяется для лечения гнойничковых заболеваний кожи стафилококковой этиологии.
· Получают из взвеси микробных клеток стафилококка, прогретых при 
С в течении 1 часа
· Иммунитет искусственный приобретённый активный антибактериальный напряжённый
· Курс лечения взрослых и детей с 7-летнего возраста состоит из однократных ежедневных инъекций в течение 8-15 суток. Для детей от 6 месяцев до 7 лет доза первой инъекции составляет 0,1 мл. Каждую последующую инъекцию делают на расстоянии 20-30 мм от места предыдущей или в другую руку.
ü Вакцина стафилококковая сухая для иммунотерапии
· Содержит комплекс антигенов белково-полисахаридной природы
· Применяют для лечения больных с затяжной хронической стафилококковой инфекцией или при её ассоциации с инфекциями другой этиологии
· Получают из специально селекционированных штаммов Staphylococcus aureus
· Иммунитет искусственный приобретённый активный антибактериальный напряжённый
· Минимальный курс состоит из 5 инъекций с интервалом 3-4 суток. При недостаточно выраженном эффекте – продлевают введение вакцины до 8-10 раз. Применять можно с 6 месяцев.
Дизентерийная (Сухая спиртовая дизентерийная вакцина Флекснер-Зонне)
· Инфекционное заболевание - дизентерия
· Применяют для лечения затяжных и хронических форм дизентерии
· Получают путём выращивания на питательных средах. Затем инактивируют этаноло
· м и лиофильно высушивают
· Иммунитет искусственный приобретённый активный антибактериальный напряжённый
Гонококковая
· Убитая гонококковая вакцина, содержащая Ag
· Применяется в лечебных целях, а также для диагностики в качестве провокационного теста
· Получают путём выращивания на питательных средах с последующей инактивацией культуры гонококков при 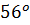
С.
· Иммунитет искусственный приобретённый активный антибактериальный напряжённый
· По показаниям. Детям старше 3х лет и взрослым. Вакцину вводят в/м в ягодичную область или подкожно с интервалом 1-2 суток в зависимости от реакции, дозу увеличивают каждый раз, количество инъекций достигает 6-8
Дата добавления: 2019-09-02 ; просмотров: 99 ;
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |

а) экстрагировать О-антиген
ацетоном;
б) разрушить Vi-антиген
кипячением;
в) разрушить К-антиген
кипячением;
г) нейтрализовать Vi-антиген
сывороткой.
51. Эшерихии можно
отдифференцировать
от шигелл с помощью
следующих тестов:
2) наличие лизиндекарбоксилазы;
3) ферментация лактозы;
4) ферментация глюкозы;
5) реакция Фогеса-Проскауэра.
52. Для рода шигелл
стабильным является:
а) отсутствие подвижности;
б) ферментация маннита;
в) отсутствие выделения
сероводорода.
1) ферментация маннита;
2) выделение индола;
3) ферментация сахарозы;
4) выделение сероводорода;
5) расщепление мочевины.
54. Основным методом диагностики дизентерии является:
г) культуральный метод.
55. Возбудители бактериальной дизентерии относятся к роду:
56. Из нижеперечисленных
бактерий не имеют жгутиков:
57. Наиболее тяжелые
клинические формы
дизентерии вызывают:
б) S. disenteriae I;
58. Наличие в фекалиях крови и слизи является симптом,
характерным для:
б) сальмонеллезного
гастроэнтерита;
г) брюшного тифа;
59. Для шигелл характерны
основные антигены:
60. Спиртовая дизентерийная вакцина Флекснера-Зонне
используется для:
а) заблаговременной
профилактики дизентерии;
б) экстренной профилактики
дизентерии;
в) лечения хронической
дизентерии.
61. Размножение возбудителя
в клетках эпителия
толстого кишечника –
ведущее звено
патогенеза:
в) сальмонеллезного
гастроэнтерита;
д) брюшного тифа;
62. Выделение сероводорода
на среде Клиглера в сочетании
с отсутствием ферментации лактозы является
характерным
признаком:
а) продукция экзотоксина
(цитотоксина);
б) выделение сероводорода;
в) ферментации лактозы.
64. Наиболее активными
по биохимическим свойствам
среди шигелл являются:
а) S. dysenteriae;
65. Для шигелл оптимальной транспортной средой является:
а) глицериновый консервант;
б) среда Китта-Тароцци;
66. Для выделения S.dysenteriae следует брать среды:
67. Видовую принадлежность шигелл определяют
по следующим признакам:
б) тинкториальные свойства;
в) ферментанивная активность;
г) особенности О-антигенов;
д) особенности Н-антигенов.
68. Укажите шигеллы, продуцирующие сильный экзотоксин (токсин Шига):
а) Sh. dysenteriae 1;
д) Sh. dysenteriae (все типы).
69. Укажите факторы, определяющие повышенную болезнетворность Sh. dysenteriae:
г) внутриэпителиальная (энтероциты) инвазия;
д) устойчивость во внешней среде.
а) является разновидностью
О-антигена;
б) является разновидностью
Н-антигена;
в) является разновидностью
К-антигена;
г) характерен для рода Salmonella;
д) характерен для S. typhi.
71. Укажите факторы
и механизмы, определяющие поражение тонкого кишечника при брюшном тифе:
а) внутриэпителиальная инвазия бактерий;
в) эндогенное реинфицирование кишечника;
г) аллергическое (Т-зависимое) воспаление в стенке кишечника;
д) действие эндотоксина.
72. Во время инкубационного периода S. Typhi размножаются:
а) в энтероцитах тонкого
кишечника;
б) в гепатоцитах;
в) в просвете тонкого кишечника;
г) в просвете толстого кишечника;
д) в макрофагах пейеровых
бляшек и солитарных фолликулов.
73. Возбудители брюшного тифа и паратифов относятся к роду:
74. Сальмонеллы образуют
колонии черного цвета:
а) на среде Плоскирева;
б) на среде Эндо;
в) на висмут-сульфит агаре;
г) на щелочном МПА.
75. При диагностике брюшного тифа для выделения гемокультуры посев крови проводят
на среду:
в) висмут-сульфит агар;
76. При диагностике брюшного тифа для выделения гемокультуры соотношение крови и питательной среды должно быть:
77. Основным методом диагностики сальмонеллезов является:
78. Для сальмонелл характерны основные антигены:
79. При кишечном
сальмонеллезе поражается:
а) тонкий кишечник;
в) толстый кишечник.
80. В основу классификации сальмонелл по схеме Кауфмана-Уайта положены:
а) биохимические свойства;
б) патогенность для животных;
в) патогенность для человека;
г) антигенные свойства.
81. У носителей сальмонелл
образуются иммуноглобулины класса:
82. Внутрибольничный
штамм сальмонелл
отличается:
1) множественной лекарственной устойчивостью;
2) устойчивостью во внешней среде;
3) способностью продуцировать колицины.
83. Сальмонеллы от эшерихий можно отдифференцировать
с помощью следующих
тестов:
1) метилового красного;
2) выделения сероводорода;
5) утилизации цитрата;
6) гидролиза мочевины.
84. Наиболее ранним
и достоверным методом
диагностики брюшного тифа является:
а) выделение копрокультуры;
в) выделение гемокультуры;
г) выделение уринокультуры.
85. Висмут-сульфит относится к элективно-дифференциальным питательным средам для:
г) холерных вибрионов.
86. В реакции Видаля
выявляют:
в) диагностический титр антител;
г) качественную сероконверсию;
д) сальмонеллезные антигены.
87. Укажите антиген S. typhi, отсутствующий у подавляющего большинства других
сальмонелл:
89. Исследуемым материалом для бактериологического исследования при брюшном тифе в период лихорадки является:
90. Исследуемым материалом для бактериологического исследования при брюшном тифе начиная со второй недели
заболевания является:
91. Для заблаговременной
профилактики брюшного тифа используется:
а) живая вакцина;
б) химическая вакцина;
д) убитая вакцина;
92. Розеолезно-папулезная сыпь при брюшном тифе появляется вследствие:
а) сенсибилизации микроорганизма аллергенами возбудителя;
б) повреждения капилляров
экзотоксином;
в) воспалительных изменений поверхностных слоев кожи в месте локализации возбудителя.
93. Короткий инкубационный
период (несколько часов),
характерен для:
а) брюшного тифа;
б) сальмонеллезных
гастроэнтеритов;
в) паратифов А и В;
94. Высокие титры антител к О-антигену и низкие к Н-антигену сальмонеллы тифи характерны:
а) для начала заболевания;
б) для бактерионосительства;
в) для конца заболевания;
г) для постинфекционного
имунитета.
95. Иерсинии являются:
96. Для выделения иерсиний следует использовать среду
накопления:
а) солевой бульон;
в) магниевую среду.
97. Оптимальной температурой для культивирования иерсиний является:
98. Y. enterocolitica можно отдифференцировать от Е. pseudotuberculosis с помощью
следующих тестов:
4) цитрата Симмонса;
99. В род эрвиний в основном входят микроорганизмы:
а) патогенные для человека;
б) условно-патогенные
для человека;
100. Представители рода Yersinia могут вызывать
следующие заболевания:
г) кишечный иерсиниоз;
д) бактериальная дизентерия.
101. Для идентификации возбудителя кишечного иерсиниоза применяют следующие
идентификационные тесты:
Изобретение относится к медицине, в частности к профилактике дизентерии Зонне. Целью изобретения является штамм Shigella sonnei 13359, обладающий высокой иммуногенностью, стабильным уровнем остаточной вирулентности, маркированный, безопасный для использования в качестве живой вакцины против дизентерии Зонне, хорошо растущий на простых питательных средах. Бактерии вакционного штамма несут две мутации - зависимость по пурину и рифампицинрезистентности, связанные с аттенуацией. Наличие оптимального уровня аттенуацйи обеспечивает высокую иммуногбнную активность вакцинного штамма, уста'новленную как в опытах эффективной защиты лабораторных животных от заражения вирулентным штаммом шигелл Зонне, так и при клиническом испытании при регистрации у вакцинированных высокого титра специфических копроантител. Две мутации у бактерий (pur'/rif*^), связанные с утратой вирулентности, обеспечивают безопасность использования штамма в качестве живой вакцины и служат маркерами, позволяющими дифференцировать вакцинный штамм от штаммов шигелл Зонне естественного происхождения. 2 табл.ч^ч*'ЁVJ о00со ел
ГОСУДАРСТВЕ ННЫ Й КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ е (21) 4799475/13 (22) 05.02.90 (46) 30.01,92. Бюл. N 4 (71) Научно-исследовательский институт эпидемиологии и микробиологии им. Н.Ф.Гамалеи, Лейпцигский институт медицинской микробиологии и эпидемиологии университета им. К.Маркса и Научно-исследовательский институт заразных и паразитарных болезней Медицинской академии Болгарии (72) В.M,Áîíäãðåíêî, K.Ëèíäe, В.Денчев, Ю,M,Poìaíoaà, С.Маринова, M.Áðàòîåâà и
И. Цветанов (53) 576.851.49 (088.8) (56) Белая Ю.А., Бирковский Ю.Е., Милованова Л.П, и др. Испытание безвредности, реактивности и имммуногенности живой дизентерийной вакцины Флекснера 2а и Зонне из спонтанных мутантов. — Жур. микробиол. 1977, ¹ 1, с.20 — 25.
Nel. D,M., Gangarosa ЕЛ., Radoranovic P.
et.al. Studies on vaccinatIon agalnst baclllary
dysentery, — Bali. Uno, 1971, Vol. 45. р. 457464. (54) ШТАММ БАКТЕРИЙ ЯН16Е(1 А
SONNEI, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ЖИВОЙ ВАКЦИНЫ ПРОТИВ
Изобретение относится к медицинской микробиологии и касается получения вакцинных штаммов, которые могут быть использованы в медицине для профилактики дизентерии Зонне, В соответствии с требованиями вакцинные штаммы должны быть высокоиммуногенными, стабильными по остаточной. Ы,, 1708351 А1 (я)5 А 61 К 39/106, С 12 N 1/20 (57) Изобретение относится к медицине, в частности к профилактике дизентерии Зонне. Целью изобретения является штамм
Shlgella зоппе! l 3359; обладающий высокой иммуногенностью, стабильным уровнем остаточной вирулентности, маркированный, безопасный для использования в качестве живой вакцины против дизентерии Зонне, хорошо растущий на простых питательных средах. Бактерии вэкционного штамма несут две мутации — зависимость по пурину и рифампицинрезистентности, связанные с аттенуацией. Наличие оптимального уровня аттенуации обеспечивает высокую иммуногенную активность вакцинного штамма, установленную как в опытах эффективной защиты лабораторных животных от заражения вирулентным штаммом шигелл Зонне, так и при клиническом испытании при регистрации у вакцинированных высокого титра спецм: ических копроантител. Две мутации у бактерий (pur/rlf ), связанные с утратой вирулентности, обеспечивают безопасность использования штамма в качестве живой вакцины и служат маркерами, позволяющими дифференцировать вакцинный штамм от штаммов шигелл Зонне естественного происхождения. 2 табл. вирулентности, безопасными и нести маркеры для их дифференциации от штаммов естественного происхождения.
Известны вакцинные штаммы Shigella
sonnei, полученные путем селекции спонтанных авирулентных клонов.
Однако спонтанные авирулентные мутанты шиггел не отвечают таким требовани17083"11 ям, как генетическая охарактеризованность в связи с трудностями расшифровки их гейотипа, приводящего к утрате вирулентности, что свидетельствует об их нестабильности и небезопасности и делает невозможным повторное выделение такого типа штаммов при утрате исходным вакциОнным штаммом иммуногенности.
Наиболее близким к предлагаемому является штамм S,sonnei !, зависимый QT стрептомицина. Штамм характеризуется достаточной им муно ген н остью, генетически охарактеризован, маркирован.
Недоста гком ст Г(ептомици нза Висимь! х штаммов яв"",ëeòñÿ нестабильность, связанная с наличием одного маркера, приведшего к аттенциации, небезопасн ость использования и необходимость добавления антибиотика в -.ðåäó Вь1ращивания, что ограничиваст применение таких вакцичных штаммов из-за возможности аллергизации организма.
Целью изобретения является штамм
S.sonnei I 3359, обладающий высокой иммуногенностью, стабильным уровнем ocTBTo÷ной Виp/ëентности, марKèpоеанHûé, безопасный для использования в качестве . живой вакцины для профилактики дизентерии Зонне, хорошо расту@и(4 на простых питательных средах.
Штамм 5.воппе! l 3359 получен с исг(ользованием траг, .;ционных гене;-::;:ко-селекционных при-мов (путем обработки мутагеном и отбором> из штамма S.sonnel I
1180, характеризу1о;цегося низкой частотой утраты плазмиды фазы, варьиру::още,"1 в
Д пределах 10 0 . Бактерии исходного ш гамма зс ВИСИМ ь(по нико ИНОВОИ кису(о Г е.
Штамм S,sonnel i 3359 депонирован в кЬ(1лекции(I ) "„K им . арасевича г(од Е
Отбор штамма производится путем первичнои селекции зависимых попурину мутантов с последующим введение;-4 в ауксотрофный: Изобретение относится к биотехнологии и касается получения нового штамма бактерий - продуцента уксуса и способа производства уксуса
Государственный стандарт качества лекарственного средства
Фармакопейная статья ФС 42-
"Вакцина дизентерийная против шигелл Зонне липополисахаридная"
Вакцина дизентерийная против шигелл Зонне липополисахаридная, представляет собой раствор липополисахарида (ЛПС), извлечённого из культуры Shigella sonnei, очищенного ферментативными и физико-химическими методами.
Технология получения вакцины дизентерийной против шигелл Зонне липополисахаридной предусматривает культивирование производственного штамма в жидкой синтетической питательной среде, выделение из полученной биомассы неочищенного липополисахарида, лиофилизацию неочищенного липополисахарида, его очистку, лиофилизацию очищенного липополисахарида.
Производственный штамм Shigella sonnei должен отвечать следующим требованиям:
- на плотной питательной среде образует круглые с ровными краями выпуклые колонии (S-формы);
- в мазках, окрашенных по Граму должны быть грамотрицательные палочки;
- не должен ферментировать сорбит, дульцит, глюкозу и сахарозу;
- не должен образовывать индол;
- должен расщеплять ксилозу, арабинозу, сбраживать рамнозу, лактозу;
- не должен образовывать сероводород;
- вирулентность штамма, при внутрибрюшинном заражении белых беспородных мышей , должна быть не выше 50 млн микробных клеток ;
- должен давать положительную кератоконьюнктивальную пробу на морских свинках.
Технология получения вакцины дизентерийной против шигелл Зонне липополисахаридной предусматривает культивирование производственного штамма в жидкой синтетической питательной среде, выделение из полученной биомассы неочищенного липополисахарида, лиофилизацию неочищенного липополисахарида, его очистку, лиофилизацию очищенного липополисахарида.
Производство вакцины включает в себя следующие этапы:
- получение биомассы и ее дезактивация;
- получение неочищенного липополисахарида (ЛПС);
- лиофилизация неочищенного липополисахарида;
- очистку липополисахарида и его лиофилизацию;
- получение готовой формы препарата.
На этапе культивирования используют синтетическую питательную среду. Полученную биомассу контролируют на бактериологическую чистоту и типичность морфологии. Инактивацию проводят формалином с массовой долей формальдегида не менее , до конечной концентрации 0,5%. Контроль инактивации проводят методом посева на МПА и среду Эндо.
Полученную инактивированную культуральную жидкость центрифугируют, раствор неочищенного липополисахарида подвергают диализу. ЛПС лиофилизируют, в полученном препарате липопополисахарида исследуют О - специфическую активность.
Этап очистки ЛПС предусматривает очистку от нуклеиновых кислот, балластных белков и диализ. Лиофильно высушенный препарат очищенного липополисахарида - субстанция для приготовления готовой формы препарата.
Описание . Белый аморфный порошок.
Подлинность . Субстанция (0,01% раствор) образует одну линию преципитации с сывороткой кроличьей против липополисахарида Shigella sonnei. Определяют в реакции преципитации в геле по Оухтерлони с сывороткой кроличьей против ЛПС S. sonnei (см. тест "Подлинность" в разделе "Испытания готового продукта").
Белок . Не более 2,0%. Испытания проводят по методу Бредфорда без предварительного осаждения белка в соответствии с ОФС "Определение белка". Субстанцию предварительно растворяют в воде очищенной до концентрации 5 мг/мл лиофилизата в объеме растворителя.
Нуклеиновые кислоты . Не более 2,0%. Испытания проводят методом Спирина в соответствии с ОФС "Определение нуклеиновых кислот по методу Спирина". Субстанцию предварительно растворяют в воде очищенной до концентрации 1мг/мл лиофилизата в объеме растворителя.
Молекулярные параметры . Не менее 50% липополисахарида должно элюироваться в объеме до Kd=0,5. Определяют методом гель-фильтрации. (см. тест "Молекулярные параметры" в разделе "Испытания готового продукта").
Специфическая активность . 0,01% раствор субстанции должен тормозить реакцию пассивной гемагглютинации с сывороткой диагностической к шигеллам Зонне неадсорбированной в концентрации не выше 6,25 мкг/мл; при отсутствии торможения с сывороткой диагностической к шигеллам Флекснера неадсорбированной в концентрации менее 25 мкг/мл (см. тест "Специфическая активность" в разделе "Испытания готового продукта").
Пирогенность . Субстанция должна быть апирогенной. Испытания проводят в соответствии с ОФС "Пирогенность". Тест-доза 0,050 мкг/мл в 1,0 мл раствора натрия хлорида 0,9% на 1,0 кг массы животного.
Аномальная токсичность . Субстанция должна быть нетоксичной. Испытания проводят в соответствии с ОФС "Аномальная токсичность" (Тест для вакцин и сывороток). Готовят раствор субстанции в концентрации 100,0 мкг в 1,0 мл раствора натрия хлорида 0,9%. Тест-доза морским свинкам - 1,0 мл испытуемого раствора подкожно, мышам - 0,5 мл испытуемого раствора внутрибрюшинно.
Испытания готового продукта
Описание . Бесцветная прозрачная или слегка опалесцирующая жидкость с запахом фенола. Определение проводят органолептически.
Подлинность . Вакцина должна образовывать одну линию преципитации с сывороткой кроличьей против липополисахарида Shigella sonnei*. Определяют в реакции преципитации в геле по Оухтерлони.
Для постановки реакции пластиковую или стеклянную пластины размером 8,5 на 9,5 см заливают гелем агарозы по 12 мл на одну пластину. В застывшем слое геля с помощью пробойника и специального трафарета делают лунки: одну центральную, остальные - на периферии. Диаметр лунок 0,4 см, расстояние между ними должно быть 0,4 см. В центральную лунку вносят по 15 мкл раствора сыворотки кроличьей против ЛПС S. sonnei (титр 1:800), в периферические - 15 мкл испытуемой вакцины. Затем пластину помещают во влажную камеру на 24-48 часов. Вакцину считают подлинной, если с сывороткой кроличьей против ЛПС S. sonnei она дает одну линию преципитации.
Прозрачность . Прозрачная или опалесцирующая не более эталона 1 жидкость. Испытания проводят в соответствии с ОФС "Прозрачность и степень мутности жидкостей".
Цветность . Бесцветная жидкость. Испытания проводят в соответствии с ОФС "Степень окраски жидкостей".
Механические включения . Видимые механические включения должны отсутствовать. Определение проводят визуально в соответствии с ОФС "Видимые механические включения в лекарственных формах для парентерального применения и глазных лекарственных формах".
рН . От 6,7 до 7,3. Испытания проводят потенциометрическим методом в соответствии с ОФС "Ионометрия".
Молекулярные параметры . Не менее 50% липополисахарида должно элюироваться в объеме до Kd=0,5. Определяют методом гель-фильтрации, используя сефарозу. Используют колонку длиной около 0,4 м, с внутренним диаметром 9 мм, уравновешенную 0,2 М раствором натрия хлорида. Через колонку пропускают около 0,9 мг лиофилизата субстанции в объеме 0,5 мл раствора 0,2 М натрия хлорида и элюируют при скорости около 14 мл/час. Элюирующиеся фракции регистрируют при помощи ультрафиолетового детектора при 206 нм. Выход липополисахарида оценивают по площади пиков до и после Кd = 0,5.
Калибровку колонки для определения полного и свободного объема колонки проводят с помощью калибровочного раствора, содержащего голубой декстран и натрия азид, в условиях, описанных выше.
Вычисление объема колонки , соответствующего Кd = 0,5, проводят по формуле:
где - свободный объем колонки, мл (объем элюции голубого декстрана), мл;
- общий объем колонки с гелем, мл (объем элюции натрия азида), мл;
0,5 - коэффициент распределения вещества на колонке.
Пересчитывают значение в мм и находят на хроматограмме:
Читайте также:


