Что такое адренергическая нервная система

Холинергические механизмы нервной системы - это вещества, которые обеспечивают передачу возбуждения в холинергическом синапсе.
Медиатор ацетилхолин (эфир холина и уксусной кислоты) образуется из аминокислоты холина и ацетил-СоА на пресинаптическом окончании нервноего волокна. Образующийся медиатор поступает в везикулы, а частично может остаться в свободном состоянии. При возбуждении медиатор выделяется из везикул. Процесс выделения медиатора С-зависим. Для нормальной работы синапса необходим запас медиатора, поэтому на пресинаптической мембране идёт ресинтез ацетилхолина. Для этого аминокислота холин выделяется из постсинаптической мембраны, частично из синаптической щели (возврат медиатора). Для образования медиатора необходима энергия метехондрий.
Фермент, способствующий синтезу ацетилхолина - ацетилхолинтрансфераза или холинацетилаза. Этот фермент образуется в теле нейрона и поступает в нервные окончания. Для нормального образования медиатора необходима целостность тела нейрона. Изолированное нервное волокно не может долго выделять медиатор.
Фермент, расщепляющий ацетилхолин - ацетилхолинэстераза. Этот фермент обладает высоким сродстворм к ацетилхолину, который находится в виде комплекса и Х-рецептором. Различают истинную ацетилхолинэстеразу (находится в синапсах и эритроцитах), которая расщепляет ацетилхолин в физиологических концентрациях и ложную ацетилхолинэстеразу (в жидкостях организма - слюне, плазме и т. д.), которая расщепляет ацетилхолин в высоких концентрациях и разрушает еще и различные производные ацетилхолина (курарекодовые препараты). Освобождённый холин с помощью переносчиков поступает на пресимпатическую мембрану, а уксусная кислота и глюкоза поступают в кровь через межтканевую жидкость.
Х-рецепторы - белковые молекулы, обладающие высоким сродством к ацетилхолину.
Существует 2 вида холинорецепторов - М и Н.
М-холинорецепторы - чувствительны к мускалину (яду мухомора) - расположены в основном во внутренних органах, эндокринных железах, сердце, сосудах, дыхательных путях, желудочнокишечном тракте. Они обладают медленным, но продолжительным действием, могут суммировать возбуждение. Существуют 2 вида М-холинорецепторов: одна - во внутренних органах, другая - в эндокринных железах. При возбуждении М-холинорецепторв происходит торможение сердечной деятельности, раширение сосудов, активация деятельности желудочно-кишечного тракта, изменяется секреция некоторых эндокринных желёз.
Н-холинорецепторы - чувствительны к никотину. Располагаются в вегетативных ганглиях, мионевральных синапсах, в хлорофильной ткани надпочечников. Эти рецепторы обладают быстрым, кратковременным действием, не могут суммировать возбуждение. Существует 3 разновидности. За счёт наличия разновидностей рецепторы могут блокироваться различными веществами. В центральной нервной системе больше Н-холинорецепторов. М-холинорецепторы преобладают в области ствола мозга, подкорковых узлах, лимбической системе, ретикулярной формации, гипоталамусе.
Адренергические механизмы нервной системы осуществляются за счет норадреналина - составляет 90 % и других катехоламинов - 10 %.
Предшественник норадреналина - изопропилнораденалин, дофамин. Для синтеза необходимы аминокислоты тиронин, фениламин, которые поступают с постсинапсической мембраны и из тела нейрона. Любые структуры могут образовывать норадреналин, но 95 % его образуется на пресимпатической мембране.
Ферменты синтеза норадреналина - трансаминазы.
Ферменты разрушения ноадреналина - группа катехоламинтрансфераз, часто моноаминоуксусная кислота и моноаминооксидант.
Адренорецепторы - белковые молекулы, обладающие сродством к норадреналину и его производным. Эти рецепторы - наружная субъединица крайней белковой молекулы, внутренняя субъединица может быть ферментом (адемилат- и гуанилатциклазы). При взаимодействии с рецептором изменяется структура молекулы белка и, как следствие, изменяется активность фермента.
Существуют 2 вида адренорецепторов:
Альфа-адренорецепторы - блокируется дегидроэрготамином, обладают повышенной чувствительностью и норадреналину, имеют низкий порог раздражения, при выделении необходимого количества медиатора возбуждаются альфа-рецепторы. Они расположены в некоторых внутренних органах и сосудистой стенке, встречается в центральной нервной системе. Различают альфа 1- и альфа 2-адренорецепторы.
Альфа 1-адренорецепторы - при их возбуждении происходит сужение сосудов, сокращение капсулы селезёнки, матки (особенно беременной), сужение зрачка и т. д. Происходит торможение желудочнокишечного тракта (моторной и секреторной), сокращение сфинктеров.
Альфа 2-адренорецепторы - в основном в центральной нервной системе.
Бетта-адренорецепторы - блокруются бетта-блокаторами (пропранолол). Они обладают высоким порогом раздражения, т. к. имеют меньшее сродство к норадреналину. Чувствительны к различным производным норадреналина (изопротеренолол).
Бетта 1-адренорецепторы - в миокарде; при их возбуждении увеличивается сила сердечных сокращений, ускоряются обменные процессы в миокарде, несколько увеличивается частота сердечных сокращений.
Бетта 2-адренорецепторы - в сосудах, внутренних органах, эндокринных железах. При их возбуждении обеспечивается тормозной эффект, расширение сосудов (коронарных, скелетных мышц), расслабление гладких мышц, дыхательных путей. В сосудах могут встречаться альфа 1- и бетта 2-рецепторы. Альфа 1-рецепторы обеспечивают сужение, а бетта 2 - расширение сосудов. Эффект зависит от: количества медиаторов, количества рецепторов данного вида.
| Предыдущая статья: | Отделы вегетативной нервной системы |
| Следующая статья: | Физиологические механизмы боли |
| Лучшая по просмотрам статья: | Высшая нервная деятельность. Сигнальные системы |
| Последняя статья: | Физиологическая сущность аппетита и жажды. Функциональная система, поддерживающая уровень питательных веществ в крови |
| Другие статьи: | Физиологические механизмы боли Проводящие пути болевой чувствительности Антиноцицептивная система. Формирование функциональных систем с участием боли Учение о медиаторах нервной системы Отделы вегетативной нервной системы Особенности вегетативной нервной системы |
Все размещенные на нашем ресурсе материалы получены из открытых источников сети Интернет и опубликованы исключительно в информационных целях. В случае получения соответствующей просьбы от правообладателей в письменном виде, материалы будут незамедлительно убраны из нашей базы. Все права на материалы принадлежат первоисточникам и/или их авторам.
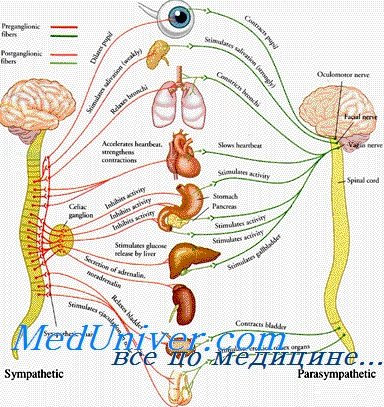
Адренергическая нервная система иннервирует многие органы, в частности:
• кишечник;
• сердце;
• легкие;
• кровеносные сосуды.
Адренергическая система иннервирует некоторые ткани (например, кишечник и мышцы дыхательных путей) через синапс в холинергическом ганглии. Это означает, что адренергическая нервная система в кишечнике и легких должна смодулировать деятельность парасимпатического холинергического ганглия. В ПНС и ЦНС найдены три тесно связанных катехоламина: норэпинефрин, эпинефрин и дофамин. Норэпинефрин — главный нейромедиатор в ПНС, а дофамин — главный нейромедиатор в ЦНС. Все три катехоламина образуются из одного предшественника — незаменимой аминокислоты тирозина. Тирозин запускает каскад ферментов в адренергических окончаниях нерва. Синтез останавливается в норадренергических нейронах на НЭ, а в дофаминергических нейронах — на дофамине. Очень небольшое количество тирозина метаболизируется в нейронах до N-метилированного продукта НЭ — эпинефрина. Эпинефрин образуется и в надпочечнике, который является специализированным нервным узлом ВНС, расположенным над почкой. Внешняя часть (кора) железы вовлечена в синтез стероидных гормонов (глюкокортикостероидов и минералокортикостероидов), а в центре железы синтезируется эпинефрин. Высокие концентрации кортизола активизируют экспрессию фениэтаноламин-N-метилтрансферазы — фермента, катализирующего превращение НЭ в эпинефрин.
Надпочечник — эффективный высокоспециализированный симпатический нервный узел. Надпочечник — нервный узел с остаточным пост-ганглионарным нейроном. Возбуждение никотиновых рецепторов в надпочечнике заканчивается высвобождением эпинефрина непосредственно в надпочечниковые вены и затем в верхнюю полую вену, откуда он достигает сердца и распределяется по организму. Эпинефрин, высвобожденный таким образом, скорее циркулирующий гормон, чем нейромедиатор.
Образование эпинефрина, норэпинефрина и дофамина инициируется одним и тем же энзиматическим каскадом. Тирозин последовательно гидроксилируется и де-карбоксилируется для выработки дофамина. Процесс может остановиться или продолжиться с последующим гидроксилированием и метилированием для образования НЭ. Дальнейшее метилирование НЭ в надпочечниках заканчивается образованием эпинефрина.
Процессы высвобождения для норэпинефрина, эпинефрина и дофамина из везикул подобны таковому для ацетилхолина. После того как НЭ, эпинефрин и дофамин упакованы в везикулы, они комплексируются с АТФ и специальным везикулярным белком. Выброс содержимого таких везикул — точно такой же процесс, как и у ацетилхолина. Потенциал действия в постганглионарном нерве заканчивается открытием Са2+-каналов N-типа и входящим в клетку потоком внутриклеточного Са2+. Увеличение Са2+ в нейроне приводит к мобилизации везикул, которые соединяются с мембраной окончания нерва. В результате высвобожденный НЭ диффундирует через синаптическую щель, чтобы связаться с постсинаптическими адренорецепторами. Использование этих лекарств обсуждается в последующих главах.
У НЭ, как и у АХ, есть высокоэффективная система для многократного использования.
После воздействия норэпинефрина на постсинаптический рецептор:
• часть норэпинефрина диффундирует через синаптическую щель;
• некоторая часть норэпинефрина действует на пресинаптические рецепторы на постганглионарных окончаниях нерва, что блокирует высвобождение еще большего количества НЭ. Пресинаптический рецептор для НЭ — подтип альфа2;
• большая часть НЭ возвращается в нервное окончание путем специального процесса, использующего транспортер НЭ в мембране клетки. Этот транспортер захватывает НЭ обратно в окончание нерва, где медиатор метаболизируется ферментом моноаминоксидазой, расположенной на митохондриях, или повторно упаковывается в везикулы.
Таким образом, как и в случае с ацетилхолином, имеется высокоэффективная система для многократного использования нейромедиатора.
Затем норэпинефрин, выходящий из синаптической щели, попадает в другие системы метаболизма, не менее важные, чем обратный захват:
• метаболизм норэпинефрина ферментом катехол-О-метилтрансферазой;
• обратный захват норэпинефрина, осуществляемый двумя способами.
Обратный захват 1 является физиологически важной системой, которая гарантирует, что нейро-медиатор используется эффективно и что время его пребывания в синаптической щели ограничено. Обратный захват 2 имеет сомнительную физиологическую значимость. Главное действие некоторых препаратов — блокада процесса обратного захвата 1. Эти лекарства известны как ингибиторы обратного захвата 1. Ингибирование обратного захвата 1 вызывает комплекс эффектов, соответствующих возбуждению симпатической нервной системы.
Ввиду чрезвычайной важности адренергической нервной системы для стимуляции сократимости здорового миокарда ее активность изучали у больных с застойной сердечной недостаточностью. Активность этой системы в покое и при физической нагрузке оценивали по концентрации норадреналина в артериальной крови. У здоровых лиц при физической нагрузке происходит относительно небольшое повышение уровней норадреналина. У больных же с сердечной недостаточностью уровни циркулирующего норадреналина даже в покое могут быть заметно повышены. Причем прогноз заболевания тем хуже, чем выше концентрации нейротрансмиттера. Кроме того, у больных с застойной сердечной недостаточностью при физической нагрузке содержание норадреналина в крови повышается в значительно большей степени, чем у здоровых людей. Это также объясняют существенно более высокой активностью адренергической нервной системы v данной группы больных, которая сохраняется и во время физической нагрузки.
Важность повышения активности адренергической нервной системы для поддержания сократимости желудочков в условиях угнетения функции миокарда при застойной сердечной недостаточности подтверждается данными о том, что блокада b-адренорецепторов может усугубить нарушение насосной функции. Таким образом, адренергическая нервная система играет важную модулирующую роль в поддержании кровообращения у больных с застойной сердечной недостаточностью. В связи с этим следует с большой осторожностью использовать антиадренергические препараты, в частности b-адреноблокаторы, при лечении больных с ограниченным резервом миокарда (гл. 182).
В то же. время концентрация и содержание норадреналина в тканях сердца у больных с сердечной недостаточностью понижены, составляя в ряде случаев лишь 10 % от нормальных значений. Механизм, лежащий в основе этого явления, полностью неизвестен. Однако считают, что длительное сохранение высокого тонуса симпатических нервов сердца играет решающую роль, вмешиваясь определенным образом в биосинтез норадреналина. Кроме того, имеются доказательства, что при хронической тяжелой сердечной недостаточности плотность b-адренорецепторов в сердце и концентрация циклической АМФ в миокарде существенно понижены.
Учитывая мощный положительный инотропный эффект норадреналина, выделяемого этими нервами, адренергическую нервную систему можно рассматривать в качестве важного потенциального источника поддержания функции страдающего миокарда. Однако увеличение частоты и силы сердечных сокращений у животных с экспериментальной сердечной недостаточностью и истощением запасов норадреналина в сердце практически отсутствует или выражено минимально при стимуляции симпатических нервов сердца. Таким образом, складывается впечатление, что в тех случаях, когда застойная сердечная недостаточность сопровождается истощением запасов норадреналина в сердце, количество его, выделяемое симпатическими нервными окончаниями в сердце, мало по отношению к той импульсации, которая передается по этим нервам. Более того, даже выделившийся норадреналин не может оказать на миокард должного воздействия вследствие угнетения эффективного адренергического механизма миокарда.
В то же время наличие запасов норадреналина в миокарде не является обязательным условием поддержания его сократимости. Однако, поскольку уменьшение запасов норадреналина в миокарде при сердечной недостаточности сочетается со снижением выброса этого нейротрансмиттера, можно предположить, что указанное истощение последнего лежит в основе утраты такой необходимой адренергической поддержки нарушенной функции миокарда. На более поздних стадиях сердечной недостаточности, когда уровни циркулирующих катехоламинов повышены, а содержание норадреналина в миокарде понижено, миокард становится во многом зависимым от более генерализованной адренергической стимуляции, исходящей из внекардиальных источников, главным образом из мозгового вещества надпочечников. Данный факт объясняет ухудшение деятельности сердца, возникающее у больных с сердечной недостаточностью, получающих b-адреноблокаторы. Это генерализованная адренергическая стимуляция, являющаяся результатом циркуляции большого количества катехоламинов в крови, может, однако, оказывать и неблагоприятные побочные эффекты, связанные с повышением сосудистого сопротивления, а следовательно, и постнагрузки, которая значительно превышает оптимальные значения.
Заключая анализ механизмов сердечной недостаточности, следует отметить, что основные нарушения кроются в угнетении взаимоотношений силы и скорости сердечных сокращений и сдвиге кривой длина — активное напряжение сердечных волокон. Это отражает уменьшение сократимости миокарда (см. рис. 181-6, кривые 1, 3). Во многих случаях сердечный выброс и внешняя работа желудочков у этих больных в покое сохраняются в пределах нормы, что, однако, обеспечивается только лишь за счет увеличения конечно-диастолической длины мышечных волокон и повышения конечно-диастолического объема желудочка, т. е. за счет механизма Франка — Старлинга (см. рис. 181-6, точки А—Г). Повышение преднагрузки левого желудочка сопровождается аналогичными изменениями давления в легочных капиллярах, вызывая одышку у больных с сердечной нeдостаточностью. Сократительная способность миокарда вследствие повышенной симпатической активности при физической нагрузке у больных с тяжелой сердечной недостаточностью не возрастает или возрастает в незначительной степени, что обусловлено истощением запасов норадреналина в миокарде (см. рис. 181-6, кривые 3 и 3). Механизмы, поддерживающие наполнение желудочков кровью во время физической нагрузки у здоровых лиц, приводят к дальнейшему ухудшению функции миокарда при его недостаточности, в результате уплощается кривая длина — активное напряжение волокон. И несмотря на то, что левый желудочек после их включения может несколько улучшить свою деятельность, этот эффект достигается исключительно благодаря чрезмерному повышению конечно-диастолического объема и давления левого желудочка, а следовательно, и давления в легочных капиллярах. Последний фактор ведет к усилению одышки, которая в свою очередь играет важную роль в ограничении интенсивности выполняемой пациентом физической нагрузки. Левожелудочковая недостаточность становится необратимой, когда кривая длина — активное напряжение мышечных волокон угнетается настолько, что сердечная деятельность не способна удовлетворить метаболические потребности периферических тканей в покое (см. рис. 181-6, кривая 4), и/или конечно-диастолическое давление в левом желудочке и давление в легочных капиллярах повышается в такой степени, что приводит к развитию отека легких (см. рис. 181-6, точка Д).
Адренергическая нервная система играет важную роль при различного рода опасных или стрессовых ситуациях, когда организм вынужден защищаться . При этом мы может отметить наиболее яркие эффекты: усиление, учащение работы сердца, повышение артериального давления, отмечается вазоконстрикция, усиливаются гликолитические процессы то есть повышается сахар, расширяются зрачки и т.д. Таким образом наблюдаются реакции направленные на преодоление опасной ситуации или стресса. В настоящее время установлено, что медиатором симпатических нервных волокон является норадреналин и лишь в 3-5% выделяется адреналин. С другой стороны мозговой слой надпочечников выделяет до 90% адреналина, а около 10% норадреналина. Адреналин и норадреналин называют катехоламинами. Принципиальной важно в практическом отношении , как синтезируются катехоламины. Исходным продуктом для биосинтеза катехоламинов является фенилаланин и тирозин. Фенилаланин гидроксилируется, превращаясь в тирозин. Следующий продукт диоксифенилаланин ( ДОФА) декарбоксилируется образуя дофамин. Следующие продукт — норадреналин и адреналин, и наконец изопропилнорадреналин. Биосинтез катехоламинов до дофамина происходит преимущественно в центральной нервной системе, в частности в substantia nigra . При недостатке дофамина ( может наблюдаться у лиц старческого возраста) развивается болезнь Паркинсона, бывает также лекарственный паркинсонизм ( при длительном применении аминазина). Норадреналин синтезируется в окончаниях симпатических нервных волокон, он является регулятором тонуса сосудов, а значит он регулирует кровяное давление. При избытке норадреналина наблюдается повышение давления. Адреналин синтезируется в мозговом веществе надпочечников, а он не является медиатором, так как для каждого медиатора существует специфический рецептор, а адреналин выбрасывается непосредственно в кровь, поэтому и является гормонов. Адреналин обеспечивает трофические процессы , влияет на углеводный обмен, на работу сердца и т.п. это зависит от того какую структур он возбуждает альфа1, альфа2 или бета1 и бета2 рецепторы. Изопропилнорадреналин расширяет бронхи поэтому на базе этого медиатора были синтезированы вещества расширяющие бронхи ( изадрин, солутан, сальбутамол). Норадреналин находится в нервных окончаниях в виде 3-х фракций:
· Стабильная фракция (депонированная) — прочно связанная с АТФ.
· Лабильная фракция, связанная с белком непрочно.
Между фракциями существуют динамическое равновесие: при использовании одной из них пополнение идет за счет двух других. Импульс идущий по симпатическим нервных волокнам возбуждает затравочную порцию ацетилхолина, которая приводит к повышению проницаемости клеточной мембраны, благодаря чему в клетку устремляется ионы кальция. Ионы кальция являются модуляторами адренергической передачи, а с другой стороны увеличение проницаемости способствует выделению медиаторы в симпатическую щель, выделяется свободная фракция, пополнение в нее идет за счет лабильной, а в нее из стабильной, а в стабильную за счет синтеза норадреналина. Синтез продолжается 12 дней. Часть выделенного медиатора вступает в связь с биохимическими структурами, с тем чтобы импульс перешел на исполнительный орган, вторая часть возвращается на пресинаптическую мембрану и депонируется там, третья взаимодействует с ферментами — моноаминооксидазой и катехолметилтрансферазой — это ферменты, ингибирующие медиатор, разрушающие его . Часть медиатором через кровеносное русло попадает в печень где происходит и разрушение с образованием сложных эфиров серной и глюкуроновой кислот. И наконец еще одна часть медиатора разрушается с образованием адренохрома и адренолитина.
Адренорецепторы . Различают 2 типа адренорецепторов: альфа ( делятся на 1 и 2), и бета , которые также делятся на 1 и 2. Альфа1адренергические системы воспринимают возбуждающие импульсы по отношению к сосуду наблюдается вазоконстрикция, бета2 адренергические рецепторы — тормозные ( при этом наблюдается расширение сосудов).
Локализация альфа1адренреактивных систем: периферические сосуды кожи, слизистых, почек, скелетных мышц, органов брюшной полости, трабекулах селезенки.
Альфа2тормозные рецепторы находятся на пресинаптических мембранах, бета1адренорецепторы находятся в миокарде, при их возбуждении отмечается усиление и учащение сердечной деятельности, повышается сердечный выброс, возбудимости миокарда, но при этом увеличивается потребность миокарда в кислороде. Бета-рецепторы локализованы в: сосудах жизненноважных органов: мозга, сердца, скелетных мышц, в бронхах. Бета2адренорецепторы выполняют тормозную функцию: бронхи расширяются, происходит угнетение сократительной способности матки, ( поэтому бета-адреномиметики применяются в акушерской практике как токолитики), при возбуждение бета-адренорецепторов наблюдается усиление гликогенолиза и гликолиза.
Препараты стимулирующие бета1 адренорецепторы стимулируют и бета2адренорецепторы поэтому при их применении может быть учащение ритма сердца и др. эффекты со стороны миокарда в качестве побочного действия.
к препаратам непрямого действия относятся: эфедрин гидрохлорид, фенамин, сиднофен.
Антиадренергические средства делятся на 3 группы: средства , блокирующие альфа-адренорецепторы, бета-адренорецепторы и вместе альфа и бетаадренорецепторы.
АЛЬФА1АДРЕНОМИМЕТИКИ. Типичным представителем этого ряд является норадреналина гидротартрат. Подобно медиатору он оказывает прямое возбуждающее действие на альфа1 адренорецепторы, что приводит к вазоконстрикции и повышению давления. Однако при подкожной или внутримышечной инъекции он вызывает сильнейшую вазоконстрикцию в мест инъекции что приводит к некрозу, поэтому норадреналина гидротартрат вливают в литре изотонического раствора ( в глюкозе) — допускается 0.1% или 0.2% растворы. Таким образом норадреналин применяют для немедленного повышения кровяного давления при значительном его снижении ( травматический шок, отравления ганглиоблокаторами, сосудистой коллапсе и т.п.). К препаратам этого ряда принадлежат мезатон, фетанол, они значительно хуже подвергаются инактивации в организме , поэтому их можно применять и подкожно и внутримышечно и внутривенно и даже в таблетках. Для местного применения используются санорин, нафтизин которые сужая сосуды уменьшают отек слизистой носа при ринитах.
АЛЬФА2АДРЕНОМИМЕТИКИ. Сюда относится клофелин. У этого препарата 2 мишени:
· альфа2рецепторы сосудодвигательного центра,
· окончания симпатических нервов.
Возбуждая альфа2адренорецепторы гипоталамуса уменьшается поток сосудосуживающих импульсов , усиливается депрессорное влияние. Возбуждая альфа2адренорецепторы на пресинаптических мембранах в нервных окончаниях препарат тормозит выделение медиаторов, использование обоих этих эффектов позволяет применять препарат не только для лечения гипертонической болезни , но и для купирования кризов. Если препарат используется для купирования криза, необходимо разбавить ампулу в 20 мл изотонического раствора так как при передозировке ( если забыли разбавить) клофелин проявляет миметическое действие. Препарат потенциирует действие снотворных , наркотиков, алкоголя.
БЕТААДРЕНОМИМЕТИКИ. Наибольшую ценность среди бета-адреномиметиков представляют вещества, которые действуют на уровне сосудов жизненноважных органов, на уровне бронхов и на уровне матки. Типичным бронхолитиком является изадрин, сюда же относятся сальбутамол , солутан, и др. Эти препараты возбуждая бета2-адренорецепторы бронхов расширяют бронхи. Изадрин применяют в виде таблеток для рассасывания и 0.5% раствор для ингаляций.
Препараты возбуждающие и бета — и альфа-адренорецепторы. К альфа и бета адренорецепторами относится адреналина гидрохлорид. Это неустойчивое соединение , поэтому его действие выраженное, но кратковременное. При внутривенной инъекции наблюдается повышение уровня кровяного давления ( в физиологической концентрации адреналин возбуждает только бета1 и бета2 адренорецепторы). Наблюдается учащение работы сердца, расширение сосудов мозга, сердца, почек , мышц , расширение бронхов, токолитическое действие на матку и усиление гликолитических процессов. При увеличении концентрации адреналин начинает действовать и на альфа-2 адренорецепторы, оказывая вазоконстрикторное действие. При применении адреналина усиливается распад гликогена, в крови повышается содержание сахара и молочной кислоты. Адреналин снимает утомление скелетных мышц. Сосудосуживающий эффект адреналина проявляется особенно при его местном действии на ткани. Адреналин угнетает моторику и секрецию желудочно-кишечного тракта, но этот эффект значительно слабее эффекта м-холинолитиков. Адреналин применяют при бронхиальной астме — подкожная инъекция до 0.5 мл 0.1% растворе широко применяет с этой целью, при гипогликемических состояниях ( передозировка инсулином). При различных аллергических состояниях ( чтобы не было отека, анафилактической шоке — адреналин является антагонистом гистамина), применяется адреналин для остановки сердца 0.5-0.7 мл вливают в левый желудочек) , для остановки поверхностного кровотечения, для уменьшения токсичности и удлинения действия местных анестетиков ( в раствор новокаина добавляют несколько капель адреналина, происходит спазм сосудов в месте введения анестезии и новокаин дольше действует).
Непрямые адреномиметики. Механизм действия — под влиянием непрямых адреномиметиков облегчается выброс медиатора связанного с белком, непрямые адреномиметики тормозят возврат медиатора и пресинаптической мембране, повышают чувствительность рецепторов к медиатору, ингибируют моноаминооксидазу (МАО), разрушающую медиатор, оказывают прежде возбуждающее действие на рецепторы. При использовании адреномиметиков непрямого типа действия в синаптической мембране накапливается медиатор — норадреналин, который проникает через гематоэнцефалический барьер и оказывает выраженное возбуждающее действие на сосудодвигательный центр. Однако при частом применении препаратов этого ряда наблюдается снижение и даже полное отсутствие эффекта в связи с опустошением пресинаптической мембраны ( нет медиатора, нужно ждать 12 дней, пока не синтезируется еще медиатор). Показания — гипотония, бронхиальная астма, коллапс, аллергические риниты, отравления, сопровождающиеся понижением уровня АД. Эфедрин вводят всеми путями. Сиднокарб, сиднофен обладают более выраженным действие по сравнению с эфедрином на ЦНС. При этом наблюдается уменьшение чувства утомления, улучшается и повышается настроение, работоспособность то есть это стимулятор, допинг для ЦНС. Однако у 15% испытуемых наблюдается обратный эффект. При длительном применении препаратов они вызывают тахифилаксию (истощение резервов).
Передача возбуждения с постганглионарных нервных окончаний симпатической нервной системы на клетки эффекторных органов в основном осуществляется норадреналином. Исходным продуктом биосинтеза норадреналина является незаменимая аминокислота фенилаланин, которая в печени гидроксилируется и превращается в тирозин (тирозин может поступать и с пищей). Тирозин в цитоплазме нервного окончания окисляется в диоксифенилаланин (ДОФА) и декарбоксилируется. Образующийся дофамин в некоторых структурах мозга, например, в экстрапирамидной системе, является медиатором. С помощью особой транспортной системы дофамин переносится в везикулу, где дофамин-гидроксилаза превращает его в норадреналин.
В нервном окончании имеются три фракции норадреналина: лабильный фонд, который выбрасывается из везикулы в цитоплазму, а затем в синаптическую щель при поступлении нервного импульса; стабильный (резервный) фонд, сохраняющийся до истощения лабильного фонда везикулы, и цитоплазматическая свободная фракция, которая состоит из норадреналина, не депонированного в везикулах (при их насыщении). Последняя пополняется также за счет молекул медиатора, реабсорбированных из синаптической щели ("обратный захват").
В нервных окончаниях биосинтез заканчивается норадреналином. Хромаффинные клетки надпочечников метилируют норадреналин, превращая в адреналин.
Адреналин, норадреналин, дофамин и другие аналогичные амины, содержащие в бензольном кольце оксигруппу в положениях 3, 4, носят название катехоламинов ("катехол" - обозначает ортодиоксибензол).
Нормальное функционирование синапса во многом зависит от транспортных систем, осуществляющих перенос дофамина и норадреналина из цитоплазмы в везикулу и обратный (или нейрональный) захват норадреналина (около 70%) адренергическими окончаниями из синаптической щели.
В цитоплазме нервного окончания норадреналин разрушается (дезаминируется) моноаминоксидазой (МАО), кроме фракции, депонированной в везикулах, в синаптической щели - катехолометилтрансферазой (КОМТ). Последняя разрушает также катехоламины, циркулирующие в крови.
Локализация, типы и функции адренорецепторов. Адренорецепторы расположены частично в клетках эффекторных органов, иннервируемых постганглионарными волокнами симпатической нервной системы, а частично - вне синапсов. Различают ( a и b -адренорецепторы, каждый из которых имеет 2 типа - a 1, a 2 и b 1, b 2:
a 1-адренорецепторы локализованы в постсинаптических мембранах;
a 2-адренорецепторы - расположены пресинаптически в ЦНС и на адренергических окончаниях, а также внесинаптически в стенке сосудов.
a 1-адренорецепторы широко представлены:
1) в сосудах; их возбуждение суживает сосуды кожи, слизистых оболочек, брюшной полости и повышает артериальное давление;
2) в радиальной мышце радужной оболочки глаза; при их активации мышца сокращается и зрачок расширяется, но внутриглазное давление не повышается;
3) в желудочно-кишечном тракте - возбуждение этих рецепторов снижает тонус и моторику кишечника, но усиливает сокращение сфинктеров;
4) в гладкой мускулатуре дистальных отделов бронхов; стимуляция a 1-рецепторов этой области ведет к сокращению просвета дистальных отделов дыхательных путей.
a 2-Адренорецепторы по механизму обратной отрицательной связи регулируют выброс норадреналина; при возбуждении центральных пресинаптических a 2-адренорецепторов угнетается сосудо-двигательный центр и снижается артериальное давление; активация периферических пресинаптических a 2-адренорецепторов тормозит выделение норадреналина в синаптическую щель, что приводит к падению артериального давления. Внесинаптические a 2- адренорецепторы локализуются во внутреннем слое сосудов и возбуждаются адреналином, циркулирующим в крови; сосуды при этом суживаются и артериальное давление повышается.
Постсинаптические b 1-адренорецепторы локализуются в мышце сердца. Их возбуждение повышает все функции сердца: автоматизм, проводимость, возбудимость, сократимость. Увеличивается частота (тахикардия) и сила сердечных сокращений, возрастает потребление кислорода миокардом. При угнетении b 1-адренорецепторов развиваются противоположные эффекты: брадикардия, снижается сократимость. сердечный выброс и потребность сердца в кислороде. Постсинаптические b 2-адренорецепторы характерны для мышц бронхов, сосудов скелетной мускулатуры, миометрия. Возбуждение b 2-адренорецепторов бронхов приводит к их расширению. Механизм этого эффекта следующий: стимуляция b 2-адренорецепторов активирует аденилатциклазу, накапливается цАМФ, связывающий свободный кальций, снижение уровня кальция приводит к расслаблению бронхиальных мышц. Нечто подобное происходит и в тучной клетке (связывание кальция цАМФ и блок мембраны), вследствие чего тормозится высвобождение медиаторов аллергии (гистамина, серотонина, медленно реагирующей субстанции анафилаксии - ЛД4 и др.). Возбуждение b 2-адренорецепторов лежит в основе расширения сосудов (расслабление гладкомышечного слоя) скелетной мускулатуры, сердца, мозга, печени. Механизм положительной обратной связи реализуется пресинаптическими b 2-адренорецепторами: их возбуждение повышает выброс норадреналина.
Адренергические средства по аналогии с холинергическими разделяют на миметики и блокаторы.
Читайте также:


