Ишемия головного мозга и болезнь паркинсона
Общие сведения
Мозг нуждается в большем потреблении кислорода, чем другие органы. Особенностью его метаболизма является интенсивный обмен. При хроническом ухудшении кровоснабжения замедляется мозговой кровоток, уменьшается содержание кислорода и глюкозы, происходит сдвиг метаболизма (анаэробный гликолиз, лактатацидоз), появляется стаз капиллярной крови и склонность к тромбообразованию, вырабатываются нейротоксины. Все эти процессы приводят к гибели клеток. При хронической ишемии диагностируются поражение белого вещества полушарий и нарушается связь лобных долей и подкорки (феномен разобщения). Эти патологические изменения при отсутствии лечения приводят к сосудистой деменции.
Именно нарастание интеллектуально-мнестического дефицита характерно для хронической ишемии мозга. Если при ранних проявлениях заболевания у больных появляется тревога и депрессия, то хроническая ишемия мозга 2 степени из-за развития деменции характеризуется дезадаптацией больного в среде (социальной и бытовой). Устранение гипоксии, улучшение микроциркуляции и метаболизма уменьшает выраженность клинических симптомов и сохраняет мозговую ткань.
Патогенез
В основе хронической ишемии мозга лежат изменения структуры сосудистой стенки, возникающие при атеросклерозе или артериальной гипертензии. Липогиалиноз сосудов (дистрофические изменения сосудов в виде отложения гиалина и липопротеидов) небольшого калибра приводит к хронической ишемии белого вещества, в котором определяются очаговые (лейкоареоз) и диффузные изменения.
Эндотелий сосудов — это важный фактор, который регулирует сосудистый тонус. Эндотелиальные клетки синтезирует антиатеросклеротические вещества (например, оксид азота). На ранних стадиях повреждения эндотелиальных клеток развиваются функция эндотелия. Прежде всего, нарушается доступность оксида азота и уменьшается степень расширения сосудов. В клетках мозга развивается окислительный стресс — накапливаются в большом количестве активные формы кислорода. Даже если синтез оксида азота нормальный, то при окислительном стрессе он быстро инактивируется.
Оксидантный стресс играет основную роль в поражении нейронов мозга, поскольку в клетках накапливаются недоокисленные продукты обмена, расширяются кальциевые каналы и происходит поступление кальция в клетки. Это приводит к снижению активности нейронов головного мозга, что ухудшает мозговой метаболизм.
Таким образом, механизмы хронической ишемии мозга включают:
- снижение кровотока;
- нарастание глутаматной токсичности;
- накопление кальция в клетках мозга;
- развитие лактатацидоза;
- активация внутриклеточных ферментов;
- прогрессирование антиоксидантного стресса;
- подавление белковых процессов в клетках и снижение энергетических процессов.
Первое время механизмы компенсации нарушенного мозгового кровообращения сдерживают появление клинических симптомов. При хорошо развитом коллатеральном кровообращении возможна хорошая компенсация. И наоборот, индивидуальные особенности строения сосудов становятся причиной декомпенсации. Со временем в условиях плохого снабжения мозга кислородом механизмы компенсации истощаются, недостаточным становится обеспечение мозга питанием и энергией и развиваются функциональные, а потом и необратимые изменения мозга в виде ишемических очагов.
Результатом сочетанных нарушений при хронической ишемии является симптомокомплекс, включающий когнитивные расстройства. При прогрессировании заболевания развиваются церебральные сосудистые кризы, присоединяются двигательные расстройства и выраженное ослабление памяти.
Классификация
Острые нарушения мозгового кровообращения:
- Инсульт (ишемический, геморрагический).
- Транзиторные ишемические атаки.
- Церебральные кризы.
Хронические нарушения кровообращения мозга:
По клиническому синдрому выделяются:
- Диффузная цереброваскулярная недостаточность.
- Поражение сосудов каротидной системы.
- Поражение вертебрально-базилярной системы кровообращения.
- Вегетососудистые пароксизмы.
- Психические расстройства.
По этиологическим причинам:
- Атеросклеротическая энцефалопатия.
- Гипертоническая.
- Венозная.
- Смешанная.
- Начальные проявления.
- Стадия субкомпенсациии.
- Стадия декомпенсации.
Церебральная ишемия 1 степени — это компенсированная стадия с начальными проявлениями. У больного появляется слабость, утомляемость, головная боль, незначительное снижение памяти и внимания, замедленность движений. При 1 степени ишемии отмечаются минимальные поражения головного мозга, выявляемые инструментальными методами.
Церебральная ишемия 2 степени — это субкомпенсированная стадия. Ишемия головного мозга 2 степени протекает с ухудшением памяти, депрессивными расстройствами, психическим истощением, неустойчивостью при ходьбе. Отмечаются признаки недостаточности кровоснабжения в отдельных сосудистых бассейнах. Самым важным является то, что для 2 степени характерно органическое поражение ЦНС (лейкоареоз).
Ишемия третьей степени — декомпенсированная стадия. Наблюдаются расстройства чувствительности, речи, параличи, ослабление мимики, мышечная слабость, утрата работоспособности, психическая деградация. Могут нарушаться функции тазовых органов.
Причины
Наиболее частыми причинами, вызывающими хроническую ишемию, являются:
Реже нарушения мозгового кровообращения развиваются при посттравматическом расслоении позвоночных артерий, патологии позвоночника, врожденных деформациях артерий, васкулитах. Чаще всего хроническая ишемия развивается у пожилых лиц, страдающих сердечно-сосудистыми заболеваниями.
Факторами риска данного заболевания являются:
- Пожилой возраст.
- Наследственная предрасположенность.
- Пол.
- Ожирение.
- Нерациональное питание.
- Недостаточная физическая нагрузка.
Симптомы ишемии головного мозга
Хроническая ишемическая болезнь головного мозга по выраженности проявлений делится на три стадии. Симптомы ишемии сосудов головного мозга разнообразны на разных стадиях. Если в начальных стадиях отмечаются астенические, тревожно-депрессивные и астено-депрессивные нарушения, то во второй в третьей стадии присоединяются выраженные интеллектуальные расстройства, которые характерны для сосудистой деменции. В начальных стадиях симптомы возникают при значительном эмоциональном и умственном напряжении, которые требуют усиления мозгового кровообращения.
В первой стадии начальных проявлений преобладают субъективные расстройства: непостоянные головные боли, тяжесть в голове, головокружения, слабость, эмоциональная лабильность, раздражительность, нарушения сна, снижение внимания, легкие расстройства памяти. В этой стадии не формируются неврологические синдромы за исключением астенического. При правильном лечении уменьшается выраженность или устраняются отдельные симптомы.
При 2-й стадии субкомпенсации чаще отмечаются нарушения памяти, неустойчивость при ходьбе, частые головокружения, реже отмечается астенический синдром. Усиливаются мнестико-интеллектуальные нарушения.
Для второй стадии характерны неврологические синдромы:
- Когнитивных расстройств, которые переходят в сосудистую деменцию.
- Псевдобульбарный. При этом страдают: артикуляция (речь), фонация (осиплость голоса), глотание и жевание.
Больные принимают пищу медленно и постоянно поперхиваются при глотании, поскольку жидкая пища попадает в нос. Часто наблюдаются приступы непроизвольного смеха или плача, возникающие вследствие насильственного сокращения мимических мышц.
- Атактический. Двигательная дисфункция, выражающаяся в изменении походки и ухудшении координации.
- Пирамидной недостаточности с легкими моно-и гемипарезами. При этом нарушается походка, отмечается скандированная речь и интенционное дрожание (дрожание конечностей).
- Неврологические расстройства мочеиспускания.
- Экстрапирамидные расстройства (гипокинезия или легкое повышение мышечного тонуса).
- Синдром паркинсонизма. В отличие от болезни Паркинсона отмечается преимущественное вовлечение ног, отсутствие тремора покоя, развитие постуральной неустойчивости (невозможность удерживать равновесие или при изменении позы) и деменции.
Признаки в 3-й стадии (декомпенсации) более выражены. Выявляются вышеперечисленные неврологические синдромы, которые имеют устойчивый характер и прогрессируют. У больных отмечаются выраженные когнитивные дисфункции:
- нарушение внимания;
- расстройства всех видов памяти (долговременной, кратковременной и ассоциативной);
- затруднения в профессиональной деятельности;
- присоединение апрактико-агностических симптомов (неспособность выполнять целенаправленные движения и нарушение зрительного, тактильного и слухового восприятия) и нарушений речи.
Для лиц пожилого возраста характерной становится эмоциональная лабильность — быстрая и беспричинная смена настроения, раздражительность и плаксивость. Отмечается замедленность мышления, трудности с переключением на другой вид деятельности. Изменяется поведение пациентов: повышенная импульсивность, снижается способность к самокритике, появляется пренебрежение правилами поведения, принятыми в обществе.
С прогрессированием процесса присоединяются нарушения праксиса (отсутствие координированного и контролированного действия) и гнозиса (нарушения узнавания, в результате которого ранее знакомый окружающий мир, становится чуждым и непонятным). Все это значительно снижает социальную адаптацию пожилых пациентов.
Анализы и диагностика
Помимо сбора анамнеза и осмотра больного необходимо инструментальное подтверждение диагноза, которое включает:
- УЗ-допплерография сосудов головы и шеи.
- Магнитно-резонансная ангиография.
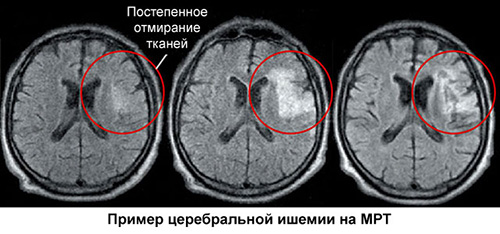
- Магнитно-резонансная томография.
- Компьютерная томография, которая позволяет выявить очаговые изменения в мозге.
- Офтальмоскопия с исследованием глазного дна. Часто определяются застойные явления или отек зрительного нерва, изменения сосудов глазного дна. Периметрия определяет границы полей зрения и области выпадения полей зрения.
- ЭКГ для выявления патологии ССС.
- Биохимические исследования крови.
- При диагностике когнитивных нарушений обязательно проводится нейропсихологическое тестирование.
Метод ультразвуковой доплерографии позволяет выявить атеросклеротические бляшки сонной артерии и дифференцировать их по эхогенности. Это дает возможность оценить их морфологическиое строение. По эхоплотности различают гипо-, гиперэхогенные и промежуточные бляшки сосудов. Также при УЗ-доплерографии выявляют стеноз внутричерепных артерий, нарушение их геометрии или спазм мозговых сосудов. К методам исследования сосудов головы и шеи относится также метод цветового дуплексного сканирования (ЦДК) и триплексное сканирование.

УЗ-допплерография сосудов головы и шеи
Лечение ишемии головного мозга
В процессе лечения ишемии сосудов головного мозга добиваются нормализации мозгового кровообращения, улучшения текучести крови и метаболизма в мозговой ткани. Фармакологическая коррекция направлена на основные звенья патогенеза, поэтому 40% больных получают как минимум три лекарственных препарата. Основными препаратами являются:
- Вазоактивные средства.
- Антиагреганты.
- Средства нейрометаболического действия.
Кроме того, важно воздействовать на имеющиеся факторы риска — атеросклероз и артериальная гипертензия. В итоге лечение ишемической болезни головного мозга в обязательном порядке предусматривает:
Метаболические препараты также оказывают ноотропный эффект. Из этой группы препаратов можно назвать Церебролизин, Цитофлавин и Актовегин. Последний уменьшает нарушение энергетического питания нейронов, улучшая метаболизм АТФ при ишемии/гипоксии. Цитофлавин — нейропротектор, антигипоксант и антиоксидант. В его составе: янтарная кислота, рибоксин, никотинамид и рибофлавин. Он замедляет реакции промежуточного обмена при гипоксии мозга, вызванной разными причинами.
Оправданным и целесообразным считается сочетанное применение вазоактивных препаратов и проведение метаболической терапии. Вазоактивные и метаболического действия препараты принимаются курсами 2 раза в год. Существуют комбинированные лекарственные формы с вазоактивным и метаболическим эффектом — Инстенон, Фезам, Винпотропил.
С учетом сопутствующей патологии в комплекс лечения лиц пожилого возраста обязательно входят:

Болезнь Паркинсона характеризуется активной гибелью нейронов, продуцирующих дофамин. Это вещество принимает участие в регулировании мышечной деятельности, поэтому его недостаток приводит к нарушениям движений – гипокинезиям, тремору, а также мышечной ригидности (патологической напряженности). Дополнительно могут развиваться когнитивные симптомы. Выявить болезнь можно, собрав анамнез и обследовав мозг больного Паркинсоном. При этом отмечается ряд изменений, которые в некоторых случаях могут быть частично обратимыми.

Изменения в головном мозге
Для проверки наличия патологических изменений в головном мозге могут использоваться такие методы диагностики:
- МРТ и КТ;
- магнитно-резонансная спектроскопия;
- сонография;
- позитронно-эмиссионная томография.
В первую очередь при Паркинсоне поражается черная субстанция – часть мозга, вырабатывающая дофамин. Также страдают бледный шар и хвостатое ядро. Кроме поражений этих участков, болезнь Паркинсона на МРТ головного мозга может быть заметна врачу как нейродегенерация мозга (особенно у людей, младше 65 лет) и атрофия отдельных участков.

Внимание! На нулевой стадии болезнь заметить трудно, поэтому часто назначается повторное обследование через непродолжительное время.
Основываясь на анамнезе, болезнь Паркинсона на ранней стадии выявить очень сложно. Причина в схожести симптомов со многими другими заболеваниями, а также в длительном (порой до 5-8 лет) доклиническом периоде, когда симптомы почти не проявляются. Поэтому, в последнее время все чаще используются методы обследования мозга, позволяющие определить наличие морфологических нарушений и исключить другие заболевания, которые схожи с Паркинсоном (например, деменцию, инсульт).
Так, врач может назначить МРТ головного мозга при Паркинсоне, в ходе которого выявляется потеря объема корковых и подкорковых образований. КТ и МРТ – предпочтительные методы обследования, которые имеют высокую точность, особенно начиная с первой стадии (на нулевой выявление бывает сложным или даже невозможным) болезни. Также они безопасны, безболезненны и не вызывают негативных реакций со стороны пациента.

Болезнь Паркинсона и паркинсонизм часто ошибочно принимают за одно заболевание. На самом деле это не так. Болезнь Паркинсона развивается как первичное, самостоятельное заболевание, которое протекает медленно и не может быть полностью вылечено. Паркинсонизм – вторичное заболевание (или симптомокомплекс), причиной которого послужили определенные факторы, влияющие на мозговую деятельность: травмы, опухоли, кровоизлияния, хронические воспалительные процессы. Заболевания бывает трудно различить, собрав анамнез (особенно если паркинсонизму предшествовали незамеченные пациентом факторы), чаще всего диагноз ставиться по тому, что мозг при болезни Паркинсона имеет более тяжелые, необратимые изменения, причина которых до конца неизвестна.
Болезнь Паркинсона и инсульт
Кроме паркинсонизма, болезнь Паркинсона также часто связывают с инсультом. Причин этому несколько:
- схожесть симптомов болезней (двигательные растройства);
- предположения, что Паркинсон провоцирует инсульт;
- мнения, что инсульт вызывает дрожательный паралич.
На самом деле, Паркинсон после инсульта не развивается, но заболевание, характеризующееся мозговыми кровоизлияниями, может вызвать вторичную болезнь – паркинсонизм. Этот факт был доказан учеными еще в прошлом столетии. Наоборот же, инсульт из-за дрожательного нарушения появиться не может. Хотя известно много случаев одновременного независимого друг от друга развития этих болезней.

Как уже было сказано, инсульт может привести к нарушениям нейронов мозга и паркинсонизму. Но, несмотря на негативное влияние инсульта, именно кровоизлияния и травмы стали причиной изучения методов стимуляции мозга. Все дело в том, что в медицине описано много случаев улучшения состояния больного после инсульта. Это связанно с поражением некоторых участков (например, таламуса) и временным прекращением аномальной двигательной активности.
В XX веке, на фоне этих наблюдений было проведено много операций, которые в большинстве случаев заканчивались трагично. Ситуация изменилась с изобретением высокочастотной электростимуляции, которая применяется избирательно. Глубокая стимуляция мозга при болезни Паркинсона не разрушает участки мозга, а лишь имитирует это (стимулирует их), уменьшая, а иногда исключая тремор и ригидность.

Паркинсон и инсульт имеют схожую симптоматику, поэтому часто могут быть неправильно диагностированы. Главный симптом, который вводит в заблуждение – поражения, которые отмечаются лишь на одной стороне тела.
| Общие проявления | Отличительная симптоматика |
|---|---|
| Нарушения двигательной активности в одной половине тела | Разница в быстроте развития, нарушения на фоне Паркинсона развиваются постепенно, медленно |
| Нарушения речи | При инсульте возникают резко, при Паркинсоне – постепенно, усугубленные другими когнитивными симптомами |
| Ригидность мышц | При инсульте возникает исключительно ригидность мышц затылка, а Паркинсон характеризуется общим напряжением |

Особенно тяжело поставить правильный диагноз, если развился инсульт при болезни Паркинсона (на ее фоне). В таком случае необходима консультация сразу с несколькими профильными специалистами: терапевтом, неврологом, кардиологом, возможно – помощь реаниматолога. Возможно, единственной отличительной чертой, которую можно узнать из анамнеза, будет резкое ухудшение состояния пациента.
Стимуляция мозга
Лечение Паркинсона можно разделить на два направления: терапевтическое и нейрохирургическое. Терапевтическое лечение – это прием препаратов леводопа и других дофаминсодержащих лекарств. При этом оно может вызывать побочные эффекты: депрессию, судороги, лейкопению, рвоту. Но главной проблемой является временное действие, которое прекращается, если перестать принимать препараты, которых, с развитием болезни, нужно все больше.
Нейрохирургическое вмешательство более действенно и редко вызывает негативные последствия. Тем не менее, побочные эффекты бывают, связанны они с оборудованием или неправильно выполненным оперативным действием. В таком случае могут возникнуть кровоизлияния, судороги, эмболия легочной артерии или инфицирование из-за проблем со стерильностью.
Справка! Как показывает практика, лечение, в том числе и с помощью нейрохирургии, лучше всего проводить на ранней (первой или нулевой) стадии.

Стимуляция мозга при болезни Паркинсона выполняется по такому сценарию:
- В определенные отделы мозга имплантируются специальные электроды.
- Под кожу (например, в районе ключицы) вводится стимулятор.
- Через некоторое время (операция происходит в несколько этапов), устройство запускается.
- Стимулятор генерирует импульсы, параметры которых настраивает врач. Настройка может занять несколько недель.
- При правильной настройке происходит возбуждение нервных отростков (аксонов). Симптомы Паркинсона пропадают.
Участок, который подлежит стимуляции, выбирается специалистом после проведения обследования (МРТ и КТ) и выявления очага поражения. Это может быть промежуточное ядро таламуса, субталамическое ядро, бледный шар (внутренняя часть). Устройство может оставаться в организме 3-5 лет, после чего легко заменяется.

Таким образом, глубокая стимуляция – самый эффективный и безопасный метод лечения Паркинсона, риск осложнений от которого менее 3%. Он одобрен еще в 1997 году и широко используется в передовых клиниках мира.
Особенности стимуляции пациентов
Доказано, что электрическая стимуляция работы мозга при болезни Паркинсона по-разному действует на пациентов. Так, более восприимчивы больные, у которых от начала развития Паркинсона прошло не более 5 лет, а также те, у кого не наблюдается когнитивных расстройств. Не рекомендовано использовать нейрохирургический метод людям с III и выше стадией (по Хен-Яру) и пациентам с вторичным паркинсонизмом. Полностью исключена возможность вмешательств больным тяжелыми сердечно-сосудистыми заболеваниями, психозами, а также тем, чей возраст более 70 лет.

Видео
Сосудистый паркинсонизм — это уменьшение числа, амплитуды и скорости произвольных движений на фоне мышечной ригидности, этиопатогенетически связанное с наличием цереброваскулярной патологии. Клинически проявляется медлительностью, шаркающей походкой, постуральной неустойчивостью, гипомимией лица, склонностью к депрессии. Сосудистый генез заболевания устанавливается на основании данных УЗДГ интра- и экстракраниальных сосудов, церебральной нейровизуализации. Лечение преимущественно консервативное, состоит из базовой (сосудистой) и симптоматической (антипаркинсонической) терапии.
МКБ-10
- Причины
- Патогенез
- Классификация
- Симптомы сосудистого паркинсонизма
- Осложнения
- Диагностика
- Лечение сосудистого паркинсонизма
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Впервые предположение о наличии сосудистого фактора среди прочих причин поражения чёрной субстанции высказал в 1894 году французский невролог Бриссауд. В 1929 году американским врачом М. Критчли было представлено первое подробное описание атеросклеротического паркинсонизма. С внедрением в практическую неврологию методов нейровизуализации в России в 1997 году были разработаны клинико-нейровизуализационные критерии диагностики, модифицированные в 2004 году. Сосудистый паркинсонизм (СП) относится к редким формам вторичного паркинсонизма и составляет, по различным данным, 2-15% от всех его случаев. Патология диагностируется у 11% пациентов, перенёсших ишемический инсульт, в 14% случаев подкорковой формы ДЭП. Средний возраст больных колеблется в диапазоне 40-90 лет.

Причины
Основным этиологическим фактором развития СП выступает поражение подкорковых ганглиев, обусловленное цереброваскулярными нарушениями. Последние могут иметь острое (инсульт, лакунарный инфаркт) и хроническое (хроническая ишемия головного мозга) течение. Заболевание чаще возникает вследствие патологических изменений, происходящих в церебральных артериях на фоне хронической артериальной гипертензии. С учетом калибра поражённых сосудов выделяют две основные группы этиофакторов:
- Поражение малых церебральных артерий. Распространённая патология артериол и малых артерий наблюдается при гипертонической энцефалопатии, артериолосклерозе, амилоидозе сосудов, СКВ, антифосфолипидном синдроме. Поражение пенетрирующих сосудов, кровоснабжающих глубинные мозговые отделы, сопровождается хронической диффузной ишемией, преходящими эпизодами более выраженной ишемии (неполными инфарктами), провоцирующими патологические изменения подкорковых узлов.
- Поражение средних и крупных артерий. Встречается реже. Обусловлено тромбоэмболией ветвей средней мозговой артерии, церебральным атеросклерозом, наличием артериовенозной мальформации, ангиопатией при узелковом периартериите, церебральным васкулитом. Сосудистый паркинсонизм является следствием ишемического или геморрагического инсульта в области базальных ядер.
Патогенез
Патологические изменения малых мозговых артерий потенцируют диффузную гипоперфузию тканей. Повышенная проницаемость стенок поражённых сосудов вызывает периваскулярный отёк, отложение гемосидерина, выход белков плазмы за пределы сосудистого русла. Результатом хронической ишемии и сосудистой проницаемости является гибель подкорковых структурных элементов. Погибшие участки недостаточно замещаются астроцитами, что становится причиной спонгиоза — патологической губчатости белого вещества.
Поражение крупных ветвей и ствола средней церебральной артерии (сосудистый стеноз, окклюзия, истончение стенки) провоцирует возникновение инсульта с образованием обширного участка некроза подкорковых элементов. Таким образом, сосудистый фактор приводит к гибели дофаминпродуцирующих нейронов, дисметаболизму дофамина, повреждению дофаминовых рецепторов. Преобладание ацетилхолиновых активирующих воздействий на тормозящее моторику хвостатое ядро ведёт к гипокинезии, развивается паркинсонизм.
Классификация
Сосудистый паркинсонизм имеет вариабельную клиническую картину, может сочетаться с иными неврологическими симптомами, связанными с гемодинамическими изменениями, вторичными дегенеративными процессами. Указанные факторы обуславливают определённые диагностические трудности. Разобраться в многообразии клинической симптоматики помогает выявление характерных особенностей течения СП. В соответствии с данным критерием выделяют три варианта:
- Острый/подострый. Характерна внезапная либо быстро развивающаяся манифестация симптомов. В последующем наблюдается стабилизация течения, возможен определённый регресс симптоматики.
- Ступенеобразно прогрессирующий. Клиника разворачивается постепенно. Период прогрессирования чередуется со стабилизацией и частичным регрессом проявлений.
- Неуклонно прогрессирующий. Наблюдается наиболее редко. Типично непрерывное нарастание выраженности симптомов, периоды стабилизации отсутствуют. Аналогичное течение типично для первично-дегенеративных заболеваний ЦНС, что затрудняет проведение дифдиагностики.
Особенности течения заболевания в значительной мере коррелируют с характером цереброваскулярной патологии. Понимание этиологии возникновения СП имеет определяющее значение для адекватного планирования лечебных мероприятий. В связи с этим целесообразно выделение следующих двух форм:
- Постинсультная. Наблюдается при поражении церебральных артерий среднего/крупного калибра. Паркинсонизм развивается на протяжении 6-12 месяцев после перенесённого инсульта. Характерно подострое или острое течение. Акинетико-ригидный синдром может иметь односторонний характер. Нейровизуализирующие методы исследования выявляют локализованную контрлатерально зону инсульта.
- Безинсультная. Типична для поражения мелких интрацеребральных артерий. Паркинсонизм имеет подострый дебют, прогрессирует ступенеобразно, реже — неуклонно. Акинетико-ригидная симптоматика носит двусторонний характер. Нейровизуализация обнаруживает диффузные изменения подкорковых структур, лакунарные очаги в скорлупе и бледном шаре.
Симптомы сосудистого паркинсонизма
В ряде случаев заболевание манифестирует появлением лёгких паркинсонических знаков: изолированной олигобрадикинезии (в пределах нижних конечностей), одного умеренно выраженного симптома паркинсонизма, нескольких проявлений лёгкой степени. Симптоматика начальной стадии суммарно не достигает определяющих истинный паркинсонизм критериев, аналогична дебюту ряда дегенеративных заболеваний, клинике возрастных подкорковых изменений. Заподозрить СП в подобных случаях можно по мере прогрессирования симптомов.
Сосудистый паркинсонизм протекает без нарушений обоняния (аносмии). Характеризующий болезнь Паркинсона тремор покоя выявляется лишь в 4% случаев СП. Сопутствующая симптоматика зависит от локализации и распространённости сосудистого поражения. Чаще наблюдаются пирамидные расстройства, мозжечковая атаксия, в дебюте заболевания маскирующие паркинсонизм. Возможны тонические расстройства, миоклонии, псевдобульбарный синдром, симптомы очагового поражения высших нервных функций (афазия, амнезия, апраксия), лобный синдром. Типично прогрессирующее интеллектуальное снижение.
Осложнения
Ранее формирование постуральных расстройств значительно затрудняет самостоятельные передвижения пациента, опасно падениями, травмированием больного. Ситуация усугубляется при наличии мозжечковых и пирамидных нарушений. Ограничение двигательной активности осложняется формированием контрактур суставов. Сопровождающие паркинсонизм изменения личности (сужение круга интересов, замкнутость, пониженный фон настроения) способствуют возникновению депрессии. Прогрессирующие когнитивные расстройства ведут к деменции. Больной утрачивает возможность самообслуживания, требует постоянного ухода. Псевдобульбарный паралич опасен аспирацией пищи с развитием аспирационной пневмонии.
Диагностика
Диагностировать сосудистый паркинсонизм врачу-неврологу позволяет наличие клинических критериев акинетико-ригидного синдрома, подтверждённого инструментальными исследованиями цереброваскулярного заболевания, выявления причинно-следственной связи между ними. Поскольку сосудистый генез патологии обуславливает полиморфизм клинических проявлений, устанавливать диагноз СП целесообразно, если паркинсонизм является доминирующим синдромом. Основные диагностические мероприятия включают:
- Неврологический осмотр. Подтверждает олигобрадикинезию с преимущественным поражением нижних конечностей, пластический мышечный тонус, постуральную неустойчивость. Паркинсонизм сочетается с другими неврологическими расстройствами. Когнитивное тестирование определяет замедленность мышления различной степени, снижение памяти, сложности концентрации внимания.
- УЗДГ церебральных сосудов.УЗИ сосудов головы и шеи дает возможность оценить состояние мозгового кровообращения, диагностировать цереброваскулярную патологию. В ходе исследования можно обнаружить сосудистый стеноз, тромбоэмболию, диффузные изменения артериальных стенок. Отсутствие гемодинамических нарушений позволяет исключить сосудистый генез болезни, но их наличие не является однозначным подтверждением СП.
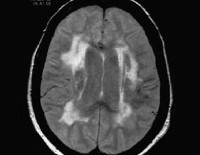
- Магнитно-ядерный резонанс.МРТ головного мозга выявляет сосудистое поражение ответственных за паркинсонизм структур. Морфологическим субстратом постинсультного СП являются подкорковые фокусы в бассейне средней и передней церебральных артерий. Безинсультная форма характеризуется диффузным характером поражения, наличием множественных лакунарных очагов. Данные КТ головного мозга менее информативны, используются при невозможности проведения магнитно-резонансной томографии.
Важное место в диагностическом поиске занимает дифференциальная диагностика. Особую сложность представляют пациенты пожилого возраста, поскольку у них часто обнаруживаются сосудистые нарушения и возрастная дегенерация базальных ганглиев. Дифференцировать сосудистый паркинсонизм от болезни Паркинсона позволяют особенности течения, отсутствие постурального тремора, расстройств обоняния, наличие пирамидной, мозжечковой сопутствующей симптоматики. Значительные сложности представляет дифдиагностика сосудистой патологии от дегенеративных поражений ЦНС (мультисистемной атрофии, деменции с тельцами Леви, кортикобазальной дегенерации). Достоверно исключить первично-дегенеративный генез подкорковых нарушений можно только на основе данных патоморфологического анализа.
Лечение сосудистого паркинсонизма
Терапия СП требует комплексного подхода, направленного на лежащий в основе патологии этиопатогенетический фактор и основные клинические проявления заболевания. Существенное значение имеет нормализация мозговой гемодинамики, профилактика возникновения ОНМК. В большинстве случаев применяется консервативное лечение, включающее:
- Базисную терапию. Направлена на сосудистый механизм развития болезни, предупреждает дальнейшее поражение мозговых тканей. Проводится коррекция артериального давления, антиагрегантная, антиатерогенная терапия. Высокий риск кардиогенной эмболии является показанием к назначению антикоагулянтов.
- Симптоматическое лечение. Паркинсонизм выступает показанием к дофаминергической терапии, осуществляемой в первую очередь препаратами леводопы. Курс пробной леводопатерапии производится в максимальной суточной дозировке в течение 1-3 месяцев, эффективен у 22-50% больных. Действие леводопы потенцируют амантадины. При отсутствии эффекта назначают терапию агонистами дофаминовых рецепторов, ингибиторами МАО. Параллельно проводят нейропротекторную, ноотропную, антидепрессантную терапию.
Хирургическое лечение сводится к стереотаксическим операциям. Наиболее распространена паллидотомия — частичное разрушение бледного шара. Вмешательство может быть эффективным при ограниченных поражениях. Многоочаговые процессы, а также экстранигральный, не связанный с патологией чёрной субстанции паркинсонизм плохо поддаются нейрохирургическому лечению.
Прогноз и профилактика
Эффективность лечения СП зависит от этиологии цереброваскулярных расстройств, локализации и обширности поражения. Компенсировать проявления паркинсонизма удаётся у пациентов с положительным ответом на терапию леводопой. Локализация поражения в стриарной и таламической областях обуславливает резистентный к дофаминовой терапии паркинсонизм, имеющий более серьёзный прогноз.
Первичная профилактика СП включает исключение факторов, приводящих к патологическим изменениям сосудов головного мозга (курения, атерогенного питания, набора избыточной массы тела), адекватную коррекцию артериальной гипертензии, своевременную терапию сердечно-сосудистых заболеваний. Вторичная профилактика заключается в поддержании полноценной мозговой гемодинамики, профилактике острых нарушений церебрального кровотока. Пациентам под наблюдением терапевта или кардиолога следует осуществлять постоянный контроль артериального давления. Рекомендованы регулярные курсы сосудистой терапии.
Читайте также:


