Роль нервной системы в регенерации
При повреждении нервов дегенеративные процессы аксона происходят дистальнее места поражения. Это связано с тем, что аксон является отростком нейрона, и его питание и рост зависят от сомы. Регенеративные процессы периферической нервной системы характеризуются высокой интенсивностью и в большинстве случае обеспечивают полное восстановление структур. В ЦНС, напротив, интенсивность процессов восстановления не высока, и регенерация не является полной.
а) Валлерова (антероградная) дегенерация периферических нервов. Основные этапы процесса дегенерации и их описание представлены на рисунке ниже и в подписи к нему. После разрушения или перерезки нерва в течение первых 48 ч аксоны и миелиновая оболочка под действием протеаз, высвобождающихся из шванновских клеток под влиянием ионов Са 2+ , распадаются на фрагменты элипсоидной формы дистальнее места нарушения целостности нерва. Продукты распада удаляют моноциты, которые перемещаются из кровотока в эндоневрий и превращаются в макрофаги.
Помимо осуществления фагоцитоза, макрофаги стимулируют митотическую активность шванновских клеток. Макрофаги и шванновские клетки выполняют трофическую (питательную) и направляющую функции для регенерирующих аксонов.
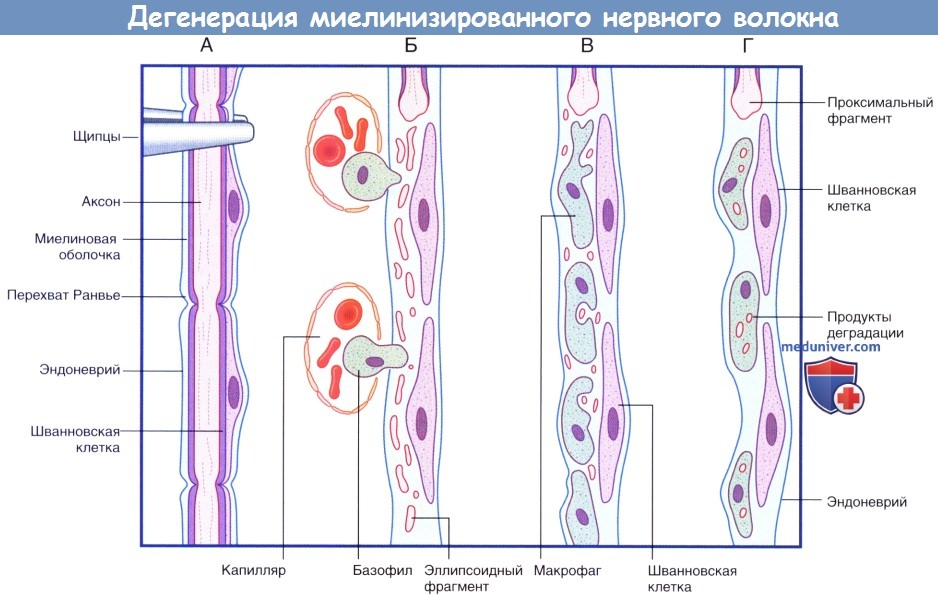
Последовательность процессов при дегенерации миелинизированного нервного волокна.
(А) Сохранное нервное волокно; продемонстрированы четыре сегмента. Выполняют пережатие нервного волокна в верхней части.
(Б) Миелиновая оболочка и аксон распадаются на мелкие частицы и фрагменты эллипсоидной формы. Моноциты проникают в эндоневрий из кровеносного русла.
(В) Мелкие продукты дегенерации поглощают моноциты.
(Г) Происходит практически полное удаление всех продуктов дегенерации. Шванновские клетки и эндоневрий сохранны. Последовательность процессов при регенерации миелинизированного нервного волокна. 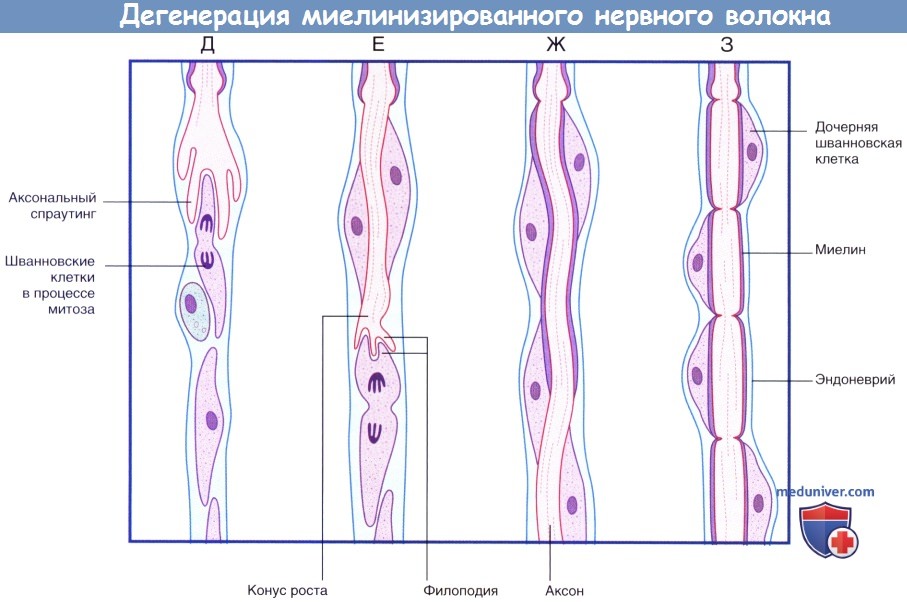
(продолжение) Последовательность процессов при дегенерации миелинизированного нервного волокна.
(Д) Аксональный спраутинг начинается с дистального участка аксона. Спраутинг оказывает митогенное дейсвтие на окружающие шванновские клетки.
(Е) Конус роста продвигается дистально вдоль поверхности шванновских клеток.
(Ж) Миелинизация начинается вдоль проксимального участка регенерирующего аксона.
(З) Общее строение вновь миелинизированного нервного волокна соответствует тем же принципам, однако миелинизированные сегменты характеризуются меньшей длиной.
б) Регенеративные процессы в периферической нервной системе. Основные этапы процесса регенерации представлены на рисунке ниже. После ровного среза нерва спраутинг (разрастание новых ветвей) на конце проксимального отрезка аксона начинается уже спустя несколько часов. Однако в клинической практике повреждения нерва часто происходят при раздавливании или разрыве. В этих случаях происходит отмирание участка нерва длиной 1 см и более, за счет чего спраутинг может продолжаться в течение недели. В случае удачной регенерации происходит тесное соприкосновение проксимального конца аксона со шванновской клеткой дистального конца пересеченного нейрона.
При нарушении формирования этой связи в месте первичного повреждения образуется псевдоневрома, представляющая собой извитые регенерирующие аксоны, погруженные в рубцовую ткань. Ампутационные псевдоневромы — источники сильных болей после ампутаций конечностей.
Регенерация нейронов при повреждении происходит двумя путями в течение нескольких часов после повреждения. На проксимальном конце пересеченного аксона появляются множественные отростки, на конце которых образуются утолщения — конусы роста. На дистальном конце шванновские клетки формируют отростки, направляющиеся навстречу конусам роста. На концах конусов роста формируются напоминающие антенны филоподии, где располагаются поверхностные рецепторы, временно связывающиеся с соответствующими поверхностными молекулами адгезии базальных мембран шванновских клеток. Актиновые филаменты филоподий прикрепляются к поверхностным рецепторам и относительно этих соединений осуществляют дальнейшее продвижение конусов роста.
Конусы роста стимулируют митотическую активность шванновских клеток. Шванновские клетки делятся и миелинизируют наиболее крупные аксоны.
При полном разрыве нервных стволов перед попыткой их восстановления, как правило, выжидают около трех недель, поскольку сразу после повреждения их соединительнотканные оболочки отечны, а в течение этого промежутка времени они становятся немного толще, что позволяет шовному материалу лучше закрепиться. Кроме того, обрезание нервов перед наложением швов приводит к развитию вторичной аксотомии проксимальной части пересеченного аксона. В ходе экспериментальных исследований на животных показано, что вторичная аксотомия стимулирует более интенсивную и длительную регенерацию.
Влияния тела нейрона на пересеченный участок нерва заключаются в следующем:
• Вследствие осмотических изменений перикариона ядро ориентируется эксцентрически.
• Клетки нейроглии заполняют все синаптические щели, изолируя исходный двигательный нейрон от синаптических контактов в сером веществе.
• В исследованиях, проведенных на обезьянах, показано, что после перерезки чувствительных нейронов 30-40 % окончаний дорсальных нервных корешков подвергается валлеровской дегенерации. Регенерация этих нейронов не происходит, поскольку их окончания располагаются в сером веществе головного мозга. Однако некоторые рецепторы восстанавливаются за счет спраутинга сохранных прилежащих нейронов. Данное наблюдение позволяет объяснить явление неполного восстановления чувствительности у таких пациентов.
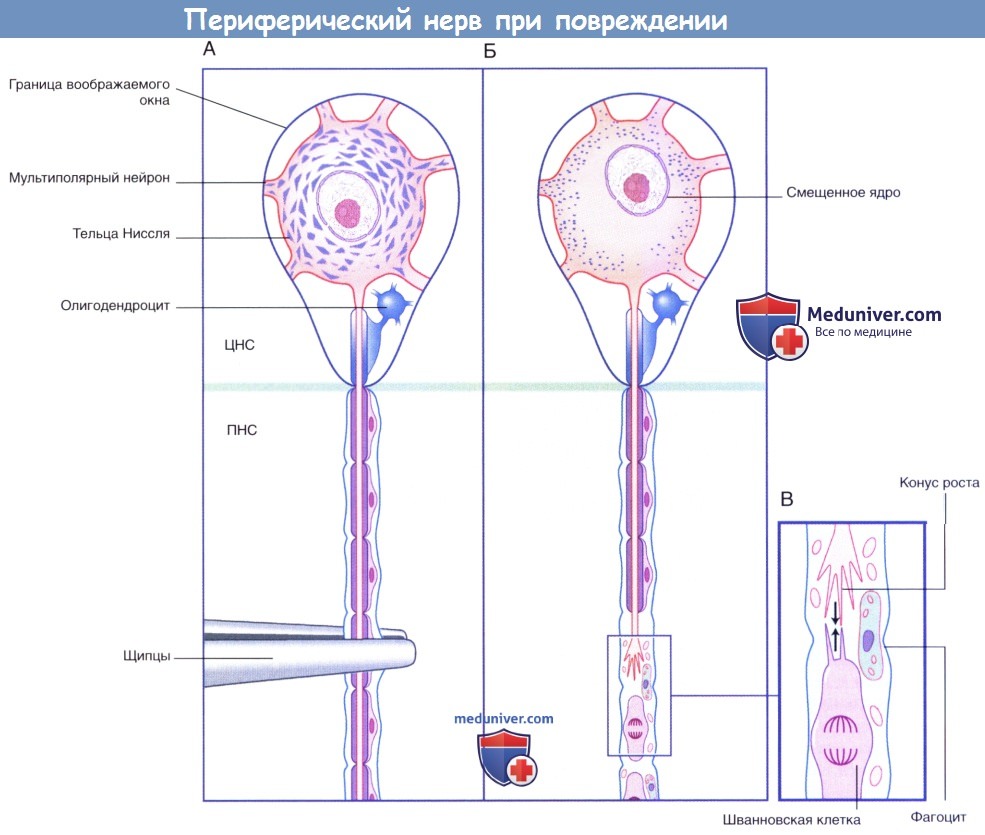
Схематическое изображение процессов, происходящих в периферическом нерве после повреждения.
(А) Двигательный нейрон ЦНС, видимый через воображаемое окно.
(Б) Хроматолизис проявляется фрагментированием и рассеиванием телец Ниссля, а также смещением ядра.
(В) В зоне повреждения в условиях удаления продуктов деградации происходит образование контакта филоподий конуса роста с проксимальными выростами шванновских клеток (указано стрелками).
ЦНС — центральная нервная система; ПНС — периферическая нервная система.
Редактор: Искандер Милевски. Дата публикации: 12.11.2018
4.1. Общая характеристика нервной ткани
Нервная ткань — это система взаимосвязанных нервных клеток и нейроглии, обеспечивающих специфические функции восприятия раздражений, возбуждения, выработки импульса и его передачи. Нервные клетки (нейроны) — основные структурные компоненты нервной ткани, выполняющие специфическую функцию. Нейроглия обеспечивает существование и функционирование нервных клеток, осуществляя опорную, трофическую, разграничительную, секреторную и защитную функции. Источником развития нервной ткани служит дорсальная эктодерма. [1],[5]
Из нервной трубки в дальнейшем формируются нейроны и макроглия центральной нервной системы. Нервный гребень дает начало нейронам чувствительных и автономных ганглиев и некоторым видам глии: нейролеммоцитам (шванновским клеткам), клеткам-сателлитам ганглиев. Нервная трубка на ранних стадиях эмбриогенеза представляет собой многорядный нейроэпителий, состоящий из вентрикулярных, или нейроэпителиальных клеток. [1],[5]
В дальнейшем в нервной трубке дифференцируется 4 концентрических зоны: внутренняя - вентрикулярная (или эпендимная) зона, вокруг нее – субвентрикулярная зона, затем промежуточная (или мантийная зона) и, наконец, наружная - краевая (или маргинальная) зона нервной трубки. Вентрикулярная (эпендимная), внутренняя, зона состоит из делящихся клеток цилиндрической формы. Вентрикулярные (или матричные) клетки являются предшественниками нейронов и клеток макроглии. Субвентрикулярная зона состоит из клеток, сохраняющих высокую пролиферативную активность и являющихся потомками матричных клеток. Промежуточная (плащевая, или мантийная) зона состоит из клеток, переместившихся из вентрикулярной и субвентрикулярной зон — нейробластов и глиобластов. Нейробласты утрачивают способность к делению и в дальнейшем дифференцируются в нейроны. Глиобласты продолжают делиться и дают начало астроцитам и олигодендроцитам. [1], [5]
Способность к делению не утрачивают полностью и зрелые глиоциты. Новообразование нейронов прекращается в раннем постнатальном периоде. Из клеток плащевого слоя образуются серое вещество спинного и часть серого вещества головного мозга. Маргинальная зона (или краевая вуаль) формируется из врастающих в нее аксонов нейробластов и макроглии и дает начало белому веществу.[5]
4.2. Регенерация нервной ткани
Рассматривая процессы регенерации в нервных тканях следует сказать, что нейроциты являются наиболее высокоспециализированными клетками организма и поэтому утратили способность к митозу. Физиологическая регенерация (восполнение естественного износа) в нейроцитах хорошая и протекает по типу "внутриклеточной регенерации" - т.е. клетка не делится, но интенсивно обновляет изношенные органоиды и другие внутриклеточные структуры. Для этого в нейроцитах хорошо выражены гранулярный ЭПС, пластинчатый комплекс и митохондрии, т.е. имеется мощный синтетический аппарат для синтеза органических компонентов внутриклеточных структур.[5]
К компенсаторно-приспособительным процессам в нервной ткани относится обнаружение многоядрышковых, двухъядерных и гипертрофированных нервных клеток при различного рода болезнях, сопровождающихся дистрофическими процессами, при условии сохранения общей структуры нервной ткани. Нервные клетки вегетативной нервной системы восстанавливаются путем гиперплазии органелл, а также не исключается возможность их размножения. Периферические нервы являются в большинстве своем смешанными и состоят из двигательных волокон передних корешков (аксонов клеток передних рогов), чувствительных волокон (дендритов клеток межпозвонковых узлов) и вазомоторно-секреторно-трофических волокон (симпатических и парасимпатических) от соответствующих клеток серого вещества боковых рогов спинного мозга и ганглиев симпатического пограничного ствола. Нервное волокно, входящее в состав периферического нерва, состоит из осевого цилиндра, расположенного в центре волокна, миелиновой или мякотной оболочки, одевающей осевой цилиндр и шванновской оболочки. Миелиновая оболочка нервного волокна местами прерывается, образуя так называемые перехваты Ранвье. В области перехватов осевой цилиндр прилежит непосредственно к шванновской оболочке. Миелиновая оболочка обеспечивает роль электрического изолятора, предполагается ее участие в процессах обмена осевого цилиндра. Шванновские клетки имеют общее происхождение с нервными элементами. Они сопровождают осевой цилиндр периферического нервного волокна подобно тому, как глиозные элементы сопровождают осевые цилиндры в центральной нервной системе, поэтому шванновские клетки иногда называют периферической глией. На месте дефекта в нервной ткани разрастается нейроглия. Она является менее дифференцированной тканью, клетки которой способны делиться митозом. Существуют глиальные клетки, обладающие высокими потенциями к размножению и развитию. Эти клетки принимают активное участие в восстановительных процессах нервной ткани. Наиболее частыми формами травматического повреждения нервов, возникающими вследствие техногенного травматизма на производстве, при дорожно- транспортных происшествиях, в ходе военных действий, являются размозжение, ушиб, растяжение, а также сдавление с наличием или отсутствием разрыва нервного ствола. Однако эффективность репарации структуры и функции поврежденной ткани с применением лечебных мероприятий и лекарственных средств остается относительно низкой. Это во многом связано с малой изученностью динамики регенерации нервов после травмы. Для исследования воздействия модулирующих средств на посттравматический процесс необходимы более полные данные о динамике репаративной регенерации поврежденного нерва.[5]
При повреждениях, приводящих к нарушению целостности нервных волокон, их периферические части распадаются на фрагменты осевых цилиндров и миелиновых оболочек, погибают и фагоцитируются макрофагами. В сохранившейся части нервного волокна начинается пролиферация нейролеммоцитов, формирующих цепочку (бюнгнеровская лента), вдоль которой происходит постепенный рост осевых цилиндров. [5],[6]
Выделяемые шванновской клеткой различные стимуляторы (нейтрофические факторы) поглощаются аксоном и ретроградно транспортируются в перикардион. В перикарионе эти факторы стимулируют синтез белка и поддерживают его на высоком уровне. В регенерирующем нерве шванновские клетки пролиферируют, синтезируют компоненты базальной мембраны, внеклеточного матрикса и формируют миелин. Шванновские клетки стимулируют удлинение аксона и контролируют его направленный рост и мишени. При отсутствии Шванновских клеток аксоны не могут расти на значительные расстояния. [5]
Восстановление утраченных связей может происходить и за счет образования коллатеральных ветвей из окружающих и неповрежденных нервных волокон. Чаще коллатеральные ветви отходят от участка аксона в области перехвата Ранвье. Наличие в зоне перерезки нерва мертвых тканей, которые стимулируют разрастание здесь рубцовой ткани, большое расстояние между отрезками нервного волокна, сильное повреждение сосудов и нарушение кровоснабжения нерва ведут к резкому нарушению его регенерации. [5],[6]
Разрастание рубцовой ткани иногда вызывает развитие ампутационной невромы, состоящей из разросшихся отростков нейронов и глии, окруженных грубой рубцовой тканью. Невромы могут вызывать сильные (фантомные) боли. Регенерация нервных отростков идет со скоростью 2-4 мм в сутки. В условиях лучевого воздействия происходит замедление процессов репаративного гистогенеза, что обусловлено в основном повреждением нейролеммоцитов и клеток соединительной ткани в составе нерва. Способность нервных волокон к регенерации после повреждения при сохранении целостности тела нейрона используется в микрохирургической практике при сшивании дистального и проксимального отростков поврежденного нерва. Если это невозможно, то используют протезы (например, участок подкожной вены), куда вставляют концы поврежденных нервов (футлериз). Регенерацию нервных волокон ускоряет фактор роста нервной ткани — вещество белковой природы, выделенное из тканей слюнных желез и из змеиного яда. Нервная ткань на повреждение реагирует неоднозначно. Повреждение клеток центральной нервной системы, нейронов спинного мозга, симпатических ганглиев завершается их гибелью. Аксоны же нервных клеток сохраняют способность к репаративной регенерации. Повреждение периферического нерва сопровождается дегенерацией и атрофией конца нерва, идущего к периферии. Регенерация начинается на конце аксона, связанного с нервной клеткой. Регенерирующий конец нерва врастает в трубочки и способен восстановить иннервацию. Если же аксон не совмещен с объектом врастания, то на его конце могут образоваться своеобразные утолщения — невромы. Эффективность процесса регенерации во многом определяется условиями, в которых он протекает.[5],[6]
Значение имеет общее состояние организма. Так, истощение, авитаминозы, нарушения иннервации затормаживают репаративную регенерацию и способствуют ее переходу в патологическую. Изменение условий, в которых протекает процесс регенерации, может приводить как к количественным, так и качественным его изменениям.[5]
4.3. Возрастные особенности периферической нервной системы.
Развитие нервной системы у детей с моментом рождения не останавливается. После рождения увеличивается количество нервных пучков в составе периферических нервов: усложняется их ветвление, расширяются межнейрональные связи, усложняются рецепторные аппараты.[5]
С возрастом увеличивается толщина нервных волокон. К 9 годам во всех периферических нервах миелинизация близится к завершению. В пожилом и старческом возрасте количество нейронов в спинномозговых ганглиях снижается на 30%, часть нейронов атрофируется. Возрастные изменения в нервной ткани связаны с утратой нейроцитов в постнатальном периоде способности к делению, и как следствие этого постепенным уменьшением количества нейроцитов, особенно чувствительных нейроцитов, а также уменьшением уровня метаболических процессов в оставшихся нейроцитах. Отсутствие клеточной формы регенерации нейроцитов обуславливает разрастание нейроглии и соединительной ткани на месте повреждения.[5]
Заключение
Таким образом, на основании проанализированной литературы, можно сделать вывод о том, что нервная ткань обладает плохой способностью к регенерации. В эксперименте показано, что клетки периферической и вегетативной нервной системы, двигательные и чувствительные нейроны в спинном мозге мало регенерируют.[5]
Регенерация нервной ткани может происходить путём роста тканей на раневой поверхности, перестройки оставшейся части органа в новый, или путём роста остатка органа без изменения его формы. [2],[5]
Уровни регенерации в ходе восстановления структур следующие: молекулярный, ультраструктурный, клеточный, тканевой, органный.[5]
Новые нейроны образуются из недифференцированных предшественников, которые способны давать начало также астроцитам и олигодендроцитам и поэтому могут рассматриваться как стволовые нервные клетки. Идентификация стволовых клеток в мозге представляет большие сложности особенно в зрелом возрасте. [2],[5]
Сочетание классических хирургических способов восстановления нервных стволов и методов прямой терапии ростовыми факторами ускоряет аксональный рост, стимулирует реваскуляризацию нерва, что подтверждается многочисленными экспериментальными исследованиями и, в итоге, улучшает результаты посттравматического восстановления функции реиннервации поврежденного органа или ткани. [5], [6]
Список литературы
1. Гистология, эмбриология, цитология: учебник / Ю. И. Афанасьев, Н. А. Юрина, Б. В. Алешин и др.; под ред. Ю. И. Афанасьева, Н. А. Юриной. - 6-е изд., перераб. и доп. – М.: ГЭОТАР-Медиа, 2014. - 800 с.
2. Корочкин Л. И. Что такое стволовые клетки // Природа. – 2005. - № 6. – С. 3-11.
3. Кузнецов С.Л., Мушкамбаров Н.Н.Гистология, цитология и эмбриология: Учебник. – М.: Медицинское Информационное Агентство, 2007. – 540с.
4. Руководство по гистологии/ под ред. Р.К. Данилов. – СПб.: СпецЛит.- 2011.–Том 1.-С.160-165; 190-195; 210-216; 252-258; 280-299; 440-442; 656-669.
5. Регенерация тканей: учебное пособие – Благовещенск, 2016. – 136 с.
Дата добавления: 2018-02-15 ; просмотров: 2322 ;
РОЛЬ НЕРВНОЙ СИСТЕМЫ В ТРОФИКЕ И РЕГЕНЕРАЦИИ МЫШЦ
Повреждение периферического нерва, сопровождающееся параличом, сравнительно быстро, через 3—5 недель, приводит к нейрогеиной атрофии мускулов, нннервируемых данным нервом. Скорость развития атрофического процесса в мускулах, степень его выраженности зависят от многих факторов, однако главным из них является, по-видимому, выпадение нейротрофического влияния, осуществляемого центральной нервной системой, посредством периферической иннервации. Поэтому роль периферической иннервации, осуществляющей взаимосвязь периферии с центральной нервной системой, исключительно велика. Именно перерыв нервного влияния, идущего по смешанному нерву конечности, приводит к дистрофическому процессу, причем не только в иннервируемых мышцах, но и в других тканях — коже, соединительной ткани, костях, сосудах.
Нужно, однако, заметить, что, несмотря на большое число исследований трофического влияния нервной системы, многие стороны этцопатогенеза и саногенеза этого процесса остаются не выясненными.
Характерной особенностью нейрогенных дистрофий мышц, поданным Тауер, 1935; Г. II. Орловой/1953, 1958; И. Д. Хлопиной, 1957, и других, является истончение мышечных волокон и так называемая фиброзная трансформация их, зернистое перерождение, вакуолизация, разрастание соединительнои ткани в денервирэраняой мышце. В атрофирующейся мышце наблюдаются кругло-клеточковая инфильтрация и явления фагоцитоза, на поздних стадиях—дегенерация ядер: кариопикнбз, карио-рексис, рассасывание и гибель ядра.
В денервированной мышце изменяются биохимические процессы: снижается содержание креатина и корнизона, фосфоркреатина, гликогена, АТФ и молочной кислоты; повышается количество глютаминовой кислоты и анасерипа, на 25—27-й день появляется свободный В-аланин (П. А. Юдаев, 1953; Н. А. Куценко, Г. А. Нечаева, 1953). Изменяется и активность ферментов: снижается концентрация адонизинфосфатазы, креатинфосфатазы, амилазы "(гликогеназы); увеличивается концентрация протеаз и пирофосфатазы (В. М. Веселкина, 1938; П. М. Зубенко, 1954).
Нарушение периферической иннервации отражается на регенеративном процессе в мышце. Уже давно было замечено, что на парализованных конечностях регенеративный процесс может значительно нарушаться, а заживление тканевых дефектов происходит медленнее; часто наблюдается образование долго не заживающих нейротрофических язв. К такому выводу пришел М. Я. Новинский еще в 1895 г.
А. Н. Студитский и А. Р. Стриганова (1951) считают наличие нервной связи определяющим и важнейшим условием восстановления поврежденной соматической мускулатуры. По их данным, в денервированных мышцах превращения миобластов из мышечных отростков в мышечные трубки, а фибробластов в клетки эндомизия, обеспечивающие развитие сарколеммы, не происходит. Наши опыты по заживлению тканевых дефектов на деаф-ферентированной конечности у собак после выключения крупных нервных стволов (седалищный, бедренный нервы) показали, что в деиннервируемых тканях создается пониженный или явно дистрофический фон для регенерации; регенеративный процесс не переходит в репаратив-ную фазу и характеризуется преимущественно деструктивными явлениями как в соединительной ткани, так и в кожном эпителии. Со временем регенерационная способность парализованных тканей понижается. Механическое нарушение только симпатической иннервации, напротив, вызывало более быстрое заживление дефекта, характеризующееся быстрым развитием и ограничением деструктивной фазы воспаления и переходом в репаративную фазу при усиленной фибробластической реакции и пролиферации кожного эпителия. Только деэффёрентация тазовой конечности собак при сохранении задних спинномозговых корешков, так же как и десимпатизация, не вызывала нарушения регенеративных процессов.
Таким образом, различные отделы нервной системы по-разному влияли на течение и исход регенеративного процесса. Если выключение эфферентных импульсов при одновременном раздражении центров вызывало замедление и извращение процесса заживления ран, то эфферентные импульсы, осуществляемые симпатической иннервацией, ускоряли регенеративный процесс и заживление происходило быстрее, чем в обычных эквивалентных условиях.
Большое значение для понимания патогенеза нейрогенных и мышечных атрофий имеет электрохимическая теория распространения нервного импульса. В настоящее время можно" считать установленным, что распространение нервных импульсов по нервным волокнам осуществляется токами действия образуемыми Na+, К+ "и С1 ", а также ацетилхолином. Термин ток действия точно выражает функциональную роль именно электрического тока, возникающего вследствие непрерывного перемещения ионов Na+ внутрь, а К+ и СО — наружу оболочки волокон, в результате чего оболочки постоянно перезаряжаются (ионный пасос). В нормальных условиях в организме по нервным волокнам пробегают импульсы, более или менее быстро следующие друг за другом. Иная картина наблюдается в тех случаях, когда на нерв воздействуют наркотиками, анестетиками, растворами солей, ядами и др. Проводимость нерва в повреждаемом участке постепенно ослабевает и может совершенно прекратиться (парабиоз). Исследования Е. Д. Эдриана, И. А. Юденич, П. О. Макарова, Д. С. Воронцова и других показали, что нервный импульс входит в альтерированный участок, но в нем затухает, декремеитирует. Скорость проведения нервного импульса зависит от толщины аксона и его миелиновой оболочки. Чем толще аксон, тем быстрее распространяется импульс; напротив, тонкие безмякотные нервные волокна проводят импульс очень медленно.
Чем толще нервное волокно, тем выше его возбудимость, короче рефракторная фаза и быстрее нарастает ого ток действия. В настоящее время принята следующая классификация нервных волокон для теплокровных животных: группа А, включающая альфа, бета, гамма и дельта-волокна со скоростями распространения импульса от 50 до 140 м/сек: группа Bi со скоростью 35 до 15 м/сек; группа В2 — от 15 до 10 м/сек и группа С—от 2 до 1 м/сек.
Повреждение периферического нерва, сопровождающееся параличом, сравнительно быстро, через. 3—5 недель, приводит к нейрогенной атрофии мускулов, иннервируемых данным нервом.
Скорость развития атрофического процесса в мускулах, степень его выраженности зависят от многих факторов, однако главным из них является, по-видимому, выпадение нейротрофического влияния, осуществляемого центральной нервной системой, посредством периферической иннервации. Поэтому роль периферической иннервации, осуществляющей взаимосвязь периферии с центральной нервной системой, исключительно велика. Именно перерыв нервного влияния, идущего по смешанному нерву конечности, приводит к дистрофическому процессу, причем не только в иннервируемых мышцах, но и в других тканях — коже, соединительной ткани, костях, сосудах.
Нужно, однако, заметить, что, несмотря на большое число исследований трофического влияния нервной системы, многие стороны этиопатогенеза и саногенеза этого процесса остаются не выясненными.
Характерной особенностью нейрогенных дистрофий мышц, по данным Тауер, 1935; Г. Н. Орловой, 1953, 1958; И. Д. Хлопиной, 1957, и других, является истончение мышечных волокон и так называемая фиброзная трансформация их, зернистое перерождение, вакуолизация, разрастание соединительной ткани в денервированной мышце. В атрофирующейся мышце наблюдаются круглоклеточковая инфильтрация и явления фагоцитоза, на поздних стадиях—дегенерация ядер: кариопикпоз, кариорексис, рассасывание и гибель ядра.
В денервированной мышце изменяются биохимические процессы: снижается содержание креатина и корнизона, фосфоркреатина, гликогена, АТФ и молочной кислоты; повышается количество глютаминовой кислоты и анасерина, на 25-27-й день появляется свободный В-аланин (Н. А. Юдаев, 1953; А. Куценко, Г. А. Нечаева, 1953). Изменяется и активность ферментов: снижается концентрация адонизинфосфатазы, креатинфосфатазы, амилазы (гликогеназы); увеличивается концентрация протеаз и пирофосфатазы (В. М. Веселкина, 1938; П. М. Зубенко, 1954).
Нарушение периферической иннервации отражается на регенеративном процессе в мышце. Уже давно было замечено, что на парализованных конечностях регенеративный процесс может значительно нарушаться, а заживление тканевых дефектов происходит медленнее; часто наблюдается образование долго не заживающих нейротрофических язв. К такому выводу пришел М. Я. Новинский еще в 1895 г.
А. Н. Студитский и А. Р. Стриганова (1951) считают наличие нервной связи определяющим и важнейшим условием восстановления поврежденной соматической мускулатуры. По их данным, в денервированных мышцах превращения миобластов из мышечных отростков в мышечные трубки, а фибробластов в клетки эндомизия, обеспечивающие развитие сарколеммы, не происходит. 11аши опыты по заживлению тканевых дефектов на деафферентированной конечности у собак после выключения крупных нервных стволов (седалищный, бедренный нерпы) показали, что в деиннервируемых тканях создается пониженный или явно дистрофический фон для регенерации; регенеративный процесс не переходит в репаративную фазу и характеризуется преимущественно деструктивными явлениями как в соединительной ткани, так и в кожном эпителии. Со временем регенерационная способность парализованных тканей понижается. Механическое нарушение только симпатической иннервации, напротив, вызывало более быстрое заживление дефекта, характеризующееся быстрым развитием и ограничением деструктивной фазы воспаления и переходом в репаративную фазу при усиленной фибробластической реакции и пролиферации кожного эпителия. Только деэфферентация тазовой конечности собак при сохранении задних спинномозговых корешков, так же как и десимпатизация, не вызывала нарушения регенеративных процессов.
Таким образом, различные отделы нервной системы по-разному влияли на течение и исход регенеративного процесса. Если выключение эфферентных импульсов при одновременном раздражении центров вызывало замедление и извращение процесса заживления ран, то эфферентные импульсы, осуществляемые симпатической иннервацией, ускоряли регенеративный процесс и заживление происходило быстрее, чем в обычных эквивалентных условиях.
Большое значение для понимания патогенеза нейрогенных и мышечных атрофий имеет электрохимическая теория распространения нервного импульса. В настоящее время можно считать установленным, что распространение нервных импульсов по нервным волокнам осуществляется токами действия образуемыми Na+, К+ и Cl — , а также ацетилхолином. Термин ток действия точно выражает функциональную роль именно электрического тока, возникающего вследствие непрерывного перемещения ионов Na+ внутрь, а К+ и Cl — —наружу оболочки волокон, в результате чего оболочки постоянно перезаряжаются (ионный насос). В нормальных условиях в организме по нервным волокнам пробегают импульсы, более или менее быстро следующие друг за другом. Иная картина наблюдается в тех случаях, когда на нерв воздействуют наркотиками, анестетиками, растворами солей, ядами и др. Проводимость нерва в повреждаемом участке постепенно ослабевает и может совершенно прекратиться (парабиоз). Исследования Е. Д. Эдриана, Н. А. Юденич, П. О. Макарова, Д. С. Воронцова и других показали, что нервный импульс входит в альтерированный участок, но в нем затухает, декрементирует. Скорость проведения нервного импульса зависит от толщины аксона и его миелиновой оболочки. Чем толще аксон, тем быстрее распространяется импульс; напротив, тонкие безмякотные нервные волокна проводят импульс очень медленно.
Чем толще нервное волокно, тем выше его возбудимость, короче рефракторная фаза и быстрее нарастает его ток действия. В настоящее время принята следующая классификация нервных волокон для теплокровных животных: группа А, включающая альфа, бета, гамма и дельта-волокна со скоростями распространения импульса от 50 до 140 м/сек: группа В1 со скоростью 35 до 15 м/сек; группа В2 — от 15 до 10 м/сек и группа С — от 2 до 1 м/сек.
Таким образом, установлено, что нарушение нормальной импульсации по поврежденному периферическому нерву не только отрицательно отражается на функции иннервируемой мышцы, но и лишает притока электрической энергии чувствительные и двигательные нервные окончания. Поскольку место стыка — синапс — нервного волокна с мышечной тканью — это такой участок, где нервное возбуждение с нерва переходит на мышцу, деятельность двигательной бляшки будет нарушена. В зоне двигательной бляшки имеются константы химического характера; в моторной бляшке образуется ацетилхолин, а подошва бляшки богата холинэстеразами, т. е. ферментами, расщепляющими ацетилхолин, вследствие чего передача нервного импульса прекращается. Если принять во внимание, что в мионевральном синапсе электрические импульсы распространяются в центробежном направлении, то повреждение нервного ствола будет препятствовать проведению по соответствующим аксонам импульсов к нервным окончаниям и нарушать функциональную подвижность мускулов. Особенно сильно синаптическая передача нарушается при отравлении фосфороорганическими ядами, в тоже время ее можно усилить инъекцией прозерина.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Читайте также:


