Симпатическая нервная система снижает артериальное давление
Сложное строение организма людей предусматривает несколько подуровней нервной регуляции каждого органа. Так, для симпатической нервной системы присуща мобилизация энергетических ресурсов для выполнения определенной задачи. Вегетативный же отдел контролирует работу структур в их функциональном покое, к примеру, в момент сна. Правильное взаимодействие и деятельность вегетативной нервной системы в целом – залог крепкого здоровья людей.
Отличительные черты и параметры
Природа мудро распределила функциональные обязанности симпатического и парасимпатического отделов вегетативной нервной системы – согласно расположению их ядер и волокон, а также предназначению и ответственности. К примеру, центральные нейроны симпатического сегмента размещены исключительно в боковых рогах спинного мозга. У парасимпатического же они локализуются в стволе полушарий.

Отдаленные, эффекторные нейроны в первом случае всегда расположены на периферии – присутствуют в околопозвонковых ганглиях. Они формируют различные сплетения, самым важным из которых признано солнечное. Оно несет ответственность за иннервацию внутрибрюшных органов. Тогда как парасимпатические эффекторные нейроны располагаются непосредственно в иннервируемых ими органах. Поэтому и ответные реакции на посылаемые к ним из мозга импульсы наступают быстрее.
Различия можно наблюдать и в функциональных характеристиках. Энергичная деятельность человека требует активации сердца, сосудов, легких – усиливается деятельность симпатических волокон. Однако, в этом случае происходит торможение процессов пищеварения.
В покое же за иннервацию внутриполостных органов отвечает парасимпатика – восстанавливается пищеварение, гомеостаз, мочевыделение. Недаром, после плотного обеда хочется полежать и поспать. В тесном сотрудничестве обоих отделов и заключается единство и неделимость нервной системы.
Структурные единицы
Главные центры вегетативной системы локализуются:
- мезэенцефальный отдел – в структурах среднего мозга, от которого они отходят волокном глазодвигательного нерва;
- бульбарный сегмент – в тканях продолговатого мозга, который далее представлен, как лицевой, так и блуждающий, языкоглоточный нерв;
- торако-люмбальный отдел – поясничные и грудные ганглии в спинномозговых сегментах;
- сакральный сегмент – в крестцовом отделе, парасимпатическая нервная система иннервирует тазовые органы.
Симпатический отдел выводит нервные волокна из головного мозга до пограничного сегмента – паравертебральными ганглиями в районе спинного мозга. Его называют симптоматический ствол, поскольку в нем имеется несколько узлов, каждый из которых взаимосвязан с отдельными органами через нервные сплетения. Передача импульса с нервных волокон на иннервируемую ткань происходит через синапсы – с помощью особых биохимических соединений, симпатинов.
Парасимпатический отдел, помимо внутричерепных центральных ядер представлен:
- преганглионарные нейроны и волокна – пролегают в составе черепно-мозговых нервов;
- постагнглионарные нейроны и волокна – проходят до иннервируемых структур;
- терминальные узлы – расположены вблизи внутриполостных органов или непосредственно в их тканях.
Периферическая нервная система, представленная двумя отделами, практически не поддается сознательному контролю и функционирует самостоятельно, поддерживая постоянство гомеостаза.
Суть взаимодействия
Для того чтобы человек мог приспособиться и адаптироваться к любой ситуации – внешней либо внутренней угрозе, симпатическая, а также парасимпатическая части вегетативной нервной системы должны тесно взаимодействовать. Однако, при этом они оказывают на организм человека прямо противоположное воздействие.

Для парасимпатики характерно:
- понижать артериальное давление;
- уряжать частоту дыхания;
- расширять просвет сосудов;
- сужать зрачки;
- корректировать концентрацию глюкозы в кровяном русле;
- улучшать пищеварительный процесс;
- тонизировать гладкую мускулатуру.
Защитные рефлексы также во введении парасимпатической деятельности – чихание, кашель, позывы на рвоту. Для симпатического отдела вегетативной нервной системы присуще повышать параметры сердечнососудистой системы – частоту пульса и цифры артериального давления, усиливать обмен веществ.
О том, что преобладает симпатикоотдел, человек узнает по ощущению жара, тахикардии, беспокойному сну и страху смерти, потоотделению. Если активна больше парасимпатика, изменения будут иными – холодная, влажная кожа, брадикардия, обморочность, чрезмерное слюноотделение и одышка. При уравновешенном функционировании обоих отделов деятельность сердца, легких, почек, кишечника соответствует возрастной норме и человек ощущает себя здоровым.
Функции
Природой определено так, что симпатический отдел принимает активное участие во многих важных процессах организма людей – особенно двигательного состояния. За ним преимущественно закреплена роль мобилизовать внутренние ресурсы, чтобы преодолеть различные препятствия. К примеру, активирует сфинктер радужной оболочки, зрачок расширяется, и поток поступающей информации усиливается.
При возбуждении симпатической нервной системы расширяются бронхи для усиления поступления кислорода к тканям, к сердцу поступает больше крови, тогда как на периферии артерии и вены становятся узкими – перераспределение питательных веществ. Одновременно происходит выброс депонированной крови из селезенки, а также расщепление гликогена – мобилизация дополнительных источников энергии. Угнетению же будут подвержены пищеварительные и мочевыделительные структуры – усвоение питательных веществ в кишечнике замедляется, ткани мочевого пузыря расслабляется. Все усилия организма направлены на поддержания высокой активности мускулатуры.
Парасимпатическое влияние на сердечную деятельность будет выражаться в восстановлении ритма и сокращений, нормализации кровяной регуляции – артериальное давление соответствует привычным для человека параметрам. Коррекции будет подвержена дыхательная система – бронхи сужаются, гипервентиляция прекращается, а концентрация глюкозы в кровяном русле снижается. Одновременно усиливается моторика в петлях кишечника – продукты усваиваются быстрее, а полые органы освобождаются от содержимого – дефекация, мочеиспускание. Дополнительно парасимпатика повышает секрецию слюны, но уменьшает потоотделение.
Нарушения и патологии
Строение вегетативной системы в целом – это сложные сплетение нервных волокон, которые действуют сообща для сохранения стабильности внутри организма. Поэтому даже незначительное повреждение одного из центров будет негативно отражаться на иннервации внутренних органов в целом. К примеру, при высоком тонусе симпатической нервной системы в кровь людей постоянно поступает огромное количество гормонов надпочечников, что провоцирует скачки артериального давления, тахикардию, потливость, гипервозбуждение, быстрое истощение сил. Тогда как вялость и сонливость, повышенный аппетит и гипотония будут признаками сбоев в вегетативном отделе.

Клинические признаки заболеваний периферической нервной системы напрямую связаны с уровнем, на котором произошло поражение нервного волокна и причины – воспаления, инфекции, либо травмы, опухолевого процесса. Характерные симптомы воспаления – отек тканей, болевой синдром, повышение температуры, нарушения движений в той части тела, которую иннервирует сегмент. Специалист обязательно учитывает возможность иррадиции признаков – их удаленность от первичного очага болезни. К примеру, изменения в глазодвигательном нерве могут выражаться в опущении век, усиления слезовыделения, затрудненности движений глазного яблока.
Если страдает симпатическая НС в районе малого таза, что присуще детям – то формируется энурез, кишечная непроходимость. Или же проблемы с репродуктивной системой у взрослых. При травмах в клинической картине будут преобладать повреждения тканей, кровотечения, а в последующем парезы и параличи.
Принципы лечения
Подозрения на расстройства симпатической системы либо парасимпатического отдела должны быть обязательно подтверждены осмотром невропатолога, результатами лабораторных и инструментальных исследований.
Только после оценки общего состояния здоровья человека, выявления причин заболевания, специалист подберет оптимальную схему терапии. При диагностированной опухоли, ее удалят оперативным образом или же подвергнут лучевой, химиотерапии. Для ускорения реабилитации после травмы врач назначит физиотерапевтические процедуры, препараты, способные ускорять регенерацию, а также средства для предупреждения вторичного инфицирования.
Если симпатическая нервная структура страдает от избытка выделения гормонов, эндокринолог подберет медикаменты для изменения концентрации их в кровяном русле. Дополнительно назначают отвары и настои целебных трав с успокоительным эффектом – мелисса, ромашка, а также мята, валериана. По индивидуальным показаниям прибегают к помощи антидепрессантов, антиконвульсантов либо нейролептиков. Наименования, дозы и продолжительность лечения – прерогатива невропатолога. Самолечение абсолютно недопустимо.
Отлично зарекомендовало себя санаторно-курортное лечение – грязелечение, водолечение, гирудотерапия, радоновые ванны. Комплексное воздействие изнутри – отдых, правильное питание, витамины и снаружи – целебные обвертывания травами, грязями, ванны с лечебной солью, приводят в норму все отделы периферической нервной системы.
Профилактика
Лучшим лечением любой болезни, безусловно, является профилактика. Для предупреждения функциональных сбоев в иннервации того или иного органа, специалисты рекомендуют людям соблюдать основные принципы здорового образа жизни:
- отказаться от вредных привычек – употребления табачной, алкогольной продукции;
- хорошо высыпаться – не менее 8–9 часов сна в проветриваемом, затемненном, спокойном помещении;
- скорректировать рацион – преобладание овощей, различных фруктов, зелени, злаковых культур;
- соблюдение водного режима – прием не менее 1.5–2 л очищенной воды, соков, морсов, компотов, чтобы из тканей удалялись токсины и шлаки;
- ежедневная активность – пешие долгие прогулки, посещение бассейна, спортивного зала, освоение йоги, пилатеса.
У человека, который тщательно следит за своим здоровьем, посещает врача для ежегодного медицинского осмотра, нервы будут спокойными на любом их уровне. Поэтому и о таких проблемах, как потливость, тахикардия, одышка, высокое давление они знают только понаслышке, от своих родственников.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
В основу гипотезы, объясняющей повышение симпатической активности при заболеваниях почек, легли результаты экспериментальных исследований Campese et al. [2,3]. Спустя неделю после субтотальной нефрэктомии у крыс (экспериментальная модель ХПН) стойко повышалось АД. Давление удавалось значительно снизить при ризотомии (перерезке чувствительных корешков спинномозговых нервов) либо при двусторонней нефрэктомии. Можно предположить, что в ответ на возбуждение баро– и хеморецепторов поврежденной почки афферентный сигнал передается в центры гипоталамуса, регулирующие АД. Это, в свою очередь, вызывает повышение эфферентной симпатической активности (рис. 1).
Рис. 1. Симпатическая активность при хронической почечной недостаточности и ее подавление препаратами-симпатолитиками
В иннервируемых симпатическими нервами органах и тканях, включая почки, наряду с норадреналином действуют его котрансмиттеры – АТФ и нейропептид Y. Все три вещества вызывают вазоконстрикцию, активируя специфические мембранные рецепторы гладких миоцитов сосудов. Кроме того, стимуляция b –адренорецепторов индуцирует пролиферативные процессы в почечной ткани, а АТФ оказывает митогенное действие на миоциты сосудов и эпителиоциты клубочков почек.
Закономерно возникает вопрос, может ли медикаментозное подавление симпатической активности при ХПН оказать комплексный благоприятный эффект – как за счет предупреждения прогрессирования нефропатии, так и за счет нормализации АД?
Проведенные Amman et al. [4] эксперименты показали, что симпатолитик центрального действия, селективный агонист имидазолиновых рецепторов моксонидин в малых дозах значительно замедляет развитие гломерулосклероза и поражения почечных сосудов. Иными словами, антигипертензивный эффект является для этого препарата основным, но не единственным.
Безусловно, клиницистов в первую очередь интересует возможность предотвратить с помощью моксонидина обусловленное гиперактивностью симпатической нервной системы прогрессирование поражения почек у человека.
В последнее время в развитых странах основной причиной развития ХПН становится диабетическая нефропатия. Инсулинотерапия продлевает жизнь больных диабетом, но, к сожалению, не предотвращает полностью развитие поздних осложнений этого заболевания. Согласно эпидемиологическим данным, нефропатия отмечается более чем у 30% больных инсулинозависимым диабетом, приводя в итоге к терминальной почечной недостаточности.
Первым проявлением диабетической нефропатии является микроальбуминурия – экскреция белка с мочой в количестве 30–300 мг/сут или 20–200 мкг/мин. Поскольку микроальбуминурия, как правило, сопровождается повышением АД, жесткий контроль давления на начальной стадии нефропатии играет важную роль в предупреждении дальнейшего прогрессирования поражения почек. Препаратами выбора при лечении гипертонии у диабетиков принято считать ингибиторы АПФ и антагонисты рецепторов ангиотензина II. Согласно последним клиническим рекомендациям больным диабетом при наличии микроальбуминурии следует принимать антигипертензивные препараты указанных групп, даже если у них нормальное давление. Однако и на этом фоне у значительной части пациентов нефропатия прогрессирует. Поэтому продолжается активный поиск новых лекарственных средств, более эффективно предотвращающих ухудшение состояния почек.
Одним из наиболее известных клинических исследований такого рода является рандомизированное перекрестное плацебо–контролируемое исследование, выполненное Strojek et al. [5]. В него вошли 15 больных с нормальным АД, которые длительное время страдали компенсированным инсулинозависимым диабетом, сопровождающимся микроальбуминурией (табл. 1). В течение 3 недель участники принимали моксонидин (0,2 мг 2 раза в день) либо плацебо. В конце каждой фазы исследования определяли показатель суточной экскреции альбумина (СЭА) по моче, собранной за ночь. Факторы, способные повлиять на величину СЭА (потребление белка и натрия с пищей, уровень гликемии), контролировались и поддерживались на постоянном уровне. По окончании каждой фазы среднесуточные показатели АД (табл. 2), а также скорость клубочковой фильтрации, оцениваемая по клиренсу креатинина, остались неизменными. В то же время после курса лечения моксонидином было отмечено значительное (p Рис. 2. Влияние моксонидина на состояние эндотелия у больных сАГ и микроалъбуминурией. Скорость экскреции альбумина с мочой в конце периодов вмешательства (определяемая по моче, собранной за ночь). Индивидуальные данные представлены, как средние значения 3-х измерений: • - больные, получавшие сначала плацебо, затем моксонидин; • - больные, получавшие сначала моксонидин, затем плацебо. Очевидно, что эффект моксонидина проявляется независимо от последовательности приема препаратов.
Следует подчеркнуть, что в данном исследовании не ставилась цель добиться максимального снижения альбуминурии. Его задачей было доказать, что симпатолитик в малой дозе способен эффективно снизить альбуминурию. Полученные данные ясно указывают на возможность и перспективность нового подхода в лечении диабетической нефропатии – воздействия на симпатическую нервную систему
Среди причин ХПН на втором месте по распространенности стоит артериальная гипертония (АГ). В последние годы частота ХПН, как осложнения гипертонии возросла на 16–26%. Микроальбуминурия встречается приблизительно у каждого четвертого больного с АГ, даже при отсутствии сопутствующих нарушений углеводного обмена. Предполагается, что микроальбуминурия, независимый предиктор сердечно–сосудистых осложнений и общей смертности при АГ, является маркером системной дисфункции эндотелия. Последняя способствует отложению атерогенных частиц липопротеинов в артериальной стенке.
Прием большинства современных антигипертензивных средств (в первую очередь ингибиторов АПФ) уменьшает повышенную экскрецию альбумина с мочой, но не нормализует ее. Поскольку в настоящее время целями терапии АГ считаются не только снижение АД, но и коррекция таких прогностически значимых факторов, как микроальбуминурия, дислипидемия, инсулинорезистентность, эндотелиальная дисфункция, возникает потребность в препаратах, обладающих комплексным положительным действием. Весьма перспективен в данном отношении агонист имидазолиновых рецепторов I типа моксонидин (Физиотенз), антигипертензивный препарат центрального действия, благоприятно влияющий на углеводный обмен.
Было проведено исследование [6] по оценке влияния терапии моксонидином на экскрецию альбумина с мочой, а также на уровни таких маркеров эндотелиальной дисфункции, как тромбомодулин (ТМ) и ингибитор–1 тканевого активатора плазминогена (ИАП–1), при мягкой и умеренной АГ, сопровождающейся микроальбуминурией. В клиническое испытание вошли 58 пациентов (32 мужчины, 26 женщин) в возрасте 56,6±8,2 лет, с индексом массы тела (ИМТ) 23,8±3,1 кг/м 2 и АД 152±15/98±5 мм рт.ст. Спустя 6 месяцев лечения моксонидином в суточной дозе 0,2–0,4 мг у всех участников нормализовалось АД (табл. 3). СЭА уменьшилась до 24,5±6,4 мкг/мин (при исходном уровне 32,3±7,2 мкг/мин; p Рис. 3. Влияние моксонидина на состояние эндотелия у больных с АГ и микроальбуминурией.
Полученные результаты свидетельствуют о благоприятном действии моксонидина на функцию почек и функцию эндотелия у больных АГ, сопровождающейся микроальбуминурией.
Безусловно, необходимы новые контролируемые испытания, с участием большего числа пациентов и более длительным сроком наблюдения, чтобы утверждать: блокада симпатической нервной системы предотвращает развитие нефропатии различной этиологии. Тем не менее, уже получены доказательства эффективности лекарственных средств, подавляющих симпатическую активность – в частности, такого препарата, как Физиотенз.
Обзор подготовлен О.В. Вихиревой ГНИЦ профилактической медицины МЗ РФ, Москва
1. Rump LC. The role of sympathetic nervous activity in chronic renal failure. J Clin Basic Cardiol 2001;4:179–81.
2. Campese VM, Kogosow E. Renal afferent denervation prevents hypertension in rats with chronic renal failure. Hypertension 1995;25:878–82.
3. Campese VM. Neurogenic factors and hypertension in renal disease. Kidney Int 2000;57 (Suppi 75):S2–S6.
4. Amman K, Rump LC, Simonavicience A, Oberhauser V, Wessels S, Orth SR, Gross ML, Koch A, Bielenberg GW, van Kats JP, Ehmke H, Mall G, Ritz E. Effects of low dose sympathetic inhibition on glomerulosclerosis and albuminuria in subtotally nephrectomised rats. J Am Soc Nephrol 2000;! 1:1469–78.
5. Strojek К, Greszczak W, Gorska J, Leschinger MI, Ritz E. Lowering of microalbuminuria in diabetic patients by a sympathoplegic agent: novel approach to prevent progression of diabetic nephropathy? J Am Soc Nephrol 2001;12:602–5.
6. Krespi PG, Makris TK, Hatzizacharias AN, Triposkiadis P, Tsoukala C, Kyriaki D, Votteas V, Kyriakidis M. Moxonidine effect on microalbuminuria, thrombomodulin, and plasminogen activator inhibitor–1 levels in patients with essential hypertension. Cardiovasc Drugs Ther 1998; 12:463–7.
Типы и виды действия лекарственных средств
Для лекарственных веществ характерны специфические виды фармакологического действия:
4. Угнетающее действие
При поступлении в организм ЛВ между ними и чувствительными структурами организма возникает несколько типов межмолекулярных химических связей. ЛВ связываются с чувствительными структурами организма при помощи ионных, водородных или гидрофобных сил, действие ЛВ в таком случае будет не продолжительным с обратимым типом действия. Именно поэтому лекарственные вещества некоторые- нитроглицерин действуют в течении нескольких минут. Действие других ЛВ более продолжительное- измеряется часами или сутками- анальгин. Наиболее прочные связи между ЛВ и организмом- ковалентные. Такие лекарства обладают необратимым типом действия, которое выраженно в глубоких структурных нарушениях клеток и в их гибели, такое действие осуществляют на организм соли тяжелых металлов( серебро, а также нитрат серебра- при сжигании бородавок). Возбуждающие и угнетающие типы действия лекарственных средств являются результатом взаимодействия лекарств, с клетками тканей и органов при которых возникает стимуляция или ингибирование(блокирование) различных рецепторов. Примерами возбуждающего типа являются психо стимуляторы центральной нервной системы- кофеин, а также адреноменетики- фенилэфрин, аналептики- сульфокамфкаин, а также слабительные(бисокадил). Примерами угнетающего типа действия лекарств могут служить миорелаксанты (аминозин), препараты понижающие АД(капотен, каптоприл), снотворные. Обратимость, необратимость ЛВ зависят от режима дозирования лекарственных средств, величины дозы, частоты и длительности курсового применения.
По степени выраженности эффекта и клинического проявления различают: главное и побочное действие лекарственных средств. Главное действие-
(нейротропные гипотензивные средства)
Высшие центры симпатической нервной системы расположены в гипоталамусе. Отсюда возбуждение передается к центру симпатической нервной системы, расположенному в ростровентролатеральной области продолговатого мозга (RVLM — rostro-ventrolateral medulla), традиционно называемому сосудодвигательным центром. От этого центра импульсы передаются к симпатическим центрам спинного мозга и далее по симпатической иннервации к сердцу и кровеносным сосудам. Активация этого центра ведет к увеличению частоты и силы сокращений сердца (увеличение сердечного выброса) и к повышению тонуса кровеносных сосудов — повышается артериальное давление.
Снизить артериальное давление можно путем угнетения центров симпатической нервной системы или путем блокады симпатической иннервации. В соответствии с этим нейротропные гипотензивные средства делят на средства центрального и периферического действия.
К гипотензивным средствам центрального действия относят кло-нидин, моксонидин, гуанфацин, метилдопу.
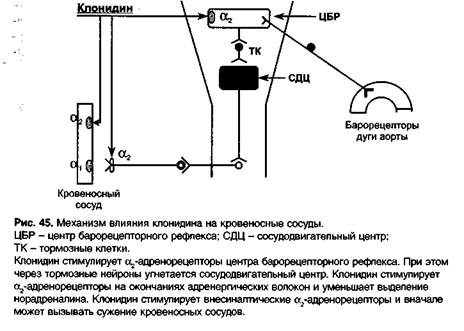
Клонидин (клофелин, гемитон) — а2-адреномиметик, стимулирует а2А-адренорецепторы в центре барорецепторного рефлекса в продолговатом мозге (ядра солитарного тракта). При этом возбуждаются центры вагуса (nucleus ambiguus) и тормозные нейроны, которые оказывают угнетающее влияние на RVLM (сосудодвигательный центр). Кроме того, угнетающее влияние клонидина на RVLM связано с тем, что клонидин стимулирует I1-рецеттгоры (имидазолиновые рецепторы).
В результате увеличивается тормозное влияние вагуса на сердце и снижается стимулирующее влияние симпатической иннервации на сердце и сосуды. Вследствие этого снижается сердечный выброс и тонус кровеносных сосудов (артериальных и венозных) — снижается артериальное давление.
Отчасти гипотензивное действие клонидина связано с активацией пресинаптических а2-адренорецепторов на окончаниях симпатических адренергических волокон — уменьшается высвобождение норадреналина.
В более высоких дозах клонидин стимулирует внесинаптические а2B-адренорецепторы гладких мышц кровеносных сосудов (рис. 45) и при быстром внутривенном введении может вызывать кратковременное сужение сосудов и повышение артериального давления (поэтому внутривенно клонидин вводят медленно, в течение 5-7 мин).
В связи с активацией а2-адренорецепторов ЦНС клонидин оказывает выраженное седативное действие, потенцирует действие этанола, проявляет анальгетические свойства.
Клонидин — высокоактивное гипотензивное средство (терапевтическая доза при назначении внутрь 0,000075 г); действует около 12 ч. Однако при систематическом применении может вызывать субъективно неприятный седативный эффект (рассеянность мыслей, невозможность сосредоточиться), депрессию, снижение толерантности к алкоголю, брадикардию, сухость глаз, ксеростомию (сухость во рту), констипацию, импотенцию. При резком прекращении приемов препарата развивается выраженный синдром отмены: через 18—25 ч артериальное давление повышается, возможен гипертензивный криз. β-Aдpeнoблoκaтopы усиливают синдром отмены клонидина, поэтому совместно эти препараты не назначают.
Применяют клонидин в основном для быстрого снижения артериального давления при гипертензивных кризах. В этом случае клонидин вводят внутривенно в течение 5—7 мин; при быстром введении возможно повышение артериального давления из-за стимуляции а2-адренорецепторов сосудов.
Растворы клонидина в виде глазных капель используют при лечении глаукомы (уменьшает продукцию внутриглазной жидкости ).
Моксонидин(цинт) стимулирует в продолговатом мозге имидазолиновые 11-рецепторы и в меньшей степени а2-адренорецепторы. В результате снижается активность сосудодвигательного центра, уменьшается сердечный выброс и тонус кровеносных сосудов -артериальное давление снижается.
Препарат назначают внутрь для систематического лечения артериальной гипертензии 1 раз в сутки. В отличие от клонидина при применении моксонидина менее выражены седативный эффект, сухость во рту, констипация, синдром отмены.
Гуанфацин(эстулик) аналогично клонидину стимулирует центральные а2-адренорецепторы. В отличие от клонидина не влияет на 11-рецепторы. Длительность гипотензивного эффекта около 24 ч. Назначают внутрь для систематического лечения артериальной гипертензии. Синдром отмены выражен меньше, чем у клонидина. 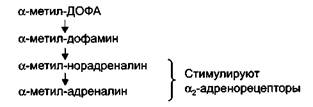
Метилдопа(допегит, альдомет) по химической структуре — а-метил-ДОФА. Препарат назначают внутрь. В организме метилдопа превращается в метилнорадреналин, а затем в метиладрена-лин, которые стимулируют а2-адренорецепторы центра барорецеп-торного рефлекса.
Гипотензивный эффект препарата развивается через 3—4 ч и продолжается около 24 ч.
Побочные эффекты метилдопы: головокружение, седативное действие, депрессия, заложенность носа, брадикардия, сухость во рту, тошнота, констипация, нарушения функции печени, лейкопения, тромбоцитопения. В связи с блокирующим влиянием а-метил-дофамина на дофаминергическую передачу возможны: паркинсонизм, повышенная продукция пролактина, галакторея, аменорея, импотенция (пролактин угнетает продукцию гонадотропных гормонов). При резком прекращении приема препарата синдром отмены проявляется через 48 ч.
Средства, блокирующие периферическую симпатическую иннервацию.
Для снижения артериального давления симпатическая иннервация может быть блокирована на уровне: 1) симпатических ганглиев, 2) окончаний постганглионарных симпатических (адренерги-ческих) волокон, 3) адренорецепторов сердца и кровеносных сосудов. Соответственно применяют ганглиоблокаторы, симпатолитики, ад-реноблокаторы.
Ганглиоблокаторы - гексаметония бензосульфонат(бензо-гексоний), азаметоний(пентамин), триметафан(арфонад) блокируют передачу возбуждения в симпатических ганглиях (блокируют NN-xo-линорецепторы ганглионарных нейронов), блокируют NN -холинорецепторы хромаффинных клеток мозгового вещества надпочечников и уменьшают выделение адреналина и норадреналина. Таким образом, ганглиоблокаторы уменьшают стимулирующее влияние симпатической иннервации и катехоламинов на сердце и кровеносные сосуды. Происходит ослабление сокращений сердца и расширение артериальных и венозных сосудов — артериальное и венозное давление снижается. Одновременно ганглиоблокаторы блокируют парасимпатические ганглии; таким образом устраняют тормозное влияние блуждающих нервов на сердце и обычно вызывают тахикардию.
Для систематического применения ганглиоблокаторы мало пригодны из-за побочных эффектов (выраженная ортостатическая ги-потензия, нарушение аккомодации, сухость во рту, тахикардия; возможны атония кишечника и мочевого пузыря, нарушение половых функций).
Гексаметоний и азаметоний действуют 2,5—3 ч; вводятся внутримышечно или под кожу при гипертензивных кризах. Азаметоний вводят также внутривенно медленно в 20 мл изотонического раствора натрия хлорида при гипертензивном кризе, отеке мозга, легких на фоне повышенного артериального давления, при спазмах периферических сосудов, при кишечной, печеночной или почечной коликах.
Триметафан действует 10—15 мин; вводится в растворах внутривенно капельно для управляемой гипотензии при хирургических операциях.
Симпатолитики— резерпин, гуанетидин(октадин) уменьшают выделение норадреналина из окончаний симпатических волокон и таким образом снижают стимулирующее влияние симпатической иннервации на сердце и сосуды — снижается артериальное и венозное давление. Резерпин снижает содержание норадреналина, дофамина и серотонина в ЦНС, а также содержание адреналина и норадреналина в надпочечниках. Гуанетидин не проникает через гематоэнцефалический барьер и не изменяет содержания ка-техоламинов в надпочечниках.
Оба препарата отличаются длительностью действия: после прекращения систематического приема гипотензивный эффект может сохраняться до 2 нед. Гуанетидин значительно эффективнее резерпина, но из-за выраженных побочных эффектов применяется редко.
В связи с избирательной блокадой симпатической иннервации преобладают влияния парасимпатической нервной системы. Поэтому при применении симпатолитиков возможны: брадикардия, по-выщение секреции НС1 (противопоказаны при язвенной болезни), диарея. Гуанетидин вызывает значительную ортостатическую гипотензию (связана со снижением венозного давления); при применении резерпина ортостатическая гипотензия мало выражена. Резерпин снижает уровень моноаминов в ЦНС, может вызывать седативный эффект, депрессию.
а-Лдреноблокаторы уменьшают сможнотимулирующее влияние симпатической иннервации на кровеносные сосуды (артерии и вены). В связи с расширением сосудов снижается артериальное и венозное давление; сокращения сердца рефлекторно учащаются.
a1-Адреноблокаторы — празозин(минипресс), доксазозин, тера-зозинназначают внутрь для систематического лечения артериальной гипертензии. Празозин действует 10—12 ч, доксазозин и тера-зозин —18—24 ч.
Побочные эффекты a1-адреноблокаторов: головокружение, заложенность носа, умеренная ортостатическая гипотензия, тахикардия, учащенное мочеиспускание.
a1 a2-Адреноблокатор фентоламинприменяют при феохромоцитоме перед операцией и во время операции удаления феохромоци-томы, а также в случаях, когда операция невозможна.
β -Адреноблокаторы — одна из наиболее употребительных групп антигипертензивных средств. При систематическом применении вызывают стойкий гипотензивный эффект, препятствуют резким подъемам артериального давления, практически не вызывают ортостатической гипотензии, обладают помимо гипотензивных свойств, антиангинальными и противоаритмическими свойствами.
β -Адреноблокаторы ослабляют и урежают сокращения сердца — систолическое артериальное давление снижается. Одновременно β -адреноблокаторы суживают кровеносные сосуды (блок β2 -адрено-рецепторов). Поэтому при однократном применении р-адреноблока-торов среднее артериальное давление снижается обычно незначительно (при изолированной систолической гипертензии артериальное давление может снизиться и после однократного применения β -адре-ноблокаторов).
Однако если р-адреноблокаторы применяют систематически, то через 1 —2 нед сужение сосудов сменяется их расширением — артериальное давление снижается. Расширение сосудов объясняют тем, что при систематическом применении р-адреноблокаторов в связи с уменьшением сердечного выброса восстанавливается барорецептор-ный депрессорный рефлекс, который при артериальной гипертензии бывает ослаблен. Кроме того, расширению сосудов способствуют уменьшение секреции ренина юкстагломерулярными клетками почек (блок β 1-адренорецепторов), а также блокада пресинаптических β 2-адренорецепторов в окончаниях адренергических волокон и уменьшение вьщеления норадреналина.
Для систематического лечения артериальной гипертензии чаще применяют β 1 -адреноблокаторы длительного действия — атенолол(тенормин; действует около 24 ч), бетаксолол(действует до 36 ч).
Побочные эффекты р-адреноблокаторов: брадикардия, сердечная недостаточность, затруднение атриовентрикулярной проводимости, снижение уровня ЛПВП в плазме крови, повышение тонуса бронхов и периферических сосудов (менее выражено у β 1 -адреноблокаторов), усиление действия гипогликемических средств, снижение физической активности.
a2 β -Адреноблокаторы - лабеталол(трандат), карведилол(дилатренд) уменьшают сердечный выброс (блок р-адренорецепто-ров) и снижают тонус периферических сосудов (блок а-адреноре-цепторов). Препараты применяют внутрь для систематического лечения артериальной гипертензии. Лабеталол, кроме того, вводят внутривенно при гипертензивных кризах.
Карведилол применяют также при хронической сердечной недостаточности .
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Читайте также:


