Утолщение всех нервных стволов


Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Ультразвуковое исследование периферической нервной системы впервые начало применяться для диагностики заболеваний нервных стволов в конце 90-х годов прошлого столетия [1]. С началом использования этого метода стали понятными его неоспоримые преимущества по сравнению с другими способами диагностики. Электрофизиологические методы, такие как электромиография и нейромиография, традиционно признаются "золотым стандартом" для выявления патологии периферической нервной системы. Однако необходимо отметить, что информация, полученная в ходе перечисленных выше обследований, не дает представления о состоянии окружающих тканей, не указывает на характер и причину повреждения нервного ствола и не всегда точно отражает локализацию изменений [2, 3]. В то же время именно эти сведения помогают определить тактику консервативного или оперативного лечения.
Внедрение ультразвуковой сонографии в клиническую практику позволило с успехом восполнить пробелы в диагностике заболеваний периферических нервов. В настоящей статье представлен опыт ультразвукового исследования периферических нервов верхней и нижней конечностей, накопленный в нашей клинике.
Для ультразвуковых исследований используются датчики с частотой 7-17 МГц, но в некоторых случаях необходимо применение трансдьюсеров с более низкой частотой - 3-5 МГц. В процессе сканирования оценивают анатомическую целость нервного ствола, его структуру, четкость контуров нерва и состояние окружающих тканей. Все перечисленные пункты выше нужно обязательно отражать в протоколе исследования. В случае выявления патологических изменений в структуре нерва указывают вид повреждения (полное или частичное), зону и степень компрессии нервного ствола (отмечают уменьшение диаметра нерва и причину сдавления). При обнаружении объемного образования описывают его размеры и структуру, контуры, взаимоотношение с окружающими мягкими тканями, наличие или отсутствие кровотока.
Ультразвуковое исследование периферических нервов целесообразно начинать с поперечной проекции в точке, где нервный ствол легче всего идентифицировать, смещаясь затем в проксимальном и дистальном направлениях, оценивая структуру нерва на протяжении 5.
Изображение нерва имеет ряд характерных признаков. В поперечной проекции он выглядит как овальное или округлое образование с четким гиперэхогенным контуром и внутренней гетерогенной упорядоченной структурой ("соль - перец", "медовые соты") [4, 6, 7]. В продольной проекции нерв лоцируется в виде линейной структуры с четким эхогенным контуром, в составе которой правильно чередуются гипо- и гиперэхогенные полосы - "электрический кабель" [7]. Толщина периферических нервов вариабельна и составляет от 1 мм для пальцевых нервов до 8 мм для седалищного нерва.
Залогом успешного проведения ультразвукового обследования служит хорошее знание анатомии исследуемой области.
Основными нервными стволами, доступными ультразвуковому исследованию на верхней конечности, являются лучевой, срединный и локтевой нервы.
Лучевой нерв представляет собой самую большую ветвь задней порции плечевого сплетения. Визуализацию нерва осуществляют на задней и латеральной поверхностях плеча, где он сопровождает плечевую артерию. В средней трети плеча лучевой нерв огибает плечевую кость и непосредственно прилегает к ней в спиральном канале (рис. 1).
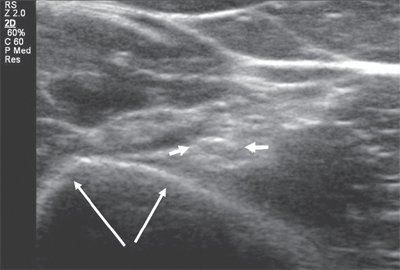
Рис. 1. Поперечная сонограмма лучевого нерва (короткие стрелки) на уровне спирального канала плечевой кости (длинные стрелки - контур плечевой кости).
Именно со спирального канала целесообразнее всего начинать процесс сканирования лучевого нерва. Как правило, для этого используются датчики с частотой 9-17 МГц, и исследование проводится преимущественно в поперечной проекции. Далее, тотчас кпереди от латерального надмыщелка плеча, n. radialis делится на чувствительную (или поверхностную) и двигательную (глубокую) ветви и задний межкостный нерв (рис. 2).
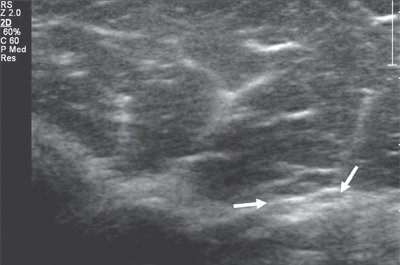
Рис. 2. Поперечная сонограмма на уровне дистального отдела плеча. Деление лучевого нерва на поверхностную и глубокую ветви (стрелки).
Поверхностная ветвь проходит по медиальному краю плечелучевой мышцы и сопровождается лучевой артерией и веной. В этом месте нерв наиболее доступен ультразвуковому исследованию, но только при условии использования датчиков высокой частоты (свыше 15 МГц), так как диаметр этой ветви очень мал.
Глубокая ветвь лучевого нерва проходит непосредственно в супинаторе, здесь нерв также доступен визуализации из-за разницы сонографической структуры между ним и окружающей его мышцей.
В дистальном отделе на разгибательной поверхности предплечья n. radialis (его поверхностная ветвь) заканчивается делением на 5 дорсальных пальцевых нервов. Ультразвуковое исследование пальцевых нервов можно осуществить только с использованием датчиков высокой частоты, но даже в этом случае получить отчетливое сонографическое изображение этих структур удается нечасто.
Срединный нерв формируется из латерального и медиального пучков плечевого сплетения. На плече n. medianus располагается в медиальной бороздке двуглавой мышцы кпереди от плечевой артерии. Срединный нерв является самым крупным нервом верхней конечности, поэтому его визуализация не представляет сложностей, однако легче всего можно получить ультразвуковое изображение нерва в области карпального канала, где он расположен поверхностно, а также на уровне локтевого сустава. В последнем случае в качестве маркера целесообразно использовать сосудистый пучок. В области локтевого сустава срединный нерв располагается медиальнее по отношению к более глубоко расположенным плечевой артерии и вене (рис. 3).
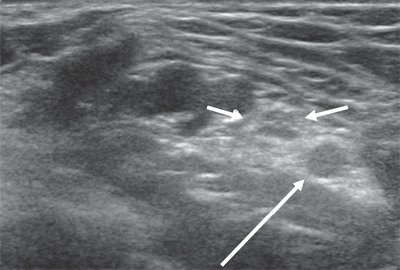
Рис. 3. Срединный нерв на уровне локтевого сустава в поперечной проекции (короткие стрелки). Рядом визуализируется плечевая артерия (длинная стрелка).
В проксимальном отделе предплечья нерв обычно проходит между двумя головками круглого пронатора. В области лучезапястного сустава срединный нерв располагается под сухожилием длинной ладонной мышцы и между сухожилиями сгибателей, проходя под удерживателем сгибателей на кисть через так называемый карпальный канал. Общие ладонные пальцевые нервы (их насчитывают три) образуются путем разветвления основного ствола срединного нерва на уровне дистального конца удерживателя сгибателей.
Локтевой нерв является главной ветвью медиального пучка плечевого сплетения. На плече n. ulnaris ветвей не дает. В области локтевого сустава нерв проходит через кубитальный канал, сформированный медиальным надмыщелком плеча и локтевым отростком. Здесь локтевой нерв прилегает непосредственно к кости и сверху покрыт только фасцией и кожей. При ультразвуковом исследовании области локтевого сустава следует обратить внимание на то, чтобы рука пациента располагалась свободно и не была согнутой. Это важно, поскольку при сгибании локтевого сустава до 90 диаметр нерва уменьшается за счет его растяжения.
На предплечье n. ulnaris обычно располагается между двумя головками локтевого сгибателя запястья, а в дистальном отделе предплечья нерв лежит между сухожилием локтевого сгибателя запястья медиально и латерально от локтевой артерии и вены. На кисть локтевой нерв попадает через канал локтевого нерва, называемый каналом Гийона. При прохождении через канал локтевой нерв сопровождается одноименными артерией и веной. В дистальном отделе канала Гийона нерв делится на глубокую моторную ветвь и поверхностную чувствительную, и именно поверхностную ветвь продолжает сопровождать локтевая артерия, что позволяет легче ориентироваться при ультразвуковом исследовании.
На нижней конечности при ультразвуковом сканировании можно без труда идентифицировать седалищный нерв и его ветви. В зарубежной литературе описывается также сонографическое исследование бедренного нерва. Необходимо отметить, что визуализация этого периферического нерва затруднена и лучшим акустическим окном является паховая область, где нерв сопровождает бедренные артерию и вену.
Седалищный нерв - самый большой из периферических нервов в организме человека. Фактически он состоит из двух крупных стволов: кнаружи находится общий малоберцовый нерв, медиально - большеберцовый нерв. Седалищный нерв выходит из полости малого таза через большое седалищное отверстие под грушевидной мышцей.
Уже в ягодичной области нерв доступен визуализации, необходимо только правильно определиться с частотой используемого датчика: при достаточной мышечной массе целесообразно применять датчики с частотой 2-5 МГц, если мышечная масса в ягодичной области не выражена, можно использовать датчики с большей частотой - 5-9 МГц. В области ягодичной складки седалищный нерв располагается близко к широкой фасции бедра, смещается латерально и далее лежит под длинной головкой двуглавой мышцы бедра, располагаясь между ней и большой приводящей мышцей (рис. 4).
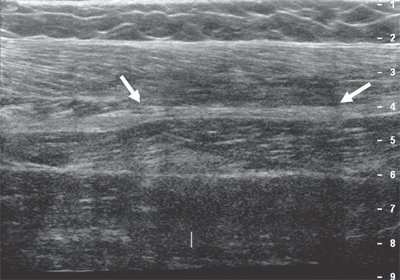
Рис. 4. Седалищный нерв (продольная проекция, панорамное сканирование) в средней трети бедра (стрелки).
В дистальных отделах бедра, чаще в верхнем углу подколенной ямки, нерв делится на две ветви: более толстую медиальную - большеберцовый нерв и более тонкую латеральную - общий малоберцовый нерв. Именно с этой области лучше всего начинать ультразвуковое исследование седалищного нерва и его ветвей.
Общий малоберцовый нерв, отделившись от основного ствола, спускается латерально под двуглавой мышцей бедра к головке бедренной кости. В области головки малоберцовой кости нерв располагается поверхностно, прикрыт только фасцией и кожей, здесь он также хорошо доступен визуализации (рис. 5).
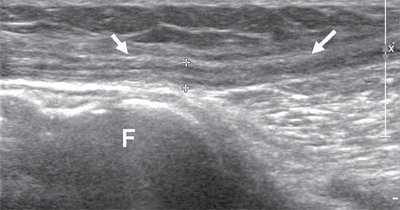
Рис. 5. Продольная сонограмма общего малоберцового нерва (стрелки) на уровне головки малоберцовой кости (F).
Далее общий малоберцовый нерв проникает в толщу проксимального отдела длинной малоберцовой мышцы и делится на две свои конечные ветви - поверхностный малоберцовый нерв и глубокий малоберцовый нерв. Визуализация конечных ветвей общего малоберцового нерва затруднена из-за их малого диаметра и отсутствия анатомических маркеров при их прохождении в толще мышц голени. Поверхностный малоберцовый нерв делится на конечные ветви (тыльные ветви стопы) на латеральной поверхности нижней трети голени. Глубокий малоберцовый нерв переходит на переднюю поверхность голени и здесь, располагаясь латерально, сопровождает передние малоберцовые сосуды. На тыл стопы нерв попадает под нижним удерживателем разгибателей и под сухожилием длинного разгибателя I пальца. Здесь он делится на концевые ветви. Для визуализации общего малоберцового нерва и его ветвей удобнее использовать датчики с частотой 9-17 МГц.
Большеберцовый нерв по своему направлению является продолжением седалищного нерва. В подколенной ямке нерв располагается над подколенными веной и артерией и несколько кнаружи от них (рис. 6).
Опухоли периферических нервов — опухолевые новообразования, поражающие ствол или оболочки нервов периферической нервной системы. Клинически проявляются парестезиями, болью, нарушением функции нерва (онемением и мышечной слабостью в зоне его иннервации). Диагностика включает клинический и неврологический осмотр, УЗИ, МРТ, электрофизиологические исследования. По показаниям проводится вылущивание опухоли или ее удаление вместе с участком нерва. При выявлении злокачественного характера новообразования оно удаляется вместе с нервным стволом в пределах интактных тканей.
- Причины опухолей периферических нервов
- Симптомы опухолей периферических нервов
- Основные виды опухолей периферических нервов
- Диагностика опухолей периферических нервов
- Лечение опухолей периферических нервов
- Цены на лечение
Общие сведения
Опухоли периферических нервов — достаточно редкая патология нервной системы. Встречаются у лиц любого возраста, чаще у взрослых. Наиболее распространены опухоли серединного, локтевого, бедренного и малоберцового нервов. В неврологии и онконейрохирургии основополагающим является разделение новообразований периферических нервных стволов на доброкачественные и злокачественные. Доброкачественными являются нейрофиброма, невринома (шваннома), перинейрома, злокачественными — нейрогенная саркома (злокачественная шваннома). Нейрофибромы зачастую носят множественный характер. В 50% случаев они ассоциированы с нейрофиброматозом Реклингхаузена. В отдельных случаях доброкачественные опухоли периферических нервов могут брать начало в жировых клетках (липомы) и в сосудах (ангиомы) эпиневрия. От опухолевых образований нервных стволов следует отличать интраневральный ганглий (ганглион, псевдоопухолевую кисту) нерва, представляющий собой внутриневральное скопление муцинозной жидкости, заключенное в плотную оболочку.
Периферические нервные стволы состоят из нервных волокон, каждое из которых покрыто слоем шванновских клеток. Нервные волокна внутри периферического нерва сгруппированы в отдельные пучки, окруженные соединительнотканной оболочкой - периневрием. Между пучками находится эпиневрий, представляющий собой рыхлую соединительнотканную структуру с расположенными в ней сосудами и скоплениями жировых клеток. Снаружи нервный ствол покрывает эпиневральная оболочка. Анатомически нервные волокна представляют собой отростки нейронов, расположенных в спинном мозге или нервных ганглиях. Сами нейроны в процессе своего развития утрачивают способность к восстановлению, но их отростки способны регенерировать. Таким образом, если тело нейрона сохранно и нервное волокно не имеет препятствий для роста, оно способно восстановиться.
В состав одного периферического нерва входят как безмиелиновые, так и миелиновые (мякотные) волокна. Последние имеют т. н. миелиновую оболочку, образованную слоями миелина, многослойно обворачивающими нервное волокно подобно рулону. Основная функция волокон — это проведение нервных импульсов, аналогично тому, как электрический ток движется по проводам. По миелиновым волокнам импульс проходит в 2-4 раза быстрее, чем по безмиелиновым. Если импульсы идут от центра к периферии, то такое волокно носит название эфферентное (двигательное), если импульсы проходят в обратную сторону, то волокно называется афферентное (чувствительное). Нервные стволы могут состоять только из афферентных или только из эфферентных волокон, но чаще они бывают смешанными.

Причины опухолей периферических нервов
Новообразования периферических нервных стволов возникают как результат бесконтрольного деления клеток различных тканей, входящих в структуру нерва. Так, невринома берет свое начало в шванновских клетках оболочки нервных волокон, нейрофиброма — в клетках соединительной ткани эпи- и периневрия, липома — в жировых клетках эпиневрия. Причины опухолевой трансформации нормально функционирующих клеток нервных стволов точно не известны. Предполагают онкогенное влияние радиации и хронического воздействия некоторых химических соединений, а также загрязненности окружающей среды. Ряд исследователей указывает на роль биологического фактора — онкогенного воздействия на организм отдельных вирусов. Кроме того, имеет значение пониженный фон противоопухолевой защиты организма. Провоцирующим триггером может выступать повреждение нерва вследствие травмы. Нельзя исключить и наследственно детерминированную предрасположенность к возникновению опухолей. Установлено, что у пациентов с нейрофибромами и болезнью Реклингхаузена имеются генные мутации в хромосоме 22, обуславливающие недостаточность фактора, ингибирующего опухолевую трансформацию шванновских клеток.
Симптомы опухолей периферических нервов
На ранних стадиях своего развития опухоли периферических нервов обычно имеют субклиническое течение. Типично медленное развитие опухолевого процесса. При поражении мелких ответвлений нервных стволов клинические проявления могут вообще отсутствовать.
Злокачественные опухоли периферических нервов характеризуются интенсивным болевым синдромом, усиливающимся при перкуссии и пальпации по ходу нерва. В зоне иннервации пораженного злокачественной опухолью нервного ствола отмечается неврологический дефицит — снижение силы иннервируемых мышц (парез), гипестезия (чувство онемения и сниженная болевая чувствительность кожи), трофические изменения (бледность, истончение, похолодание, повышенная ранимость кожи). При злокачественном характере новообразования нерва оно плотно спаяно с прилежащими тканями и не смещается относительно них.
Нейрофиброма — доброкачественное новообразование, развивающееся из фиброцитов соединительнотканных структур нервного ствола. Опухоль может быть единичной или множественной (чаще при нейрофиброматозе). Плексиформные нейрофибромы широко инфильтрируют ствол нерва и прилежащие ткани. Такие опухоли наиболее часто встречаются при болезни Реклингхаузена 1-го типа. В 5% случаев плексиформная нейрофиброма претерпевает злокачественную трансформацию.
Невринома (шваннома) — новообразование, берущее начало из шванновских клеток нерва. Чаще наблюдается в возрастном периоде от 30 до 60 лет. Представляет собой округлое утолщение нервного ствола. Обычно имеет единичный характер и медленный рост. Крайне редко отмечается малигнизация с возникновением нейрогенной саркомы.
Перинейрома (периневрома) — редкая доброкачественная опухоль из клеток периневрия. Имеет вид единичного или мультифокального утолщения нерва, протяженностью до 10 см.
Липома — не нейрогенная доброкачественная опухоль, развивающаяся из жировой ткани эпиневрия. Чаще встречается среди лиц, страдающих ожирением. Имеет желтую окраску и плотно срастается с нервным стволом. Не малигнизируется.
Нейрогенная саркома (нейрофибросаркома, злокачественная шваннома) — злокачественная опухоль из оболочек нерва, составляет 6,7% от общего числа сарком мягких тканей. По микроскопическому строению схожа с фибросаркомой. Более подвержены заболеванию лица мужского пола и среднего возраста. Нейрогенная саркома локализуется преимущественно на периферических нервах конечностей, реже — на шее. Редко метастазирует (примерно в 12-15% случаев). Наиболее типичны метастазы в легкие и лимфатические узлы. По микроскопическим особенностям выделяют железистый, меланоцитарный, эпителиоидный вариант опухоли.
Диагностика опухолей периферических нервов
В случае локализации опухоли в доступном для пальпирования месте предположительный диагноз может быть определен неврологом после проведенного осмотра. Для его уточнения, а также в случае глубокого расположения новообразования необходимо УЗИ, МРТ мягких тканей. В случае опухоли на УЗИ обнаруживается округлое или веретенообразное образование, локализующееся внутри нервного ствола или тесно связанное с ним.
Невриномы характеризуются ровным контуром, пониженной эхогенностью, неоднородностью структуры; при длительном существовании могут содержать кисты и кальцификаты. Нейрофибромы отличаются более однородной структурой, могут иметь волнистый контур. МРТ позволяет более точно и детально визуализировать опухоль, определить ее границы.
С целью оценки степени нарушения проведения нервных импульсов по пораженному участку нерва осуществляется электронейрография. Пункционная биопсия опухоли периферических нервов не проводится, поскольку провоцирует ускоренный рост и малигнизацию новообразования. Гистологическое исследование возможно при взятии образца ткани опухоли во время операции по ее удалению.
Лечение опухолей периферических нервов
Основным способом лечения новообразований периферических нервных стволов является радикальное хирургическое удаление опухоли. Однако, учитывая частое рецидивирование таких образований и травматичность оперативного вмешательства, нейрохирург рекомендует операцию только при наличии показаний. К последним относятся интенсивный болевой синдром, выраженное нарушение проводимости по пораженному нерву, сдавление опухолью сосудистого пучка, приводящее к ишемии конечности. Решение об операции в случае нейрофиброматоза Реклингхаузена чаще отрицательное, поскольку удаление нейрофибромы зачастую приводит к ее рецидиву и провоцирует рост других имеющихся опухолей.
Оперативные вмешательства в отношении доброкачественных новообразований подразделяются на 3 метода: вылущивание опухоли, ее резекция вместе с участком нервного ствола, краевая резекция нерва с опухолью. Последние два метода проводятся с наложением шва нерва. В ряде случаев образование большого дефекта при иссечении участка нервного ствола делает невозможным выполнение эпиневрального шва и требует проведения пластики нерва. При признаках злокачественности образования (отсутствие границ между опухолью и пучками нервных волокон, невозможность определить оболочки нерва), подтвержденных результатами интраоперационной экспресс-биопсии, проводится иссечение нерва с опухолью до границы здоровых тканей. В запущенных случаях может потребоваться ампутация конечности.
Болезнь Шарко-Мари-Тута болезнь Шарко Мари Тута, наследственная моторно-сенсорная невропатия I типа, наследственная нейропатия Шарко-Мари-Тута, ШМТ, невральная амиотрофия
Лечение болезни Шарко-Мари-Тута
Лечение назначается только после подтверждения диагноза врачом-специалистом. Показаны дозированная ЛФК и массаж, ортопедические мероприятия, витаминные препараты, средства нейротрофического действия, улучшающие микроциркуляцию, антихолинэстеразные препараты.
Имеются противопоказания. Необходима консультация специалиста.



- Аденозинтрифосфат натрия (средство, улучшающее метаболизм и энергообеспечение тканей). Режим дозирования: в/м, в первые 2-3 дня вводят 1 раз в день по 1 мл 1%-ного раствора, в последующие дни 2 раза в день или сразу 2 мл 1%-ного раствора 1 раз в день. На курс лечения — 30-40 инъекций.
- Пентоксифиллин (средство, улучшающее микроциркуляцию). Режим дозирования: внутрь, проглатывая целиком, во время или сразу после приема пищи, запивая достаточным количеством воды, в дозе 100 мг 3 раза в сутки с последующим медленным повышением дозы до 200 мг 2-3 раза в сутки.
- Мильгамма (комплекс витаминов группы В). Режим дозирования: терапию начинают с 2 мл внутримышечно 1 р/д на протяжении 5-10 дней. Поддерживающая терапия — 2 мл в/м два или три раза в неделю.
- Метандростенолон (анаболическое стероидное средство). Режим дозирования: внутрь, перед едой в дозе 0,005-0,01 г 1-2 раза в день. Курс лечения у взрослых длится 4-8 недель. Перерывы между курсами 4-8 недель.
- Церебролизин (ноотропное средство). Режим дозирования: применяют парентерально в виде в/м инъекций (до 5 мл) и в/в инъекций (до 10 мл). Препарат в дозе от 10 мл до 50 мл рекомендуется вводить только посредством медленных в/в инфузий после разведения стандартными растворами для инфузий. Продолжительность инфузий составляет от 15 до 60 мин. Вводят парентерально в дозе от 5 мл до 30 мл/сут. Рекомендуемый оптималь-ный курс лечения — ежедневные инъекции в течение 10-20 дней.
- Галантамин (антихолинэстеразное средство). Режим дозирования: внутрь, суточная доза для взрослых составляет 10-40 мг в 2-4 приема.
Формы болезни Шарко-Мари-Тута
Существует много форм болезни Шарко-Мари-Тута, включая CMT1, CMT2, CMT3, CMT4 и CMTX. CMT1, вызванный аномалиями в оболочке миелина, имеет три основных типа. CMT1A является аутосомно-доминантным заболеванием, которое возникает в результате дублирования гена на хромосоме 17, которая несет инструкции по производству периферического белка миелина-22 (PMP-22). Белок PMP-22 является критическим компонентом миелиновой оболочки. Сверхэкспрессия этого гена вызывает ненормальность структуры и функции миелиновой оболочки. Пациенты испытывают слабость и атрофию мышц нижних конечностей, начиная с подросткового возраста; позже они испытывают слабость рук и сенсорную потерю. Интересно, что другая невропатия, отличная от CMT1A, называемая наследственной невропатией с предрасположенностью к параличу давления (HNPP), вызвана удалением одного из генов PMP-22. В этом случае аномально низкие уровни гена PMP-22 приводят к эпизодической рецидивирующей демиелинизирующей нейропатии. CMT1B является аутосомно-доминантным заболеванием, вызванным мутациями в гене, который несет инструкции по изготовлению нуклеотида миелина (P0), который является еще одним критическим компонентом миелиновой оболочки. Большинство из этих мутаций являются точечными мутациями, что означает, что ошибка встречается только в одной букве генетического кода ДНК. На сегодняшний день ученые выявили более 120 различных точечных мутаций в гене P0. В результате аномалий в P0 CMT1B вызывает симптомы, сходные с симптомами, обнаруженными в CMT1A. Менее распространенные CMT1C, CMT1D и CMT1E, которые также имеют симптомы, сходные с симптомами, обнаруженными в CMT1A, вызваны мутациями в генах LITAF, EGR2 и NEFL соответственно.
Болезнь Шарко-Мари-Тута является результатом аномалий в аксоне периферической нервной клетки, а не в оболочке миелина. Он менее распространен, чем CMT1. CMT2A, наиболее распространенная аксоновская форма CMT, вызвана мутациями в Mitofusin 2, белке, связанном с митохондриальным слиянием. CMT2A также был связан с мутациями в гене, который кодирует белок 1B-бета-члена семейства кинезина, но в других случаях он не реплицируется. Кинезины — это белки, которые действуют как двигатели, чтобы помочь обеспечить транспортировку материалов вдоль клетки. Другие менее распространенные формы CMT2 были недавно идентифицированы и связаны с различными генами: CMT2B (связанный с RAB7), CMT2D (GARS). CMT2E (NEFL), CMT2H (HSP27) и CMT2l (HSP22).
CMT3 или Dejerine-Sottas — тяжелая демиелинизирующая невропатия, которая начинается в младенчестве. У младенцев происходит тяжелая атрофия мышц, слабость и сенсорные проблемы. Это редкое расстройство может быть вызвано определенной точечной мутацией в гене P0 или точечной мутацией в гене PMP-22.
CMT4 включает несколько различных подтипов аутосомно-рецессивного демиелинизирующего двигателя и сенсорных невропатий. Каждый подтип невропатии вызван другой генетической мутацией, может влиять на конкретную этническую популяцию и производит различные физиологические или клинические характеристики. Лица с CMT4 обычно развивают симптомы слабости ног в детстве, а в подростковом возрасте они не могут ходить. Несколько генов были идентифицированы как вызывающие CMT4, включая GDAP1 (CMT4A), MTMR13 (CMT4B1), MTMR2 (CMT4B2), SH3TC2 (CMT4C), NDG1 (CMT4D), EGR2 (CMT4E), PRX (CMT4F), FDG4 (CMT4H) и фиг.4 (CMT4J).
CMTX возникает точечной мутацией гена connexin-32 на Х-хромосоме. Коннексин-32-белок экспрессируется в клетках Schwann-клеток, которые обертывают нервные аксоны, составляя один сегмент миелиновой оболочки. Этот белок может участвовать в связи с клеткой Шванна с аксоном. Мужчины, которые наследуют один мутированный ген от своих матерей, проявляют умеренные или тяжелые симптомы заболевания, начиная с позднего детства или подросткового возраста (Y-хромосома, которую самцы наследуют от своих отцов, не имеет ген коннексин-32). Женщины, которые наследуют один мутированный ген от одного родителя и одного нормального гена от другого родителя, могут проявлять мягкие симптомы в подростковом возрасте или позже или вообще не могут развиваться симптомы заболевания.
Возможные осложнения ШМТ
Дыхание может быть затруднено, если болезнь поражает нервы, контролирующую диафрагму. Пациенту может понадобиться бронхолитические лекарственные средства или искусственная вентиляция легких. Избыточный вес или ожирение может затруднять дыхание.
Депрессия может быть результатом психического стресса, тревоги и разочарования жизни с любым прогрессирующим заболеванием. Когнитивная поведенческая терапия помогает пациентам лучше справляться с повседневной жизнью и, при необходимости, с депрессией.
Хотя ШМТ нельзя вылечить, некоторые меры помогут избежать дальнейших проблем. Они включают в себя хороший уход за ногами, так как существует повышенный риск травмы и инфекции, отказ от кофе, алкоголя и курения.
Понравилась новость? Читайте нас в Facebook
Приглашаем подписаться на наш канал в Яндекс Дзен
Как диагностировать ШМТ
Врач спросит о семейном анамнезе, и выявит признаки мышечной слабости — снижение мышечного тонуса, плоскостопие или высокий свод стоп (кавус).
Для исследования нервной проводимости проводится измерение силы и скорости электрических сигналов, которые проходят через нервы (Электромиография). Электроды помещаются на кожу, и вызывают слабые поражения электрическим током, которые стимулируют нервы. Задержанный или слабый ответ предполагает расстройство нервной системы, и, возможно, ШМТ.
При электромиографии (ЭМГ) тонкую иглу вводят в мышцы. Когда пациент расслабляет или сокращает мышцы, измеряется электрическая активность. Тестирование различных мышц покажет, какая из них страдает.
Генетическое тестирование проводится с помощью пробы крови, которая может показать, имеет ли пациент мутации гена.
Симптомы
Клиническая картина болезни имеет общие симптомы независимо от типа, но при этом может проявляться индивидуально. Даже в одной семье, когда заболевание провоцируется одним и тем же геном, у двух близких родственников оно далеко не всегда проявляется одинаково.
Общие симптомы болезни Шарко:
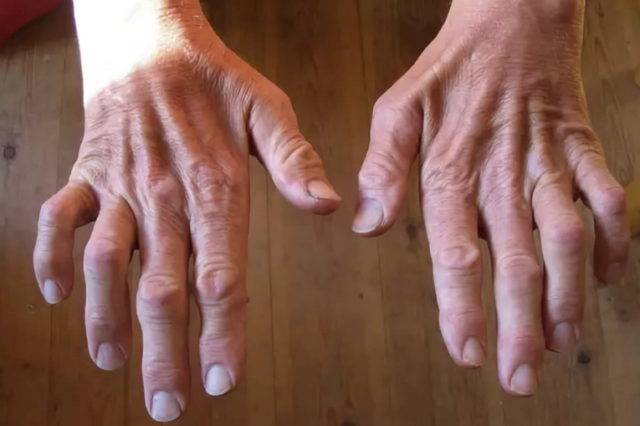
Дополнительные симптомы при 1-м типе болезни:
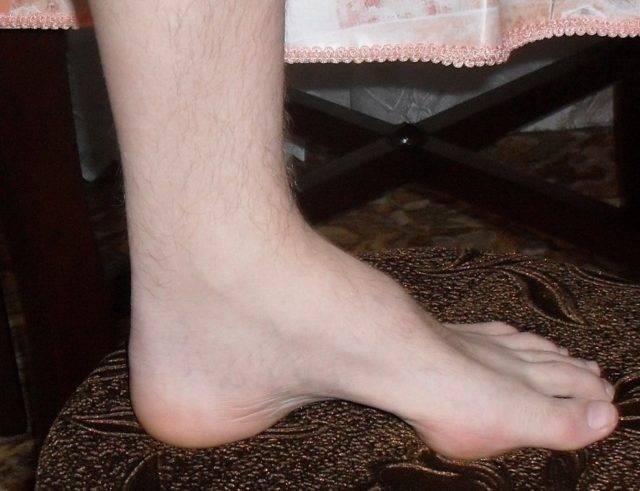
Особенности 2-го типа заболевания:
- изменения подъема стопы и формы пальцев встречаются реже, чем при 1-м типе;
- не наблюдаются утолщения нервных стволов;
- меньшая степень нарушения чувствительности;
- наблюдается синдром беспокойных ног перед сном;
- реже встречается ослабевание мышц в руках;
- возможно нарушение слуха (когда болезнь передается по женской линии);
- транзисторная энцефалопатия после физической активности на высоте: нарушения речи, шатание при ходьбе, затрудненное глотание, слабость проксимальных (ближних к туловищу) отделах конечностей.
Проявлением данной патологии обоих типов могут стать аутоиммунные реакции, когда вырабатываемые организмом специальные антитела разрушают миелиновые оболочки нервных волокон.
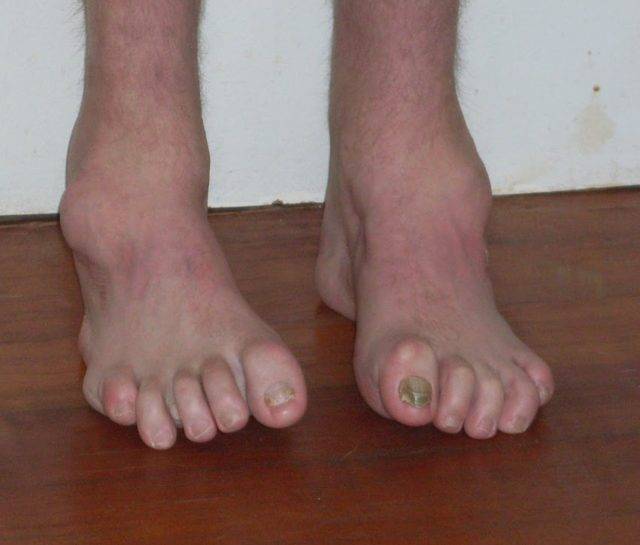
Симптомы болезни Шарко-Мари-Тута
Дебют заболевания отмечается в возрасте 10–20 лет. Первоначально появляются слабость в дистальных отделах ног, утомляемость в мышцах ног при длительном стоянии (постепенно нарастают на протяжении десятков лет). Позже может присоединяться боль в мышцах голени после долгой ходьбы (70%). При ходьбе приходится высоко поднимать ноги. Онемение в стопах отмечается в 80% случаев. Мышечная слабость в руках появляется спустя 10–15 лет после начала заболевания.
| Рис. 1 | Рис. 2 |
Диагностика
Диагностическая процедура включает ряд методов, среди которых:
- подробный личный и семейный анамнез;
- клиническая оценка мышечной силы, чувствительности;
- электрофизиологическое исследование скорости проводимости нервного волокна;
- неврологическое исследование.
Наиболее распространенные формы заболевания могут быть диагностированы путем анализа ДНК из крови пациента.
При диагностике необходимо тесное сотрудничество невролога, генетика, реабилитолога, хирурга-ортопеда и протезиста. В соответствии с выводами обследования, даются рекомендации относительно индивидуального плана реабилитации, при необходимости, назначается ортопедическая операция.
Значительная изменчивость клинических признаков болезни, наряду с отсутствием знаний о ней у многих врачей, часто приводит к неправильной диагностике.
Симптомы ШМТ у взрослых людей
- Слабость в мышцах ног и лодыжек;
- Искривление пальцев ног;
- Трудности подъема стопы из-за слабых мышц голеностопного сустава;
- Онемение в руках и ногах;
- Изменение формы голени, при этом нога становится очень тонкой ниже колена, в то время как бедра сохраняют нормальный объем мышц и форму (нога аиста);
- Со временем руки ослабевают и пациентам трудно выполнять повседневную работу;
- Появляются боли в мышцах и в суставах, человеку тяжело ходить. Нейропатическая боль возникает вследствие поврежденных нервов;
- В тяжелых случаях пациент может нуждаться в коляске, в то время как другие могут использовать специальная обувь или другие ортопедические устройства.
Факторы риска и причины ШMT
ШMT является наследственным заболеванием, так что люди, которые имеют близких родственников с заболеванием, имеют более высокий риск развития болезни.
Заболевание поражает периферические нервы. Периферический нервы состоит из двух основных частей: аксона — внутренняя часть нерва и миелиновой оболочки, которая является защитным слоем вокруг аксона. ШМТ может влиять на аксон и миелиновую оболочку.
При ШMT 1 мутируют гены, которые вызывают распад миелиновой оболочки. В конце концов, повреждается аксон, и мышцы пациента больше не получают четких сообщений от мозга. Это приводит к мышечной слабости и потере чувствительности или онемению.
При ШМТ 2 мутирующий ген влияет непосредственно на аксоны. Сигналы передаются не достаточно сильно, чтобы активизировать мышцы и органы чувств, так что пациенты имеют слабые мышцы, плохую чувствительность или онемение.
ШМТ 3 или болезнь Дежерин-Соттас, редкий тип заболевания. Повреждение миелиновой оболочки приводит к выраженной мышечной слабости и чувствительности. Симптомы могут быть заметны у детей.
ШМТ 4 является редким заболеванием, которое влияет на миелиновую оболочку. Симптомы обычно появляются в детстве, и пациенты часто нуждаются в инвалидном кресле.
ШМТ Х вызывается мутацией Х-хромосомы. Она чаще встречается у мужчин. Женщина с CMT X будет иметь очень слабые симптомы.
Читайте также:


