В ганглиях есть синапсы
Ганглии симпатического отдела вегетативной нервной системы в зависимости от их локализации разделяют на вертебральные (иначе их называют паравертебральными) и превертебральные. Ганглии парасимпатического отдела вегетативной нервной системы расположены внутри органов или вблизи них.
Вегетативные ганглии имеют большую продолжительность ВПСП. Длительный период следовой гиперполяризации, поэтому легко возникает торможение после возбуждения. Очень малая скорость проведения возбуждения - в 5-10 раз больше, чем в центральной нервной системе. Нейроны вегетативных ганглиев характеризуются низкой лабильностью, пропуская из центральной нервной системы на периферию малое количество импульсов. При частоте 100 импульсов в секунду в вегетативных ганглиях возникает полный блок. Таким образом, вегетативные ганглии - автономное образование, регулирующее проведение импульсов к рабочим органам.
Феномен мультипликации (умножения) в вегетативном ганглии - в вегетативном ганглии одновременно выражены феномены конвергенции и дивергенции импульсов: на теле одного постганглионарного нейрона конвергируют импульсы от нескольких преганглионарных нейронов и любой преганглионарный нейрон иннервирует много постганглионарных нейронов. Это обеспечивает надёжность передачи возбуждения. Вегетативные ганглии играют важную роль в распределении и распространении проходящих через них нервных влияний. Число нервных клеток в ганглиях в несколько раз больше числа приходящих к ганглию преганглионарных волокон. Каждое из этих волокон сильно ветвится и образует синапсы на многих клетках ганглия. Поэтому нервные импульсы, поступающие по преганглионарному волокну в ганглий, могут оказывать влияние на большое число ганглионарных нейронов и, следовательно, на еще большее число мышечных и железистых клеток иннервируемого органа. Таким образом, достигается расширение зоны влияния преганглионарных волокон.
Адренергические синапсы. В адренергических синапсах передача возбуждения осуществляется посредством норадреналина. В пределах периферической иннервации норадреналин принимает участие в передаче импульсов с адренергических волокон на эффекторные клетки. Адренергические аксоны, подходя к эффектору, разветвляются на тонкую сеть волокон с варикозными утолщениями, выполняющими функцию нервных окончаний. Последние участвуют в образовании синаптических контактов с эффекторными клетками. В варикозных утолщениях находятся везикулы (пузырьки), содержащие медиатор норадреналин. Биосинтез норадреналина осуществляется в адренергических нейронах из тирозина с участием ряда энзимов. Образование ДОФА и дофамина происходит в цитоплазме нейронов, а норадреналина — в везикулах.
В ответ на нервные импульсы происходит высвобождение норадреналина в синаптическую щель и последующее его взаимодействие с адренорецепторами постсинаптической мембраны. Существующие в организме адренорецепторы обладают неодинаковой чувствительностью к химическим соединениям.
Основываясь на этом, выделяют:
- Альфа-1и бета-1рецепторы локализуются в основном на постсинаптических мембранах и реагируют на действие норадреналина, выделяющегося из нервных окончаний постганглионарных нейронов симпатического отдела.
- Альфа-2и бета-2 рецепторы являются внесинаптическими, а также имеются на пресинаптической мембране тех же нейронов. На альфа-2 рецепторы действуют как адреналин, так и норадреналин. Бета-2 рецепторы чувствительны в основном к адреналину. На альфа-2 рецепторы пресинаптической мембраны норадреналин действует по принципу отрицательной обратной связи - ингибирует собственное выделение. При действии адреналина на бета-2 адренорецепторы пресинаптической мембраны выделение норадреналина усиливается. Поскольку адреналин выделяется из мозгового слоя надпочечников под действием норадреналина, возникает петля положительной обратной связи.
Холинергические синапсы. Медиатор холинергического синапса - ацетилхолин - синтезируется в нервном окончании из ацетилкоэнзима-А и холина и накапливается в пузырьках у пресинаптической мембраны. Под действием нервного импульса пузырьки лопаются, и ацетилхолин высвобождается в синаптическую щель. Далее он посредством диффузии достигает постсинаптической мембраны и возбуждает холинорецепторы, находящиеся на ней, что и обеспечивает контакт. В конечном итоге все выделенные в синаптическую щель молекулы ацетилхолина расщепляются до холина и уксусной кислоты при помощи специфического фермента ацетилхолинэстеразы, что прекращает активирующее действие медиатора на холинорецепторы. Активность ацетилхолинэстеразы настолько велика, что период полужизни ацетилхолина в синаптической щели измеряется в миллисекундах.
Рецепторы ацетилхолина на постсинаптической мембране (холинорецепторы) неоднородны, они разделяются на два больших класса в зависимости от чувствительности к двум природным алкалоидам - мускарину и никотину. Выделяют М-холинорецепторы, которые специфически активируются мускарином и блокируются атропином, и Н-холинорецепторы, которые специфически активируются малыми концентрациями никотина и блокируются большими концентрациями никотина. Для понимания эффектов препаратов, влияющих на холинергические процессы, важно знать локализацию М- и Н-холинорецепторов в организме. Препараты, влияющие на холинергические процессы, могут быть разделены на два больших класса:
1) препараты, активирующие холинорецепторы, т.е. влияющие подобно самому ацетилхолину, и поэтому они называются холиномиметиками.
2) препараты, блокирующие холинорецепторы, т.е. препятствующие действию ацетилхолина, и они называются холиноблокаторами.
Центральная нервная система человека осуществляет контроль над деятельностью его организма и разделяется на несколько отделов. Головной мозг посылает и получает сигналы из организма и после их обработки имеет информацию о процессах. Нервная система разделяется на вегетативную и соматическую нервную системы.
Отличия вегетативной и соматической нервной системы
Соматическая нервная система регулируется сознанием человека и может управлять деятельностью скелетной мускулатуры. Все компоненты реакции человека на внешние факторы находятся под контролем полушарий мозга. Она обеспечивает сенсорные и моторные реакции человека, контролируя их возбуждение и торможение.
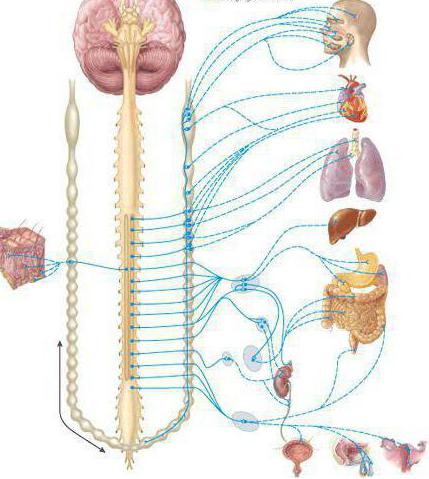
Вегетативная нервная система контролирует периферическую деятельность организма и не контролируется сознанием. Для нее характерны автономность и генерализованность воздействия на организм при полном отсутствии сознания. Эфферентная иннервация внутренних органов позволяет ей контролировать обменные процессы в организме и осуществлять обеспечение трофических процессов скелетной мускулатуры, рецепторов, кожи и внутренних органов.
Строение вегетативной системы
Работа вегетативной нервной системы контролируется гипоталамусом, который находится в центральной нервной системе. Вегетативная нервная система имеет метасегментарное строение. Ее центры находятся в головном, спинном мозге и коре головного мозга. Периферические отделы образованы стволами, ганглиями, сплетениями.
В вегетативной нервной системе различают:
- Симпатическую. Ее центр расположен в грудопоясничном отделе спинного мозга. Для нее характерны паравертебральные и предвертебральные ганглии ВНС.
- Парасимпатическую. Ее центры сосредоточены в среднем и продолговатом мозге, крестцовом отделе спинного мозга. Нервные узлы в основном интрамуральные.
- Метасимпатическую. Иннервирует желудочно-кишечный тракт, сосуды, внутренние органы организма.
В состав ее входит:
- Ядра нервных центров, расположенных в головном и спинном мозге.
- Вегетативные ганглии, которые расположены по периферии.
- Нервные волокна.
Рефлекторная дуга автономной нервной системы
Рефлекторная дуга вегетативной нервной системы состоит из трех звеньев:
- чувствительное или афферентное;
- вставочное или ассоциативное;
- эффекторное.

Чувствительное звено
Чувствительное звено расположено в спинномозговом ганглии. Этот ганглий имеет нервные клетки, сформированные группами, и их контроль осуществляется ядрами центрального головного мозга, большими полушариями и их структурами.
Чувствительное звено представлено частично униполярными клетками, которые имеют один приносящий или уносящий аксон, и они принадлежат спинальным или черепно-мозговым узлам. А также узлами блуждающих нервов, имеющих строение, похожее на спинальные клетки. В это звено входят клетки Догеля II типа, которые являются компонентами вегетативных ганглиев.
Вставочное звено
Вставочное звено в вегетативной нервной системе служит для передачи через низшие нервные центры, которыми являются вегетативные ганглии, и осуществляется это через синапсы. Расположено оно в боковых рогах спинного мозга. Нет прямой связи от афферентного звена на преганглионарные нейроны для их связи, существует кратчайший путь от афферентного нейрона до ассоциативного и от него до преганглионарного нейрона. Передача сигналов и нервных импульсов от афферентных нейронов в различных центрах осуществляется с различным количеством вставочных нейронов.
Например, в дуге спинального автономного рефлекса между чувствительным и эффекторным звеном существует три синапса, два из которых расположены в спинном мозге, а один в вегетативном узле, в котором расположен эфферентный нейрон.
Эфферентное звено
Эфферентное звено представлено эффекторными нейронами, которые расположены в вегетативных узлах. Их аксоны образуют безмиелиновые волокна, которые в составе со смешанными нервными волокнами иннервируют внутренние органы.
Вегетативные рефлекторные дуги расположены в боковых рогах.
Строение нервного узла
Ганглий – это скопление нервных клеток, которые имеют вид узелковых расширений толщиной около 10 мм. По своему строению вегетативный ганглий сверху покрыт соединительнотканной капсулой, которая образует строму из рыхлой соединительной ткани внутри органов. Мультиполярные нейроны, которые строятся из округлого ядра и крупных ядрышек, состоят из одного эфферентного нейрона и нескольких расходящихся афферентных нейронов. Эти клетки относятся по своему типу к клеткам головного мозга и являются двигательными. Их окружает неплотная оболочка – мантийная глия, которая создает постоянную среду для нервной ткани и обеспечивает полноценное функционирование нервных клеток.
Вегетативный ганглий имеет диффузное расположение нервных клеток и множество отростков, дендритов и аксонов.
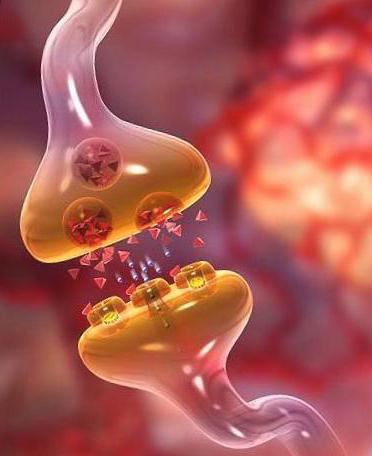
Спинномозговой ганглий имеет нервные клетки, которые расположены группами, и их расположение имеет порядок обусловленный.
Вегетативные нервные ганглии разделяются на:
- Сенсорные нейроны, которые расположены близко к спинному или центральному отделу мозга. Униполярные нейроны, из которых состоит этот ганглий, представляют собой приносящий или уносящий отросток. Они служат для афферентной передачи импульсов, и их нейроны образуют бифуркацию при ветвлении отростков. Эти отростки передают информацию от периферии к центральному афферентному нейрону – это периферический отросток, центральный – от тела нейрона в мозговой центр.
- Моторные, двигательные состоят из эфферентных нейронов, и в зависимости от их положения их называют паравертебральные, предвертебральные.
Симпатические ганглии
Паравертебральные цепочки ганглиев расположены вдоль позвоночного столба в симпатических стволах, которые идут длинной вереницей от основания черепа до копчика.
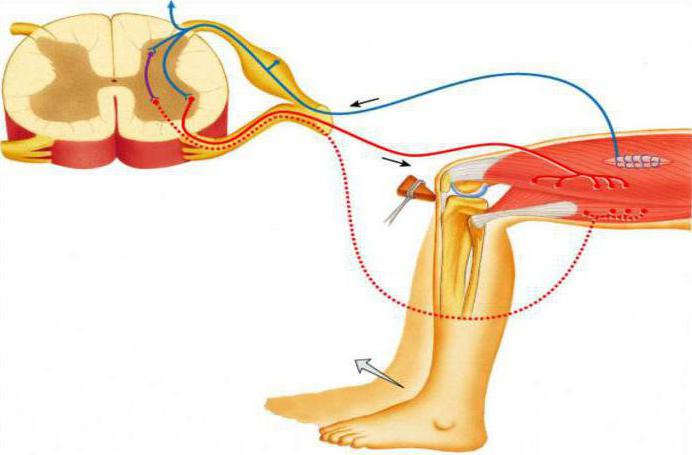
Предвертебральные нервные сплетения находятся ближе к внутренним органам, и их локализация сосредоточена перед аортой. Они образуют брюшное сплетение, которое состоит из солнечного, нижне- и верхнебрыжеечного сплетений. Они представлены двигательными адренергическими и тормозящими действие холинергическими нейронами. Также связь между нейронами осуществляется преганглионарными и постганглионарными нейронами, которые используют медиаторы ацетилхолин и норадреналин.
Интрамуральные нервные узлы имеют нейроны трех типов. Их описание было сделано русским ученым Догелем А.С., который, исследуя гистологию нейронов вегетативной нервной системы, выделил такие нейроны, как длинноаксонные эфферентные клетки первого типа, равноотросчатые афферентные клетки второго типа и ассоциативные клетки третьего типа.
Рецепторы ганглиев
Афферентные нейроны выполняют узкоспециализированую функцию, и их роль заключается в восприятии раздражителей. Такими рецепторами являются механорецепторы (реакция на растяжение или давление), фоторецепторы, терморецепторы, хеморецепторы (отвечают за реакции в организме, химические связи), ноцицепторы (реакция организма на болевые раздражители – это повреждение кожи и другие).
В симпатических стволах эти рецепторы по рефлекторной дуге передают в центральную нервную систему информацию, которая служит сигналом о повреждениях или нарушениях в организме, а также нормальной его работе.
Функции ганглиев
Каждый ганглий имеет свое местоположение, кровоснабжение, и его функции определяются этими параметрами. Спинномозговой ганглий, имеющий иннервацию из ядер головного мозга, обеспечивает непосредственную связь процессов в организме через рефлекторную дугу. От этих структурных компонентов спинного мозга иннервируются железы, гладкая мускулатура мышц внутренних органов. Сигналы, поступающие по рефлекторной дуге, идут медленнее, чем в ЦНС, и они полностью регулируются вегетативной системой, также она обладает трофической, сосудодвигательной функцией.
ГАНГЛИИ (ganglia нервные узлы)— скопления нервных клеток, окруженные соединительной тканью и клетками глии, расположенные по ходу периферических нервов.
Различают Г. вегетативной и соматической нервной системы. Г. вегетативной нервной системы делятся на симпатические и парасимпатические и содержат тела постганглионарных нейронов. Г. соматической нервной системы представлены спинномозговыми узлами и Г. чувствительных и смешаных черепных нервов, содержащих тела чувствительных нейронов и дающих начало чувствительным порциям спинномозговых и черепных нервов.
Содержание
- 1 Эмбриология
- 2 Анатомия
- 3 Гистология
- 4 Физиология
- 5 Патология
- 6 Краткая анатомическая характеристика нервных ганглиев (узлов)
Эмбриология
Зачатком спинномозговых и вегетативных узлов является ганглиозная пластинка. Она образуется у эмбриона в тех отделах нервной трубки, которые граничат с эктодермой. У зародыша человека на 14—16-й день развития ганглиозная пластинка располагается по дорсальной поверхности замкнувшейся нервной трубки. Затем она расщепляется по всей длине, обе ее половины перемещаются вентрально и в виде нервных валиков лежат между нервной трубкой и поверхностной эктодермой. В дальнейшем соответственно сегментам дорсальной стороны зародыша в нервных валиках возникают очаги пролиферации клеточных элементов; эти участки утолщаются, обособляются и превращаются в спинномозговые узлы. Из ганглиозной пластинки развиваются также чувствительные ганглии У, VII—X пар черепных нервов, аналогичные спинномозговым ганглиям. Зародышевые нервные клетки, нейробласты, формирующие спинномозговые ганглии, представляют собой биполярные клетки, т. е. имеют два отростка, отходящих от противоположных полюсов клетки. Биполярная форма чувствительных нейронов у взрослых млекопитающих и человека сохраняется только в чувствительных клетках преддверно-улит кового нерва, преддверного и спирального ганглиев. В остальных, как спинномозговых, так и черепных чувствительных узлах, отростки биполярных нервных клеток в процессе их роста и развития сближаются и сливаются в большинстве случаев в один общий отросток (processus communis). По этому признаку чувствительные нейроциты (нейроны) называют псевдоуниполярными (neurocytus pseudounipolaris), реже протонейронами, подчеркивая древность их происхождения. Спинномозговые узлы и узлы в. н. с. отличаются характером развития и строения нейронов. Развитие и морфология вегетативных ганглиев — см. Вегетативная нервная система.
Анатомия
Основные сведения об анатомии Г. приведены в таблице.
Гистология


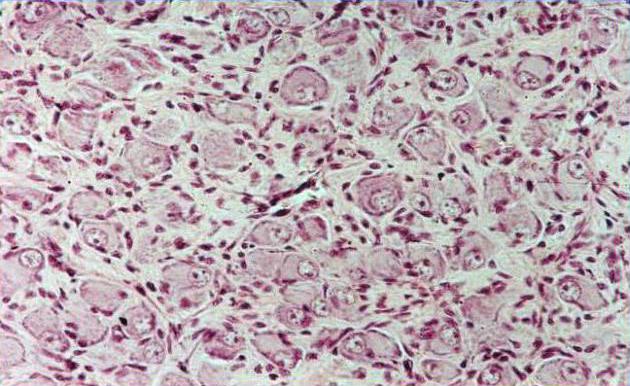
Возраст и перенесенные заболевания сказываются на структуре спинномозговых ганглиев — в них появляется значительно большее, чем у здоровых, количество различных атипичных нейронов, в особенности с дополнительными отростками, снабженными колбовидными утолщениями, как, напр., при ревматическом пороке сердца (рис. 2), стенокардии и др. Клинические наблюдения, а также экспериментальные исследования на животных показали, что чувствительные нейроны спинномозговых узлов реагируют значительно быстрее интенсивным ростом дополнительных отростков на различные эндогенные и экзогенные вредности, нежели моторные соматические или вегетативные нейроны. Эта способность чувствительных нейронов иногда выражена значительно. В случаях хрон, раздражений вновь образованные отростки могут обвиваться (в виде намотки) вокруг тела собственного или соседнего нейрона, напоминая кокон. Чувствительные нейроны спинномозговых узлов, как и другие типы нервных клеток, имеют ядро, различные органеллы и включения в цитоплазме (см. Нервная клетка). Т. о., отличительным свойством чувствительных нейронов спинномозговых и узлов черепных нервов является их яркая морфол, реактивность, выражающаяся в изменчивости их структурных компонентов. Это обеспечено высоким уровнем синтеза белков и различных активных веществ и свидетельствует об их функциональной подвижности.
Физиология
У беспозвоночных Г. играют ту же роль, что и ц. н. с. у позвоночных, являясь высшими центрами координации соматических и вегетативных функций. В эволюционном ряду от червей до головоногих моллюсков и членистоногих Г., перерабатывающие всю информацию о состоянии окружающей и внутренней среды, достигают высокой степени организации. Это обстоятельство, а также простота анатомической препаровки, относительно большие размеры тел нервных клеток, возможность введения в сому нейронов под прямым визуальным контролем одновременно нескольких микроэлектродов сделали Г. беспозвоночных общераспространенным объектом нейрофизиол, экспериментов. На нейронах круглых червей, октапод, декапод, брюхоногих и головоногих моллюсков методами электрофореза, прямого измерения активности ионов и фиксации напряжения проводят исследования механизмов генерации потенциалов и процесса синаптической передачи возбуждения и торможения, зачастую невыполнимые на большинстве нейронов млекопитающих. Несмотря на эволюционные различия, основные электрофизиол, константы и нейрофизиол, механизмы работы нейронов во многом одинаковы у беспозвоночных и высших позвоночных животных. Поэтому исследования Г., беспозвоночных имеют общефизиол. значение.
У позвоночных соматосенсорные черепные и спинномозговые Г. функционально однотипны. Они содержат тела и проксимальные части отростков афферентных нейронов, передающих импульсацию от периферических рецепторов в ц. н. с. В сомато-сенсорных Г. нет синаптических переключений, эфферентных нейронов и волокон. Так, нейроны спинномозговых Г. у жабы характеризуются следующими основными электрофизиол, параметрами: специфическим сопротивлением — 2,25 кОм/см 2 для деполяризующего и 4,03 кОм/см 2 для гиперполяризующего тока и удельной емкостью 1,07 мкФ/см 2 . Полное входное сопротивление нейронов сомато-сенсорных Г. существенно ниже, чем соответствующий параметр аксонов, поэтому при высокочастотной афферентной импульсации (до 100 импульсов в 1 сек.) проведение возбуждения может блокироваться на уровне тела клетки. В этом случае потенциалы действия, хотя и не регистрируются от тела клетки, продолжают проводиться с периферического нерва в задний корешок и сохраняются даже после экстирпации тел нервных клеток при условии интактности Т-образных ветвлений аксонов. Следовательно, возбуждение сомы нейронов сомато-сенсорных Г. для передачи импульсов от периферических рецепторов к спинному мозгу не обязательно. Эта особенность впервые появляется в эволюционном ряду у бесхвостых амфибий.
Вегетативные Г. позвоночных в функциональном плане принято разделять на симпатические и парасимпатические. Во всех вегетативных Г. происходит синаптическое переключение с преганглионарных волокон на постганглионарные нейроны. В подавляющем большинстве случаев синаптическая передача осуществляется хим. путем с помощью ацетилхолина (см. Медиаторы). В парасимпатическом цилиарном Г. птиц обнаружена электрическая передача импульсов при помощи так наз. потенциалов соединения, или потенциалов связи. Электрическая передача возбуждения через один и тот же синапс возможна в двух направлениях; в процессе онтогенеза она формируется позже химической. Функциональное значение электрической передачи пока не ясно. В симпатических Г. амфибий выявлено небольшое количество синапсов с хим. передачей нехолинергической природы. В ответ на сильное одиночное раздражение преганглионарных волокон симпатического Г. в постганглионарном нерве прежде всего возникает ранняя отрицательная волна (O-волна), обусловленная возбуждающими постсинаптическими потенциалами (ВПСП) при активации н-холинорецепторов постганглионарных нейронов. Тормозной постсинаптический потенциал (ТПСП), возникающий в постганглионарных нейронах под действием катехоламинов, выделяемых хромаффинными клетками в ответ на активацию их м-холинорецепторов, формирует следующую за 0-волной положительную волну (П-волна). Поздняя отрицательная волна (ПО-волна) отражает ВПСП постганглионарных нейронов при активации их м-холинорецепторов. Завершает процесс длительная поздняя отрицательная волна (ДПО-волна), возникающая вследствие суммации ВПСП нехолинергической природы в постганглионарных нейронах. В нормальных условиях на высоте О-волны при достижении ВПСП величины 8—25 мв возникает распространяющийся потенциал возбуждения с амплитудой 55—96 мв, длительностью 1,5—3,0 мсек, сопровождаемый волной следовой гиперполяризации. Последняя существенно маскирует волны П и ПО. На высоте следовой гиперполяризации возбудимость снижается (период рефрактерности), поэтому обычно частота разрядов постганглионарных нейронов не превышает 20—30 импульсов в 1 сек. По основным электрофизиол. характеристикам нейроны вегетативных Г. идентичны большинству нейронов ц. н. с. Нейрофизиол. особенностью нейронов вегетативных Г. является отсутствие истинной спонтанной активности при деафферентации. Среди пре- и постганглионарных нейронов преобладают нейроны групп В и С по классификации Гассера — Эрлангера, основанной на электрофизиол, характеристиках нервных волокон (см.). Преганглионарные волокна обширно ветвятся, поэтому раздражение одной преганглионарной ветви приводит к возникновению ВПСП во многих нейронах нескольких Г. (феномен мультипликации). В свою очередь на каждом постганглионарном нейроне оканчиваются терминали многих преганглионарных нейронов, отличающихся по порогу раздражения и скорости проведения (феномен конвергенции). Условно мерой конвергенции можно считать отношение количества постганглионарных нейронов к количеству преганглионарных нервных волокон. Во всех вегетативных Г. оно больше единицы (за исключением цилиарного ганглия птиц). В эволюционном ряду это отношение возрастает, достигая в симпатических Г. человека величины 100:1. Мультипликация и конвергенция, обеспечивающие пространственную суммации) нервных импульсов, в сочетании с временной суммацией являются основой интегрирующей функции Г. при обработке центробежной и периферической импульсации. Через все вегетативные Г. проходят афферентные пути, тела нейронов которых лежат в спинномозговых Г. Для нижнего брыжеечного Г., чревного сплетения и некоторых интрамуральных парасимпатических Г. доказано существование истинных периферических рефлексов. Афферентные волокна, проводящие возбуждение с малой скоростью (ок. 0,3 м/сек), входят в Г. в составе постганглионарных нервов и оканчиваются на постганглионарных нейронах. В вегетативных Г. обнаружены окончания афферентных волокон. Последние информируют ц. н. с. о происходящих в Г. функционально-хим. изменениях.
Патология
В клин, практике наиболее часто встречается ганглионит (см.), называемый также симпато-ганглионитом, — заболевание, связанное с поражением ганглиев симпатического ствола. Поражение нескольких узлов определяют как полиганглионит, или трунцит (см.).
Спинальные ганглии нередко вовлекаются в патологический процесс при радикулитах (см.).
Эфферентная (центробежная) иннервация включает:
1) вегетативные нервы всех внутренних органов, кровеносных сосудов, желез внешней секреции;
2) двигательные (соматические) нервные волокна скелетной мускулатуры.
Центральные отделы вегетативной нервной системы представлены в спинном, продолговатом и головном мозге. Эфферентный путь вегетативной нервной системы прерывается в нервных узлах - ганглиях. Они делят вегетативные волокна на преганглионарные, осуществляющие нервную передачу из центров вегетативной нервной системы к ганглиям, и постганглионарные, проводящие нервные импульсы с ганглиев на исполнительные органы.
Вегетативная иннервация подразделяется на парасимпатическую часть и симпатическую.
Парасимпатические нервы начинаются от клеток (первый нейрон) стволовой части головного мозга и крестцовой части спинного мозга (преганглионарные волокна) и заканчиваются в интрамуральных (расположенных внутри органов) ганглиях (второй нейрон), откуда короткие аксоны (постганглионарные волокна) достигают исполнительных клеток.
Симпатические нервы исходят из клеток боковых рогов грудного и поясничного отделов спинного мозга (первый нейрон) и прерываются в симпатических ганглиях (второй нейрон), аксоны (постганглионарные волокна) которых заканчиваются на клетках исполнительных органов и тканей.
Синапсы (от греческого synopsis -соединение, "смыкать") - место контакта аксона (нервного окончания) и иннервируемого им ганглия, органа или мышечного волокна. Контакт реализуется химическим посредником - медиатором (ацетилхолином или норадреналином).
Преганглионарные волокна парасимпатической и симпатической нервной системы выделяют ацетилхолин, и синаптическая передача во всех ганглиях осуществляется с помощью ацетилхолина. Постганглионарные нервные окончания парасимпатической нервной системы выделяют ацетилхолин, следовательно в синапсах, образованных этими окончаниями и клетками органов (постганглионарные синапсы парасимпатической нервной системы), медиатором является ацетилхолин.
В постганглионарных синапсах симпатической нервной системы передача осуществляется за счет медиатора норадреналина. Таким
образом, вегетативные нервы включают два нейрона (один расположен преганглионарно, другой - в составе ганглия), преганглионарные и постганглионарные волокна и два синапса - ганглионарный и постганглионарный.
Некоторые структуры организма (мозговой слой надпочечников, синокаротидная зона) эмбрионально являются симпатическими ганглиями и получают только преганглионарную импульсацию (от боковых рогов спинного мозга) при участии медиатора ацетилхолина. Последний стимулирует, например, хромаффинные клетки надпочечников, выделяющие адреналин.
Двигательные соматические нервы являются аксонами нервных клеток, расположенных в передних рогах спинного мозга; заканчиваются они в скелетной мускулатуре. Медиатор нервно-мышечного синапса - ацетилхолин.
При исследовании различных синапсов выяснена однотипность их строения. В синапсе различают пресинаптическую мембрану (поверхность нервного окончания, обращенная к иннервируемому органу или мышце) и постсинаптическую мембрану. Участок клеток органа или мышцы постсинаптической мембраны, воспринимающий импульс нейрона, называется рецептором. Пресинаптическую и постсинаптическую мембраны разделяет синаптическая щель, куда выделяется медиатор. Медиатор синтезируется в цитоплазме нервного окончания и депонируется в синаптических пузырьках (везикулах). При поступлении импульса медиатор выбрасывается в синаптическую щель, взаимодействует с рецепторами постсинаптической мембраны, а затем инактивируется (разрушается).
Эфферентные нервы и синапсы делятся на холинергические и адренергические, в зависимости от синтезирующегося в окончаниях и выделяющегося в синаптическую щель медиатора.
Холинергическими являются все двигательные, все преганглионарные (парасимпатические и симпатические), постганглионарные парасимпатические волокна, а также постганглионарные симпатические нервные волокна, иннервирующие потовые железы.
К адренергическим относятся только постганглионарные симпатические нервные волокна (исключая иннервацию потовых желез). Средства, влияющие на передачу импульса в холинергических синапсах, называют холинергическими, в адренергических - адренергическими.
Содержание
В холинергической передаче важнейшую роль играют два фермента, отвечающие соответственно за синтез и расщепление ацетилхолина — холинацетилтрансфераза и ацетилхолинэстераза (АХЭ).
Этот фермент катализирует последнюю реакцию синтеза ацетилхолина — соединение холина с ацетил-КоА (Wu and Hersh, 1994; Parsons et al., 1993). Первичная структура холинацетилтрансферазы была установлена с помощью молекулярного клонирования. Ее иммуногистохимическое определение — ценный метод, позволяющий выявлять тела и отростки холинергических нейронов.
Ацетил-КоА, используемый для синтеза ацетилхолина, образуется либо из пирувата путем его окислительного декарбоксилирования (многостадийной реакции, катализируемой пируватдегидрогеназным комплексом), либо из ацетата. В последнем случае под действием фермента ацетил-КоА-синтетазы ацетат соединяется с АТФ с образованием связанного с ферментом ациладенилата (ацетил-АМФ), и далее в присутствии КоА происходит трансацетилирование и синтез ацетил-КоА.
Как и другие нейрональные белки, холинацетилтрансфераза синтезируется в теле нейрона. Затем она переносится по аксону в окончания. В последних имеется множество митохондрий, в которых образуется ацетил-КоА. Холин захватывается из внеклеточной жидкости путем активного транспорта. Ацетилхолин синтезируется в цитоплазме и затем депонируется в синаптических пузырьках. Существуют ингибиторы холинацетилтрансферазы, в том числе с умеренной активностью. Однако их фармакологический эффект невелик, частично из-за того, что лимитирующей реакцией в синтезе ацетилхолина служит захват холина.
Захват холина из внеклеточной жидкости осуществляется с помощью двух разных систем — высоко- и низкоаффинной. Высокоаффинная система (константа Михаэлиса 1—5 мкмоль/л) имеется только в холинергических нейронах; ее активность зависит от концентрации Na+ во внеклеточной среде, и она блокируется гемихолинием. Концентрация холина в плазме составляет около 10 мкмоль/л, и поэтому она не ограничивает транспорт холина в нейрон. Большая часть холина, образующегося при гидролизе ацетилхолина под действием АХЭ, захватывается обратно в пресинаптическое окончание. Недавно методом молекулярного клонирования была установлена структура высокоаффинного переносчика холина, выделенного из пресинаптических окончаний. Оказалось, что он отличается от переносчиков других медиаторов, но сходен с Na+-3aвисимым переносчиком глюкозы (Okuda et al., 2000).
Синтезируемый ацетилхолин переносится в синаптические пузырьки. Этот перенос осуществляется системой, в которой используется энергия электрохимического градиента для протонов. Везамикол в микромолярных концентрациях блокирует перенос в пузырьки ацетилхолина. Гены холинацетилтрансферазы и переносчика ацетилхолина располагаются в одном и том же локусе (ген переносчика локализован в 1-м интроне гена холинацетилтрансферазы). Поэтому экспрессия обоих этих генов регулируется одним и тем же промотором (Eiden, 1998). АХЭ. Непременным условием эффективной холинергической передачи в нервно-мышечных и некоторых межнейронных синапсах является быстрая инактивация ацетилхолина. Так, в нервно-мышечном синапсе его удаление должно быть буквально, по словам Дейла, молниеносным — иначе ацетилхолин будет диффундировать и активировать рецепторы соседних мышечных волокон.
С помощью современных биохимических методов удалось установить, что гидролиз ацетилхолина АХЭ в нервно-мышечном синапсе занимает меньше 1 мс. Действие же холина на N-холинорецепторы в этом синапсе в 10_3— 10
5 раз слабее, чем действие ацетилхолина.
АХЭ обнаруживается не только в холинергических синапсах, но и в других структурах холинергических нейронов (дендритах, теле, аксонах). Ее концентрация особенно высока в области постсинаптической мембраны нервно-мышечных синапсов.
В глиальных клетках ЦНС и мантийных глиоцитах в низкой концентрации содержится псевдохолинэстераза (бутирилхолинэстераза, холинэстераза); в центральных и периферических нейронах она почти отсутствует. Псевдохолинэстераза обнаруживается главным образом в печени (где она в основном и образуется) и в плазме. Возможно, она выполняет рудиментарную физиологическую функцию — гидролиз эфиров холина, содержащихся в растительной пище. АХЭ и псевдохолинэстераза различаются по скорости гидролиза ацетилхолина и бутирилхолина и по реакции на избирательные ингибиторы. Почти все фармакологические эффекты ингибиторов АХЭ обусловлены подавлением активности именно этого фермента и, как следствие, накоплением эндогенного ацетилхолина в холинергических синапсах и окружающих тканях. У млекопитающих АХЭ и псевдохолинэстераза кодируются разными генами. Разнообразие строения АХЭ обусловлено альтернативным сплайсингом РНК (Taylor et al., 2000).
Выше мы уже упоминали о том, что между различными холинергическими синапсами существуют значительные отличия, касающиеся строения этих синапсов, распределения АХЭ и холинорецепторов, временных параметров синаптической передачи и т. п. Так, в скелетной мышце нервно-мышечный синапс занимает лишь небольшой участок на мышечном волокне, и эти синапсы расположены довольно далеко друг от друга — на соседних волокнах. Напротив, в верхнем шейном ганглии на несколько кубических миллиметров ткани приходится около 100 000 нейронов, и пресинаптические окончания образуют здесь сложную и густую сеть с постсинаптическими дендритами.
Скелетные мышцы. Раздражение двигательного нерва вызывает выделение ацетилхолина в перфузат, оттекающий от соответствующей мышцы; с другой стороны, введение ацетилхолина непосредственно в снабжающие мышцу артерии приводит к ее сокращению. Минимальное количество ацетилхолина (10
17 моль), способное вызвать типичный потенциал концевой пластинки при микроионофоретической аппликации на область концевой пластинки диафрагмы крысы, равно тому количеству этого медиатора, которое выделяется из одного пресинаптического окончания при раздражении диафрагмального нерва (Kmjevic and Mitchell, 1961).
Соединение ацетилхолина с N-холинорецептором постсинаптической мембраны приводит к немедленному и выраженному повышению проницаемости этой мембраны для катионов. Это обусловлено тем, что активация N-холинорецептора сопровождается открыванием связанного с этим рецептором канала. Время пребывания канала в открытом состоянии составляет около 1 мс, и при этом через канал проходит примерно 50 000 ионов Na+ (Katz and Miledi, 1972). В результате открывания множества таких каналов развивается местный деполяризующий потенциал — потенциал концевой пластинки, который, в свою очередь, запускает потенциал действия. Последний вызывает сокращение мышцы. Подробнее все эти процессы и влияние на них средств, блокирующих нервно-мышечные синапсы, описаны в гл. 9.
После перерезки и дегенерации двигательного соматического нерва либо постганглионарных вегетативных волокон реакции денервированных органов возникают в ответ на значительно меньшие дозы медиатора (и некоторых фармакологических средств). Это явление было названо повышением чувствительности денервированных структур. В скелетной мышце при этом N-холинорецепторы появляются за пределами концевой пластинки — сначала рядом с ней, а затем на всей сарколемме. Эмбриональные мышечные волокна до прорастания в них нервных волокон также чувствительны к ацетилхолину на всей своей поверхности. Таким образом, иннервация мышцы приводит к подавлению экспрессии гена N-холинорецептора в ядрах, лежащих в отдалении от синапсов, и, напротив, к повышению экспрессии этого гена (и генов, кодирующих другие синаптические белки) в субсинаптических ядрах (Sanes and Lichtman, 1999).
Внутренние органы. Передача стимулирующих или тормозных сигналов от вегетативных нервов к внутренним органам обусловлена активацией М-холинорецепторов (см. ниже). Эти рецепторы, в отличие от N-холинорецепторов, связаны не с ионными каналами, а с G-белками. В отличие от скелетных мышц и нейронов, у гладких мышц и структур проводящей системы сердца (синусового узла, предсердных пучков, АВ-узла, пучка Гиса с его ножками и волокон Пуркинье) имеется собственная — автоматическая — электрическая и механическая активность. Эта активность не запускается, а лишь модулируется нервными воздействиями. В отсутствие последних в гладкомышечных клетках возникают волны деполяризации и — иногда — потенциалы действия; и те, и другие передаются от клетки к клетке, но значительно медленнее, чем распространяются импульсы по аксонам или волокнам скелетных мышц. Потенциалы действия в гладких и сердечной мышцах возникают в результате ритмичных колебаний мембранного потенциала — спонтанной деполяризации. В гладких мышцах ЖКТ область зарождения возбуждения (ведущий водитель ритма, или пейсмекер) постоянно смещается. В сердце же этой областью в норме всегда является синусовый узел; если же его активность подавляется, то функцию ведущего водителя ритма берут на себя другие структуры проводящей системы.
Аппликация ацетилхолина (в концентрации 0,1—1 мкмоль/л) на изолированные гладкие мышцы кишечника вызывает снижение мембранного потенциала (то есть он становится менее отрицательным) и повышение частоты потенциалов действия; тонус мышц при этом возрастает. Очевидно, это действие ацетилхолина, опосредованное активацией М-холинорецепторов, обусловлено повышением натриевой и, иногда, кальциевой проницаемости. Кроме того, в кальцийсодержащем растворе ацетидхолин может вызвать сокращения некоторых гладких мышц, полностью деполяризованных в результате повышения внеклеточной концентрации К+. Таким образом, ацетилхолин повышает трансмембранные ионные потоки и вызывает выход в цитоплазму кальция из внутриклеточных депо.
В структурах проводящей системы сердца (в частности, в синусовом узле) раздражение холинергических нервов или прямая аппликация ацетилхолина вызывает снижение частоты потенциалов действия, обусловленное гиперполяризацией и замедлением скорости спонтанной деполяризации. Эти эффекты частично обусловлены избирательным повышением калиевой проницаемости (Hille, 1992).
Вегетативные ганглии. Механизмы холинергической передачи в вегетативных ганглиях в основном такие же, как в скелетных мышцах. Потенциалы действия в постганглионарных волокнах можно вызвать введением в ганглий очень небольших количеств ацетилхолина. ВПСП в постганглионарных нейронах возникает в результате активации N-холинорецепторов, непосредственно связанных с ионными каналами (как и в скелетных мышцах). Некоторые другие медиаторы, или так называемые нейромодумторы, снижают либо повышают чувствительность постганглионарных нейронов к ацетилхолину — видимо, меняя мембранный потенциал тел или дендритов этих нейронов. Подробнее передача возбуждения в вегетативных ганглиях рассматривается в гл. 9.
Большое количество работ было посвящено возможной роли пресинаптических холинорецепторов в холинергической и нехолинергической передаче и действии ряда лекарственных средств. На симпатических сосудосуживающих нервах, видимо, присутствуют пресинаптические М-холинорецепторы (Steinsland et al., 1973). Их активация сопровождается снижением выброса норадреналина в ответ на нервные импульсы. Физиологическая роль этих рецепторов не ясна, ведь холинергическая иннервация сосудов выражена слабо, а поскольку ацетилхолин быстро гидролизуется тканевыми и плазменными эстеразами, маловероятно, чтобы он, подобно адреналину, играл роль гормона.
Введение эфиров холина приводит к расширению сосудов. Точек приложения у этих веществ несколько; к ним относятся холинорецепторы тормозных синапсов на пресинаптических симпатических окончаниях и холинорецепторы на сосудах, расположенные вне синапсов. Сосудорасширяющее действие ацетилхолина возможно только при неповрежденном эндотелии. Активация М-холинорецепторов эндотелия приводит к выделению из него N0 (эндотелиального фактора расслабления сосудов). Диффундируя от эндотелия к гладким мышцам, N0 вызывает их расслабление, а следовательно, расширение сосудов (Furchgott, 1999).
Сэр Генри Дейл впервые показал, что различные эфиры холина могут оказывать эффекты, сходные с таковыми либо никотина, либо мускарина (Dale, 1914). Было также обнаружено, что последствия раздражения парасимпатических нервов воспроизводятся мускарином. Это позволило Дейлу предположить, что медиатором вегетативной нервной системы служит ацетилхолин либо какой-либо другой эфир холина. Кроме того, отметив двоякое действие ацетилхолина, он ввел термины никотиноподобный и мускариноподобный для обозначения соответствующих эффектов.
Дальнейшие доказательства наличия двух типов холинорецепторов были получены в опытах с применением тубокурарина и атропина. Оказалось, что эти вещества блокируют соответственно никотиноподобный и мускариноподобный эффекты ацетилхолина. Дейл имел дело лишь с неочищенными алкалоидами Amanita muscaria и Nicotiana tabacum, структуры которых в то время были не известны, однако его классификация холинорецепторов действительна и по сей день — хотя и дополнилась представлениями о нескольких подтипах N- и М-холинорецепторов.
Ацетилхолин и некоторые другие вещества активируют оба типа холинорецепторов; другие же стимуляторы и блокаторы действуют избирательно на один из них. Молекула ацетилхолина способна легко деформироваться; по непрямым данным, при связывании с N- и М-холинорецепторами ее конформация различна.
N-холинорецепторы непосредственно связаны с ионными каналами. Активация этих рецепторов всегда вызывает кратковременное (около 1 мс) открывание соответствующих каналов, повышение натриевой и кальциевой проницаемости и деполяризацию — ВПСП или потенциал концевой пластинки. Что же касается М-холинорецепторов, то они принадлежат к суперсемейству рецепторов, сопряженных с G-белками. Реакции на активацию М-холинорецепторов гораздо медленнее, они могут быть как стимуляторными, так и тормозными и не обязательно связаны с изменениями ионных проницаемостей.
Первичная структура различных подтипов N-холинорецепторов (Numa et al., 1983; Changeux and Edelstein, 1998) и М-холинорецепторов (Bonner, 1989; Caulfield and Birdsall, 1998) была установлена на основании данных о строении соответствующих генов. Оказалось, что эти два типа холинорецепторов принадлежат к белкам разных семейств — что не удивительно, учитывая различия в их фармакологических свойствах и функции.
N-холинорецепторы — это пентамеры, состоящие из гомологичных субъединиц. Существуют несколько типов таких субъединиц. В состав каждого пентамерного N-холинорецептора могут входить субъединицы разных типов — но не более 4 типов, так как а-субъединиц обязательно должно быть две. Участки связывания ацетилхолина образуются в местах стыков а-субъединиц с соседними субъединицами. Стенки ионного канала образованы трансмембранными а-спиральными структурами субъединиц (Changeux and Edelstein, 1998; см. также гл. 9 и 12). Структура и свойства М-холинорецепторов описаны в гл. 2 и 7.
Уже давно было известно, что многие стимуляторы и блокаторы действуют только на N-холинорецепторы либо скелетных мышц, либо вегетативных ганглиев — а значит, эти рецепторы различаются. Эти различия были подтверждены и с помощью молекулярного клонирования. Оказалось, например, что N-холинорецепторы скелетных мышц включают субъединицы 4 типов. Структура этих рецепторов соответствует формуле а2р8у или а2рбе: у рецепторов эмбриональных или денервированных мышц имеется субъединица у, у нормальных мышц взрослого — е. Замена субъединицы у на субъединицу I сопровождается некоторым изменением избирательности рецептора к лиганду, но важнее, видимо, то, что такая замена может влиять на скорость обновления рецепторов или их локализацию в клетке. Нейрональные N-холинорецепторы также представляют собой пентамеры. Субъединицы нейрональных N-холинорецепторов очень разнообразны. Они подразделяются на типы а и β; в свою очередь, тип а в нервной системе млекопитающих включает 8 подтипов (а2—а9), а тип β — 3 подтипа (β2—β4)- Не все сочетания этих субъединиц образуют функционирующие рецепторы, но тем не менее число вариантов таких рецепторов слишком велико для того, чтобы различать их на основании сродства к лигандам. В частности, функционирующими рецепторами служат гомоолигомерные пентамеры субъединиц а7, а8 и а9. Особенности N-холинорецепторов скелетных мышц, периферических вегетативных и центральных нейронов приведены в табл. 6.2. Подробнее структура, функция, распределение и подтипы N-холинорецепторов рассматриваются в гл. 9.
С помощью молекулярного клонирования были выделены 5 подтипов М-холинорецепторов. Как и подтипы N-холинорецепторов, они различаются по локализации и фармакологическим свойствам. Все М-холинорецепторы сопряжены с G-белками (см. ниже и табл. 6.2).
В течение нескольких десятилетий исследовались многие М-холиноблокаторы, но только полученный в 1970-х гг. пирензепин обладал способностью подавлять желудочную секрецию соляной кислоты в концентрациях, не оказывающих иных эффектов. Эти данные, исследование эффектов других стимуляторов и блокаторов, а затем клонирование кДНК М-холинорецепторов привели к разделению этих рецепторов на 5 подтипов, обозначаемых M1—М5 (Bonner, 1989).
Холинорецепторы подтипа М, обнаруживаются в вегетативных ганглиях и некоторых железах, М2 — в миокарде и, возможно, в гладких мышцах, М3 и М4 — в гладких мышцах и железах. В ЦНС имеются рецепторы всех 5 подтипов. Во многих тканях содержатся одновременно рецепторы нескольких подтипов. То же касается и интрамуральных парасимпатических ганглиев.
Как уже говорилось, М-холинорецепторы сопряжены с G-белками, и поэтому их стимуляция приводит к изменению активности ряда внутриклеточных белков. Соединение лигандов с рецепторами подтипов М]( М3 и М5 приводит к активации белков Gq и G11. Это, в свою очередь, вызывает повышение активности фосфолипазы С, гидролизу мембранных фосфолипидов — фосфатидилинозитолполифосфатов — и образованию инозитолполифосфатов. Некоторые из последних — главным образом ИФ3 — вызывают выход Са2+ из эндоплазматического ретикулума. Таким образом, активация рецепторов этих подтипов отвечает за такие кальцийзависимые процессы, как сокращение гладких мышц и секреция (Berridge, 1993; см. также гл. 2). Второй продукт гидролиза фосфатидилинозитолполифосфатов — ДАГ — в присутствии Са + активирует протеинки-назу С. Этот механизм отвечает за модуляцию клеточных функций (в том числе запускаемых ИФ3) и за отсроченные реакции на ацетилхолин (Dempsey et al., 2000).
Рецепторы подтипов М2 и М4 сопряжены с белками Gj и G11. Их активация приводит к ингибированию аденилатциклазы, открыванию калиевых каналов (в частности, в сердце) и в некоторых клетках к снижению вероятности открывания медленных кальциевых каналов. Функциональные последствия этих эффектов наиболее изучены на сердце: именно ингибирование аденилатциклазы и открывание калиевых каналов, видимо, ответственны за отрицательные хронотропный и инотропный эффекты ацетилхолина.
Активация М-холинорецепторов может приводить и к другим событиям, в частности активации гуанилатциклазы и образованию арахидоновой кислоты. Обычно эти процессы вторичны по отношению к иным внутриклеточным реакциям.
Читайте также:


