Цикл кори взаимосвязь гликолиза в мышцах и глюконеогенеза в печени
Название работы: Биосинтез глюкозы (глюконеогенез) из аминокислот, глицерина и молочной кислоты. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори)
Предметная область: Биология и генетика
Описание: Глюконеогенез процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Эти ткани могут обеспечивать синтез 80100 г глюкозы в сутки.
Дата добавления: 2015-02-20
Размер файла: 215.46 KB
Работу скачали: 26 чел.
Биосинтез глюкозы (глюконеогенез) из аминокислот, глицерина и молочной кислоты. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
Глюконеогенез - процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Процесс протекает в основном в печени и менее интенсивно в корковом веществе почек, а также в слизистой оболочке кишечника. Эти ткани могут обеспечивать синтез 80-100 г глюкозы в сутки. На долю мозга при голодании приходится большая часть потребности организма в глюкозе. Это объясняется тем, что клетки мозга не способны, в отличие от других тканей, обеспечивать потребности в энергии за счёт окисления жирных кислот .Кроме мозга, в глюкозе нуждаются ткани и клетки, в которых аэробный путь распада невозможен или ограничен, например эритроциты (они лишены митохондрий), клетки сетчатки, мозгового слоя надпочечников и др. Первичные субстраты глюконеогенеза - лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма.
- Лактат - продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно.
- Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке.
- Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
Большинство реакций глюконеогенеза протекает за счёт обратимых реакций гликолиза и катализируется теми же ферментами. Однако 3 реакции гликолиза термодинамически необратимы. На этих стадиях реакции глюконеогенеза протекают другими путями. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях.

- Образование фосфоенолпирувата из пирувата . Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций первая из которых протекает в митохондриях. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата.

Пируват-карбоксилаза, катализирующая данную реакцию, - митохондриальный фермент, коферментом которого является биотин. Реакция протекает с использованием АТФ.
Дальнейшие превращения оксалоацетата протекают в цитозоле. Следовательно, на этом этапе должна существовать система транспорта оксалоацетата через митохондриальную мембрану, которая для него непроницаема. Оксалоацетат в митохондриальном матриксе восстанавливается с образованием малата при участии NADH (обратная реакция цитратного цикла).

Образовавшийся малат затем проходит через митохондриальную мембрану с помощью специальных переносчиков. Кроме того, оксалоацетат способен транспортироваться из митохондрий в цитозоль в виде аспартата в ходе малат-аспартатного челночного механизма. В цитозоле малат вновь превращается в оксалоацетат в ходе реакции окисления с участием кофермента NAD+. Обе реакции: восстановление оксалоацетата и окисление малага катализируют малатдегидрогеназа, но в первом случае это митохондриальный фермент, а во втором - цитозольный. Образованный в цитозоле из ма-лата оксалоацетат затем превращается в фосфоенолпируват в ходе реакции, катализируемой фосфоенолпируваткарбоксикиназой - ГТФ-зависимым ферментом.
- Образование глюкозы из лактата. Лактат, образовавшийся в интенсивно работающих мышцах или в клетках с преобладающим анаэробным способом катаболизма глюкозы, поступает в кровь, а затем в печень. В печени отношение NADH/NAD+ ниже, чем в сокращающейся мышце, поэтому лактатдегидрогеназная реакция протекает в обратном направлении, т.е. в сторону образования пирувата из лактата. Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами. Эту последовательность событий называют "глюкозо-лактатным циклом", или "циклом Кори".

Цикл Кори выполняет 2 важнейшие функции: 1 - обеспечивает утилизацию лактата; 2 - предотвращает накопление лактата и, как следствие этого, опасное снижение рН (лактоацидоз). Часть пирувата, образованного из лактата, окисляется печенью до СО2 и Н2О. Энергия окисления может использоваться для синтеза АТФ, необходимого для реакций глюконеогенеза.
- Образование глюкозы из аминокислот. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, окса-лоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратногр цикла, так и глюконеогенеза. Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в мышцах → аланин в печени → глюкоза в печени → глюкоза в мышцах. Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.

- Образование глюкозы из глицерола . Глицерол образуется при гидролизе триацил-глицеролов, главным образом в жировой ткани. Использовать его могут только те ткани, в которых имеется фермент глицерол киназа, например печень, почки. Этот АТФ-зависимый фермент катализирует превращение глицерола в α-глицерофосфат (глицерол-3-фосфат). При включении глицерол-3-фосфата в глюконеогенез происходит его дегидрирование NAD-зависимой дегидрогеназой с образованием дигидроксиацетонфосфата, который далее превращается в глюкозу.
Выход АТФ при аэробном распаде глюкозы.
Образование АТФ при гликолизе может идти 2 путями:
1. Субстратным фосфорилированием, когда для синтеза АТФ из АДФ и Н3РО4 используется энергия макроэргической связи субстрата.
2. Окислительным фосфорилированием за счет энергии переноса электронов и протонов по ЦПЭ (комплексы тканевого дыхания).
Если в дыхательной цепи окисляются ФАД-зависимые субстраты, то пунктов сопряжения остается 2: III и IV комплексы (Р/О = 2) на одну молекулу О2 – 2 молекулы Н3РО4.
Таким образом на третьем этапе за счет водороддонорной и собственно энергетической функции цикла Кребса получаем 24 АТФ.
В сумме на всех трех этапах аэробного окисления 1 моля глюкозы получаем 38 молей АТФ.
Полная энергия распада глюкозы составляет 2880 кДж/моль. Свободная энергия гидролиза высокоэнергетической связи АТФ равна 50 кДж/моль. Для синтеза АТФ при окислении глюкозы используется 38 · 50 = 1900 кДж, что составляет 65% от всей энергии распада глюкозы. Это максимально возможная эффективность использования энергии глюкозы.
Значение анаэробного гликолиза.
Анаэробный гликолиз, несмотря на небольшой энергетический эффект, является основным источником энергии для скелетных мышц в начальном периоде интенсивной работы, т.е. в условиях, когда снабжение кислородом ограничено.
Кроме того, зрелые эритроциты извлекают энергию за счет анаэробного окисления глюкозы, потому что не имеют митохондрий.
Глюконеогенез– это синтез глюкозы из веществ неуглеводной природы.
Главные субстраты глюконеогенеза:
Жирные кислоты служить источником глюкозы не могут.
Схема включения субстратов в глюконеогенез.

Глюконеогенез обеспечивает потребность организма в глюкозе в тех случаях, когда понижение уровня глюкозы не компенсируется гликогеном печени. Например: при относительно длительном голодании или резком ограничении углеводов в питании.
Процесс глюконеогенеза в основном протекает в печени и менее интенсивно в корковом веществе почек, а также слизистой оболочке кишечника.
Реакции гликолиза протекают в цитозоле, а часть реакций глюконеогенеза протекает в митохондриях.
Включение различных субстратов в гликонеогенез зависит от физиологического состояния организма.
Суммарное уравнение глюконеогенеза:
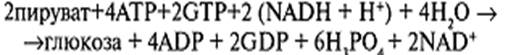
Наиболее значимо образование глюкозы, в первую очередь из пирувата, так как в него легко превращается основная гликогенная аминокислота – аланин, а так же молочная кислота, которая, поступая в значительных количествах в кровь из мышц после физической нагрузки, в печени под действием ЛДГ окисляется в пируват. В процессе катаболизма субстратов цикла Кребса образуется оксалоацетат, который также включается в реакции глюконеогенеза.
Основные стадии глюконеогенеза совпадают с реакциями гликолиза и катализируются теми же ферментами , только протекают они в обратном направлении.
Однако имеется очень важная особенность, обусловленная тем, что 3 реакции в гликолизе, катализируемые киназами: гексокиназой, фосфофруктокиназой и пируваткиназой, необратимы. Эти барьеры обходятся в глюконеогенезе с помощью специальных реакций.
Рассмотрим реакции глюконеогенеза, которые отличаются от реакций гликолиза и происходят в глюконеогенезе с использованием других ферментов.
- Образование фосфоенолпирувата из пирувата (обход пируваткиназной реакции).
Реакция катализируется двумя ферментами: пируваткарбоксилазой и фосфоенолпируваткарбоксикиназой.
Первая реакция протекает в митохондриях. Фермент – пируваткарбоксилаза является биотинзависимым (реакции карбоксилирования в клетках протекают с участием витамина Н):

Пируват + СО2 + АТФ + Н2О пируваткарбоксилаза Оксалоацетат (ЩУК) +АДФ + Н3РО4
Реакция протекает с использованием АТФ.
Затем в реакцию вступает второй собственный фермент глюконеогенеза – фосфоенолпируваткарбоксикиназа, реакция протекает в цитозоле:

ЩУК + ГТФ фосфоенолпируваткарбокскниаза Фосфоенолпируват + СО2 + ГДФ
В этой реакции образование мактоэргической связи фосфоенолпирувата осуществляется за счет энергии ГТФ, одновременно происходит декарбоксилирование оксалоацетата.
Далее следуют реакции гликолиза в обратном направлении до стадии образования фруктозо-1,6-дифосфата.
- Гидролиз фруктозо-1,6-дифосфата (обход фосфофруктокиназной реакции).

Фруктозо-1,6-дифосфат +Н2О Фруктозобифосфатаза Фруктозо-6-фосфат + Н3РО4
- Гидролиз фруктозо-6-фосфата (обход гексокиназной реакции)
Фермент - фосфатаза глюкозо-6-фосфата – фосфогексоизомераза.

Глюкозо-6-фосфат+Н2О Глюкозо-6-фосфатаза Глюкоза + Н3РО4
Свободная глюкоза, образующаяся в ходе этой реакции, поступает из печени в кровь и утилизируется тканями.
Энергетический баланс глюконеогенеза из пирувата: расходуется 6 моль АТФ на синтез 1 моль глюкозы и 2 моль пирувата.
Важное значение имеет глюконеогенез из глицерина и аминокислот.
При голодании, когда усиленно потребляются в качестве источников энергии жирные кислоты, в большом количестве образуется глицерин, который, активируясь с помощью АТФ под воздействием глицерокиназы превращается в α-глицерофосфат, затем окисляющийся под действием глицерофосфатдегидрогеназы в фосфодиоксиацетон – субстрат гликолиза.
Далее фосфодиоксиацетон используется в синтезе глюкозы т.е. в глюконеогенезе.
Глюконеогенез из лактата.
Лактат , образовавшийся при аэробном гликолизе превращается в печени в пируват, а лактат, образовавшийся в интенсивно работающих мышцах поступает в кровь, а затем в печень и превращается под действием ЛДГ в пируват, который включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами – эту последовательность называют циклом Кори или глюкозо-лактатным циклом.
На каждую молекулу лактата при глюконеогенезе расходуется три молекулы АТФ (точнее, две АТФ и одна ГТФ); поскольку для образования глюкозы необходимо 2 молекулы лактата, суммарный процесс глюконеогенеза из лактата описывается так:
2 лактат + 6 АТФ + 6 Н2О → глюкоза + 6 АДФ + 6 Н3РО4.
Образовавшаяся глюкоза может вновь поступать в мышцы и там превращаться в молочную кислоту.
Глюкоза + 2 АДФ + 2 Н3РО4 → 2 лактат + 2 АТФ + 2 Н2О.
Следовательно, в результате действия цикла Кори (глюкозо – лактатного цикла) работающие мышцы добывают 2 АТФ за счет расходования 6 АТФ в печени.
| | | следующая лекция ==> | |
| Аэробное окисление глюкозы. Энергетический баланс аэробного окисления 1 молекулы глюкозы | | | Лекция 16 |
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
[youtube.player]Глюконеогенез - процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Процесс протекает в основном в печени и менее интенсивно в корковом веществе почек, а также в слизистой оболочке кишечника. Эти ткани могут обеспечивать синтез 80-100 г глюкозы в сутки. На долю мозга при голодании приходится большая часть потребности организма в глюкозе. Это объясняется тем, что клетки мозга не способны, в отличие от других тканей, обеспечивать потребности в энергии за счёт окисления жирных кислот .Кроме мозга, в глюкозе нуждаются ткани и клетки, в которых аэробный путь распада невозможен или ограничен, например эритроциты (они лишены митохондрий), клетки сетчатки, мозгового слоя надпочечников и др. Первичные субстраты глюконеогенеза - лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма.
Лактат - продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно.
Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке.
Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
Большинство реакций глюконеогенеза протекает за счёт обратимых реакций гликолиза и катализируется теми же ферментами. Однако 3 реакции гликолиза термодинамически необратимы. На этих стадиях реакции глюконеогенеза протекают другими путями. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях.
Образование фосфоенолпирувата из пирувата . Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций первая из которых протекает в митохондриях. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата.
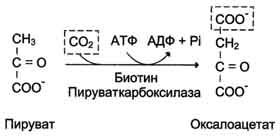
Пируват-карбоксилаза, катализирующая данную реакцию, - митохондриальный фермент, коферментом которого является биотин. Реакция протекает с использованием АТФ.
Дальнейшие превращения оксалоацетата протекают в цитозоле. Следовательно, на этом этапе должна существовать система транспорта оксалоацетата через митохондриальную мембрану, которая для него непроницаема. Оксалоацетат в митохондриальном матриксе восстанавливается с образованием малата при участии NADH (обратная реакция цитратного цикла).
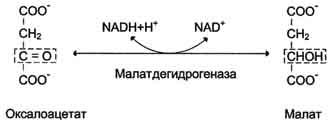
Образовавшийся малат затем проходит через митохондриальную мембрану с помощью специальных переносчиков. Кроме того, оксалоацетат способен транспортироваться из митохондрий в цитозоль в виде аспартата в ходе малат-аспартатного челночного механизма. В цитозоле малат вновь превращается в оксалоацетат в ходе реакции окисления с участием кофермента NAD + . Обе реакции: восстановление оксалоацетата и окисление малага катализируют малатдегидрогеназа, но в первом случае это митохондриальный фермент, а во втором - цитозольный. Образованный в цитозоле из ма-лата оксалоацетат затем превращается в фосфоенолпируват в ходе реакции, катализируемой фосфоенолпируваткарбоксикиназой - ГТФ-зависимым ферментом.
Образование глюкозы из лактата. Лактат, образовавшийся в интенсивно работающих мышцах или в клетках с преобладающим анаэробным способом катаболизма глюкозы, поступает в кровь, а затем в печень. В печени отношение NADH/NAD + ниже, чем в сокращающейся мышце, поэтому лактатдегидрогеназная реакция протекает в обратном направлении, т.е. в сторону образования пирувата из лактата. Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами. Эту последовательность событий называют "глюкозо-лактатным циклом", или "циклом Кори".
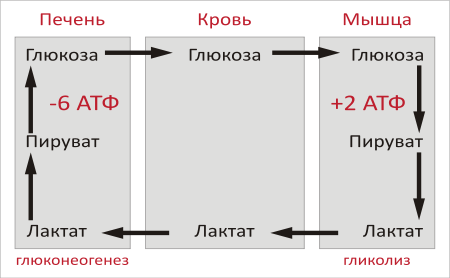
Цикл Кори выполняет 2 важнейшие функции: 1 - обеспечивает утилизацию лактата; 2 - предотвращает накопление лактата и, как следствие этого, опасное снижение рН (лактоацидоз). Часть пирувата, образованного из лактата, окисляется печенью до СО2 и Н2О. Энергия окисления может использоваться для синтеза АТФ, необходимого для реакций глюконеогенеза.
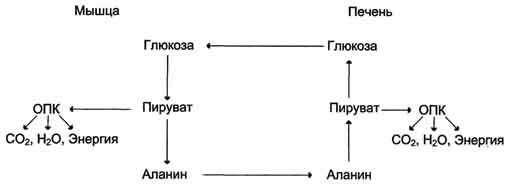
Образование глюкозы из аминокислот. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, окса-лоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратногр цикла, так и глюконеогенеза. Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в мышцах → аланин в печени → глюкоза в печени → глюкоза в мышцах. Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
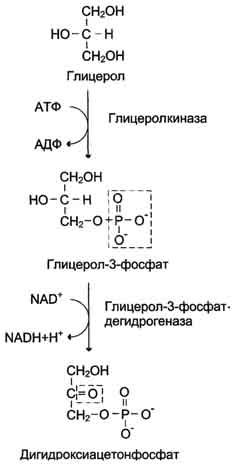
Образование глюкозы из глицерола. Глицерол образуется при гидролизе триацил-глицеролов, главным образом в жировой ткани. Использовать его могут только те ткани, в которых имеется фермент глицерол киназа, например печень, почки. Этот АТФ-зависимый фермент катализирует превращение глицерола в α-глицерофосфат (глицерол-3-фосфат). При включении глицерол-3-фосфата в глюконеогенез происходит его дегидрирование NAD-зависимой дегидрогеназой с образованием дигидроксиацетонфосфата, который далее превращается в глюкозу.
35.35 Представление о пентозофосфатном пути превращений глюкозы. Окислительные реакции (до стадии рибулозо-5-фосфата). Распространение и суммарные результаты этого пути (образование пентоз, НАДФН и энергетика)
Пентозофосфатный путь, называемый также гексомонофосфатным шунтом, служит альтернативным путём окисления глюкозо-6-фосфата. Пентозофосфатный путь состоит из 2 фаз (частей) - окислительной и неокислительной.
В окислительной фазе глюкозо-6-фосфат необратимо окисляется в пентозу - рибулозо-5-фосфат, и образуется восстановленный NADPH. В неокислительной фазе рибулозо-5-фосфат обратимо превращается в рибозо-5-фосфат и метаболиты гликолиза. Пентозофосфатный путь обеспечивает клетки рибозой для синтеза пуриновых и пиримидиновых нуклеотидов и гидрированным коферментом NADPH, который используется в восстановительных процессах. Суммарное уравнение пентозофосфатного пути выражается следующим образом:
3 Глюкозо-6-фосфат + 6 NADP + → 3 СО2 + 6 (NADPH + Н + ) + 2 Фруктозо-6-фосфат + Глицеральдегид- 3 -фосфат.
Ферменты пентозофосфатного пути, так же, как и ферменты гликолиза, локализованы в цитозоле. Наиболее активно пентозофосфатный путь протекает в жировой ткани, печени, коре надпочечников, эритроцитах, молочной железе в период лактации, семенниках.
В окислительной части пентозофосфатного путиглюкозо-6-фосфат подвергается окислительному декарбоксилированию, в результате которого образуются пентозы. Этот этап включает 2 реакции дегидрирования.
Первая реакция дегидрирования - превращение глюкозо-6-фосфата в глюконолактон-6-фосфат - катализируется NАDР + -зависимой глюкозо-6-фосфатдегидрогеназой и сопровождается окислением альдегидной группы у первого атома углерода и образованием одной молекулы восстановленного кофермента NADPH. Далее глюконолактон-6-фосфат быстро превращается в 6-фосфоглюконат при участии фермента глюконолактонгидратазы. Фермент 6-фосфоглюконатдегидрогеназа катализирует вторую реакцию дегидрирования окислительной части, в ходе которой происходит также и декарбоксилирование. При этом углеродная цепь укорачивается на один атом углерода, образуется рибулозо-5-фосфат и вторая молекула гидрированного NADPH. Восстановленный NADPH ингибирует первый фермент окислительного этапа пентозофосфатного пути - глюкозо-6-фосфатдегидрогеназу. Превращение NADPH в окисленное состояние NADP + приводит к ослаблению ингибирования фермента. При этом скорость соответствующей реакции возрастает, и образуется большее количество NADPH.
Суммарное уравнение окислительного этапа пентозофосфатногопути можно представить в виде:
Реакции окислительного этапа служат основным источником NADPH в клетках. Гидрированные коферменты снабжают водородом биосинтетические процессы, окислительно-восстановительные реакции, включающие защиту клеток от активных форм кислорода.
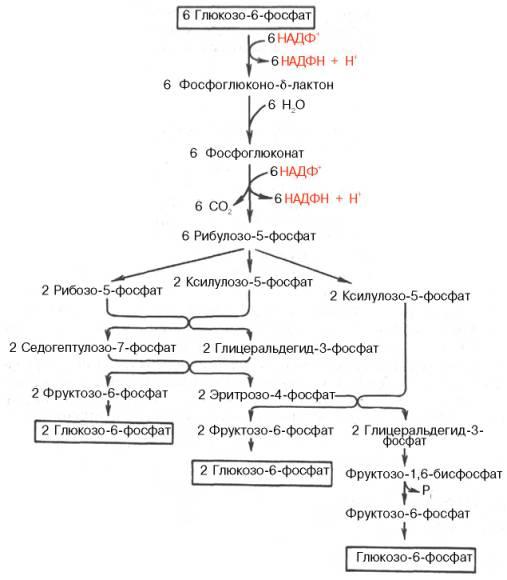
Окислительный этап образования пентоз и неокислительный этап (путь возвращения пентоз в гексозы) составляют вместе циклический процесс. Такой процесс можно описать общим уравнением:
Это означает, что из 6 молекул глюкозы образуются 6 молекул рибулозо-5-фосфат (пентозы) и 6 молекул СО2. Ферменты неокислительнойфазы превращают 6 молекул рибулозо-5-фосфат в 5 молекул глюкозы (гексозы). При последовательном проведении этих реакций единственным полезным продуктом является NADPH, образующийся в окислительной фазе пентозофосфатного пути. Такой процесс называют пентозофосфатным циклом. Протекание пентозофосфатного цикла позволяет клеткам продуцировать NADPH, необходимый для синтеза жиров, не накапливая пентозы.
Энергия, выделяющаяся при распаде глюкозы, трансформируется в энергию высокоэнергетического донора водорода - NADPH. Гидрированный NADPH служит источником водорода для восстановительных синтезов, а энергия NADPH преобразуется и сохраняется во вновь синтезированных веществах, например жирных кислотах, высвобождается при их катаболизме и используется клетками.
[youtube.player]Некоторые ткани, например, мозг, нуждаются в постоянном поступлении глюкозы. Когда поступление углеводов в составе пищи недостаточно, содержание глюкозы в крови некоторое время поддерживается в пределах нормы за счёт расщепления гликогена в печени. Однако запасы гликогена в печени невелики. Они значительно уменьшаются к 6 —10 ч голодания и практически полностью исчерпываются после суточного голодания. В этом случае в печени начинается синтез глюкозы de novo — глюконеогенез.Глюконеогенез — процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Процесс протекает в основном в печени и менее интенсивно в корковом веществе почек, а также в слизистой оболочке кишечника. Эти ткани могут обеспечивать синтез 80 — 100 г глюкозы в сутки. На долю мозга при голодании приходится большая часть потребности организма в глюкозе. Это объясняется тем, что клетки мозга не способны, в отличие от других тканей, обеспечивать потребности в энергии за счёт окисления жирных кислот (см. раздел 8).
Кроме мозга, в глюкозе нуждаются ткани и клетки, в которых аэробный путь распада невозможен или ограничен, например, эритроциты (они лишены митохондрий), клетки сетчатки, мозгового слоя надпочечников и др.
Первичные субстраты глюконеогенеза — лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма.
• Лактат — продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно.
• Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке.
• Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
На рисунке 7-44 показаны пункты включения первичных субстратов в глюконеогенез.
Рис. 7-44. Включение субстратов в глюконеогенез.
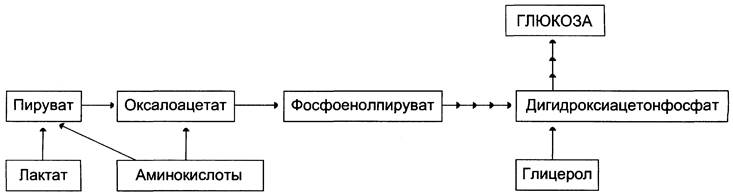
А. Реакции глюконеогенеза
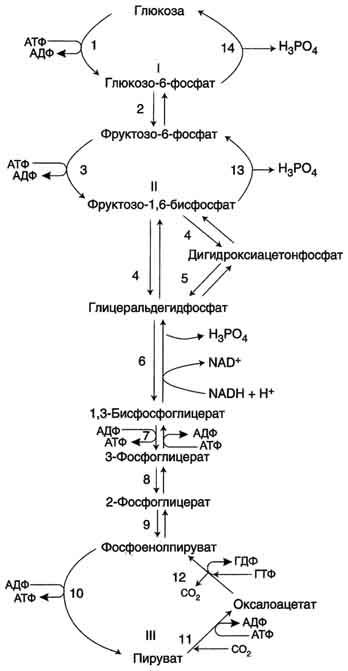
Большинство реакций глюконеогенеза протекает за счёт обратимых реакций гликолиза (рис. 7-45, реакции 9, 8, 7, 6, 5, 4, 2) и катализируется теми же ферментами. Однако 3 реакции гликолиза термодинамически необратимы. На этих стадиях реакции глюконеогенеза протекают другими путями.
Рис. 7-45. Гликолиз и глюконеогенез. Ферменты обратимых реакций гликолиза и глюконеогенеза: 2 — фосфоглюкоизомераза; 4 — альдолаза; 5 — триозофосфатизомераза; 6 — глицеральдегидфосфатдегидрогеназа; 7 — фосфоглицераткиназа; 8 — фосфоглицератмутаза; 9 — енолаза. Ферменты необратимых реакций глюконеогенеза: 11 — пируваткарбоксилаза; 12 — фосфоенолпируваткарбоксикиназа; 13 — фруктозо- 1,6-бисфосфатаза; 14 — глюкозо-6-фосфатаза. I-III —субстратные циклы.
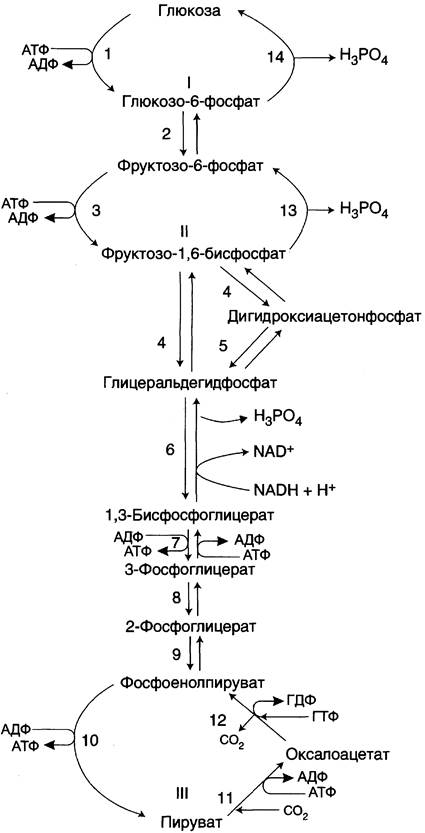
Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях.
Рассмотрим более подробно те реакции глюконеогенеза, которые отличаются от реакций гликолиза и происходят в глюконеогенезе с использованием других ферментов. Рассмотрим процесс синтеза глюкозы из пирувата.
1. Образование фосфоенолпирувата из пирувата — первая из необратимых стадий глюконеогенеза
Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций (рис. 7-45, реакции 11, 12), первая из которых протекает в митохондриях. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата (рис. 7-46). Пируват- карбоксилаза,катализирующая данную реакцию, — митохондриальный фермент, коферментом которого является биотин. Реакция протекает с использованием АТФ.
Рис. 7-46. Образование оксалоацетата из пирувата.
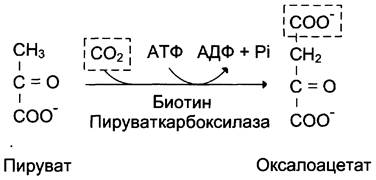
Дальнейшие превращения оксалоацетата протекают в цитозоле. Следовательно, на этом этапе должна существовать система транспорта оксалоацетата через митохондриальную мембрану, которая для него непроницаема. Оксалоацетат в митохондриальном матриксе восстанавливается с образованием малата (рис. 7-47) при участии НАDН (обратная реакция цитратного цикла). Образовавшийся малат затем проходит через митохондриальную мембрану с помощью специальных переносчиков. Кроме того, оксалоацетат способен транспортироваться из митохондрий в цитозоль в виде аспартата в ходе малат-аспартатного челночного механизма, рассмотренного ранее (рис. 7-39).
Рис. 7-47. Превращение оксалоацетата в малат.
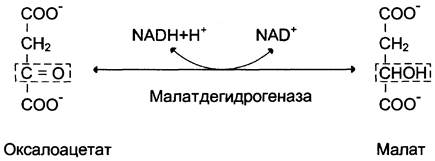
В цитозоле малат вновь превращается в оксалоацетат в ходе реакции окисления с участием кофермента NAD + . Обе реакции: восстановление оксалоацетата и окисление малата катализируют малатдегидрогеназа, но в первом случае это митохондриальный фермент, а во втором — цитозольный. Образованный в цитозоле из малата оксалоацетат затем превращается в фосфоенолпируват в ходе реакции, катализируемой фосфоенолпируваткарбоксикиназой — ГТФ-зависимым ферментом (рис. 7-48). Название фермента дано по обратной реакции.
Рис. 7-48. Превращение оксалоацетата в фосфоенолпируват.
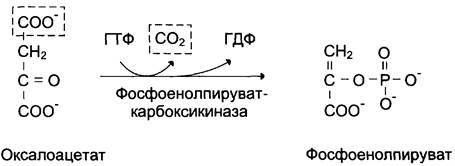
Схема всех реакций, протекающих на первой необратимой стадии глюконеогенеза, представлена на рис. 7-49.
Рис. 7-49. Образование оксалоацетата, транспорт в цитозоль и превращение в фосфоенолпируват. 1 — транспорт пирувата из цитозоля в митохондрию; 2 — превращение пирувата в оксалоацетат (ОА); 3 — превращение ОА в малат или аспартат; 4 — транспорт аспартата и маната из митохондрии в цитозоль; 5 — превращение аспартата и маната в ОА; 6 — превращение ОА в фосфоенолпируват.
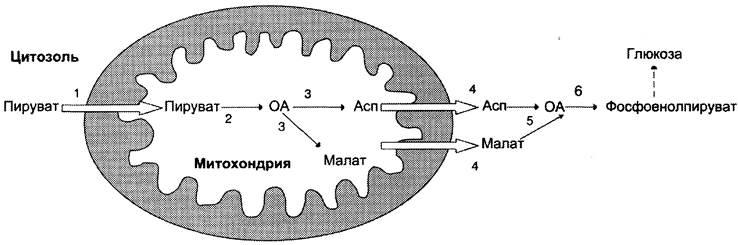
Следует отметить, что этот обходной участок глюконеогенеза требует расхода двух молекул с макроэргическими связями (АТФ и ГТФ) в расчёте на одну молекулу исходного вещества — пирувата. В пересчёте на синтез одной молекулы глюкозы из двух молекул пирувата расход составляет 2 моль АТФ и 2 моль ГТФ или 4 моль АТФ (для удобства рассуждений предлагается считать, что энергозатраты на синтез АТФ и ГТФ равны). После образования фосфоенолпирувата все остальные реакции также
протекают в цитозоле вплоть до образования фруктозо-1,6-бисфосфата и катализируются гликолитическими ферментами.
2. Гидролиз фруктозо-1,6-бисфосфата и глюкозо-6-фосфата
Отщепление фосфатной группы из фруктозо-1,6-бисфосфата и глюкозо-6-фосфата — также необратимые реакции глюконеогенеза. В ходе гликолиза эти реакции катализируют специфические киназы с использованием энергии АТФ. В глюконеогенезе они протекают без участия АТФ и АДФ и ускоряются не киназами, а фосфатазами — ферментами, принадлежащими к классу гидролаз. Ферменты фруктозо-1,6-бисфосфатаза и глюкозо-6-фосфатаза катализируют отщепление фосфатной группы от фруктозо-1,6-бисфосфата и глюкозо-6-фосфата. После чего свободная глюкоза выходит из клетки в кровь. Схема всех реакций глюконеогенеза представлена на рис. 7-45.
Итак, в печени существуют 4 фермента, которые принимают участие только в глюконеогенезе и катализируют обходные реакции необратимых стадий гликолиза. Это — пируват- карбоксилаза, фосфоенолпируваткарбоксикиназа, фруктозо-1,6-бисфосфатаза и глюкозо-6- фосфатаза.
3. Энергетический баланс глюконеогенеза из пирувата
В ходе этого процесса расходуются 6 моль АТФ на синтез 1 моль глюкозы из 2 моль пирувата. Четыре моль АТФ расходуются на стадии синтеза фосфоенолпирувата из оксалоацетата и ещё 2 моль АТФ на стадиях образования 1,3-бисфосфоглицерата из 3-фосфоглицерата.
Суммарный результат глюконеогенеза из пирувата выражается следующим уравнением:
2 Пируват + 4 АТФ + 2 ГТФ + 2 (NАDН + Н + ) + 4 Н2O —> Глюкоза + 4 АДФ + 2 ГДФ + 6 Н3РO4 + 2 NАD + .
Б. Синтез глюкозы из лактата
Лактат, образованный в анаэробном гликолизе, не является конечным продуктом метаболизма. Использование лактата связано с его превращением в печени в пируват. Лактат как источник пирувата важен не столько при голодании, сколько при нормальной жизнедеятельности организма. Его превращение в пируват и дальнейшее использование последнего являются способом утилизации лактата.
Лактат, образовавшийся в интенсивно работающих мышцах или в клетках с преобладающим анаэробным способом катаболизма глюкозы, поступает в кровь, а затем в печень. В печени отношение NАDН/NАD + ниже, чем в сокращающейся мышце, поэтому лакгатдегидрогеназная реакция протекает в обратном направлении, т. е. в сторону образования пирувата из лактата. Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами. Эту
Рис. 7-50. Цикл Кори (глюкозо-лактатный цикл). 1 — поступление лактата из сокращающейся мышцы с током крови в печень; 2 — синтез глюкозы из лактата в печени; 3 — поступление глюкозы из печени с током крови в работающую мышцу; 4 — использование глюкозы как энергетического субстрата сокращающейся мышцей и образование лактата.
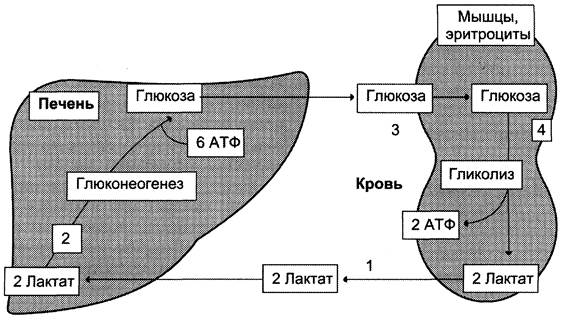
тиляции и, следовательно, ускорением выведения СO2 из организма. Однако основную роль в компенсации ацидоза играют почечные механизмы с участием аммиачного буфера (см. раздел 9). Одной из причин метаболического ацидоза может быть накопление молочной кислоты. В норме лактат в печени превращается обратно в глюкозу путём глюконеогенеза либо окисляется. Кроме печени, другим потребителем лактата служат почки и сердечная мышца, где лактат может окисляться до СO2 и Н2O и использоваться как источник энергии, особенно при физической работе.
Уровень лактата в крови — результат равновесия между процессами его образования и утилизации. Кратковременный компенсированный лактоацидоз встречается довольно часто даже у здоровых людей при интенсивной мышечной работе. У нетренированных людей лактоацидоз при физической работе возникает как следствие относительного недостатка кислорода в мышцах и развивается достаточно быстро. Компенсация осуществляется путём гипервентиляции.
При некомпенсированном лактоацидозе содержание лактата в крови увеличивается до 5 ммоль/л (в норме до 2 ммоль/л). При этом pH крови может составлять 7,25 и менее (в норме 7,36-7,44).
Повышение содержания лактата в крови может быть следствием нарушения метаболизма пирувата (рис. 7-51).
Рис. 7-51. Нарушения метаболизма пирувата при лактоацидозе. 1 — нарушение использования пирувата в глюконеогенезе; 2 — нарушение окисления пирувата.
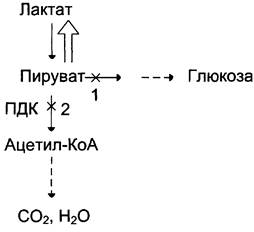
Так, при гипоксии, возникающей вследствие нарушения снабжения тканей кислородом или кровью, уменьшается активность пируватдегидрогеназного комплекса и снижается окислительное декарбоксилирование пирувата. В этих условиях равновесие реакции пируват лактат сдвинуто в сторону образования лактата. Кроме того, при гипоксии уменьшается синтез АТФ, что, следовательно, ведёт к снижению скорости глюконеогенеза — другого пути утилизации лактата. Повышение концентрации лактата и снижение внутриклеточного pH отрицательно влияют на активность всех ферментов, в том числе и пируваткарбоксилазы, катализирующей начальную реакцию глюконеогенеза.
Возникновению лактоацидоза также способствуют нарушения глюконеогенеза при печёночной недостаточности различного происхождения. Кроме того, лактоацидозом может сопровождаться гиповитаминоз В1, так как производное этого витамина (тиаминдифосфат) выполняет коферментную функцию в составе ПДК при окислительном декарбоксилировании пирувата (см. раздел 6). Дефицит тиамина может возникать, например, у алкоголиков с нарушенным режимом питания.
Итак, причинами накопления молочной кислоты и развития лактоацидоза могут быть:
• активация анаэробного гликолиза вследствие тканевой гипоксии различного происхождения;
• поражения печени (токсические дистрофии, цирроз и др.);
• нарушение использования лактата вследствие наследственных дефектов ферментов глюконеогенеза, недостаточности глюкозо-6-фосфатазы;
• нарушение работы ПДК вследствие дефектов ферментов или гиповитаминозов;
• применение ряда лекарственных препаратов, например, бигуанидов (блокаторы глюконеогенеза, используемые при лечении сахарного диабета).
В. Синтез глюкозы из аминокислот
В условиях голодания часть белков мышечной ткани распадается до аминокислот, которые далее включаются в процесс катаболизма. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты нитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, оксалоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как нитратного цикла, так и глюконеогенеза.
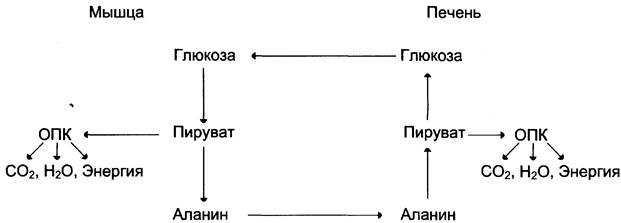
Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюконеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах —> пируват в мышцах —> аланин в мышцах —> аланин в печени —> глюкоза в печени —> глюкоза в мышцах (рис. 7-52). Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
Рис. 7-52. Глюкозо-аланиновый цикл.
Г. Синтез глюкозы из глицерола
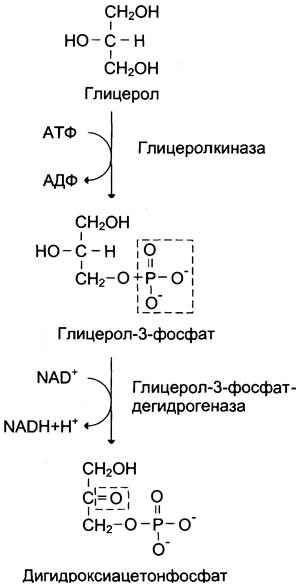
Глицерол образуется при гидролизе триацил- глицеролов, главным образом в жировой ткани. Использовать его могут только те ткани, в которых имеется фермент глицерол киназа, например, печень, почки. Этот АТФ-зависимый фермент катализирует превращение глицерола в α-глицерофосфат (глицерол-3-фосфат). При включении глицерол-3-фосфата в глюконеогенез происходит его дегидрирование NAD-зaвисимой дегидрогеназой с образованием дигидроксиацетонфосфата (рис. 7-53), который далее превращается в глюкозу.
Рис. 7-53. Превращение глицерола в дигидроксиацетон- фосфат.
Биологическая библиотека - материалы для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
[youtube.player]Читайте также:


