Герпес 6 типа микробиология
ВИРУС ЭПСТАЙНА-БАРР (ВЭБ)
ВЭБ вызывает инфекционный мононуклеоз, а также лимфопролиферативные болезни. Инфекционный мононуклеоз протекает с интоксикацией, поражением нёбных и глоточных миндалин, увеличением лимфатических узлов, печени, селезенки, изменениями в крови. ВЭБ относится к роду Lymphocryptovirus, семейству Herpesviridae.
Структура. Вирус имеет ядерные антигены – nuclear antigens (EBNAs) 1, 2, ЗА, ЗВ, 3C; латентные протеины (LPs), латентные мембранные протеины (LMPs) 1, 2 и две маленькие Эпстайна-Барр-кодируемые РНК (EBER)-молекулы – EBER-1 и EBER-2. EBNAs и LPs являются ДНК-связывающими белками, считающимися основными для развития инфекции (EBNA-1), иммортализации (EBNA-2) и других целей. LMPs – латентные мембранные белки (LMP-1, 2) с онкогенноподобным действием.
Эпидемиология. Антитела к вирусу имеются у большинства населения. Источником инфекции является больной человек или вирусоноситель. Вирус передается воздушно-капельным путем, при контакте через слюну.
Патогенез. После первичного размножения в эпителии носоглотки ВЭБ взаимодействует с молекулой CD21 В-лимфоцита и, проникнув в клетку, вызывает размножение В-лимфоцитов, персистирует в них. Особенно много инфицированных В-лимфоцитов находится в нёбных миндалинах. ВЭБ обусловливает латентную инфекцию в лимфоидной ткани, эпителиальных клетках рта и глотки, слюнных желез. Он вызывает бессимптомную, хроническую или острую инфекцию (в виде инфекционного мононуклеоза), а также лимфопролиферативные болезни.
Клиническая картина. Инфекционный мононуклеоз характеризуется высокой лихорадкой, недомоганием, лимфаденопатией, фарингитом, спленомегалией и изменениями крови. Мононуклеоз обусловлен появлением многочисленных бластоподобных мононуклеаров. Хроническая инфекция может развиваться как циклическая рекуррентная болезнь, которая сопровождается низкой лихорадкой, повышенной утомляемостью, головной болью и воспалением горла.
ВЭБ также может индуцировать лимфопролиферативные болезни и способствовать развитию опухолей. Люди с дефектом Т-клеточного иммунитета вместо инфекционного мононуклеоза могут страдать поликлональной лейкемияподобной В-клеточной пролиферативной болезнью и лимфомой. У реципиентов трансплантата после иммуносупрессивной терапии может развиться посттрансплантационная лимфопролиферативная болезнь вследствие контакта с ВЭБ или реактивации латентного вируса. Подобные болезни развиваются у больных с ВИЧ-инфекцией. У ВИЧ-инфицированных часто возникает волосистая оральная лейкоплакия - характерное для СПИДа поражение слизистой оболочки рта. Источником лимфомы Беркитта (эндемическая лимфома) – опухоли верхней челюсти – являются трансформированные В-лимфоциты. Лимфома Беркитта ассоциирована с малярией в Африке. Большой процент больных с лимфомой Ходжкина также содержат последовательности ДНК ВЭБ. Аналогично последовательности ДНК ВЭБ содержат и опухолевые клетки назофарингеальной карциномы, эндемичной на Востоке. В отличие от лимфомы Беркитта, в которой опухолевые клетки получены из лимфоцитов, опухолевые клетки носоглоточной карциномы, вызываемые ВЭБ, имеют эпителиальное начало.
Иммунитет клеточный (действие CD8 + -цитотоксических лимфоцитов) и гуморальный, обусловленный действием антител. Повторные заболевания не описаны.
Диагностика. Для инфекционного мононуклеоза характерны наличие атипичных лимфоцитов, лимфоцитоз (моноциты составляют 60-70 % белых кровяных клеток с 30 % атипичных лимфоцитов). Ранее применяли вспомогательные реакции, выявляющие гетерофильные антитела (агглютинация эритроцитов барана сывороткой крови больного и др.).
Свежая ВЭБ-инфекция выявляется в ИФА по различным показателям: появляются IgM-антитела к вирусному капсидному антигену (VCA), повышается титр EBNA и др. Затем при развитии клинических проявлений повышается уровень IgG-антител к VCA.
Лечение не разработано.
Профилактика. Специфическая профилактика инфекционного мононуклеоза не разработана. Больные изолируются на срок лихорадочного периода. Госпитализация проводится по клиническим показаниям. За лицами, контактировавшими с больными, устанавливают наблюдение в течение 20 суток с последнего дня контакта.
ГВЧ-6 и ГВЧ-7 относятся к роду Roseolovirus. Они являются лимфотропными вирусами, инфицируют Т-лимфоциты. ГВЧ-6 был выделен в 1986 г. группой Р. Галло из лимфоцитов крови больных лимфопролиферативными заболеваниями и СПИДом. Это распространенный лимфотропный вирус, как ВЭБ и ЦМВ. Предполагают, что ГВЧ-6 может постоянно инфицировать слюнные железы и выделяться из них. Очевидно, вирус становится латентным после первичного инфицирования и может реактивироваться после иммуносупрессии. Известны две разновидности: ГВЧ-6А и ГВЧ-6В.
ГВЧ-6 (Herpes lymphotropic virus) вызывает внезапную экзантему – exanthema subitum у младенцев (0,5-3 лет жизни) или roseola infantum с внезапным подъемом температуры (40 °С) и таким же спадом через 3 дня на фоне неяркой розовой папуломакулезной сыпи; синдром хронической усталости с субфебрильной температурой, потливостью, артралгией и слабостью. Возможны лимфаденопатия и неврологические нарушения.
ГВЧ-7 был выделен в 1990 г. Френкелем из Т-лимфоцитов здоровых людей, а затем его выделяли от больных СПИДом, синдромом хронической усталости.
ГВЧ-8 относится к роду Rhadinovirus. Он известен как герпесвирус, ассоциированный с саркомой Капоши. Обладает нейроинвазивными свойствами, определяясь в дорсальных спинальных ганглиях у больных саркомой Капоши и в цереброспинальной жидкости у ВИЧ-инфицированных.
Диагностика. ГВЧ-6 или ГВЧ-7 выделяют при кокультивировании лимфоцитов периферической крови с митогенактивированными лимфоцитами. В культуре образуются большие многоядерные клетки. Вирионы можно выделить из слюны.
В диагностике, в том числе ГВЧ-8, определяют маркерные гены возбудителя в ПЦР.
Лечение. Для лечения применяют аналоги нуклеозидов (ганцикловир, фоскарнет и др.), иммуномодуляторы (интерфероны).
Профилактика не разработана.
ГЛАВА 3. ГЕПАДНАВИРУСЫ (СЕМ. HEPADNAVIRIDAE)
Название семейства происходит от греч. hepar – печень и англ. DNA. Это семейство ДНК-содержащих оболочечных вирусов; представлено двумя родами: Orthohepadnavirus (от греч. orthos – правильный) и Avihepadnavirus (от лат. avis – птица).
 |
Структура. Вирус гепатита В – сложноорганизованный, ДНК-содержащий вирус сферической формы, диаметром 42-47 нм. Он состоит из сердцевины (core), построенной по кубическому типу симметрии, состоящей из 180 белковых частиц, составляющих сердцевинный НВс-антиген, диаметром 28 нм, и липидной оболочки, содержащей поверхностный HBs-антиген. Внутри сердцевины находятся ДНК-полимераза, обладающая ревертазной активностью, протеинкиназа и концевой белок НВе-антигена (рис. 29).
Рис. 29. Строение вируса гепатита В.
ДНК-полимераза является полифункциональным ферментом, она вовлекается во многие функции жизненного цикла вируса: способна синтезировать новые цепи ДНК, на матрице как ДНК, так и РНК, обладая как полимеразной, так и ревертазной активностью. Нуклеазная активность деградирует РНК-цепь в гибриде РНК-ДНК.
Геном представлен двухнитевой ДНК кольцевой формы, у которой плюс-цепь укорочена на 1/3 длины. Вирусный геном записан на минус-цепи и состоит из 4 открытых частично перекрывающихся рамок считывания: Р, С, S и X. Рамка считывания Р кодирует вирусную полимеразу и терминальный белок, найденный на минус-цепи ДНК. Рамка считывания С кодирует структурные белки нуклеокапсида и НВе-антиген. Рамка считывания S кодирует вирусные поверхностные гликопротеины. Продукт гена Х усиливает транскрипцию гомологичных и гетерологичных клеточных генов, участвуя в процессе развития гепатоцеллюлярной карциномы.
Полноценная минус-цепь ковалентно связана с ДНК-полимеразой, которая достраивает плюс-цепь до полноценной структуры.
Репродукция.Прикрепление HBV к гепатоцитам определяется HBs-антигеном, который связывается с полимеризованным человеческим сывороточным альбумином и другими сывороточными белками, что облегчает взаимодействие вируса и мишени в печени. После проникновения сердцевины вируса (рис. 30, 1) в гепатоцит неполная нить ДНК-генома достраивается; формируется полная двунитевая циркулярная ДНК (рис. 30, 2), созревший геном (рис. 30, 3) попадает в ядро клетки. Транскрипция генома контролируется клеточными элементами транскрипции, находящимися в гепатоцитах. При транскрипции генома образуются четыре иРНК, включая иРНК-прегеном (рис. 30, 4), больший (3500 нуклеотидов), чем геном (3200 нуклеотидов). Прегеном кодирует HBe- и HBc-антигены, полимеразу и белковый праймер для репликации ДНК, а также является матрицей для репликации генома вируса. Информационная РНК перемещаются из ядра клетки в цитоплазму и транслируются с образованием белков вируса. Белки сердцевины собираются вокруг прегенома. Нуклеокапсид сердцевины содержит РНК-зависимую ДНК-полимеразу, имеющую активность обратной транскриптазы и рибонуклеазы. В результате синтезируется минус-нить ДНК (рис. 30, 5), после чего РНК разрушается действием рибонуклеазы, поскольку далее синтезируется плюс-нить ДНК на матрице минус-нити ДНК (рис. 30, 6). Оболочка вириона образуется на HBs-содержащих мембранах эндоплазматической сети или аппарата Гольджи (рис. 30, 7). Сформировавшийся вирион выходит из клетки
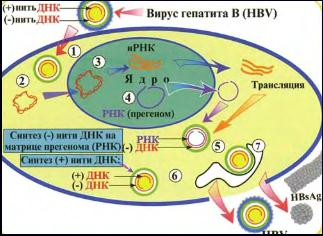 |
экзоцитозом.
Рис. 30. Репродукция вируса гепатита В.
Культивирование. Вирус гепатита В не культивируется на куриных эмбрионах, не обладает гемолитической и гемагглютинирующей активностью. Культивируется только в культуре клеток, полученной из ткани первичного рака печени в виде персистирующей инфекции, без оказания цитопатического и цитолитического действий и с малым накоплением вирионов. К вирусу чувствительны приматы: гориллы, шимпанзе, африканские зеленые мартышки.
Антигенная структура. В сердцевине вирионов находится ДНК-полимераза, НВе-антиген и НВс-антиген (антиген сердцевины). В свободном виде НВс-антиген не обнаруживается, он ассоциирован с частицей Дейна и выявляется в ядрах зараженных гепатоцитов. Напротив, НВе-антиген обнаруживается в свободном виде в крови обычно при наличии HBs-антигена.
Впервые HBs-антиген был обнаружен в 1963 г.и описан в 1965 г. Блюмбергом, в крови австралийских аборигенов, поэтому получил название австралийского антигена. HBs-антиген обнаруживается в крови не только в составе вириона, но и в виде самостоятельных фрагментов. Помимо полноценных вирионов, частиц Дейна, в крови обнаруживаются пустые неинфекционные частицы диаметром 22 нм, сферической или филаментозной формы, состоящие из HBs-антигена как результат его избыточной продукции. Сферические и филаментозные пустые частицы неинфекционны, но высокоиммуногенны и индуцируют анти-HBs-нейтрализующие антитела. Присутствие HBs-антигена в крови свидетельствует об инфицированности организма вирусом. HBs-антиген обладает гетерогенностью, подразделяясь на 4 антигенных подтипа, имея общую антигенную детерминанту, обозначаемую как а, и две пары взаимно исключающих детерминант: d и y, w и r, образующих 4 главных подтипа: adw, ayw, adr и ayr, которые распространены в различных географических зонах. Связи между клиническим течением и подтипом не наблюдается. Защита против одного подтипа обеспечивает защиту и против других за счет наличия общей детерминанты.
Резистентность. Вирионы чувствительны к эфиру и детергентам. Необычным свойством вирионов является устойчивость к высокой температуре: они выдерживают нагревание до 100 °С в течение 1-2 минут, при этом устойчивость к температуре повышается, если они находятся в сыворотке крови. После 10-минутного кипячения инфекционная активность вируса утрачивается, но антигенность сохраняется. Антигенность сохраняется при низких значениях рН (2,4). Инфекционная активность и антигенность не утрачиваются при ультрафиолетовом облучении плазмы крови, хранении при температуре -20 °С в течение многих лет, повторном замораживании и оттаивании.
Этиология парентерального гепатита В.Гепатит В – одно из наиболее серьезных, широко распространенных заболеваний вирусной этиологии. Возбудитель относится к семейству Hepadnaviridae, роду Orthohepadnavirus. Для него известно 8 генотипов (HBV-A, HBV-B, HBV-C…HBV-H), поражающих человека.
Эпидемиология. Вирус гепатита В передается восприимчивым лицам при контакте с кровью или другими жидкостями организма больных в острой стадии заболевания, но чаще с хроническими формами. Инфекция может возникнуть при введении крови или ее препаратов, при использовании нестерильных шприцев или игл (особенно у наркоманов), при гомосексуальных контактах, а также при гетеросексуальных контактах во время острой или хронической стадии инфекции. Возможна передача вируса от беременной матери к плоду путем трансплацентарной передачи вируса, либо во время родов и после родов, через молоко, слюну или сыворотку матери.
Важнейшими моментами эпидемического процесса при гепатите В являются: 1) длительное хроническое носительство; 2) вовлечение в эпидемический процесс лиц разного возраста; 3) наличие групп высокого риска заражения; 4) отсутствие сезонности заболевания.
Патогенез. Вирус проникает в клетки печени благодаря наличию на их поверхности специфических рецепторов, после разрушения наружных оболочек освобождается внутренний компонент, имеющаяся в его составе вирусная ДНК-полимераза достраивает недостающий участок плюс-цепи ДНК. Инфекция может проходить по одному из двух механизмов – продуктивному и интегративному. При продуктивном типе инфекции происходит транскрипция ДНК с помощью клеточных ферментов, образование иРНК, синтез вирусных белков. Репликация ДНК происходит по уникальному механизму с использованием в качестве промежуточной формы не ДНК, а РНК. Цикл репродукции оканчивается сборкой вирусных частиц в цитоплазме гепатоцитов с участием мембран ретикулоэндотелиальной системы. При интегративной инфекции после достройки второй нити ДНК происходит интеграция ДНК с клеточным геномом вблизи сильного промотора. В этом случае клетка начинает в огромном количестве производить HBs-антиген.
Клиническая картина. Инкубационный период острого гепатита В составляет от 45 до 180 суток (в среднем 90 суток). Чаще всего болезнь имеет циклическое течение. Преджелтушный период (продолжительность 1-4 недели) характеризуется постепенным началом. Появляется слабость, быстрая утомляемость, снижается работоспособность. Наряду с астеническими явлениями имеют место диспептические (ухудшение аппетита, тошнота, рвота). Повышение температуры тела нехарактерно. В этот период, как правило, увеличены печень и селезенка, а в конце его темнеет моча и светлеет кал.
Появление желтухи отмечают у 20-35 % больных остым гепатитом В. В желтушный период симптомы интоксикации, астенические и диспептические явления достигают наибольшей выраженности, еще больше увеличивается печень и селезенка. Продолжительность этого периода колеблется в широких пределах, но к концу 1-го месяца у большинства больных желтуха исчезает, хотя у некоторых из них восстановительный период приобретает затяжной характер (до 6 месяцев).
Полное выздоровление регистрируют у 90-95 % больных острым гепатитом В и лишь у 5-10 % из них отмечают переход в хронический гепатит. У больных с безжетушной формой острого гепатита В клиническая симптоматика отличается скудностью, что не исключает возможности перехода острого гепатита в хронический.
При фульминантной (молниеносной) форме острого гепатита В в течение короткого периода времени (несколько суток) развиваются симптомы острой печеночной недостаточности и появляются признаки печеночной энцефалопатии. У 76 % больных с фульминантной формой острого гепатита обнаруживаются маркеры дельта-вирусной инфекции (вирус гепатита D). Часто эта форма гепатита В завершается летальным исходом.
У больных с хроническим гепатитом В нередко сохраняются умеренно выраженные симптомы интоксикации, слабая желтуха, гепатомегалия, ряд внепеченочных поражений.
Иммунитет. При заболевании формируется специфический иммунитет, который в большинстве случаев приводит к освобождению организма от вируса. Образование антител индуцируют три вирусных антигена – HBs, HBc и HBe. Основным антигеном, индуцирующим протективные антитела, является HBs-антиген. В период реконвалесценции обнаруживаются антитела ко всем трем антигенам. Показаетлем перенесенной острой инфекции являются анти-HBc и анти-HBe-антитела, в то время как анти-HBs-антитела могут обнаруживаться и у носителей.
Диагностика строится на определении ряда специфических маркеров гепатита В методом ИФА. Основным серологическим маркером перенесенной и хронической инфекции является HBs-антиген. Не менее важным является определение в крови HBe-антигена – маркера инфекционности (свидетельствует об активной репликации вируса). Кроме этих маркеров, широкое применение находит выявление ДНК вируса с использованием ПЦР и ПЦР в реальном времени с определением вирусной нагрузки, а также обнаружение специфических антител методом ИФА. Из биохимических тестов используют определение в крови активности аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) и анализ уровня билирубина. Большое значение для диагностики и выбора терапии больных хроническим гепатитом В имеет исследование биоптатов печени.
Лечение. В терапии используют интерферон и ингибиторы ДНК-полимеразы.
Профилактика. Важнейшим и наиболее эффективным методом профилактики гепатита В является исключение попадания вируса при парентеральных манипуляциях, переливаниях крови. Для предотвращения предачи вируса половым путем принимают меры, аналогичные таковым при ВИЧ-инфекции.
Специфическая профилактика осуществляется вакцинацией в соответствии с национальным календарем прививок. Новорожденных детей (кроме родившихся у больных хроническим гепатитом В и носителей вируса) вакцинируют трижды по схеме 0-1-6 месяцев. Первоначально вакцину вводят в первые сутки жизни ребенка, повторно – через месяц и третий раз – в возрасте 6 месяцев (одновременно с третьей прививкой против коклюша, столбняка, дифтерии, а также полиомиелита). Третья иммунизация против гепатита В важна для достижения высокой концентрации специфических антител и длительного (до 10 лет) их сохранения. Осуществление такой схемы иммунизации позволяет эффективно предупреждать возможное перинатальное инфицирование.
Детей, родившихся у женщин с хронической инфекцией, острым гепатитом В в III триместре беременности, носителей вируса вакцинируют 4 раза по схеме: 1-е сутки жизни, 1-2-12 месяцев. У этих детей, имеющих наиболее реальный риск инфицирования вирусом при прохождении родовых путей, важно своевременно ввести вакцину (в первые 12-24 ч жизни). Четырехкратная иммунизация позволяет в наиболее ранние сроки достичь у них появления в крови анти-HBs в защитной концентрации и тем самым предупредить развитее инфекционного процесса.
Не нашли то, что искали? Воспользуйтесь поиском:
Герпес. Семейство Herpesviridae – большая группа широко распространенных в природе вирусов. Особенностью этих вирусов является способность вызывать латентную инфекцию, которая может активироваться через месяцы и годы в течение всей жизни индивидуума. У человека эта инфекция проявляется весьма разнообразно. Вирусы герпеса могут быть причиной врожденных уродств плода и новорожденных, тяжелых энцефалитов у взрослых и инфекционого мононуклеоза у молодых людей. Показано, что вирусы герпеса являются пусковым механизмом в возникновении некоторых опухолей. К настоящему времени более или менее полно изучены 6 видов герпесвирусов человека:
- Herpesvirus hominis 1 (HSV 1) – вирус простого герпеса 1 типа;
- Herpesvirus hominis 2 (HSV 2) – вирус простого герпеса 2 типа;
- Herpesvirus hominis 3 (HSV 3) – вирус ветряной оспы – опоясывающего лишая;
- Herpesvirus hominis 4 (HSV 4) – вирус Эпштейн-Барра;
- Herpesv
вирусов герпеса содержит линейную двухцепочечную ДНК, которая кодирует более 50 различных белков. Вирусные частицы сферической формы, крупные (180-200 нм), сложно устроенные. Тип симметрии нуклеокапсида – кубический. Вирус имеет суперкапсид.
Герпес. Репродукция вируса. Репродукция герпесвирусов происходит быстрее других ДНК-содержащих вирусов. Вирус попадает в клетку путем слияния мембраны суперкапсида с клеточной мембраной. После депротеинизации вирусная ДНК реплицируется в ядре зараженной клетки. Синтез вирусных белков происходит в цитоплазме, затем они мигрируют в ядро. Сборка вирусных частиц осуществляется на внутренней поверхности ядерной мембраны. Новое поколение вирионов (до 10 5 вирусных частиц) появляется в ядре клетки уже через 6 часов после заражения. Выход вирионов происходит после лизиса зараженной клетки.
Устойчивость во внешней среде. Герпесвирусы термолабильны, быстро инактивируются УФ лучами, спиртом, детергентами.
Герпес. Виды вируса. Заболевание у человека вызывают два серологических типа вируса. Herpes simplex virus 1 (HSV1) вызывает преимущественно поражение слизистых оболочек губ, полости рта, носа, в то время как Herpes simplex virus 2 (HSV2) обычно ассоциируется с инфекцией слизистых оболочек полового тракта. Частые рецидивы заболевания наблюдаются не более, чем у 1% инфицированных. У 25% латентная инфекция протекает более-менее благоприятно и сопровождается периодическими обострениями, при которых симптомы болезни время от времени возвращаются.
Ниже приведена характеристика клинических симптомов болезни, вызванной разными вирусами герпеса.
HSV1
Вирусом HSV1 инфицировано около 90% взрослых людей. Первичная инфекция наблюдается обычно у детей младшего возраста и носит генерализованный характер. Помимо лихорадки, симптомов общей интоксикации у больных развивается герпетический (афтозный) стоматит, проявлениями которого являются множественные изъязвления слизистой оболочки полости рта, воспаление десен. В процесс могут вовлекаться миндалины, задняя стенка глотки, нос. Обычно продолжительность заболевания не превышает 2-3 недель. В редких случаях генерализованная инфекция может протекать в виде герпетической экземы, которая сопровождается лихорадкой и пузырьковыми высыпаниями на большей части поверхности тела. Заболевание протекает тяжело, иногда с летальным исходом.
Герпес. Латентная инфекция. После первичной инфекции вирус персистирует (переживает) в течение всей жизни организма-хозяина в ганглиях тройничного нерва. По-видимому, небольшое количество вирионов все же синтезируется, поскольку вирус иногда удается выделить из секрета слизистой полости рта. В сыворотке крови поддерживается достаточно высокий уровень антител. При ослаблении иммунитета, причинами которого могут быть переохлаждение, избыточная инсоляция, инфекционные заболевания (например, ВИЧ-инфекция), происходит активация вирусной репродукции и возникает рецидив простого герпеса.
При рецидиве HSV 1 могут наблюдаться следующие клинические формы заболевания.
- Герпес губ и носа (herpes labialis et nasalis) – пузырьковые высыпания на границе кожи и слизистой оболочки;
- Герпетический кератоконъюнктивит. Инфицирование глаз. HSV1 вызывает необычайно болезненное изъязвление роговицы. Эта форма инфекции встречается довольно часто. Рецидивы инфекции могут приводить к развитию слепоты.
- Герпетический менингит. Чаще наблюдается у взрослых людей. Обычно протекает без серьезных осложнений и заканчивается полным выздоровлением.
- Герпетический энцефалит. Для этого заболевания характерна прогрессирующая демиелинизация нервных волокон с последующим развитием коматозного состояния. Отмечается высокий процент летальных исходов.
- Раневой герпес. Может осложнять открытые раны. Такие поражения часто возникают на пальцах и особенно опасны для врачей и сестер стоматологов.
В случае тяжелого иммунодефицита, например, при ВИЧ-инфекции, развивается хроническая генерализованная форма герпетической инфекции с обширными поражениями слизистой оболочки дыхательных путей или пищеварительного тракта.
HSV 2
Вирус простого герпеса 2-го типа является распространенным возбудителем генитального герпеса, передающегося половым путем. Продолжительность инкубационного периода 2-3 дня. При первичной инфекции развивается вирусемия с лихорадкой. Наблюдается увеличение региональных лимфоузлов. Вирус может быть выделен из уретры, шейки матки, задней стенки глотки у женщин, и из уретры и задней стенки глотки у мужчин. HSV 2 проникает в пояснично-крестцовые нервные ганглии, где он персистирует.
В 75% случаев персистентной инфекции могут быть возвраты симптомов болезни. Рецидив генитального герпеса сопровождается появлением на половых органах болезненных везикул с красноватым приподнятым снованием. В 1 мл жидкости везикул может содержаться от 1 до 10 млн вирусных частиц. Через 1-2 дня везикулы лопаются, изъязвляются и покрываются корочкой (струпом).
Больной заразен со времени появления везикул и 2-3 недели после формирования струпа. Наиболее тяжело болезнь протекает у женщин.
Имеются веские основания для заключения о связи частых рецидивов генитального герпеса и развития рака шейки матки.
Неонатальный герпес может развиться у новорожденных при прохождении плода через зараженный HSV 2 родовой канал. Болезнь младенца отличается особо тяжелым течением, проявляется уже в первый месяц жизни. У перенесших эту форму инфекции могут наблюдаться остаточные поражения нервной системы, глаз. Однако, в части случаев инфекция новорожденных протекает бессимптомно. Инфицирование беременных HSV2 может приводить к гибели и абортированию плода, иногда к формированию врожденной патологии.
Герпес. Лабораторная диагностика.
1. Выделение вируса из элементов герпетических высыпаний в различных клеточных культурах.
2. Выявление характерных для этой инфекции внутриклеточных телец -включений и многоядерных гигантских клеток в мазках – отпечатках с помощью световой микроскопии.
3. Иммуннофлуоресцентная микроскопия.
4. Обнаружение вирусного генома в эпителиальных соскобах и сыворотке крови методом полимеразной цепной реакции (ПЦР).
Герпес. Лечение. Используют противовирусные химиопрепараты – модифицированные нуклеозиды: ацикловир, зовиракс и др.
Вирус ветряной оспы – опоясывающего лишая (Herpesvirus hominis 3).
Две болезни – ветряная оспа (varicella) и опоясывающий лишай (herpes zoster), – представляют две фазы активности одного герпетического вируса – Herpesvirus hominis 3. Другое общепринятое название вируса – Varicella-Zoster virus (V-Z). Первичная инфекция V-Z – ветряная оспа – протекает в генерализованной форме с вирусемией, лихорадкой, высыпаниями на коже и слизистых оболочках. Опоясывающий лишай – это локальная инфекция в частично иммунном организме, рецидив инфекции V-Z.
Герпес тип 3. Патогенез.
Реактивация вируса (обычно у взрослых) часто следует за имевшими место травмами, перенесенными инфекционными заболеваниями, снижением общей резистентности организма, появлением опухолей, иммунодепрессией. Опоясывающий лишай проявляется везикулярными болезненными высыпаниями, сходными с теми, что наблюдаются при ветряной оспе, но с совершенно другим расположением. При zoster везикулы возникают на одной стороне грудной клетки или на животе, следуя направлениям чувствительных нервов, связанных с этой частью тела. Больной zoster заразен. У неиммунных лиц после контакта с больным herpes zoster развивается клиника типичной ветряной оспы.
Герпес тип 3. Диагноз инфекции вирусом V-Z ставится на основани клинических данных. При гистологическом исследовании тканей выявляются типичные для герпесвирусной инфекции гигантские клетки с внутриядерными тельцами – включениями.
Герпес тип 3. Профилактика. При частых рецидивах возможна активная иммунизация с помощью убитой вакцины. Пассивная иммунизация – выборочная – с помощью специфического иммуноглобулина.
Herpesvirus hominis 4 (HSV4, вирус Эпштейн-Барра)
Герпес тип 4. Вирус Эпштейн-Барра (ЕВ – вирус) назван так по имени исследователей, которые описали это вирус. ЕВ-вирус является этиологическим агентом инфекционного мононуклеоза, а также индуцирует развитие злокачественных опухолей – лимфомы Беркитта и карциномы носоглотки.
Герпес тип 4. Инфекционный мононуклеоз. Заболевание получило свое название потому, что в крови больных обнаруживается большое число моноцитов. Вирус передается со слюной. Самый распространенный путь инфицирования – через поцелуй (kissing disease).
Инфекционный мононуклеоз (ИМ) чаще возникает у молодых людей. Симптомами болезни являются лихорадка, увеличение шейных лимфатических узлов, головная боль, озноб, потливость, ощущение усталости. У больных развивается тяжелая ангина. Болезнь может длиться от нескольких дней до нескольких недель и сопровождаться симптомами гепатита и менингита.
Герпес тип 4. Диагностику ИМ проводят на основании клинических проявлений и обнаружения в крови атипичных больших лимфоцитов. При ИМ часто наблюдается повышение концентрации антител разной специфичности -гетерофильных антител, что может привести к появлению ложноположительных серологических реакций с различными антигенами (например, может иметь место ложноположительная реакции Вассермана).
Вирус ЕВ может индуцировать возникновение злокачественной опухоли клеток лимфатических узлов – лимфомы Беркитта. Большая часть инфицированных вирусом В-лимфоцитов погибает. В оставшейся части зараженных В-лимфоцитов вирус ЕВ персистирует, что приводит к их злокачественной трансформации. Трансформированные клетки приобретают способность к неконтролруемой пролиферации.
Herpesvirus hominis 5 ( цитомегаловирус)
Цитомегаловирус (ЦМВ) вызывает персистентную инфекцию клеток, которые увеличиваются в размерах. Хроническая ЦМВ-инфекция обнаруживается более чем у 80% взрослых людей. Вирус передается воздушно-капельным и контактным путем. Первичная инфекция обычно протекает в стертой форме сопровождается гепато-спленомегалией и вирусемией. Вирус длительное время выделяется со слюной и с мочой. Если первичное инфицирование происходит во время беременности, вирус может преодолевать плацентарный барьер и инфицировать плод. Инфекция приводит либо к гибели плода, либо к формированию дефектов развития (микроцефалия, атрофия зрительного нерва, глухота). У новорожденных с ЦМВ-инфекцией наблюдается судорожный синдром, желтуха, пневмония, тромбоцитопения, гастроэнтерит. Внутриутробное ифицирование ЦМВ является самой частой причиной умственной отсталости.
Особенно восприимчивы к ЦМВ-инфекции пациенты с онкологическими заболеваниями и ВИЧ-инфицированные.
ЦМВ опасен для реципиентов крови, костного мозга и органных трансплантантов. Инфекция часто протекает бессимптомно, но может привести к развитию тяжелой пневмонии. Генерализованная форма ЦМВ инфекции может привести к гибели больного.
Герпес тип 5. Лабораторная диагностика. Первичную инфекцию можно диагностировать с помощью исследования парных сывороток крови методом ИФА. Нарастание титра антител к ЦМВ во второй пробе сыворотки в 4 и более раз может свидетельствовать об активном инфекционном процессе. Диагностику вирусемии проводят методом полимеразной цепной реакции: определяют присутствие в сыворотке крови вирусной ДНК.
Herpesvirus hominis 6 (HSV 6)
Вирус впервые выделен из моноцитов периферической крови больного ВИЧ-инфекцией. Первоначально HSV 6 вирус считали возбудителем В – клеточной лимфомы. Позже была доказана способность этого вируса поражать Т-лимфоциты и другие клетки. Вирус широко распространен в человеческой популяции. Инфекция часто наблюдается уже у 6-месячных детей. К периоду половой зрелости 100% населения имеют антитела к HSV 6.
Механизм передачи неизвестен. Вирус культивируется in vitro только в В-лимфоцитах. В фазе лихорадки вирус обнаруживают примерно в 10% нуклеаров крови. Персистентная инфекция не описана.
Герпес тип 6. Клинические проявления.
В большинстве случаев инфекция бессимптомная и лишь у 30% наблюдается клинически выраженное заболевание. Продолжительность инкубационного периода – около 5 дней. В остром периоде отмечается трехдневная лихорадка (38-40 0 С), на высоте которой появляются высыпания у основания ушей и за ушами. Это заболевание имеет несколько названий: Exanthema subitum, Roseola infantum, ложная краснуха. Иногда при этой болезни регистрируется тонзиллит, лимфаденит подъязычных лимфоузлов, судорожный синдром, потеря голоса.
Читайте также:


