Дисбиоз кишечника кандидозного генеза
… иногда представляет значительные проблемы, связанные с недостаточной осведомленностью врачей в области клинической микологии.
Представители рода Candida представляют собой дрожжевые грибы, родственные Ascomycetes. Род Candida включает разнообразные виды (Candida spp.), среди которых основное значение, как возбудители кандидоза, имеют: Candida albicans, Candida tropicalis, Candida parapsilosis, Candida glabrata, Candida dubliniensis, Candida lusitaniae, Candida krusei.
Candida spp. представляют собой компонент микрофлоры, симбионтной для человека. У 10-25% населения, не имеющих клинических признаков грибкового поражения, Candida spp. непостоянно выявляются в полости рта, у 65-80% в содержимом кишечника. Candida spp. обнаруживаются в детрите гастродуоденальных язв примерно в 17% случаев.
Весьма важная роль в ограничении роста популяции Candida принадлежит также бактериям кишечным симбионтам. Нормальная микрофлора, населяющая просвет желудочнокишечного тракта, вырабатывает вещества с антибактериальной активностью (в частности, бактериокины и короткоцепочечные жирные кислоты), которые предотвращают внедрение патогенных микроорганизмов и избыточный рост, развитие условнопатогенной флоры. Кишечные палочки, энтерококки, бифидобактерии и лактобациллы обладают наиболее выраженными антагонистическими свойствами.
( ! ) Важно отметить, что кандидоз слизистой оболочки кишечника часто протекает как микст-инфекция. Это происходит из-за того, что дисбиоз (то есть дефицит облигатных бифидумбактерий и лактобацилл) создает условия для адгезии на слизистой оболочке кишечника не только дрожжеподобных грибов, но и условно-патогенной бактериобиоты. Так, частота микст-инфекции при дисбиозе кишечника с повышенной пролиферацией грибов рода Candida составляет 63%. При этом чаще обнаруживают ассоциацию со значительным количеством бактерий с так называемым протеолитическим основным путем метаболизма (условно-патогенными): Esherichia coli, Ristella spp., Clostridium perfringens, Klebsiella spp., Morganella spp., Bacteroides spp., Staphilococcus aureus, Pseudomonas aeruginosa.
Клиническая картина . ( ! ) В основе дисбиоза кишечника с избыточным ростом грибов рода Candida spp. лежит действие метаболитов грибов, резорбируемых в кишечнике при массивном росте последних в просвете кишки. При кандидозном дисбиозе кишечника общее состояние больных, как правило, удовлетворительное. Симптомы заболевания: флатуленция, умеренный абдоминальный дискомфорт, изменения в консистенции кала и частоте стула (обычно кал кашицеобразный, чаще 2-3 раз в сутки), признаки умеренной интоксикации и тенденция к обострению аллергических и псевдоаллергических заболеваний, зуд в области заднего прохода.
В литературе имеются указания на возможность предъявления жалоб пациентами с первичным ростом грибов Candida albicans в желудочно-кишечном тракте (и вторично - на слизистых оболочках половых органов) не отличающиеся от таковых при синдроме хронической усталости. Нет только гриппоподобных симптомов. Показано, что многие больные с синдромом хронической усталости положительно реагируют на противогрибковую терапию и диету, препятствующую избыточному росту Candida spp. Предполагают, что механизм эффекта от такой терапии связан с тем, что C.albicans подавляет функцию Т- и NK-клеток слизистых оболочек, как и вирусы герпеса, цитомегалии и Эпштейна–Барра. Иными словами, наряду с вирусами, значение хронического кандидоза в патогенезе синдрома хронической усталости достаточно весомо.
Связь между микрофлорой кишечника и псориазом, хронической рецидивируюшей крапивницей, а также топическим и себорейным дерматитом до сих пор остается лишь предположением. Во всяком случае, при псориазе возможен импульс усиления из-за поражения грибом Candida кишечника, а при подтвержденной колонизации кишечника, когда применяют лечение и удаляют патогенную микрофлору, кожная симптоматика улучшается. Взаимосвязь с колонизацией грибом Candida кишечника имеется также при себорейной экземе, которая часто встречается уже у младенцев в виде млечных струпьев, часто вместе с пеленочным дерматитом (проф. Нольтинг в этих случаях предлагает проводить санацию кишечника с помощью нистатина).
Учитывая то, что специфические клинические проявления кандидоза отсутствуют (что и осложняет диагностику данной патологии) заподозрить кандидозное поражение кишечника позволяет наличие характерных факторов риска.
К факторам риска кандидоза пищеварительного тракта относят :
• детский возраст (недоношенные дети, дети со сниженной массой тела);
• старческий возраст;
• лечение антибактериальными препаратами и глюкокортикостероидами;
• интенсивная цитостатическая полихимиотерапия, лучевая терапия;
• сахарный диабет и другие заболевания эндокринной системы,
• СПИД и генетически детерминированные иммунодефициты;
• гемодиализ;
• тяжелые и хронические истощающие заболевания (в том числе онокологические заболевания включая гемобластозы), нарушения трофологического статуса;
• несбалансированное питание (дефицит в рационе белков и витаминов).
( ! ) Таким образом, диагноз дисбиоза кишечника с избыточным ростом Candida spp. устанавливают при наличии следующих критериев:
• синдром кишечной диспепсии;
• лабораторно подтвержденный дисбиоз кишечника;
• рост Candida spp. свыше 1000 КОЕ/г при посеве кала.
Эндоскопические исследования с цитологическим изучением препаратов малоинформативны, так как чаще всего патологических изменений не выявляют.
Дифференциальный диагноз кандидоза кишечника проводят также с хроническими инфекционными колитами, ферментопатиями (лактазной, глютеновой), опухолями, синдромом раздраженной толстой кишки.
Лечение кандидозного дисбиоза кишечника . Показано, что лечение флуконазолом может угнетать рост Candida spp. в кишечнике, результатом чего является его полная санация у 1/3 пациентов, а у остальных происходит снижение степени контаминации фекалий более чем в 6 раз. В то же время у 2/3 пациентов полной деконтаминации кишечника от дрожжеподобных грибов не происходит. Вероятно, это связано с тем, что около 80% активных метаболитов флуконазола выводятся из макроорганизма с мочой, а в просвете кишечника данный антифунгальный препарат накапливается мало. Чаще всего для селективной деконтаминации кишечника от микромицетов рода Candida назначают нистатин и натамицин, которые практически не резорбируются в кишечнике, что делает лечение относительно безопасным и обусловливает стабильно высокую концентрацию указанных препаратов именно в просвете кишечника, что является залогом успешного лечения дисбиоза кишечника с избыточным ростом Candida spp. Самым частым нежелательным эффектом при назначении этих средств является раздражение слизистых оболочек и обусловленная этим тошнота и диарея. Необходимо отметить, что в отличие от нистатина натамицин разрешен для применения у новорожденных, беременных, кормящих, а также при язвенной болезни и панкреатите. Натамицин назначают per os (в таблетках) взрослым по 100 мг 4 раза в день, а детям по 100 мг 2 раза в день. Курсы лечения этим средством длительностью 5-10 дней обычно приводят к элиминации дрожжеподобных грибов из кишечника (однако при сохранении факторов, снижающих эффективность местных антифунгальных барьеров, возможна реинфекция).
Успешная деконтаминация позволяет рассчитывать на успех в восстановления и консолидации эубиоза, то есть стойкого устранения дефицита нормобиоты кишечника. С этой целью традиционно используют про- и пребиотики. Выбор пребиотиков, то есть стимуляторов интестинального роста резидентной нормобиоты, не содержащих живые культуры нормобиоты, сегодня достаточно широк. Действующим началом таких средств может являться лактулоза, пектин, некоторые биологически активные продукты обмена облигатных бактерий и другие.
В последние десятилетия оппортунистические инфекции, вызываемые условно–патогенными грибами, занимают особое место в практике клиницистов различных специальностей.
Как ни парадоксально, отчасти это связано с теми успехами, которых достигла современная медицина в лечении онкологических заболеваний и в борьбе с возбудителями серьезных инфекций. Кроме того, очевидно, что в последние десятилетия наблюдается увеличение интенсивности воздействия на организм человека внешних факторов, вызывающих развитие иммуносупрессивных состояний.
Помимо этого, конец XX века ознаменовался значительным распространением фатального заболевания – ВИЧ–инфекции.
Патологические состояния, вызванные воздействием грибов рода Candida на организм человека, также относятся к разряду оппортунистических микозов.
Характеристика возбудителя
Представители рода Candida представляют собой дрожжевые грибы, родственные Ascomycetes.
Род Candida включает разнообразные виды (Candida spp.), среди которых основное значение, как возбудители кандидоза, имеют: Candida albicans, Candida tropicalis, Candida parapsilosis, Candida glabrata, Candida dubliniensis, Candida lusitaniae, Candida krusei.
Candida spp. представляют собой компонент микрофлоры, симбионтной для человека. У 10–25% населения, не имеющих клинических признаков грибкового поражения, Candida spp. непостоянно выявляются в полости рта, у 65–80% – в содержимом кишечника. Candida spp. обнаруживаются в детрите гастродуоденальных язв примерно в 17% случаев.
Весьма важная роль в ограничении роста популяции Candida принадлежит также бактериям – кишечным симбионтам. Нормальная микрофлора, населяющая просвет желудочно–кишечного тракта, вырабатывает вещества с антибактериальной активностью (в частности, бактериокины и короткоцепочечные жирные кислоты), которые предотвращают внедрение патогенных микроорганизмов и избыточный рост, развитие условно–патогенной флоры. Кишечные палочки, энтерококки, бифидобактерии и лактобациллы обладают наиболее выраженными антагонистическими свойствами.
Факторы вирулентности Candida
Грибы рода Candida обладают адгезивностью к эпителиальным клеткам. Прикрепление к слизистой оболочке является одним из условий для дальнейшей инвазии микроорганизма в подлежащие ткани.
Способность к адгезии у представителей различных видов Candida значительно различается; наиболее высока эта способность у C.albicans, C.tropicalis, C.dubliniensis; наименьшая – у Candida glabrata, Candida krusei. В качестве защитного барьера, препятствующего прикреплению микроба к слизистой оболочке, важную роль играет муцин – гликопротеин клеточной стенки эпителиальных клеток.
Факторы агрессии этих микроорганизмов включают протеазы и гликозидазы, способные интенсивно расщеплять муцин.
Как фактор вирулентности также рассматривают способность к быстрому образованию нитей псевдомицелия; эта особенность в наибольшей степени выражена у C.albicans.
Вирулентность микроорганизмов подвержена внутривидовой изменчивости, в зависимости от генотипа [1,3].
Факторы риска развития кандидоза
В качестве общих факторов, предрасполагающих к развитию кандидоза органов пищеварения и последующей лимфо–гематогенной диссеминацией грибков, как и в случаях других оппортунистических инфекций, выступают состояния, при которых наблюдается недостаточность иммунной защиты организма. Они включают:
1) Физиологические иммунодефициты (период новорожденности и ранний детский период, сенильный иммунодефицит, беременность, стрессовые состояния).
2) Врожденные иммунодефициты (синдром Ди– Джорджи, Незелофа, Шедиака–Хигаши и др.).
3) Инфекция вирусом иммунодефицита человека в терминальной стадии (синдром приобретенного иммунодефицита). Микозы составляют 70% в структуре клинических проявлений ВИЧ–инфекции.
4) Онкологические заболевания (включая гемобластозы); химиотерапия злокачественных опухолей, сопровождающаяся тяжелой гранулоцитопенией ( Патогенез развития кандидоза кишечника
Исследования последних лет в большой степени прояснили закономерности взаимодействия грибков Candida с организмом хозяина. По современным представлениям, можно выделить два принципиально различных механизма патогенеза кандидоза органов пищеварения: инвазивный и неинвазивный кандидоз [3].
Инвазивный кандидоз обусловлен внедрением нитчатой формы гриба Candida в ткани. Первым этапом кандидоза, как инфекционного процесса, служит адгезия к эпителиоцитам, затем происходит инвазия в эпителиальный слой, проникновение за пределы базальной мембраны.
Этим проявлениям микробной агрессии макроскопически соответствуют эрозивно–язвенные дефекты стенки кишечника различного размера и формы, трещины, мембранные наложения (сходные с таковыми при псевдомембранозном колите), полиповидные или сегментарные циркулярные образования.
При прогрессирующей инвазии возможно развитие лимфо–гематогенной диссеминации грибов (системный кандидоз с поражением слизистых оболочек других органов; генерализованный кандидоз с поражением висцеральных органов).
В экспериментальной модели на животных, перорально инфицированных C.albicans в условиях иммуносупрессии, показано первоначальное возникновение эрозий и язв слизистой оболочки в подвздошной кишке, колонизация лимфоидных образований кишечника, их некроз и дальнейшая диссеминация. Отсутствие макроскопических изменений, по всей видимости, не должно рассматриваться, как свидетельство против инвазивного кандидоза.
При диссеминированных формах кандидоза в лимфатических узлах и протоках обнаруживаются многоядерные гигантские клетки, содержащие грибы, что, вероятно, отражает феномен незавершенного фагоцитоза.
Инвазивный кандидоз чаще наблюдается в органах, выстланных многослойным плоским эпителием (полость рта, пищевод), и реже – цилиндрическим эпителием (желудок, кишечник), что, вероятно, связано с особенностями местной иммунной защиты.
Неинвазивный кандидоз не сопровождается превращением грибка в нитчатую форму; наблюдается избыточный рост его колоний в просвете полого органа – кишечника. Предполагается, что важное патогенетическое значение при этом имеет нарушение полостного и пристеночного пищеварения, проникновение в системный кровоток микробных компонентов и метаболитов, развитие в той или иной степени выраженной системной иммунно–воспалительной реакции.
Ниже приводится классификация кандидоза органов пищеварения:
1. Оро–фарингеальный кандидоз (хейлит, гингивит, заеды, глоссит, стоматит, фарингит).
2. Кандидоз пищевода (осложнения – кровотечение, стриктура).
3. Кандидоз желудка:
– диффузный (специфический эрозивно–фибринозный гастрит);
– фокальный (вторичный для язвы желудка).
4. Кандидоз кишечника:
– фокальный (вторичный для язвы 12–перстной кишки, при неспецифическом язвенном колите);
– неинвазивный (избыточный рост Candida в просвете кишечника).
5. Ано–ректальный кандидоз:
– инвазивный кандидоз прямой кишки,
– перианальный кандидозный дерматит.
Ниже охарактеризованы основные проявления кандидозного поражения кишечника, который, как уже было сказано выше, является основой для развития системных проявлений.
Клиническая картина кандидоза кишечника
Особенности течения кандидоза кишечника недостаточно четко очерчены, недостаточно хорошо изучены и мало знакомы большей части практикующих врачей. Характерно, что у погибших от разных причин больных, у которых при аутопсии были обнаружены макроскопические изменения кишечника, соответствующие инвазивному кандидозу, при жизни, как правило, отмечалась весьма скудная симптоматика со стороны желудочно–кишечного тракта, а эндоскопический диагноз часто был ошибочным.
Нередко при обнаружении единичных изъязвлений кишечной стенки врач затрудняется в их трактовке, а по результатам морфологического исследования дается заключение о неспецифических воспалительных изменениях в краях язвенных дефектов, тогда как целенаправленное микологическое исследование не проводится.
Клинические проявления кандидоза кишечника могут быть различными в зависимости от уровня поражения.
При диффузном инвазивном кандидозе кишечника имеются проявления энтероколита: жалобы на боли в животе спастического характера, метеоризм, наличие патологических примесей в стуле (крови и слизи), обычно имеются признаки системного кандидоза (поражение слизистых оболочек полости рта, гениталий). При эндоскопическом исследовании выявляются изменения по типу фибринозно–язвенного колита.
При инвазивном фокальном кандидозе кишечника проявления заболевания могут напоминать упорное, резистентное к традиционной терапии, течение язвенной болезни 12–перстной кишки или неспецифического язвенного колита.
При неинвазивном кандидозе кишечника пациенты предъявляют жалобы на неоформленный стул, метеоризм, дискомфорт в животе, с положительной клинико–лабораторной динамикой при лечении антимикотическими препаратами.
При инвазивном кандидозе прямой кишки могут отмечаться симптомы проктита (боли, тенезмы, патологические примеси в кале). В ряде случаев этому сопутствуют явления перианального кандидо–дерматита.
Кандидоз кишечника нередко сопровождается субфебрильной лихорадкой [1,3,5].
Осложнения
В качестве осложнений кандидоза кишечника возможно развитие кишечной перфорации, пенетрации язв в окружающие органы, кровотечения, генерализации с поражением паренхима тозных органов, развитием грибкового сепсиса.
Поражение паренхиматозных органов (печень, желчный пузырь, поджелудочная железа и др.) весьма часто сопутствует глубокой нейтропении (менее 500 нейтрофилов в мм3 крови) и наблюдается в терминальной фазе СПИДа [1,3,5].
Летальность при инвазивном кандидозе достигает 25–55%. Для некоторых категорий больных (реципиенты трансплантатов, пациенты с острым лейкозом) инвазивные микозы являются основной причиной летального исхода.
Диагностика
Вопрос о диагностике кандидоза кишечника и определении показаний к противогрибковой терапии исключительно важен.
Для диагностики кандидоза абсолютно информативно обнаружение Candida в стерильных жидкостях (спинно–мозговой, лаважной, перитонеальной и др.) или обнаружение грибов в тканях (нередко обнаруживаются изменения по типу гранулем с некрозом).
Для повышения чувствительности культуральных и морфологических методов диагностики кандидоза рекомендуется исследовать несколько биоптатов слизистой оболочки.
Биопсированную ткань собирают в 2 стерильные чашки Петри или стерильные баночки с завинчивающейся крышкой; одну пробу заливают 10% раствором формальдегида и направляют для гистологического исследования, вторую используют для микологического исследования.
Материал транспортируют в микробиологическую лабораторию, защищая от прямых солнечных лучей. Необходимо, чтобы материал был доставлен на микологическое исследование не позднее 1 ч после взятия при хранении в условиях комнатной температуры или не более чем через 3 ч при хранении при +4°С.
Микроскопическое исследование необходимо проводить в нативных и окрашенных препаратах.
Псевдомицелий Candida также можно выявить в мазке–отпечатке слизистой оболочки или мазке–отпечатке из дна язвы (окраска по Романовскому–Гимзе).
На поверхности плотной питательной среды в чашке Петри делают отпечаток исследуемым кусочком ткани, затем производят рассев петлей. Этот же кусочек ткани помещают в 50 мл жидкой питательной среды (среда Сабуро, сусло) и инкубируют при +37°С в течение 5 дней.
Широко применяются методы быстрой идентификации C.albicans. Этот вид Candida способен образовывать ростковые трубки и короткие нити псевдомицелия в течение 2–4 часов при +37°С на сыворотке крови, яичном белке и др. подобных средах. Для вида C.albicans этот феномен характерен в 90% случаев.
Для эффективного лечения необходимо стремиться к определению видовой принадлежности грибков Candida и определению индивидуальной чувствительности штамма к антимикотическим средствам; некоторые штаммы Candida lusitanlae устойчивы к амфотерицину, Candida krusei и Candida glabrata – к флуконазолу.
Обнаружение Candida в крови позволяет поставить диагноз генерализованного кандидоза только в сочетании с соответствующей клинической симптоматикой (особенно информативно повторное обнаружение Candida в крови). Следует помнить о том, что у 70–80% больных, реально страдающих генерализованным кандидозом, выявить грибы при посеве крови не удается.
Значение серологических методов состоит, главным образом, в выявлении больных с вероятными инвазивными микозами. Ложноположительные результаты серологических проб возможны при миконосительстве и у здоровых людей, сенсибилизированных антигенами грибов; ложноотрицательные пробы могут наблюдаться при иммунодефиците.
Набор Platelia Candida может использоваться для определения антигена–маннана Candida, например, в сыворотке крови пациента с циркуляцией микроорганизма. С помощью первого набора порог определения антигенных структур равен 2,5 нг/мл, с помощью второго в связке с методом порог определения – 0,5 нг/мл.
В диагностике неинвазивного кишечного кандидоза, при котором отсутствует тканевой биопсийный материал для микологического исследования, в качестве стандарта диагностики предлагается использовать следующие критерии: рост свыше 1000 КОЕ/г Candida spp. при посеве кишечного содержимого, взятого в стерильных условиях, в сочетании с явлениями кишечной диспепсии и положительной клинико–лабораторной динамикой при лечении антимикотическими препаратами [1].
Дифференциальный диагноз инвазивного кишечного кандидоза (при обнаружении макроскопических изменений кишечника) необходимо проводить с хроническими воспалительными заболеваниями кишечника, антибиотикоассоциированной диареей, обусловленной инфекцией C. difficile, злокачественным поражением, ишемическим колитом.
Неинвазивную форму кандидоза следует дифференцировать с широким спектром энтеритов и колитов другой этиологии. Косвенным свидетельством в пользу наличия кандидоза кишечика могут выступать внекишечные системные проявления кандидоза.
Лечение
Следует еще раз подчеркнуть, что одно лишь обнаружение грибов рода Candida при бактериологическом анализе испражнений (по принятой методике в России), независимо от наличия или отсутствия симптомов кишечной диспепсии, не может служить показанием для назначения пациенту антимикотических средств.
Для лечения кандидоза кишечника необходимо назначение препаратов, неадсорбирующихся из просвета кишечника.
Сегодня существуют разнообразные антимикотические средства. Такие препараты, как амфотерицин В, итраконазол, кетоконазол, флуконазол, обладают системным действием, могут применяться местно, перорально и внутривенно.
К практически неадсорбирующимся антимикотическим средствам относятся леворин, нистатин и натамицин (Пимафуцин). Назначение леворина и нистатина с достаточно высокой частотой сопровождается развитием побочных эффектов (диспепсические явления, аллергия, токсический гепатит).
Пимафуцин (натамицин) – противогрибковый полиеновый антибиотик широкого спектра. Обладает фунгицидным потенциалом. Пимафуцин связывает стеролы клеточных мембран, нарушая их целостность и функции, что приводит к гибели микроорганизмов. К натамицину чувствительно большинство патогенных дрожжевых грибов, в наибольшей степени – Candida albicans.
Пимафуцин обладает более высокой эффективностью по сравнению с нистатином. Случаев резистентности к натамицину в клинической практике не встречалось; при многократном применении этого препарата минимальная подавляющая концентрация его в отношении C.albicans не меняется. Пимафуцин в таблетках действует только в просвете кишечника, практически не всасывается из желудочно–кишечного тракта.
При применении таблеток в первые дни лечения возможны диспепсические явления – тошнота и диарея, которые не требуют отмены препарата и самостоятельно разрешаются в ходе лечения. Единственным противопоказанием к назначению Пимафуцина является повышенная чувствительность к компонентам препарата. Пимафуцин можно назначать в периоды беременности и лактации, а также новорожденным детям.
Для лечения кишечного кандидоза необходимо проведение курса лечения невсасывающимися противогрибковыми препаратами в течение 7–10 дней. Нистатин назначают по 250000 ЕД 6–8 раз в сутки (суточная доза – до 3 млн ЕД) в течение 14 дней. Его назначают по 100 мг (1 таблетке) 2–4 раза в день в течение 7–10 дней [1].
Опираясь на изложенные выше положения и клинический опыт, приходится признать, что тактика лечения кандидоза слизистых оболочек внекишечной локализации только местными противогрибковыми средствами или препаратами системного действия, всасывающимися желудочно–кишечного тракта, по своей сути ошибочна.
Поскольку источником лимфо–гематогенного распространения вирулентных штаммов Candida, вызывающих системный кандидоз, является кишечник,– без подавления роста грибов в его просвете противогрибковая терапия оказывается неэффективной или наблюдается лишь кратковременный нестойкий эффект.
При системном кандидозе доза нистатина может быть повышена до 4–6 млн ЕД/сут, одновременно назначается местно действующее противогрибковое средство. При системном кандидозе Пимафуцин используется в той же дозе при одновременном назначении местно действующего противогрибкового средства. В тяжелых случаях к комплексной терапии добавляются препараты с системным действием [1,5].
Особенно важны своевременное распознавание и терапия кишечного кандидоза, как профилактика системного и генерализованного кандидоза у больных групп риска, к которым относятся прежде всего пациенты, получающие противоопухолевую лучевую и/или химиотрепию, противотуберкулезные препараты, пациенты, готовящиеся к плановым операциям на органах брюшной полости.
В данных ситуациях наиболее предпочтительно назначение невсасывающихся противогрибковых препаратов, поскольку их длительный и повторный прием существенно не влиет на фармакодинамику других препаратов.
Основным критерием эффективности терапии является не получение отрицательного результата посева на грибы, а прежде всего исчезновение основных проявлений болезни, нормализация количества грибов по данным микологического исследования (при возможности адекватного проведения посева кишечного содержимого). Для достижения эффекта нередко приходится прибегать к повторным курсам лечения [1].
В данной статье ставилась цель расширить представления практических врачей о гибкости взаимодействия организма человека с симбионтной микрофлорой, о патогенном потенциале, которым обладает безобидный кишечный комменсал – Candida.
Перед интернистами и специалистами по медицинской микологии стоят актуальные задачи отчетливого определения распространенности и клинического значения грибковых инфекций в клинической практике, разработки алгоритма диагностики и показаний к лечению кандидоза кишечника.
1. Златкина А.Р., Исаков В.А., Иваников И.О. Кандидоз кишечника как новая проблема гастроэнтерологии. // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2001. – №6. – С.33–38.
2. Danna P.L., Urban C., Bellin E., Rahal J.J. Role of Candida in pathogenesis of antibiotic–associated diarrhoea in elderly patients.//Lancet/–1991.–Vol.337.–P.511–514.
3. Prescott R.J., Harris M., Banerjee S.S. Fungal infections of small and large intestine.//J.clin.Path.–1992.–Vol.45.–P.806–811.
4. Redmond H.P., Shou J., Kelly C.J. et al. Protein–calorie malnutrition impairs host defense against Candida albicans.//J.Surg.Res.–1991.–Vol.50.–P.552–559.
5. The Merck Manual. Sixteenth edition. Copyright (c) 1992 by Merck&Co., Inc.
Сегодня мало кто знает, что кандидоз кишечника является болезнью, которая формируется при разрастании грибков Candida. Инфекционные микроорганизмы довольно интенсивно распространяются в человеческом кишечнике, желудке. Это приводит к нарушениям микрофлоры кишечника с проявлением сильного дисбактериоза.
Непременное условие формирования этого недуга – сокращение защитной функции организма, поскольку нормальный показатель иммунитета может прекрасно пресекать размножение таких грибков. Сегодня будут описаны причины, симптомы и лечение этого неприятного, а подчас и опасного недуга. 
Этиология кишечного кандидоза
Изначально микроорганизм Candida присутствует у всех людей и прекрасно уживается с их микрофлорой. Однако при сокращении охранных реакций организма, инфекция стремительно распространяется и приводит к появлению типичной симптоматики кандидоза. Но иммунитет не снижается беспричинно.
Кишечная молочница может сформироваться у человека, регулярно подвергающегося стрессам, болеющим теми недугами, при терапии которых приписываются антибиотики. Да, да – употребление антибиотиков способно стать причиной формирования кандидоза. Но есть и прочие этиологии сокращения охранных функций организма.
К таковым относят:
- иммунная, аллергическая патология;
- вновь появившийся либо врожденный иммунодефицит;
- болезни ЖКТ хронических форм;
- сокращение иммунитета физиологической природы (старение, вынашивание плода, младенчество и т.д.);
- состояние после лучевой, химиотерапий;
- неправильный рацион питания.
Если же вести речь об этиологии формирования Кандида в кишечнике у грудничков, то здесь инфекция заносится путем бытового либо вертикального путей. Помимо этого, микроорганизмы в кишках у малыша могут появиться вследствие получения недостаточного объема требуемых элементов с едой (молоком мамы).
Симптоматика кишечного кандидоза
Характерные симптомы кандидоза кишечника могут быть различны, что связано со степенью серьезности недуга.
Общие признаки формирования микроорганизмов Candida выглядят следующим образом:
- появление субфебрильной температуры тела;
- наличие спазмов в животе с сильными болевыми синдромами;
- диареи;
- вздутие кишечника;
- повышенное газообразование;
- в кале проявляются кровяные и слизистые примеси.
Обычно молочница кишечника, имеющая такие симптомы, проявляется при не инвазивном виде болезни. Инвазивный вид одновременно с общей симптоматикой сопровождается еще и воспалительным процессом кишечника. Одновременно с этим пациент может страдать молочницей полости рта, урогенитальных органов.
Если говорить об очаговой инвазивной болезни, она способна сопровождаться язвами двенадцатиперстной кишки. Подчас развивается проктит либо наблюдается появление инфецирований участков прямой кишки грибками дрожжеподобной природы. Обычно вылечить кандидоз такой формы достаточно проблематично.
Формы заболевания
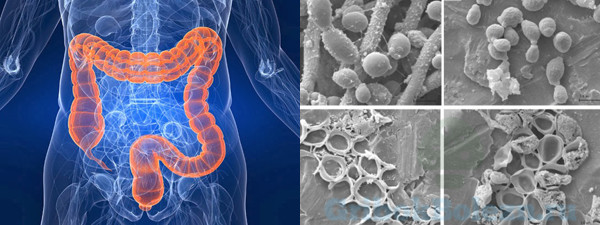
Сегодня описываемый недуг встречается в 2-х формах. Это зависит от механизмов его формирования.
Кишечный кандидоз бывает:
- Инвазивным, когда отмечается проникновение грибка дрожжеподобной природы в каждую клетку кишечника.
– Инвазивная форма в свою очередь бывает очаговой, фокальной и диффузной. - Не инвазивным, когда происходит значительное увеличение численности инфекции исключительно в кишечном просвете.
Для того чтобы правильно ответить на вопрос, как лечить кандидоз кишечника, необходимо верно диагностировать его форму.
Диагностика заболевания
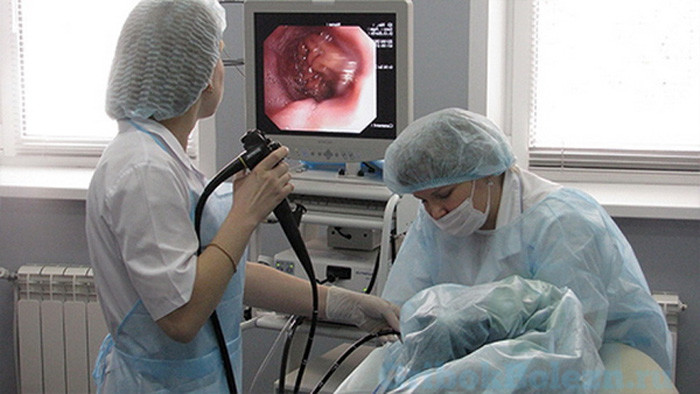
Процесс диагностирования этого недуга проблематичен. Это объясняется тем, что кандидоз способен находиться в пассивной форме либо принимать участие в иных патологических процессах.
Если нет возможности установить визуально признаки кандидоза кишечника, осуществляются следующие процедуры:
- Эндоскопический процесс исследования.
– Предоставляет возможность дать оценку слизистой органа, подтвердить либо опровергнуть наличие беловатого налета или язвенного дефекта. - Рентген.
- Микробиологический процесс исследования.
– Дает возможность установить вид инфекции и осуществить верный вариант терапии.
– Диагностировать недуг позволяет и кал пациента. - Цитологический и гистологический процесс исследования.
– Делается путем соскоба с оболочки слизистой кишечника, щипцовой биопсии и браш-биопсии.
Обычно молочница кишечника проявляется в зависимости от механизма попадания инфекции в ткань органа. К примеру, при непопадании нитчатого вида грибка непосредственно в ткани, а интенсивного его распространения в кишечном просвете, относится к категории не инвазивной болезни.
Важно! Поскольку речь идет о достаточно серьезной болезни, заниматься самостоятельной диагностикой, а тем более, лечением строго запрещено.
Последствия заболевания

Доктора утверждают, что кандидоз кишечника такое заболевание, лечение которого нужно начинать как можно раньше. Иначе недуг способен привести к развитию серьезных осложнений. При установлении факта появления молочницы, с лечением затягивать не следует для предотвращения ее трансформации в хронический тип.
Помимо этого, инфекция с течением времени станет поражать ткань органа на большую глубину, разрушая их целостность, что может явиться причиной появления кровотечения. Поэтому кишечная молочница должна лечиться незамедлительно после диагностирования. Наличие болезни в период беременности может привести к заражению плода либо прервать беременность.
Но максимально пострадать от кандидоза кишечника могут малыши, поскольку с регулярным жидким стулом из их организма выводятся витамины, полезные вещества, так необходимые для полноценного развития. Как итог – понижаются показатели массы тела, роста и налицо визуально определяемое отставание в развитии от одногодок в физическом плане.
Общие правила терапии
Как только была диагностирована молочница в кишечнике, назначается комплексный курс терапии, состоящий из 3-х направлений.
- Противогрибкового лечения, что необходимо для сокращения жизнеспособности грибков дрожжеподобной природы.
- Так же лечащим доктором приписывается комплексное лечение, нужное для нормализации работы гастроинтестинальной функции – восстановления бактериального микробиоценоза, активизации местной защиты организма и налаживания работы кишечника.
- Врачами приписывается специальная диета при кандидозе кишечника, основная задача которой – восстановление функционирования системы пищеварения.
Только системный, комплексный подход позволит решить проблему кишечного кандидоза.
Чтобы грибы Кандида не развивались в кишечнике, доктора прописывают средства с антимикотическим действием. В процессе выбора лекарства обычно отдается предпочтение средствам местного воздействия (обычно ректальным).
К наиболее востребованным препаратам относятся:
В случае формирования серьезных форм болезни используются средства для системной терапии – Итраконазол, Флуконазол и др. Эти препараты приписываются докторами для устранения таких неприятностей, как дисбактериоз и молочница кишечника. Они могут быть пероральной формы выпуска (таблетки), внутривенной (раствор) либо ректальной (свечки). Предусмотрено комбинирование формы комплексного и местного действий.
Важно! Определять средство и тактику терапии может лишь врач исключительно при индивидуальном подходе.
Применять ректальные препараты следует лишь после тщательной гигиены (подмывание мылом для деток без добавок). Только такое отношение к собственному организму даст положительный итог при борьбе с недугом.
Многие доктора для облегчения симптоматики любого типа кишечного кандидоза приписывают различные ферменты. Процесс интенсивного расщепления еды под воздействием ферментов дает возможность устранить у пациента метеоризм, а также нормализовать кишечную моторику.
Здесь большую роль играет правильное питание при кандидозе кишечника, предписанное диетологом.
В случае сокращения иммунных функций организма при лечении грибков используют иммуномодуляторы и иммунокорректоры. Причем определять перечень требуемых медикаментозных препаратов должен иммунолог лишь после установления точного показателя баланса, а также установления этиологии болезни.

В процессе терапии кишечного кандидоза народные средства имеют второстепенное значение и должны подбираться исключительно доктором.
Важно! Самостоятельное лечение недуга способно привести к негативным, необратимым последствиям. В особенности это касается женщин в положении и малышей самого раннего возраста.
Ниже рассмотрим несколько вариантов средств народной медицины.
Против грибковой инфекции кишечника результативным средством оказывается масло облепихи. Кроме борьбы с воспалительным процессом масло обеспечивает стимуляцию иммунитета организма, а также способно оказывать охранную функцию на раздраженную стенку пищеварительного тракта.
Масло облепихи относится к наиболее действенному средству народной медицины, запускающему механизмы восстановления ткани. Это средство на каждый день следует употреблять по 1-2 чайных ложки ежедневно длительностью 10 дней во время еды.
Отличный вариант – это терапия препаратами, где основой выступают травы с лекарственным воздействием. Они имеют противовоспалительное, восстанавливающее, иммуникорректирующее действия.
Самые распространенные травы и материалы – это:
- белая ромашка;
- зверобой;
- шалфей;
- корки граната;
- кора дуба;
- литья черной смородины;
- черемуха и пр.
Нужно помнить, что лечение кандидоза кишечника народными средствами должно осуществляться под контролем доктора.
Заключение
Подводя итоги статьи можно сделать такой вывод – чтобы Кандиды в кишечнике человека, симптомы которых были рассмотрены чуть выше не распространялись, необходима комплексная терапия. Она должна включать повышение защитных функций иммунитета, процедуры по закаливанию, прием медикаментозных средств.
Помимо этого, вне зависимости от того, какой способ терапии будет выбран, он должен учитывать возрастную категорию пациента, его физиологические возможности и имеющиеся недуги. Если принимались антибиотики, необходимо обязательно восстанавливать микрофлору с использованием лекарственных медикаментов и рационального, сбалансированного рациона питания.
Читайте также:


