Лабораторный практикум микозы пчел
Правильный сбор материала из пораженных ногтей - залог успешного микробиологического исследования. Забирая материал, не всегда захватывают участки ногтя, содержащие жизнеспособные грибы. Нежизнеспособные грибы в культуре, естественно, не вырастут, и их вид установить не удастся.
Участок ногтя, который надо взять, определяется формой онихомикоза.
Так, при поверхностной форме онихомикоза следует делать соскобы с поверхности ногтевой пластинки.
При самой распространенной дистальной подногтевой форме наиболее жизнеспособные грибы располагаются под ногтевой пластинкой. Материал, который направляют на исследование, должен включать не только обрезок ногтевой пластинки, но и соскоб с ногтевого ложа, из-под пластинки.
Кроме того, следует захватывать и области неизмененного ногтя, поскольку на границе между ними и пораженными участками ногтя располагаются самые активные грибы.
При проксимальной подногтевой форме брать материал трудно. В этих случаях иногда, особенно если собираются проводить гистологическое исследование или дифференциальную диагностику, предпринимают биопсию ногтя, изредка используют бормашину.
При паронихиях делают соскобы с проксимального валика и из-под него.
Во всех случаях, чтобы избежать бактериальной контаминации, перед взятием образца следует обработать ноготь этиловым спиртом.
МИКРОСКОПИЧЕСКОЕ ИССЛЕДОВАНИЕ
Микроскопическое исследование патологического материала на грибы производят в нативных и окрашенных препаратах.
Для приготовления неокрашенных препаратов полученный материал размельчают при помощи скальпеля или препаровальной иглы и помещают на середину предметного стекла. Для более четкого выявления элементов гриба производят просветление (мацерацию) материала. С этой целью прибегают к помощи различных веществ, чаще всего едкой щелочи (КОН, NaOH), которые растворяют эпидермальные чешуйки, слизь, гной, просветляют пигмент волоса и тем самым делают грибы доступными для исследования.
На размягченные чешуйки кожи или ногтя, которые помещают на середину предметного стекла, наносят 1-3 капли 20 - 30% раствора КОН (NaOH). Исследуемый материал в каплях щелочи осторожно подогревают над пламенем спиртовки до появления нежного белого ободка из кристаллов щелочи по периферии капли. Подогревать до кипячения не следует. После подогревания каплю накрывают покровным стеклом, избегая попадания пузырьков воздуха.
Р. А. Аравийский и Г. И. Горшкова (1995) рекомендуют просветленные и накрытые покровным стеклом препараты кожных чешуек и волос оставлять на 5 - 10 мин, а ногтевых пластинок – на 30 - 40 мин до микроскопирования.
Просветление препаратов можно проводить без подогревания, для этого их оставляют в 20% растворе КОН на 30 - 60 мин или используют другие методы просветления патологического материала: хлораллактофенолом по Аману; лактофенолом; раствором, содержащим по 15% диметилсульфоксида и КОН в воде. Хорошие результаты получают после просветления ногтевых пластинок, помещенных в 5% раствор КОН на 24 ч, подогревания в этом случае не требуется.
Микроскопическое исследование производят на обычном лабораторном микроскопе без иммерсии.
Конденсор микроскопа должен быть опущен, диафрагма сужена. В начале препарат находят на стекле при малом увеличении (40х), последующее исследование производят при большем увеличении (100х);
детально препарат изучают при увеличении 400х. Необходимо исследовать несколько препаратов с тем, чтобы увеличить надежность анализа и избежать ложноположительных результатов.
Ошибки в микроскопической диагностике грибов могут возникнуть в связи как с дефектами приготовления препарата, так и с недостаточной опытностью лаборанта.
Дефекты изготовления прежде всего бывают связаны:
с перегреванием препарата, что может привести к выпадению кристаллов щелочи, разрушению волоса и появлению мелкозернистого распада в патологическом материале.
Линейное расположение удлиненных ровных кристаллов щелочи весьма напоминает нити септированного мицелия даже на чистом стекле без патологического материала.
Дифференциально-диагностическими признаками являются исключительное однообразие кристаллов, их стекловидная прозрачность, многогранность краев и отсутствие неразрывной связи одного элемента с другим. В сомнительных случаях рекомендуется добавить к препарату капельки слегка подогретой дистиллированной воды, которые быстро растворяют кристаллы щелочи.
За элементы гриба ошибочно могут быть приняты:
Липиды кожных покровов, жировой распад клеток и зерна кератогиалина, особенно имеющие правильную форму, могут напоминать отдельные споры гриба. Но разнообразие формы и, главное, размеров, отсутствие внутренней структуры образований (вакуоли, оболочки) говорят против грибковой природы данных элементов. Липиды также могут попасть в препарат при взятии патологического материала с недостаточно очищенного очага поражения.
Пузырьки воздуха могут напоминать споры дрожжеподобных клеток, но в отличие от последних они окружены плотной темной оболочкой, и даже самые маленькие пузырьки воздуха всегда больше клеток гриба.
Нити от ткани носков, одежды и т. п. обычно лежат отдельно от патологического материала, они всегда больше гифов, грубее и не септированы.
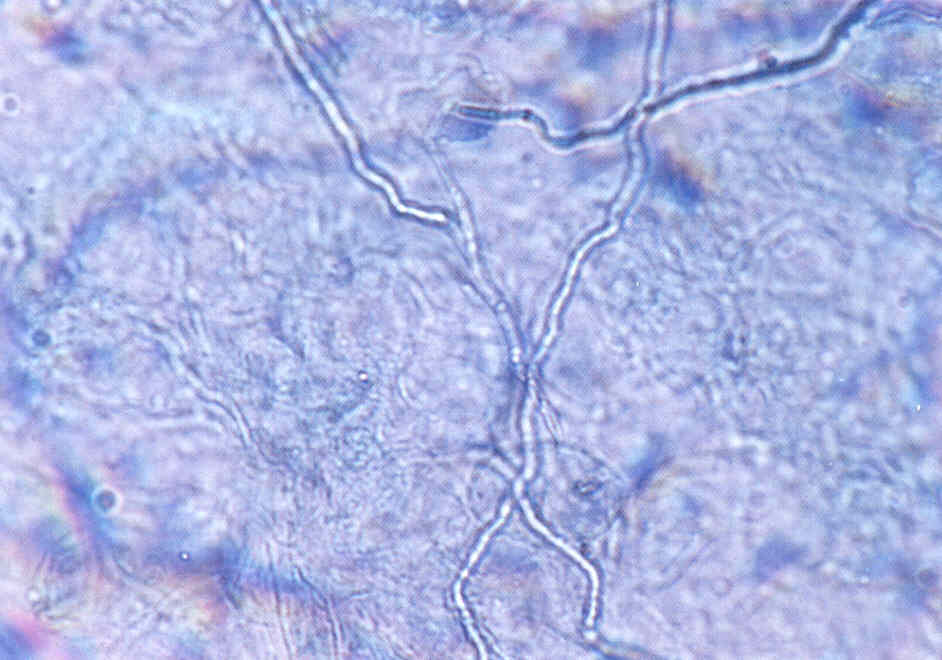
В некоторых лабораториях просветление препаратов для микроскопического исследования проводят 15 - 30% раствором КОН, в который добавляют 5 - 10% коммерческих темно-синих чернил фирмы Паркер (Parker's Superchrome Blue-Black Ink).
При этой окраске гифы и споры окрашиваются в голубой цвет.
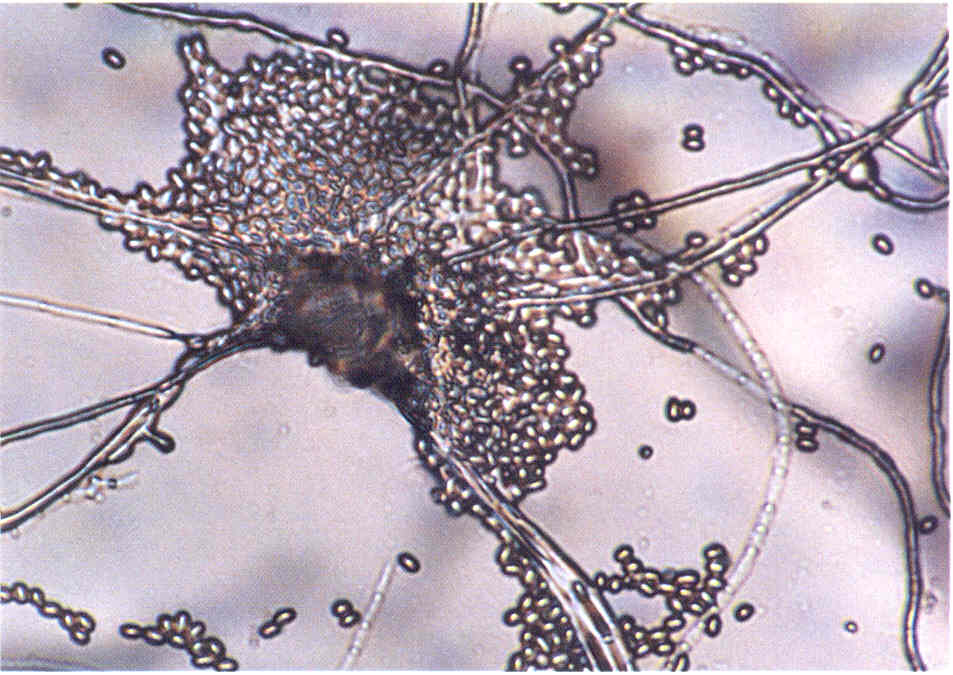
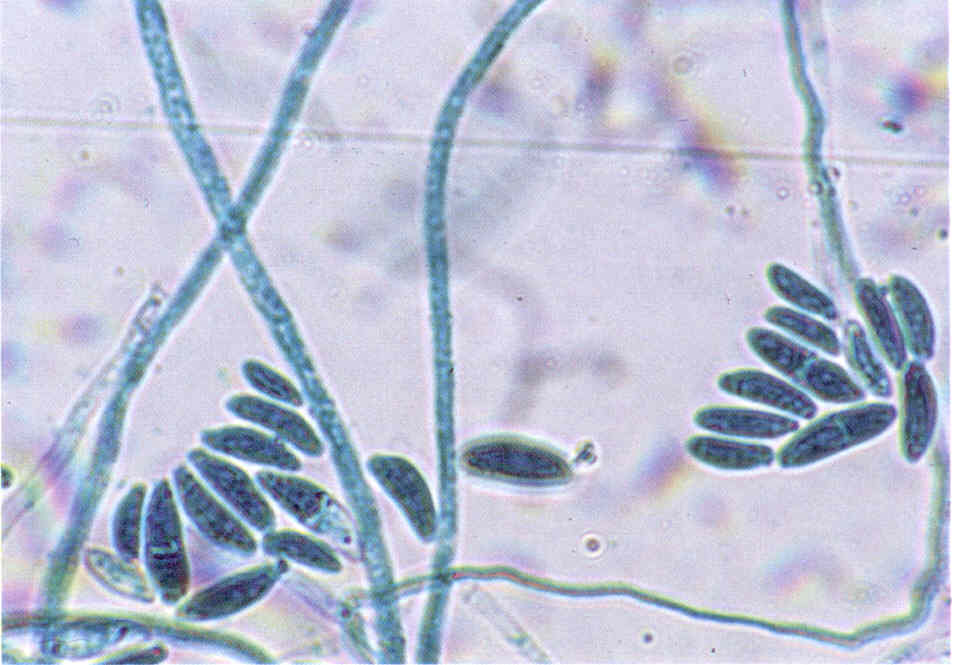
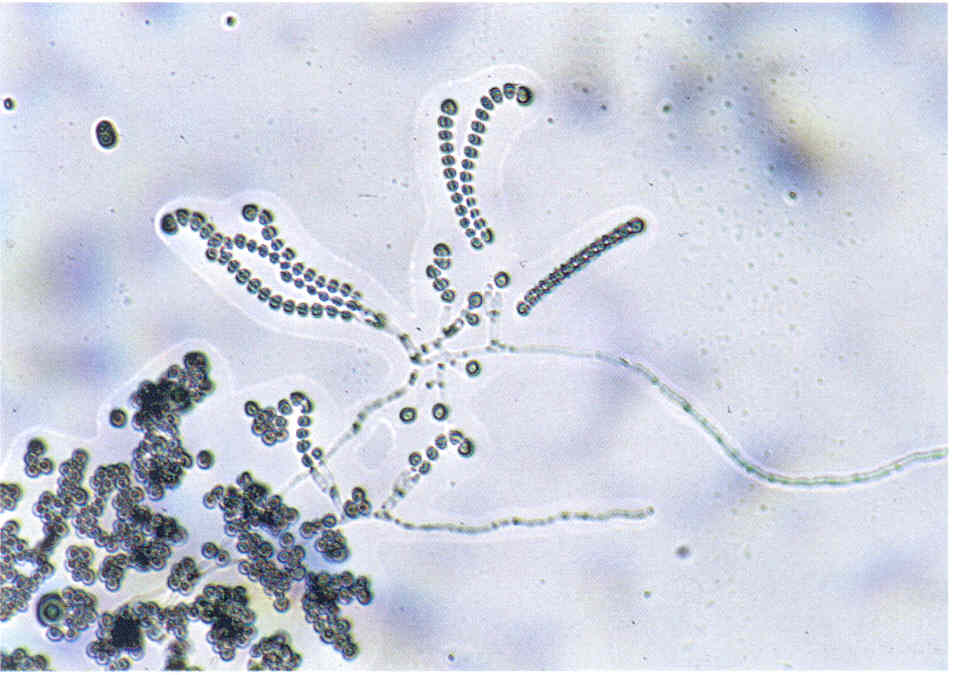
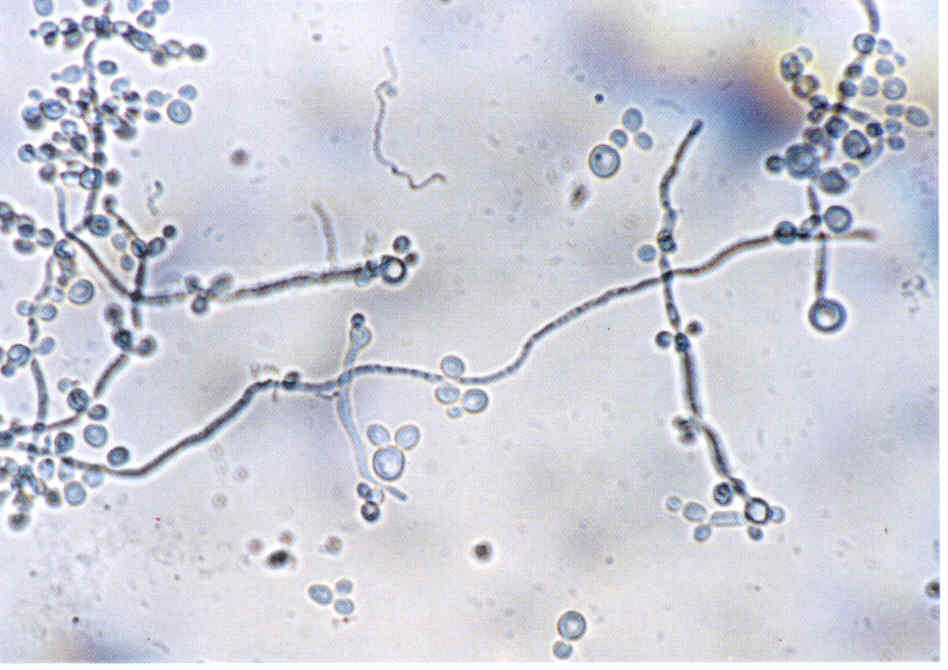
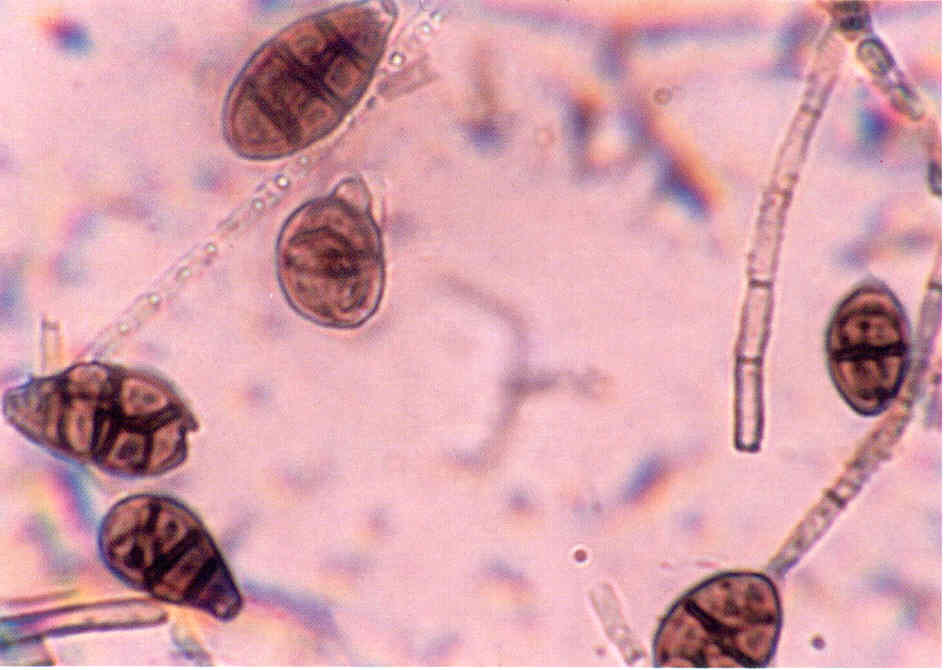
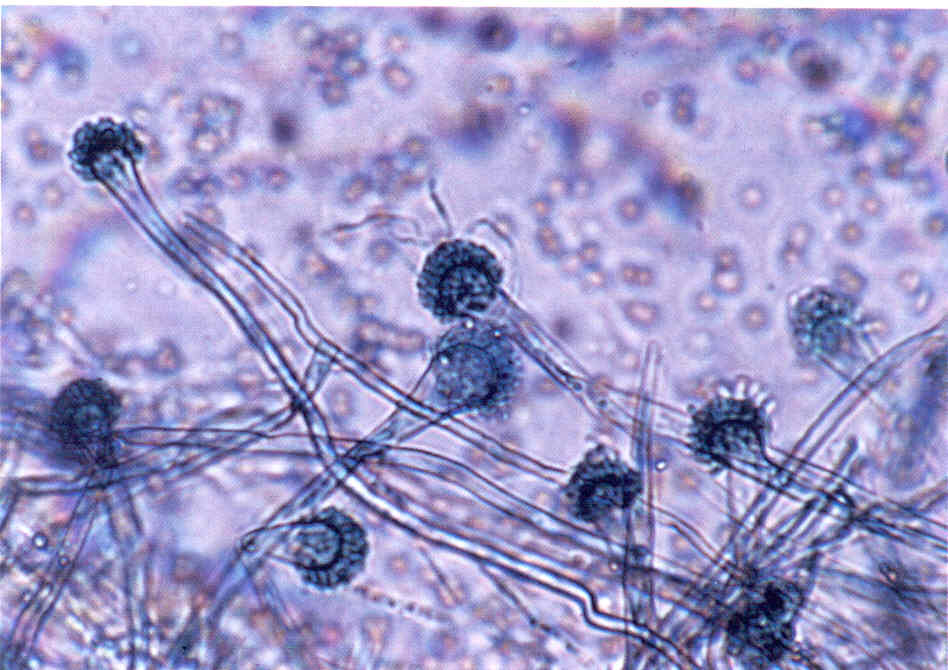
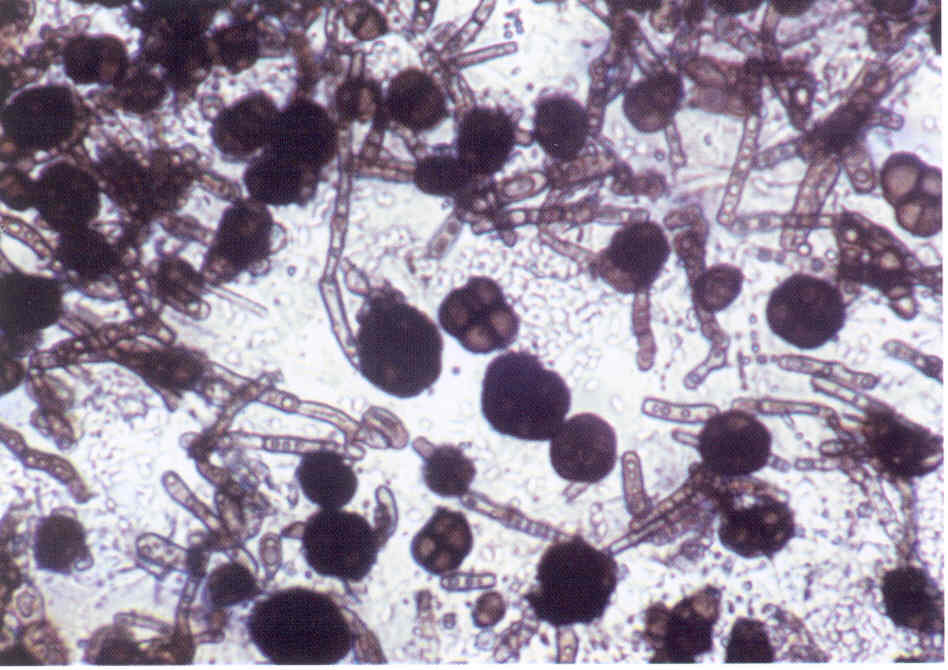
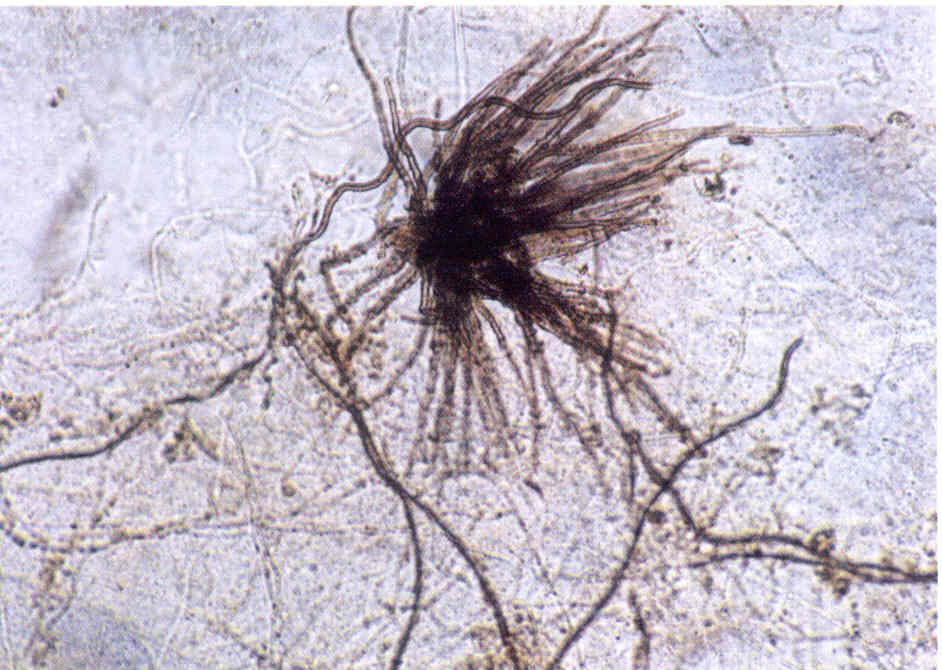
При микроскопии обнаруживают нитевидные гифы грибов или почкующиеся клетки (рис.1).
Таким образом, микроскопия дает заключение только о грибковой природе инфекции, но не о виде гриба-возбудителя.
Конечно, результативность микроскопического исследования зависит от квалификации сотрудника лаборатории.
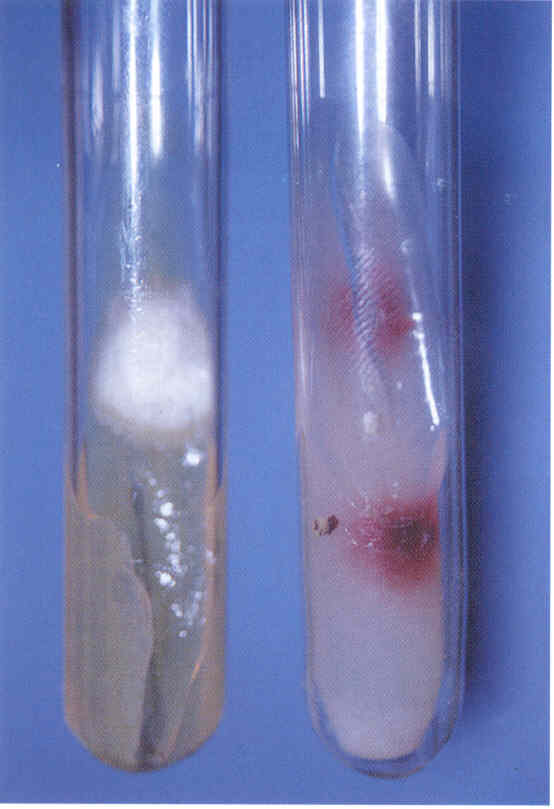
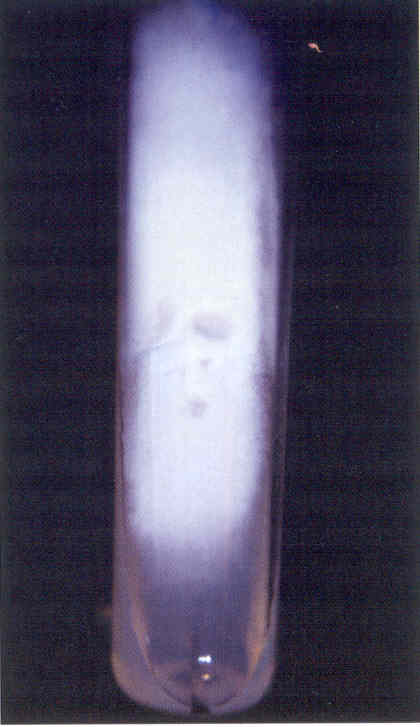
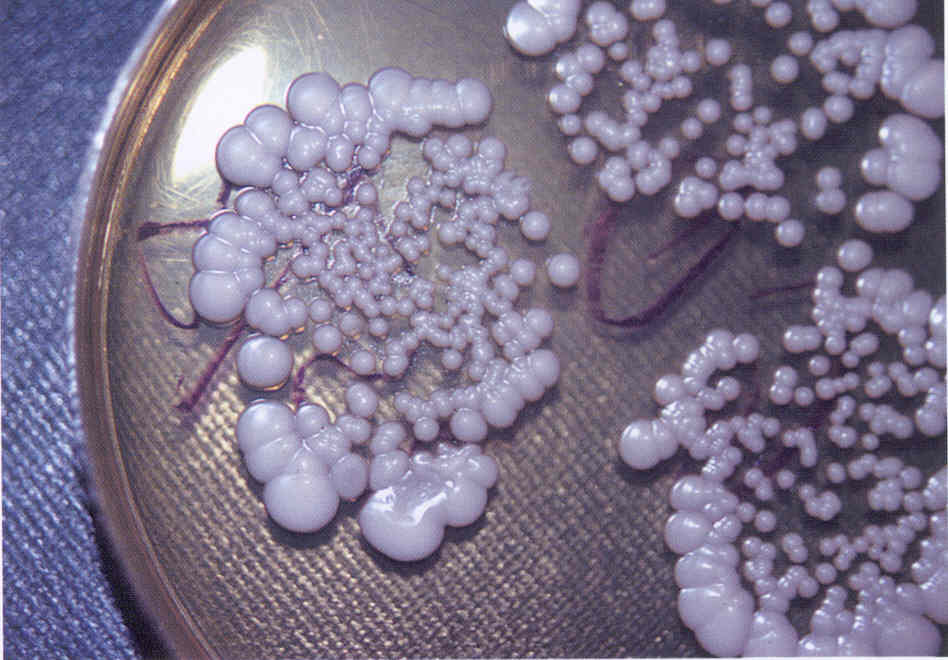


Следует учесть, что некоторые плесневые грибы, в том числе дерматофиты, в культуре вырастают медленно, за 2-3 нед.
Даже при соблюдении всех правил сбора материала, при хорошем оборудовании лаборатории и высокой квалификации ее персонала число положительных результатов культурального исследования очень невелико.
По данным зарубежной литературы, процент положительных исследований не превышает 50.
Процент положительных результатов в лучших отечественных лабораториях едва достигает 30.
Таким образом, в 2 из каждых 3 случаев онихомикоза его этиологию установить не удается.
ЛЮМИНЕСЦЕНТНОЕ ИССЛЕДОВАНИЕ
В 1925 г. Margaret и Deveze обнаружили, что волосы, пораженные некоторыми дерматофитами, дают характерное свечение в ультрафиолетовых лучах, пропущенных через фильтр Byда. Стекло Byда состоит из сульфата бария, содержит около 9% окиси никеля; оно пропускает лучи длиной 365 нм. В качестве источника ультрафиолетовых лучей можно использовать различные приборы. Природа свечения точно не установлена. Волос продолжает светиться после гибели гриба и после попыток экстрагировать флюоресцирующий материал горячей водой или холодным раствором бромида натрия. Интенсивность и характер свечения зависят от рН раствора. Полагают, что флюоресцирующая субстанция появляется в процессе взаимодействия гриба и растущего волоса.
Свечение в ультрафиолетовых лучах, пропущенных через фильтр Вуда, характерно только для волос, пораженных грибами рода Microsporum (M. canis, M. audouinii, M. ferrugineum, M. distortium, изредка M. gypseum и M. nanum), a также Trichophyton schonleinii. Волосы, пораженные микроспорумами, особенно M. canis и M. audouinii, дают наиболее яркое свечение; волосы, пораженные Т. schonleinii, имеют тусклую зеленоватую флюоресценцию.
Свечение наблюдается только в полностью пораженных грибом волосах. Его может не быть в свежих очагах поражения. В этих случаях следует эпилировать волосы из краевой, наиболее активной зоны, и свечение можно обнаружить в корневой части волос.
Люминесцентный метод можно использовать как для диагностики и контроля за эффективностью лечения у отдельных больных, так и в эпидемиологических очагах. Компактные передвижные установки удобны для обследования контактных людей в школах, детских садах и т. п.
Люминесцентное обследование необходимо производить в затемненной комнате, очаги поражения должны быть предварительно очищены от корок, остатков мази и т. п. Люминесцентный метод можно использовать для диагностики отрубевидного лишая, особенно при локализации очагов поражения на волосистой части головы. Очаги поражения при этом заболевании имеют красновато-желтое или бурое свечение. Это свечение, однако, не является строго специфичным, так как может наблюдаться при наличии перхоти на волосистой части головы и даже у здоровых людей в области устьев волосяных фолликулов на лице и верхней части туловища. Выявленные с помощью люминесцентного метода пораженные волосы должны обязательно подвергаться микроскопическому исследованию.
ИММУНОЛОГИЧЕСКОЕ И БИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЯ
Иммунологические методы исследования используют для выявления специфической перестройки организма и серологической диагностики грибковых заболеваний. Для обнаружения специфических антител в сыворотке пробы проводят следующие серологические реакции: агглютинации, преципитации, связывания комплемента, иммунофлюоресценции с соответствующими антигенами.
Аллергическое состояние организма больного выявляют с помощью аллергических кожных проб. Аллергены наносят на скарифицированную кожу по Пирке или втиранием в кожу по Моро, внутрикожно по Манту, а также уколом в кожу. С помощью этих проб выявляют аллергические реакции как немедленного, так и замедленного типа, что позволяет оценить состояние гуморального и клеточного иммунитета.
Для выявления специфической сенсибилизации лимфоцитов используют реакции дегрануляции базофилов, агломерации и альтерации, тест бластной трансформации, подавления миграции макрофагов и т. п.
Сопоставление результатов серологических и аллергических реакций оказывается полезным как для диагностики, так и для прогноза течения микозов.
Биологический метод. Используется для лабораторной диагностики глубоких и особо опасных микозов. Основан на заражении животных патологическим материалом от больного или культурой исследуемого гриба. Осуществляется в специальных лабораториях.
ГИСТОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ
Гистология микозов кожи, обусловленных дерматофитами
Патоморфологические изменения в очагах поражения обусловлены внедрением грибов в роговой слой эпидермиса, волосы и ногти и ответной воспалительной реакцией кожи, которая может быть острой, подострой или хронической. Диагноз можно считать установленным только в том случае, если в гистологических препаратах обнаруживают элементы грибов. Для этого используют различные гистологические окраски, наиболее информативной является периодическая кислотная реакция (PAS), позволяющая выявить полисахариды, имеющиеся в целлюлозе и хитине клеточной стенки большинства дерматофитов (окраска по Шифу и ее модификации). Можно также использовать реакции сульфатирования и импрегнацию гистологических срезов серебром [Хмельницкий О. К., 1973; Lewer W. F. и Schaumburg-Lewerl.,1983].
Грибы в роговом слое эпидермиса, даже при использовании специальных окрасок, выявляются в небольшом количестве в виде нитей мицелия и спор. В редких случаях, когда грибов в очагах поражения много, их можно обнаружить в срезах, окрашенных гемотоксилин-эозином, в виде нежных базофильных структур в роговом слое.
Воспалительные изменения в эпидермисе могут быть различными: от незначительного внутри- и внеклеточного отека шиповатых клеток до выраженного спонгиоза. Спонгиоз обычно развивается при дисгидротических вариантах микозов стоп и кистей, клинически в этих случаях отмечаются пузырьки. Причиной этой реакции обычно является Т. mentagrophytes var. interdigitale. Иногда в эпидермисе отмечается выраженный гиперкератоз, что чаще всего наблюдается при микозе, обусловленном Т. rubrum.
Гистологические изменения в дерме неспецифичны и соответствуют острому, подострому и хроническому воспалению.
При микозе гладкой кожи, вызванном Т. rubrum, грибы иногда выявляются в пушковых волосах и волосяных фолликулах. Вокруг фолликулов развивается воспалительная реакция, которая за счет попадания в дерму грибов может приобретать гранулематозный характер. Центральная часть инфильтрата в этих случаях может подвергаться нагноению и некрозу, а периферическая состоять из лимфоцитов, гистоцитов, эпителиоидных и многоядерных гигантских клеток, внутри которых иногда обнаруживаются споры гриба. Размеры спор здесь достигают 6 мкм в диаметре, в волосе обычно не превышают 2 мкм.
При инфильтративно-нагноительной форме микозов волосистой части головы и области роста бороды и усов элементы грибов обнаруживаются в волосяном фолликуле, внутри и вокруг волоса. В волосе они определяются чуть выше зоны начала кератинизации (примерно на уровне 30 мкм). В дерме отмечают воспалительную реакцию различной интенсивности, наиболее выраженную при kerion Celsii. При острой гнойной реакции в составе инфильтрата отмечают большое количество нейтрофильных лейкоцитов, элементы грибов в этом случае могут полностью исчезать. При хроническом течении процесса инфильтрат может приобретать гранулематозный характер, в нем появляются многоядерные гигантские клетки. Для подтверждения диагноза при отсутствии в инфильтрате грибов можно использовать иммунофлюоресцентные методы окраски. Для этих целей применяют меченную флюоресцином антисыворотку к Т. mentagrophytes, которая позволяет обнаружить антигены гриба в волосе и в перифолликулярном инфильтрате.
Формирование инфильтративно-нагноительной реакции кожи при микозе волосистой части головы (kerion Celsii) и области роста бороды и усов, обусловленных грибами М. саnis, Т. tonsurans и Т. verrucosum, представляет собой проявление иммунологической реакции. Об этом свидетельствуют:
1. Склонность очагов поражения к спонтанному разрешению.
2. Отсутствие элементов гриба при очень выраженной воспалительной реакции со стороны кожи при микозе, вызванном Т. verrucosum (faviforme) и Т. tonsurans.
3. Постоянная положительная реакция в ответ на внутрикожное введение трихофитина при инфильтративно-нагноительных формах микоза, вызванного зоофильными трихофитинами (например, Т. tonsurans), и отрицательная — при поверхностных микозах, обусловленных тем же Т. tonsurans.
При фавусе в роговом слое эпидермиса обнаруживается большое количество нитей мицелия и единичные споры гриба. Скутула представлена экссудатом, паракератотическими клетками эпидермиса, клетками воспалительного инфильтрата, а также нитями мицелия и спорами гриба, которые расположены преимущественно в периферической зоне скутулы. В активной стадии болезни в дерме вокруг дегенеративных волосяных фолликулов отмечается выраженный воспалительный инфильтрат, содержащий многоядерные гигантские и плазматические клетки. В старых очагах поражения волосы и сальные железы отсутствуют, имеются явления фиброза.
Гистология микозов кожи и слизистых оболочек, обусловленных дрожжеподобными грибами
При кандидозе кожи и слизистых оболочек грибы рода Candida обнаруживаются в роговом слое эпидермиса или в поверхностных слоях эпителия слизистой оболочки. Элементов гриба обычно мало, они хорошо окрашиваются PAS-peакцией или по Граму; представлены в виде нитей септированного ветвящегося мицелия, размером 2-4 мкм в диаметре, или овоидными спорами, размером 3 - 5мкм в диаметре. Диагностическое значение имеет обнаружение мицелиальной формы гриба.
При гистологическом исследовании хронического гранулематозного кандидоза кожи и слизистых оболочек элементы гриба также преимущественно обнаруживают в роговом слое эпидермиса или в самых верхних отделах эпителия слизистой оболочки, но иногда в шиповатом слое, внутри волоса и в дерме. Отмечается также выраженный гиперкератоз и папилломатоз; в дерме – густой воспалительный инфильтрат, состоящий из лимфоидных клеток, нейтрофилов, плазматических и многоядерных гигантских клеток. Инфильтрат может распространяться в подкожную жировую клетчатку.
При отрубевидном лишае в роговом слое эпидермиса обнаруживают большое количество элементов гриба в виде нежных базофильных структур, которые хорошо видны даже при окраске препаратов гемотоксилин-эозином. Грибы представлены как нитями, так и спорами.
При фолликулярной форме отрубевидного лишая отмечается скопление роговых масс и клеток воспалительного инфильтрата в расширенных устьях волосяных фолликулов. Вокруг фолликулов также отмечают воспалительный инфильтрат. При PAS-реакции сферические или овальные споры гриба, размером 2—4 мкм в диаметре, обнаруживают внутри устья волосяных фолликулов, а иногда в перифолликулярном инфильтрате. Мицелий никогда не выявляется.
Нарушение пигментации кожи у больных отрубевидным лишаем обусловлено способностью гриба Pityrosporum вырабатывать субстанцию, которая угнетает процесс пигментообразования в эпидермисе. Электронно-микроскопическое изучение биоптатов кожи с гипопигментированных участков показало, что в меланоцитах образуются очень маленькие меланосомы, которые не способны проникать в кератиноциты. В гиперпигментированных участках кожи, наоборот, меланосомы крупные и содержат большое количество меланина.
Микозы — инфекционные болезни, вызываемые некоторыми видами грибов, поражающих расплод и взрослых пчел.
Из большого количества видов грибов, встречаемых на поверхности тела, в кишечнике пчёл и в пчелином гнезде, только некоторые вызывают у них заболевания.
К грибковым заболеваниям относятся:
- • аскосфероз;
- • аспергиллез;
- • меланоз;
- • кандидамикоз;
- • мукормикоз;
- • актиномикоз;
- • альгозы.
Наибольший вред пчелам наносят следующие микозы. Аскосфероз (перицистисмикоз, известковый расплод, меловой расплод) поражает личинок трутней, рабочих пчел, а также маток (рис. 8.7).
Болезнь вызывается грибом Ascosphera apis, известным ранее как Pericystis apis. Оптимальная температура для роста гриба 22—30 °С, но он может выносить и 35—37 °С. Споры сохраняют жизнеспособность свыше 15 лет и устойчивы к воздействию сернистого ангидрида и паров формалина. Источником инфекции являются пораженные личинки, зараженные пчелы, мед, перга. Споры возбудителя от больных семей к здоровым могут переносить блуждающие пчелы, вредители пчел, а также пчеловоды при неаккуратном выполнении пасечных работ. Внутри улья болезнь распространяется пчелами-корми- лицами. Заражение спорами гриба может произойти до запечатывания личинки в любом возрасте. Споры с кормом попадают в их кишечник, где прорастают в тело. Мицелий выходит наружу, покрывая труп личинки белым налетом. Личинки погибают в стадии предкуколки. Болезнь может проявляться с апреля по октябрь, но чаще развивается в июне—августе. Семьи, зараженные спорами в сентябре, заболевают в мае следующего года. Болезнь может протекать самостоятельно или как вторичная инфекция при европейском гнильце, мешотчатом или застуженном расплоде. Развитию болезни способствуют повышенная влажность и недостаточное утепление пчелиного гнезда. Больные личинки перестают двигаться,

Рис. 8.7. Аскосфероз [12]:
Аскосфероз определяют по наличию обызвествленных личинок, покрытых серо-белым налетом мицелия, а также на основе лабораторного микологического исследования. Заболевание можно предупредить содержанием сильных, обеспеченных кормом семей, хорошим утеплением гнезд, расположением пасеки в сухом месте. При наличии болезни из гнезда удаляют соты с пораженным расплодом, семьи переводят в чистые продезинфицированные ульи, утепляют и подкармливают сахарным сиропом.
Аспергиллез (аспергилломикоз, каменный расплод) поражает личинок, куколок и взрослых пчел. Болезнь вызывается чаще видом Asperillus flavus, реже — Asperillus niger и некоторыми другими патогенными видами этого рода (рис. 8.8).
Гриб развивается при температуре 7—40 °С. Он образует сильный токсин. Устойчивость гриба к действию высокой температуры и дезсредствам невелика.
Кроме пчёл аспергилл патогенен для многих других видов насекомых, а также животных и человека. Аспергиллы широко распространены во внешней среде на мертвом субстрате, а также пыльниках и нектарниках цветков живых растений, с которых пчелы заносят споры в улей. Возникновение заболевания зависит от вирулентности штамма гриба, соответствующей температуры (25—45 °С) и влажности (95—100%) в ульях и внешней среде, а также от резистентности пчел. При благоприятных условиях гриб начинает расти на сотах, в пыльце, на мертвых пчелах, рамках, охлажденном или голодающем расплоде и на живых пчелах при слабом утеплении гнезд и недостатке корма. Заражаются личинки и пчелы через кишечник при

Рис. 8.8. Аспергиллез [12]:
А — возбудитель аспергиллеза — гриб Aspergillus flavus; Б — сот с пораженным
расплодом питании инфицированным медом или пергой, а также через наружный покров при контакте с инфекционным началом. Заражение личинок и пчёл может происходить в любом возрасте. Смерть наступает от интоксикации.
Заболевание отмечается главным образом весной при повышенной влажности. Свежепораженный расплод, в зависимости от вида аспергилла, покрывается белым, серым, желтовато-зеленым или черным налетом прорастающего гриба. В дальнейшем личинки и куколки высыхают и твердеют, превращаясь в окаменелые мумии, свободно лежащие в ячейках, и легко вываливаются. Взрослые пчелы при поражении слабеют, брюшко их, вначале плотное, затем твердеет; гриб прорастает через покровы и образует налет плесени на поверхности трупа. Аспергиллез определяют по внешним признакам пораженного расплода и взрослых пчёл на основе лабораторного микробиологического исследования. Меры борьбы те же, что и при аскосферозе.
Меланоз поражает рабочих пчел, трутней и особенно маток (рис. 8.9).

Рис. 8.9. Меланоз [12]:
А — возбудитель меланоза — гриб Melanosella mors apis; Б — задний конец тела пораженной матки с пробкой из подсохших испражнений; 1— проросшая хламидоспора; 2 — хламидоспоры; 3 — оидии; 4 — гифы
Возбудитель болезни — гриб Melanosella mors apis. Гриб заносится пчелами в улей с энтомофильных растений и, возможно, с собранной падью. Из рабочих пчёл в основном поражаются пчелы-сборщицы. Источником болезни служит пища. Матки заражаются при их кормлении. Заражение происходит через маточное молочко от пораженных пчел, у которых паразит развивается в глоточных железах. Из пищеварительного тракта возбудитель проникает в гемолимфу, где постоянно присутствует в большом количестве и, оседая у пчёл в различных железах, мальпигиевых сосудах и других органах, а у маток и в половом аппарате, образует некротические очаги с черным пигментом. Обычно болезнь развивается во вторую половину лета. Ее развитию способствует принос пчелами большого количества пади. Чаще болезнь протекает в скрытой форме, и гибель пчёл может остаться незамеченной, а смерть маток при отсутствии характерных внешних признаков болезни относят за счет других причин. Характерным внешним признаком болезни у маток является образование из подсохших испражнений каловой пробки, выступающей из анального отверстия. Однако гибель матки может наступить и до образования пробки. В таких случаях меланоз можно определить по другим признакам: прекращению кладки яиц, слабости, неподвижности маток, увеличению их объема и опущению брюшка. Пораженных маток пчелы выбрасывают из улья. Так как в семье нет молодого расплода, пчелы не могут вывести новую матку, и семья трутневеет. При подозрении на меланоз диагноз ставят по выявлению возбудителя, а также с помощью гистологического исследования больных маток (при наличии некротических очагов и пигментации в пораженных органах). Меры борьбы сводятся к хорошему содержанию пчёл и замене падевого меда на цветочный или сахарный сироп, а также к своевременной замене больных маток на здоровых.
Согласно инструкции СП 1.2.036-95 Госкомэпиднадзора РФ, Москва, 1996 г. "Порядок учета, хранения, передачи и транспортирования микроорганизмов I-IV групп патогенности” по эпидемиологической опасности дрожжевые и плесневые грибы, а также дерматофиты относятся к III-IV группам возбудителей инфекционных болезней, поэтому при работе с ними необходимо соблюдать особые правила техники безопасности, производственной санитарии, противоэпидемического режима и личной гигиены, направленные на обеспечение личной и общественной профилактики заражения, аллергизации и распространения инфекции.
Лаборатория для работы с микроорганизмами III-IV групп патогенности укомплектовывается легко дезинфицирующейся мебелью, включая шкафы для чистой лабораторной посуды, реактивов, питательных сред, соответствующим оборудованием и инструментами. Для работы необходимы спиртовки или газовые горелки, микробиологические петли, микологические лопаточки, шпатели, эпиляционные и анатомические пинцеты, кусачки маникюрные, скальпели, ножницы, ложечки Фолькмана, пипетки, пастеровские пипетки, иглы препаровальные, стеклянные палочки, шприцы, низкоскоростная центрифуга, аппарат для встряхивания, чашки Петри, пробирки, стеклянная посуда, ультрафиолетовая лампа Вуда с фильтром, микроскопы, осветители, термостаты, автоклавы, холодильники, сухожаровые шкафы, бактерицидные лампы.
Микроскопическая диагностика микозов подразумевает обнаружение мицелия и спор в исследуемом биоматериале. В качестве исследуемого биоматериала рассматриваются чешуйки эпидермиса, волосы и ногти. Непременным требованием перед проведением исследования является отсутствие местного лечения в течение, как минимум, десяти дней и системного лечения – в течение месяца. Следует иметь в виду, что использование пациентом моющих средств (особенно содержащих антисептики) способно повлиять на достоверность результатов исследования, поэтому за 3-4 дня до его проведения запрещают мытьё.
Инструментарий для взятия биоматериала и приготовления препарата представлен на рисунке:

При подозрении на микоз гладкой кожи, микоз кистей и стоп без поражения ногтевых пластинок исследуются чешуйки эпидермиса с поверхности очага поражения. При микозе гладкой кожи является предпочтительным исследование эпидермиса с краевой зоны очага поражения, так как в центральной зоне патологический процесс нередко разрешается. При этом не следует забывать о возможности поражения пушковых волос, что определяет выбор дальнейшей тактики лечения. Волосы извлекают эпиляционным пинцетом. При микозе кистей и стоп без поражения ногтевых пластинок исследуются чешуйки эпидермиса из третьей и четвертой межпальцевых складок, а также с ладоней и со свода стоп.
При подозрении на грибковое поражение длинных волос (волосистой части головы, бороды, усов и лобка), а также пушковых волос выполняется их микроскопическое исследование. При трихофитии волосистой части головы волосы обламываются на расстоянии 1-2 мм над уровнем устья волосяного фолликула, напоминая при этом пеньки и точки. Если волос не удаётся захватить эпиляционным пинцетом, то в этом случае его стараются извлечь острым концом скальпеля или препаровальной иглой.
При фавусе исследуют истончённые волосы над поверхностью скутулы.
При подозрении на онихомикоз исследуется легко измельчающийся материал из зоны подногтевого гиперкератоза, а также сами измененные ногтевые пластинки.
Необходимо понимать, что любой исследуемый материал от пациента потенциально заразен, поэтому его взятие необходимо осуществлять в помещении, где осуществляется ежедневная влажная уборка с применением дезинфицирующих средств (5% раствор хлорамина, 5% осветленная хлорная известь), а воздух стерилизуется ультрафиолетовыми облучателями (их включают на 1-1,5 ч и входят в помещение через 20 мин после выключения). Термостаты еженедельно протирают 0,5% раствором хлорамина, стены обрабатывают дезсредствами 1 раз в месяц. Врач при работе должен быть защищён маской, защитными очками, халатом и перчатками. Инструментарий для взятия биоматериала, перчатки, предметные и покровные стёкла, одноразовые пелерины и салфетки обеззараживают после использования, погружая в 1,5% раствор клиндезина-экстра (5% раствор фенола или 5% раствор лизола) на 30 минут. Оставшийся патологический материал (волосы, кожные и ногтевые чешуйки) автоклавируют при 2 атм. и 132˚ С в течение 20 мин (контроль - мочевина) или при 1,5 атм. и 126˚ С в течение 30 мин (контроль - бензойная кислота), либо кипятят 1 час в воде или 30 мин в 1% мыльно-содовом растворе.
Патологический материал транспортируют в лабораторию в специальной таре или металлических биксах, защищая его от прямых солнечных лучей. В сопроводительном документе указывают фамилию, имя, отчество, пол, возраст и адрес больного, предполагаемый клинический диагноз, наименование исследуемого материала, время его взятия, локализацию очага, номер истории болезни, фамилию врача и учреждение, направляющее материал.
После получения чешуек эпидермиса с очага поражения производится приготовление препарата для микроскопического исследования. На исследуемый материал, помещенный на предметное стекло, наносят 1-2 капли 20% КОН, после чего предметное стекло подогревают над пламенем горелки до появления белесоватого ободка кристаллизованной щелочи по периферии. Затем препарат накрывают покровным стеклом (которое придавливают препаровальной иглой) и микроскопируют. Исследование необходимо проводить не позднее 2-х часов после приготовления препарата из-за возможности кристаллизации щёлочи.
Способ приготовления препарата волоса при подозрении на его грибковое поражение соответствует ранее описанному, с той лишь разницей, что покровное стекло не придавливается препаровальной иглой (во избежание раздавливания волоса).

Для приготовления препарата кусочки срезанных ногтевых пластинок опускают в пробирку с 20% КОН и экспонируют в термостате в течение 1 часа (t≈37˚C), а затем получившуюся желеобразную массу переносят на предметное стекло, накрывают покровным и исследуют под микроскопом.
В отличие от ногтевых пластинок образцы из легко измельчающегося материала зоны подногтевого гиперкератоза помещают на предметное стекло, на них наносят 1-2 капли 20% КОН, после чего предметное стекло подогревают над пламенем горелки до появления белесоватого ободка кристаллизованной щелочи по периферии (рис.65). Затем препарат накрывают покровным стеклом, которое осторожно придавливают препаровальной иглой, и исследуют под микроскопом.
Препараты необходимо просмотреть не позднее 2 часов с момента их приготовления из-за возможности кристаллизации щелочи. Для повышения надежности диагностики следует сделать несколько препаратов (не менее двух) из одного очага поражения. Возможные ошибки при микроскопической диагностике микозов могут быть связаны как с некачественным приготовлением препаратов (перегревом над пламенем горелки, что сопровождается преждевременной кристаллизацией щелочи), а также с недостаточным опытом исследователя (когда за нити мицелия нередко принимают волокна ткани, случайно оказавшейся в препарате).
Читайте также:


