Антидотная терапия при профессиональных интоксикациях
Детоксикация. Для лечения отравлений необходимы прекращение воздействия токсичных веществ и удаление их из организма, т.е. детоксикация.
- естественная детоксикация
- искусственная детоксикация
- антидотная детоксикация.
Естественная детоксикация – усиление физиологических процессов выведения яда из организма. Для этого используют очищение желудочно-кишечного тракта, форсированный диурез, регуляцию активности ферментов, создание гипер- и гипотермии. Соответственно применяют рвотные и слабительные средства, осмотические диуретики, препараты, обеспечивающие водно-электролитный гомеостаз.
Следует отметить, что стимуляция естественных механизмов детоксикации возможна только при условии сохранения функции элиминирующих систем организма.
Форсированный диурез – наиболее распространенный метод консервативного лечения отравлений, когда токсичные вещества выводятся преимущественно почками. Форсированный диурез был впервые использован в терапии острых отравлений барбитуратами внутривенное введение большого количества изотонического раствора хлорида натрия и ртутных диуретиков.
При применении форсированного диуреза для восстановления кислотно-основного состояния и эффективного выведения барбитуратов из организма целесообразно парентеральное введение раствора гидрокарбоната натрия (NaHCО3).
Метод форсированного диуреза остается достаточно универсальным способом быстрого удаления из организма не только барбитуратов, но и морфина, фосфорорганических инсектицидов, хинина и пилокарпина, дихлорэтана, солей тяжелых металлов и других токсикантов, которые элиминируются почками.
Для очищения желудочно-кишечного тракта применяют простое или зондовое промывание желудка. Для промывания кишечника используют зондовый лаваж, клизмы, солевые, масляные, растительные слабительные средства. В некоторых случаях проводят электростимуляцию кишечника.
При отравлении токсичными газами, например угарным газом, показана лечебная гипервентиляция легких.
Усиления естественной детоксикации можно достигнуть также регуляцией ферментативной активности.
Искусственная детоксикация организма основана на разведении, диализе и сорбции, это разведение и замещение крови (лимфы), например гемоферез (замещение крови), плазмоферез (замещение плазмы) с использованием различных крове- и плазмозаменителей.
Методики плазмофереза включают:
- извлечение плазмы крови
- ее замещение плазмозамещаюшими растворами (сухой плазмы, альбумина) или возвращение плазмы в организм больного после ее очищения (диализ, фильтрация, сорбция).
Диализные и фильтрационные методы включают:
- гемодиализ
- плазмодиализ
- лимфодиализ
- перитонеальный и кишечный диализ
- ультрафильтрацию
- гемофильтрацию.
Диализ (разделение) – процесс удаления низкомолекулярных веществ, основанный на способности полупроницаемых мембран пропускать низкомолекулярные вещества и ионы, соответствующие по размеру их порам (до 50 нм), и задерживать коллоидные частицы и молекулы высокомолекулярных соединений.
Современные диализаторы снабжены высокопроницаемой полисульфоновой мембраной, и их можно использовать для ультрафильтрации.
Среди многих методов внепочечного очищения организма перитонеальный диализ считается наиболее простым и общедоступным. Однако опасность развития перитонита долго препятствовала широкому распространению этого метода. Благодаря применению антибиотиков перитонеальный диализ стал одним из основных хирургических методов искусственного очищения организма при ряде острых экзогенных отравлений.
Для искусственной детоксикации используют сорбционные методы
Сорбция (поглощение) – процесс поглощения молекул токсиканта поверхностью твердого тела или жидкости. В отличие от диализа и фильтрации, позволяющих выводить из организма низкомолекулярные токсичные вещества, при гемосорбции возможно выведение более крупных молекул.
Факторы, влияющие на выбор метода детоксикации:
- физико-химические свойства токсичного вещества
- природа токсичного вещества
- доза токсичного вещества
- экспозиция яда
- тяжесть отравления.
Антидотная терапия занимает особое место при детоксикации.
Антидотная терапия эффективна только в раннем токсикогенном периоде острых отравлений. Антидот – лекарственное средство, обезвреживающее яд путем химического или физико-химического взаимодействия с ним или уменьшающее вызванные им нарушения в организме.
Антидот (по ВОЗ) – препарат, способный ослаблять или усиливать специфические эффекты ксенобиотика в результате его иммобилизации и уменьшения концентрации за счет химического взаимодействия – окисления, восстановления, осаждения, хелатообразования, изменения метаболизма, адсорбции или противодействия на уровне рецептора (фармакологические антагонисты).
Антидотная терапия высокоспецифична и используется только при достоверно установленном клинико-лабораторном диагнозе. При ошибочном введении антидота, особенно в большой дозе, возможно токсическое воздействие на организм самого антидота. Антидотная терапия нецелесообразна в соматогенном периоде острых отравлений, когда элиминация яда практически завершена.
Методы детоксикации при подострых и хронических отравлениях имеют свои особенности. В этих случаях выведение токсичных веществ затруднено, так как возможно депонирование токсиканта (Тох) в организме, сопровождающееся его прочным связыванием с клеточными рецепторами (R):
Гемодиализ и гемосорбция зачастую оказываются малоэффективными. При лечении хронических отравлений следует применять лекарственные средства, воздействующие не только на сам ксенобиотик, но и на продукты его метаболизма.
Детоксикация антидотными средствами позволяет непосредственно воздействовать на токсичное вещество или его рецепторы. Специфические антидоты существуют для небольшого числа ксенобиотиков (не более 5%), а механизмы их действия разнообразны, поэтому любая систематизация противоядий условна.
Эффективность иммунохимических антидотов зависит от:
- клинического состояния больного
- токсикокинетических факторов
- токсикодинамических (поглощенной дозы, типа экспозиции яда, периода его полувыведения, механизмов связывания яда с клеточными рецепторами, химической природы метаболитов токсиканта).
Если период полувыведения антидота меньше, чем токсиканта, то проводят повторные курсы антидотной терапии. Иногда необходимо длительное применение антидота повторными курсами.
Выделяют противоядия в клинической токсикологии:
- химические противоядия контактного действия
- биохимические (токсикокинетические) противоядия
- фармакологические (симптоматические) антагонисты
- иммунохимические противоядия.
Химические противоядия контактного действия включают в себя специфические и неспецифические антидоты. В основе действия неспецифических антидотов лежит физико-химический процесс – адсорбция. Например, неспецифическими антидотами являются активированный уголь, специальные смолы, лигнин.
Биохимические (токсикокинетические) противоядия способны изменять механизмы метаболических процессов с участием токсичных веществ. Например, при отравлении метгемоглобинобразователями, в том числе цианидами, применяют метиленовый синий – тетраметилтионина хлорид, который в крови способен окислять железо (II) гемоглобина, т. е. превращать его в метгемоглобин.
Попавшие в кровь цианиды образуют более прочные связи с метгемоглобином, покидая менее прочные центры связывания – геминовые структуры тканей. Происходит восстановление функции цитохромоксидаз тканей. Комплекс MetHb•CN- постепенно отщепляет цианид в печени и метаболизируется до безопасных продуктов. Связывание цианида можно усилить введением специфического химического антидота – натрия тиосульфата:
Этанол при отравлениях метанолом или двухатомными спиртами конкурентно быстро взаимодействует с алкогольдегидрогеназой и препятствует участию этого фермента в образовании токсичных метаболитов метанола (муравьиной кислоты и формальдегида) и этиленгликоля (гликолевой, глиоксиловой и щавелевой кислот).
К группе биохимических антидотов следует отнести также цинка сульфат, используемый при отравлении соединениями меди (II), в частности при генетическом нарушении контроля содержания меди в организме – болезни Вильсона-Коновалова. Введение ионов цинка катализирует синтез металлотионеинов, а образующиеся при этом прочные тиолаты меди выводятся из организма.
Фармакологические (симптоматические) антагонисты – вещества, конкурирующие с ядом в действии на клеточные рецепторы. Это реактиваторы холинэстеразы при отравлениях фосфорорганическими пестицидами, атропин как антидот при отравлении пилокарпином, налорфин при отравлении морфином, ионы калия при отравлении сердечными гликозидами.
Среди фармакологических антагонистов имеется группа лекарственных средств, относящихся к синаптотропным препаратам. Например, флумазенил применяют при отравлении бензодиазепинами.
Фармакологические антидоты позволяют купировать большинство не все симптомы интоксикации, так как антагонизм обычно бывает полным. При этом могут развиваться побочные эффекты, поскольку конкурентное действие предполагает использование высоких концентраций антидота-антагониста.
В отличие от химических антидотов, биохимические (токсикокинетические) антидоты не образуют прочных ковалентных химических связей с токсичным веществом.
Большую группу составляют антидоты, используемые для профилактики и коррекции токсических эффектов ряда лекарственных средств. Амифостин используют для коррекции токсичности препаратов платины, ацетилцистеин – токсичности парацетамола, кальция фолиат – токсичности метотрексата.
Иммунологические противоядия применяют для лечения отравлений животными ядами, вызванных укусами змей и насекомых (противозмеинная, противокаракуртовая сыворотки и др.). Антитоксическая иммунотерапия эффективна лишь в первые часы после отравления.
К ним относятся соединения, обезвреживающие яд при различных химических реакциях: кислотно-основных, окислительно-восстановительных, комплексообразования, осаждения.
Приведенные примеры не могут охватить широкий круг медикаментов для детоксикации. Более полную информацию можно получить в учебниках по клинической токсикологии и в соответствующей справочной литературе.
Таким образом, при острых отравлениях необходимы методы активной детоксикации, специфической (антидотной) фармакотерапии (методы пассивной детоксикации) и симптоматической терапии с учетом избирательной токсичности вещества.
Антидоты (противоядия) - применяемые при лечении отравлений лекарства, в основе механизма действия которых лежит обезвреживание яда или предупреждение и устранение вызываемого им токсического эффекта.
Действие антидотов может заключаться:
1) в связывании яда (путем химических и физико-химических реакций);
2) в вытеснении яда из его соединений с субстратом;
3) в возмещении биологически активных веществ, разрушенных под влиянием яда;
4) в функциональном антагонизме, противодействии токсическому эффекту яда.
Антидотная терапия широко применяется в комплексе лечебных мероприятий при профессиональных отравлениях. Так, для предупреждения всасывания яда и его удаления из желудочно-кишечного тракта используются антидоты физико-химического действия, например активированный уголь, адсорбирующий па своей поверхности некоторые яды (никотин, таллий и др.). Другие антидоты оказывают обезвреживающее действие, вступая с ядом в химическую реакцию, путем нейтрализации, осаждения, окисления, восстановления или связывания яда. Так, метод нейтрализации используется при отравлениях кислотами (вводят, например, раствор окиси магния - жженой магнезии) и щелочами (назначают слабый раствор уксусной кислоты).
Для осаждения некоторых металлов (при отравлениях ртутью, сулемой, мышьяком) применяют белковую воду, яичный белок, молоко, переводящие растворы соли в нерастворимые альбуминаты, или специальное противоядие против металлов (Antidotum metallorum), в состав которого входит стабилизированный сероводород, образующий практически нерастворимые сульфиды металлов.
Примером противоядия, действующего путем окисления, может служить калия перманганат, активный при отравлениях фенолом.
Принцип химического связывания яда лежит в основе антидотного действия глюкозы и тиосульфата натрия при отравлении цианидами (происходит превращение синильной кислоты соответственно в циангидрины или в роданиды).
При отравлении тяжелыми металлами для связывания уже всосавшегося яда широко используются комплексообразующие вещества, например унитиол, тетацин-кальций, пентацин, тетоксации, образующие с ионами многих металлов стойкие нетоксичные комплексные соединения, выводимые с мочой.
С лечебной целью тетацин и пентацин применяются при профессиональных интоксикациях свинцом. Комплексонотерапия (тетацин, тетоксацин) способствует также выведению из организма некоторых радиоактивных элементов и радиоактивных изотопов тяжелых металлов, например иттрия, церия.
Введение комплексонов рекомендуется и в диагностических целях, например в том случае, когда имеется подозрение на свинцовую интоксикацию, но концентрация свинца в крови и моче не увеличена. Резкое усиление выведения свинца с мочой после внутривенной инъекции комплексона указывает на наличие яда в организме.
На принципе комплексообразования основан антидотный эффект дитиолов при отравлениях некоторыми органическими и неорганическими соединениями тяжелых металлов и другими веществами (иприт и его азотистые аналоги, йодацетат и др.), относящимися к группе так называемых тиоловых ядов. Из числа изученных в настоящее время дитиолов наибольшее практическое применение нашли унитиол и сукцимер. Эти средства являются эффективными антидотами мышьяка, ртути, кадмия, никеля, сурьмы, хрома. В результате взаимодействия дитиолов с солями тяжелых металлов образуются прочные водорастворимые циклические комплексы, легко выводимые почками.
Антидотом при отравлении мышьяковистым водородом служит мекаптид. В последнее время показан высокий антидотный эффект комплексообразователя а-пеницилламина при отравлении соединениями свинца, ртути, мышьяка и некоторыми тяжелыми металлами. Тетацинкальций включают в состав мазей и паст, применяемых для защиты кожных покровов рабочих, имеющих контакт с хромом, никелем, кобальтом.
С целью уменьшения всасывания из желудочно-кишечного тракта свинца, марганца и некоторых других металлов, которые попадают в кишечник с заглатываемой пылью, а также в результате выведения с желчью, эффективно использование пектина.
Для профилактики и лечения отравлений сероуглеродом рекомендуется глутаминовая кислота, вступающая в реакцию с ядом и усиливающая его выведение с мочой. В качестве антидотного лечения рассматривается применение средств, которые тормозят превращение яда в высокотоксичные метаболиты.
Примером противоядия, действие которого сводится к вытеснению яда из его соединения с биологическим субстратом, может быть кислород при отравлениях окисью углерода. При повышении концентрации кислорода в крови окись углерода вытесняется. При отравлениях нитритами, нитробензолом, анилином. прибегают к воздействию на биологические процессы, участвующие в восстановлении метгемоглобина в гемоглобин. Ускоряют процесс деметгемоглобинизации метиленовый синий, цистамин, никотиновая кислота, липамид. Эффективными антидотами при отравлении фосфорорганическими пестицидами является группа средств, способных реактивировать блокированную ядом холинэстеразу (например, 2-ПАМ, токсогонин, дипироксима бромид).
Роль антидотов могут играть некоторые витамины и микроэлементы, вступающие во взаимодействие с каталитическим центром ферментов, ингибированных ядом, и восстанавливающие их активность.
Противоядием может служить средство, которое не вытесняет яд из его соединения с субстратом, а путем взаимодействия с каким-либо иным биологическим субстратом делает последний способным связывать яд, экранируя другие жизненно важные биологические системы. Так, при отравлении цианидами применяются метгемоглобинобразующие вещества. При этом метгемоглобин, связываясь с цианом, образует цианметгемоглобин и тем самым предохраняет от инактивации ядом железосодержащие тканевые ферменты.
На принципе функционального антагонизма основано применение аналептиков - при отравлении наркотическими веществами и, наоборот, наркотических веществ при отравлении ядами, вызывающими судороги. При отравлениях ядами, вызывающими угнетение холинэстеразы (многие фосфорорганические соединения и др.), широко используются холинолитические препараты, которые являются функциональными антагонистами ацетилхолина, например атропин, тропацин, пептафен.
Не нашли то, что искали? Воспользуйтесь поиском:
К активным методам экстренной детоксикации организма при острых отравлениях принадлежит специфическая антидотная терапия. Цель ее — связывание яда, циркулирующего в организме, соответствующими веществами (антидотами). Кроме того, с целью значительного ограничения действия яда на соответствующие рецепторы используют лекарственные средства, которые проявляют антагонистическое, т.е. конкурентное для токсического агента, воздействие на эти рецепторы (фармакологические антагонисты). Антидоты при отравлениях и фармакологические антагонисты применяют только тогда, когда точно установлено, какое именно вещество вызвало острое отравление.
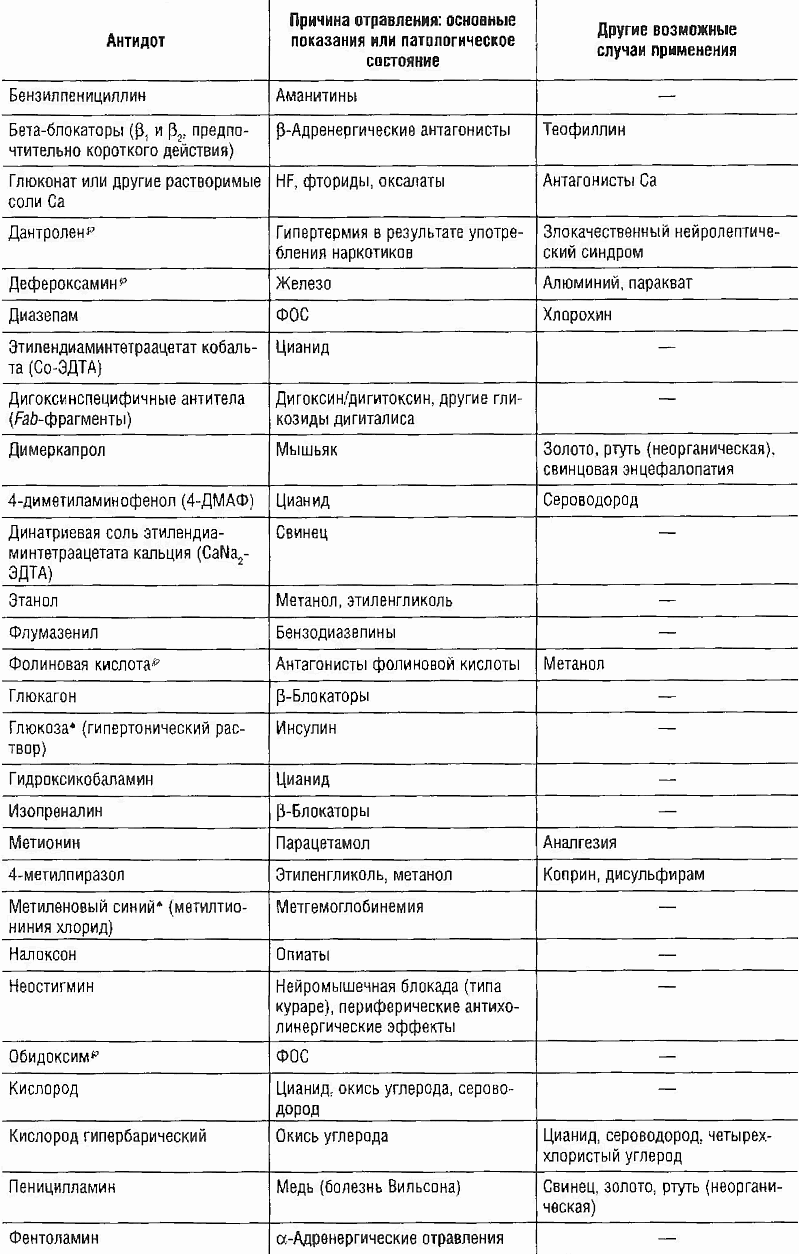
Существующее мнение о наличии противоядий для любого токсичного вещества не подтверждается действительностью. Относительно селективные эффективные антидоты существуют лишь для немногих классов токсичных веществ. Основные антидоты и антагонисты представлены в таблице.
Основные антидоты при отравлениях
Основные антидоты и фармакологические антагонисты, применяемые при острых отравлениях химическими агентами — таблица
| Антидот, фармакологический антагонист | Наименование токсического агента | Дозы и способы использования антидотов и фармакологических антагонистов |
| 1 | 2 | 3 |
| Тримефацин | Уран, бериллий | Внутривенно или ингаляционно в виде 5% раствора или 2,5% раствора в растворе кальция хлорида |
| Фероцин | Радиоизотопы цезия и рубидия, а также продукты деления урана | Внутрь по 1 г в виде водной суспензии (в 1/2 стакана воды) 2-3 раза в течение 10 дней |
| Унитиол | Соединения мышьяка, соли ртути, висмута и других тяжелых металлов, сердечные гликозиды, анаприлин, амитриптилин т.д. | Подкожно, внутримышечно или внутривенно по 5-10 мл 5% раствора (по 1 мл на 10 кг массы тела): в 1-й день — через каждые 6-8 ч, на 2-й день — через 8-12 ч , в последующие дни — по 1-2 инъекции в сутки в течение 6-7 дней и более |
| Цитохром С | Снотворные препараты, оксид углерода | Внутривенно капельно 20-40 мл 0,25% раствора в 250-500 мл изотонического раствора натрия хлорида или глюкозы (после биологической пробы — 0,1 мл 0,25% раствора внутрикожно) |

Наиболее эффективными антидотами при отравлениях металлами следует считать комплексоны (хелатные соединения). Из-за наличия в их структуре таких функциональных групп, как ОН,-SH и -NH, они могут отдавать электроны для связи с катионами металлов, т.е. образовывать координационно-ковалентные связи. В таком виде токсичные соединения выводятся из организма.
Эффективность хелатного соединения в значительной мере определяется количеством лиганд в его основе, способных связываться с металлом. Чем их больше, тем более стабильный и менее токсичен метало хелатный комплекс. Следует помнить, что комплексоны как антидоты имеют невысокую избирательность действия. Наряду с токсичными агентами они могут связывать необходимые для организма эндогенные ионы, например кальция и цинка.
Конечный результат такого взаимодействия определяется аффинитетом токсичных экзогенных и эссенциальных (эндогенных) металлов в хелатных соединений. Для того чтобы наступило значительное снижение уровня эндогенных металлов, их родство с комплексонами должен превышать аффинитет к эндогенным лиганд. В свою очередь, относительная скорость обмена металла между эндогенными лигандами и хелатных соединений должна превышать скорость элиминации комплексонов в комплексе с металлами. Если комплексоны выводится быстрее, чем комплекс металоэндогенных лиганд, его концентрация может не достичь того уровня, который необходим для эффективной конкуренции с эндогенными местами связывания.
Этот фактор особенно весомый в случае, когда вывод осуществляется через образование тройного комплекса, т.е. эндогенный лиганд-металоэкзогенный комплекс.
К комплексонам относятся:
- дефероксамин,
- тетацин-кальций,
- димеркапрол,
- пеницилламин,
- унитиол и др..
Дефероксамин (десферал) — комплексон, который активно связывает железо, в незначительной степени — эссенциальные микроэлементы. Может быть использован для ускорения выделения алюминия из организма при почечной недостаточности. Конкурируя за слабо связано железо в таких железосодержащих белках, как гемосидерин и ферритин дефероксамин не в состоянии конкурировать за то железо, которое содержится в биологических хелатных комплексах: микросомальных и митохондриальных цитохромах, гемопротеины т.п..
Фероксамин (комплекс железа с дефероксамином) представлен для демонстрации его функциональных групп. Здесь железо активно содержится в замкнутой системе. Димеркапрол, по сукцимер, захватывает металл (м) в стабильное гетероциклическое кольцо ковалентной связью.
Две молекулы пенициламина способны связывать одну молекулу меди или другого металла.
Продукты метаболизма дефероксамина выделяются почками, окрашивая мочу в темно-красный цвет. В процессе лечения дефероксамином могут возникнуть аллергические реакции (крапивница, кожная сыпь), коллапс (при быстром введении в вену), глухота, нарушение зрения, помутнение хрусталика. Встречается также коагулопатия, печеночная и почечная недостаточность, инфаркт кишечника.
Тетацин-кальций (кальций-динатриевая соль этилен-диаминтет-раоцтовой кислоты) — эффективный комплексон для многих двух-и трехвалентных тяжелых металлов и редкоземельных элементов, в частности для свинца, кадмия, кобальта, урана, иттрия, цезия и др.. Относительно плохо проникает через клеточные мембраны, поэтому более эффективно связывает внеклеточные ионы металла. Высокополярные ионные свойства тетацин-кальция препятствуют более или менее значительно энтеральному его всасыванию, поэтому он используется преимущественно для медленного внутримышечного или внутривенного введения.
В тетацин-кальции кальций замещается только ионами тех металлов и редкоземельных элементов, образующих более прочный комплекс (свинец, торий и др.), чем сам кальций. Барий и стронций, константа устойчивости комплекса которых ниже, чем кальция, не вступают в реакцию с тетацин-кальцием. Использование антидота тетацин-кальция для мобилизации ртути также неэффективно, видимо, из-за незначительного поступления этого комплексона в те ткани, где концентрируется ртуть, а также через менее успешную конкуренцию ее со связанным кальцием.
В больших дозах тетацин-кальций может вызвать повреждение почек, особенно их канальцев.
Пентацин — кальций-тринатриевая соль диетилентриамин-пентаоцтовой кислоты также эффективен как комплексон. В отличие от тетацин-кальция, он не влияет на выделение урана, полония, радия и радиоактивного стронция. При длительном введении элиминация металлов из организма снижается.
После введения пентацина возможно головокружение, головная боль, боли в груди и конечностях, поражение почек.
Димеркапрол (2,3-димеркаптопропанол, британский антилюизит, БАЛ). Выпускается в виде 10% раствора в арахисовом масле; вводится внутримышечно, инъекции болезненны. Своими SH-группами димеркапрол образует прочные хелатные комплексы с ионами ртути, мышьяка, свинца и золота, ускоряет их выведение из организма и восстановление функциональных белков, подавленных ядом. Эффективность этого антидота возрастает при минимальных сроках его применения после отравления. Он неэффективен, если лечение проводится через 24 ч и более.
Поэтому считают, что лечебные эффекты БАЛ обусловлены скорее предупреждением связывания металлов с компонентами клеток, крови и тканевой жидкости, а не удалением уже связанного яда.
Менее токсичными оказались некоторые производные димеркапрола, в частности сукцимер (димеркапрол сукцинат) и 2,3-димеркапропропан-1-сульфонат. Они более полярные, чем БАЛ; распределяются преимущественно во внеклеточной жидкости, поэтому в меньшей степени повреждают клеточные структуры крови и тканей.
Пеницилламин — Д-3 ,3-диметилцистеин гидрохлорид (купренил) — водорастворимый продукт метаболизма пенициллина. Д-изомер его относительно нетоксичен. Устойчив к метаболической деградации. Используется преимущественно при отравлении соединениями меди или для предупреждения их кумуляции, а также для лечения болезни Вильсона.
Как вспомогательное средство пеницилламин иногда применяют при лечении отравлений свинцом, золотом и мышьяком. Как и препараты золота, этот антидот тормозит прогрессирование деструкции костей и хрящей, поэтому используется в лечении ревматоидного артрита. Может быть причиной появления аллергических реакций, диспепсии, тромбоцитопении, лейкопении, анемии и т.д..
Натрия тиосульфат — серосодержащий антидот. В отличие от предыдущих препаратов, с металлами комплексных соединений не образует. Нейтрализует галоиды, цианиды, соединения мышьяка, ртути, свинца.
Как антидоты широкое распространение получили также окислители, адсорбенты. Слабые растворы кислот, обычно органических, ранее широко применяли для нейтрализации щелочей, а луга (натрия гидрокарбонат, магния оксид) — при отравлениях кислотами. Теперь преимущество предоставляется не нейтрализации кислот и щелочей, а их разведению.
Калия перманганат эффективен при отравлении морфином и другими алкалоидами, фосфором; танин — алкалоидами и тяжелыми металлами. Уголь активированный широко применяют при пероральном отравлении различными лекарственными средствами, а также алкалоидами, солями тяжелых металлов, бактериальными токсинами и т.д.. Он не адсорбирует железо, литий, калий и лишь в незначительной степени — алкоголь и цианиды. Совсем неэффективное при отравлении кислотами и щелочами, кислотой борной, тольбутамидом т.п..
Повторные приемы активированного угля через каждые 4 ч эффективны при отравлениях карбамазепином, дигитоксином, теофиллином и т.д..
В последние годы с целью ликвидации экзогенной (как и эндогенной) интоксикации начали использовать энтеросорбенты. Эти лекарственные препараты имеют свойство сорбировать (удерживать на своей поверхности) токсичные агенты, находящиеся в просвете желудочно-кишечного тракта. Сюда токсичные вещества могут попадать извне, выделяться путем диффузии из крови, находиться в составе пищеварительных соков и желчи или здесь образовываться. Энтеросорбенты, не являясь в полной мере антидотами, способствуют уменьшению уровня интоксикации, тем самым защищают организм от повреждения ядом.
Кроме того, энтеросорбенты улучшают пищеварение в желудке и кишечнике, так как способствуют более рациональной действия пищеварительных ферментов на элементы пищи, особенно белки. Они способствуют обезвреживанию ядовитых агентов в печени, улучшают окислительные процессы, процессы распада перекисных соединений и т.д.. Доказана их высокая эффективность при острой интоксикации микробными токсинами, атропином, сибазоном, грибами, бензином.
В медицинской практике используются как антидоты в основном углеродистые и полимерные сорбенты, в частности углеродные СКН (сферический карбонит насыщенный) и кремниевые — Полисорб, энтеросгель.
Клинический опыт показывает, что энтеросорбция эффективна при пищевых, медикаментозных, промышленных отравлениях. Энтеросорбенты эффективны также при заболеваниях, сопровождающихся эндотоксикозом, в частности органов пищеварения, сердечно-сосудистой, дыхательной и эндокринной систем, аллергических заболеваниях, токсикозах беременности.
В частности, при отравлении препаратами, оказывающими угнетающее влияние на ЦНС, используют стимуляторы ЦНС и аналептики:
- кофеин-бензоат натрия,
- эфедрина гидрохлорид,
- кордиамин,
- бемегрид,
- цититон и др..
В случае интоксикации ядами, возбуждающих ЦНС, как антагонисты используют препараты с подавляющим типом действия, в частности эфир для наркоза, нередко барбитураты, сибазон и т.д.. При отравлении холиномиметическими или Антихолинестеразными средствами применяют холинолитики (чаще атропина сульфат, скополамина гидробромид), а при отравлении атропином и ганглиолитикамы — антихолинэстеразные препараты (особенно прозерин).
- Антагонистом морфина и других наркотических болеутоляющих средств является налоксон;
- оксида углерода, сероводорода, сероуглерода и др. — кислород в ингаляции.
Налоксон назначается в начальной дозе 1-2 мг парентерально. Дозы увеличивают при интоксикации кодеином и фентанилом. Противопоказано использование физостигмина салицилата при отравлении трициклическими антидепрессантами.
Читайте также:
|


