Лейшманиоз при кала азаре
Кала-азар — заболевание, которое может быть эндемическим, эпидемическим •или спорадическим, вызывается Leishmania donovani. Хотя общая характеристика заболевания аналогична во всех районах мира, определенные местные особенности его клинических проявлений оправдывают разделение висцерального лейшманиоза на три основных типа. Эти различия связывают главным образом с длительностью периодов эндемичности этого заболевания на территории.
Африканский кала-азар встречается в восточной части Африки от Сахары на севере до экватора на юге . В западной части Африки отмечались спорадические случаи болезни. Болеют, как правило, дети старшего возраста и люди молодого возраста (от 10 до 25 лет); чаще поражаются лица мужского пола. Во многих районах оно встречается у собак и у ряда диких плотоядных животных и отличается большей устойчивостью к лечению препаратами сурьмы по сравнению с формами кала-азара в других районах мира.
Средиземноморский, или детский, кала-азар распространен главным образом в районах Средиземноморья, в Китае, Латинской Америке и на территории нашей страны. Он поражает обычно детей моложе 4 лет, однако не щадит и взрослых, особенно тех, кто путешествует по эндемичным районам. Резервуаром возбудителя служат собаки, шакалы и лисицы. В Италии потенциальным резервуаром возбудителя являются крысы. Штаммы возбудителя, вызывающие евроазиатские и американские разновидности болезни, иногда называют L. infantum и L. chagasi соответственно.
Индийский кала-азар по возрастному и половому распределению случаев болезни сходен с африканским кала-азаром. Человек является при этой форме болезни единственным из известных резервуаров возбудителя, причем передача инфекции происходит через антропофильные виды москитов.
Клинические проявления. Инкубационный период составляет в целом примерно 3 мес (от 3 нед до 18 мес). Первичный кожный элемент (лейшманиома) в Африке встречается редко. Начало заболевания может быть постепенным или острым; последний вариант встречается чаще у лиц из неэндемичных районов. Типично повышение температуры тела в ночное время, реже отмечается два пика температуры в течение суток, причем лихорадка является почти постоянным признаком болезни и сопровождается тахикардией без признаков токсемии. Ежедневная лихорадка переходит в рецидивирующие лихорадочные волны. Часто отмечаются диарея и кашель. К 3-му месяцу болезни формируется весьма выраженная безболезненная спленомегалия. Печень увеличивается не так резко. Примерно у 10% больных отмечаются цирроз печени и портальная гипертензия. В ряде случаев при африканском кала-азаре наблюдается лимфаденопатия. Описаны атипичные формы болезни, в частности изолированное поражение миндалин и шейная лимфаденопатия. Предполагается существование бессимптомных или субклинических форм инфекции.
Характерна панцитопения. Анемия обусловлена многими факторами: аутоиммунный гемолиз, спленомегалия и желудочно-кишечные кровотечения — все это способствует ее развитию. Анемия усугубляется вследствие тромбоцитопении. При отсутствии лечения заболевание осложняется агранулоцитозом, раком ротовой полости и вторичной инфекцией. Обширная инфильтрация лейшманиями желудочно-кишечного тракта может привести к мальабсорбции. Постоянными признаками болезни являются гипоальбуминемия и поликлональная гипергаммаглобулинемия (IgG и IgM). Часто выявляют циркулирующие иммунные комплексы. Описаны случаи иммунокомплексного гломерулонефрита и интерстициального нефрита. У больных с хронической формой болезни возможно развитие амилоидоза. На поздних стадиях болезни развиваются отеки, кахексия и гиперпигментация (кала-азар означает черная болезнь). При отсутствии лечения болезнь заканчивается летальным исходом в сроки от 3 до 20 мес у 90 — 95% взрослых больных и у 75 — 85% детей обычно вследствие вторичной инфекции или желудочно-кишечного кровотечения.
После успешного лечения в 3% случаев при африканской форме и в 10% случаев при индийской форме болезни развивается посткала-азарный дермальный лейшманиоз (ПКДЛ), характеризующийся наличием целого спектра поражений от депигментированных пятен до бородавчатых узелков на коже лица и разгибательной поверхности конечностей. ПКДЛ появляется вскоре после угасания симптомов при африканской форме болезни и обычно исчезает через несколько недель. В случае индийской формы болезни ПКДЛ появляется после латентного периода длительностью от 1 до 2 лет и может сохраняться в течение нескольких лет, такие больные служат постоянным резервуаром инфекции.
Диагностика. Диагностика основана на обнаружении паразитов в препара тах из слоя лейкоцитов, особенно при индийском кала-азаре (90%). В пунктатах костного мозга и в биоптатах тканей возбудители обнаруживаются более чем в 85% случаев. В Кении пункция селезенки в 95% случаев оказалась совершенно безопасной и проводилась повторно для оценки эффективности лечения. Однако в целом пункция селезенки или печени (75%) не рекомендуется ввиду риска развития смертельного кровотечения. В пунктатах или биоптатах увеличенных лимфатических узлов паразиты обнаруживаются в 60% случаев. Биопсию следует проводить также в области подозрительно измененных участков кожи. Прямая реакция агглютинации становится положительной на ранней стадии болезни. Кожная лейшманиновая реакция становится положительной через 6—8 нед после выздоровления. Другие причины лихорадки, в частности малярия, бруцеллез, туберкулез, брюшной тиф и печеночный абсцесс, можно отдифференцировать с помощью соответствующих тестов. ПКДЛ следует дифференцировать от лепры, сифилиса и фрамбезии.
Лечение. Специфическая терапия должна быть дополнена трансфузиями и лечением вторичной инфекции. Препараты пятивалентной сурьмы высокоэффективны против лейшманий и относительно нетоксичны. Антимонила натрия глюконат (Пентостам; 100 мг Sb 5+ на 1 мл) вводится внутривенно или внутримышечно 1 раз в сутки в дозе 10 мг/кг для взрослых и 20 мг/кг для лиц моложе 18 лет. Продолжительность лечения 20 дней при индийском кала-азаре и 30 дней при других формах болезни. Можно применять также меглюмина антимониат (Глюкантим; 85 мг Sb 5+ на 1 мл). Курс лечения следует повторить в суточной дозе 20 мг/кг в течение 40 — 60 дней у больных с рецидивами или при неполном излечении. Целесообразно дополнительно применять аллопуринол (от 20 до 30 мг/кг в сутки дробно в 3 приема внутрь). В том случае, если эффект от проводимого лечения незначителен, рекомендуется внутривенное введение амфотерицина В (0,5 — 1 мг/кг через день) или пентамидина (3—4 мг/кг 3 раза в неделю в течение 5—25 нед, в зависимости от клинического эффекта). В некоторых случаях лекарственно-устойчивой формы кала-азара положительный эффект дает спленэктомия (в качестве дополнительного мероприятия). На поздних стадиях болезни летальность остается на уровне 15—25%, хотя показатель излечения превышает 90% в тех случаях, когда терапия начата своевременно (в ранние сроки болезни). Для выявления рецидивов за больным рекомендуется наблюдать в течение 3— 12 мес после проведения курса лечения. Больных с ПДКЛ следует лечить по той же схеме, что и в случае начального заболевания.
Профилактика. Профилактические мероприятия включают раннее лечение больных, устранение заболевших собак, а также обработку ДДТ против москитов. Применение репеллентов и использование мелкоячеистых сеток от москитов весьма важно при посещении эндемичных районов. Надежных профилактических препаратов в настоящее время не имеется.
Основные факты
- Существует 3 основных типа лейшманиоза — висцеральный (также известен как кала-азар и являющийся самой тяжелой формой болезни), кожный (наиболее распространенный) и слизисто-кожный.
- Возбудителем лейшманиоза является простейший паразит Leishmania, который передается при укусе инфицированных москитов.
- Болезнь поражает самых бедных людей планеты и связана с недостаточностью питания, перемещением населения, плохими жилищными условиями, слабой иммунной системой и отсутствием ресурсов.
- Лейшманиоз связан с изменениями в окружающей среде, такими как обезлесение, строительно дамб и ирригационных систем и урбанизация.
- По оценкам, ежегодно происходит 700 000–1 миллион новых случаев инфицирования и от 26 000 до 65 000 случаев смерти.
- Лишь у небольшой доли людей, инфицированных паразитами Leishmania, в конечном итоге разовьется болезнь.
Возбудителем лейшманиоза является паразит протозоа, один из более чем 20 видов Leishmania. Установлено, что переносчиками паразита Leishmania являются более 90 видов москитов. Существует 3 основных типа этой болезни:
- Висцеральный лейшманиоз (ВЛ, известный также как кала-азар) без лечения заканчивается смертельным исходом. Для него характерны нерегулярные приступы лихорадки, потеря веса, увеличение селезенки и печени и анемия. Большинство случаев происходит в Бразилии, Восточной Африке и Юго-Восточной Азии. По имеющимся оценкам, в мире ежегодно происходит от 50 000 до 90 000 новых случаев заболевания ВЛ, однако ВОЗ получает информацию лишь в отношении 25-45% случаев. В 2017 г. более 95% новых случаев заболевания, о которых была извещена ВОЗ, произошли в 10 странах: Бангладеш, Бразилии, Китае, Эфиопии, Индии, Кении, Непале, Сомали, Южном Судане и Судане.
- Кожный лейшманиоз (КЛ) является наиболее распространенной формой лейшманиоза и вызывает повреждения кожи, главным образом язвы, на открытых участках тела, после которых на всю жизнь остаются шрамы, тяжелая инвалидность или стигма. Около 95% случаев заболевания КЛ происходит в странах Американского континента, в Средиземноморском бассейне, на Ближнем Востоке и в Средней Азии. В 2017 г. более 95% новых случаев заболевания КЛ произошли в 7 странах: Алжире, Афганистане, Бразилии, Ираке, Иране (Исламской Республике), Колумбии и Сирийской Арабской Республике. По оценкам, в мире ежегодно происходит от 600 000 до 1 миллиона новых случаев заболевания.
- Слизисто-кожный лейшманиоз приводит к частичному или полному разрушению слизистых оболочек носа, рта и горла. Более 90% случаев заболевания слизисто-кожным лейшманиозом происходит в Многонациональном Государстве Боливия, Бразилии, Перу и Эфиопии.
Паразиты, вызывающие лейшманиоз, передаются при укусах инфицированных самок phlebotomine sandflies, которые питаются кровью для откладывания яиц. Эпидемиология лейшманиоза зависит от характеристик паразита и вида москита, экологических особенностей мест, где происходит передача инфекции, текущего и прошлого воздействия паразита на данную группу населения и поведения людей. Установлено, что около 70 видов животных, в том числе человек, являются естественными резервуарами паразитов Leishmania.
Специфика по регионам ВОЗ
Висцеральный, кожный и слизисто-кожный лейшманиоз является эндемическим в Алжире и странах Восточной Африки, которые характеризуются высокой эндемичностью. В Восточной Африке часто происходят вспышки висцерального лейшманиоза.
Эпидемиология кожного лейшманиоза в Америке очень сложна и характеризуется разными циклами передачи, резервуарными хозяевами, типами москитов-переносчиков, клиническими проявлениями и ответными реакциями на лечение, а также тем, что в одном и том же географическом районе могут циркулировать разные виды Leishmania. 90% случаев ВЛ в этом регионе приходится на Бразилию.
На этот регион приходится 70% случаев кожного лейшманиоза в мире. Висцеральный лейшманиоз является высокоэндемическим в Ираке, Сомали и Судане.
Этот регион эндемичен по кожному и висцеральному лейшманиозу. Кроме того, регистрируются завезенные случаи заболевания, главным образом из Африки и Америки.
Основной формой болезни в этом регионе является висцеральный лейшманиоз, но регион также эндемичен по кожному лейшманиозу. Это единственный регион, выступивший с региональной инициативой ликвидировать висцеральный лейшманиоз как проблему общественного здравоохранения к 2020 г.
PDKL является осложнением висцерального лейшманиоза, обычно проявляющимся в виде макулезной, папулезной или узелковой сыпи обычно на лице, верхней части рук, туловище и других частях тела. Он характерен, в основном, для Восточной Африки и Индостана, где это состояние регистрируется у 5-10% пациентов с кала-азар. Обычно сыпь появляется через 6 месяцев — один или более лет после видимого излечения кала-азар, но может появиться и раньше. Люди с PDKL считаются потенциальным источником инфекции Leishmania.
Существует высокая вероятность, что у людей с коинфекцией лейшмании и ВИЧ разовьется резко выраженная клиническая болезнь с частыми рецидивами и высокими показателями смертности. Антиретровирусное лечение ограничивает развитие болезни, отдаляет наступление рецидивов и повышает выживаемость коинфицированных пациентов. Высокие показатели сочетанной инфекции Leishmania-ВИЧ зарегистрированы в Бразилии, Эфиопии и индийском штате Бихар.
Белково-энергетическая недостаточность и недостаточное потребление железа, витамина А и цинка в питании повышают риск развития заболевания в результате инфицирования.
Эпидемии обеих основных форм лейшманиоза часто связанны с миграцией и передвижением людей, не имеющих иммунитета, в районы, где сохраняются циклы передачи инфекции. Важными факторами остаются воздействие на рабочих местах, а также широко распространившееся обезлесение.
На заболеваемость лейшманиозом может повлиять урбанизация и вторжение человека в лесные районы.
Лейшманиоз чувствителен к климату так как он воздействует на эпидемиологию лейшманиоза разными путями:
- изменения температуры, выпадения осадков и влажности могут оказывать значительное воздействие на переносчиков и хозяев путем изменения мест их распространения и воздействия на их выживаемость и размеры популяций;
- небольшие температурные колебания могут оказывать глубокое воздействие на цикл развития промастигот лейшманий в организме москитов, что может привести к установлению передачи паразита в районах, ранее не являющихся эндемичными по этой болезни;
- засуха, голод и наводнения могут приводить к массовому перемещению и миграции людей в районы с передачей лейшманиоза, а плохое питание может ослаблять их иммунитет.
При висцеральном лейшманиозе диагноз ставится на основе клинических признаков в сочетании с результатами паразитологических или серологических тестов (диагностических экспресс-тестов и других). При кожном и слизисто-кожном лейшманиозе серологические тесты имеют ограниченную ценность. Эффективность лечения лейшманиоза зависит от ряда факторов, включая тип болезни, сопутствующие патологии, вид паразита и географическое положение. Диагноз подтверждают клинические проявления и результаты паразитологических тестов.
Лечение лейшманиоза зависит от нескольких факторов, включая тип болезни, вид паразитов, географическое расположение. Лейшманиоз можно лечить и излечивать, но для того, чтобы лекарства помогли организму избавиться от паразитов, необходим здоровый иммунитет, а при иммунодефиците существует риск рецидивов. Всем пациентам, у которых диагностирован висцеральный лейшманиоз, требуется безотлагательное и полное лечение. Детальная информация о лечении разных форм болезни в зависимости от географического расположения доступна в серии технических докладов ВОЗ 949 о борьбе с лейшманиозом.
Для профилактики лейшманиоза и борьбы с ним необходимо проводить комбинированные стратегии, так как передача инфекции происходит в сложной биологической системе с участием человека (хозяина), паразита, москита (переносчика) и в некоторых случаях животного резервуара (хозяина). Основные стратегии включают следующие:
- Ранняя диагностика, эффективное и своевременное лечение способствуют уменьшению распространенности болезни и предотвращают инвалидность и смерть. Это способствует снижению уровней передачи инфекции и мониторингу распространения и бремени болезни. В настоящее время существуют высокоэффективные и безопасные препараты для лечения лейшманиоза, особенно его висцеральной формы, хотя их применение может быть сопряжено с трудностями. Доступ к этим препаратам значительно улучшился благодаря системе ВОЗ по согласованию цен и программе бесплатного предоставления лекарств через ВОЗ.
- Борьба с переносчиками способствует снижению заболеваемости или прерыванию передачи инфекции путем сокращения числа москитов. Методы борьбы включают распыление инсектицидов, использование обработанных инсектицидом сеток, рациональное использование окружающей среды и личную защиту.
- Эффективный эпиднадзор за болезнью Очень важно вести эффективный эпиднадзор за болезнью. Мониторинг и принятие мер во время эпидемий и в ситуациях с высокими коэффициентами летальности среди получающих лечение пациентов.
- Борьба с животными-хозяевами является сложным мероприятием, требующим учета местных условий.
- Социальная мобилизация и укрепление партнерств — мобилизация и санитарное просвещение местных сообществ при проведении эффективных мероприятий, направленных на изменение поведения, и коммуникационных стратегий, адаптированных к местным условиям. Партнерство и сотрудничество с различными заинтересованными сторонами и программами по борьбе с другими трансмиссивными болезнями имеет критически важное значение на всех уровнях.
Работа ВОЗ в области борьбы с лейшманиозом ведется по следующим направлениям:
- Техническое и финансовое содействие национальным программам по борьбе с лейшманиозом в области обновления руководящих принципов и составления планов борьбы с болезнью, охватывающих формирование устойчивых и эффективных систем эпиднадзора и систем обеспечения готовности к эпидемиям и реагирования на них.
- Мониторинг тенденций заболеваемости и оценка воздействия мероприятий по борьбе, которые позволят повысить осведомленность и улучшить информационно-разъяснительную работу в отношении бремени лейшманиоза и содействовать справедливому доступу к услугам здравоохранения.
- Разработка основанных на фактических данных руководящих принципов политики, стратегий и стандартов по профилактике лейшманиоза и борьбе с ним, и мониторинг их осуществления; повышение осведомленности и информационно-разъяснительная работа в отношении глобального бремени лейшманиоза и обеспечение справедливого доступа к службам здравоохранения для профилактики болезни и ведения случаев заболевания;
- Укрепление сотрудничества и координации среди партнеров, заинтересованных сторон и других структур;
- Стимулирование научных исследований и использование эффективной борьбы с лейшманиозом, в том числе безопасных, эффективных и доступных по стоимости лекарств, диагностических средств и вакцин;
- Оказание поддержки национальным программам борьбы для обеспечения доступа к лекарственным препаратам гарантированного качества.
Медицинский эксперт статьи

Индийский висцеральный лейшманиоз (синонимы: черная болезнь, лихорадка дум-дум, кала-азар).

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14]
Код по МКБ-10
Эпидемиология индийского висцерального лейшманиоза
Кала-азар - антропоноз. Источник заражения - больной человек, у которого возбудитель присутствует в коже при развитии посткала-азарного кожного лейшманоида. Наибольшая заболеваемость регистрируется среди детей 5-9 лет. Второй наиболее пораженной группой являются подростки.
Переносчик - москит Phlebotomus (Euphlebotomus) argentipes. Кроме Индии кала-азар встречается в Бангладеш, Непале и, возможно, в Пакистане. Висцеральный лейшманиоз, по клинике сходный с индийским кала-азаром, распространен в северо-восточной части Китая, где переносчиком возбудителя служат Ph. chinensis и Ph. longidudus. Антропонозный висцеральный лейшманиоз, вызываемый L. donovani, встречается также на Африканском континенте - в Кении, Судане, Уганде и Эфиопии, где переносчиком выступает Ph. martini, и на Аравийском полуострове - на юго-западе Саудовской Аравии и в горных районах Йемена (переносчики - Ph. arabicus и Ph. orientalis).

[15], [16], [17], [18], [19], [20], [21], [22], [23], [24]
Что вызывает индийский висцеральный лейшманиоз?
Индийский висцеральный лейшманиоз вызывается Leishmania donovani, которая в организме человека паразитирует внутриклеточно в стадии амастиготы (безжгутиковой), а в организме переносчика - в стадии промастиготы (жгутиковой).
Симптомы индийского висцерального лейшманиоза
Клинические симптомы кала-азара в целом сходны с таковыми при висцеральном лейшманиозе, однако существуют и отличия, имеющие важное эпидемиологическое значение. Наряду с поражением внутренних органов, для него характерны появления на коже вторичных папул - лейшманоидов с локализацией в них паразитов, а также незначительная циркуляция лейшманий в коже.
Инкубационный период при кала-азаре (висцеральном лейшманиозе) составляет от 20 дней до 3-5 месяцев. Известны случаи удлинения инкубационного периода до 2-х лет. Болезнь развивается медленно. Нередко первичные симптомы индийского висцерального лейшманиоза у инвазированных людей проявляются вследствие каких-либо провоцирующих факторов (инфекционное заболевание, беременность и др.). Одним из основных симптомов болезни является лихорадка. Чаще всего температура тела больных повышается постепенно, достигая 38-39 С. Реже повышение температуры наступает внезапно после озноба, температурная кривая обычно ундулирующего типа. Периоды лихорадки, длящиеся от нескольких дней до месяца и более, чередуются с периодами ремиссии, протекающими при нормальной температуре. В один и тот же лихорадочный период температура может быть постоянной, субфебрильной, ремитирующей.
Кожные покровы могут приобретать темный цвет (индийский кала-азар), восковидный оттенок или сохраняться бледными. Темное окрашивание кожи объясняется гипофункцией надпочечников, что связано с поражением их коркового слоя лейшманиями.
При прогрессирующем течении болезни у больных развивается кахексия. Она сопровождается петехиальными или милиарными высыпаниями, преимущественно в области нижних конечностей, ломкостью волос с образованием на голове мелкоочаговых alopecia areata.
Лимфатические узлы могут быть увеличенными, но без выраженного периаденита.
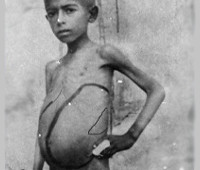
Внутриклеточное паразитирование лейшманий обусловливает развитие селезеночно-печеночного синдрома. Селезенка значительно увеличивается в размерах в течение первых 3-6 месяцев болезни; она приобретает плотную консистенцию, верхняя ее граница доходит до VII-VI ребер; нижний край - до полости малого таза. Происходит также и увеличение печени. Гепатоспленомегалия выражена у всех больных висцеральным лейшманиозом и при сильном исхудании приводит к заметному расширению вен на коже живота.
Изменения со стороны сердечно-сосудистой системы проявляются в виде миокардиодистрофии, снижения артериального давления. Значительные изменения возникают в кроветворной системе, которые приводят к резко выраженной анемии. При этом наблюдаются лейкопения, анэозинофилия, тромбоцитопения, нейтропения со сдвигом влево, СОЭ ускорена (до 92 мм/час).
При висцеральном лейшманиозе изменения распространяются и на органы дыхания, но они чаще всего обусловлены осложнением течения заболевания патогенной микрофлорой.
В некоторых странах зон жаркого климата (Индия, Судан, Восточная Африка, Китай) у 5-10% больных спустя 1-2 года после видимого выздоровления наблюдается развитие посткала-азарных кожных лейшманоидов, которые могут держаться несколько лет. Кожные лейшманоиды появляются вначале в виде гипопигментированных или эритематозных пятен; в дальнейшем отмечается высыпания узелкового характера, величиной с чечевицу. В этих кожных образованиях могут обнаруживаться лейшманий.
Таким образом, лейшманоиды являются источниками заражения москитов лейшманиями, а сами люди, обладатели кожных лейшманоидов, служат резервуарами инфекции кала-азар.
Диагностика индийского висцерального лейшманиоза
Несколько изменчивые симптомы индийского висцерального лейшманиоза обычно подтверждается лейкопенией, высоким уровнем содержания гамма-глобулина в крови, обнаруживаемого с помощью бумажного электрофореза и положительного формолового теста (последний производится путем добавления 1 мл сыворотки больного). В положительном случае сыворотка становится плотной и непрозрачной спустя 20 мин после добавления формалина.
Может быть поставлена реакция связывания комплемента. Разработан также иммунолюминесцентный метод, который используется в ранней диагностике до развития основных симптомов болезни. L. donovani могут быть обнаружены в окрашенных препаратах из пунктата костного мозга, лимфатических узлов, селезенки и печени. При посеве инвазированной крови или пунктата на специальные среды (NNN-arap) или выращивании в культуре ткани могут быть получены жгутиковые формы лейшманий.
Кала-азар подлежит дифференциации от брюшного тифа и бруцеллеза, для диагностики которых применяются реакция агглютинации и посевы крови. Дифференциация лейшманиоза от малярии производится путем исследования мазков крови. Кала-азар следует дифференцировать также от шистомозиаза, туберкулеза, лейкемии и ретикулеза. Любая из этих инфекций может наблюдаться наравне с кала-азаром, особенно в эндемических очагах.
Посткала-азарные кожные лейшманоиды должны быть отдифференцированны от проказы, фрамбезии, сифилиса, lupus vulgaris, повышенной чувствительности к лекарственным препаратам и других дерматозов.
Диагностика индийского висцерального лейшманиоза и кала-азара, как и кожного лейшманиоза, основана на анамнестических, клинических и лабораторных данных. Решающим является паразитологическое исследование - обнаружение возбудителя в мазках из пунктата костного мозга, реже - из лимфоузлов. Приготовление мазков, фиксация, окраска и микроскопирование аналогичны таковым при кожном лейшманиозе. В качестве дополнительных методов диагностики применяют реакцию иммунофлюоресценции.

[25], [26], [27], [28], [29], [30], [31], [32], [33], [34]
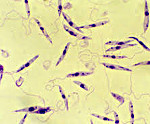
Висцеральный лейшманиоз – это хроническое инфекционное протозойное заболевание с поражением печени и селезенки, развитием анемии и кахексии. Другими симптомами являются лихорадка, увеличение лимфоузлов, кожные проявления. Диагностика включает выявление возбудителя из крови и биоптатов внутренних органов, реже путем биопроб на грызунах, поиск антител к возбудителю. Лечение состоит из курса этиотропных препаратов (преимущественно пятивалентной сурьмы) и коррекции органных дисфункций в качестве симптоматической терапии. В некоторых случаях показаны гемотрансфузии.
МКБ-10
Общие сведения
Висцеральный лейшманиоз (лихорадка дум-дум, кала-азар, черная лихорадка) принадлежит к трансмиссивным инфекциям, вызываемым простейшими. В 1903 году английский патолог Лейшман совместно с итальянским ученым Донованом описал морфологию органных поражений и выделил возбудителя. В честь исследователей инфекционный агент получил своё название Leishmania donovani. Болезнь наиболее распространена в тропических и субтропических странах, сезонный рост заболеваемости зависит от особенностей жизненного цикла переносчика и приходится на период с мая по ноябрь.

Причины
Возбудитель инфекции – простейший паразитический микроорганизм лейшмания. Источниками и резервуарами инфекции служат теплокровные дикие и домашние животные (грызуны, ленивцы, лисы, собаки), люди. Путь инфицирования преимущественно трансмиссивный, переносчики – самки москитов рода Phlebotomus. Имеются данные о единичных случаях заражения при переливаниях крови, передачи лейшманий от матери плоду, при использовании нестерильного медицинского инструментария и игл во время внутривенного введения наркотических средств.
В своем развитии лейшманиям необходимо пройти две стадии: безжгутиковую и жгутиковую в организме человека либо животного и переносчика соответственно. Амастиготы обитают внутри клеток, лишены способности к перемещению, промастиготы имеют жгутики для активных движений в пространстве. Находясь внутри самки москита, лейшмании активно размножаются в пищеварительном канале насекомого, после чего перемещаются к хоботку. Наиболее подвержены заражению дети до 5 лет, молодые мужчины, сельскохозяйственные работники, туристы, пациенты с ВИЧ-инфекцией, онкопатологиями.
Патогенез
В месте укуса переносчика формируется первичный аффект в виде гранулемы, которая состоит из макрофагов с размножающимися внутри лейшманиями, ретикулоцитов, эпителиоцитов и гигантских клеток. Через некоторое время гранулема подвергается обратному развитию, реже рубцеванию, а находящиеся в макрофагах возбудители с током лимфы и крови попадают во внутренние органы. При нормальном состоянии иммунной системы происходит разрушение пораженных клеток. В случае иммунодефицита лейшмании размножаются с увеличенной скоростью, поражают паренхиматозные органы.
Это приводит к возникновению воспалительных изменений, активному фиброзированию и увеличению размеров органов. В печеночной ткани при патогистологическом исследовании обнаруживаются участки интерлобулярного фиброза и дистрофия гепатоцитов, в лимфатических узлах – дистрофические изменения зародышевого центра и аплазия костного мозга, в селезенке – атрофия пульпы, зоны инфарктов, некроза и геморрагических инфильтратов. При длительном течении висцерального лейшманиоза возникает амилоидоз внутренних органов.
Классификация
Разделение висцерального лейшманиоза на сельский и городской виды подразумевает разные источники инфекции (домашние и дикие животные), а также тяжесть течения патологии – считается, что при городском типе болезнь протекает доброкачественнее. Выделяют острый, подострый и хронический варианты органного лейшманиоза. Наиболее благоприятным течением отличается хроническая форма, острый тип данной протозойной инфекции чаще всего встречается у детей, характеризуется бурным развитием симптомов и нередкими летальными исходами. Для подострого варианта типично наличие осложнений.
Симптомы висцерального лейшманиоза
Инкубационный период составляет от 20 дней до 1 года, чаще 3-5 месяцев. Для манифестации болезни характерно постепенное начало, появление кожной папулы бледно-розового цвета на месте внедрения возбудителя, сменяющейся участком депигментации (лейшманоид). Отмечается слабость, беспричинная усталость, снижение аппетита, похудание. В дальнейшем присоединяется лихорадка до 39-40° C, которая протекает с чередованием высокой и нормальной температуры тела на продолжении нескольких месяцев.
Наблюдается безболезненное увеличение всех групп лимфатических узлов, изменение их консистенции до плотно-эластической. Пациенты с висцеральным лейшманиозом почти всегда отмечают тяжесть и дискомфорт в подреберьях. При прогрессировании болезни наблюдается гепатоспленомегалия с появлением отеков и увеличением живота. Снижается количество выделяемой мочи. В связи с развитием гиперспленизма и поражения костного мозга возникают кровотечения. Обнаруживается одышка, язвенно-некротические поражения ротовой полости, бледность кожи, нарушения дефекации.
Осложнения
Наиболее частые осложнения (тромбогеморрагический синдром, гранулоцитопения, агранулоцитоз) связаны с поражением кроветворной системы, следствием чего является некроз миндалин, слизистой рта и десен (нома). Отечно-асцитический синдром при висцеральном лейшманиозе возникает из-за вовлечения печени, сопровождается хронической сердечной недостаточностью, нарушениями в работе ЖКТ (энтероколитом), нефритом, снижением либидо, олиго- и аменореей. Характерны случаи бактериальной пневмонии ввиду высокого стояния диафрагмы и снижения дыхательной емкости легких. К редким осложнениям относят разрывы селезенки, геморрагический шок, ДВС-синдром.
Диагностика
Определение висцеральной формы лейшманиоза требует осмотра инфекциониста, по показаниям назначаются консультации других специалистов. Важно уточнить у пациента факт пребывания в эндемичных зонах земного шара в течение предшествующих пяти лет, наличие вакцинации от лейшманиоза, род профессиональных занятий. Лабораторные и инструментальные методы верификации болезни включают в себя:
- Физикальное исследование. Во время объективного осмотра обращает на себя внимание бледность, сухость, истончение кожи, наличие язв в полости рта. Лимфоузлы плотные, увеличенные, безболезненные. При аускультации тоны сердца приглушены, выслушивается тахикардия, шумы, в легких могут определяться участки ослабленного дыхания. Пальпация живота безболезненна, размеры селезенки и печени резко увеличены. Часто обнаруживаются периферические отеки, асцит.
- Лабораторные исследования. Признаками лейшманиоза в общем анализе крови служат анемия, пойкилоцитоз, анизоцитоз, лейкопения, нейтропения, анэозинофилия, тромбоцитопения, резкое ускорение СОЭ. Биохимические параметры изменены в сторону повышения АЛТ, АСТ, СРБ, креатинина и мочевины, гипоальбуминемии. Наблюдается увеличение времени свертывания крови. В общеклиническом анализе мочи отмечается повышение плотности мочевого осадка, протеинурия, гематурия.
- Выявление инфекционных агентов. Для обнаружения лейшманий проводится микроскопия, посев биологических препаратов и крови, реже биопробы на хомячках. Серологическая диагностика (ИФА) направлена на выявление противолейшманиозных антител. Использование внутрикожной пробы Монтенегро является косвенным методом подтверждения диагноза в период реконвалесценции, применяется при эпидемиологических исследованиях в популяции.
- Инструментальные методики. Рентгенография ОГК выполняется для исключения пневмонии, туберкулезного поражения. Сонография брюшной полости визуализирует увеличение размеров печени, селезенки, признаки портальной гипертензии, наличие асцита. УЗИ и биопсию лимфатических узлов, стернальную пункцию, трепанобиопсию костного мозга, диагностическую торакоскопию и лапароскопию осуществляют по показаниям.
Туберкулез проявляется длительным субфебрилитетом, редко сухим кашлем и симптомами дисфункции вовлеченных в патологический процесс органов; часто диагноз верифицируется только лабораторно-инструментальными методиками. Схожесть клинических симптомов заболевания наблюдается с такими патологиями, как лейкоз и лимфогранулематоз, при данных патологиях диагностическими критериями становятся данные анализов крови и биопсии костного мозга. Сепсис клинически протекает схоже, но обычно имеет первичный очаг поражения (рана, гнойное образование и др.).
Лечение висцерального лейшманиоза
Пациенты с данным заболеванием госпитализируются в стационар. В обязательном порядке необходимо ограничить возможность контакта с москитами, поэтому над кроватями и в оконных проемах устанавливают противомоскитные сетки. Постельный режим показан до устойчивых нормальных цифр температуры тела в течение 3-5 дней, из-за риска разрыва селезенки при её значительном увеличении не рекомендуются резкие наклоны, повороты, поднятие тяжестей более 10 кг. Режим питания предусматривает высококалорийную, богатую белками пищу, водная нагрузка подбирается индивидуально.
Этиотропная терапия висцерального лейшманиоза должна включать препараты сурьмы (натрия стибоглюконат) либо пентамидин, милтефозин, липосомальный амфотерицин В. Некоторые исследования показали эффективность терапевтического приема производных пятивалентной сурьмы в сочетании с сульфатом паромомицина, при этом сокращается длительность курса лечения. Пациентам с осложнениями, ВИЧ-инфекцией, тяжелыми сопутствующими болезнями рекомендовано курсовое введение амфотерицина В как первой линии лечения висцерального лейшманиоза.
Выраженная анемия является показанием для эритроцитарных гемотрансфузий, реже требуется введение тромбомассы и донорских лейкоцитов. Коррекция анемии заключается в длительном приеме препаратов железа, по показаниям – колониестимулирующих факторов. Симптоматическое лечение предполагает дезинтоксикацию, прием жаропонижающих средств (аспирин – с осторожностью), антибиотиков в случае присоединения вторичных инфекций. Важной составляющей лечения является борьба с отеками, в числе прочего в план терапии включаются мочегонные средства и растворы альбумина.
Прогноз и профилактика
Прогноз при ранней диагностике благоприятный за исключением случаев болезни у ВИЧ-инфицированных пациентов – у данной категории больных даже слабопатогенные штаммы лейшманий вызывают органные поражения. Продолжительность лечения составляет 14-30 дней, наблюдение за реконвалесцентами занимает 4-6 месяцев из-за возможных рецидивов лейшманиоза. У 17% пролеченных пациентов в течение 5 лет после выздоровления могут обнаруживаться симптомы посткала-азарного дермального лейшманиоза, протоколы диагностики и лечения для которого окончательно не разработаны.
Специфическая профилактика заключается в плановом введении живой вакцины, рекомендована лицам, проживающим или планирующим длительное либо кратковременное пребывание на эндемичных территориях, туристам. Введение препарата необходимо осуществлять зимой или осенью минимум за три месяца до поездки. Неспецифические меры предотвращения висцерального лейшманиоза включают своевременное выявление, изоляцию и лечение больных, использование противомоскитных сеток, вакцинацию собак, устранение свалок, меры дезинсекции и дератизации. Борьба с москитами заключается, в том числе, в осушении болот, подвалов и овощехранилищ.
Читайте также:


