Иммуномодулятор для лечения рассеянного склероза что это такое
Ведущую роль в развитии рассеянного склероза играют аутоиммунные процессы - патологические реакции иммунной системы пациента против миелиновой оболочки собственных клеток нервной системы. При этом основным механизмом, приводящим к повреждению нервной ткани, является активность аутоиммунных Т-лимфоцитов против белка миелина, а непосредственно клетками, осуществляющими разрушение оболочек нервных волокон, являются клетки иммунной системы, которые имеют название макрофаги.
Поскольку рассеянный склероз возникает, прежде всего, как результат дефекта в иммунной системе, иммунные клетки являются основной мишенью для лечения этого заболевания. Лекарственные препараты, зарегистрированные для лечения рассеянного склероза, делят на иммуномодуляторы (бета-интерфероны и глатирамер ацетат - Копаксон) и иммуносупрессанты (митоксантрон, циклофосфан, азатиоприн и др.). Отдельные исследователи изучают возможности метода Т-клеточной аутовакцинации. Кроме того, в последние годы была убедительно показана высокая эффективность высокодозной иммуносупрессивной терапии с трансплантацией кроветворных стволовых клеток. Кратко рассмотрим каждый из методов иммунотерапии рассеянного склероза.
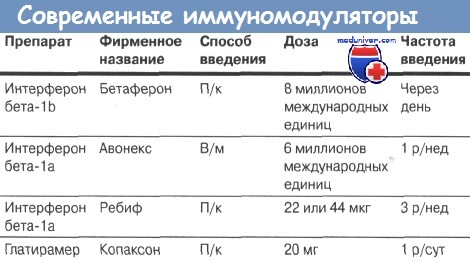
ИФНβ-1b (Бетаферон) стал первым препаратом, одобренным для лечения рассеянного склероза в 1993 г. Затем были зарегистрированы две версии ИФН-1а, несколько отличающегося от Бетаферона по химической структуре (Авонекс и Ребиф). Клиническая эффективность различных препаратов ИФНβ при выборе оптимальной дозировки и режима лечения одинакова.
Действие ИФНβ обусловлено связыванием с рецепторами на поверхности клетки и запуском продукции ряда белков, обладающих противовирусным и противовоспалительным действием. Терапевтический эффект ИФНβ при рассеянном склерозе обусловлен торможением размножения клеток иммунной системы и созданием противовоспалительного фона, что способствует уменьшению выраженности патологического процесса. Другим важным механизмом действия является снижение темпа миграции лейкоцитов из крови в центральную нервную систему. Кроме того, было показано, что ИФНβ способствует ускорению естественной гибели патологических Т-лимфоцитов, а также является антагонистом ИФНβ - белка, играющего важную роль в патогенезе рассеянного склероза.
При использовании ИФНβ курс лечения составляет, по меньшей мере, 6 месяцев, и при наличии эффекта должен продолжаться пожизненно. Анализ результатов клинической эффективности ИФНβ при рассеянном склерозе показывает, что терапия ИФН? несколько уменьшает частоту рецидивов в течение первого года лечения. Долгосрочная эффективность ИФНβ неочевидна и требует дальнейшего изучения.
Копаксон (Глатирамер ацетат)
Глатирамер ацетат был разработан как аналог той части белка миелина, против которой направлена атака аутоиммунных Т-лимфоцитов. Глатирамер ацетат подавляет аутоиммунную реакцию за счет запуска продукции противовоспалительных белков-цитокинов и активации Т-супрессоров: Т-лимфоцитов, специализирующихся на подавлении иммунных реакций. С иммунологической точки зрения данный механизм действия представляется достаточно сомнительным, и неоднократно подвергался критике.
Снижение количества и площади очагов поражения при терапии Копаксоном наблюдается не ранее чем, через 6-7 месяцев после начала терапии. Обзор результатов клинических исследований Копаксона, опубликованный в 2003 г, не подтвердил наличия какого-либо положительного эффекта от назначения Копаксона при рассеянном склерозе. Однако более поздние исследования показали некоторую эффективность препарата в ряде ситуаций. С точки зрения соотношения стоимость/эффективность, Копаксон является самым невыгодным из всех препаратов, применяемых для лечения рассеянного склероза.
Перечень препаратов, которые относятся к группе иммуносупрессантов, достаточно велик. Одним из новых лекарственных средств этой группы является митоксантрон.
Митоксантрон - препарат, нередко применяемый также для лечения злокачественных новообразований, химически связывается с ДНК, вызывая гибель клеток.
Эффективность митоксантрона при рассеянном склерозе обусловлена снижением активности аутоиммунного процесса за счет гибели части лимфоцитов и макрофагов и снижения секреции провоспалительных белков-цитокинов. Митоксантрон стимулирует функциональную активность Т-супрессоров, снижает продукцию патологических антител В-лимфоцитами и уменьшает деградацию миелина макрофагами.
В настоящее время у пациентов с высокой активностью рассеянного склероза активно исследуется эффективность комбинированной схемы лечения, при которой за индукцией митоксантроном (3 ежемесячных введения) следует многолетнее назначение ИФНβ.
Обзор результатов клинических исследований эффективности митоксантрона при рассеянном склерозе, опубликованный в 2005 г, подтвердил эффективность препарата при рецидивирущем-ремиттирующем и вторично-прогрессирующем рассеянном склерозе. С точки зрения соотношения стоимость/эффективность, митоксантрон является самым выгодным из всех препаратов, применяемых для лечения рассеянного склероза.
Однако следует помнить, что продолжительность его применения ограничена 2-3 годами, после чего применение митоксантрона невозможно вследствие развития серьезных токсических эффектов.
Т - клеточная аутовакцинация
В последние годы отдельные исследователи изучают безопасность и терапевтическую эффективность у пациентов с рассеянным склерозом метода так называемой Т-клеточной аутовакцинации. Суть метода заключается в получении у пациента образца лейкоцитов и их стимуляции вне организма клетками нервной ткани (как правило, полученными от крупного рогатого скота). При этом происходит преимущественное размножение Т-лимфоцитов, способных реагировать с миелином, аналогичных аутоиммунным Т-лимфоцитам. После стимуляции, полученные в лаборатории Т-лимфоциты, облучают высокими дозами радиации и вводят пациенту. Облученные клетки не способны к размножению. Однако они могут быть распознаны иммунной системой пациента как чужеродные клетки, следствием чего является индукция иммунного ответа против них. Поскольку имевшиеся у пациента аутоиммунные Т-лимфоциты аналогичны облученным клеткам, развившаяся иммунная реакция может привести также и к их частичному уничтожению, ослабляя, таким образом, активность патологического процесса.
Обстоятельством, снижающим терапевтическую эффективность данного метода, является тот факт, что патологические иммунные реакции, лежащие в основе прогрессирования рассеянного склероза, чрезвычайно разнообразны, и поэтому добиться идентичности получаемых при стимуляции вне организма клеток тем, которые присутствуют в организме, невозможно. Кроме того, Т-клеточная аутовакцинация воздействует лишь на одно звено патологического процесса, не влияя непосредственно на активность макрофагов и провоспалительное микроокружение в нервной ткани.
Ввиду этого, несмотря на оригинальность идеи, данные клинических испытаний пока не подтверждают высокой эффективности этого подхода.
Трансплантация кроветворных стволовых клеток (ТКСК)
К сожалению, существующие методы лекарственной терапии имеют весьма ограниченную эффективность у пациентов с прогрессирующим течением рассеянного склероза. В связи с этим в последние годы при лечении рассеянного склероза все чаще применяют высокодозную иммуносупрессивную терапию с трансплантацией кроветворных стволовых клеток.
Высокодозная терапия позволяет обеспечить немедленный эффект за счет уничтожения аутоиммунных Т-лимфоцитов и снятия остроты иммунного воспаления. Долгосрочный эффект трансплантации кроветворных стволовых клеток заключается в репрограммировании иммунной системы, связанном с устранением дефекта в иммунной системе, поддерживающего прогрессирование рассеянного склероза.
С 1997 года высокодозная иммуносупрессивная терапия с трансплантацией кроветворных стволовых клеток выполнена более чем 300 пациентам с рассеянным склерозом. Как показывают результаты клинических исследований, с помощью этого метода удается остановить прогрессирование заболевания у подавляющего большинства пациентов.
В целом, исследования показывают, что высокодозная терапия с трансплантацией кроветворных стволовых клеток наиболее эффективна у молодых пациентов с быстро прогрессирующим заболеванием в ранних стадиях, когда основным механизмом развития заболевания является аутоиммунное воспаление. В более поздних стадиях рассеянного склероза преобладают нейродегенеративные процессы, и эффективность трансплантации снижается. Важным обстоятельством является то, что после проведения трансплантации кроветворных стволовых клеток пациенты не нуждаются в каком-либо поддерживающем лечении.
Анализ современных подходов к терапии рассеянного склероза свидетельствует об отсутствии на сегодняшний день "золотого стандарта" в лечении данного заболевания. В этих условиях предпочтение следует отдавать тем методам, эффективность которых доказана клиническими испытаниями. В свете этого, особого внимания заслуживает метод высокодозной терапии с трансплантацией кроветворных стволовых клеток, как позволяющий достичь высокой частоты стабилизации или улучшения в течении заболевания при отсутствии необходимости в поддерживающем лечении. Исследования, посвященные изучению новых методов лечения рассеянного склероза, продолжаются во многих странах.
Обзор подготовлен зав. лабораторией клеточных технологий Национального медико-хирургического центра им. Н.И Пирогова к.м.н. Ивановым Р.А.
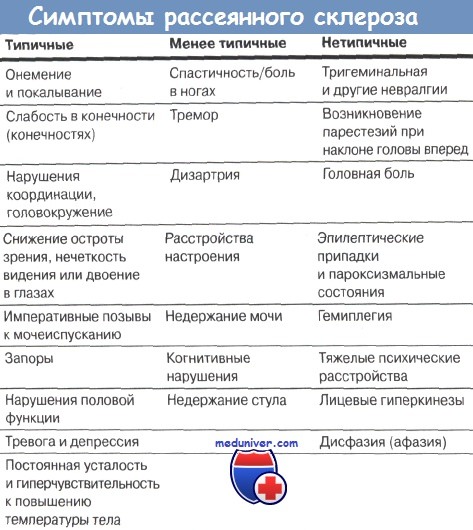
Ключ к успешному лечению больных с рассеянным склерозом находится в понимании разнообразных иммунологических, неврологических, психологических и социальных проблем, связанных с этим заболеванием. Особое внимания следует обратить на:
• тип течения рассеянного склероза: рецидивирующе-ремигтирующий, первично-прогрессирующий, рецидивирующе-емиттирующий с последующим прогрессирова-нием (вторично-рогрессирующий) и прогрессирующий с обострениями;
• тяжесть болезни;
• широкий спектр встречающихся симптомов;
• множество факторов, способных вызывать симптомы, не связанные с обострением рассеянного склероза.
Хотя гемиплегия, эпилептические припадки и афазия иногда и встречаются при рассеянном склерозе, они не типичны для него, и их появление требует пересмотра диагноза. Подтвердить клинический диагноз рассеянного склероза позволяют магнитно-резонансная томография, исследования спинномозговой жидкости и зрения. Магнитно-резонансная томография в большей степени служит диагностическим целям, чем мониторированию прогрессирования заболевания.
Причиной рецидивирующе-ремиттирующей симптоматики могут быть другие иммунные и инфекционные болезни (например, системная красная волчанка, саркоидоз, СПИД), а также коагулопатии и эмболии. Клинику рассеянного склероза способны имитировать компрессионные или дегенеративные поражения спинного мозга и ствола головного мозга.
От врача требуется умение объяснить и обсудить с больными новые способы терапии, возможность лечить отдельные симптомы заболевания, а также способность разбираться в проблемах, связанных с трудоустройством и семейными взаимоотношениями пациента. Для большинства больных предпочтительны регулярные осмотры врача. Каталог детских врачей и клиник Москвы позволит вам быстро найти опытного врача невролога.
Особое значение придается объективизации обострений или хронического прогрессирования заболевания, что может быть важно при отборе пациента для назначения определенного препарата или участия в клинических испытаниях. Сами больные часто судят о прогрессировании болезни лишь на основании оценки своих двигательных функций, игнорируя степень утомляемости, расстройств со стороны органов таза или нарушений памяти.
У 10—20% больных рассеянный склероз имеет доброкачественное, "мягкое" течение, которое не приводит к тяжелым ограничениям жизнедеятельности. После установления диагноза такие больные живут в среднем еще 35—40 лет. Необходимость в посторонней помощи при ходьбе возникает в среднем через 16 лет. Через 10 лет после начала заболевания рецидивирующе-ремиттирующее течение приблизительно в половине случаев становится вторично-прогрессирующим, что ухудшает прогноз. Около 20% больных с самого начала имеет первично-прогрессирующее течение болезни.
При резком ухудшении состояния больного чрезвычайно важно определить, являются ли симптомы "обострения" заболевания истинно неврологическими или они вызваны интеркуррентным заболеванием или психогенно обусловлены, представляя "крик о помощи". Интеркуррентная инфекция, повышение температуры тела, повышение температуры окружающей среды, повышенная чувствительность к телесным ощущениям и депрессия — все эти состояния могут вызывать так называемые "псевдообострения".
Лечебные воздействия в таких случаях должны быть направлены на устранение инфекции или неблагоприятных психосоциальных воздействий. Многие "острые атаки", преимущественно на первом году заболевания, объясняются повышенной восприимчивостью больных к телесным симптомам и тревожностью. Прежде чем связывать ухудшение состояния с экзацербацией болезни, важно исключить сопутствующую вирусную респираторную инфекцию и асимптомную инфекцию мочевыводящих путей, а также объективизировать неврологические нарушения.
Необходимый в сомнительных случаях период наблюдения за больным не нанесет ему вреда, поскольку кортикостероиды, хотя и уменьшают воспалительные реакции и соответствующие симптомы поражения центральной нервной системы при обострении, не влияют на последующее течение заболевания.
При обострениях, проявляющихся "мягкой" симптоматикой, например, чувством онемения и покалывания, требуется лишь подтвердить эти симптомы, успокоить больного и порекомендовать ему отдых.
В случаях, когда возникшие при обострении симптомы сильно беспокоят больного и нарушают его жизнедеятельность, назначают пероральный курс кортикостероидов:
Преднизолон или преднизон 75 мг внутрь 1 р/сут (утром) в течение 4 дней, затем 50мг/сут в течение 4 дней и затем 25 мг/сут в течение 4 дней.
Такая схема позволяет больным лечиться амбулаторно. Однако при этом у них особенно легко возникают симптомы эмоциональной лабильности, связанные с приемом кортикостероидов. Некоторые больные становятся стероиднозависимыми.
Лечение тяжелого обострения, сопровождающегося развитием ретробульбарного неврита со снижением остроты зрения, параплегией или стволовой симптоматикой, рекомендуется проводить в стационарных условиях путем внутривенного введения метилпреднизолона (прошел клинические испытания). Такое лечение может осуществляться и в условиях дневного стационара.
Метилпреднизолон 0,5 г в/в капельно в течение 2 ч 1 р/сут на протяжении 5 дней или 1 г в/в капельно в течение 3 ч 1 р/сут на протяжении 3 дней.
Во время лечения необходим тщательный клинический и инструментальный контроль за больным в связи с возможностью развития аритмий или анафилактических реакций, особенно при использовании высоких доз. Другими частыми осложнениями являются психические расстройства, нарушения со стороны желудочно-кишечного тракта и ухудшение сна. Проводить подобный курс корти-костероидов по возможности следует не чаще чем один раз в шесть месяцев, для предупреждения остеопороза и такого, хотя и редкого осложнения, как асептический некроз головки бедренной кости.
В стационарных условиях доступны также физические методы лечения, трудотерапия, диетотерапия, психологическая помощь и социальное консультирование.
Какой бы ни была этиология рассеянного склероза, его патогенетические механизмы связаны с аутоиммунными нарушениями, на уменьшение которых и направлено лечение. Для этих целей предложено очень большое число препаратов, начиная от иммунодепрессантов широкого спектра действия до недавно появившихся иммуномодуляторов, селективно модифицирующих продукцию цитокинов при демиелинизации.
Применение как иммуномодуляторов, так и иммуносупрессоров психологически тяжело для больных. Эти лекарственные средства могут уменьшить частоту обострений и замедлить прогрессирование болезни, но они не устраняют непосредственные симптомы болезни. При этом пациент обычно замечает лишь повторное развитие обострений и нарастание симптоматики, что заставляет его разувериться в пользе лечения. Такие неблагоприятные проявления, как недержание мочи или падения, часто остаются, что только укрепляет пациента в его мнении. От врача требуются настойчивая разъяснительная работа и поддержка больного. Возникновение первого после начала иммуномодулирующей терапии обострения всегда воспринимается психологически тяжело.
Опубликованные результаты клинических испытаний подтвердили, что бета-интерферон, натуральный белок с противовирусными и иммуномодулирующими свойствами, способен уменьшать частоту и тяжесть обострений, а также количество и размеры очагов демиелинизации в мозге по данным магнитно-резонансной томографии. Остается неясным, в какой степени бета-интерферон может предупреждать развитие стойких ограничений жизнедеятельности. Однако установлено, что при его применении частота обострений сокращается в среднем на одну треть, их тяжесть уменьшается, а скорость прогрессирования заболевания замедляется.
Подобные результаты получены и при использовании препарата глатирамера, представляющего собой синтетическую смесь из полипептидов, близких по структуре к основному белку миелина.
Доказательства, послужившие основанием для широкого применения иммуномодуляторов, были накоплены в ходе большого числа морфологических, нейрорентгенологических и нейропсихологических исследований, в ходе которых изучались процессы демиелинизации и повреждения клеток головного мозга на ранних стадиях болезни. Эти препараты назначает невролог. Согласно требованиям, закрепленным в Pharmaceutical Benefits Scheme, иммуномодуляторы используются лишь в следующих случаях:
• рецидивирующе-ремиттирующее течение рассеянного склероза;
• больной относится группе амбулаторных ("ходячих") больных, не требующих посторонней помощи или ухода;
• за предшествующие два года отмечалось не менее двух обострений;
• диагноз подтвержден данными магнитно-резонансной томографии.
Возможные побочные действия бета-интерферона включают гриппоподобные явления, кожные реакции в месте введения и депрессию. Обычно через несколько месяцев они проходят. Анализы крови могут обнаруживать изменения биохимических показателей функции печени, лейко- и тромбоцитопению, тиреоидные аутоантитела. У ряда больных выявляются нейтрализующие антитела к бета-интерферону в низких или высоких титрах, способные, как предполагают, снижать его эффективность.
Побочные эффекты глатирамера включают локальные боли в месте инъекции и труднообъяснимую постинъекционную реакцию в виде появления пугающего больного, хотя и безопасного ощущения удушья и дискомфорта в груди.
Выбор иммуномодулятора осуществляет невролог совместно с врачом иммунологом (//gorps.ru/doctors/immunolog/), анализируя результаты клинических испытаний в различных группах больных и учитывая образ жизни пациента, его возможность делать самому себе инъекции и его медицинский анамнез, в том числе наличие кожной, психической, гематологической патологии, заболеваний печени и щитовидной железы. Все больше больных сами изучают литературу и принимают участие в выборе иммуномодулирующего препарата.
Иммунодепрессанты назначают некоторым больным с первично- или вторично прогрессирующим рассеянным склерозом либо тем больным, которым не помогла иммуномодулирующая терапия. Следует сопоставить их положительный эффект при рассеянном склерозе с негативным действием на здоровье в целом. Помимо всего прочего, опасно применять иммуносупрессоры у больных с рецидивирующей инфекцией мочевыводящих путей.
Ограниченное число исследований показало, что малые дозы метотрексата могут замедлять скорость прогрессирования рассеянного склероза. Однако из-за его высокой токсичности решение о назначении этого препарата следует хорошо взвесить. В начале терапии необходимо ежемесячно проводить полные анализы крови и оценивать биохимические показатели функции печени.
Метотрексат 7,5 мг внутрь 1 р/нед в один и тот же отведенный для этого день + фолиевая кислота 5 мг п/о 1 р/нед спустя 3 дня после приема метотрексата.
Азатиоприн проходил клинические испытания в период до появления магнитно-резонансной томографии, однако метаанализ ранее проведенных исследований показал, что оказываемое им положительное действие сопоставимо с эффектом от применения иммуномодуляторов у тех пациентов, которым иммуномодуляторы не показаны или не помогли. В начале лечения необходимо ежемесячно проводить полный анализ крови и исследовать биохимические показатели функции печени.
Азатиоприн от 50 до 150 мг внутрь 1 р/сут.
Клиническими испытаниями подтверждены положительные результаты применения митозантрона, который может стабилизировать тяжелое и прогрессирующее течение болезни. Этот препарат относится к средствам большой химиотерапии и может быть назначен лишь после консультации с онкологом.
Митозантрон 12мг/м2 в/в 1 р/Змес.
Помимо обычных для цитостатиков побочных эффектов (выпадение волос, подверженность инфекциям, гепатотоксичность, угнетение кроветворения, повышение риска неопластических заболеваний), он может оказывать также и кардиотоксическое действие. Эти осложнения являются дозозависимыми и ограничивают безопасный период применения митозантрона двумя годами. Его положительный эффект сохраняется в течение еще одного года после отмены. Больным необходимо исследовать и контролировать сердечную деятельность. Лечение этим препаратом в настоящее время рассматривается как "терапия отчаяния" для очень тяжелых больных.
Актуальность проблемы
Рассеянный склероз (РС) — воспалительное заболевание спинного и головного мозга, являющееся следствием взаимодействия между неопределенными факторами внешней среды и предрасполагающими генами. При РС происходит несколько патологических процессов, включающих иммунную систему, Т- и В- клеточно опосредованные механизмы, демиелинизацию, ремиелинизацию, активацию микроглии и хроническую нейродегенерацию. Клиническое течение характеризуется атаками неврологической дисфункции с восстановлением, атаками, оставляющими персистирующие дефициты, и прогрессированием, приводящим к перманентной потере когнитивного и физического функционирования.
РС имеет несколько клинических фенотипов, включая релапсирующе-ремиттирующий, первичнопрогрессирующий, вторичнопрогрессирующий и прогрессивно-релапсирующий. За развитие перманентной длительной инвалидности ответственно прогрессирование после релапсирующе-ремиттирующего течения (Lublin F., Reingold S., 1996). Установлено, что с начала заболевания (обычно в молодом возрасте) до необходимости оказания посторонней помощи, развития состояния, когда пациент не может встать с постели, и до смерти проходит в среднем 14; 24 и 45 лет соответственно, а с момента вторичного прогрессирования — 3; 12 и 30 лет соответственно (Scalfari A. et al., 2014).
С учетом этого в мире проводится активный поиск эффективных средств лечения при указанном заболевании. К сожалению, на данный момент не существует препаратов, исцеляющих от РС, все доступное лечение направлено на замедление его прогрессирования, снижение частоты обострений и облегчение симптоматики. К методам терапии, изменяющей течение болезни, относят препараты с иммуносупрессивными или иммуномодулирующими свойствами. Ниже перечислены некоторые их них.
Механизм действия интерферонов β до конца не выяснен. Интерфероны — это цитокины, которые продуцируются клетками в качестве антивирусного ответа, обладающие противовоспалительными свойствами. Рекомбинантные формы интерферонов- β, предположительно, прямо повышают концентрацию противовоспалительных агентов и вместе с этим уменьшают выработку провоспалительных цитокинов (Kieseier B.C., 2011).
Натализумаб является моноклональным антителом против α4-интегрина на поверхности лимфоцитов. Интегрин играет ключевую роль в процессах, с помощью которых лимфоциты получают доступ к мозгу путем пропуска через гематоэнцефалический барьер. Натализумаб блокирует действие α4-интегрина и, таким образом, лимфоциты перестают проходить в мозг и атаковать миелиновый протеин (Yednock T.A. et al., 1992).
Финголимод действует как функциональный антагонист сфингозин-1-фосфат рецепторов на лимфоцитах, что обусловливает снижение выхода лимфоцитов из лимфатических узлов. Таким образом предотвращается рециркулирование аутоагрессивных Т-клеток в центральной нервной системе (Mandala S. et al., 2002).
Алемтузумаб является моноклональным антителом против CD52-антигенов, экспрессируемых на лимфоцитах и моноцитах. Их эффекты при РС, предположительно, опосредованы изменениями в составе лимфоцитов и их исчерпанием. Причем, как установлено в исследованиях, возникающая лимфоцитопения не ассоциирована с высоким риском оппортунистических инфекций (Hill-Cawthorne G.A. et al., 2012).
Анализ исследований
I. Tramacere и соавторами (2015) опубликованы результаты нового Кокрановского систематического обзора, посвященного эффективности иммуномодулирующей и иммуносупрессивной терапии при релапсирующе-ремиттирующем РС. Авторский коллектив провел анализ всех релевантных рандомизированных контролируемых клинических испытаний, в которых изучены, кроме вышеперечисленных препаратов, митоксантрон (цитотоксический препарат), терифлуномид (ингибитор дигидрооротатдегидрогеназы), диметилфумарат (производное фумаровой кислоты), пегилированный интерферон β-1а, даклизумаб (моноклональное антитело против СD25-антигена, экспрессируемого на иммунных клетках), окрелизумаб (моноклональное антитело против СD20-антигена, экспрессированного на В- лимфоцитах), лаквинимод (иммуномодулятор), азатиоприн (иммуносупрессор) и глатирамера ацетат (иммуномодулятор).
Всего в анализ включили 39 исследований с общим участием 25 113 пациентов. Средний период наблюдения составил 24 мес. Из рассматриваемых работ 24 были плацебо-контролируемыми, 15 — с прямым сравнением препаратов. 51% всех исследований имели высокий, 41% — умеренный и лишь 8% — низкий риск системной ошибки. Результаты анализа для одного из изучаемых исходов представлены в таблице.
| Препарат | Количество обострений на 100 человек (в общей популяции в среднем 41–89 на каждые 100 человек) | Относительный риск обострений (95% доверительный интервал) | Количество участников (исследований), n | Качество доказательств |
|---|---|---|---|---|
| Алемтузумаб | 16–36 | 0,40 (0,31–0,51) | Не указано | Умеренное |
| Митоксантрон | 16–36 | 0,40 (0,20–0,76) | 51 (1) | Низкое |
| Натализумаб | 23–50 | 0,56 (0,43–0,73) | 942 (1) | Высокое |
| Финголимод | 23–50 | 0,63 (0,53–0,74) | 2355 (2) | Низкое |
| Диметилфумарат | 32–69 | 0,78 (0,65–0,93) | 2307 (2) | Умеренное |
| Иммуноглобулины | 32–69 | 0,78 (0,61–1,00) | 219 (3) | Очень низкое |
| Глатирамера ацетат | 33–71 | 0,80 (0,68–0,93) | 2416 (4) | Умеренное |
| Даклизумаб | 32–70 | 0,79 (0,61–1,02) | 621 (1) | Умеренное |
| Терифлуномид | 34–75 | 0,84 (0,72–0,99) | 2257 (2) | Низкое |
| Азатиоприн | 36–77 | 0,87 (0,58–1,31) | 59 (1) | Очень низкое |
| Интерферон β-1b | 40–87 | 0,98 (0,54–1,75) | Не указано | Очень низкое |
| Интерферон β-1а | 38–83 | 0,93 (0,78–1,10) | 301 (1) | Умеренное |
Также результаты анализа свидетельствуют, что, кроме митоксантрона, алетузумаба и натализумаба, ни один препарат не оказывал влияние на ухудшение функционирования вследствие РС. Причем умеренный уровень эффективности продемонстрировал только натализумаб, у других двух препаратов она была низкой.
К сожалению, применение практически всех препаратов, включенных в обзор, ассоциировано с большим количеством пациентов, отказавшихся от лечения в связи с побочными эффектами. Проанализировать различия в побочных эффектах между препаратами не удалось в связи с недостаточным количеством данных. Кроме того, в исследованиях уделяли мало внимания тяжелым побочным эффектам, недостаточно освещали их в результатах, а сами эти данные были сильно гетерогенными.
Выводы
На основании полученной информации ученые заключили, что в контексте предотвращения обострений на протяжении первых 12 и 24 мес алемтузумаб, натализумаб и финголомид более эффективны, чем другие виды лечения. Эти препараты выбрали на основании статистической достоверности различий с плацебо и другими лекарственными средствами, а также на основании качества доказательств. В контексте влияния на ухудшение функционирования наибольшую эффективность продемонстрировал натализумаб. Такой вывод сделан только на основании сравнения с плацебо и качества полученных доказательств.
Вдобавок к этому авторы подчеркнули, что поскольку длительность заболевания составляет 30–40 лет, делать выводы об эффективности препаратов в отдаленной перспективе на основании данных исследований со средним периодом наблюдения 24 мес не представляется возможным. Это же касается и переносимости лечения. Таким образом, существует необходимость в проведении дальнейших исследований в этой сфере. Отмечено также, что около 70% исследований спонсировали фармацевтические компании, что могло повлиять на конечные результаты.
Читайте также:


