Бас с поясничным дебютом
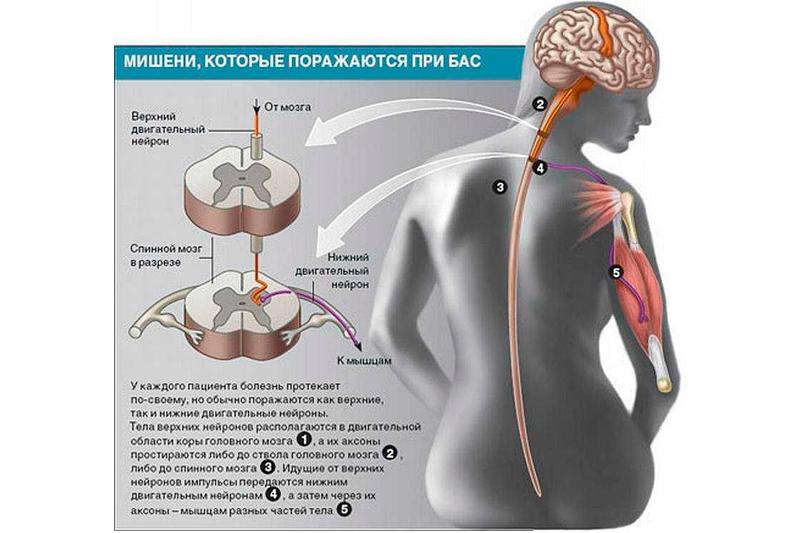
Боковой амиотрофический склероз (БАС) — это неизлечимое прогрессирующее заболевание ЦНС, при котором у больного наблюдается поражение верхних и нижних двигательных нейронов, что провоцирует атрофию мышц и паралич. Частота данной патологии составляет около 2-7 случаев заболевания на 100 тысяч человек. Чаще всего болезнь диагностируют у больных старше 50 лет.
- Классификация бокового амиотрофического склероза
- Клиническая картина бокового амиотрофического склероза
- Этиология и патогенез бокового амиотрофического склероза
- Диагноз бокового амиотрофического склероза
- Дифференциальный диагноз
- Лечение бокового амиотрофического склероза
- Прогноз при боковом амиотрофическом склерозе
Классификация бокового амиотрофического склероза
Единой комплексной классификации БАС ученые на сегодняшний день еще не создали. Существует несколько подходов к классификации болезни. Например, североамериканский подход предусматривает выделение следующих видов БАС: спорадический, семейный, спорадический эндемический. Классификация бокового амиотрофического склероза предусматривает следующие формы заболевания: бульбарную, пояснично-крестцовую, шейно-грудную и первично-генерализованную. Выделяют также несколько вариантов болезни: смешанный, пирамидный и сегментарно-ядерный.
Клиническая картина бокового амиотрофического склероза
К наиболее распространенным начальным симптомам заболевания относятся крампы (болезненные мышечные спазмы), вялость и слабость в области дистальных отделов рук, бульбарные расстройства, атрофия мышц ног, слабость в плечевом поясе. Кроме того, для разных вариантов заболевания характерны различные клинические проявления.
- Классический вариант БАС (с шейным дебютом). Первым признаком заболевания считается формирование ассиметричного парапареза с пирамидными знаками. Кроме того, появляется спастический парапарез, который сопровождается гиперрефлексией. Со временем у больного начинают проявляться признаки бульбарного синдрома.
- Сегментоядерный вариант БАС (с шейным дебютом). Эта разновидность заболевания проявляется формированием асимметричного вялого парапареза, который сопровождается гипорефлексией. При этом у пациентов на некоторое время сохраняется возможность передвигаться самостоятельно.
- Классический вариант БАС (с диффузным дебютом). Этот вариант патологии начинает проявляться обычно вялым асимметричным тетрапарезом. Кроме него, у больных диагностируют также бульбарный синдром, который проявляется в форме дисфагии и дисфонии. У больного нередко наблюдается резкое снижение массы тела, одышка и быстрая утомляемость.
- Классический вариант БАС (с поясничным дебютом). Начинается этот вариант патологии с нижнего вялого парапареза. Позднее добавляются такие симптомы, как гипертонус мышц и гиперрефлексия. В начале заболевания пациенты еще могут самостоятельно двигаться.
- Пирамидный вариант БАС (с поясничным дебютом). Этот вид заболевания начинается с возникновения нижнего асимметричного парапареза, к которому затем присоединяется верхний спастический парапарез.
- Классический вариант БАС (в начале заболевания наблюдается бульбарный паралич). Для этого заболевания характерными являются дисфагия, дисфония, дизартрия, верхний и нижний асимметрические парапарезы. Больной стремительно теряет вес, у него наблюдаются дыхательные нарушения.
- Сегментоядерный вариант БАС (с бульбарным параличем). Для этого варианта заболевания характерными считаются назофония, дисфагия, дизартрия. Как и в предыдущем случае, больной теряет массу тела и у него появляются дыхательные патологии.
Этиология и патогенез бокового амиотрофического склероза
Точные причины бокового амиотрофического склероза еще исследуются учеными. Однако можно назвать несколько факторов, провоцирующих заболевание. Например, около 5% заболеваний имеют наследственную этиологию. Не меньше 20% случаев связаны с мутациями гена супероксиддисмутазы-1. Ученые доказали, что важную роль в появлении болезни играет высокая активность глутаматергической системы. Дело в том, что избыток глутаминовой кислоты провоцирует перевозбуждение и внезапную гибель нейронов. Доказан также молекулярно-генетический механизм возникновения патологии. Он обусловлен повышением в клетках уровня ДНК и РНК, что в итоге ведет к нарушению синтеза белка.
Учены выделяют также несколько предрасполагающих факторов, которые играют немаловажную роль в появлении БАС. В первую очередь к таким факторам относят возраст. Дело в том, что болезнь обычно развивается у пациентов в возрасте 30-50 лет. Стоит помнить, что всего около 5% заболевших имеют наследственную предрасположенность к БАС. В подавляющем количестве случаев заболевания БАС причины патологии установить не удается.
Для раннего течения заболевания характерны такие симптомы, как судороги, подергивания, онемение мышц, затрудненная речь, слабость в конечностях. Поскольку такие симптомы характерны для многих неврологических заболеваний, диагностировать БАС на ранней стадии затруднительно. В большинстве случаев диагностировать болезнь удается на стадии мышечной атрофии.
В зависимости от поражения болезнью разных частей тела, выделяют БАС конечностей и бульбарный БАС. В первом случае у больных ухудшается гибкость в голеностопе, появляется неловкость при ходьбе, они начинают спотыкаться. Бульбарный БАС проявляется затрудненной речью (гнусавость, трудности с глотанием). Вскоре больному становится трудно передвигаться или он вовсе больше не может двигаться самостоятельно. Обычно болезнь не влияет губительно на умственные способности пациента, однако приводит к сильной депрессии. От появления первых симптомов до летального исхода в большинстве случаев проходит около трех-пяти лет.
Диагноз бокового амиотрофического склероза
Так как БАС является неизлечимым заболеванием, которое стремительно сокращает жизнь человека, обследование пациента должно быть комплексным и точным. Крайне важно поставить правильный диагноз пациенту, чтобы вовремя приступить к купированию его основных симптомов, поскольку это может продлить жизнь больного. План обследования обычно включает сбор анамнеза жизни и заболевания, неврологический и физикальный осмотр, МРТ спинного и головного мозга, ЭМГ, лабораторные анализы.
-
Сбор анамнеза и осмотр
Диагностика заболевания начинается с детального опроса пациента. А именно, врачу необходимо уточнить, жалуется ли больной на мышечные спазмы и подергивания, слабость и скованность, нарушение движения в кистях, речи, ходьбы, глотания, слюноотделения, частую нехватку воздуха, снижение массы тела, быструю утомляемость, одышку во время выполнения физических упражнений. Кроме того, врач должен поинтересоваться, не замечал ли пациент двоения в глазах, ухудшение памяти, чувства ползания мурашек на телу, нарушения мочеиспускания. Обязательно нужно поинтересоваться у пациента его семейным анамнезом — нет ли у него родственников, больных хроническими нарушениями движений.
Основной целью физикального осмотра является оценка конституции пациента, его взвешивание, измерение роста, вычисление индекса массы тела. Неврологический осмотр обычно предусматривает нейропсихологическое тестирование. Во время оценки бульбарных функций врач обращает внимание на тембр голоса, скорость речи, глоточный рефлекс, наличие атрофий языка, парезов мягкого неба. Кроме того, во время осмотра проверяется сила трапециевидных мышц.
Инструментальные методы исследования
Основным инструментальным методом диагностики заболевания считается игольчатая ЭМГ. Данная методика позволяет выявить такие признаки заболевания, как острая или хроническая денервация. На ранних стадиях болезни применять стимуляционную ЭМГ неэффективно, поскольку она не выявляет заметных признаков БАС.
В процессе диагностики заболевания врачи также применяют методы нейровизуализации. Большое значение в дифференциальной диагностике БАС играет МРТ спинного и головного мозга. Во время проведения МРТ у 17-67% пациентов удается выявить симптомы дегенерации пирамидных трактов, атрофию моторной коры мозга. Однако стоит отметить, что данная методика оказывается неэффективной во время диагностики заболевания у пациентов с бульбарным синдромом.
В процессе диагностики БАС проводится множество лабораторных анализов. В частности, врачи могут назначить клинический и биохимический анализы крови, исследование ликвора, серологические исследования. Однако единственным эффективным и достоверным методом анализа считается все же проведение молекулярно-генетического анализа. Наличие у гена супероксиддисмутазы-l мутаций считается подозрением для БАС.
Дифференциальный диагноз
Поскольку симптомы бокового амиотрофического склероза схожи во многом с проявлениями других неврологических патологий, врачи обязательно проводят дифференциальную диагностику. Точнее всего поставить диагноз можно с помощью МРТ головного мозга и позвоночника. Прежде всего БАС необходимо дифференцировать от болезней мышц, к которым можно отнести дистрофическую миотонию Россолимо-Штейнерта-Куршмана, миозит с клеточными отклонениями, окулофаренгиальную миодистрофию.
Отличить БАС также нужно от патологий спинного мозга:
- хроническая вертеброгенная ишемическая миелопатия;
- бульбоспинальная амиотрофия Кеннеди;
- сирингомиелия;
- опухоли;
- семейная спастическая параплегия;
- хронический лимфолейкоз;
- дефицит гексозаминидазы;
- лимфома.
Дифференциальная диагностика необходима также для того, чтобы отличить заболевание от системных патологий, поражений нервно-мышечного синапса, патологий головного мозга вроде мультисистемной атрофии, дисциркуляторной энцефалопатии, сирингобульбии.
Лечение бокового амиотрофического склероза
Главными целями лечения бокового амиотрофического склероза считается замедление развития заболевания, а также устранение его симптомов, которые существенно ухудшают качество жизни больного. Следует помнить, что БАС — серьезное неизлечимое заболевание, которое сокращает продолжительность жизни человека. Именно поэтому врач имеет право сообщить пациенту диагноз только после комплексного и тщательного осмотра.
Лечение заболевания включает медикаментозную и немедикаментозную терапию. Последняя подразумевает режимные мероприятия. Больной должен ограничить физические нагрузки, которые могут ускорить прогрессирование БАС. Кроме того, очень важно правильно и полноценно питаться. Лекарственная терапия подразделяется на два вида: патогенетическую и паллиативную.
Патогенетическая терапия
На сегодняшний день единственным препаратом, который способен замедлять прогрессирование БАС, является рилузол. Доказано, что его прием способен продлить жизнь больного в среднем на три месяца. Этот препарат показан больным, длительность болезни у которых составляет меньше 5 лет. Ежедневно пациент должен получать 100 мг препарата. Для того, чтобы избежать риска появления лекарственного гепатита, каждые три месяца необходимо проверять уровень АСТ, АЛТ и ЛДГ. Поскольку у мужчин и курильщиков концентрация рилузола в крови ниже, им стоит либо ограничить себя в курении, либо вовсе избавиться от этой вредной привычки. Принимать препарат необходимо будет пожизненно.
Ученые неоднократно пытались применять для патогенетической терапии и другие препараты. Однако такие эксперименты не оказались эффективными. Среди них были:
- ксалипроден;
- метаболические средства;
- антиконвульсанты;
- противопаркинсонические средства;
- антибиотики;
- антиоксиданты;
- блокаторы кальциевых каналов;
- иммуномодуляторы.
Не доказана также эффективность приема высоких доз церебролизина, не смотря на то, что этот препарат способен немного улучшать состояние больных.
Паллиативная терапия
Паллиативная терапия предназначена для устранения комплекса симптомов заболевания и улучшения тем самым качества жизни пациента. Для устранения тех или иных симптомов БАС применяются следующие методики:
- спастичность — назначают баклофен и тизанидин;
- фаскуляции (подергивание мышц) — помимо баклофена и тизанидина назначают также карбамазепин;
- депрессия и эмоциональная лабильность — флуоксетин и амитриптилин;
- нарушение ходьбы — для устранения этого симптома показаны ходунки, трости и коляски;
- деформация стоп — больному стоит носить ортопедическую обувь;
- парез шеи — показан жесткий или полужесткий головодержатель;
- тромбозы вен нижних конечностей — назначается эластичное бинтование ног;
- быстрое утомление — выполнение гимнастических упражнений, а также прием амантадина и этосуксимида;
- плечелопаточный периартроз — назначаются компрессы с прокаином, раствором диметилсульфоксида, гиалуронидазом;
- синдром оральной гиперсекреции — для устранения этого симптома показаны коррекция обезвоживания, портативные отсосы, муколитики и бронхолитики;
- синдром апноэ во время сна — флуоксетин;
- дыхательные нарушения — назначается периодическая неинвазивная ИВЛ;
- дисфагия — соблюдение специальной диеты (исключение блюд с твердыми и плотными компонентами, предпочтение протертым блюдам, суфле, кашам, пюре);
- дизартрия — прием миорелаксантов, применение аппликаций льда на язык, использование электронных пишущих машинок, специальной компьютерной системы набора, соблюдение речевых рекомендаций, составленных Британской ассоциацией БАС;
- слюнотечение — регулярная санация ротовой полости (необходимо чистить зубы трижды в день, часто полоскать полость антисептическими растворами), ограничение употребления кисломолочных продуктов, прием атропина и амитриптилина.
Для улучшения метаболизма мышц больному БАС могут быть назначены следующие лекарства: креатин, карнитин, раствор левокарнитина, триметилгидразиния пропионат. Показана пациентам также поливитаминная терапия, которая предусматривает прием поливитаминов (нейромультивит, мильгамм) и тиоктовой кислоты.
У большинства пациентов с БАС болезнь сопровождается серьезными двигательными нарушениями вплоть до ограничения подвижности. Разумеется, это доставляет сильный дискомфорт больному, который постоянно нуждается в помощи других людей. Устранить некоторые двигательные нарушения помогают ортопедические методики коррекции. Врачу необходимо объяснить пациенту, что применение вспомогательных средств не свидетельствует о его инвалидности, а только уменьшает трудности, обусловленные заболеванием.
Наиболее опасным для жизни симптомом заболевания по праву считается дыхательная недостаточность. Самыми ранними ее симптомами будет утренняя разбитость, яркие сны, дневная сонливость, неудовлетворенность сном. Для обнаружения дыхательной недостаточности на ранней стадии проводятся полисомнография и спирография. Для устранения апноэ показан прием медикаментов и неинвазивная вентиляция легких. Доказано, что эти методики могут продлить жизнь пациента на один год. Если же у пациента есть необходимость во вспомогательном дыхании в течение более 20 часов, врач ставит вопрос о полном переходе на инвазивную вентиляцию легких.
Больные, которые прошли первичный осмотр или повторное заключение о заболевании, должны пребывать под амбулаторным наблюдением. По мере появления каких-либо новых симптомов они также должны получать квалифицированные консультации. Большинство медикаментов пациенты должны принимать регулярно. Только витамины и миотропные препараты принимаются курсами поэтапно.
Каждые три месяца больному необходимо проходить процедуру спирографии. Если он регулярно принимает рилузол, ему нужно каждые полгода определять активность ЛДГ, АСТ и АЛТ. Если у пациента наблюдается дисфагия, следует периодически измерять уровень глюкозы в крови и трофический статус. У пациентов есть выбор режима лечения: они могут находиться как дома, так и пребывать в хосписе.
Прогноз при боковом амиотрофическом склерозе
Прогноз для больных БАС во многом зависит от течения болезни. Доказано, что около 80-90% пациентов, у которых наблюдаются тяжелые дыхательные осложнения, умирают в течение 3-5 лет после проявления первых признаков болезни. У остальных 10% пациентов наблюдается доброкачественное течение болезни. Длительность заболевания значительно сокращается при наличии следующих факторов: возраст пациента меньше 45 лет, бульбарный дебют БАС, быстрое прогрессирование болезни.
Г.Н. Левицкий (1,2,3), К.И. Почигаева (4), Е.Ю. Захарова (5),О.С. Левин (6)
Боковой амиотрофический склероз (БАС) – нейродегенеративное заболевание, сопровождающееся поражением центральных (ЦМН) и периферических мотонейронов (ПМН), прогрессирующим течением и неизбежным наступлением терминальной дыхательной недостаточности.
Эпидемиология
Заболеваемость БАС составляет 0,2 до 2,4, а распространенность - 0,8 до 7,3 случая на 100 000 в год. Лишь 7% больных БАС болеют дольше 5 лет, средняя продолжительность жизни составляет 2,5 года при бульбарном и 3,5 года при спинальном дебюте БАС (56).
Классификации и естественный патоморфоз БАС
БАС является самой распространенной (80%) формой болезни двигательного нейрона (БДН). По классификациям Hudson, а также Shwartz and Swash к БДН помимо БАС относят прогрессирующий бульбарный паралич (ПБП, изолированное поражение бульбарных мотонейронов – 9%), прогрессирующую мышечную атрофию (ПМА, 8%) и первичный боковой склероз (ПБС, 2%) - медленно прогрессирующе поражение ПМН или ЦМН мотонейронов, соответственно, а также псевдобульбарный паралич (прогрессирующее поражение ЦМН, контролирующих бульбарные функции – менее 1%) (30,50).
Соавтором обзора (Г.Н.Л.) проводилось собственное исследование естественного патоморфоза дебютов БАС у 147 больных. Так при грудном дебюте БАС достоверно раньше наступала дисфункция ипсилатеральной ноги, чем контралатеральной руки (4,6±2,1 и 11,8±6,9 мес, р = 0,009) и ипсилатеральной ноги при шейном дебюте БАС (4,6±2,1 и 10,7±5,2 мес, р = 0,0001). При шейном дебюте БАС, напротив, достоверно раньше наступала дисфункция контралатеральной руки, чем ипсилатеральной ноги (4,7±2,7 и 11,8±6,9 мес, р = 0,003) и контралатеральной руки при грудном дебюте (4,7±2,7 и 10,7±5,2 мес, р = 0,0001). Дыхательные нарушения наступали раньше при грудном, чем при шейном дебюте, однако различия не были достоверными (13,8±6,4 и 20,0±4,8 мес, р = 0,7). Сроки наступления бульбарных нарушений при шейном и грудном дебютах достоверно не различались (13,0±5,8 и 12,0±5,5 мес, р = 0,66). Таким образом, была доказана правомерность выделения грудного дебюта БАС (4).
По классификации О.А. Хондкариана (10) выделяют бульбарную, шейно-грудную, пояснично-крестцовую форму, генерализованную и высокую форму БАС. Генерализованная форма соответствует диффузному дебюту БАС, а высокая – псевдобульбарному параличу или первичному боковому склерозу. Грудной дебют БАС не выделяется. Такие формы БДН как ПБП, ПМА, ПБС в данной классификации не рассматриваются. В связи с этим авторы обзора рекомендуют пользоваться зарубежной классификацией дебютов БАС.
Клинико-электромиографические критерии диагностики БАС
При БАС не встречаются глазодвигательные нарушения (за исключением редкой апраксии закрывания глаз) и пролежни. Крайне редко возможны тазовые расстройства. Обычно они являются вторичными и связаны со слабостью мышц тазового дна. Чувствительные расстройства при БАС являются сопутствующими или связаны с нарушением кровоснабжения грубо атрофированных конечностей. Когнитивные нарушения более не являются отрицательным критерием диагностики БАС (51).
Согласно электромиографическим (ЭМГ) критериям Айрли Хаус признаками БАС считаются: 1) сочетание признаков острой и хронической денервации в клинически пораженных и/или непораженных мышцах (фибрилляции, положительные острые волны, фасцикуляции, а также увеличение амплитуды, длительности и полифазии потенциалов двигательных единиц) и разрежение паттерна рекрутирования; если у пациента выявлен один уровень, где сочетаются эти признаки, а на другом, клинически непораженном, уровне выявлены изолированные фасцикуляции, это также считается лабораторно-подтвержденным БАС (ранее, в ЭМГ критериях Ламберта, этого не допускалось); 2) снижение скоростей проведения по двигательным волокнам в пределах 10%; 3) отсутствие не характерных для БАС ЭМГ данных (блоки проведения, декремент, изменение чувствительных волокон). В настоящее время поправка к критериям Ламберта позволяет ускорять постановку диагноза (52).
Больным БАС показано проведение нейровизуализации (магнитно-резонансной томографии) в проекции дебюта заболевания и на соседнем (ростральном или вышележащем) уровне (например, шейного отдела и головного мозга при шейном дебюте или грудного и шейного отдела спинного мозга при поясничном дебюте) для исключения очаговых поражений спинного и головного мозга, которые могли бы вызвать симптомы, напоминающие БАС. МРТ пояснично-крестцового отдела позвоночника может проводиться для исключения корешковой патологии, но не патологии спинного мозга, который заканчивается на уровне Т12. В ряде случаев при БАС выявляется валлеровская дегенерация пирамидных трактов на уровне головного мозга (гиперинтенсивность в семиовальных центрах в режиме Т2) (4,51).
Больным БАС показана транскраниальная магнитная стимуляция, которая может выявить снижение времени центрального моторного проведения по кортиколюмбальным и/или кортикоцервикальным пирамидным трактам, а также снижение возбудимости моторной коры (4, 51).
Таблица 1. Уровень КФК при различных клинических характеристиках БАС
| Подгруппы больных | Активность КФК (ед/л) |
| Спинальный БАС | 398,5±392 |
| Бульбарный БАС | 147±58,2 |
| Классический вариант | 277,3±205,2 |
| Сегментарно-ядерный вариант | 508,8±479,2* |
| Пирамидный вариант | 121±62,4 |
* p 0,06 ). Проводится исследование эффективности НВЛ у больных бульбарным БАС, начавших терапию с ФЖЁЛ выше и ниже 65%. Больным с бульбарным БАС показана ранняя трахеостомия с целью выведения мокроты из трахеи портативным электроотсосом. Именно скопление мокроты в трахее и синдром оральной гиперсекреции мешают больным бульбарным БАС приспособиться к НВЛ. Необходимо специальное исследование, чтобы установить продлевает ли жизнь больным бульбарным БАС ранняя трахеостомия. Если БАС сочетается с хронической обструктивной болезнью легких, рекомендуется консультация пульмонолога с назначением дополнительной бронхолитической терапии. Истинная ФЖЁЛ, определяющая показания к началу НВЛ, у таких больных определяется при спирографии только после пробы с бронхолитиком. Получив рекомендацию невролога и пульмонолога по применению НВЛ, больному БАС следует попытаться получить аппарат НВЛ от государства, обратиться в профильную благотворительную организацию или приобрести прибор.
Коррекция двигательных нарушений
Коррекция двигательных нарушений при БАС проводится с помощью ортопедических устройств. Рекомендуется ходить с тростью, ходунками или пользоваться коляской во избежание травм. Можно пользоваться вспомогательными устройствами в быту (ричер-ухват, ложки и вилки с длинными и гибкими ручками, шины для улучшения разгибания кисти). При парезе разгибателей шеи рекомендуется головодержатель, и он обязателен во время еды. Стоподержатели в виде туторов неудобны, так как не улучшают подъема по лестнице и вызывают дискомфортное ощущение инородного тела в обуви, поэтому используют стоподержатели в виде ремня, одеваемого на голеностопный сустав с крючком для шнуровки обуви. С учетом быстрого прогрессирования болезни во многих случаях ортопедическая обувь не получила широкого применения. При выраженном тетрапарезе рекомендуется электроподъемник. Для профилактики подвывиха головки плечевой кости показано ношение рук на разгрузочной повязке 3-5 часов в день. При развитии болевого синдрома в плечевых суставах применяют физиотерапию, компрессы с димексидом, новокаином, лидазой, вольтареном и гидрокортизоном, блокады с гормональными препаратами и местными анестетиками. Для профилактики флеботромбозов у пациентов с обездвиженностью, отеками стоп или кистей, рекомендуется эластичное бинтование конечностей (4,5,7,40, 51).
Для коррекции спастичности применяются препараты, снижающие мышечный тонус (баклофен или тизанидин в терапевтических дозах на ночь). Возможно использование ботулотоксина (например, для расслабления сгибательной контрактуры кисти или локтя). Применяется лечебная гимнастика 10-15 минут 3 раза в день. При слабости мышц тазового дна рекомендуется его электростимуляция. Для профилактики ларингоспазма применяют диазепам 5 мг или лоразепам 2 мг на ночь (4).
Фасцикуляции и крампи при БАС могут быть болезненными, нарушать сон. По мере течения болезни пациент с БАС замечает, что там, где первоначально имели место фасцикуляции, затем развиваются парезы. Для уменьшения фасцикуляций рекомендуется карбамазепин 100 мг 2 раза в день. Этот препарат обладает дополнительным действием в виде стабилизации настроения, что также полезно больным БАС, в 50% случаев страдающим депрессией (4,44).
Коррекция эмоционально-волевых и психических нарушений
Для лечения когнитивных нарушений при БАС может быть использован антагонист NMDA-глутаматных рецепторов акатинола мемантин. В одном пилотном исследовании показано, что он может обладать и патогенетическим действием (18). При наличии апато-абулического симптома могут быть эффективны умеренные дозы психостимулятора отечественного производства семакса. Ранее показано, что препарат может улучшать эмоциональное состояние больных БАС (9).
Коррекция бульбарных нарушений
Наряду с нарушениями дыхания, фатальным симптомом БАС является нарушение глотания (дисфагия). Фатальность этого симптома связана не с риском развития недостаточности питания, а с риском аспирации и аспирационной пневмонии, которая смертельна в 50% случаев (22). Нарушение автоматического глотания слюны при БАС приводит к слюнотечению, при этом аспирация возможна и собственной слюной, что делает коррекцию и этого симптома жизненно важным.
Оценка риска аспирации проводится в помощью теста на дисфагию с пикфлуометрией. Больным делают пикфлуометрию, затем дают 5,10 и 20 мл нектара, затем жидкости, а затем пудинга и после каждого приема болюса делают пикфлуометрию. Оценивают эффективность и безопасность глотания. Появление кашля или уменьшение показателя пикфлуометрии на 5 л/мин после глотания являются признаками явной или скрытой аспирации. На Рисунке 2 представлено выполнение теста и выявление скрытой аспирации жидкостью (20).
Рисунок 1. Тест на дисфагию с пикфлуометрией.
Золотым стандартом лечения нарушений глотания, профилактики аспирационной пневмонии и алиментарной недостаточности является гастростомия. При БАС предпочтительна чрескожная эндоскопическая гастростомия (ЧЭГ), в связи с простотой и тем, что она может быть выполнена под местным обезболиванием. Показано, что ЧЭГ и энтеральное питание достоверно продлевают жизнь больным БАС, 38±17 мес в группе БАС с ЧЭГ и 30±13 мес в группе БАС без ЧЭГ (38). ЧЭГ желательно выполнять, пока ФЖЁЛ выше 50%. В процессе операции эндоскопически раздувается желудок, что может уменьшить экскурсию диафрагмы во время операции и привести к послеоперационным дыхательным расстройствам. ЧЭГ безопаснее всего проводить на фоне интраоперационной НВЛ (4).
Объем энтерального питания рассчитывается по формуле Харриса-Бенедикта, формуле действительного расхода энергии с учетом факторов активности, увечья и температуры по В.М. Луфту и А.Л. Костюченко (8). Очень важно, чтобы энтеральная смесь соответствовала современным стандартам, предполагающим калорическую плотность не менее 1 ккал/мл, низкое содержание лактозы или ее отсутствие, соотношение ккал/азот 130-180:1, осмолярность менее 300-340 мосмоль, отсутствие опасной стимуляции кишечной моторики, отсутствие генетически модифицированных компонентов (8) . Нормализация микрофлоры кишечника и его моторики достигается путем добавления в энтеральное питание пищевых волокон (например, Метамуцил, Резорс Файбер + 2,0 Нестле).
Следует отметить, что до 80% больных БАС отказываются от гастростомии. Установка назогастрального зонда не предохраняет от аспирации и снижает качество жизни больного БАС. Парентеральное питание растворами аминоплазмаля, липофундина, 40% глюкозы значительно дороже энтерального питания, должно проводиться в условиях хотя бы дневного стационара, чревато флеботромбозами, энцефалопатией. Внутривенные инфузии больным БАС, отказавшимся от гастростомии, должны проводиться исключительно на глюкозе. Введение хлорида натрия в условиях гипонатриемии может привести к центральному понтинному или экстрапонтинному миелинолизу (8). Кроме того, для профилактики аспирационной пневмонии больным БАС показаны внутримышечные (а при атрофии ягодичных мышц и мышц верхнего плечевого пояса) внутривенные инъекции антибиотиков цефалоспоринового ряда 5 дней каждого месяца. Показано, что назначение этих препаратов ассоциировано с увеличением продолжительности жизни больных БАС (35). Ранняя трахеостомия при бульбарном БАС также, очевидно, является профилактической мерой против аспирации.
Коррекция слюнотечения важна не только в связи с необходимостью уменьшения риска аспирации, но и в связи с тем, что слюнотечение значимо ухудшает качество жизни больных БАС (способность к общению и эмоциональное состояние). Применяют амитриптилин в дозе от 25 до 100 мг на ночь (40). Однако, препарат противопоказан больным с глаукомой и аденомой предстательной железы, а в дозах свыше 37,5 мг часто вызывает холинолитические побочные эффекты, ухудшает когнитивные функции (54). Альтернативой или сопутствующей терапией могут выступать глазные капли атропина 0,1% или 1% раствора, раствор атровента, пластырь Скополодерм. Однако системное введение атропиноподобных препаратов часто вызывает побочные эффекты со стороны сердечно-сосудистой системы. По мере течения болезни и прогрессирования дисфагии слюнотечение нарастает, и эффективность указанных средств обсуждается (4,5). Безопасной и эффективной на определенной стадии болезни является комбинация амитриптилина и подкожной инъекции ботулотоксина в дозе 250 ед (3). Безопасность применения более высоких доз ботулотоксина обсуждается. Еще одной альтернативой является облучение слюнных желез однократно в дозе 6-7 Грей (1). Оценка эффективности проводится гравиметрией слюны, а также подсчетом количества раз, когда используется платок для вытирания слюны. Последний метод контроля более нагляден с точки зрения качества жизни пациента. Сравнительных исследований этих видов терапии слюнотечения при БАС не проводилось.
Искусственная вентиляция легких
При БАС целесообразно применение препаратов липоевой кислоты. Собственное исследование соавтора обзора (Г.Н.Л.) показало, что назначение 10 внутривенных инфузий и двухмесячного курса таблетированных препаратов липоевой кислоты в дозе 600 мг может позитивно влиять на показатели стимуляционной миографии при БАС.
С интервалом в три месяца 13 больным БАС проводилась повторная стимуляционная ЭНМГ. С двух сторон исследовались подъязычные нервы (всего 26), ДВ срединных нервов (всего 26), малоберцовых (всего 4) и задних большеберцовых нервов (всего 26). При исследовании подъязычных нервов оценивались дистальные латентности и амплитуды М-ответов мышц языка, при исследовании двигательным волокнам нервов конечностей оценивались резидуальные латентности, амплитуды М-ответов и скорости проведения возбуждения по дистальным отрезкам нервов. Исследование проводилось в 2005-2007 гг. на базе неврологического отделения ГКБ № 31 г. Москвы.
Установлено, что на фоне лечения эспа-липоном достоверно уменьшались дистальные латентности М-ответов мышц языка (2,74±0,65 и 2,33±0,68 мс, р = 0,031) при отсутствии изменений их амплитуд (2,57±1,27 и 2,01±0,93 мс, р > 0,1). Кроме того, достоверно снижалась резидуальная латентность М-ответов срединных нервов (2,98±0,9 и 2,53±0,77 мс, р = 0,034). Амплитуда М-ответов срединных нервов (4,57±5,0 и 4,28±3,2 мВ, р > 0,1), СРВ по дистальным отрезкам срединных нервов (49,3±9,5 и 49,4±9,2 м/с, р > 0,1), а также нервов нижних конечностей (41,7±6,6 и 44,4±1,9 м/с, р > 0,1), как и резидуальная латентность М-ответов нервов нижних конечностей (3,1±0,9 и 2,8±0,2 мс, p > 0,1), достоверно не изменились. За период наблюдения достоверно снизилась амплитуда М-ответов нервов нижних конечностей (13,6±14,6 и 5,77±2,95 мВ, р = 0,016), что отражало естественное прогрессирование заболевания. В контрольной группе больных спинальным и бульбарным БАС динамика электромиографических показателей за указанных интервал наблюдения не наблюдалась. Эти позитивные изменения отражали благоприятное влияние препарата на процессы вторичной демиелинизации при БАС (4).
Целесообразность применения препаратов карнитина и витаминов группы В при БАС не исследовалась. КИ креатина при БАС было отрицательным (28).
Показано, что в группе военнослужащих США, длительно принимавших витамин Е, достоверно снижалась заболеваемость БАС, однако лечение витамином Е больных БАС не приводило к замедлению прогрессирования болезни (25). КИ других антиоксидантов (коэнзима Q10, препаратов глутатиона) были отрицательными или не проводились, соответственно (33).
Заключение
Следует отметить, что эффективное ведение больного БАС возможно лишь при участии не только невролога, но и смежных специалистов – по функциональной диагностике, психиатра, психотерапевта, пульмонолога, эндоскопического хирурга, диетолога, логопеда, специалиста по лечебной физкультуре и физиотерапевта (40). В нашей стране такая практика в пределах одного лечебного учреждения отсутствует. Кроме того, в РФ не зарегистрирован рилутек, а практика предоставления НВЛ и ИВЛ на льготных основаниях государством отсутствует. Общество больных БАС в РФ пока не создано.
Список литературы
- Currently 4.09/10
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
Рейтинг: 4.1/10 (75- проголосовавших)
Читайте также:


