Что такое деструкция крестца

Комментариев пока нет. Будь первым! 7,522 просмотров
Разрушение костной ткани – признак, указывающий на ярко выраженную патологию в организме, которая может негативно влиять на протекание сопутствующих заболеваний. В медицине этот процесс известен, как деструкция кости. В процессе деструкции (разрушения) нарушается целостность костной ткани, которая замещается такими патологическими образованиями, как опухолевые разрастания, липоиды, дегенеративные и дистрофические изменения, грануляции, гемангиомы тел позвонков. Такое состояние приводит к снижению плотности костей, увеличению их ломкости, деформации и полному разрушению.
Характеристика деструкции кости
Деструкция – это процесс разрушения структуры кости с ее заменой опухолевой тканью, грануляциями, гноем. Разрушение кости только в редких случаях проходит ускоренными темпами, в большинстве случаев этот процесс достаточно продолжительный. Часто деструкцию путают с остеопорозом, но, несмотря на неизменный факт разрушения, эти два процесса имеют существенные отличия. Если при остеопорозе костная ткань разрушается с замещением элементами, сходными с костью, то есть кровью, жиром, остеоидной тканью, то при деструкции происходит замещение патологической тканью.
Рентгенограмма – метод исследования, позволяющий распознать деструктивные изменения кости. В этом случае, если при остеопорозе на снимках можно заметить разлитые пятнистые просветления, не имеющие четких границ, то деструктивные очаги будут выражены в виде дефекта кости. На снимках свежие следы деструкции имеют неровные очертания, в то время как контуры старых очагов, наоборот, выглядят плотными и ровными. Разрушения костной ткани не всегда протекают одинаково, они отличаются формой, размерами, контурами, реакцией окружающих тканей, а также наличием внутри деструктивных очагов теней и количеством очагов.
В человеческом организме часто отмечается деструкция кости зуба, тел позвонков и других костей в результате неправильного питания, несоблюдения гигиены, развития гемангиомы, других сопутствующих заболеваний.
Почему разрушается кость зуба?
Заболевания зубов относятся к патологии, которая сопровождается разрушением костной ткани. Среди разных заболеваний зуба, вызывающих деструктивные изменения костной ткани, самыми распространенными считаются пародонтоз и пародонтит.
При пародонтите происходит разрушение всех тканей пародонта, включая десну, костную ткань альвеол, непосредственно пародонт. Развитие патологии вызывает патогенная микрофлора, которая попадает в бляшку зуба и десну, окружающую его. Инфекция кроется в зубном налете, где обитают грамотрицательные бактерии, спирохеты и другие микроорганизмы.
Активность негативной микрофлоры провоцируют следующие факторы:
- проблемы с прикусом;
- вредные привычки;
- протезирование зуба;
- неправильное питание;
- укорочение уздечки языка и губ;
- несоблюдение гигиены ротовой полости;
- кариозные полости, расположенные около десен;
- нарушения межзубных контактов;
- врожденные патологии пародонта;
- общие заболевания.

Все вышеперечисленные факторы являются причинами развития пародонтита и способствуют активизации патогенной микрофлоры, что особенно негативно сказывается на прикреплении зуба к десне.
Пародонтит – заболевание, при котором происходит разрушение соединений ткани зуба и десны с образованием пародонтального кармана.
Патология вызывает деструктивные изменения костных тканей пародонта и альвеолярных отростков. Развитие острой формы заболевания вызывают ферменты, негативно влияющие на межклеточную связь эпителия, который становится чувствительным и проницаемым. Бактерии вырабатывают токсины, которые наносят вред клеткам, основному веществу, соединительнотканным образованиям, при этом развиваются гуморальные иммунные и клеточные реакции. Развитие воспалительного процесса в десне приводит к разрушению кости альвеол, образованию серотонина и гистамина, которые воздействуют на клеточные мембраны сосудов.
Пародонтальный карман образовывается в результате разрушения эпителия, который прорастает в соединительные ткани, расположенные уровнем ниже. 
При дальнейшем прогрессировании болезни соединительная ткань вокруг зуба начинает постепенно разрушаться, что одновременно приводит к формированию грануляции и деструкции костной ткани альвеол. Без своевременного лечения конструкция зуба может полностью разрушиться, что повлечет за собой постепенную потерю всех зубов.
Деструктивные изменения позвоночника
Деструкция кости – это опасный процесс, дальнейшее развитие которого необходимо предупредить при первых признаках патологии. Деструктивные изменения затрагивают не только костную ткань зуба, без соответствующего лечения они могут распространяться и на другие кости в организме. Например, в результате развития спондилита, гемангиомы деструктивные изменения затрагивают позвоночник в целом или позвонковые тела в отдельности. Патология позвоночника может привести к нежелательным последствиям, осложнениям, частичной или полной потере подвижности.
Спондилит – заболевание, хронически воспалительного характера, является разновидностью спондилопатии. В процессе развития болезни отмечается патология тел позвонков, их разрушение, что грозит деформацией позвоночника.
Встречается специфический и неспецифический спондилит. Специфический спондилит вызывают разные инфекции, которые попадают в кровь и с ее помощью разносятся по всему организму, поражая на своем пути кости и суставы. 
К инфекционным возбудителям относятся микробактерии:
- туберкулеза;
- сифилиса;
- гонорейный гонококк;
- кишечные палочки;
- стрептококк;
- трихомонада;
- золотистый стафилококк;
- возбудители оспы, тифа, чумы.
Иногда недуг могут спровоцировать грибковые клетки или ревматизм. Неспецифический спондилит встречается в виде гематогенного гнойного спондилита, болезни Бехтерева или анкилозирующего спондилоартроза.
Независимо от причины развития заболевания, к лечению необходимо приступать сразу после диагностики.
Спондилит – причина развития деструкции тел позвонков
При туберкулезном спондилите отмечается поражение тел позвонков шейного и грудного отдела. Патология приводит к развитию одиночных гнойных абсцессов, порезов, часто необратимому параличу верхних конечностей, образованию горба остроконечной формы, деформации грудной клетки, воспалению спинного мозга.
При бруцеллезном спондилите отмечается поражение тел позвонков поясничного отдела. На рентгеновских снимках отмечается мелкоочаговая деструкция костных тел позвонков. Для диагностики применяют серологическое исследование.
Сифилитический спондилит — редкая патология, поражающая шейные позвонки.
При тифозной форме патологии происходит поражение двух смежных тел позвонков и соединяющего их межпозвоночного диска. Процесс разрушения в груднопоясничном и пояснично-крестцовом секторе происходит быстро, при этом образуются множественные гнойные очаги.
Поражение надкостницы тел позвонков в грудном отделе происходит при поражении актиномикотическом спондилите. При развитии патологии образовываются гнойные очаги, точечные свищи, отмечается выделение белесых веществ, разрушение костной ткани.
В результате травмы позвоночника может развиться асептический спондилит, при котором отмечается воспаление тел позвоночника. Патология опасна тем, что может протекать длительное время бессимптомно. В этом случае пациенты о деструкции позвоночника могут узнать с опозданием, когда позвонок приобретет клиновидную форму, а в позвоночнике возникнут очаги некроза.
Деструкция – патология, которая может поражать как мягкие ткани, так и кости, у пациентов часто наблюдаются гемангиомы тел позвонков.
Гемангиома – опухолевое новообразование доброкачественного характера. Развитие гемангиомы может наблюдаться у человека независимо от возраста. Часто патология встречается у детей вследствие неправильного развития кровеносных сосудов в эмбриональном периоде.
Обычно явных нарушений со стороны новообразовавшейся опухоли не отмечается, поскольку она не проявляется какими-либо симптомами, но это зависит от ее размеров и места локализации. Дискомфорт, некоторые нарушения в работе внутренних органов, разные осложнения может вызвать развитие гемангиомы в ушной раковине, почках, печени и других органах.
Несмотря на то, что опухоль является доброкачественным новообразованием, у детей отмечается ускоренный ее рост в ширину и глубину мягких тканей без метастазирования. Встречаются гемангиомы слизистой оболочки, внутренние и костных тканей (вертебральная гемангиома).
Гемангиомы тел позвонков у детей встречаются крайне редко. Развиваются они в результате врожденной неполноценности структуры кровеносных сосудов. Когда на пораженный позвонок припадает повышенная нагрузка, возникает кровоизлияние, активирующее работу клеток, разрушающих костную ткань, так происходит деструкция тел позвонков. 
В месте поражения образовываются тромбы (сгустки крови), а на месте разрушенной ткани кости появляются новые сосуды, опять неполноценные. При новой нагрузке на поврежденный участок позвоночника они снова лопаются, происходит кровоизлияние. Все эти процессы один за другим приводят к образованию гемангиомы тел позвонка.
У детей чаще всего встречается гемангиома внешних покровов, чем внутренних органов или позвоночника. Зависимо от структуры опухоли, патология бывает:
- простой;
- кавернозной;
- комбинированной;
- смешанной.
Опухолевое новообразование никак не влияет на дальнейшее развитие ребенка, выглядит как косметический дефект. Но поскольку опухоли свойственно быстро разрастаться, врачи рекомендуют все время следить за ее состоянием, в случае ее активного роста, потребуется немедленное лечение. 
Для этих целей используется:
- криодеструкция;
- склерозирование;
- прижигание;
- хирургическое вмешательство.
Одним из самых эффективных методов считается криодеструкция – удаление капиллярных поверхностных гемангиом, которые у детей встречаются чаще всего. Этот метод можно применять при активном росте опухоли. Нельзя его использовать для лечения кавернозных или комбинированных гемангиом, поскольку на коже могут остаться следы уродливых рубцов. Криодеструкция – способ удаления опухоли с применением жидкого азота, который разрушает ее структуру. Для полного удаления новообразования необходимо пройти три сеанса лечения, после чего поврежденные кожные ткани начнут заново восстанавливаться.
Деструктивные изменения костных тканей – патология, требующая своевременной диагностики и правильного лечения. Такой подход к патологии поможет избежать многих заболеваний костной системы и осложнений в будущем.
Гиперостоз — это остеосклероз плюс увеличение объема, утолщение кости. Такое состояние прямо противоположно атрофии. Гиперостоз — это утолщение кости за счет периостального костеобразования, он наблюдается при хронических остеомиелитах, сифилисе, болезни Педжета.
Различают гиперостоз одной или нескольких костей, например, при сифилисе, болезни Педжета и гиперостоз генерализованный, когда наблюдается поражение всех длинных костей скелета при хронических заболеваниях легких: хроническом абсцессе, длительно текущих хронических пневмониях, раке легких.
Различают также гормональные гиперостозы, к примеру, увеличение объема костей при акромегалии.
Эностозом называют увеличение массы кости за счет склероза эндооста.
Воспалительная деструкция. Различают специфическую и неспецифическую воспалительную деструкцию. Основой неспецифической воспалительной деструкции является гной и грануляционная ткань, что характеризует сущность гнойного остеомиелита. В начале процесса контуры очага нечеткие, смазанные; в последующем костная ткань в окружности очага деструкции уплотняется, склеротизируется, а сам очаг деструкции превращается в полость с толстыми, плотными, хорошо сформированными стенками, нередко с секвестральным содержимым. В процесс вовлекается надкостница, возникают обширные периостальные разрастания.
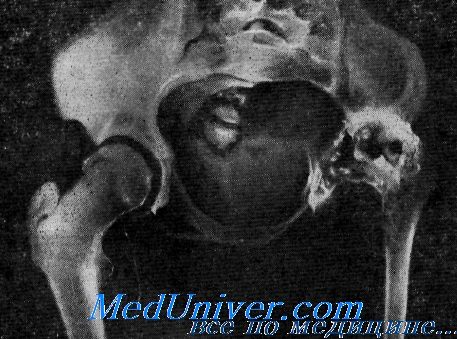
Прямая рентгенограмма таза и тазобедренных суставов.
Определяется резкая деформация тазового кольца. Правый тазобедренный сустав в норме. Выраженные изменения в левом тазобедренном суставе: суставная впадина углублена, суставная щель не прослеживается, головка деформирована с множественными очагами деструкции. Регионарный остеопороз, атрофия бедренной кости. Левосторонний туберкулезный коксит.
Специфическая воспалительная деструкция — это туберкулез, сифилис и др, при которых костная ткань замещается специфической гранулемой. Деструкция при этих заболеваниях отличается по локализации, форме, размерам и характеру очагов, а также особенностью реакции со стороны окружающей костной ткани и надкостницы. Очаг деструкции при туберкулезе, как правило, располагается в губчатом веществе эпифиза, он небольших размеров, округлой формы без или с очень незначительной склеротической реакцией вокруг. Реакция надкостницы чаще отсутствует.
Гуммозный сифилис, наоборот, характеризуется множественными мелкими очагами деструкции продолговатой формы, располагающимися в корковом слое диафизов и сопровождающимися значительным реактивным утолщением коркового слоя за счет эндостального и периостального костеобразования.
Опухолевая деструкция. Деструкция на почве злокачественной опухоли характеризуется наличием сплошных дефектов вследствие разрушения всей костной массы как губчатого, так и коркового слоя в связи с инфильтрирующим ее ростом.
При остеолитических формах деструкция обычно начинается с коркового слоя и распространяется к центру кости, имеет смазанные, неровные контуры, сопровождается обрывом и расщеплением краевой компактной кости. Процесс в основном локализуется в метафизе одной кости, не переходит в другую кость и не разрушает замыкающую пластинку суставной головки, хотя эпифиз или его часть может быть расплавлена совсем. Сохранившийся свободный конец диафиза имеет неровный, изъеденный край.
Деструкция при остеобластическом или смешанном типе остеогенных сарком характеризуется сочетанием участков разрушения кости, которые отличаются наличием хаотической костной структуры с избыточным атипичным костеобразованием; проявляющимся округлой или веретенообразной тенью вокруг мало разрушенной основы кости. Основным признаком, свидетельствующим о злокачественном характере указанных опухолей, остается отсутствие резкой границы между участками деструкции и неизмененной костью, а также разрушение коркового слоя.
Много общего имеют остеолитические метастазы и миелома по картине деструктивного просветления, которое проявляется в виде округлых, резко очерченных дефектов кости и характеризуется множественностью и полиморфностью (разной величины) поражения.
Участки просветления при доброкачественных опухолях указанного типа имеют овально-округлую правильную форму, однообразную структуру рисунка, ровные и отчетливо выраженные контуры, четко отграниченные от кости. Кортикальный слой опухоли является продолжением компактной кости здоровых участков; отсутствуют реактивные костные изменения в виде остеопороза в окружности опухоли и периостальные наслоения. Кортикальный слой кости в области опухоли может быть резко истончен, но он всегда сохраняет свою целостность. Если будет выявлен разрыв, перерыв его, то это часто является свидетельством злокачественного перехода и тогда правомерно предполагать истинную опухолевую деструкцию.
- Вернуться в оглавление раздела "Лучевая медицина"
Процессом разрушений в структуре костей, что постепенно приводит к ее замене на злокачественную ткань, грануляции, гной – это деструкция кости. Прогрессирующий патологический процесс сопровождается снижением показателя плотности у костей и увеличения их хрупкости. Гармония в развитии костной ткани до двадцатилетнего возраста происходит нормально, естественно. После этой возрастной границы формировка таких тканей стает медленнее, а разрушительный процесс только усугубляется.
Кости – это твердый орган в нашем организме, их функции заключаются в обеспечении опорно-механической и защитной функции. Они состоят из гидроксиапатита, минерального вещества, около 60-70% от веса кости и органического коллагена первого типа около 30-40%.
Когда же этот состав изменяется, плотность костей уменьшается. Это одна из причин, когда пожилым людям вылечится после любых травм сложнее, чем человеку в юном возрасте. Небольшие негативные внешние факторы могут легко привести к травме, ведь слабые кости больше поддаются воздействию. Ускорить этот процесс могут ряд факторов.
8 важных причины
Внутренний источник разрушения костных тканей – остеопороз. Это заболевание имеет системный прогрессирующий характер. Это обменный или клинический синдром, характеризующий уменьшением плотности, увеличением хрупкости. Метаболизм данной ткани уменьшается, она становится менее прочной, повышается уровень переломов.
Эта болезнь впервые была найдена у индейцев Северной Америки, около 2500-2000 лет до нашей эры. Также характерные осанки этой болезни можно увидеть в картинах художников Древнего Китая, Греции.
Степень риска определяется, ориентируясь на объективные данные анамнеза и результаты обследований.
Остеопороз приводит к пористости костной ткани. Также негативно повлиять на этот процесс могут несколько факторов. Деструкция кости причины:
- заболевания, вызваны расстройством одного или нескольких эндокринных желез – эндокринные, хронические болезни;
- недостаток питательных веществ, это строители костей в нашем организме – магний, калий, витамин Д, главной причиной дефицита является несбалансированное питание;
- последняя самостоятельная менструация, то есть период менопаузы;
- недостаток весового показателя;
- наличие вредных привычек, усугубление их прогрессивности;
- наследственность, опасть грозит людям, у которых есть кровные родственники до пятидесятилетнего возраста, что диагностировали у себя эту болезнь;
- минувшие травмы, что усугублены переломами;
- профессиональные спортсмены также в зоне риска, великая часть физической нагрузки является причиной появления этой болезни;
Важно! Остеопороз в запущенных формах лечится тяжелее. Стоит больше бдительности уделить профилактике.
Деструкция костей черепа
Самое распространенное поражение. После длительного периода времени некоторые очаги костей замещаются совсем другими. Выявить дефект костной ткани поможет рентгенологическое исследование.
Очаги деструкции могут быть десяти сантиметровым размером и больше в диаметральном измерении. В таком случаи люди ощущают сильную головную боль, ушную боль. Болевые ощущения преимущественно ночью отмечаются у людей с пораженными трубчатыми костями.
Дети проявляют в этот период большую пассивность. Она проявляется в сокращении подвижности, отказами поднимать какой-либо предмет руками, или банально ходить.
Форма очагов – продолговатая, вытянутая по длине кости. Осложнение в зоне позвоночника, человек перестает двигаться.
Деструкция лобной кости
Воздушное пространство внутри нее из-за воспалительного заболевания выполняется патологически – содержимым элементом. Наполнение серозное или гнойное, отечное слизистой, или кистой. Возможно также нарушения гармоничного состояния стенок вследствие переломов, поражение опухолью. Особо сомнительные случаи требуют использование введенных в пазушную часть йодолипола, майодила.
Деструкция кости челюсти
Являет свое действие повторно вследствие прорастаний опухолей. Они развиваются из ткани эпителия в слизистую оболочку ротовой полости. До десяти процентов занимает сарком, больший процент приходится на рак. Аденокарцинома молочная, щитовидная, предстательных желез – одни из причин возникновения метастаз.
Важно! Именно рентгенологическое вмешательство поможет увидеть изолированные дефекты и разного рода поражение.
Деструкция бедренной кости
Следствие нарушений кровотока и некрозных элементов. Это заболевание усугубляется под воздействием повышенного употребления спиртных напитков, употребления кордиостероида, травм суставов, панкреатит. Возможность ранней диагностики возможна при применении томографии.
Деструкция височной кости
Диагностируется лучше всего с помощью компьютерной томографии и магнитного-резонансного исследования. Такие способы наиболее информативные, они доступные большинству людей и это позволяет ограничить величину проведенного поиска.
В пирамидной части такой кости часто встречаются опухоли: невритомные, фибромные, гломусные, остеомные. Чаще всего подвержены ушные участки.
Метастические поражения возможны при раковой опухоли молочных желез, легких, почек.
Важно! Рентгенологически можно опередить проявление опухоли в данной области, с соответственным размером. Необходимо знать особенности строения кости, основы анатомии для своевременного обнаружения первых признаков разного характера и подходов их устранения.
Деструкция плечевой кости
Является серьезной болезнью, что действует от костного элемента с появлением омертвевших участков. Далее меняется на жировую ткань. Это заболевание называют ишемическим некрозом. В основе патологии – изменение нормального состояния кровоснабжения костей. Вследствие этого, данную ткань лишают стопроцентного питания – она медленно отмирает.
Страшнее всего-то, что данная болезнь приводит к необратимости в состоянии костей. Минимальный процент восстановления структурной части костей.
Важно! Прохождение пациентом всех стадий патологии совершается в течение от нескольких месяцев до 1-1,5 лет. Если деструкция плечевой кости начала свое действие – остановить этот процесс уже нельзя. Больной проходит через все стадии, вследствие чего, что больше всего вероятно, приводит к инвалидному креслу.
Деструкция костей таза
Сопровождается длительным бессимптомным лечением. Чаще всего это крыло подвздошных костей рядом с крестцово – подвздошным сочленением. Первый признак – это изменение костей, припухлость. Дети и подростки наиболее подвержены этой болезни. Болевой порог умеренный, ощущение имеет ноющий характер. С патологической точки зрения – отсутствие переломов. Лечить можно только хирургически – резекцией костей. Большие размеры образуют дефект и их показывают аутопластические и аллопластические замещения.
Меры профилактики
Из-за специального метода диагностирования, возможна большая точность выявления изменений в плотность.
Есть ультразвуковая методика, что называется денситометрия. Благодаря этой методике можно определить даже минимальные показатели снижения плотности. Иные аппаратные вмешательства на ранних стадиях неэффективны. Для сравнения: рентгеновский аппарат покажет результат при показателе в двадцать пять – тридцать процентов.
Специалисты обговаривают некоторые признаки, указывающие на протекание данной болезни: уменьшение роста больше десяти миллиметров, позвоночная часть искривляется, поясница и грудная часть болит, особенно при активном занятии физическими нагрузками, быстро утомляетесь, работоспособность минимальная.
Подвижная жизнь является наилучшей профилактической мерой развития данного заболевания. Это:
- сбалансированное питание: правильное соотношение белков, жиров, углеводов, большое количество употребление свежих овощей и фруктов;
- ходьба на чистом воздухе;
- утренняя зарядка, физкультурные тренировки, не на износ;
- сведение к минимуму пагубных привычек в образе сигар, спиртных напитков и употребление кофейных напитков;
- расслабляющие и тонизирующие массажи.
Обратите внимание! До подбора упражнений подойдите осознанно, не лишней будет консультация врачей, или инструктора по фитнесу. В течение нескольких месяцев совмещения сбалансированного питания плюс умеренных физических нагрузок – косная масса увеличивается на несколько процентов.
Лечебная терапия
Аналогичные профилактическим мерам терапевтические методы лечения. Различие состоит в большей направленности действий. Сама болезнь характеризуется длительностью и трудоемкостью.
Обратите внимание! Человек ежедневно должен употреблять рыбий жир, порошок яичной скорлупы, он легче усваивается.
Деструкция кости лечение помогает медикаментозная терапия. Вам предоставлен большой ассортимент лекарств. Специалист в индивидуальном порядке назначает лечение.
Самолечение бесполезно, болезнь приводит к ухудшению качества проживания.
Для минимизации возникновения болезни – лучше использовать профилактические меры.
Метастазы рака в крестце выявлены у 72 пациентов (или 8 %) из 908 оперированных с метастатическими поражениями костей скелета раком.
Метастазы наблюдались преимущественно у больных старше 40 лет, часто сопровождались сильной болью.
Иногда метастазы были множественными и характеризовались быстрым литическим процессом.
J.Genin, G,Messenard (1987) в Институте Густава Руссу с 1960 по 1984 г. наблюдали 6 первичных больных и 10 — с рецидивами хордомы после операции.
Они приводят следующие данные об опухолях крестца (с 1936 по 1976 г.).
Злокачественные опухоли:
хордома — 40 больных,
хондросаркома — 6,
остеогенная саркома — 5,
саркома Юинга — 5,
ретикулосаркома — 4,
плазмоцитома — 4,
фибросаркома — 3,
саркомы — 3 больных
(всего 70 пациентов).
Доброкачественные опухоли:
гигантоклеточная опухоль — 13,
остеобластома — 3,
аневризматическая костная киста — 3,
остеохондрома — 2 больных
(всего 21 пациент).
50 % всех хордом развиваются в крестце и представляют значительные сложности для лечения, поскольку очень часто наблюдаются рецидивы после резекции крестца вместе с опухолью. Мы наблюдали больного, у которого хордома развилась в переднем отделе таза; нам пришлось резецировать лобковую, седалищную и часть тела вместе с вертлужной впадиной. Больной жив без рецидива 17 лет.
Все остальные опухоли лечат так же, как и при других локализациях комплексно.
Некоторые доступы для резекции крестца
Задний срединный доступ наиболее часто применяют при опухолях небольшого и среднего размера.
Очень осторожно отсепарируют прямую кишку от копчика и V крестцового позвонка, так как кишка очень прочно фиксирована к ним m.levator ani. Дальше прямая кишка легко отделяется от передней поверхности крестца, и можно легко дойти до V поясничного позвонка. Ягодичные мышцы от крестца можно отсекать электроножом, тогда кровотечение значительно меньше. После их выделения ножом и ножницами пересекают крестцово-остистую и крестцово-бугорную связки. Если есть подозрение на опухоль, то необходимы ламинэктомия, обследование спинномозгового канала, концевой цистерны и определение хода нервных корешков.
Нами проведены резекция крестца вместе с хордомой на уровне II крестцового позвонка, ламинэктомия крестца. Положение больного на животе. Линейным разрезом по линии остистых отростков, а затем несколько влево, т.е. над опухолью, иссекаем место пункционной биопсии и оставляем канал на опухоли, послойно рассекаем кожу, подкожную клетчатку, фасцию. Значительная часть крестца практически до уровня I крестцового позвонка занята опухолевидным образованием мягкоэластической консистенции. Отсекаем ягодичные мышцы, вследствие чего появилась возможность освободить боковые массы крестца и выйти на небольшом участке на переднюю поверхность крестца. После рассечения соединения крестца с копчиком стало ясно, что опухоль разрушает переднюю стенку крестца и интимно спаяна с прямой кишкой. Учитывая значительные размеры опухоли, наличие множества опухолевых выростов, решено провести ламинэктомию крестца.
После ламинэктомии I, II крестцовых позвонков обнаружено, что концевая цистерна входит в состав опухоли, поэтому толстой атравматичной иглой концевая цистерна примерно на 1 см от места вхождения ее в опухоль прошита и дважды перевязана и пересечена. С помощью долота и кусачек частично перекушены крестцово-подвздршные сочленения. Установлено, что нервные корешки входили в опухоль, и с точки зрения абластики сохранить их не представлялось возможным. После этих мероприятий дистальный отдел крестца стал подвижным. Тупой препаровкой от опухоли отделена прямая кишка. После полного отделения прямой кишки от опухоли крестца резецированный его участок вместе с опухолью удалены. Выполнен гемостаз. Рана послойно ушита наглухо и дренирована. При значительном распространении хордомы, ее активном росте она часто прорастает не только концевую цистерну, но и прямые мышцы спины.
Оперативное вмешательство трудно выполнить, если оно повторное.
Так, больной Ш-з, 64 лет, с аденомой предстательной железы 2 раза в сутки спускал мочу катетером. У него нарушена половая функция, выраженное ожирение, резко расширены венозные сосуды таза. Сначала была предпринята попытка резецировать крестец, затем крестец вместе с хордомой на уровне II—III крестцовых позвонков двумя доступами — чрезбрюшинным и задним.
Разрезом по средней линии от уровня пупка и на 3 см не доходя до симфиза послойно с разведением прямых мышц живота вскрыта брюшная полость. Тонкие кишки отведены кверху, сигмовидная кишка — влево. Определены бифуркация аорты и нижней полой вены, уровень I крестцового позвонка, после чего продольным разрезом рассечен задний листок брюшины. После тупой препаровки и разведения заднего листка брюшины обнаружен толстый слой жировой клетчатки, из которой выделены, перевязаны шелком и пересечены срединная артерия и вена крестца. Средняя вена крестца была необычно большого диаметра, что, очевидно, связано с нарушением мочеиспускания и акта дефекации.
Большое количество жировой клетчатки таза, вероятно, можно объяснить нарушением половой функции. Постепенно тупым путем выделена передняя поверхность I, II крестцовых позвонков и верхняя граница хордомы, которая плавно снижалась на уровне тел III и II крестцовых позвонков. Долотом пересечен крестец на 0,7 см выше верхней границы опухоли. Появилось небольшое кровотечение, которое было быстро остановлено. Наложен непрерывный шов заднего листка брюшины шелковой нитью на атравматичной игле. Проведен осмотр брюшной полости. Рана передней брюшной стенки послойно зашита наглухо.
Выполнен разрез по средней линии от уровня остистого отростка VI поясничного позвонка с частичным иссечением рубца после резекции копчика, постепенно послойно выделена задняя поверхность крестца, а затем его боковые поверхности. Из массивных рубцов, образовавшихся после первой операции, — обильное кровотечение, которое трудно остановить. Применены обшивание кровоточащих сосудов, электрокоагуляция, тампонада горячим изотоническим раствором натрия хлорида.
После этого кусачками Люера выполнена вне пределов опухоли резекция боковых масс крестца в виде двух каналов, верхние концы которых сходились по направлению спинномозгового канала на уровне II, III крестцовых позвонков. Произведена ламинэктомия I, II и III крестцовых позвонков. Обнаружено, что хордома припаяна к твердой мозговой оболочке спинного мозга, которая при попытке отделить твердую оболочку от опухоли образует расширение диаметром до 1,5 см. Твердая мозговая оболочка разорвалась, вылилось до 10— 15 мл спинномозговой жидкости, а затем ее истечение самопроизвольно прекратилось.
Твердая мозговая оболочка выделена выше разрыва, прошита лавсановой нитью на атравматичной игле, после чего твердая мозговая оболочка ниже шва пересечена так, что ее дистальный конец остался на опухоли. Затем приступили к отделению прямой кишки от передней поверхности крестца и опухоли, что было чрезвычайно трудно выполнить изза массивных рубцовых спаек, образовавшихся после первой операции.
Осторожно долотом и кусачками перекушены костные перемычки на уровне границы II и III крестцовых позвонков, где ранее была проведена остеотомия крестца из переднего доступа, что позволило приподнять дистальный конец крестца кзади и отделить острым и тупым путем прямую кишку от крестца и опухоли.
После этого от передней поверхности опухоли и крестца отделены крестцовые корешки верхних крестцовых сегментов и дистальная часть крестца, которые вместе с опухолью (выделенной абластично) удалены. Выполнен тщательный гемостаз из расширенных и многочисленных вен таза (расстройство акта дефекации, геморрой, нарушение мочеиспускания — спускал мочу катетером 2—3 раза в день в течение года). Рана промыта перекисью водорода и раствором фурацилина; после введения через дополнительный прокол трубки от одноразовой системы для дренажа раны последняя послойно защита наглухо лавсановыми и кетгутовыми швами. Наложена асептическая повязка. Артериальное давление 120/80 мм рт.ст. Чрезбрюшинный нижний срединный доступ описан давно, и некоторые хирурги им пользуются.
После отведения тонких кишок кверху, а сигмовидной — влево и рассечения задней париетальной брюшины обнажаются передняя поверхность крестца, передняя крестцовая артерия и вена, после перевязки и рассечения которых можно отслоить прямую кишку и надрубить долотом тело крестцового позвонка.
Передний чрезбрюшинный доступ был осуществлен нами еще два раза у молодых людей, имевших доброкачественную нейрогенную опухоль крестца. После отведения тонких кишок через тонкую заднюю периостальную брюшину срединная артерия крестца была хорошо видна и без труда перевязана и пересечена.
У одного больного с хордомой размером 28 см, располагавшейся по задней (а не передней, как у всех) поверхности крестца, нам пришлось сделать поперечный горизонтальный разрез.
Два других доступа приводятся нами далее. В литературе описаны многочисленные модификации доступов к крестцу. На практике используется более 15 таких модификаций.
R.G.Wirbel и др. (1998) оперировали 16 больных со злокачественными опухолями крестца:
у 12 — хордома,
у 3 — хондросаркома,
у 1 — фибросаркома.
В 10 случаях применяли задний доступ, в 5 — переднезадний, в 1 — биопсию.
Ампутация прямой кишки с колостомией понадобилась 9 больным, 8 человек умерли, местные рецидивы были у 4, отдаленные — у 3 пациентов, 8 больных живы в сроки от 21 до 112 мес с хорошими и отличными результатами.
Особую группу составляют больные с односторонним поражением пояснично-крестцовой области. Здесь имеются свои особенности хирургического вмешательства: нужно с помощью ламинэктомии по возможности сохранить корешки со здоровой стороны, блоком удалить опухоль, поразившую тело позвонков, и заместить дефект аутотрансплантатами, предварив оперативное вмешательство эмболизацией сосудов, и закончить вмешательство металл оостеосинтезом.
R.Garom, G.Horn (1969) описали больного с метастазами крестцовокопчиковой хордомы в сердце, мышцы, кожу, что встречается очень редко. A.W. Pearlman, M.Friedman (1970) подтверждают, что хордома устойчива к лучевой терапии; по их мнению, лучевую терапию можно проводить после операции для предотвращения рецидивов, с чем, конечно, согласиться нельзя.
Французские ортопеды придают очень большое значение артериографии и эмболизации при опухолях позвоночника и крестца. R.Roy-Camille и др. (1987) представили описание 4 больных с метастазами щитовидной железы в крестец, которым были проведены артериография и эмболизации опухоли, что значительно уменьшает кровопотерю, а в некоторых случаях без предварительной эмболизации вообще было бы невозможно выполнить оперативное вмешательство. При необходимости резекции верхних крестцовых позвонков стабилизацию осуществляли пластинками, привинчиваемыми к нижним отделам крестца и поясничным позвонкам, или заполняли дефект аутотрансплантатами из гребня подвздошной кости, которые фиксировали к подвздошным костям винтами. У 10 больных была применена лучевая терапия.
S.Shapiro, J.Scott, K.Kaufman (1999) сообщили о больных с метастазами ангиосарком в сердце. Они наблюдали больного через 17 мес после операции на сердце и химиотерапии по поводу ангиосаркомы сердца, у которого появилась боль в шее и левой руке. На КТ — литический процесс в позвонке Сз со сдавлением спинного мозга. Попытка подойти и удалить опухоль из переднего доступа оказалась неудачной из-за сильного кровотечения; после эмболизации предпринята вторая операция — удаление опухоли тела позвонка, замещение дефекта фрагментом малоберцовой консервированной костью, фиксация пластинкой, уменьшение патологических симптомов. Это второй случай, описанный в литературе. J.Berkefeld и др. (1999) у 55 больных с метастазами в позвоночник применили эмболизацию, при этом указали на значительное уменьшение кровотечения.
R.R.Lonser и др. (1998) сообщают, что для уменьшения кровоснабжения опухоли и кровотечения во время операции, например при гемангиоме позвонка или другой опухоли с повышенным кровоснабжением, показана чрескожная инфузия в опухоль этанола (ЕТОН), которая значительно уменьшает кровотечение и облегчает операцию.
Большое значение имеет лучевая и химиотерапия при опухолях крестца. E.Toubout и др. (1987), G.Missenard, G.Genin, J.Dubousset (1987) описывают широкий доступ для удаления опухолей верхнего конца крестца, начинающийся в паховой области, идущий вверх по косым мышцам живота, огибающий крыло подвздошной мышцы до средней линии и идущий по остистым отростками нижнепоясничного отдела и крестца.
Такой же доступ использовала и группа хирургов из Торонто. А.Н.R.W.Simpson и др. (1995) разработали методику резекции верхнего отдела крестца из комбинированного расширенного подвздошно-пахового и заднего доступа у 12 больных с большими размерами хордом, гигантоклеточными опухолями, остеогенной саркомой и хондросаркомой. Разрез из паховой области с отсечением в нижнем отделе обеих прямых мышц от лобковых костей проводят по краю косых брюшных мышц кверху, затем выше и параллельно гребню подвздошной кости до остистого отростка V поясничного позвонка и по средней линии вниз на несколько сантиметров, не доводя его до ануса. Брюшину вместе с мочеточником тупо отслаивают, при этом обнажаются общие подвздошные сосуды, передняя поверхность крестца с опухолью; перевязывают внутренние подвздошные сосуды с этой стороны.
Авторами с 1986 по 1992 г. прооперировано 6 мужчин и 6 женщин, которым была произведена резекция от верхнего отдела крестца, включая II крестцовый позвонок, так что линия резекции проходила у 6 больных через I крестцовый позвонок, у 3 — через II позвонок; у 2 была полностью удалена половина крестца в сагиттальном направлении и у 1 пациента крестец был удален полностью.
У 6 больных выявлена хордома, у 3 — гигантоклеточная опухоль, у 2 — остеогенная саркома и у одного — хондросаркома.
Один больной с остеогенной саркомой умер от кровопотери после операции.
Только у 1 больного наступил рецидив, у 10 человек нет рецидива в сроки от 23 до 69 мес.
Продолжительность операции — от 4,5 до 16 ч, средняя продолжительность — 10 ч. Кровопотеря — от 2 до 20 л, в среднем 7 л. У 6 больных возникли осложнения со стороны раны, у 2 — гематома, у 1 — длительное заживление, у 3 — инфицированное нагноение раны, у 1 — печеночно-почечная недостаточность и у 1 больного — множественные легочные эмболии, желудочно-кишечные кровотечения как результат применения антикоагулянтной терапии.
Судя по отсутствию рецидивов, результаты лечения можно считать хорошими, хотя у 5 больных срок наблюдения составил 2—2,5 года, а этого недостаточно, чтобы быть уверенными, что рецидива хордомы не будет. Только у 2 больных срок достаточно большой — 4 и 5,5 года. Умеренно выражены неврологические расстройства, но все же 1 больной пользуется креслом-качалкой, 4 — палкой.
К сожалению, недостаточно четко описано, какой принцип сохранения нервных корешков использован, так как самым главным в операции резекции крестца является доступ, а также решение, какой нервный корешок можно сохранить. Вызывает удивление, почему авторы не использовали эмболизацию для уменьшения кровопотери. Ведь кровопотеря 20 л опасна для жизни. Авторы не пишут, в какой момент операции теряется наибольшее количество крови. Восхищаясь смелостью авторов этой статьи, у читателей возникает много вопросов.
С.Т.Зацепин
Костная патология взрослых
Читайте также:


