Аутолиз легких. Признаки аутолиза печени
Добавил пользователь Дмитрий К. Обновлено: 22.01.2026
Мертворождённость (син. мертворождение) — рождение или извлечение из организма матери плода при сроке беременности от 28 нед. и более, т. е. плода ростом 35 см и более, весом 1000 г и более, который после отделения от тела матери не сделал ни одного вдоха. Статистический показатель Мертворождённости исчисляется следующим образом:
([число детей, родившихся мертвыми] / [число детей, родившихся всего (живых и мертвых)]) x 1000
При этом мертворожденным считается плод, у к-рого отсутствует самостоятельное внеутробное легочное дыхание при рождении и при безуспешности оживления искусственным путем независимо от наличия сердцебиения или других признаков жизни.
Аналогично исчисляются показатели частоты мертворождений доношенных и недоношенных детей (к числу всех доношенных или недоношенных). По данным Г. Ф. Церковного (1976), антенатально погибшие плоды составляют около 40% от всех мертворожденных; недоношенные дети в 7—8 раз чаще рождаются мертвыми по сравнению с доношенными. По данным В. И. Грищенко и А. Ф. Яковцова (1978), уровень показателя Мертворождённости по отдельным странам колеблется от 5 до 20 промилле, в т. ч. в развитых странах показатели М. наиболее низкие.
В зависимости от срока наступления смерти по отношению к родам М. делят на антенатальную и интранатальную. Антенатальной считается М. в случаях, когда смерть плода наступила в срок от 28 нед. и до родов; антенатальная смерть плода устанавливается на основании клин, (прекращение сердцебиения и шевеления плода до начала родового акта) и рентгенологических признаков. Интранатальной считается М. в случаях, когда смерть наступила во время родового акта; к умершим интранатально следует относить и новорожденных, родившихся с сердцебиением, но не начавших дышать после реанимационных мероприятий.
Содержание
Причины мертворождения
Причины мертворождения разнообразны и изучены не полностью: имеют значение патологические процессы в организме матери, самого плода и в так наз. плодном яйце. Патология плода и изменения в последе во многом зависят от предшествующих и сопутствующих заболеваний матери, осложнений беременности и родов. Причины анте- и интранатальной) мертворождения можно разделить на основные и непосредственные. Основными причинами М. являются: усложнения беременности (поздние токсикозы, кровотечения и др.), аномалии родовой деятельности, положения плода и предлежания плаценты, патология пуповины и плаценты, заболевания матери, не связанные с беременностью: пороки сердца, гипертоническая болезнь, нефропатия, диабет, острые и хрон. инф. болезни, острые отравления, иммунологическая несовместимость матери и плода и др. Непосредственными причинами антенатальной гибели плода могут быть асфиксия, гемолитическая болезнь, внутриутробная инфекция, врожденные пороки развития и генетические заболевания. Интранатально плод может погибнуть при патол, течении родов (внутричерепная родовая травма, асфиксия плода, эклампсия матери, предлежание плаценты и др.).
Патологоанатомическое исследование преследует цель выяснить причину смерти плода: асфиксия плода, родовая травма, а также был ли плод жизнеспособным или имелись несовместимые с жизнью пороки развития или внутриутробное заболевание. В каждом конкретном случае асфиксии или родовой травмы плода необходимо установить, явились ли эти состояния основной причиной смерти или осложнением предшествующей внутриутробной болезни плода — Фетопатии (см.). Макроскопическими признаками мертворожденного плода, погибшего антенатально, являются, как правило, выраженная мацерация кожного покрова, аутолиз внутренних органов, отсутствие воздуха в желудке и полный первичный ателектаз легких. В результате мацерации эпидермис плода отпадает пластами в виде серовато-белых пленок, обнажается влажная синевато-красная дерма; внутренние органы дряблые, на разрезе расползаются, в полостях тела большее или меньшее количество прозрачной кровянистой жидкости. Аутолиз внутренних органов затрудняет микроскопическое исследование. Дольше других органов сохраняются легкие, к-рые всегда необходимо подвергать микроскопическому исследованию. Мацерация кожного покрова и аутолиз внутренних органов выражены тем значительнее, чем дольше мертвый плод находился внутриутробно; если плод был извлечен быстро, мацерации и аутолиза может не быть.
Плацента вследствие прекращения плодного и сохранения материнского кровообращения малокровна в результате сдавления сосудов ворсинок.

Рис. 1. Микропрепарат легкого мертворожденного плода после реанимационных мероприятий (искусственной вентиляции легких): видны растянутые воздухом крупные полости (1), образовавшиеся из-за разрыва альвеолярных перегородок (2).
Желудок у мертворожденного не содержит воздуха, спавшийся; легкие поджаты к корню, не заполняют грудной полости, мясистые, синевато-красные, на поверхности разреза при надавливании появляется темная жидкая кровь. Гидростатические жизненные пробы (см.) отрицательные. Обязательно следует учитывать наличие воздушных участков в легких, возникающих вследствие искусственного дыхания при реанимации; микроскопически искусственно-воздушные участки отличаются от естественного расправления легких наличием крупных воздушных полостей с разрывами альвеолярных перегородок (рис. 1), перемежающихся с участками ателектаза (см.).
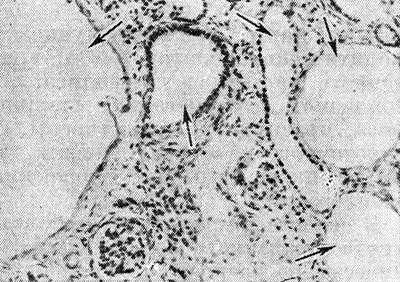
При отсутствии или незначительной выраженности мацерации и аутолиза можно выявить признаки болезни плода в органах, характерные для фетопатий любой этиологии. К ним относятся увеличение или уменьшение общей массы плода, не соответствующее его возрасту, наличие дистрофических и очаговых некротических изменений в паренхиматозных органах, гепато- и спленомегалия с наличием крупных очагов миелоэритропоэза, не соответствующих (по размеру) возрасту плода, интерстициальные инфильтраты преимущественно из эозинофильных миелоцитов в печени, поджелудочной и вилочковой железе, акцидентальная инволюция с уменьшением массы вилочковой железы, наличие незрелости и пороков развития тканей, напр, кистозная дисплазия почек (рис. 2). Кроме этих общих признаков, наблюдаются изменения, харак-терные, напр., для изоиммунной гемолитической болезни плода, врожденного листериоза, сифилиса, токсоплазмоза, цитомегалии, микоплазмоза, краснухи, ветряной оспы, сывороточного гепатита, диабета, тиреотоксикоза, нек-рых врожденных заболеваний.
В связи с тем, что многие болезни мертворожденного плода макроскопически не распознаются, необходимо комплексно применять микроскопические, бактериол., цитогенетические, иммунофлюоресцентные и биохим. методы исследования органов и последа.
Рентгенодиагностика
Необходимость в рентгенодиагностике может возникнуть перед патологоанатомическим и суд.-мед. вскрытием трупа плода, а также в случае клин, признаков внутриутробной смерти плода. Поводом для рентгенологического исследования могут оказаться нек-рые трудности дифференциации живорождения и мертво рождения при секционном исследовании, необходимость сопоставления результатов гидростатических жизненных проб с результатами рентгенол, исследования, а также случаи выраженного трупного разложения.
Так наз. проба Диллона, к-рая заключается в обнаружении на рентгенограмме признаков газа в пищеварительном тракте трупа (по утверждению ученого, это свидетельствует о живорожденности), не может рассматриваться как надежный показатель. По мнению многих исследователей, такое рентгенол, исследование теряет диагностическое значение спустя 48 час. после смерти вследствие развития гнилостных процессов в жел.-киш. тракте и в случаях применения искусственного дыхания.
При рентгенол. исследовании должно быть получено изображение всего трупа, а при необходимости и отдельных органов. Рентгенограммы производят в прямой и боковой, а иногда и в дополнительной целенаправленной проекциях.
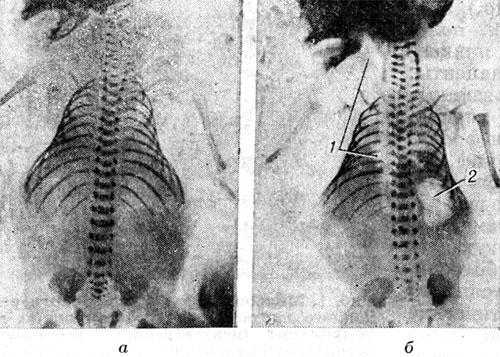
Рис. 3. Рентгенограммы мертворожденного плода: а — полное отсутствие газа в грудной клетке и других полостях тела; б — наличие газа в полостях сердца и крупных сосудов (1), а также в желудке (2).
Основные рентгенол, признаки мертворождения: 1) полное отсутствие газа в легких, желудке и кишечнике (рис. 3, а); 2) отсутствие газа в легких, однако возможно наличие газа в пищеварительном тракте, но не далее двенадцатиперстной кишки (рис. 3, б); 3) возможно небольшое развертывание легких при полном отсутствии газа в желудке и кишечнике; 4) наличие газа в полостях сердца и крупных сосудах (рис. 3, б). Указанные признаки исключают живорождение ребенка.
Нек-рое сходство с перечисленными выше рентгенол, признаками может наблюдаться у живорожденного в случае отсутствия развертывания легких в сочетании с наличием газа в кишечнике; однако газ при этом занимает тонкую кишку на большом протяжении — за пределами двенадцатиперстной кишки, что указывает на несомненное живорождение ребенка даже при полной безвоздушности легких. Возможность жизни новорожденного в течение нескольких часов при полном неразвертывании легких объясняется тем, что из газа жел.-киш. тракта диффундирует нек-рое количество кислорода. Как показали исследования А. Ильине, даже 5% от нормального количества необходимого для жизни кислорода могут временно поддерживать жизнь новорожденного в состоянии покоя.
Несмотря на относительную диагностическую ценность рентгенол, исследования, оно в сочетании с другими методами имеет несомненное значение для суд.-мед. экспертизы.
Мертворождение в судебно-медицинском отношении
Установление факта мертворождения имеет значение при расследовании уголовных дел, связанных с детоубийством (см.) при родах вне мед. учреждений.
При исследовании трупа обращают внимание на наличие внешних признаков легочного дыхания :форма грудной клетки у мертворожденных менее выпуклая, чем у живорожденных, уровень стояния купола диафрагмы у мертворожденных соответствует IV, у живорожденных — VI ребру (однако указанные признаки непостоянны и ненадежны). Диагностическое значение имеет объем и цвет легких: легкие мертворожденного не расправлены, спавшиеся, как правило, они находятся в задних отделах грудной полости; цвет их красно-бурый или коричневато-красный, на ощупь легкие плотные, упругие. Для определения мертворождения. или живорождения обязательно проведение двух жизненных гидростатических (плавательных) проб — легочной и желудочно-кишечной, основанных на определении наличия воздуха в легких и жел.-киш. тракте (см. Жизненные пробы).
Большое диагностическое значение имеет гистол, исследование легких трупа. Для мертворожденного характерно: нерасправленные альвеолы и бронхи, кубическая форма эпителия альвеол, толстые Межальвеолярные перегородки, извитые эластические волокна, идущие в составе менее толстых пучков, тонкие извитые аргирофильные волокна. Исследуются и другие органы и ткани трупа, напр, пупочное кольцо, пуповина.
Для дифференциальной диагностики мертворождения и живорождения И. К. Есиповой, О. Я. Кауфманом (1968) разработана методика посмертной рентгеновазографии в сочетании с микрометрией артерий уровня дыхательных бронхиол, весовые соотношения отделов сердца, состояния пупочных сосудов и артериального (боталлова) протока. У мертворожденных на рентгенограммах выявляется разная степень наполнения сосудов контрастной массой. Просвет артерий уровня респираторных бронхиол мертворожденных равен 0,2±0,54 мкм. У живорожденных внутридольковые артерии легких образуют чрезвычайно густую сеть, местами сливающуюся. Просвет артерий уровня респираторных бронхиол у живорожденных ко второму дню жизни равен 18—20 мкм. Однако введение контрастного вещества в легочный ствол или в аорту трупа делает невозможным проведение плавательных проб.
В связи с прекращением кровотока через пуповинные сосуды, а позднее и через артериальный проток диагностическое значение имеет начало организации свертков крови в пупочных сосудах и пролиферации клеток в субэндотелиальном слое артериального протока. Развитие этих процессов начинается довольно рано и служит доказательством живорождения.
В экспертной практике нередко приходится исследовать трупы новорожденных не только вскоре после наступления смерти, но и спустя различные сроки, когда наступают гнилостные изменения, высыхание. К оценке результатов описанных выше проб в этих случаях надо подходить осторожно. При экспертизе мертворождения, особенно в случаях гнилостных изменений или высыхания трупов, используется метод эмиссионного спектрального анализа легких, печени, крови, миокарда и плаценты (см. Спектральный анализ). При спектрографическом исследовании пользуются величинами коэффициенте в отношения нек-рых макро- и микроэлементов. Целесообразно применять комплекс лаб. методов, что уменьшает количество экспертных ошибок.
Предупреждение мертворождения
Предупреждение мертворождения включает комплекс оздоровительных мероприятий (гимнастика, прогулки, полноценное питание беременной, соблюдение режима труда и отдыха и пр.), особенно при отягощенном акушерском анамнезе (смерть плода в прошлом), при заболеваниях женщины, могущих вызвать впоследствии гибель плода при беременности (сахарный диабет, пороки сердца, гипертоническая болезнь, заболевания половых органов, Токсоплазмоз и др.), а также при антенатальной патологии (см.). При возможности проводят медико-генетическую консультацию (см.). Беременных, имеющих ту или иную патологию, для профилактики самопроизвольных абортов или гибели жизнеспособного плода направляют в специализированный стационар для контроля за состоянием беременной и плода и соответствующего лечения (см. Антенатальная охрана плода).
Библиография: Буров С. А. и Резников Б. Д. Рентгенология в судебной медицине, с. 206, Саратов, 1975; Грищенко В. И. и Яковлева А. Д. Антенатальная смерть плода, М., 1978, библиогр.; Диллон Я. Г. Рентгенологическая жизненная проба и ее обоснование, Вестн, рентгенол., т. 23, № 2, с. 91, 1939; Поттер Э. Патологическая анатомия плодов, новорожденных и детей раннего возраста, пер. с англ., М., 1971, библиогр.; Церковный Г. Ф., Фролова О. Г. и Кобозева Н. В. О статистических критериях перинатального периода, Акуш, и гинек., № 3, с. 24, 1976; Ellenbogen L. S., Bayer H. a. Gottlie b M. Roentgen demonstration of gas in the fetal circulatory system, a valuable sign of fetal death, Radiology, v. 67, p. 410, 1956; Gruber Gas in the umbilical vessels as a sign of fetal death, ibid., v. 89, p. 881, 1967; Ylpоe A. Uber Magenatmung beirn Menschen, Biochem. Z., Bd 78, S. 273, 1917.
О. Г. Фролова; Т. E. Ивановская (пат. ан.), Г. А. Пашинян, П. П. Ширинекий (суд.), С. А. Свиридов (рент.).
Прижизненный некроз и посмертный аутолиз: проблема дифференциальной диагностики
Прижизненный некроз и посмертный аутолиз: проблема дифференциальной диагностики / Богомолова И.Н., Богомолов Д.В. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2012. — №12. — С. 25-31.
библиографическое описание:
Прижизненный некроз и посмертный аутолиз: проблема дифференциальной диагностики / Богомолова И.Н., Богомолов Д.В. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2012. — №12. — С. 25-31.
код для вставки на форум:
Аутолиз бывает не только посмертным, но и прижизненным - в виде распада отдельных органоидов клетки, клеток или части ткани (органа) при сохранении основных жизненных функций целого организма. Прижизненный аутолиз представляет собой одну из форм клеточного некроза, при которой ферменты, осуществляющие распад, происходят из самой клетки, - колликвационный некроз. Коагуляция белков, напротив, препятствует аутолизу. Кроме того, аутолиз часто начинается еще в период обратимых изменений, т. е. еще до момента смерти клетки или организма.
В доступной литературе нам не удалось найти критериев различия посмертного аутолиза и прижизненного некроза и даже просто подробных описаний светооптической картины аутолиза всех органов и тканей, соответствующих реально наблюдаемым без привлечения сложных гистохимических и т.д. методов. Большинство авторов ссылаются на мутность цитоплазмы, но слово «мутность» означает утрату прозрачности. Оценить прозрачность на окрашенных гистопрепаратах практически невозможно! Авторы пишут о зернистости цитоплазмы, вакуолизации ее и ядра, фрагментации и извитости мышечных волокон [2, 3, 4].
Но эти же изменения описаны как диагностические признаки различных прижизненных синдромов [1, 3, 4, 5]. Как же их интерпретировать?
Материалом для данного исследования послужили 683 набора образцов органов и тканей от трупов, исследованных в различных бюро судебно-медицинской экспертизы Российской Федерации, а также акты судебно-медицинского исследования трупа и заключения экспертов. Среди погибших была 181 женщина. Возраст их варьировал от 1 до 98 лет. Во всех случаях были известны причина и давность смерти. Интервал времени между смертью и изъятием и фиксацией материала составлял не менее суток. 202 человека умерли в стационаре через сроки от нескольких минут до 47 суток с момента поступления, и еще один скончался в машине «скорой помощи».
Для сравнения использовался биопсийный и операционный (прижизненный) материал, полученный на базе ПАО ГКБ № 50 г. Москвы и в ходе проведения патологоанатомических исследований, а также образцы органов и тканей от 20 трупов с выраженными аутолитическими и гнилостными изменениями.
Во всех случаях проводилось стандартное гистологической исследование с парафиновой заливкой, окраской гематоксилином и эозином и световой микроскопией. Для исследования скелетных мышц и миокарда использовались либо целлоидиновая заливка и просмотр с полузакрытой диафрагмой, либо поляризационная микроскопия.
Полученные результаты можно резюмировать следующим образом. Посмертный аутолиз относят к ранним трупным изменениям, поскольку он начинается в 1-е сутки после смерти, однако в более позднем периоде он продолжается наряду с поздними трупными изменениями.
Проявления аутолиза на светооптическом уровне:
- временное увеличение размеров ядра вследствие его набухания;
- просветление нуклеоплазмы;
- появление в ядре оптических пустот;
- резко выраженная агрегация хроматина с преимущественным скоплением вдоль ядерной оболочки и вокруг ядрышек; проявляется как подчеркнутость и извилистость наружного контура ядра;
- кариопикноз - сжатие ядра в плотную массу с интенсивной окраской (при разрыве ядерной оболочки и выходе воды и других компонентов в цитоплазму);
- кариорексис - распад ядер на фрагменты, ассоциированный с маргинацией хроматина и гиперхромазией;
- кариолизис - утрата четкости контуров и последующее растворение ядра;
- набухание цитоплазмы, изменение ее тинкториальных свойств (возможно любое - гипохромазия, эозиноили базофилия и даже амбифильность), иногда появление в ней мелких жировых и гидропических вакуолей, утрата четкости ее контуров и постепенное растворение;
- ослабление связей межу клетками, которое проявляется в виде отторжения пластов эндотелия сосудов и эпителия (повреждение менее прочных связей между клетками и мембранами при относительной сохранности десмосом), дискомплексации трабекулярных структур (в печени, пучковой зоне надпочечников), диссоциации клеток (особенно в железах ацинарного строения);
- базофильный отек стромы с набуханием волокон;
- разрушение эластических мембран, распад волокон соединительной ткани и, наконец, полная потеря структуры ткани и гомогенизация ее образцов.
- 1) равномерности посмертных аутолитических изменений (они приблизительно одинаково выражены в разных полях зрения, разных частях органа и разных органах);
- 2) отсутствии реакции организма (сосудистой, клеточной и т.д.);
- 3) наличии гемолиза, степень выраженности которого параллельна степени аутолиза паренхимы;
- 4) сведениях о давности наступления смерти и условиях хранения трупа.
Конкретно по органам аутолиз развивается и проявляется следующим образом.
МОЗГ. Аутолиз в ткани головного мозга проявляется диффузными кариолизом (побледнением и утратой четкости контуров ядра вплоть до полного исчезновения), хроматолизом (побледнением и растворением вещества Ниссля) и цитолизом (аналогичными изменениями цитоплазмы).
На определенном этапе аутолиза ядра клеток набухают, увеличиваются в размерах, в них появляются просветления, а хроматин конденсируется в области ядерной мембраны и ядрышка.
Аутолиз нейронов может проявляться и кариопикнозом - изменениями ядра, при которых оно уменьшается в размерах, становится гомогенным и интенсивно базофильным. Такие изменения объясняют тем, что оболочка ядра разрывается и жидкое содержимое выходит в цитоплазму.
Посмертный аутолиз и прижизненные повреждения нейронов имеют одинаковые механизмы развития и сходную морфологическую картину, поэтому их не всегда можно различить. Решающую роль в их дифференциальной диагностике имеет сопоставление характера и степени изменений разных клеток, полей зрения, частей мозга и вообще органов. Изменения, вызванные прижизненным повреждением, либо не достигают такой распространенности и имеют очаговый характер, либо сопровождаются клеточной глиальной реакцией. Кроме того, при посмертном аутолизе бледнеют и постепенно растворяются также ядра глиоцитов, развивается пикноз ядер эндотелия капилляров, гемолиз содержимого более крупных сосудов и слущивание их эндотелия.
ЛЕГКИЕ. Аутолиз легких вначале выражается в лизисе ядер и десквамации альвеолярных макрофагов. Далее такие же изменения происходят с альвеолярным и бронхиальным эпителием, а в сосудах развивается гемолиз эритроцитов (обесцвечивание, потеря четкости контуров и при полнокр овии - слияние в гомогенную эозинофильную массу, иногда с оранжевым или коричневатым оттенком, а при малокровии - образование хлопьев). Последними подвергаются кариолизу эндотелий капилляров, клетки стенок более крупных сосудов и лимфоциты, входящие в состав БАЛТ - бронхассоциированной лимфоидной ткани. Если в альвеолах имеется гнойный экссудат, то ядра сегментоядерных лейкоцитов также сохраняются дольше, чем эпителий. На этих стадиях аутолиза возможно выявление таких изменений, как полнокровие сосудов и кровоизлияния (они видны до полного обесцвечивания гемоглобина), отек легких, фибрин и лейкоциты, гемосидероз, склеротические процессы и т.д.
При далеко зашедшем аутолизе набухают, бледнеют и теряют четкость контуров структуры, окрашиваемые эозином - цитоплазмы клеток, волокна соединительной ткани, стенки сосудов, бронхов и альвеол.
СЕРДЦЕ. Посмертный аутолиз сердца начинается с изменений эндотелия интрамуральных артерий. Он набухает, приобретает вертикальное (перпендикулярное к базальной мембране) положение и, наконец, полностью слущивается в просвет сосудов.
Далее происходит лизис ядер кардиомиоцитов. Их поперечная исчерченность и липофусцин могут сохраняться дольше.
Следующая стадия аутолиза сердца включает гемолиз, а также лизис ядер клеток стромы и стенок сосудов.
Контуры кардиомиоцитов, сосудов и соединительнотканных прослоек сохраняются довольно долго, медленно теряя четкость. В этот период еще можно выявить диссоциацию, волнообразную извитость и фрагментацию кардиомиоцитов, их гипер- и атрофию, зернистый и глыбчатый распад, кардиосклероз, стромальный липоматоз. Особо подчеркнем, что при трупном аутолизе подобные изменения не возникают.
ЖЕЛУДОЧНО-КИШЕЧНЫЙ ТРАКТ. Аутолиз желудка и кишечника развивается быстро ввиду богатства этих органов ферментами. Раньше всего десквамируется покровный эпителий. Затем начинаются изменения железистого - кариолиз и/или кариопикноз, потом дискомплексация желез и, наконец, полная потеря структуры и превращение ткани в гомогенную массу. Гемолиз и аутолиз стенок сосудов обычно развиваются позже.
ПЕЧЕНЬ. Аутолиз печени в первую очередь проявляется маргинацией хроматина и последующим лизисом ядер гепатоцитов. Далее начинают растворяться ядра других клеток (звездчатых ретикулоэндотелиоцитов и т.д.), а в цитоплазме гепатоцитов может появиться много мелких округлых вакуолей вследствие распада липопротеидов и высвобождения липидов. Крупные вакуоли при аутолизе не образуются вообще, а мелкие - не всегда. Балочное строение печени и отложения пигмента в гепатоцитах сохраняются долго, даже при гниении.
Прижизненная жировая дистрофия обычно отличается от посмертного липофанероза характерным расположением (перипортально, перицентрально или диссеминированно среди лишенных вакуолей клеток) и крупными размерами капель в очаге при отсутствии их вне очага. Жировая дистрофия может выявляться даже при далеко зашедшем аутолизе, когда ядра гепатоцитов почти не определяются, а цитоплазма становится амбифильной (сиреневой).
В портальных трактах аутолиз начинается с гемолиза, лизиса ядер эндотелия сосудов и его десквамации. Воспалительные инфильтраты и признаки склеротических процессов сохраняются долго.
В центральных венах происходит гемолиз и гомогенизация стенок, к оторые перестают контурироваться. Однако за счет сохранения гистоархите ктоники долек места, где должны находиться центральные вены, определяются четко.
На последних стадиях аутолиза структура печени почти стерта, базофильные структуры (кроме колоний микробов) отсутствуют, но контуры портальных трактов, центральных вен и балок еще прослеживаются, хотя и теряют четкость.
ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА. Эпителий протоков поджелудочной железы подвергается аутолизу особенно рано - ядра лизируются или пикнотизируются, клетки десквамируются. Далее начинается кариолизис в экскреторной паренхиме, причем, в отличие от других органов, неравномерно, полями, чаще вблизи протоков. Это связано с различиями ферментативной активности в разных ацинусах и клетках. Цитоплазма клеток приобретает базофильный оттенок, увеличивается в объеме, потом уменьшается, и начинается дискомплексация ацинусов, потом стирание их структуры. Островки также постепенно становятся неразличимыми, но держатся дольше. Клетки воспалительных инфильтратов, волокна стромы, жировые клетки и контуры сосудов сохраняются долго.
Аутолиз жировой ткани при липоматозе проявляется в виде лизиса ядер и деформации контуров клеток. Оценить распространенность липоматоза можно даже при далеко зашедшем аутолизе. Если в аутолизированной паренхиме поджелудочной железы встречаются округлые просветления, оптически пустые или с базофильным оттенком, то это проявления внутридолькового липоматоза - аутолизированные жировые клетки.
Последний этап аутолиза состоит в постепенном исчезновении контуров клеток и волокон, стирании структуры и гомогенизации ткани.
ПОЧКИ. Первыми проявлениями аутолиза в почке обычно служит кариолиз в извитых канальцах. При этом очень трудно отдифференцировать некротический нефроз (прижизненную гибель нефротелия) от трупного аутолиза.
Одним из признаков может служить дистрофия. Некроз всегда развивается в результате тяжелого дистрофического процесса. Если признаки баллонной, гиалиново-капельной, пигментной или тяжелой жировой дистрофии отсутствуют, цитоплазма диффузно окрашена эозином и однородна, зерниста или содержит мелкие, придающие цитоплазме вид пены вакуоли, то кариолиз обычно оказывается посмертным.
Некротический нефроз обычно развивается на фоне ишемии коры. Полнокровная кора почек - один из аргументов в пользу посмертного кариолиза.
Кроме того, если имеются признаки гемолиза, то и нефротелий должен успеть аутолизироваться.
Если аутолиз затрагивает более резистентные к нему структуры - нефротелий дистальных канальцев и петель Генле, клетки клубочков и сосудов, то его посмертный характер очевиден; однако нельзя исключить, что имелся и некротический нефроз, к которому позже присоединился аутолиз.
Эпителий аутолизированных канальцев десквамируется в их просвет, и структура почки постепенно стирается.
Прижизненная дистрофия сохраняется и посмертно, в том числе при полном кариолизе. Посмертная вакуолизация цитоплазмы, имитирующая прижизненную дистрофию, встречается редко и выражена слабо.
СЕЛЕЗЕНКА. Аутолиз селезенки начинается с гемолиза крови, находящейся в ее синусоидах и других сосудах. Далее развивается кариорексис и кариолиз ядер лимфоцитов белой и красной пульпы. Границы фолликулов становятся все менее четкими. Эндотелий сосудов десквамируется. Лизируются ядра макрофагов, клеток, входящих в состав стенок сосудов и трабекул. На поздних этапах сохраняются только контуры капсулы, трабекул и сосудов, которые постепенно теряют четкость.
НАДПОЧЕЧНИКИ. Аутолиз надпочечников начинается с кариолиза клеток сетчатого слоя и мозгового вещества. Он начинается очагово и может имитировать прижизненный некроз. Чтобы различить прижизненную и посмертную гибель клеток, надо при вырезке, заливке и нарезке стараться, чтобы хотя бы остатки мозгового вещества попали в препарат. Сохранность мозгового вещества при наличии очагов кариолиза в корковом слое доказывает прижизненность последнего, а она - факт стресс-реакции в фазе истощения.
Далее кариолиз становится диффузным, присоединяется базофилия цитоплазмы и дискомплексация клеток.
Когда аутолиз распространяется на все слои, его проявления зависят от степени их делипоидизации. Если количество липидов велико, то в гомогенизирующейся, безъядерной ткани видно много жировых капель, деформирующихся и сливающихся. Таким образом, делипоидизацию - признак стресс-реакции - можно обнаружить даже при далеко зашедшем аутолизе. Ядра эндотелия сохраняются дольше, и их расположение подчеркивает контуры структур коры. После их лизиса в течение некоторого времени еще можно определить толщину и состояние каждого слоя коры, потом характерное расположение клеток в виде клубочков, пучков или сетки стирается.
ПРОЧИЕ ТКАНИ И ОРГАНЫ.
Аутолиз эпидермиса либо сочетается с гниением, либо протекает в особой форме, именуемой мацерацией. Поэтому его надлежит рассматривать отдельно.
Аутолиз жировой ткани проявляется кариолизисом, деформацией клеток и слиянием жировых капель.
В поперечнополосатых мышцах аутолиз ведет к лизису ядер и постепенной гомогенизации миоплазмы. Вопреки утверждениям ряда авторов, зернистой она не становится.
В сосудах относительно рано начинают определяться изменения эндотелия. Он вначале приобретает положение, перпендикулярное к стенке сосуда, затем пластами десквамируется, причем в артериях этот процесс происходит раньше, чем в венах. Следующим этапом становится растворение его ядер и ядер других клеток, слагающих сосудистую стенку. Однако очертания клеток и волокон сохраняются долго, благодаря чему можно различать слои стенок сосудов и устанавливать их толщину.
В крови происходит обесцвечивание и деформация эритроцитов, затем они гемолизируются и сливаются в гомогенную массу, иногда имеющую оранжевый или буроватый оттенок за счет остатков гемоглобина.
В щитовидной железе аутолиз проявляется десквамацией эпителия фолликулов и кариолизисом в нем.
В тестикулах такие же изменения происходят со сперматогенным эпителием, а в простате - с железистым.
ГНИЕНИЕ. Микроскопически гниение проявляется прежде всего появлением колоний микробов в сосудах, потом - вне их, в тканях. При медленной смерти микробы распространяются из кишечника с кровотоком еще в период агонии. Затем начинается образование гнилостных пузырей, разрывающих аутолизированные ткани. Аутолиз не прекращается с началом гниения, и главную роль в стирании структуры тканей играет именно он. Поэт ому при выраженном гниении, но умеренном аутолизе основные тканевые структуры еще доступны оценке, а при обратном соотношении этих проце ссов - уже нет.
Судебно-гистологическое исследование внутренних органов при аутолизе затруднено, однако многие признаки продолжают определяться. Даже при далеко зашедшем аутолизе выявляются степень кровенаполнения сосудов и воздушности ткани легких, склероз и липоматоз стромы органов, нарушения пигментного обмена, жировая дистрофия печени. В канальцах нефротелия можно определить вид дистрофии. Клетки воспалительных инфильтратов нередко сохраняются дольше паренхимы, позволяя уточнить состав инфильтрата даже при выраженном аутолизе. Через трое суток пребывания трупа или трупного материала при комнатной температуре в клетках отчетливо выявляется липофусцин, в мышечных волокнах - поперечная исчерченность, в сосудах можно оценить состояние всех слоев стенки. Не является аутолиз препятствием и для выявления кровоизлияний.
Таким образом, наши данные позволяют во многих случаях отличить прижизненные изменения тканей от посмертного аутолиза.
- Капустин, А. В. О диагностическом значении острых микроскопических изменений миокарда / А. В. Капустин // Судебно-медицинская экспертиза. - 2000. - Т. 43, № 1. - С. 7-11.
- Лушников, Е. Ф. Аутолиз (морфология и механизмы развития) / Е. Ф. Лушников, Н. А. Шапиро. - М.: Медицина, 1974. - 200 с.
- Науменко, В. Г. Гистологический и цитологический методы исследования в судебной медицине: рук. / В. Г. Науменко, Н. А. Митяева. - М.: Медицина, 1980. - 334 с.
- Пермяков, А. В. Судебно-медицинская гистология: рук. для врачей / А. В. Пермяков, В. И. Витер, Н. И. Неволин. - 2-е изд. - Ижевск; Екатеринбург: Экспертиза, 2003. - 214 с.
- Пиголкин, Ю. И. Атлас по судебной медицине / под ред. Ю. И. Пиголкина, И. Н. Богомоловой. - М.: МИА, 2006. - 310 с.
похожие статьи
К вопросу об определении давности смерти при аутолитических изменениях некоторых органов (по данным литературы) / Хорошилова А.С., Власюк И.В., Авдеев А.И. // Избранные вопросы судебно-медицинской экспертизы. — Хабаровск, 2019. — №18. — С. 194-199.
Автолиз
Авто́лиз, ауто́лиз, самоперева́ривание (от др.-греч. αὐτός — сам и λύσις — разложение, распад) — саморастворение живых клеток и тканей под действием их собственных гидролитических ферментов, разрушающих структурные молекулы. Происходит в организме при некоторых физиологических процессах (например, метаморфоз, автотомия и др.), в очагах омертвения, а также после смерти. Автолиз микроорганизмов происходит при старении микробной культуры или повреждении клеток различными агентами.
В норме процессы автолиза сопровождают многие явления, связанные с развитием организма и дифференцировкой клеток. Так, автолиз клеток описывается как механизм разрушения тканей у личинок насекомых при полном превращении, а также при рассасывании хвоста у головастика. Правда, эти описания относятся к периоду, когда различия между апоптозом и некрозом ещё не были установлены, и в каждом случае требуется выяснять, не лежит ли на самом деле в основе деградации органа или ткани апоптоз, не связанный с автолизом.
Профессор А. М. Уголев также говорит о таком явлении, как индуцированный аутолиз. Описывая его как результат лабораторных экспериментов, в результате проведения которых было выяснено, например, что помещённые в камеру с человеческим желудочным соком «живая» и прошедшая термическую обработку лягушки разлагались с разной скоростью. «Живая» растворялась полностью за 2-3 дня, в то время как прошедшая термическую обработку за этот период в значительной мере сохранялась. Также примером индуцированного аутолиза можно назвать процесс переваривания удавом проглоченного кролика, когда переваривание жертвы осуществляется не только за счёт ферментов желудочного сока хищника, но и сам организм жертвы будет аутолизироваться за счёт индуцированного аутолиза. Кроме этого, профессор Уголев А. М. считал, что именно аутолиз представляет собой настоящую ценность пищи для организма.
У растений автолизом сопровождается дифференциация клеток, которые функционируют после смерти (например, трахеид или члеников сосудов). Частичный автолиз происходит и при созревании клеток флоэмы — члеников ситовидных трубок.
Виды аутолиза
Исходя из видов разложения тканей, выделяют следующие виды аутолиза:
- Прижизненный аутолиз — происходит в живом организме и включает в себя процесс изменения отдельных типов тканей, плода или конкретной клетки, которая подверглась физиологическому воздействию (инволюцияматки после родов, инволюция молочной железы после прекращения секреции молока, инволюции вилочковой железы, а также в атрофии тканей после их денервации);
- Посмертный аутолиз — возникает после смерти живого организма. Ввиду того, что наибольшее количество катепсинов находится в поджелудочной железе, печени, селезёнке и почках, аутолиз в этих тканях после смерти возникает раньше, чем в других.
Практическое применение
В виноделии
При выработке игристых вин проводится долговременная выдержка (9 месяцев и более) на осадке, состоящем из отмерших после завершения брожения дрожжевых клеток. За это время происходит частичный автолиз дрожжей, приводящий к попаданию его продуктов в вино, что способствует обогащению букета вина. Размер дрожжевой клетки при этом заметно уменьшается, но клеточная стенка не разрушается. Форма клетки изменяется, из овально-округлой принимая чрезвычайно сморщенную форму.
Результатом автолиза являются характерные (так называемые «лизатные») тона в вине — нюансы аромата, напоминающие корочку свежевыпеченного хлеба, крекеров, иногда сушёных грибов, вплоть до небольших нефтяных оттенков.
Созревание (выдержка) мяса
После прекращения жизни животного, в связи с прекращением поступления кислорода, отсутствием окислительных превращений и кровообращения, торможением синтеза и выработки энергии, накопления в тканях конечных продуктов обмена и нарушения осмотического давления клеток, в мясе имеет место самораспад прижизненных систем и самопроизвольное развитие ферментативных процессов, которые сохраняют свою каталитическую активность долгое время. В результате их развития происходит распад тканевых компонентов, изменяются качественные характеристики мяса (механическая прочность, уровень водосвязывающей способности, вкус, цвет, аромат) и его устойчивость к микробиологическим процессам.
В основе автолитических превращений мяса лежат изменения углеводной системы, системы ресинтеза АТФ и состояния миофибриллярных белков, входящих в систему сокращения.
В медицине
В некоторых видах нетрадиционной медицины процесс аутолиза используется с целью избавления от опухолей и других наростов в организме, используя одно из свойств аутолиза, а именно первоочередность «самопереваривания» тех образований, которые представляют наименьшую ценность для организма.
Трупный аутолиз
Трупный аутолиз - разрушение тканей их собственными протеолитическими ферментами, в основном лизосомальными. Макроскопически аутолиз проявляется размягчением и разжижением тканей. Первыми подвергаются этому процессу ткани, богатые ферментами, - слизистая оболочка желудка и кишечника, поджелудочная железа, мозговое вещество надпочечников.
Определение давности наступления смерти по выраженности аутолиза
Для определения давности наступления смерти можно исследовать выраженность аутолиза гистологическим методом. Судебно-гистологическое исследование внутренних органов при этом проводится по стандартным методикам, но дополняется измерением основных микроскопических структур внутренних органов, так как их линейные размеры и объемные соотношения заметно меняются в ходе посмертного аутолиза.
Через 6 ч после наступления смерти во всех паренхиматозных органах отмечаются нарушения кровераспределения в виде неравномерного кровенаполнения, свежих экстравазатов, дистонии сосудов, стазов. Гистоархитектоника органов на этой стадии сохраняется.
Через 12 ч наблюдаются набухание базальных мембран капилляров и кариопикноз в эндотелиоцитах, эндотелиальная выстилка вен прослеживается с трудом. Стенки артерий отекают, ядра гладкомышечных клеток сосудов приобретают извитую форму. Нарастают явления гемолиза. В паренхиме начинают определяться аутолитические изменения (десквамация бронхиального и альвеолярного эпителия, набухание ядер и фрагментация кардиомиоцитов, мелкая базофильная зернистость и вакуолизация гепатоцитов с маргинацией ядерного хроматина, уменьшение диаметра клубочков почек при расширении капсулы, набухание и зернистая дистрофия нефротелия канальцев, участки запустевания в красной пульпе селезенки и в герминативных центрах ее фолликулов, подчеркивание ее ретикулярной стромы, обеднение лимфоидных структур клетками).
К 18 ч заметно убывает число ядер клеток в поле зрения, появляются ядра-тени, повсеместно наблюдается отек интерстиция, структурные элементы органов видны нечетко, с явлениями специфичной для каждого органа дегенерации, увеличивается количество продуктов распада элементов крови. К 24 ч в миокарде появляются признаки фрагментарного распада кардиомиоцитов, в легких прогрессирует разрушение альвеолярных перегородок, в почках наблюдается десквамация эпителия проксимальных канальцев, в дистальном отделе нефронов формируются различные цилиндры, красная пульпа селезенки представлена гомогенной розовой массой, фолликулы определяются с трудом. К 36 ч гистоархитектоника органов определяется нечетко, элементы паренхимы и стромы различаются лишь контурно, бóльшая часть клеток в состоянии аутолиза. В дальнейшем явления аутолиза прогрессирующе нарастают. При этом структурные элементы внутренних органов все еще поддаются измерению и соответствующие числовые параметры увеличиваются, что позволяет судить о давности наступления смерти. Так, наблюдается рост относительной площади аутолизированной ткани (для печени с 8,4±1,2% через 6 ч после смерти до 52,6±2,5% через 72 ч). В селезенке и лимфатических узлах наблюдается относительный рост доли ретикулярных клеток и макрофагов за счет убыли лимфоидных клеток. Комплексный математический анализ цифровых данных помогает уточнить давность наступления смерти.
Другим способом объективной количественной оценки степени аутолиза является применение электрофизических методов, например посмертной импедансометрии с помощью реографа. Омическая составляющая импеданса обусловлена целостью клеточных мембран и закономерно изменяется в раннем посмертном периоде. Внедряются в практику методы определения относительной диэлектрической проницаемости различных тканей трупа в условиях 10-сантиметровых радиоволн. С этой же целью используется метод электронного парамагнитного резонанса, который наиболее эффективен для определения давности наступления смерти через 6 сут после нее и более.
Аутолиз относят к ранним трупным изменениям, поскольку он начинается в 1-е сутки после смерти, однако в более позднем периоде он продолжается наряду с поздними трупными изменениями.
АУТОЛИЗ
АУТОЛИЗ, автолиз (греческий autos сам + lysis разрушение) — распад белков тканей организма, происходящий под влиянием специфических клеточных ферментов этих тканей (катепсинов и др.). Оптимум pH катепсинов лежит в пределах 3—5, далеких от pH нормальных тканей (6,8—7,2), вследствие чего при жизни организма они обладают незначительной активностью и распад белков, вызываемый катепсинами, полностью компенсируется синтезом белков в процессе их обновления.
Кроме того, катепсины, а также другие гидролитические ферменты, активные в кислой среде, практически изолированы от неповрежденных тканей и находятся главным образом в лизосомах (см.) — особых клеточных органеллах, отделенных от цитоплазмы мембраной. После гибели организма либо при некрозе тканей под влиянием травмы или других причин, не связанных с деятельностью патогенных микробов, происходит разрушение лизосом, а pH тканей быстро сдвигается в кислую сторону вследствие ослабления аэробных окислительных процессов и усиления гликолиза (см.). В этих условиях активность катепсинов резко усиливается, распад белков погибших клеток повышается и происходит самопереваривание клеток — аутолиз. Наибольшее количество катепсинов находится в поджелудочной железе, печени, селезенке и почках, в связи с чем аутолиз в этих тканях после смерти возникает раньше, чем в других.
В некоторых случаях аутолиз тканей может происходить и в нормальных условиях. Так, аутолиз играет большую роль в инволюции матки после родов, молочной железы после прекращения секреции молока, инволюции вилочковой железы, а также в атрофии тканей после их денервации. В этих случаях сдвиг pH в кислую сторону возникает вследствие уменьшения кровоснабжения и соответствующего снижения окислительных процессов.
Читайте также:
