Эмбриогенез человека. Зародошевые и стволовые клетки
Добавил пользователь Skiper Обновлено: 29.01.2026
АМНИОТИЧЕСКАЯ ОБОЛОЧКА - состоит из однослойного призматического эпителия и внезародышевой соединительной ткани.
Строму (основу) хориальной пластины и ворсин составляет рыхлая соединительная ткань (содержит аморфное вещество, аргирофтльные волокна, множество капилляров и клетки Кащенко-Ховбауэра - примитивные макрофаги). Сверху пластины покрыты трофобластным эпителием. В первом триместре покрыты цитотрофобластом, во втором покрыты цито- и симпластотрофобластом. В третьем - фибриноидом (гомогенная оксифильная масса, которая является продуктом сыворотки крови и распада трофобластных элементов). В ходе беременности ворсины сильно увеличиваются в размерах и возрастает их ветвление. Они собираются группами по 15-16 штук и формируют котиледоны (группа ворсин, связанная с помощью ствола ворсин с хориальной пластинкой). Выделяют якорные ворсины (соприкасаются с материнской тканью) и конечные ворсины (соприкасаются с материнской кровью). Образуется соединительная ткань: септы на границе между котиледонами.
Материнская часть
ОСНОВНАЯ ОТПАДАЮЩАЯ ОБОЛОЧКА (базальная пластина)
ЛАКУНЫ, ЗАПОЛНЕННЫЕ МАТЕРИНСКОЙ КРОВЬЮ
В соединительнотканной слизистой оболочке появляются децидуальные клетки (те же соединительнотканные клетки крупных размеров и богатые гликогеном. Увеличивается просвет сосудов и гидратация слизистой, появляется исключительная фагоцитарная активность
ФУНКЦИИ ПЛАЦЕНТЫ:
Ионы Ca, Fe, Zn, Mg, Cu, P
Депонирует и содержит витамины групп: A, B1, B2, B6, C, D, E
Факторы свертывания крови
Эндокринная - все гормоны синтезируются симпластотрофобластом. Они необходимы для роста и развития плода, готовят организм матери к родам и лактации.
хорионический гонадотропин (поддержание желтого тела, выделяется с первых дней беременности, действует на желтое тело и стимулирует секрецию прогестеронов и эстрогенов, которые действуют на эндометрий, вызывая рост зародыша
хорионический соматомаммотропин (действует на молочную железу и желтое тело, вызывая изменения в организме матери)
кортиколиберин (определяет срок наступления родов)
МЕХАНИЗМЫ ЗАЩИТЫ ПЛОДА: симпластотрофобласт - синтезирует белки тормозящие иммунный ответ матери, гормоны плаценты - угнетают материнские лимфоциты, фибриноид плаценты
Барьерная (защитная) - выражена слабо, поэтому проникают наркотики, алкоголь, никотин, яды, лекарства (антибиотики, сульфаниламиды, анальгетики), вирусы, бактерии
ПЛАЦЕНТАРНЫЙ БАРЬЕР: барьер между кровью матери и плода. К барьеру подходят: цитотрофобласт с его базальной мембраной, соединительная ткань, строма ворсины, эндотелий кровеносного сосуда и его базальная мембрана. С материнской стороны кровь поступает в межворсинковое пространство через 30 спирально извитых артерий матки по давлением 70-80 мм рт. ст. Материнская кровь омывает ворсины, а затем скапливается на дне плацентарных отсеков, откуда уносится через краевой синус в маточные вены. Объем крови 150 мл.
Понятие и значение плацентации. Плацентация у человека: временная и морфологическая характеристика. Тип и строение сформированной плаценты.
Ядерный матриархат, LLPS-революция и анеуплоидия

Обзор
рисунок автора статьи
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Сегодня проблемы репродукции являются одними из самых обсуждаемых в мире. Но что мы знаем о молекулярной кухне процессов оо- и эмбриогенеза? Ученые из лаборатории морфологии клетки Института цитологии РАН попытались разобраться в закономерностях перестроек хроматина, протекающих в ядрах ооцитов и ранних эмбрионов млекопитающих, и предложили возможные эпигенетические механизмы регуляции данных процессов. Мне, в свою очередь, удалось заглянуть в закулисье и лично пообщаться с авторами статьи. Здесь я не просто хочу поделиться опытом коллег, предупреждающих о возможных трудностях в изучении данной темы. Я хочу объяснить, почему это настолько заинтересовало даже меня, молекулярного онколога, совершенно незнакомого с данной областью исследования.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Такие разные конфигурации
Ирина и Дмитрий Боголюбовы из Института цитологии РАН исследовали закономерности перестроек хроматина в ядрах ооцитов и ранних эмбрионов млекопитающих) и предложили возможные эпигенетические механизмы регуляции этих перестроек (рис. 1) [1], [2]. Но давайте обо всем поговорим по порядку, а вместе с тем послушаем мнение и самих авторов исследования.
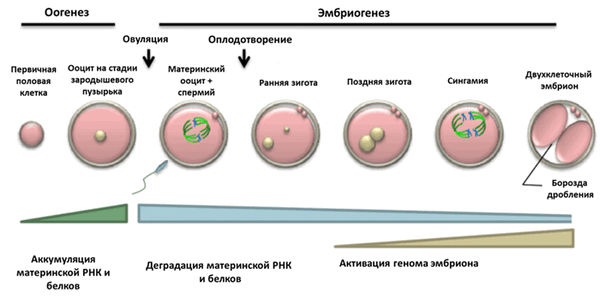
Рисунок 1. Основные стадии раннего развития.
Оогенез и эмбриогенез — это непрерывные, сменяющие друг друга процессы; происходящие в это время преобразования хроматина ооцита предопределяют дальнейшее развитие зиготы после оплодотворения. У некоторых млекопитающих, включая человека, на завершающей стадии развития ооцита перераспределение хроматина в ядре совпадает с преобразованием ядрышка в так называемые атипичные ядрышки или ядрышкоподобные тела (ЯПТ) . Образовавшиеся ЯПТ начинают созывать к себе повсеместно конденсирующийся хроматин, который постепенно окружает ЯПТ по типу «кольца», или, по-научному, хроматин переходит из NSN-состояния (non-surrounded nucleolus) в SN-состояние (surrounded nucleolus) (рис. 2). Почему атипичные ядрышки являются центрообразующей единицей для хроматина, вам не ответит даже самый опытный цитолог. Но давайте поговорим обо всем этом подробно.
ЯПТ (nucleolus-like body, NLB) — особенная ядерная структура, представляющая собой хромосомы, собранные вокруг центрального тела, состоящего преимущественно из фибриллярных белков (ламинов типа А и В). Точный состав центрального тела ЯПТ остается неизвестен [3].
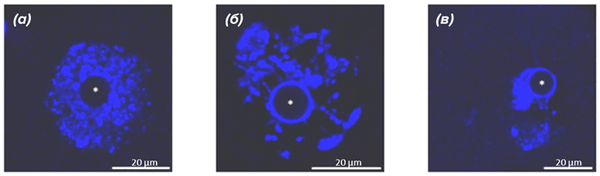
Рисунок 2. Различная конфигурация хроматина в мышиных ооцитах.
(а) — NSN-состояние;
(б) — раннее SN-состояние;
(в) — SN-состояние.
Первым, кто решил разобраться в хроматиновом безобразии, был Молсби Уиллетт Блэкман. Еще в 1901 г. Блэкман работал с хилоподами, правда, не с ооцитами, а со спермацитами (в которых происходят схожие с ооцитами процессы), и наблюдал конденсацию хроматина в ограниченном пространстве ядра на стадии диплотены профазы мейоза [4]. Данному явлению Блэкман дал название «кариосфера», и спорить с ним никто не стал. «Раз никто не спорит, — подумал Блэкман, — можно ввести в историю еще один термин — „кариосома“». Так кариосомой начали обозначать частный подтип кариосферы, когда гетерохроматиновые агрегаты не связаны с какими-либо экстрахроматиновыми включениями. Другой подтип кариосферы — те же самые гетерохроматиновые агрегаты, но уже окруженные внешней капсулой. Данному варианту был гордо присвоен термин «типичная кариосфера». Однако у млекопитающих, которые интересуют биологов больше всего, все совершенно иначе. Поэтому далее мы будем рассматривать процессы оогенеза и эмбриогенеза в контексте именно млекопитающих модельных объектов.
У человека, как и у мыши, хромосомный материал располагается вне экстрахромосомного элемента (тех самых ЯПТ). В таком случае принято говорить «инвертированная кариосфера» (рис. 3) [5].
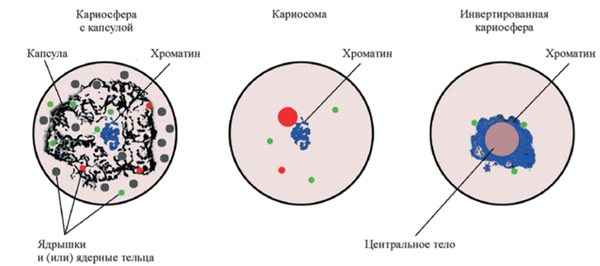
Рисунок 3. Основные типы кариосфер.
С терминологией немного разобрались. Вернемся к морфодинамике. В оогенезе, по мере перехода хроматина из NSN- в SN-состояние происходит инактивация транскрипционной активности ядра, и это очень важный параметр для дальнейшего завершения деления, созревания и осуществления правильного мейоза. Забегая вперед, можно сказать, что на начальных стадиях эмбриогенеза организация хроматина в зиготе морфологически поразительно похожа на таковую в ооцитах на поздних стадиях развития. За исключением того, что случается «рекапитуляция» транскрипционной активности, и она начинает волнообразно нарастать. Но редкая птица долетит до середины Днепра! Проблема заключается в том, что, если мы возьмем фолликулы одинакового размера в яичнике человека или мыши, то в них будут встречаться как SN-, так и NSN-ооциты, с постепенным увеличением процента SN-ооцитов в поздних антральных (готовых к овуляции) фолликулах. Тем не менее, какой-то процент NSN-ооцитов останется. Такие ооциты даже способны к оплодотворению, но развитие получившихся из них эмбрионов останавливается на двухклеточной стадии. Значимость перехода NSN—SN была подтверждена сравнением транскриптомных профилей: уровни мРНК большого набора генов, кодирующих материнские факторы, необходимые для расщепления и развития эмбриона, повышаются именно в SN-ооцитах. В связи с этим встает важный вопрос об отборе качественных ооцитов (например, для ЭКО), поскольку довольно трудно провести сегрегацию между SN- и NSN-ооцитами, полученными из антральных фолликулов одного размера. А размер для специалистов ЭКО имеет значение (как критерий оценки качества, разумеется).
Хорошо, с ооцитами стало понятнее. А у эмбрионов как обстоят дела?
Как уже говорилось ранее, морфологические картины, отражающие изменения конфигурации гетерохроматина в раннем эмбриогенезе, на первый взгляд, напоминают таковые в оогенезе. После оплодотворения ядро ооцита «разбирается», и в зиготе происходит формирование материнского и отцовского пронуклеусов de novo. В этом ведущую роль играют регуляторные белки материнского происхождения. На ранних стадиях эмбриогенеза тельца-предшественники ядрышек или ТПЯ (аналоги ЯПТ) служат платформой для формирования общего хроматинового ландшафта зиготы. Вокруг ТПЯ и ЯПТ конденсируется хроматин, образуя своеобразное гетерохроматиновое кольцо, содержащее области центромер и перицентромер. Именно пространственное расположение определенных гетерохроматиновых участков определяет дальнейшие стадии дробления зиготы (рис. 4).
Рисунок 4. Организация хроматина в ранних эмбрионах мышей, развивающихся in vivo.
(а) — зигота: mPN — материнский пронуклеус; pPN — отцовский пронуклеус; вокруг ТПЯ видны гетерохроматиновые кольца;
(б) — двухклеточная стадия: PB — полярное тело; на этом этапе начинают формироваться хромоцентры;
(в) — четырехклеточная стадия: видны многочисленные хромоцентры; гетерохроматиновые кольца вокруг некоторых ТПЯ начинают исчезать;
(г) — морула.
Мощным инструментом в изучении структуры гетерохроматина в ооцитах и зиготах млекопитающих является так называемая «энуклеоляция» — микрохирургическое удаление ЯПТ из ооцитов мыши и ТПЯ из пронуклеусов зигот. Так, было установлено, что ТПЯ/ЯПТ незаменимы для регуляции MaSat и MiSat вскоре после оплодотворения и служат основной структурой, организующей гетерохроматин в ооцитах и зиготах мышей.
MaSat (major satellite DNA, перицентромерный мажорный сателлит) и MiSat (minor satellite DNA, центромерный минорный сателлит) — повторяющиеся участки некодирующей ДНК, образующие тандемные повторы. Различия, главным образом, заключаются в количестве повторяющихся нуклеотидных мономеров и их локализации [6].
Состав самих ЯПТ (как и ТПЯ) пока остается малоизученным. Все дело в том, что на морфологическом уровне компактизация фибриллярных волокон атипичных ядрышек настолько плотная, что не все антитела, использующиеся в традиционных методах выявления белков-мишеней (например, вестерн-блот и иммуноцитохимический анализ), физически могут «достать» свою мишень [7]. Однако доподлинно известно, что ЯПТ и ТПЯ формируются схожим, весьма необычным, образом [8]. «Сейчас в биологии происходит настоящая LLPS-революция (LLPS: liquid-liquid phase separation) [9], т.е. изучается процесс формирования биомакромолекулярных конденсатов, возникающих в результате разделения жидких фаз. Сборка, разборка атипичных ядрышек и телец-предшественников ядрышек, как и протекание дальнейших процессов реорганизации хроматина также определяется законами фазового перехода», — комментирует доктор биологических наук, один из авторов обозреваемой статьи, Дмитрий Сергеевич Боголюбов.
Если все так сложно реализуется уже на уровне макромолекулярных комплексов — что уж говорить про геномный уровень?
Тут правильнее сказать — эпигеномный. В оогенезе и раннем развитии млекопитающих функциональная активность хроматина в значительной степени регулируется уникальным эпигенетическим ландшафтом. В его создании принимают участие следующие процессы [10]:
- пострепликационные модификации ДНК;
- посттрансляционные модификации ДНК-связывающих белков;
- АТФ-зависимое ремоделирование нуклеосом.
Казалось бы, ключевые эпигенетические игроки проанализированы и хорошо изучены. Однако полногеномных исследований с разрешением до одной клетки (single-cell sequencing), позволяющих установить корреляцию между SN- и NSN-состояниями хроматина, на данный момент не так уж много [11], [12]. Еще бы, ведь энуклеоляция с последующим анализом ядра каждой отдельной клетки — задачи не из легких.
Поскольку на поздних стадиях оогенеза происходит инактивация транскрипционной активности ядра, логично предположить, что в районах активно транскрибирующихся генов появляется определенный стоп-сигнал для транскрипционных или хроматин-ремодулирующих факторов, который всем своим видом провозглашает, что сейчас не время для транскрипции. Метилирование ДНК, которое изменяет сайты связывания ряда факторов транскрипции, является таким стоп-сигналом. Метильные группы обнаруживаются в динуклеотидах CpG, которые часто присутствуют в богатых CpG областях генома, называемых CpG-островками. В ооцитах, взятых из примордиальных (зародышевых) фолликулов, ДНК практически не метилирована по сравнению с ооцитами, присутствующими в антральных фолликулах, которые демонстрируют примерно 40% глобального метилирования ДНК. Кроме того, метилирование ДНК «конкурирует» с метилированием гистонов. Например, гистон H3 должен быть триметилирован по лизину 36 (H3K36me3), но не должен быть ди- или триметилирован по лизину 4 (H3K4me2/me3) и лизину 9 (H3K9me2) в областях, предназначенных для метилирования ДНК. Но стоит только часам пробить полночь, а оплодотворению случиться, как несущаяся карета метилирования генома превращается в тыкву деметилирование. Деметилироваться отцовскому и материнскому геномам помогают ДНК-метилтрансферазы DNMT3a и DNMT, опосредующие присутствие и отсутствие метильных групп на 5-метилцитозинах (5mC) и 5-гидроксиметилцитозинах (5hmC). После такого глобального сброса настроек ДНК в зиготе уже метилируется de novo; запускается процесс дробления.
В то время как с самой ДНК все просто (либо метилирована, либо нет), от разнообразия ковалентных гистоновых модификаций, определяющих гистоновый код, голова идет кругом. Здесь нужно пояснить, что гистоновый код — это посттрансляционные модификации определенных аминокислотных остатков гистонов на N-терминальном конце, например, ацетилирование, метилирование, фосфорилирование, убиквитинирование или рибозилирование. Гистоновые модификации необходимы для привлечения хроматин-ремодулирующих белков и, как следствие, для поддержания определенного состояния хроматина. Следует учитывать, что гистоновые модификации довольно видоспецифичны. Тем не менее, общей тенденцией для репрограммирования хроматина как в ооцитах, так и в зиготах млекопитающих, является метилирование гистона Н3 (H3K4me2, H3K4me3, H3K9me2 и H3K9me3) и ацетилирование гистонов Н3 и Н4 (H3K9ac, H3K18ac, H4K5ac и H4K12ac). К примеру, репрезентативными метками «активного» состояния хроматина является наличие паттернов распределения Н3К4me3 и H4K5ac, в то время как за «спящее» состояние хроматина отвечают Н3K27me3 и H3K9me3.
Посттрансляционные модификации гистонов — это, конечно, хорошо. Но только если есть, что модифицировать. Некоторые постоянные или коровые гистоны имеют своих дублеров — вариантные гистоны, замещающие коровые в составе нуклеосом. К примеру, отсутствие материнского гистонового варианта Н3—Н3.3 в зиготе приводит к нарушению репрограммирования и подавлению ключевых генов плюрипотентности [13]. Кроме того, присутствие Н3.3 и гистонового варианта Н1—Н1foo необходимо для замещения протаминов и сборки отцовского пронуклеуса. Вот такие вот они нужные и важные. Не важнее только, пожалуй, варианты гистона Н2A. Например, H2A.Z участвует в активации транскрипции и эпигенетической памяти, H2A.X играет центральную роль в ответе на повреждение ДНК, а MacroH2.A предположительно участвует в инактивации Х-хромосомы.
Помимо всего вышеперечисленного, ни один NSN-SN переход не обходится без участия дополнительных негистоновых белков, а присутствие некоторых даже является критически необходимым. Например, PCBP1 (poly(rC)-binding protein 1) играет ключевую роль в установлении транскрипционно-неактивного состояния хроматина во время формирования кариосферы. Мутации в гене одного из хроматин-ремоделирующих белков, ATRX (α-thalassemia/mental retardation X-linked protein), приводят к нестабильности перицентромерного хроматина и резкому возрастанию числа анеуплоидных ооцитов и эмбрионов. Белок DPPA3 (developmental pluripotency-associated protein 3), как и PCBP1, способствует репрессии транскрипции. Не дремлют и активируемые MAPK (mitogen-activated proteinkinase) сигнальные каскады, регулирующие NSN-SN переход при участии гормонов.
Несмотря на значительный прогресс в понимании молекулярных механизмов перестроек хроматина на поздних стадиях оогенеза и ранних стадиях эмбриогенеза, цельное видение регуляции таких сложных процессов еще не сформировано. Однако актуальность исследования не оставляет сомнений в том, что игра стоит свеч. «С фундаментальной точки зрения, изучение таких уникальных объектов поможет лучше понять законы организации клеточного ядра в целом, — говорит другой автор статьи, доктор биологических наук, Боголюбова Ирина Олеговна. — С прикладной — любые данные о преобразовании ядра в оогенезе позволяют увидеть слабые места уже в эмбриогенезе».
ПРАМАТЕРЬ ВСЕХ КЛЕТОК
Все великое многообразие многоклеточных существ имеет весьма скромное начало - оплодотворенную клетку (зиготу). Но у зиготы и во взрослом организме есть "двойник" - так называемая эмбриональная стволовая клетка. Она не только "хранит" информацию обо всем организме, но и "знает", как ею воспользоваться, чтобы размножиться в миллиарды клеток растущего живого существа. Никакие другие клетки "не умеют" этого делать. Эмбриональные стволовые клетки человека впервые были выделены в 1998 году, а уже в 1999-м журнал "Science" ("Наука") признал выделение эмбриональных стволовых клеток человека третьим по важности событием в биологии ХХ века после открытия двойной спирали ДНК и расшифровки генома человека. Что стоит за этим? В чем важность получения эмбриональной стволовой клетки?
Впервые во внутриутробном развитии человека эмбриональные стволовые клетки появляются на 5-7-й день после оплодотворения.
Эмбриональные стволовые клетки можно размножать в лаборатории, содержа их в термостате (cлева) на питательной среде (справа).
Этой крысе, у которой наблюдали симптомы болезни Паркинсона, ввели препарат клеток мозга, выращенных из бычьих эмбриональных стволовых клеток, после чего у нее практически исчезли тремор и непроизвольные движения, характерные для этой болезни.
Клетки "без имени-отчества"
Миллионы людей до нас и миллионы после нас задумывались и будут задумываться над простым вопросом: как вся информация о живом организме может "упаковаться" в одну микроскопическую живую капельку, а затем разнестись по миллионам самых разных клеток? Еще 20 лет назад все рассуждения на эту тему не имели никакого экспериментального обоснования: в руках у исследователей не было той самой клетки-"праматери", клетки - предшественницы всех клеток организма, так называемой эмбриональной стволовой клетки. Правда, у растений рост зародыша из неполовых клеток-предшественников хорошо известен. Так, из кусочка зародышевой ткани моркови или женьшеня можно вырастить полноценное растение с половыми клетками.
Только в 1981 году американскому ученому Мартину Эвансу впервые удалось выделить животную стволовую эмбриональную клетку из зародыша мыши. Все последующие годы усилия ученых были направлены на получение эмбриональной стволовой клетки из человеческого зародыша. И в 1998 году удача улыбнулась американским исследователям Джеймсу Томпсону и Джону Беккеру. Сейчас каждый из них имеет в своей лаборатории до 10 бессмертных саморазмножающихся клеточных линий человеческих эмбриональных стволовых клеток.
В нашей стране одним из признанных лидеров исследований в области эмбриональных стволовых клеток является профессор В. Репин. Данная статья представляет собой запись его доклада, сделанного в мае этого года на заседании президиума Российской академии медицинских наук.
Самое главное свойство эмбриональной стволовой клетки состоит в том, что генетическая информация, заключенная в ее ядре, находится как бы в "нулевой точке" отсчета. Дело в том, что все неполовые клетки живых организмов (соматические клетки) специализированы, то есть выполняют какие-либо функции: клетки костной ткани формируют скелет, клетки крови отвечают за иммунитет и разносят кислород, нервные клетки проводят электрический импульс и так далее. А эмбриональная стволовая клетка еще не "включила" механизмы, определяющие ее специализацию. В "нулевой точке" ее геном еще не "запустил" ни одной программы и, что особенно важно, не начал выполнять программу размножения и формирования многоклеточного зародыша. Таких "нулевых" клеток в зародыше очень мало - всего сотые доли процента, вот почему исследователям так трудно было получить их в "чистом виде".
Эмбриональные стволовые клетки не работают в автоматическом режиме, как, например, тромбоциты или лимфоциты, они могут принять любую программу и превратиться в один из 150 возможных типов зародышевых клеток. Эмбриональная клетка лишь ждет специального "сигнала", чтобы начать одно из своих превращений. Это означает, что она не имеет никаких функций, кроме переноса мРНК в следующее клеточное поколение. Все клетки имеют, а она - нет. Эмбриональная клетка - кассета с информацией, клетка-аноним, клетка "без имени-отчества".
Еще один важный момент. Из эмбриональных стволовых клеток формируются островки в различных органах и тканях. По сути, наши органы являются смесью взрослых специализированных клеток с вкраплениями зародышевой ткани в виде эмбриональных стволовых клеток. Эти клетки растут, рождаются и умирают. И лишь их "праматерь" бессмертна. Сейчас уже научились выделять из головного мозга зародышей не просто отдельные эмбриональные стволовые клетки, а зародышевую ткань, из которой, как из куска глины, природа "лепит" все живое. При хранении зародыша в холодильнике при +4 о С через 4-5 часов все клетки погибают, остаются лишь эмбриональные стволовые клетки-предшественники.
Эмбриональная стволовая клетка расскажет ученым о том, как "работают" гены
Томпсон и Беккер сделали для биологиче ской науки ХХI века то же самое, что Уотсон и Крик для молекулярной биологии ХХ века. Уотсон и Крик нашли научный плацдарм для работы в области генетики, а Томпсон и Беккер - в области функциональной геномики. И действитель но, их авторитет и количество публикаций по изучению эмбриональной стволовой клетки растут лавинообразно, несмотря на то, что они опубликовали всего лишь по одной работе в международных научных журналах "Science" и "Proceedings of National Academy of Sciences USA" (Труды американской национальной Академии наук) в 1998 году, а уже в 1999 году журнал "Science" признал выделение эмбриональных стволовых клеток человека третьим по важности событием в биологии ХХ века.
С открытием в 1953 году Уотсоном и Криком двойной спирали ДНК ученые поняли, где в живой клетке хранится и как передается наследственная информация. Уотсон и Крик помогли понять, как законы наследственности "работают" в масштабе одной клетки. В 2001 году ученые полностью расшифровали молекулярную структуру ДНК человека, но не поняли, как "работают" составляющие ее гены. И вот эмбриональная стволовая клетка оказалась прекрасной моделью для понимания того, как 5000 генов эмбриогенеза тиражируют генетическую информацию, чтобы из одной клетки вырос человеческий организм, состоящий из 10 14 клеток.
Вся "работа" генома контролируется определенным набором генов, которые сначала формируют "костяк" клетки, потом ее внутреннюю структуру (органеллы) и, наконец, целиком клетку с полным набором генов. Говоря языком компьютерщиков, устройство клетки - это hardware - аппаратное обеспечение компьютера. И в последний момент в клетку "встраивается" software - генетическая программа, определяющая ее специализацию, ее место в организме. Проще говоря, это инструкция к тому, будет ли данная клетка, к примеру, частью соединительной ткани или она станет элементом крови.
Итак, все клетки одного организма имеют одинаковый набор генов, но у каждого из нас есть по меньшей мере 350 типов клеток, "работающих" по различным генетическим программам.
Перед одной-единственной клеткой стоит задача превратиться в организм, состоящий из миллиардов клеток. Для этого в ней имеются 5000 так называемых генов эмбриогенеза, регулирующих этот процесс на начальной стадии развития зародыша. Сначала оплодотворенная яйцеклетка размножается, превращаясь в клетки, которым не суждено стать зачатками будущих органов или тканей, они просто переносчики генетической информации в виде молекул РНК.
И только когда накопится уже достаточное количество информации, в работу включаются гены, ответственные за специализацию, после чего начинают формироваться семейства различных стволовых клеток и происходит сегментация зародыша (структурно выделяются участки будущих органов). Причем количество клеток в том или ином сегменте (будущем органе) генетически запрограммировано, а значит - конечно. Поэтому ученым при выращивании семейства эмбриональных стволовых клеток чрезвычайно важно брать клетку-"праматерь" на стадии, когда еще "молчат" гены сегментации. Томпсону и Беккеру это удалось, и потому они на сегодняшний день имеют практически неограниченное количество бессмертных эмбриональных стволовых клеток.
Эмбриональная стволовая клетка, клонирование и клеточная терапия
Удивительная способность эмбриональной стволовой клетки стать любой клеткой организма продиктована наличием в ней избытка РНК всех генов, отвечающих за рост зародыша на ранней стадии развития эмбриона. Факторы, делающие эмбриональную клетку уникальной, находятся в ее клеточной жидкости - цитоплазме. Именно поэтому возможно клонирование живых существ. Можно "вынуть" ядро с генетическим материалом из клетки любого организма, "вставить" его в оболочку яйцеклетки, и система начнет "работать" - копировать содержащуюся в ДНК информацию, а затем формировать новое живое существо, идентичное донору.
Хочу отметить, что в статье затронут исключительно научный аспект изучения эмбриональных стволовых клеток и ничего не сказано о терапии с использованием эмбриональных стволовых клеток, о том, что происходит с эмбриональными клетками при их пересадке в различные органы и ткани животных и человека. А между тем это огромная и очень важная тема. При пересадке эмбриональных стволовых клеток в какой-либо орган из них всегда образуются только клетки этого органа, что позволяет использовать эмбриональные стволовые клетки для восстановления поврежденных органов и тканей, лечения множества тяжелых заболеваний.
Эмбриональная стволовая клетка и мозг человека
Программа "Геном человека" показала, что мы отличаемся от обезьян и других млекопитающих очень немногим - так называемыми генами эмбриогенеза, то есть теми генами, которые отвечают за раннее развитие зародыша из эмбриональной стволовой клетки. Причем это относится не ко всем клеткам, а только к тем, которые управляют развитием мозга. Интересно, что, в отличие от всех живых существ, передняя доля мозга человека уже на ранних стадиях перестает контролироваться генами, которые определяют, сколько клеток будет в том или ином органе. Вот поэтому мозг человека может расти. То есть только "наши" (только человеческие) гены позволяют будущим клеткам мозга совершить такую экспансию. Более того, формирующиеся в процессе развития мозга новые нейроны не стоят на месте - они мигрируют, создавая новые и новые клеточные образования. Такого нет ни у кого из живых существ, кроме человека.
Благодаря новым генам мозг зародыша человека и других млекопитающих приобрел и новый орган - нервный гребень. Его клетки - "марафонцы", они способны пройти расстояние в несколько метров. Из мигрирующих клеток гребня образуются вся костно-мышечная система лица, тимус, все элементы внутреннего уха, проводящая система сердца, периферическая нервная система, надпочечники.
Изучение превращений стволовых клеток выявило множество удивительных взаимосвязей в системе органов и тканей человека. Можно привести один яркий пример.
Президент Клинтон за год до президентских выборов в США выступил по телевидению. Он обещал пяти миллионам имеющих право голоса диабетиков решить проблему инсулина раз и навсегда за два года. Дело в том, что за два года до этого известный американский ученый Ро Маккей, выращивая нервные клетки из их предшественников - нейрональных стволовых клеток, неожиданно обнаружил в межклеточной среде появление инсулина. В это было трудно поверить, но ученый решил идти до конца, сумел убедить в своей правоте многих и получил под научный проект огромное финансирование. И весной 2001 года в своей публикации в журнале "Science" он сообщил о том, что при определенных условиях нейрональные стволовые клетки способны превращаться в бета-клетки поджелудочной железы, то есть в клетки, вырабатывающие инсулин. Но самое интересное, что бета-клетки состоят "в очень близком родстве" с клетками стриатума - важной части головного мозга, управляющей многими процессами. Конечно, это неспроста, и здесь ученых ждут удивительные открытия.
Эмбриональные стволовые клетки и биоэтика
Несмотря на то, что исследования в области эмбриональных клеток сулят ученым грандиозный прорыв во всех отраслях биологии и медицины, в США и Германии они сейчас "заморожены", но продолжают проводиться в Англии, Японии, Австралии и многих других развитых странах. Основная причина запрещения научных исследований - этическая. Ведь пока основной источник эмбриональных клеток - материал, остающийся от искусственного оплодотворения, и фетальная ткань от медицинских абортов. Католическая церковь, религиозные общины, различные общественные организации, которые борются за запрещение абортов, оказывают колоссальное давление на правительства и президентов, призывая вместе с абортами запретить и исследование эмбриональных стволовых клеток, и лечение с их применением.
В ответ на это совсем недавно 80 нобелевских лауреатов отправили письмо президенту США Дж. Бушу о необходимости продолжения научных работ с эмбриональными стволовыми клетками. В нем утверждается, что, несмотря на религиозные и этические проблемы, достижения в этой области принесут пользу человечеству, несоизмеримую с моральными издержками на пути продвижения к истине. Кто прав - покажет время.
Читайте в любое время
Впервые во внутриутробном развитии человека эмбриональные стволовые клетки появляются на 5-7-й день после оплодотворения. Они образуют комочек внутри бластоциста - шарика, состоящего из 140 клеток. На снимке показаны бластоцисты человека, полученные путем оплодотворения в пробирке. Скопление стволовых клеток хорошо видно у стенки бластоциста в левом нижнем углу фотографии.
Схема получения 'запчастей' из эмбриональных стволовых клеток. После оплодотворе ния яйцеклетка начинает делиться и дает сначала 2, потом 4, а затем и 140 клеток, образующих шарик-бластоцист. Его наружную оболочку разрушают вручную (микромани пулятором) или ферментами, получая стволовые клетки. Содержа в культуре, их можно размножать и вызывать превращение в специализированные клетки организма - нервные, мышечные, печеночные, кожные и т. д., которые затем пересаживают больному взамен таких же отмерших или заболевших его собственных клеток.
Эмбриогенез человека. Зародошевые и стволовые клетки
Содержание темы
2. а) В разделе 3 (темы 5-6) мы уже рассматривали со сравнительных позиций ранние стадии развития различных животных - от ланцетника до млекопитающих.
б) Это дало нам общие представления о происхождении различных тканей и органов.
3. а) Теперь же (в теме 31) дадим последовательное описание ранних этапов развития человека - с привязкой этих этапов к конкретным срокам беременности и конкретному "месту действия".
б) Затем (в теме 32) будут рассмотрены строение и функционирование внезародышевых органов - в первую очередь, плаценты.
31.1. Периодика внутриутробного развития человека
2. а) Как видно, в эмбриогенезе человека различают 3 периода:
б) Заметим, что существуют и иные подразделения эмбриогенеза на периоды:
| зародышевый - первые 3 недели, | начальный - 1-я неделя, |
| эмбриональный - 4-8 недели, | зародышевый - 2-8 недели, |
| плодный - 9-40 недели. | плодный - 9-40 недели. |
в) Таким образом, разночтения касаются первых восьми недель развития.
3. а) Их-то мы и будем рассматривать в этой теме.
31.2. Половые клетки
31.2.1.1. Особенности строения
имеет объём 2-3 мл и
содержит 200-350 млн сперматозоидов ( Сз).
2. а) Подробно строение Сз излагалось в п. 5.1.2.
б) Напомним: в Сз различают 2 части -
в) При этом у человека головка Сз сильно уплощена.
таксисе Сз и
связывании с яйцеклеткой.
2. а) Заметим: эти белки (по крайней мере, те, что участвуют в связывании с яйцеклеткой) имеют
б) Узкой ножкой с мешочком связан также небольшой акросомный пузырёк (2а).
р езко уплотнено и
содержит гаплоидный набор хромосом.
б) О т одной из них начинается аксонема (7), или осевая нить хвоста, образованная микротрубочками по схеме
9 наружных фибрилл,
митохондриальная спиральная оболочка (6) и
фибриллярное влагалище (8) (9 наружных фибрилл и волокнистая оболочка), а также
31.2.1.2. Детерминация пола ребёнка
у 50 % Сз имеется Х-хромосома ,
а у других 50 % Сз - Y-хромосома .
2. Пол ребёнка определяется "полом" сперматозоида:
31.2.1.3. Препарат
На снимке (который нам знаком по п. 5.1.2.1) мы видим основные компоненты сперматозоида:
головку (1) и хвост (2),
31.2.2.1. Условность термина "яйцеклетка"
ооциты I и затем
(непосредственно перед овуляцией) ооциты II.
окружён блестящей и зернистой оболочками и
находится на стадии метафазы второго деления созревания.
происходят последние стадии этого деления (метафаза, анафаза и телофаза);
в результате, ядро ооцита II делится на 2 ядра с гаплоидными наборами хромосом,
и одно из этих ядер остаётся в качестве женского пронуклеуса (сосуществующего с мужским пронуклеусом),
так что из ооцита II, минуя стадию собственно яйцеклетки, образуется сразу зигота.
ооцит I (после стадии роста),
ооцит II или
только что образовавшуюся зиготу.
31.2.2.2. Специфические структуры цитоплазмы
I. Содержание желтка
в цитоплазме (1) равномерно распределено относительно небольшое количество желтка;
причём, в эволюции это вторично : впервые такой тип яйцеклетки встречается у ланцентника.
объём яйцеклетки человека в несколько тысяч раз больше объёма сперматозоида.
II. Перечень специфических структур
Специфические структуры цитоплазмы яйцеклетки (известные нам по п. 5.1.3.6) суммированы в таблице. -
после оплодотворения участвуют в кортикальной реакции (см. ниже - п. 31.3.1.2.III).
31.2.2.3. Другие особенности строения
Яйцеклетке присущи также следующие особенности. -
б) Отсутств уют центриол и;
в связи с этим, способность к делениям восстанавливается только тогда,
когда в клетку попадают центриоли сперматозоида.
блестящая, или прозрачная (zona pellucida, или Zp) ( 4 ) , и
зернистая ( 5 ) , образованная фолликулярны ми клетк ами.
а гликопротеины фракции Zp2 после кортикальной реакции
не окружены базальной мембраной (поскольку представляют собой лишь часть фолликулярного эпителия),
но имеют длинные отростки , пронизывающие блестящую оболочку.
либо только внутренние части фолликулярных клеток с отходящими от них отростками,
либо всю совокупность зернистого слоя и блестящей оболочки.
31.2.2.4. Препараты
Приведём два снимка из п. 5.1.3.4.
I. Окраска гематоксилин-эозином
б) Тем не менее, яйцеклетка имеет практически такое же строение.
2. На снимке видны следующие структуры :
ядро ооцита (1) и в нём - ядрышки (2),
цитоплазма ооцита с желточными гранулами (3),
блестящая (4) и зернистая (5) оболочк и,
соединительнотканная оболочка - тека ( 6 ).
II. Окраска по Маллори
2. Более отчётливо, чем при предыдущей окраске, видны следующие структуры:
ядро ооцита (1) и ядрышки (2) в нём,
цитоплазма ооцита (3),
блестящая (4) и зернистая (5) оболочки.
31.3. Зародышевый период развития
31.3.1.1. Общая характеристика
только один сперматозоид может проникнуть в яйцеклетку (точнее, ооцит II).
б) При этом в женских половых путях сперматозоиды сохраняют оплодотворяющую способность в течение 1-2 суток .
2. Оптимальный срок для оплодотворения - первые 24 часа после овуляции
(хотя ооцит II может сохранять способность к оплодотворению ещё некоторое время).
3. Таким образом, оплодотворение может наступить лишь в том случае, если половой акт совершается в интервал времени
момент овуляции + 1-2 суток
(минус - за счёт сохранения сперматозоидов в женских половых путях,
а плюс - за счёт сохранения ооцита II).
31.3.1.2. Основные события
Фазы оплодотворения были описаны в п. 5.2.2.
Кратко напомни м приводи вшуюся там информаци ю.
I. Сближение и дистантное взаимодействие половых клеток
это происходит пассивно - благодаря току слизи (выделяемой под действием эстрогенов).
б) Данный ток вызывается
биением ресничек мерцательных клеток и
тоническими сокращениями маточных труб (под действием прогестерона).
В матку они попадают, в основном, пассивно - благодаря тоническим сокращениям женских половых путей.
б) Затем часть Сз также, в основном, пассивно, достигает маточных труб.
2. Считается, что сокращения влагалища и матки усиливаются под влиянием простагландинов - гормональных компонентов спермы (синтезируемых в простате).
метаболизм и подвижность Сз резко усиливаются (п. 29.2.4.8).
а мембраны Сз в области головки теряют поверхностные гликопротеины и поэтому приобретают
способность связываться с блестящей оболочкой ооцита,
а также лабильн ость (что необходимо для последующего разрыва акросомы);
б) Вероятно, капацитацию инициируют
гиногамоны II , выделяемые ооцитом.
становится преимущественно активным
и обеспечивается биением их жгутиков .
б) При этом сперматозоиды одновременно
двигаются поступательно
и вращаются вокруг своей оси.
в) Направленность этого движения сперматозоидов обеспечивается
реотаксисом - способностью определять направление тока жидкости (в данном случае, слизи маточных труб) и двигаться против него),
а также хемотаксисом (способностью определять градиент концентрации определённых веществ - аттрактантов - и двигаться против него).
г) Считают, что такими аттрактантами являются
определённые пептиды, выделяемые ооцитом II или его окружением.
II. Контактное взаимодействие половых клеток
а) разрываются передние участки плазмолеммы и мембраны акросомы,
б) отчего высвобождаются акросомальные ферменты :
гиалуронидаза разъединяет клетки зернистой оболочки ,
а трипсиноподобный фермент акрозин и ряд других ферментов растворяют блестящую оболочку в месте прохождения Сз .
III. Проникновение сперматозоида в ооцит II
часть плазмолеммы Сз встраивается в мембрану ооцита,
а в ооцит проникают ядро ( 2 ) Сз и центриоли.
благодаря ионным каналам встроенной мембраны Сз, изменяется трансмембранный потенциал ооцита,
что стимулирует выброс содержимого кортикальных гранул (3) за пределы клетки.
б) Под влиянием выделяемых веществ
мембрана ооцита теряет рецепторную активность (модифицируются рецепторные гликопротеины Zp3 );
создаётся перивителлярное пространство (4) - между плазмолеммой и блестящей оболочкой (т.к. сюда привлекается вода ),
блестящая оболочка уплотняется (за счёт перестройки гликопротеинов Zp2 ) - образуется оболочка оплодотворения .
в) Всё это препятствует проникновению в ооцит II других Сз.
г) Кроме того, ооцитом выделяются
гиногамоны I, которые вызывают агглютинацию оставшихся сперматозоидов.
IV. Подготовка зиготы к дроблению
набухает (превращаясь в мужской пронуклеус (2) )
и сближается с женским пронуклеусом (сближенные ядра называются синкарионом ),
молекулы ДНК (в пронуклеусах) и
пришедшие с Сз центриоли (6) .
V. Начало первого митотического деления
а) их оболочки разрушаются,
б) а хромосомы
конденсируются и
в метафазе образуют единую материнскую звезду (7).
Заметим: всё это время продолжается медленное пассивное продвижение ооцита II, а затем зиготы, по яйцеводу к матке.
31.3.1.3. Дополнительная иллюстрация
она не имеет клеточной структуры, т.к. происходит из блестящей оболочки .
2. а) Внутри зиготы - два ядра-пронуклеуса (2) почти равного объёма.
б) Поскольку ядра уже соприкасаются (что является сигналом к началу митоза), в них
уже совершилось удвоение ДНК ,
и хромосомы стали двухроматидными.
31.3.2.1. Общая характеристика
б) Рост клеток затруднён оттого, что вокруг зародыша сохраняется плотная оболочка оплодотворения (1), которая препятствует
и притоку питательных веществ извне,
(жизнедеятельность поддерживается за счёт расходования резервов яйцеклетки);и самому увеличению размера зародыша.
образуются всё более мелкие клетки и
общий объём зародыша не увеличивается .
Дробление происходит в просвете яйцевода,
и к концу его зародыш достигает (продвигаясь по яйцеводу) полости матки.
полное: дробятся все клетки зародыша ;
асинхронное : клетки делятся не одновременно; поэтому могут быть стадии с нечётным количеством бластомеров;
неравномерное: образуются клетки разного размера.
б) Поэтому при диссоциации клеток на этих стадиях каждый бластомер даёт начало самостоятельному зародышу,
чем и объясняется появление однояйцевых близнецов.
всё более различаются друг от друга по виду и потенциям развития,
а вместе с тем теряют и свойство тотипотентности (способность развиваться в отдельный организм).
В т.ч. в центре находятся 3-4 тёмные и крупные клетки - предшественники эмбриобласта.
Остальные, периферические, клетки - светлые и мелкие; это предшественники трофобласта.
31.3.2.2. Динамика увеличения числа клеток
первое деление дробления завершается через 30 часов,
а всего на стадии дробления происходит 5 циклов делений (2 5 = 32).
31.3.3. Образование бластоцисты
31.3.3.1. Общая характеристика
зародышевый пузырёк, заполненный жидкостью.
2. В вид е свободной бластоцисты зародыш находится в полости матки около 2-х суток -
3. Деления клеток в бластоцисте по-прежнему являются
б) В самих бластомерах всё более активируются синтетические процессы.
2 . а) В трофобласте появляются выросты,
которые постепенно разрушают оболочку оплодотворения вокруг зародыша.
б) В результате, за несколько часов до имплантации (см. ниже) зародыш теряет эту оболочку.
3. а) После этого оболочка уже не мешает зародышу увеличиваться в размере,
и с этих пор митотические циклы клеток становятся обычными, т.е. включают фазу роста.
Понятие прогенеза и эмбриогенеза. Периоды и основные стадии эмбриогенеза у человека. Половые клетки человека, их структурно- генетическая характеристика.
ЭМБРИОГЕНЕЗ -эмбриональное развитие человека. Продолжается 280 дней, делится на три периода: начальный (первая неделя развития), зародышевый (2-8 неделя развития - закладка основных органов), плодный (9неделя - до рождения).
Ранний эмбриогенез делится на стадии:
1. ЗИГОТА - начало синтеза ДНК и белка
2. ДРОБЛЕНИЕ - начало синтеза основных типов РНК
3. МОРУЛА - клетки зародыша тотипотентны (взаимозаменяемы)
4. БЛАСТОЦИСТА - происходит утрата тотипотентности и клетки детерминируются к образованию зародышевых и внезародышевых структур.
5. ГАСТРУЛА - появляются зародышевые листки и стволовые клетки
6. ОРГАНОГЕНЕЗ - из ткани формируются органы, идет формирование зачатков органов из клеточных клонов
ПРОГЕНЕЗ -период развития и созревания половых клеток - яйцеклеток и сперматозоидов, в результате в зрелых половых клетках возникает гаплоидный набор хромосом, формируются структуры, обеспечивающие их способность к оплодотворению и развитию нового организма.
ПОЛОВЫЕ КЛЕТКИ - ПРИЗНАКИ:
· Гаплоидный набор хромосом
· Измененная ядерно-цитоплазматическое отношение - отношение объема ядра и цитоплазма
· Изменен метаболизм клетки
· Клетки высоко дифференцированы (не способны делиться)
ЯЙЦЕКЛЕТКА (открыта Бером) - имеет оолемму, ооплазму (цитоплазму), ядро; органоиды развиты все за исключением центриолей, из включений преобладает желток.
ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ: ядро неактивно ни в отношении транскрипции, ни в отношении репликации, т.е. ведет себя пассивно; яйцеклетка накапливает ферменты, факторы и гликоген.
СТРУКТУРНЫЕ ОСОБЕННОСТИ: имеет кортикальный слой цитоплазмы - периферическая гиалоплазма с кортикальными гранулами (мукополисахариды, белки, ферменты); полярна - выделяют два полюса: анимальный (сосредоточены органоиды) и вегитативный (содержит < или >количество белка)
У человека маложелтковая, вторичноолиголецитальная, изолецитальная
Яйцеклетку окружают прозрачная (лецитальная) оболочка - zona pellucida (ее образуют Zp белки). Среди них есть Zp2 белок - препятствует полиспермии, Zp3 рецептор к сперматозоиду.
Яйцеклетка окружена фолликулярными клетками, которые доставляют к ней питание - формируют лучистый венец.
СПЕРМАТОЗОИД -выделяют четыре отдела: головка (содержит крупное ядро и акросому - видоизмененная лизосома), шейка(проксимальная центриоль), тело (митохондриальные спирали и дистальная центриоль), хвостик (представлен жгутиком)
Максимальная способность к оплодотворению до двух суток.
Направленная миграция сперматозоидов определяется хемотаксисом и реотаксисом, важными показателями при этом являются рН и слизь. Происходит капоцитация - под действием секретов женских половых путей сперматозоид приобретают оплодотворяющие способности.
Продвижение сперматозоида облегчают простогландины (действуют на оболочку маточных труб)
Читайте также:
