Факторы влияющие на КДО. Влияние температуры на кривую диссоциации оксигемоглобина (КДО)
Добавил пользователь Владимир З. Обновлено: 22.01.2026
Патофизиология. Том 2
Под ред. В.В. Новицкого, Е.Д. Гольдберга, О.И. Уразовой
Библиография:
Патофизиология : учебник : в 2 т. / под ред. В.В. Новицкого, Е.Д. Гольдберга, О.И.
Уразовой. - 4-е изд., перераб. и доп. - ГЭОТАР-Медиа, 2009. - Т. 2. - 640 с. : ил.
Учебник подготовлен коллективом авторов - ведущими патофизиологами России и стран
СНГ (Украина, Грузия). В его создании принимали участие известные педагоги -
представители московской, томской, казанской, харьковской и тбилисской научных школ
патофизиологов, а также крупнейшие специалисты, работающие в научно-
исследовательских институтах Российской академии медицинских наук.
Настоящее издание является практически полностью переработанным и дополненным
вариантом учебников "Патологическая физиология" под редакцией А.Д. Адо и В.В.
Новицкого (Томск, 1994 г.) и "Патофизиология" под редакцией В.В. Новицкого и Е.Д.
Гольдберга (Томск, 2001, 2006 гг.).
Второй том посвящен патологической физиологии органов и систем. Существенно
изменены и дополнены разделы по патофизиологии кроветворной, дыхательной и
пищеварительной систем, опухолевого роста, типовых нарушений обмена веществ. В
значительной степени пересмотрены и дополнены другие главы учебника.
Для студентов медицинских вузов (всех факультетов).
ЧАСТЬ III ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ ГЛАВА 14
ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ
ГЛАВА 15 ПАТОФИЗИОЛОГИЯ СЕРДЕЧНО- СОСУДИСТОЙ СИСТЕМЫ
ГЛАВА 16 ПАТОФИЗИОЛОГИЯ ДЫХАНИЯ
ГЛАВА 17 ПАТОФИЗИОЛОГИЯ ПИЩЕВАРЕНИЯ
ГЛАВА 18 ПАТОФИЗИОЛОГИЯ ПЕЧЕНИ
ГЛАВА 19 ПАТОФИЗИОЛОГИЯ ПОЧЕК
ГЛАВА 20 ПАТОФИЗИОЛОГИЯ ЭНДОКРИННОЙ СИСТЕМЫ
ГЛАВА 21 ПАТОФИЗИОЛОГИЯ НЕРВНОЙ СИСТЕМЫ
ГЛАВА 22 ПАТОФИЗИОЛОГИЯ ВЫСШЕЙ НЕРВНОЙ ДЕЯТЕЛЬНОСТИ
АВТОРСКИЙ КОЛЛЕКТИВ
Академики РАМН: А.Д. Адо, И.Г. Акмаев, Н.П. Бочков, Ю.А. Владимиров, Е.Д.
Гольдберг, Г.Н. Крыжановский, А.А. Кубатиев, В.А. Неговский, В.В. Новицкий, В.П.
Пузырев, М.М. Хананашвили.
Члены-корреспонденты РАМН: З.С. Баркаган, Н.Е. Кушлинский, Ю.Б. Лишманов, Г.В.Порядин, С.Б. Ткаченко;
Профессоры: М.Б. Баскаков, Э.И. Белобородова, В.Т. Долгих, В.В. Долгов, Н.А.
Клименко, В.В. Климов, В.С. Лаврова, Л.Н. Маслов, Г.И. Мчедлишвили, Н.П. Пирогова, В.И. Пыцкий, Е.А. Степовая, Ф.Ф. Тетенев, О.И. Уразова, Б.М. Федоров, Т.С. Федорова, О.Ю. Филатов, И.А. Хлусов.
Доценты: С.Э. Бармина, Г.В. Бурлаков, Л.М. Далингер, О.Б. Запускалова, М.Ю. Хлусова, Е.Н. Чернова
СПИСОК СОКРАЩЕНИЙ
АДГ - антидиуретический гормон АДФ - аденозидифосфат
АИГА - аутоиммунная гемолитическая анемия АКМ - альвеолярно-капиллярная мембрана
АКТГ - адренокортикотропный гормон АлАТ - аланинаминотрансфераза АМФ -
АПТВ - активированное парциальное тромбопластиновое время АПФ -
ангиотензинпревращающий фермент АсАТ (АСТ) - аспартатаминотрансфераза АТ -
АТ-рТТГ - антитела к рецептору тиреотропного гормона
АТ-ТГ - антитела к тиреоглобулину
АТ-ТПО - антитела к тиреопероксидазе
АФК - активные формы кислорода
АФС - антифосфолипидный синдром
АХЗ - анемия хронических заболеваний
Ацетил-КоА - ацетил-коэнзим А
АЭС - атомная электростанция
БАВ - биологически активные вещества
БОЕ-Э - бурстобразующая единица эритроцитов
БТШ - белок теплового шока
ВИП - вазоактивный интестинальный полипептид
ВИЧ - вирус иммунодефицита человека
ВМК - высокомолекулярный кининоген
ВОЗ - Всемирная организация здравоохранения
ГАМК - γ-аминомасляная кислота
ГБН - гемолитическая болезнь новорожденного
ГЗТ - гиперчувствительность замедленного типа
ГИМ - гемопоэзиндуцирующее микроокружение
ГИП - гастринингибирующий пептид
Г-КСФ - гранулоцитарный колониестимулирующий фактор ГЛП - гиперлипопротеинемия
ГЛЮТ - глюкозный транспортер
ГМ-КСФ - гранулоцитарно-макрофагальный колониестимулирующий фактор
ГОМК - γ-оксимасляная кислота ГОЭ - гормон-отвечающий элемент ГП - гликопротеин
ГПП - глюкагоноподобный пептид
ГПУВ - генератор патологически усиленного возбуждения
ГР - глюкокортикоидный рецептор
Гр - грэй, единица измерения дозы облучения
ГСИК - гормон, стимулирующий интерстициальные клетки
ГТГ - гонадотропный гормон
ГТТ - глюкозотолерантный тест
ГУС - гемолитико-уремический синдром
ГЭБ - гематоэнцефалический барьер
ДL - диффузионная способность легких
ДВС - диссеминированное внутрисосудистое свертывание
ДГР - дуоденогастральный рефлюкс
ДНК - дезоксирибонуклеиновая кислота
ДНТК - диффузный ноцицептивный тормозной контроль
ДО - дыхательный объем
ДПК - двенадцатиперстная кишка
ЕК - естественные (или натуральные) киллеры
ЖЕЛ - жизненная емкость легких
ЖКТ - желудочно-кишечный тракт
ИБС - ишемическая болезнь сердца
ИВЛ - искусственная вентиляция легких
ИГА - индекс гистологической активности
ИК - иммунный комплекс
ИМТ - индекс массы тела
иРНК - информационная рибонуклеиновая кислота ИФР - инсулиноподобный фактор
роста КОЕ-Ба - колониеобразующая единица базофилов КОЕ-Г - колониеобразующая
единица гранулоцитов КОЕ-ГМ - колониеобразующая единица гранулоцитов и
макрофагов КОЕ-ГЭММ - колониеобразующая единица гранулоцитов, эритроцитов,
макрофагов, мегакариоцитов КОЕ-М - колониеобразующая единица макрофагов КОЕ-
Мгкц - колониеобразующая единица мегакариоцитов КОЕ-Н - колониеобразующая
единица нейтрофилов КОЕс - колониеобразующая единица селезенки КОЕ-Э -
колониеобразующая единица эритроцитов КОЕ-Эо - колониеобразующая единица
эозинофилов КОС - кислотно-основное состояние КСМ - кислые сульфатированные
мукополисахариды КФК - креатинфосфокиназа ЛГ - лютеинизирующий гормон ЛДГ -
лактатдегидрогеназа ЛП - липопротеины
ЛП-липаза - липопротеиновая липаза
α-ЛП - α-липопротеины (липопротеины высокой плотности) β-ЛП - β-липопротеины
(липопротеины низкой плотности) ЛПВП - липопротеины высокой плотности ЛПНП -
липопротеины низкой плотности ЛПОНП - липопротеины очень низкой плотности ЛППП -
липопротеины промежуточной плотности ЛПС - лихорадоподобное состояние ЛПТ - липотрофин
Вопрос 104. Транспорт кислорода кровью. Кривая диссоциации оксигемоглобина. Ее характеристика.
Этот газ переносится кровью преимущественно в химически связанном виде — в соединении с гемоглобином.Будучи идеальным переносчиком кислорода, гемоглобин отвечает следующим трем требованиям:
¾ связывает большое количество кислорода в легких;
¾ отдает большое количество кислорода в тканях;
¾ еще больше увеличивает отдачу кислорода в активно работающих тканях.
Из этого вытекает характер сатурационной кривой для кислорода.
Сатурационная кривая для кислорода
Эта кривая приведена на рис. 10.8.
· У нее имеется почти горизонтальный участок, соответствующий полному насыщению гемоглобина кислородом. Этот участок начинается при парциальном давлении кислорода (pO2) около 70 мм рт. ст. В альвеолярном воздухе (и артериальной крови) pO2 составляет около 100 мм рт. ст. Благодаря этому:
¾ в легких кровь максимально насыщается кислородом;
¾ при снижении pO2 в альвеолярном воздухе даже до 70 мм рт. ст. кровь все равно максимально насыщается кислородом — важный механизм защиты от гипоксии.
Благодаря горизонтальному участку сатурационной кривой гемоглобин отвечает первому требованию — связывает большое количество кислорода в легких.
· У нее имеется наклонный участок, соответствующий pO2 менее 70 мм рт. ст. Значит, при низких значениях pO2 (в тканях) сродство гемоглобина к кислороду падает, и кислород высвобождается в ткани.
Благодаря наклонному участку сатурационной кривой гемоглобин отвечает второму требованию — отдает большое количество кислорода в тканях.
· При снижении pH (ацидозе), увеличении парциального давления углекислого газа (pCO2) и повышении температуры кривая сдвигается вправо, то есть сродство гемоглобина к кислороду падает. Все три фактора имеются в активно работающих тканях. Следовательно, омывая активно работающие ткани, кровь отдает им еще больше кислорода.
Благодаря сдвигу сатурационной кривой гемоглобин отвечает третьему требованию — еще больше увеличивает отдачу кислорода в активно работающих тканях.
Механизм изменения сродства гемоглобина к кислороду
Как мы только что выяснили, снижение сродства гемоглобина к кислороду в активно работающих тканях обусловлено действием трех факторов 1 :
1 Существует еще один, четвертый фактор, оказывающий выраженное влияние на сродство гемоглобина к кислороду — концентрация в крови 2,3-дифосфоглицерата. Однако эта концентрация меняется, по-видимому, только при патологических или по меньшей мере пограничных условиях (например, при хронической гипоксии) и поэтому здесь не рассматривается.
¾ снижением pH, то есть повышением содержания H + .
Механизмы действия этих трех факторов следующие.
· Повышениетемпературывызывает неспецифический сдвиг равновесия в реакции связывания кислорода с гемоглобином в сторону диссоциации (так же как, например, при повышенной температуре лучше растворяется любая соль — равновесие сдвигается в сторону диссоциированных ионов).
· CO2 и H + ,как и кислород, связываются с гемоглобином (см. ниже), однако не с железом гема, а с различными аминокислотными остатками белковой части — глобина. Присоединение CO2 и H + к соответствующим центрам связывания вызывает снижение сродства кислородного центра (гема) к кислороду (по механизму аллостерического взаимодействия, то есть влияния одних участков белка на свойства других участков) (рис. 10.9, А).
Кривая диссоциации оксигемоглобина
Вместо сатурационной кривой для кислорода часто приводят очень похожую на нее кривую диссоциации оксигемоглобина (рис. 10.10). Она отличается тем, что по вертикальной оси отложена не объемная концентрация кислорода, а степень насыщения гемоглобина кислородом. Горизонтальному участку при этом соответствует насыщение, равное 100%.
Связь между насыщением гемоглобина кислородом и объемной концентрацией кислорода в крови
Из сопоставления сатурационной кривой для кислорода (рис. 10.8) и кривой диссоциации оксигемоглобина (рис. 10.10) видно, что при 100% насыщении гемоглобина кислородом объемная концентрация кислорода в крови составляет (в норме!) около 20 об%. Рассмотрим, каким образом получается такое значение.
Поскольку подавляющая часть кислорода в крови приходится на химически связанный с гемоглобином кислород, объемная концентрация кислорода в крови зависит от:
¾ концентрациигемоглобина;
¾ кислородной емкости гемоглобина, то есть максимального количества кислорода, которое может связать 1 г гемоглобина при полном насыщении;
¾ степени насыщениягемоглобина кислородом:
где cO2 — объемная концентрация кислорода; Hb% — концентрация гемоглобина в крови; КЕHb — кислородная емкость гемоглобина; sO2 — насыщениегемоглобина кислородом.
В идеальном случае для артериальной крови:
¾ Hb% равна 15 г/100 мл;
¾ КЕHb равна 1,34 — один грамм гемоглобина при полном насыщении способен связать до 1,34 мл кислорода;
cO2 = 15 (г Hb/100 мл крови) 1,34 (мл O2/г Hb) 100%= 20 (мл O2/100 мл крови).(17)
Парциальные давления и объемные концентрации кислорода в артериальной и венозной крови приведены в табл. 10.1.
Факторы, влияющие на кривую диссоциации оксигемоглобина
Форма кривой диссоциации НbО2 обусловлена главным образом реакционноспособностью гемоглобина, однако сродство крови к кислороду может измениться под действием других факторов, как правило, приводящим к увеличению или уменьшению наклона кривой диссоциации без изменения ее S-образной формы. Такое влияние оказывают температура, рН, напряжение СO2 и некоторые другие факторы, роль которых возрастает при патологических состояниях.
Влияние температуры. Равновесие реакции оксигенации гемоглобина (как и большинства химических реакций вообще) зависит от температуры. При понижении температуры наклон кривой диссоциации оксигемоглобина увеличивается, а при ее повышении - снижается
Таблица. Параметры дыхательных газов и рН для артериальной и венозной крови у здоровых молодых людей в покое
| РO2 | SO2% | [O2], л O2 /л крови | PCO2 | [CO2], л CO2 /л крови | рН |
| Мм рт.ст. | кПа | Мм рт.ст. | кПа | ||
| Артериальная кровь | 12,6 | 0,20 | 5,3 | 0,48 | 7,40 |
| Венозная кровь | 5,3 | 0,15 | 6,1 | 0,52 | 7,37 |
| Артериовенозная разница | 0,05 | 0,04 |
Влияние рН и PСO2. Форма кривой диссоциации оксигемоглобина в значительной степени зависит от содержания в крови ионов Н + .При снижении рН, т. е. подкислении крови, сродство гемоглобина к кислороду уменьшается и угол наклона кривой диссоциации оксигемоглобина уменьшается. рН крови тесно связан с напряжением в ней СO2 (рСO2): чем выше РO2 , тем ниже рН. Очевидно, сам диоксид углерода оказывает на диссоциацию оксигемоглобина специфическое действие.
Поглощение O2 идет одновременно с выделением СO2, поэтому по мере насыщения гемоглобина кислородом кривая диссоциации оксигемоглобина сдвигается влево. По мере того как венозная кровь (точка в; pO2 = 40 мм рт. ст., РCO2 = 46 мм рт. ст.), насыщаясь кислородом, превращается в артериальную (точка а;PO2 = 95 мм рт. ст., РCO2 = 40мм рт. ст.), сродство гемоглобина к кислороду постоянно увеличивается. В результате, хотя перенос кислорода осуществляется путем диффузии, скорость этой диффузии несколько возрастает.
Поскольку одновременно с выходом кислорода из крови в нее поступает СO2, кривая диссоциации оксигемоглобина смещается вправо. Снижение сродства гемоглобина к кислороду приводит к еще большему падению содержания оксигемоглобина, и в результате кислород поступает в ткани при относительно высоком рО2 в капилляре.
Сродство гемоглобина к кислороду зависит также от содержания в эритроцитах катионов. Необходимо отметить и влияние патологических сдвигов рН: при повышении рН (алкалозе) захват кислорода в легких облегчается, но его отдача в тканях затрудняется, а при снижении рН (ацидозе) наблюдается обратная картина. Наконец, значительный сдвиг кривой диссоциации оксигемоглобина влево имеет место при отравлении СО.
37. Способы определения величины плеврального давления учебник
Измерение давления в плевральной полости: (1) прямой метод - прокол грудной стенки и введение в плевральную полость иглы, связанной с манометром; (2) непрямой метод - измерение давления с помощью зонда, введенного в пищевод (внутрипищеводное давление соответствует давлению в плевральной полости). В конце выдоха давление = -3-6 мм рт.ст (объем легкого уменьшился, ЭТЛ уменьшилась), а в конце вдоха давление = -6-9 мм рт.ст (объем легкого увеличился, ЭТЛ увеличилась).
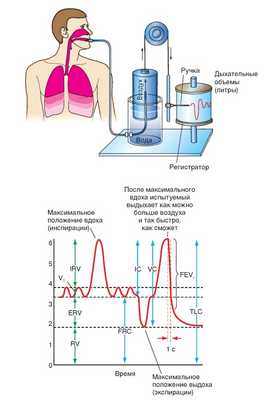
38. Спирометрия, спирография. Работы 3.17, 18- стр.102, 104
(1) дыхательный объем (ДО) - объем воздуха, который мы вдыхаем (и выдыхаем) во время одного спокойного вдоха (и выдоха) - 500 мл. Определяется методом спирометрии.
(2) резервный объем вдоха (РОвд) - объем воздуха, который мы можем вдохнуть после спокойного вдоха - 2000 мл. Определяется методом спирометрии.
(3) резервный объем выдоха (РОвыд) - объем воздуха, который мы можем выдохнуть после спокойного выдоха - 1500 мл. Определяется методом спирометрии.
(4) остаточный объем (ОО) - объем воздуха, который остается в легких после максимального выдоха - 1000 мл. Определяется методом разведения индикатора (гелий).
ЛЕГОЧНЫЕ ЕМКОСТИ (каждая емкость состоит из 2-х и более объемов)
(1) жизненная емкость легких (ЖЕЛ) - максимальный объем воздуха, который мы можем выдохнуть после максимально глубокого вдоха (ДО + РОвд + РОвыд) = 4-5 литров (значение: показатель общего физического развития). Определяется методом спирометрии.
(2) емкость вдоха - максимальный объем воздуха, который мы можем вдохнуть после спокойного выдоха (ДО + РОвд). Определяется методом спирометрии.
(3) функциональная остаточная емкость (ФОЕ) - объем воздуха, который остается в легких после спокойного выдоха (РОвыд + ОО) = 2500 мл (значение: показатель состояния эластической тяги легких. При снижении ЭТЛ этот показатель увеличивается). Определяется методом плетизмографии, разведения индикатора.
(4) общая емкость легких (ОЕЛ) - объем воздуха, который находится в легких после максимально глубокого вдоха (сумма всех 4-х объемов) = 5-6 литров. Определяется методом плетизмографии, разведения индикатора.
39.Показатели вентиляции: минутный объем дыхания, альвеолярная вентиляция, максимальная вентиляция легких. . Работа 3.21- стр.110 + учебник
Минутный объем дыхания (МОД) - объем воздуха, который проходит через легкие за минуту. МОД = ДО (дыхательный объем) х ЧД (частота дыхания) = 6-8 л/мин
Альвеолярная вентиляция (АВ) - объем воздуха, который проходит через альвеолярное пространство за минуту и участвует в газообмене.
АВ = (ДО - ОМП) х ЧД, где ОМП - объем мертвого пространства (150 мл - объем дыхательных путей, в котором не происходит газообмен). Например, АВ = (500 - 150) х 12 = 4200 мл/мин
Максимальная вентиляция легких (МВЛ) - максимальный объем воздуха, который может пройти через легкие за минуту (при максимально возможной глубине и частоте дыхания). Показывает резервные возможности дыхательного аппарата. Достигает 180 л/мин. (Исследование проводится 10-15 сек).
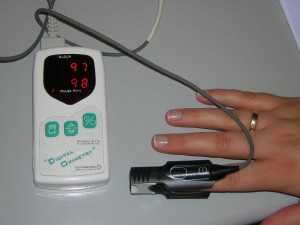
40. Оксигемометрия, пульсоксиметрия . Работа 3.25- стр.114
Пульсоксиметрия — методика определения количества кислорода, связанного с гемоглобином, в артериальной крови. К каждой молекуле гемоглобина может присоединится до четырех молекул кислорода. Средний процент насыщения молекул гемоглобина является кислородной сатурацией крови. 100% сатурация означает, что к каждая молекула гемоглобина в исследуемом объеме крови переносит четыре молекулы кислорода.
Принцип работы пульсоксометра основан на дифференцированном поглощении света с разной длинной волны гемоглобином в зависимости от степени насыщения кислородом.
Пульсоксиметор состоит из источника света двух длин волн (660 нм «красный» и 940 нм «инфракрасный»), фотоприемника, процессора, монитора.
- Периферический датчик изучает «красный» и «инфракрасный» свет.
- Кровь поглощает излучение (степень зависит от сатурации кислорода).
- Оставшийся световой поток улавливается фотоприемником.
- Полученные данные обрабатываются в процессорном блоке и выводятся на экран монитора.
1.
41. Пневмотахометрия и пик-флоуметрия, индекс Тиффно . Работы 3.19, 20- стр.107, 108
Пневмотахометрия- определение объемной скорости движения воздуха (л/сек) через датчик во время (а) форсированного вдоха и (б) форсированного выдоха. При увеличении сопротивления дыхательных путей пневмотахометрические показатели уменьшаются.
Пикфлоуметрия(англ. Peak Flow) - метод функциональной диагностики для определения пиковой объемной скорости форсированного выдоха. Иными словами данный метод помогает оценить, с какой скоростью человек может выдохнуть воздух, и таким образом оценить степень обструкции (сужения) дыхательных путей.
Для данного метода исследования существует специальный прибор - пикфлоуметр, который представляет собой компактную трубочку с градуированной шкалой.
Процедура проводится в положении сидя (или стоя). Сначала следует сделать несколько спокойных вдохов и выдохов, после чего делается глубокий вдох, мундштук пикфлоуметра плотно обхватывается губами и производится глубокий форсированный выдох. При этом следует держать аппарат строго параллельно поверхности пола. За каждый сеанс требуется сделать не менее 3 выдохов через некоторые промежутки времени (2-3 мин.), и выбрать максимальное значение.

При достижении им максимального результата (которые должны быть приближены к норме) его умножают на коэффициент 0.8 - например, если максимальный показатель пикфлоуметрии 400 л/мин, то 400 умножают на 0,8. Получаем 320 л/мин. Значение измерения выше этого показателя будет относиться к «зеленой зоне» - то есть нормальному уровню проходимости дыхательных путей. «Желтая зона» - это максимальный показатель исследования, умноженный на коэффициент 0,5. То есть 400 умножаем на 0,5 и получаем 200 мл/мин (это будет нижней границей желтой зоны). В этом случае границами «желтой зоны» будут значения от 200 л/мин до 320 л/мин.
Определение объема форсированного выдоха (проба Тиффно) за первую секунду (ОФВ1) - во время спирометрического исследования пациент должен сделать максимальный вдох, задержать дыхание на вдохе, а потом как можно быстрее выдохнуть. За первую секунду форсированного выдоха в норме он должен выдохнуть 70% от форсированной жизненной емкости легких. При увеличении сопротивления дыхательных путей этот показатель уменьшается.
Сенсорные системы
42. Определение остроты зрения. Работа 6.1- стр.232
43. Аккомодационный рефлекс. Значение. Работа 6.2- стр.233
44. Зрачковый рефлекс Физиологическое значение. Работа 6.9- стр.239
45. Исследование цветового зрения. Работа 6.5- стр.236
46. Определение световой и темновой адаптации зрения (адаптометрия) учебник
На процесс присоединения кислорода к гемоглобину влияют следующие факторы: концентрация ионов водорода, напряжение углекислого газа, температура, концентрация 2,3-дифосфоглице-рата (2,3-ДФГ). Их суммарный эффект на взаимодействие гемоглобина с кислородом отражает величина P50 — значение напряжения кислорода, при котором гемоглобин насыщен на 50% (рис. 22-23). Изменение каждого из факторов способно смещать кривую диссоциации вправо (увеличение P50) или влево (уменьшение Р.™). Сдвиг вправо вызывает снижение сродства гемоглобина к кислороду, вытесняет кислород из связи с гемоглобином и увеличивает количество кислорода, доступного тканям; сдвиг влево дает обратный эффект. В норме P50 составляет 26,6 мм рт. ст. (3,4 кПа).
Увеличение концентрации ионов водорода в крови снижает связывание гемоглобина с кислородом (эффект Бора).Форма кривой диссоциации оксигемоглобинатакова, что этот эффект более выражен в венозной крови, чем в артериальной (рис. 22-23); данный феномен облегчает осво-
бождение кислорода в тканях, практически не сказываясь на потреблении кислорода (в отсутствие тяжелой гипоксии).
Влияние напряжения CO2 на сродство гемоглобина к кислороду имеет важное физиологическое значение; вместе с тем оно вторично по отношению к увеличению концентрации ионов водорода, которая возрастает с увеличением PCO2. Высокое содержание CO2 в венозном сегменте капилляров, снижая сродство гемоглобина к кислороду, облегчает освобождение кислорода в тканях; наоборот, низкое содержание CO2 в легочных капиллярах вновь увеличивает сродство гемоглобина к кислороду, облегчая поглощение кислорода из альвеол.
2,3-ДФГ, побочный продукт гликолиза (шунт Rapoport-Luebering), накапливается при анаэробном метаболизме. Хотя эффект 2,3-ДФГ на гемоглобин теоретически благоприятен для организма (уменьшается сродство гемоглобина к кислороду и облегчается освобождение O2 в тканях.— Примеч. ред.), его физиологическое значение невелико. 2,3-ДФГ, тем не менее, играет важную компенсаторную роль при хронической анемии и существенно влияет на транспортную функцию гемоглобина донорской крови при гемотрансфузиях (гл. 29).
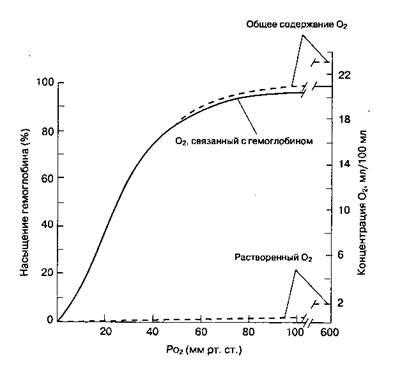
Рис. 22-22. Кривая диссоциации оксигемоглобина у здорового взрослого человека. (С разрешения. Из: West J. В. Respiratory Physiology: The Essentials, 3rd ed. Williams & Wilkins, 1985.)
Аномальные лиганды и аномальные формы гемоглобина
Окись углерода (СО), цианиды, азотная кислота и аммиак moitt связываться с гемоглобином в местах соединения с кислородом. Они вытесняют кислород и смещают кривую диссоциации влево. Угарный газ отличается особенной активностью: его сродство к гемоглобину в 200-300раз выше, чем у кислорода. СО связывается с гемоглобином, образуя карбоксигемоглобин, что снижает кислородную емкость гемоглобина и нарушает освобождение кислорода в тканях.
При окислении железа тема до трехвалентной формы образуется метгемоглобин. В редких случаях нитраты, нитриты, сульфаниламиды и другие лекарственные средства могут вызывать сильную метгемоглобинемию. Метгемоглобин неспособен связывать кислород, до тех пор пока он не будет восстановлен с помощью фермента метгемо-глобинредуктазы; кроме того, метгемоглобин смещает кривую диссоциации оксигемоглобина влево. Метгемоглобинемия, как и отравление угарным газом, снижает кислородную емкость крови и нарушает высвобождение кислорода в тканях. Метилено-вый синий и аскорбиновая кислота способствуют восстановлению метгемоглобина в гемоглобин.
Аномальные формы гемоглобина возникают в результате изменений в составе белковых субъединиц. Каждый вариант имеет собственные характеристики связывания с кислородом. Наиболее распространенные аномальные формы гемоглобина включают фе-тальный гемоглобин, гемоглобин A2, гемоглобин при серповидно-клеточной анемии (гл. 29).
Содержание кислорода в крови
Общее содержание кислорода в крови равно сумме физически растворенного и связанного с гемоглобином кислорода. Связывание кислорода с гемоглобином никогда не достигает теоретического максимума, поэтому считают, что 1 г гемоглобина может связать приблизительно 1,31 мл кислорода. Содержание кислорода в крови (С, от англ, content — содержание) выражается следующим уравнением:
Содержание кислорода (в 100 мл крови) = = [(0,003 мл О2/ЮО мл крови/мм рт. ст.) х PO2] + + (SO2X HbX 1,31 мл/1 OO мл крови),
где Hb — концентрация гемоглобина (г/100 мл крови), a SO2 — насыщение гемоглобина кислородом (S, от англ, saturation — насыщенеие) при данном PO2.
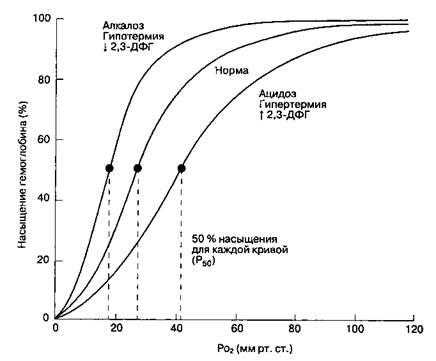
Рис. 22-23.Сдвиги кривой диссоциации оксигемоглобина при изменениях рН, температуры тела и концентрации 2,3-дифосфоглицерата (2,3-ДФГ) в эритроцитах
Используя эту формулу и величину Hb, равную 15 г/100 мл, можно рассчитать содержание O2 в артериальной pi смешанной венозной крови, а также артериовенозную разницу по кислороду (при SaO2 - 97,5 % и SvO2 = 75 %):
= 19,5 мл О2/100 мл крови;
CvO2-(0,003 х 40)+ (0,75 х 15 х 1,31) =
- 14,8 мл О2/100 мл крови;
Транспорт кислорода
Транспорт кислорода зависит как от дыхания, так и от кровообращения (гл. 19). Общая доставка кислорода (DO2; от англ, delivery — доставка) к тканям равна произведению содержания кислорода в артериальной крови и сердечного выброса:
Заметим, что содержание кислорода в артериальной крови зависит как от РлО2, так и от концентрации гемоглобина. Следовательно, недостаточная доставка кислорода может быть результатом низкого РлО2, низкой концентрации гемоглобина или низкого сердечного выброса. В норме расчет доставки кислорода выглядит так:
DO2 = 20 мл О2/1OO мл крови х 5000 мл /мин =
Уравнение Фикавыражает связь между потреблением O2, артериовенозной разницей по кислороду и сердечным выбросом:
Потребление O2 = VO2 = Qt x (CaO2 - CvO2). После преобразования получаем:
Следовательно, артериовенозную разницу можно рассматривать как меру адекватности доставки кислорода.
При нормальном потреблении кислорода около 250 мл/мин и сердечном выбросе 5000 мл/мин нормальная артериовенозная разница, согласно этому уравнению, составит 5 мл O2/!OO мл крови. Заметим, что при этом нормальный коэффициент экстракции O2 [(CaO2 - CvO2)/CaO2] составит 25 %, т. е. 5 мл/20 мл. Таким образом, в норме организм потребляет только 25 % кислорода, переносимого гемоглобином. Когда потребность в O2 превосходит возможность его доставки, то коэффициент экстракции становится выше 25 %. На-
оборот, если доставка O2 превышает потребность, то коэффициент экстракции падает ниже 25 %.
Если доставка кислорода снижена умеренно, потребление кислорода не изменяется благодаря увеличению экстракции O2 (насыщение гемоглобина кислородом в смешанной венозной крови снижается); в этом случае VO2 не зависит от доставки. По мере дальнейшего снижения DO2 достигается критическая точка, в которой VO2 становится прямо пропорционально DO2. Состояние, при котором потребление кислорода зависит от доставки, характеризуется прогрессирующим лак-тат-ацидозом (гл. 30), обусловленным клеточной гипоксией.
Кислородный резерв
Понятие кислородного резерва имеет большое значение в анестезиологии. Когда в результате апноэ прекращается поступление в организм кислорода, то в ходе клеточного метаболизма потребляется имеющийся кислородный резерв; после того как резерв исчерпан, развивается гипоксия и наступает смерть клеток. Теоретически нормальный кислородный резерв у взрослого человека составляет около 1500 мл. Он включает остатки кислорода в легких; кислород, находящийся в связи с гемоглобином и миоглобином; кислород, растворенный в жидкостях организма. К сожалению, высокое сродство гемоглобина к кислороду (сродство мио-глобина к кислороду еще выше), а также незначительное количество кислорода, физически растворенного в тканях, представляют собой очень малый резерв. Следовательно, основным источником кислорода является дыхательная смесь, находящаяся в легких в объеме, соответствующем ФОЕ (исходный объем при апноэ). Необходимо отметить, что только около 80 % этого объема может быть использовано.
При наступлении апноэ у больного, дышавшего перед этим атмосферным воздухом, в легких имеется примерно 480 мл кислорода (если FiO2 = 0,21 и ФОЕ = 2300 мл, то объем кислорода составит FiO2 X ФОЕ; 0,21 X 2300 мл = 480 мл). Метаболически активные ткани быстро используют этот резерв (предположительно со скоростью потребления кислорода); в течение 90 с развивается тяжелая гипоксемия. Возникновение гипоксемии можно отсрочить путем увеличения FiO2 перед апноэ. После дыхания чистым кислородом легкие содержат 2300 мл кислорода, что задерживат развитие гипоксемии после апноэ на 4-5 мин. Данная концепция лежит в основе проведения преоксигена-ции перед индукцией анестезии (гл. 5).
УГЛЕКИСЛЫЙ ГАЗ
CO2 транспортируется кровью в физически растворенном виде, в составе бикарбоната и в комплексе с белками в виде карбаминовых соединений (табл. 22-6). Сумма всех трех форм составляет общее содержание CO2 в крови, которое стандартным образом измеряется при анализе электролитов.
Физически растворенный CO2
CO2 растворяется в крови лучше, чем кислород, коэффициент его растворимости 0,031 ммоль/л/ мм рт. ст. при 37 0 C (0,067 мл/100 мл/мм рт. ст.)
Бикарбонат
В водных растворах CO2 медленно вступает в связь с водой, образуя бикарбонат:
В плазме в эту реакцию вступает менее 1 % растворенного CO2, тогда как в эритроцитах и в эндо-телиальных клетках имеется фермент карбо-ангидраза, который ее ускоряет. В результате бикарбонат представляет самую большую фракцию CO2 в крови (табл. 22-6). Ацетазоламид, будучи ингибитором карбоангидразы, может нарушать доставку CO2 от тканей к альвеолам.
В венозных сегментах капилляров большого круга кровообращения CO2 поступает в эритроциты, где трансфомируется в бикарбонат, который диффундирует из эритроцитов в плазму. Для поддержания электрического равновесия из плазмы в эритроциты перемещаются ионы Cl". В легочных капиллярах происходит обратный процесс: ионы Cl" выходят из эритроцитов, а бикарбонат поступает в них для превращения в CO2, который диффундирует в альвеолы. Перемещение ионов
Cl" носит название хлоридного сдвига,или сдвига Гамбургера.
Почему человек чувствует себя несчастным?: Для начала определим, что такое несчастье. Несчастьем мы будем считать психологическое состояние.
Как распознать напряжение: Говоря о мышечном напряжении, мы в первую очередь имеем в виду мускулы, прикрепленные к костям .
Почему двоичная система счисления так распространена?: Каждая цифра должна быть как-то представлена на физическом носителе.
Факторы влияющие на КДО. Влияние температуры на кривую диссоциации оксигемоглобина (КДО)
4.1. Транспорт кислорода
В сложных механизмах транспорта газов кровью и газообмена в тканях важная роль отводится эритроцитам, ответственным за доставку О2 к различным органам и удаление образующегося в процессе метаболизма СО2.
Эритроцит - безъядерная клетка, лишенная митохондрий, основным источником энергии для эритроцита служит глюкоза, метаболизируемая в гексозомонофосфатном шунте или цикле Эмбдена-Мейергофа. Транспорт О2 обеспечивается в значительной мере гемоглобином, состоящим из белка глобина и гема. Последний представляет собой комплексное соединение железа и порфирина. Глобин представляет собой тетрамер полипептидной цепи. Hb A (HbA) - основной гемоглобин взрослых содержит 2 - альфа и 2 - бета - цепи, Hb A2 - содержит две альфа и две дельта цепи.
Гем состоит из иона железа, встроенного в порфириновое кольцо. Ион железа гема обратимо связывает одну молекулу О2. С одной молекулой Hb максимально связываются 4 молекулы О2 с образованием оксигемоглобина.
Гем может подвергаться не только оксигенации, но и истинному окислению, когда железо становится из двухвалентного трехвалентным. Окисленный гем носит название гематина, а молекула гемоглобина становится метгемоглобином. В крови человека метгемоглобин находится в незначительных количествах, его уровень резко возрастает при отравлениях. Метгемоглобин не способен отдавать кислород тканям.
В норме метгемоглобин составляет менее 3% общего Hb крови. Основная форма транспорта О2 - в виде оксигемоглобина. Кислород транспортируется артериальной кровью не только в связи с гемоглобином, но и в растворенном виде. Принимая во внимание тот факт, что 1 г Hb может связать 1,34 мл О2, кислородная емкость крови в среднем у взрослого человека составляет около 200 мл/л крови. Одним из показателей кислородного транспорта является насыщение артериальной крови О2(Sa O2), равного отношению О2, связанного с Hb, к кислородной емкости крови:
SaO2=O2, связанного с Hb/O2 емкость крови* 100%.
В соответствии с кривой диссоциации оксигемоглобина насыщение артериальной крови кислородом в среднем составляет 97%, в венозной крови - 75%.
PaO2 в артериальной крови около 100 мм. рт. ст., а в венозной - около 40 мм. рт. ст.
Количество растворенного кислорода в крови пропорционально парциальному давлению О2 и коэффициэнту его растворимости.
Последний для О2 составляет 0,0031/100 мл крови/ 1 мм. рт. ст.. Таким образом, 100 мл крови при PaO2, равном 100 мм. рт. ст., содержит менее 0,31 мл O2.
Диссоциация оксигемоглобина в тканях обусловлена главным образом химическими свойствами гемоглобина, а также рядом других факторов - температурой тела, рН среды, р СО2.
При понижении температуры тела наклон кривой диссоциации оксигемоглобина возрастает, а при ее повышении - снижается, и соответственно снижается сродство Hb к О2.
При снижении рН, т.е. при закислении среды, сродство гемоглобина к О2 уменьшается. Увеличение напряжения в крови СО2 также сопровождается снижением сродства Hb к О2 и уплощением кривой диссоциации оксигемоглобина.
Известно, что степень диссоциации оксигемоглобина определяется содержанием в эритроцитах некоторых фосфорорганических соединений, главным из которых является 2,3 - ДФГ (2,3 дифосфоглицерат), а также содержанием в эритроцитах катионов. В случаях развития алкалозов, поглощение О2 в легких увеличивается, но в то же время затрудняется отдача кислорода тканями. При ацидозах наблюдается обратная картина.
4.2.Утилизация кислорода тканями
Тканевое или клеточное дыхание включает три стадии. На первой стадии пируват, аминокислоты и жирные кислоты окисляются до двухуглеродных фрагментов ацетильных групп, входящих в состав ацетилкофермента А. Последние на втором этапе окисления включаются в цикл лимонной кислоты, где происходит образование высокоэнергетических атомов водорода и высвобождение СО2 - конечного продукта окисления органических субстратов. На третьей стадии клеточного дыхания атомы водорода делятся на протоны (Н+) и «высокоэнергетические» электроны, передающиеся по дыхательной цепи на молекулярный О2 и восстанавливающие его до НО2. Перенос электронов сопряжен с запасом энергии в форме АТФ, т.е. с окислительным фосфорилированием (рис.6).
Касаясь патогенеза метаболических сдвигов, свойственных гипоксическим состояниям, следует отметить, что в организме человека более 90% всего потребляемого кислорода восстанавливается с участием цитохромоксидазы митохондрий, и лишь около 10% кислорода метаболизируется в тканях с участием оксигеназ: диоксигеназы и монооксигеназы.
Рис.6. Схема тканевого дыхания. Конечные продукты каждой стадии даны в рамке (Ленинджер А., 1999)
Наиболее многочисленны и сложны монооксигеназные реакции, протекающие в эндоплазматическом ретикулуме клеток при участии цитохрома Р-450 и обеспечивающие гидроксилирование субстрата (стероидных гормонов, лекарственных препаратов и различных др. соединений) и, как правило, его инактивацию.
Диоксигеназы катализируют реакции, в которых в молекулу органического субстрата включаются оба атома молекулы кислорода (например, реакция окисления катехола молекулярным кислородом с раскрытием кольца).
В реакциях, связанных с переносом электронов, т.е. в реакциях окисления-восстановления, где, как указывалось выше, используется более 90% потребляемого кислорода, атомы водорода, отщепленные дегидрогеназами от субстратов в цикле лимонной кислоты, передают свои электроны в цепь переноса электронов и превращаются также в Н +. Как известно, помимо 4 пар атомов водорода, поставляемых каждым оборотом цикла лимонной кислоты, образуются и другие атомы водорода, отщепленные дегидрогеназами от пирувата, жирных кислот и аминокислот в процессе их расщепления до Ацетил-СоА и других продуктов.
Таким образом, все атомы водорода, отщепляемые дегидрогеназами от субстратов, передают свои электроны в дыхательную цепь к конечному акцептору электронов - кислороду.
Касаясь последовательности транспорта электронов в окислительно-восстановительных реакциях, протекающих на внутренней мембране митохондрий, прежде всего, следует отметить, что от всех НАД - зависимых реакций дегидрирования восстановленные эквиваленты переходят к митохондриальной НАДН - дегидрогеназе, затем через ряд железосерных ферментов передаются на убихинон М цитохрому b. Далее электроны переходят последовательно на цитохромы С1 и С, затем на цитохромы аа 3 (цитохромоксидазу - медьсодержащий фермент). В свою очередь цитохромоксидаза передает электроны на кислород. Для того, чтобы полностью восстановить кислород с образованием 2-х молекул воды требуется 4 электрона и четыре Н+ .
Скорость утилизации О2 в различных тканях различна. В среднем взрослый человек потребляет 250 мл О2 в 1 мин. Максимальное извлечение О2 из притекающей артериальной крови свойственно миокарду.
Кислород используется в клетках, в основном в метаболизме белков, жиров, углеводов, ксенобиотиков, в окислительно-восстановительных реакциях в различных субклеточных фракциях: в митохондриях, в эндоплазматическом ретикулуме, в реакциях липопероксидации, а также в межклеточном матриксе и в биологических жидкостях.
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность - кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
Обмен дыхательных газов в тканях происходит в процессе свободной и облегченной диффузии. При этом О2 переносится по градиенту напряжения газа из эритроцитов и плазмы крови в окружающие ткани.
Одновременно происходит диффузия СО2 из тканей в кровь. На выход О2 из крови в ткани влияет диссоциация оксигемоглобина в эритроцитах, что обеспечивает так называемую облегченную диффузию О2. Интенсивность диффузионного потока О2 и СО2 определяется градиентом их напряжения между кровью и тканями, а также площадью газообмена, плотностью капилляров, распределением кровотока в микроциркуляторном русле. Интенсивность окислительных процессов в тканях определяется величиной критического напряжения О2 в митохондриях, которое в условиях нормы должно превосходить 0,1-1 мм рт. ст.
Соответствие доставки О2 к органам и тканям, возросшим потребностям в оксигенации обеспечивается на клеточном, органном уровнях за счет образования метаболитов изнашивания, а также при участии нервных, гормональных и гуморальных влияний.
Основная масса углекислого газа (СО2) образуется в организме как конечный продукт различных метаболических реакций и транспортируется к легким с кровью. Вдыхаемый воздух содержит лишь незначительное количество СО2.
Транспорт СО2 кровью осуществляется в 3-х состояниях: в виде аниона бикарбоната, в растворенной форме и в виде карбаминовых соединений.
СО2 хорошо растворяется в плазме крови и в артериальной крови, около 5% от общей двуокиси углерода содержится в крови в растворенной форме.
Анион бикарбоната составляет около 90% от общего содержания СО2 в артериальной крови: СО2+Н2О - Н++НСО-3.
Эта реакция медленно протекает в плазме крови, но чрезвычайно интенсивно происходит в эритроцитах при участии фермента карбоангидразы. Мембрана эритроцита относительно непроницаема для Н+, как и вообще для катионов, но в тоже время, проницаема для ионов НСО-3, выход которых из эритроцитов в плазму обеспечивается притоком Cl- из плазмы в эритроциты. Часть Н+ забуферивается гемоглобином с образованием восстановленного гемоглобина.
Третьей формой транспорта СО2 кровью являются карбаминовые соединения, образованные взаимодействием СО2 с концевыми группами белков крови преимущественно с гемоглобином:
Hb NH2 + CO2 - Hb NH COOH > Hb NH COO + Н+
Карбаминовые соединения составляют около 5% от общего количества СО2, транспортируемого кровью.
В оксигенированной артериальной крови напряжение СО2 составляет 40 мм. рт. ст., а в венозной крови Рv СО2 равно 46 мм. рт. ст.
4.4.Связывание гемоглобина с окисью углерода
Угарный газ (СО) - окись углерода обладает значительно большим сродством к гемоглобину, чем О2, с последующим образованием карбоксигемоглобина. СО входит в состав бытового газа, а также выделяется при работе двигателей внутреннего сгорания. При концентрации СО во вдыхаемом воздухе всего в количестве 7*10- 4 около 50% гемоглобина превращается в карбоксигемоглобин. В норме в крови содержится около 1% HbCO, у курильщиков - 3% . В крови водителей такси концентрация карбоксигемоглобина достигает 20%. Карбоксигемоглобин диссоциирует с отдачей О2 в 200 раз медленней оксигемоглобина и в то же время препятствует его диссоциации в тканях.
Читайте также:
