Фазы развития сердца. Теория филогенетического происхождения пороков сердца
Добавил пользователь Владимир З. Обновлено: 22.01.2026
Такое деление в значительной мере условно, так как при одном и том же ВПС возможны сочетания, которые изменяют направления сброса крови в течение жизни, сделав его из «бледного» — «синим», или сочетаются с нарушениями ритма. Тем не менее, такая классификация наиболее широко применяется и охватывает большинство известных ВПС . Она достаточно проста и понятна, и известна врачам и родителям. Рассмотрим ее более подробно.
К порокам со сбросом слева-направо («бледные пороки») относят, в частности, открытый артериальный проток, дефекты межпредсердной и межжелудочковой перегородок, общее предсердие, аномальный дренаж легочных вен, открытый общий атрио-вентрикулярный канал, дефекты аорто-легочной перегородки.
К порокам с преимущественным сбросом справа-налево («синие пороки») относятся тетрада Фалло, многочисленные варианты транспозиций магистральных сосудов, аномалия Эбштейна, атрезия трехстворчатого клапана, общий артериальный ствол, варианты единственного желудочка, синдром гипоплазии левого сердца, гипоплазия правого желудочка.
Пороки с перекрестным сбросом могут включать все три перечисленные группы, если имеются те или иные сочетания, например, атро-вентрикулярный канал и тетрада Фалло, общий артериальный ствол.
Группа пороков с препятствием кровотоку включает коарктации аорты, сужение или стеноз аортального клапана, стеноз клапана легочной артерии, стеноз митрального клапана, стенозы ветвей легочной артерии.
Пороки клапанного аппарата — это отдельная группа, в которую включаются только нарушения развития атрио-вентрикулярных или полулунных клапанов без сочетания с другими внутрисердечными нарушениями. Сюда относят пролапс (недостаточность) митрального (и трикуспидального) клапана и его стеноз и недостаточность клапанов аорты и легочной артерии.
Пороки венечных артерий включают все нарушения их нормального развития: аномальное отхождение их устьев, коронаро-сердечные фистулы.
Кардиомиопатии, или врожденные нарушения мышечного аппарата желудочков сердца.
Врожденные нарушения ритма сердца, которые не сочетаются ни с какими другими ВПС, а являются единственным заболеванием.
Цитируется по книге Г. Э. Фальковский, С. М. Крупянко. Сердце ребенка. Книга для родителей о врожденных пороках сердца
Филогенетически обусловленные пороки сердечно сосудистой системы у человека
Пороки сердца и сосудов одна из распространенных групп пороков и составляет 6-10 случаев на 1000 новорожденных. Их имеют 6,6% детей умерших в возрасте до 1 года. Для некоторых пороков прослеживаются и половые различия. Например, стеноз, коартация аорты, транспозиция крупных сосудов - чаще встречается у лиц мужского пола; Дефект перегородки, Баталов проток - у женщин. Пороки сердца могут сочетаться с пороками других систем (61% - множественные пороки). Они постоянные спутники генных и хромосомных синдромов.
1. Пороки положения сердца
1. Эктопия сердца- расположение сердца вне грудной полости. Различают: шейную, абдоминальную, экстрастернальную.
Шейную форму объясняют задержкой дислокации сердца с места формирования его зачатка (шея) в переднее средостение. Плод погибает сразу же после рождения.
Абдоминальная форма связана с аномалиями развития диафрагмы. Сердце при этом располагается в эпигастрии или в области одной из почек. Протекает бессимптомно. Если сердце нормально сформировано, пациенты могут достигать преклонного возраста.
Экстрастернальная форма является следствием аномалий развития грудины (аплазия, щель). Составляет 51.2% от всех случаев эктопий. Порок редкий, обычно сочетается с другими кардинальными и экстракардиальными пороками. При этой форме эктопии показано срочное оперативное вмешательство.
2. Декстрокардия— расположение сердца справа.
1. Наблюдается при обратном расположении всех внутренних органов. Т.Т.П. - до З-й недели беременности.
2. Изолированный порок с инверсией полостей. Т.Т.П. - до 7-й недели беременности.
3. Только декстрокардия с нормальным расположением полостей. Т.Т.П. - до 7-й недели беременности.
II. Пороки сердца и его камер
1. Акардия— отсутствие сердца (полное или зачаточный вид). Т.Т.П. - до З недели.
2. Микрокардия- как самостоятельный порок неизвестна. Обычно сочетается с гипоплазией других висцеральных органов.
З. Макрокардия(кардиомегалия) - избыточное развитие миокарда. Как правило, сочетанный порок.
4.Двухкамерное сердце- отсутствие межпредсердной и межжелудочковой перегородок. Редкий летальный порок. ТТП - до 3 4-го дня беременности.
5. Трехкамерное сердце с одним общим желудочком- полное отсутствие межжелудочковой перегородки. Редкий порок, обычно сочетающийся с гипоплазией сердца транспозицией или стенозом легочного ствола. Дети умирают вскоре после рождения. ТТП - до 44-го дня беременности.
6.Трехкамерное сердце с одним общим предсердием- отсутствие межпредсердной перегородки. Довольно редкий, летальный порок, сочетающийся с другими пороками сердца и крупных сосудов.
7. Дефект межпредсердной перегородки- один из наиболее часто встречающихся пороков сердца. Частота встречаемости 1 случай на 1000 рождений. Как изолированный порок составляет 7 - 25% всех случаев врожденных пороков сердца.
Чаще встречается у женщин (1,7 1), чем у мужчин. Различают дефекты первичной и вторичной межпредсердных перегородок.
Дефект первичной межпредсердной перегородки - низкий дефект, располагающийся непосредственно над атриовентрикулярными клапанами. Образуется в результате остановки в развитии, вследствие чего не происходит срастания между перегородкой и растущими снизу вверх эндокардиальными подушками предсердно-желудочкового канала. ТТП - до 7-ой недели внутриутробного развития.
Дефект вторичной межпредсердной перегородки - высокий дефект, формирующийся так же, как и низкий, о нарушение развития в основном касается вторичной перегородки. В таком случае вместо овального окна имеется дефект диаметром 1-6 см. ТТП - до 55-го дня. Встречается реже первичного дефекта.
8. Дефект межжелудочковой перегородки - Изолированные дефекты встречаются с частотой 2,5-5 случаев на 1000 живорожденных. В 85 - 90% случаев дефект располагается в верхней, перепончатой части перегородки, непосредственно под устьем аорты. ТТП - до 44-го дня беременности. Жизненный прогноз при малых дефектах благоприятный, при значительных - большая часть детей погибает в возрасте до 1 года, продолжительность жизни остальных в среднем 20 - 25 лет. Лечение хирургическое. В 15 - 10% случаях дефект (до 1 ем) располагается в мышечной части межжелудочковой перегородки. Прогноз благоприятный, хирургического лечения не требует.
Врожденные пороки сердца
Врожденные пороки сердца - группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции - оперативной коррекции выявленной аномалии.
Общие сведения
Врожденные пороки сердца - весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП - 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий - глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца - болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой - электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
99.Филогенез кровеносной системы хордовых животных. Филогенез артериальных жаберных дуг. Онтофилогенетические пороки сердца и кровеносных сосудов у человека.
Необходимым условием существования высокоорганизованных крупных многоклеточных организмов является наличие жидкой подвижной внутренней среды,которая обеспечивает интеграцию организма в целостную систему, выполняя транспортные функции. Эти функции являются основными для кровеносной системы. Конкретная функция кровеносной системы зависит от того, что она транспортирует: питательные вещества, кислород, углекислый газ, другие продукты диссимиляции или гормоны. Кровеносная система всех хордовых замкнутая и состоит из двух основных артериальных сосудов:брюшной испинной аорт.По брюшной аорте венозная кровь продвигается кпереди, обогащается кислородом в органах дыхания, а по спинной — кзади. Из спинной аорты кровь через систему капилляров возвращается по венам в брюшную аорту. Брюшная аорта или ее часть, периодически сокращаясь, проталкивает кровь по сосудам (рис. 14.27).
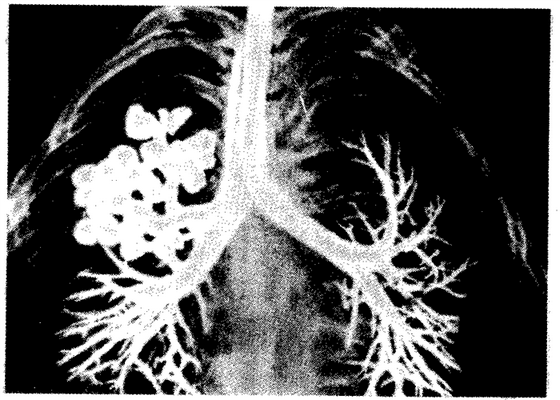
Рис. 14.26.Кистозная гипоплазия легкого
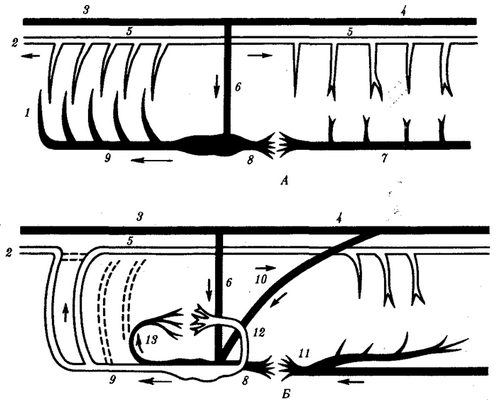
Рис. 14.27.Строение кровеносной системы водных (А)и наземных (Б) позвоночных:
1—жаберные артерии, 2—сонная артериям—передняя кардинальная вена, 4—задняя кардинальная вена,5—спинная аорта, 6—кювьеров проток, 7—подкишечная вена, 8—печеночная вена,9—брюшная аорта, 10—задняя (нижняя) полая вена, 11—воротная вена печени, 12—легочная вена, 13—легочная артерия; стрелками указано направление движения крови
14.4.1. Эволюция общего плана строения
Кровеносной системы хордовых
У ланцетника кровеносная система наиболее проста (рис. 14.28,А). Круг кровообращения один. По брюшной аорте венозная кровь поступает в приносящие жаберные артерии, которые по количеству соответствуют числу межжаберных перегородок (до 150пар), где и обогащается кислородом.
По выносящим жаберным артериям кровь поступает в корни спинной аорты, расположенные симметрично с двух сторон тела. Они продолжаются как вперед, неся артериальную кровь к головному мозгу, так и назад. Передние ветви этих двух сосудов являются сонными артериями.На уровне заднего конца глотки задние ветви образуют спинную аорту, которая разветвляется на многочисленные артерии, направляющиеся к органам и распадающиеся на капилляры.
После тканевого газообмена кровь поступает в парные передниеилизадние кардинальные вены,расположенные симметрично. Передняя и задняя кардинальные вены с каждой стороны впадают вкювьеров проток.Оба кювьеровых протока впадают с двух сторон в брюшную аорту. От стенок пищеварительной системы венозная кровь оттекает поворотной вене печенив печеночный вырост, где формируется система капилляров. Затем капилляры вновь собираются в венозный сосуд — печеночную вену,по которой кровь поступает вбрюшную аорту.
Таким образом, несмотря на простоту кровеносной системы в целом, уже у ланцетника имеются основные магистральные артерии, характерные для позвоночных, в том числе для человека: это брюшная аорта, преобразующаяся позже в сердце, восходящую часть дуги аорты и корень легочной артерии; спинная аорта,становящаяся позже собственно аортой, исонные артерии.Основные вены, имеющиеся у ланцетника, также сохраняются у более высокоорганизованных животных. Так, передние кардинальные вены станут позжеяремными венами, правый кювьеров проток преобразуется вверхнюю полую вену,а левый, сильно редуцировавшись, —вкоронарный синус сердца.Для того чтобы понять, как это происходит, необходимо сопоставить кровеносные системы всех классов позвоночных животных.
Более активный образ жизни рыб предполагает более интенсивный метаболизм. В связи с этим на фоне олигомеризации их артериальных жаберных дуг в конечном счете до четырех пар в них отмечается высокая степень дифференцировки: жаберные сосуды распадаются на капилляры, пронизывающие жаберные лепестки. В процессе интенсификации сократительной функции брюшной аорты часть ее преобразовалась в двухкамерное сердце,состоящее из предсердия и желудочка и располагающееся под нижней челюстью, рядом с жаберным аппаратом. В остальном кровеносная система рыб соответствует строению ее у ланцетника (рис. 14.28,Б).
В связи с выходом земноводных на сушу и появлением легочного дыхания у них возникает два круга кровообращения. Соответственно этому в строении сердца и артерий появляются приспособления, направленные на разделение артериальной и венозной крови. Перемещение земноводных в основном за счет парных конечностей, а не хвоста обусловливает изменения в венозной системе задней части туловища.
Сердце амфибий расположено каудальнее, чем у рыб, рядом с легкими; оно трехкамерное,но, как и у рыб, от правой половины единственного желудочка начинается единственный сосуд —артериальный конус,разветвляющийся последовательно на три пары сосудов:
кожно-легочные артерии, дуги аорты и сонные артерии. Как и у всех более высокоорганизованных классов, в правое предсердие впадают вены большого круга, несущие венозную кровь, в левое— малого с артериальной кровью. При сокращении предсердий в желудочек, внутренняя стенка которого снабжена большим количеством мышечных перекладин, одновременно попадают обе порции крови. Полного их смешения из-за своеобразного строения стенки желудочка не происходит, поэтому при его сокращении первая порция венозной крови поступает в артериальный конус и с помощью спирального клапана, находящегося там, направляется в кожно-легочные артерии. Кровь из середины желудочка, смешанная, поступает таким же образом в дуги аорты, а оставшееся небольшое количество артериальной крови, последней попадающей в артериальный конус, направляется в сонные артерии.
Две дуги аорты, несущие смешанную кровь, огибают сердце и пищевод сзади, образуя спинную аорту, снабжающую все тело, кроме головы, смешанной кровью. Задние кардинальные вены сильно редуцируются и собирают кровь только с боковых поверхностей туловища. Функционально их замещает возникшая заново задняя полая вена, собирающая кровь в основном из задних конечностей. Она располагается рядом со спинной аортой и, находясь позади печени, вбирает в себя печеночную вену, которая у рыб впадала непосредственно в венозный синус сердца. Передние кардинальные вены, обеспечивая отток крови от головы, называют теперь яремными венами,а кювьеровы потоки, в которые они впадают вместе с подключичными венами, — передними полыми венами(рис. 14.28,В).
В кровеносной системе пресмыкающихся возникают следующие прогрессивные изменения: в желудочке их сердца имеется неполная перегородка, затрудняющая смешение крови, поступающей из правого и левого предсердий; от сердца отходит не один, а три сосуда, образовавшихся в результате разделения артериального ствола. Из левой половины желудочка начинается правая дуга аорты, несущая артериальную кровь, а из правой —легочная артерия с венозной кровью. Из середины желудочка, в области неполной перегородки, начинается левая дуга аорты со смешанной кровью. Обе дуги аорты, как и у предков, срастаются позади сердца, трахеи и пищевода в спинную аорту, кровь в которой смешанная, но более богата кислородом, чем у земноводных, в связи с тем что до слияния сосудов только по левой дуге течет смешанная кровь. Кроме того, сонные и подключичные артерии с обеих сторон берут начало от правой дуги аорты, в результате чего артериальной кровью снабжается не только голова, но и передние конечности. В связи с появлением шеи сердце располагается еще более каудально, чем у земноводных. Венозная система пресмыкающихся принципиально не отличается от системы вен земноводных (рис. 14.28,Г).
Прогрессивные изменения кровеносной системы млекопитающих сводятся к полному разделениювенозного и артериального кровотоков. Это достигается, во-первых, завершеннойчетырехкамерностью сердца и, во-вторых, редукцией правой дуги аорты и сохранением только левой, начинающейся от левого желудочка. В результате все органы млекопитающих снабжаются артериальной кровью. В венах большого круга кровообращения также обнаруживаются прогрессивные изменения: возникла безымянная вена, объединяющая левые яремную и подключичную вены с правыми, в результате чего остается лишь одна передняя полая вена, располагающаяся справа. Левый кювьеров проток в виде рудиментарного сосудаsinuscoronariusтеперь собирает венозную кровь только от миокарда, а непарная и полунепарная вены —рудименты задних кардинальных вен, имеют существенное значение в основном в случаях формирования обходных путей венозного оттока через кава-кавальные анастомозы, формируемые ими (рис. 14.28,Д).
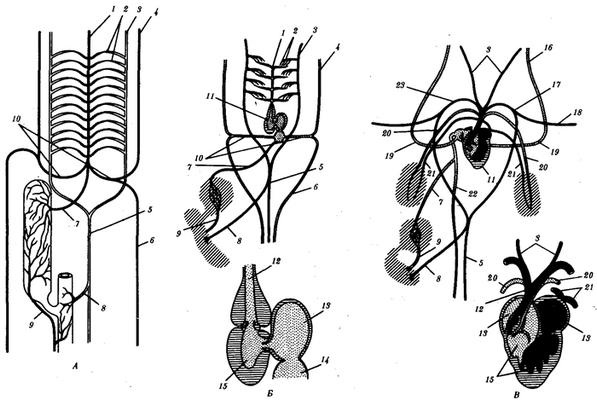
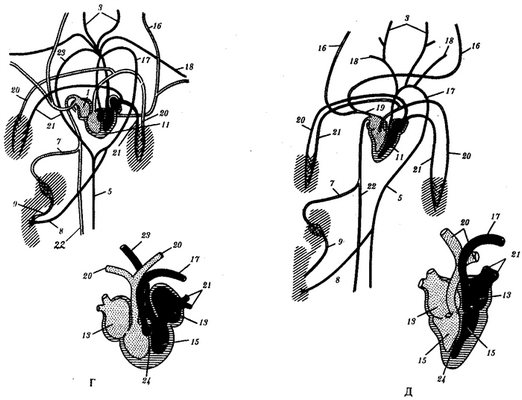
Рис 14.28.Строение кровеносной системы и сердца хордовых животных.
А—ланцетника;Б—рыбы;В—земноводного;Г—пресмыкающегося; Д—млекопитающего:
1—брюшная аорта, 2—жаберные артерии, 3—сонная артерия,4—передняя кардинальная вена,5—спинная аорта, 6—задняя кардинальная вена, 7—печеночная вена, 8—чревная артерия, 9—воротная вена печени, 10—кювьеровы протоки,11—сердце, 12—артериальный конус,13—предсердие, 14—венозный синус,15—желудочек,16—яремная вена, 17—левая дуга аорты,18—подключичная артерия, 19—передняя полая вена, 20—легочная артерия, 21—легочная вена, 22—задняя полая вена, 23—правая дуга аорты, 24—межжелудочковая перегородка
В эмбриональном развитии млекопитающих и человека рекапитулируют закладки сердца и основных кровеносных сосудов предковых классов.
Сердцезакладывается на первых этапах развития в виде недифференцированной брюшной аорты, которая за счет изгибания, появления в просвете перегородок и клапанов, становится последовательно двух-, трех- и четырехкамерным (рис. 14.29).Однако рекапитуляции здесь неполны в связи с тем, что межжелудочковая перегородка млекопитающих формируется иначе и из другого материала по сравнению с рептилиями. Поэтому можно считать, что четырехкамерное сердце млекопитающих формируется на базе трехкамерного сердца, а межжелудочковая перегородка является новообразованием, а не результатом доразвития перегородки пресмыкающихся. Таким образом, в филогенезе сердца позвоночных проявляется девиация: в процессе морфогенеза этого органа у млекопитающих рекапитулируют ранние филогенетические стадии, а затем развитие его идет в ином направлении, характерном лишь для этого класса.
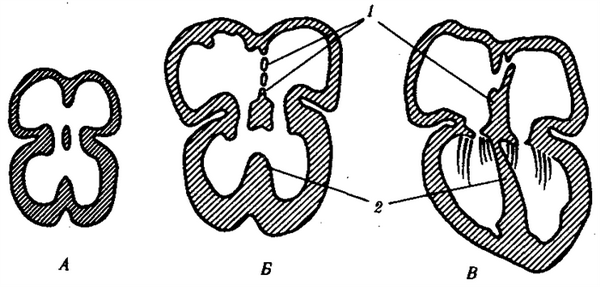
Рис. 14.29.Развитие перегородок сердца у зародыша человека в возрасте 30сут (А) 35сут (Б) и 2мес (Д):1—межпредсердная, 2—межжелудочковая
Интересно, что место закладки и положение сердца в филогенетическом ряду позвоночных полностью рекапитулируют у млекопитающих и человека. Так, закладка сердца у человека осуществляется на 20-е сутки эмбриогенеза, как у всех позвоночных, позади головы. Позже за счет изменения пропорций тела, появления шейной области, смещения легких в грудную полость осуществляется и перемещение сердца в переднее средостение.
Нарушения развития сердцамогут выражаться как в возникновении аномалий строения, так и места его положения. Возможно сохранение к моменту рождения двухкамерного сердца. Этот порок совершенно не совместим с жизнью.
Чаще встречаются дефекты межпредсердной перегородки (1случай на 1000рождений), межжелудочковой перегородки (2,5—5случаев на1000рождений), вплоть до трехкамерного сердца с одним общим желудочком (см. рис. 14.31,В).Известен и такой порок, как шейная эктопия сердца, при которой оно находится в шейной области. Этот порок связывают с задержкой сердца в области его первоначальной закладки. При этом ребенок обычно погибает сразу после рождения. Перечисленные пороки сердца наиболее часто встречаются не в изолированном виде, а в комплексе с другими аномалиями сердца, сосудов, а нередко и других органов. Это свидетельствует о том, что в морфо-генезе сердца большое значение имеют онтогенетические корреляции (см. § 13.4).Состояние больных при таких пороках зависит от того, насколько сильно нарушается гемодинамика и осуществляется смешение крови в кровеносном русле.
Когда происходит формирование врожденного порока сердца
Беременным женщинам важно знать, что формирование порока сердца происходит на самых ранних этапах развития зародыша, в период с 4-ой по 7-ую неделю беременности. Именно в это время осуществляется закладка и построение основных структур сердца и сосудов будущего ребенка. Наиболее важным моментом является пятая неделя беременности , ответственная за процессы разделения различных структур и отделов сердца. В это время осуществляется интенсивное формирование межжелудочковой и межпредсердной перегородок (стенок, разделяющих правые и левые отделы сердца), разделение артериального ствола на аорту и легочную артерию (главные артерии организма), разделение правого и левого предсердно-желудочковых клапанов. В результате образуется нормальное сердце, в котором правое предсердие через правый предсердно-желудочковый клапан сообщается с правым желудочком, от которого отходит легочная артерия, доставляющая кровь в легкие.
Обогащенная кислородом кровь из легких попадает в левое предсердие, которое через левый предсердно-желудочковый клапан сообщается с левым желудочком. Из левого желудочка выходит аорта, несущая артериальную кровь ко всем органам и системам организма.
На сроке в 6-7 недель, в уже практически “готовом” сердце заканчивается построение межжелудочковой перегородки, разделяющей правый и левый желудочек сердца. Если в эти сроки, по какой-либо причине, происходит сбой в любом из перечисленных механизмов нормального развития сердца, это приводит к формированию определенного дефекта структуры сердца — врожденного порока. Поэтому любые вредные воздействия, такие как употребление алкоголя, наркотиков, курение, прием антибиотиков, перенесенные инфекции (даже такие как банальный грипп и ОРВИ) являются чрезвычайно опасными именно в первые 10 недель беременности.
Читайте также:
