Освобождение макрофагов в легких. Двойные инфекции легких
Добавил пользователь Morpheus Обновлено: 08.01.2026
Эмфизема легких (происходит от греч. «вздутие») — патологическое состояние, которое характеризуется расширением воздушных пространств дистальнее конечных бронхиол и сопровождается деструктивными изменениями стенок альвеол. Эмфизема легких является составляющей хронической обструктивной болезни легких (ХОБЛ).
Эпидемиология
Среди населения больные с проявлениями эмфиземы легких составляют 4% и более. С возрастом процент больных становится всё больше. Чаще всего она беспокоит лиц в возрасте от 60 лет.
Классификация
Эмфизему легких делят на виды по патогенезу и по месту нахождения поражения в дыхательных путях. Анатомическая классификация предлагает такие виды:
- панацинарная
- буллезная
- проксимальная ацинарная
- иррегулярная
- дистальная ацинарная
По патогенезу рассматриваемое заболевание делится на две формы: первичную и вторичную. Первичная является врожденной, а вторичная возникает как следствие хронических болезней легких.
Причины
Любая причина, которая приводит к хроническому воспалению альвеол, влияет на эмфизематозные изменения, особенно есть отмечается недостаточность антипротеолитических факторов. Курение вызывает протекающее вяло воспаление в дыхательных путях. Потому из лейкоцитов постоянно или рецидивирующе высвобождаются протеолитические ферменты. Вторичная эмфизема бывает у пациентов с ХОБЛ, что говорит о тяжелом течении заболевания.
Факторы риска эмфиземы легких:
- поллютанты окружающей среды
- профессиональные вредные факторы
- длительный прием некоторых лекарственных препаратов
- болезни дыхательных путей инфекционной природы
Недостаточность альфа-антитрипсина — генетический фактор, предрасполагающий к развитию эмфиземы. Из-за этого повышается чувствительность легочной ткани к аутолизу собственными протеазами. Курение приводит к более быстрому развитию процесса.
Патогенез
Ключевым моментом патогенеза является разрушение волокон легочной ткани, причиной которого является дисбаланс в системах «протеолиз-антипротеолиз». Некоторые исследователи считают, что дисфункция фибробластов также имеет значение. При недостаточности альфа-антитрипсина возрастает активность эластазы нейтрофилов, которая расщепляет коллаген и эластин, из-за чего происходит разрушение респираторной ткани.
Разрушение альвеолярных стенок и поддерживающих структур приводит к тому, что образуются сильно расширенные воздушные пространство. Исследователи считают, что отсутствие тканевого каркаса нижних дыхательных путей приводит к их сужению вследствие динамического спадения во время выдоха на уровне малых легочных объемов. Также разрушение альвеолярно-капиллярной мембраны снижает диффузионную способность легких за счет уменьшения площади дыхательной поверхности.
Патоморфология
Эмфизема легких является деструктивным процессом эластического остова легочной ткани, как уже было отмечено выше. При проксимальной ацинарной эмфиземе бронхиола имеет размеры, превышающие норму, а также нарушена ее целостность. Проксимальная ацинарная эмфизема делится условно на центрилобулярную и эмфизему при пневмокониозе шахтеров. При первой форме происходят изменения в респираторной бронхиоле проксимальней ацинуса. Эта форма эмфиземы отмечается в основном в верхних долях легких. При пневмокониозе шахтеров фокальные эмфизематозные участки чередуются с интерстициальным фиброзом легких.
При панацинарной эмфиземе, которая также известна как генерализованная, происходит единообразный характер изменений с вовлечением в процесс ацинуса. Изначально патологический процесс затрагивает альвеолярные ходы и мешочки. Позже между ними пропадают границы. Эта эмфизема локализируется в основном нижних долях легких. Течение болезни тяжелое.
При дистальной ацинарной форме эмфиземы процесс затрагивает альвеолярные ходы. Иррегулярная форма характеризуется многообразием увеличения ацинусов и их разрушением, при этом в легочной ткани выражен рубцовый процесс. Такая форма эмфиземы бывает при таких заболеваниях:
Буллезная эмфизема отмечается формированием эмфизематозных участков легкого размером от 1 сантиметра. Чаще всего заболевание врожденное, проходит со спонтанным пневмотораксом.
Симптомы и диагностика
Симптоматика становится всё более выраженным по мере прогрессирования болезни. Со временем прогрессирует одышка. Чаще всего она проявляется в возрасте больного от 50 лет. Усиливается она, когда присоединяются респираторные инфекции. Мокрота при кашле слизистая, в небольшом количестве, потому что при эмфиземе не происходит бактериальный воспалительный процесс.
Обычно больной теряет вес, потому что у него активизируется напряженная работа дыхательных мышц. В анамнезе отмечается в большинстве случаев табакокурение, хронические или возобновляющиеся болезни органов дыхания, профессиональные вредности. У нескольких поколений прямых родственников могут отмечаться разные болезни дыхательных органов, что у медиков называется семейной слабостью легких. При буллезной эмфиземе фиксируют рецидивирующие спонтанные пневмотораксы.
Физическое обследование
При осмотре медики отмечают, что грудная клетка имеет цилиндрическую форму. Ее подвижность при дыхательных движениях ограничены. Вспомогательная мускулатура активно задействована при дыхании. Перкуторный звук над всей поверхностью грудной клетки имеет коробочный оттенок. Нижние границы легких смещены книзу на 1-2 ребра, их подвижность ограничена.
Аускультация выявляет ослабление дыхания, хрипы появляются при сопутствующем хроническом бронхите во время кашлевой пробы, аускультации в положении человека лежа, форсированного выдоха. Тоны сердца лучше выслушиваются в надчревной области.
Инструментальные исследования
Рентгенологическое исследование обнаруживает, что подвижность диафрагмы ограничена. Фиксируют повышенную воздушность легочных полей. Купол диафрагмы расположен низко и уплощен. В легочных полях мало сосудистых теней. Усиление легочного рисунка можно обнаружить при буллезной эмфиземе. С помощью рентгенографии можно обнаруживать характерное осложнение буллезной формы эмфиземы — спонтанный пневмоторакс.
С помощью компьютерной томографии подтверждают обеднение сосудистого рисунка легочных полей, повышенную воздушность легких. Также метод актуален для определение наличия, места нахождения и размеров булл. В начале болезни можно обнаружить, что размер легких выше нормы. При тяжелом течении болезни уменьшается поверхность легких. Исследование дает врачам возможность неинвазивно определять массу и объем легких.
Исследование ФВД — высокоинформативный диагностический метод при подозрении на эмфизему легких. По кривой «поток-объем» на ранних стадиях выявляют обструкцию дистального отрезка дыхательного дерева. При эмфиземе не может быть обратимой обструкции.
Лабораторные исследования
Общий анализ крови при эмфиземе легких не покажет воспалительных изменений. Они могут быть, только при наличии у человека вместе с эмфиземой и другого заболевания. Для выраженной эмфиземе типична прогрессирующая гипоксемия, которая приводит к полицитемическому синдрому: в крови возрастает содержание эритроцитов и гемоглобина, увеличивается вязкость крови.
Осложнения
Осложнениями являются развитие и прогрессирование необратимой дыхательной, легочной и сердечной недостаточности. Эмфизема легких может вызвать такое неотложное состояние как спонтанный пневмоторакс, особенно клапанный, при котором нарастает давление внутри груди.
Дифференциальная диагностика
Вторичная эмфизема нуждается в дифференциальной диагностике с первичной и с формами заболевания, которые обусловлены расширением воздушных пространств легких без вовлечения сосудистого русла. Вторичная форма может быть, например, при хроническом обструктивном бронхите или бронхиальной астме.
Первичная эмфизема обнаруживается у пациентов молодого и среднего возраста, часто ее могут найти у 2 и более родственников. Подтверждают диагноз, находя в сыворотке крови низкую концентрацию альфа-антитрипсина. При вторичной эмфиземе могут проявляться симптомы другой болезни, которая затронула нижние дыхательные пути.
Инволютивная форма эмфиземы обусловлена расширением воздушных пространств легких (как и гипертрофическая и инволютивная). При ней не отмечается гипоксия, бронхообструктивный синдром, гиперкапния. При гипертрофической форме, которая известна также как компенсаторная или викарная, объем оставшегося легкого увеличивается, что говорит о процессе компенсации. Острое вздутие легких — обратимая реакции компенсации при аспирации инородного тела с неполной обструкцией бронхов, тяжелом приступе бронхиальной астмы, утоплении, иногда при резких физических перегрузках.
Лечение эмфиземы легких
Мер специфического лечения данного заболевания на сегодня не существуют. Актуальны терапевтические программы, как и при всех ХОБЛ. Нужно устранить факторы, которые вызвали развитие эмфиземы. Это может быть инфекционный процесс хронического характера в дыхательных путях, действие грязного воздуха, курение и пр.
Медикаментозное лечение включает прием средств для расширения бронхов:
- или фенотерол
- М-холиноблокаторы
- формотерол или салметерол
- комбинация выше названных препаратов
- препараты теофиллина пролонгированного действия
Людям в возрасте лучше назначать м-холиноблокаторы. Теофиллины для них почти никогда не актуальны.
Глюкокортикоиды эффективны при тяжелом течении эмфиземы легких. Назначается преднизолон короткими курсами преднизолона до 20-30 мг внутрь с быстрым снижением дозы и отменой препарата на протяжении 7-12 дней. Необходим контроль эффективности терапии по кривой «поток-объем». Если эффекта не достигают, то ГК больше давать пациенту не нужно. При положительном действии системных ГК лучше всего продолжать применять ингаляционные лекарства. Например, эффективен будесонидом по 400-500 мкг 2 раза в сутки.
Заместительная терапия человеческим альфа-1-антитрипсином может дать нужный эффект, особенно при генетической предрасположенности к рассматриваемому заболеванию. Но в клиническую практику на сегодня не внедрен ни один из препаратов этого ряда.
Ацетилцистеин оказывает антиоксидантное действие. Внутрь назначают по 600 мг, прием 1 раз в сутки перед сном.
Хирургическое лечение заключается в уменьшении объема легких. Проводится буллэктомия, лучше всего — торакоскопическая. Делают резекцию периферических участков легких, потому остальные участки декомпрессируются. Функциональное состояние легких улучшается. Медики также пытаются внедрить метод трансплантации легких, в том числе в странах СНГ. При развитии спонтанного пневмоторакса применяют дренирование плевральной полости и аспирация воздуха.
Прогноз
Прогноз эмфиземы легких зависит от степени снижения жизненной емкости легких и бронхиальной проходимости, от возможности и скорости устранения факторов риска, от течения основной болезни (если речь идет о вторичной эмфиземе). Если пациент не пожилого возраста, и у него нет нехватки альфа-антитрипсина и ОФВ1 более 50%, прогноз благоприятный.
Профилактика
Важное профилактическое значение имеют антитабачные программы, направленные на предупреждения курения детей и подростков, а также на прекращение курение лиц любого возраста. Также нужно вовремя лечить болезни легких, чтобы они не переходили в хроническую форму. Имеет значение наблюдение у пульмонолога больных с хроническими заболеваниями органов дыхания, проведение вакцин среди населения и пр.
Роль макрофагов и цитокинов в формировании воспаления и прогрессировании хронической обструктивной болезни легких
Цель обзора. Рассмотреть некоторые приоритетные патогенетические механизмы формирования хронической обструктивной болезни легких.
Основные положения. Продемонстрировать приоритетное действие цитокинов в очаге воспаления и на территории реагирующих лимфоидных органов, а также связь реализации неспецифических и специфических иммунных реакций при хронической обструктивной болезни легких (ХОБЛ) с влиянием на различные гомеостатические системы организма целого ряда универсальных медиаторов, среди которых особое место занимает цитокиновая сеть, контролирующая процессы реализации иммунной и воспалительной реактивности.
Заключение. Изучение хронического альвеолярного/бронхиального воспаления является ключевым фактором в развитии теории патогенеза многих легочных патологий.
Хроническая обструктивная болезнь легких (ХОБЛ) - одна из важнейших проблем современного здравоохранения, причем это характерно практически для всех стран в связи с постоянно возрастающей распространенностью и смертностью от этого заболевания. ХОБЛ является единственной болезнью, от которой смертность продолжает увеличиваться. По данным исследования, проведенного Всемирной организацией здравоохранения и Мировым банком, к 2020 г. ХОБЛ будет занимать 5-е место по заболеваемости и 3-е место в структуре смертности среди всех болезней.
Известно, что острое или хроническое альвеолярное/бронхиальное воспаление является ключевым фактором в развитии патогенеза многих легочных патологий, таких как бронхиальная астма, ХОБЛ, респираторный дистресс-синдром взрослых, идиопатический фиброз легких. Локализация и специфические особенности воспалительного ответа могут быть различными для каждого из этих заболеваний, однако, для всех них характерно привлечение в легочную ткань и активация воспалительных клеток. Эти активированные клетки могут продуцировать цитокины, оксиданты и многие другие медиаторы, которые вовлечены в воспаление 3.
Основу патогенеза ХОБЛ составляет хроническое, диффузное, неаллергическое воспалительное поражение дыхательных путей, которое проходит с участием нейтрофилов, с повышенной активностью миелоперексидазы, нейтрофильной эластазы, металлопротеиназ. Воспалительная реакция связана с нейтрофильной инфильтрацией в очаге воспаления при повышенной активности интерлейкинов-6 и -8 и фактора некроза опухоли-альфа (TNF-альфа) 7. Процесс воспаления имеет многофакторную природу и представляет собой сложную систему взаимодействия клеток воспаления, продуцируемых ими цитокинов и факторов роста, а также активации рецепторного ответа каждой группы клеток, вовлеченных в воспалительный процесс. Повышение симпатической активности у больных ХОБЛ способствует активации ренин-ангиотензин-альдостероновой системы (РААС) и других нейрогормонов и медиаторов (цитокинов, эндотелинов, вазопрессина и др.).
Цитокины - это гормоноподобные белки, вырабатываемые различными клетками (лимфоцитами, моноцитами, гранулоцитами, мастоцитами, эндотелиоцитами, фибробластами, и др. клетками), обладающие широким спектром биологической активности, осуществляющие межклеточные взаимодействия при гемопоэзе, иммунном и воспалительном ответах, межсистемных взаимодействиях 15.
Цитокины традиционно делят на интерлейкины (Ил-1 - ИЛ-15), факторы некроза опухоли (TNF-альфа и -бетта), фактор, ингибирующий миграцию, интерфероны, хемотаксические факторы, ростовые факторы (фактор роста фибробластов, трансформирующий фактор роста - ТФР-бетта, эпителиалные и эндотелиальные факторы роста и т.д.) [7,8,19,20].
Основная часть провоспалительных цитокинов продуцируется нейтрофилами, активированными лимфоцитами, эндотелитальными и гладкомышечными клетками. В норме провоспалительные цитокины не должны находится в циркуляции, однако в ряде случаев они могут появляться, являсь проявлением вялотекущих скрытых воспалительных процессов, а также иммунопатологических состояний. ФНО-aльфа обладает широким спектром эффектов. Благодаря ФНО-опосредованной индукции генов факторов роста, цитокинов, факторов транскрипции, рецепторов, медиаторов и белков острой фазы воспаления, пирогенов, он вовлечен в индукцию кахексии. Существуют экспериментальные подтверждения того, что активация системы цитокинов, главным образом продукция ФНОальфа, связана с высокой активностью САС, РААС и состоянием хронической гипоксии [13]. Повышенная активность нейрогуморальной системы стимулирует выработку цитокинов, обладающих провоспалительным действием, что определяет развитие патологических изменений. Ведущая роль в патогенезе воспаления при ХОБЛ отведена нейтрофилам. Как показывают уже существующие данные, в регуляции апоптоза нейтрофилов крайне важно соблюдение баланса между провоспалительными и противовоспалительными цитокинами, который обеспечивает своевременное устранение “излишних” гранулоцитов после исполнения их функции в очаге воспаления. Если же происходит торможение апоптоза нейтрофилов, то появляется риск развития персистенции воспаления окружающих тканей, так как нейтрофилы крайне агрессивно вырабатывают цитокины воспаления, что наблюдается у больных с гнойно-септическими заболеваниями при исследованиях различных маркеров апоптоза в бронхо-альвеолярном лаваже, при биопсии в слизистой бронхов и в крови [5,9,15,21].
В развитии и функционировании нейтрофилов можно выделить три стадии, когда наблюдаются наиболее существенные различия по готовности клеток к реализации процесса апоптоза: 1) созревание в костном мозге; 2) пребывание в циркуляции; 3) нахождение в тканях, в том числе сюда необходимо отнести и экссудативные нейтрофилы (саливарные, перитонеальные, раневые, интраназальные, вагинальные, бронхоальвеолярные) [22,23].
Таким образом, активация системы цитокинов у больных ХОБЛ является маркером прогрессирования заболевания с вовлечением в патогенез все новых и новых составляющих, включая нейрогуморальную систему организма человека, приводящую к появлению и прогрессированию ЛГ, что требует особой фармакотерапевтической тактики в ведении этих больных [6].
При исследовании нейтрофилов у больных с тяжелыми гнойно-септическими заболеваниями обнаружен интересный факт - наличие высокого процента нейтрофилов (по сравнению со здоровыми людьми) с выраженной экспрессией CD95 (АРО-1, Fas) на мембранах клеток, что означало высокую готовность клеток к реализации апоптоза. Однако, при этом обнаружено торможение гибели нейтрофилов по времени (по сравнению с нейтрофилами, CD95-экспрессированными у здоровых людей), что означает наличие несостоятельности иммунитета у больных с тяжелыми гнойно-септическими заболеваниями в связи с дисбалансом между проапоптическими и антиапоптическими цитокинами.
Известно, что уровень некоторых циркулирующих в крови цитокинов и острофазных белков у пациентов ХОБЛ выше нормы. Пока не исследовалось, как базисная терапия ХОБЛ влияет на их динамику. Задачей исследования Malo O., Sauleda J. и др.[9,17,23] было описание изменений, происходящих в системе взаимодействия некоторых провоспалительных цитокинов, циркулирующих в крови во время обострения заболевания у больных ХОБЛ тяжелого течения и оценка потенциального эффекта проводимой кортикостероидной терапии. Исследователи определяли уровень TNF-альфа, ИЛ-6 и ИЛ-8 сыворотки крови и СРБ у 10 больных с ХОБЛ тяжелого течения в первые 24 ч. госпитализации по поводу внезапно нараставшей дыхательной недостаточности; повтороное лабораторное исследование проводили при выписке больного и спустя 2 месяца. Была набрана контрольная группа из 8 здоровых человек того же возраста [24]. По результатам исследования уровень сывороточного ИЛ-6 были значительно выше у пациентов с ХОБЛ по сравнению с группой контроля, а уровни ИЛ-8 в сыворотке крови в группе контроля и у больных ХОБЛ были похожими. Не было статистически значимого изменения исследованных показателей ни во время улучшения течения заболевания (несмотря на кортикостероидную терапию), ни спустя 2 месяца. Таким образом, полученные результаты продемонстрировали наличие системного воспаления во время обострения ХОБЛ, которое практически не изменилось даже под действием внутривенного введения кортикостероидов [23]. Определение TNF-альфа методом тест-системы ELISA является мало чувствительным, и не рекомендуется применять для подобного исследования.
Интересное исследование проведено группой испанских ученых - M.Miravitlles и соавт. [17], целью которого было определение роли повышенного уровня сывороточного ИЛ-6 или его растворимого рецептора (sRIl-6) в активации системы воспаления у больных с дефицитом альфа1-антитрипсин Обследованы 7 человек с дефицитом альфа1-антитрипсина и 23 человека с диагнозом ХОБЛ с такой же степенью обструкции по данным ФВД (ОФВ1 35.5-38.3%). Пациенты обеих групп были сопоставимы во возрасту (51-63 года). При сравнении показателей сывороточного ИЛ-6 и его растворимого рецептора в этих двух группах оказалось, что у больных с дефицитом альфа1-антитрипсина уровни ИЛ-6 сыворотки и растворимого рецептора ИЛ-6 в среднем составляли 4.7 pg/ml и 129.1 ng/ml соответственно, а у больных ХОБЛ с нормальным значением альфа-1-антитрипсина уровни ИЛ-6 и sRIl-6 - 4.1 pg/ml и sRIl-6 140.8 ng/ml соответственно. И только у одного больного с дефицитом альфа1-антитрипсина уровень ИЛ-6 был выше нормы. Таким образом, были обнаружены статистически не значимые различия значений уровня ИЛ-6 и рецептора ИЛ-6 сыворотки крови в обеих группах пациентов, что означает отсутствие разницы между этими показателями. Однако, динамическое исследование этих цитокинов на фоне терапии не проводилось [7-9,21,25].
В настоящее время альвеолярный макрофаг считается централь¬ной клеткой воспаления и регулятором сложных межклеточных взаимодействий. В результате активации альвеолярных макрофагов происходит скопление лимфоцитов, фибробластов, моноцитов, а также значи¬тельно активируются Т-лимфоциты. Активированные Т-лимфоциты выделяют интерлейкин-2, под влиянием которого Т-эффекторные лимфоциты активируются и продуцируют ряд лимфокинов. Наряду с этим Т-лимфоциты, как и альвеолярные макрофаги, вырабаты¬вают ряд веществ, стимулирующих пролиферацию фибробластов и, следовательно, развитие фиброза.
Альвеолярные макрофаги гиперпродуцируют ряд биологически активных веществ, в том числе интерлейкин-1, который стимулирует Т-лимфоциты и привлекает их в очаг воспаления, т.е. интерстициальную ткань легких и альвеолы [26].
Роль макрофагов в иммунитете исключительно важна - они обеспечивают фагоцитоз, переработку и представление антигена Т-клеткам, секретируют лизоцим, нейтральные протеазы, кислые гидролазы, аргиназу, многие компоненты комплемента, ингибиторы ферментов (антиактиватор плазминогена, альфа2-макроглобулин), транспортные белки (трансферрин, фибронектин, трансбаламин II), нуклеозиды и цитокины (ФНО альфа, ИЛ-1 ,ИЛ-8, ИЛ-12). ИЛ-1 выполняет много важных функций: воздействуя на гипоталамус, вызывает лихорадку; стимулирует выход нейтрофилов из костного мозга; активирует лимфоциты и нейтрофилы. Макрофаги являются одним из орудий врожденного иммунитета. Кроме того макрофаги, наряду с В- и Т-лимфоцитами, участвуют и в приобретенном иммунном ответе, являясь «дополнительным» типом клеток иммунного ответа: макрофаги являются фагоцитирующими клетками, чья функция - «проглатывание» иммуногенов и процессирование их для представления Т-лимфоцитами в форме, пригодной для иммунного ответа [27].
Т-лимфоциты распознают инфицированный макрофаг по экспонированию на его поверхности микробного антигена, находящегося в комплексе с гликопротеином МНС класса II, который в данном случае служит сигналом макрофага. В результате распознавания Т-клетки выделяют лимфокины, стимулирующие внутриклеточное уничтожение возбудителя макрофагом.
Таким образом, терапия, направленная на коррекцию моноцитарно-макрофагальной системы, является приоритетной у больных, имеющих воспалительную природу заболевания, на всех этапах воспалительного процесса и независимо от его локализации, как в бронхолегочной системе, так и в других.
Оценку прогрессирования хронической обструктивной болезнь легких необходимо проводить, сравнивая клинические показатели состояния пациента с показателями функции внешнего дыхания и с биомаркерами воспаления как специфическими, так и неспецифическими, так как прогрессирование заболевания у данной группы больных обусловлено особенностями процессов ремоделирования стенок бронхов [28]. Для оценки возможности влияния медикаментозной терапии на замедление прогрессирования заболевания важно изучить динамику уровня провоспалительных цитокинов [5,19].
Известно, что коварство ХОБЛ заключается в медленном, но неуклонном прогрессировании. Выраженная клиническая симптоматика появляется лишь в развернутой стадии болезни (2 стадия). На ранних стадиях ХОБЛ протекает скрыто, без постоянных клинических симптомов.
Совершенствование наших представлений о сущности заболевания - патогенеза ХОБЛ - является важнейшим инструментом, влияющим на основные подходы к классификации ХОБЛ, лечнению и профилактике заболевания.
С ХОБЛ нужно и можно бороться. Существуют лечебные мероприятия, способные уменьшить симптомы болезни, замедлить ее прогрессирование и улучшить качество жизни пациентов.
Саркоидоз легких
Саркоидоз — это системное доброкачественное заболевание, при котором в органах образуется множество воспалительных очагов. Точная причина болезни пока не установлена, но врачи говорят о наследственных предрасполагающих факторах и влиянии экологии на здоровье. Саркоидоз легких распространен больше других видов патологии, и чаще всего у пациентов с этим диагнозом прогноз благоприятный. Основная же опасность болезни — выраженная дыхательная недостаточность. В этом материале рассказываем о том, как правильно лечить саркоидоз легких и не допустить возможных осложнений.
Определение болезни
Саркоидоз относят к числу интерстициальных заболеваний легких. Интерстиций — это соединительная ткань внутри легкого, которая образует стенки альвеол, перегородки и другие его структуры. При саркоидозе легких происходит патологическое скопление в тканях иммунных клеток — фагоцитов и лимфоцитов. В дальнейшем это приводит к образованию воспалительных узелков, которые называют гранулемами. Поэтому саркоидоз еще называют доброкачественным гранулематозом. Причина болезни непонятна, но исследования показывают, что саркоидоз можно отнести к числу аутоиммунных заболеваний. Это заболевания, при которых иммунитет атакует собственные клетки организма.
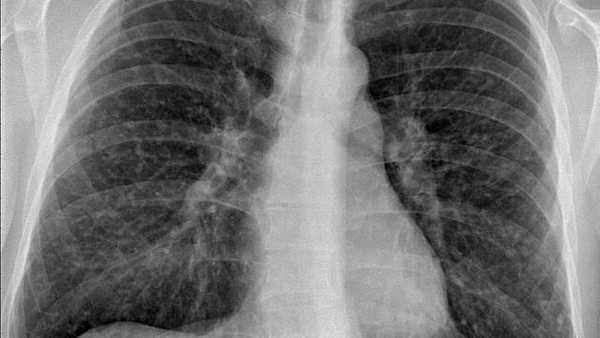
Белые пятна на рентгеновском снимке — гранулемы. Источник: Mikael Häggström / Wikipedia (CC0)
Опасность саркоидоза легких заключается в том, что гранулемы могут расти и сливаться, образуя обширные воспалительные очаги. Затем они рассасываются, но оставляют после себя не функциональную рубцовую ткань. Таким образом, уменьшается количество легочной ткани, в которой происходит газообмен. Функция легких ухудшается, что приводит к нарушению работы всего организма, ведь в кровь поступает недостаточно кислорода (который необходим всем тканям и органам).
Поскольку болезнь носит системный характер, то поражаться могут не только легкие, но и другие органы. В частности, это печень, лимфатические узлы и селезенка. В редких случаях саркоидоз затрагивает кожу, кости и органы зрения.
Заболевание встречается во всех странах, но больше всего саркоидозом легких страдают жители северных широт (60 случаев на 100 тыс. населения). Чем ближе к экватору, тем реже встречается эта болезнь. Основная категория больных — люди в возрасте 20-40 лет, а также женщины старше 50 лет¹˒².
Женщины саркоидозом болеют чаще мужчин. Кроме того, у заболевания имеются и расовые особенности. Многолетние наблюдения в США показывают, что среди темнокожих саркоидоз легких встречается в 2,5-5 раз чаще, чем у светлокожих.
Может ли саркоидоз переродиться в рак легких?
Нет, поскольку изначально эта болезнь является доброкачественной. Вероятность развития злокачественного процесса при саркоидозе такая же, как и при любых других воспалительных заболеваниях (если рассматривать воспаление в качестве фактора озлокачествления). Но это вовсе не значит, что саркоидоз не опасен. Если болезнь не лечить, то существенно возрастает риск развития дыхательной недостаточности. Это тяжелое осложнение, которое в дальнейшем затрагивает почти все органы, поскольку организм при этом недополучает кислород.
Симптомы саркоидоза легких
Саркоидоз органов дыхания может протекать в хронической и острой форме. Симптоматика первого часто малозаметна или вовсе отсутствует. Почти у половины больных с хронической формой саркоидоза заболевание выявляют случайно при очередном флюорографическом обследовании. У других пациентов симптомы незначительные, нарастают постепенно. Возможно появление таких неспецифических признаков неблагополучия, как повышенная утомляемость, слабость и потливость. В некоторых случаях пациентов беспокоит малопродуктивный кашель. Если появилась одышка при незначительных физических нагрузках, это указывает на прогрессирование болезни.
Связь между стадией болезни и симптомами
Примечательно, что для саркоидоза нет четкой взаимосвязи между количеством образовавшихся в легких гранулем и выраженностью симптомов. Например, больше половины больных саркоидозом не страдают одышкой, несмотря на серьезные поражения легких. При этом, если у пациента есть одышка (связанная с саркоидозом), то это почти всегда далеко зашедшая стадия.
Что касается острых форм заболевания, то для них характерна более выраженная симптоматика. Кроме увеличения лимфоузлов, пациентов также беспокоят:
- высокая температура тела;
- боли в суставах и костях;
- узловатая эритема — воспалительное поражение мелких сосудов кожи и подкожной клетчатки;
- увеличение периферических лимфатических сосудов;
- сухой кашель;
- боли в грудной клетке;
- потеря веса.
Несмотря на «бурное» начало, острые формы в большинстве случаев проходят спонтанно, сами собой.
Саркоидоз легких может сочетаться и с поражением болезнью других органов. Поэтому у пациентов могут возникать внелегочные симптомы. Например, увеличение печени, селезенки, поражения кожи, глаз и сердца. Очень редко саркоидоз затрагивает почки, щитовидную железу, органы пищеварения, костный мозг или нервную систему. Поэтому саркоидоз легких — это повод для обследования всего организма.
Лечение саркоидоза легких
Поскольку саркоидоз часто проходит самостоятельно, то при бессимптомном его течении рекомендуют выжидательную тактику³. В этом случае пациенту нужны регулярные осмотры у врача (периодичность осмотров определяет специалист). Это и регулярные рентгенологические исследования грудной клетки, и исследование других органов, которые могут быть затронуты саркоидозом.
Лечение при саркоидозе оправдано в случаях активного, тяжелого или прогрессирующего течения заболевания. Основой терапии являются глюкокортикоиды. Это гормональные противовоспалительные препараты — аналоги стероидных гормонов, продуцируемых корой надпочечников.
Из системных глюкокортикоидов при саркоидозе легких, как правило, применяют преднизолон или метпреднизолон. Последний обладает более выраженной противовоспалительной активностью.
В большинстве случаев преднизолон назначается в дозировке 20-40 мг в сутки. Терапевтический ответ обычно наступает спустя 6-12 недель. Именно в этом временном промежутке врач оценивает функцию легких и динамику выздоровления. Если положительный эффект от преднизолона присутствует, дозировку постепенно снижают до поддерживающей терапии — 10-15 мг в сутки на протяжении 6-9 месяцев.
Почему глюкокортикоиды нельзя резко отменять
По завершении лечебного курса важно четко придерживаться прописанной врачом схемы отмены преднизолона и других глюкокортикоидов. Такие лекарства нельзя отменять одномоментно. Во-первых, резкая отмена может спровоцировать появление симптомов надпочечниковой недостаточности, когда в организме неожиданно снижается концентрация стероидных гормонов. Во-вторых, в случае с саркоидозом резкое (преждевременное) прекращение приема препарата в дальнейшем может привести к рецидиву заболевания.
В некоторых случаях глюкокортикоиды совмещают с нестероидными противовоспалительными препаратами — индометацином, аспирином и другими.
Помимо глюкокортикоидов в лечении саркоидоза также используются цитостатические препараты (метотрексат, циклофосфамид), иммунодепрессанты (азатиоприн, микофенолата мофетил), ингибиторы фактора некроза опухолей, витамины, гидроксихлорохин и другие.
Схема лечения и подбор соответствующих лекарств определяется врачом. Дополнительные медикаменты (кроме глюкокортикоидов) назначаются при отсутствии желаемого эффекта от стероидов.
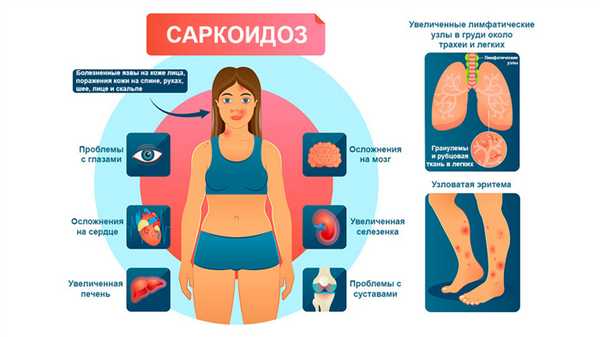
Рисунок 1. Саркоидоз часто наносит удар не только по легким. Внелегочные симптомы говорят о том, что от саркоидоза страдает весь организм. Источник: VectorMine / Depositphotos
Что учитывают при лечении саркоидоза
При лечении саркоидоза легких обязательно учитывается состояние других органов и систем, в частности, сердца и сосудов. Некоторые пациенты нуждаются в установке кардиостимулятора из-за нарушения внутрисердечной проводимости.
Легочная артериальная гипертензия — одно из осложнений, возникающих на фоне саркоидоза. В данном случае пациент нуждается в приеме диуретических препаратов и оксигенотерапии. А вот применение вазодилататоров (сосудорасширяющих препаратов) при легочной артериальной гипертензии малоэффективно⁴.
Лекарства, которые предотвращают развитие фиброза легких, пока не разработаны. Тяжелые поражения с терминальными стадиями легочной недостаточности нуждаются в проведении трансплантации легких. Это относится и к другим органам, которые затрагиваются болезнью (например, печень или сердце). При этом нужно учитывать, что саркоидоз может рецидивировать и в пересаженном органе.
Реабилитация и диспансерное наблюдение
Стандартизированной схемы реабилитации больных с саркоидозом легких не существует. Однако есть отдельные исследования, в которых отмечался положительный эффект от:
- сбалансированного питания (ограничения в питании устанавливаются в индивидуальном порядке, в зависимости от состояния здоровья пациента);
- физических нагрузок (рекомендуется сохранять максимально возможную физическую активность);
- респираторной физиотерапии и дыхательных упражнений;
- психотерапии и усиления мотивации пациента вести здоровый образ жизни⁵.
Поскольку саркоидоз в любой момент может рецидивировать, крайне важно диспансерное наблюдение. В каждом отдельном случае оно подбирается индивидуально. Врач учитывает как особенности течения заболевания, так и объем поражений легких и наличие осложнений.
Пациенты, у которых болезнь выявлена впервые, в течение первого года (а также больше года при условии сохранения активного процесса) должны наблюдаться у пульмонолога каждые 3 месяца. При стабилизации патологического процесса на 2-м году осматриваться у врача нужно каждые 6 месяцев. В последующие годы приходить на осмотр необходимо минимум 1 раз в год.
Если болезнь прогрессирует или произошел рецидив, следует вернуться к первой схеме наблюдения — каждые 3 месяца, но на протяжении 2-х лет.
Осложнения саркоидоза легких
Саркоидоз легких — опасное заболевание, которое чревато следующими осложнениями:
- Эмфизема — патологическое расширение альвеол легких и деструктивное изменение их стенок.
- Бронхообтурационный синдром — симптомокомплекс, при котором нарушается проходимость бронхов. Характеризуется отеком легких и появлением бронхоспазмов.
- Дыхательная недостаточность — снижение функций легких за счет замещение легочной ткани рубцовой.
- Легочное сердце — патологическое состояние, при котором увеличивается правый желудочек сердца. Развивается на фоне артериальной легочной гипертензии. В конечном итоге легочное сердце приводит к сердечной недостаточности.
- Присоединение легочных инфекций — грибковых (аспергиллез) или бактериальных (например, туберкулез). Инфекционный процесс связан со сниженной сопротивляемостью легочных тканей инфекционным агентам на фоне саркоидоза.
- Диффузный интерстициальный пневмосклероз — замещение легочной ткани соединительной. По мере прогрессирования пневмосклероза снижается уровень газообмена в легких, что в конечном счете приводит к развитию дыхательной недостаточности.
Диагностика саркоидоза легких
При подозрении на саркоидоз проводятся как инструментальные, так и лабораторные исследования. Прежде всего это рентгенография легких, по которой определяют стадию заболевания. Для уточнения структуры легких и обнаружения других патологических изменений также проводится компьютерная и магнитно-резонансная томографии.
Поставить верный диагноз врачу помогает бронхоскопия с биопсией (забор небольшого фрагмента легочной ткани). Полученный таким образом биоптат отправляют в лабораторию для проведения микроскопического и гистологического анализа, чтобы выявить наличие гигантских эпителиоидных многоядерных клеток (из которых состоят гранулемы), а также признаков воспалительного и/или некротического поражения. Микроскопическое исследование биоптата позволяет дифференцировать саркоидоз легких от ряда других легочных патологий, в частности, рака легких, туберкулеза и других.
Саркоидоз и туберкулез
Гранулемы при саркоидозе напоминают таковые при туберкулезе. Единственное отличие — в саркоидной гранулеме нет казеозного некроза (омертвевшая ткань, напоминающая творожистую массу). Дифференцировать саркоидоз от туберкулеза также позволяют иммунологические и морфологические (микроскопические) исследования.
Анализы крови при саркоидозе показывают повышенный уровень СОЭ (скорость оседания эритроцитов) и лейкоцитоз (повышенный уровень лейкоцитов крови), что указывает на наличие выраженного воспалительного процесса в организме.
Диагностические мероприятия позволяют не только установить болезнь, но и ее стадию (подробнее см. в разделе «Классификация»), на основании чего пациенту составляют схему лечения.
Когда обратиться к врачу
Коварность данного заболевания в том, что часто оно протекает бессимптомно. Нередко саркоидоз выявляют в ходе профилактического осмотра у врача, что только подчеркивает важность проведения своевременных чек-апов. Острое начало заболевания с появлением ярких симптомов является поводом для скорейшего обращения к врачу.
Прогноз и профилактика
Саркоидоз легких — сравнительно доброкачественное заболевание, но предопределить исход его лечения достаточно сложно. Примерно у 30-40% пациентов болезнь спонтанно саморазрешается, другим нужны месяцы терапии. У 10-30% больных саркоидоз приводит к фиброзу легких. Иногда он также заканчивается выраженной дыхательной недостаточностью, что существенно ухудшает качество жизни больного.
Профилактика саркоидоза осложнена ввиду неопределенных причин заболевания. Так как некоторые исследования показывают, что фактором риска болезни выступают некоторые химикаты и неблагоприятная экологическая обстановка, считается, что предупредить болезнь можно, сократив воздействие на организм вредных веществ. В частности, это касается группы риска — людей с повышенной иммунной реактивностью.
Причины саркоидоза легких
Причины саркоидоза до сих пор неизвестны. В настоящее время рассматривается несколько гипотез происхождения этого заболевания. Считается, что болезнь развивается при стечении ряда обстоятельств — наследственной предрасположенности к аутоиммунным реакциям, негативного воздействия окружающей среды и наличия инфекционных агентов (грибков, микобактерий, вызывающих туберкулез, риккетсий и боррелий)⁶˒⁷.
Установлено, что вклад наследственного фактора зависит от расы. У 20% афроамериканцев, больных саркоидозом, есть прямые родственники с таким же диагнозом. А у европейцев этот показатель составляет всего 5%. Кроме того, для афроамериканцев достоверно известно, что чем сложнее протекает саркоидоз, тем выше вероятность развития данного заболевания у родственников больного.
Чем бы ни была вызвана болезнь, механизм ее развития всегда одинаков.
Патогенез заболевания
Болезнь относят к категории аутоиммунных, поскольку она связана с чрезмерной активацией защитных Т-клеток и макрофагов (фагоцитирующих иммунных клеток), выделяющих ряд провоспалительных веществ. Последние провоцируют образование воспалительных узелков (гранулем) в паренхиме органов, в частности, легких.
При саркоидозе легких изначально поражаются ткани альвеол. Затем патологический процесс перерастает в пневмонит или альвеолит с образованием гранулем. Последняя в дальнейшем либо рассасывается, либо обрастает соединительной тканью (фиброз).
Сама по себе гранулема представляет скопление иммунных клеток (мононуклеаров и макрофагов), которые дифференцируются в эпителиоидные гигантские многоядерные клетки. Степень и глубина поражения легких, количество и локализация гранулем при саркоидозе может сильно разниться.
Выделяют несколько параметров, по которым классифицируют саркоидоз легких. Один из основных — локализация воспалительного процесса. По этому критерию выделяют следующие виды саркоидозов:
- внутригрудных лимфатических узлов;
- легких и внутригрудных лимфоузлов;
- лимфатических узлов;
- саркоидоз легких;
- саркоидоз органов дыхания с поражением других органов;
- генерализованный саркоидоз, при котором наблюдается множественное поражение органов.
Как правило, саркоидоз протекает в несколько фаз:
- Активная фаза — период обострения или нарастания симптомов;
- Фаза стабилизации — замедление или остановка развития патологического процесса.
- Фаза обратного развития — затухание патологического процесса. На этом этапе рассасываются гранулемы и уплотнения. В редких случаях в гранулемах откладываются соли кальция (кальцинация).
Стадии заболевания
На основании рентгенологической картины легких выделяют 5 стадий заболевания:
Двусторонняя пневмония
Двусторонняя пневмония - инфекционно-воспалительное поражение, протекающее сразу в обоих легких. В отличие от односторонней пневмонии, двустороннее воспаление протекает тяжелее и чаще приводит к осложнениям. Как протекает болезнь и каковы особенности лечения - подробности в тексте.
Особенности двусторонней пневмонии
Легкие - парный орган, главной задачей которого является дыхание. Этот процесс происходит в альвеолах легких, где осуществляется газообмен с легочными капиллярами. Таким образом, вдыхаемый кислород легко поступает в кровь, и одновременно углекислый газ перемещается из крови в альвеолы.
Функция дыхания заметно нарушается при воспалительных патологиях легких. Чаще всего пациенты сталкиваются с односторонним инфекционно-воспалительным поражением. Однако нередки и случаи двустороннего поражения легких. Данная проблема особенно актуальна в периоды вирусных эпидемий. В частности, это касается свиного гриппа (H1N1) и новой коронавирусной инфекции COVID-19. У всех пациентов со среднетяжелым, тяжелым и крайне тяжелым течением COVID-19 наблюдается именно двустороннее поражение легких.
Первая, основная особенность такого поражения, которое следует отметить - двусторонняя пневмония протекает тяжелее односторонней. Когда у пациента одно легкое здоровое, то оно вполне справляется со всеми нуждами организма по обеспечению кислородом органов и тканей. Как правило, уровень сатурации (обеспеченность тканей кислородом) при одностороннем поражении в норме, чего не наблюдается при двустороннем воспалении легких.
Как и одностороннее поражение легких, двусторонняя пневмония протекает в различных морфологических формах. Легче всего переносится очаговая пневмония, при которой размер пневмонической инфильтрации (скопления иммунных клеток и воспалительных элементов в легком) составляет не более 2 см. Также различают сегментарную (поражение в рамках одного сегмента легкого), полисегментарную (вовлечено несколько сегментов легких) и лобарную (поражена доля легкого). Как несложно догадаться, чем больше зона поражения, тем тяжелее протекает болезнь.
Двусторонние пневмонии особенно тяжело протекают у людей старше 65 лет, детей младше 5 лет, а также у людей с хроническими заболеваниями сердечно-сосудистой, дыхательной системы и сахарным диабетом.
И у взрослых, и у детей, тяжелее всего протекают двусторонние интерстициальные пневмонии. В данном случае воспаление затрагивает как альвеолы, так и периальвеолярные ткани. Таким образом, функция дыхания значительно ослабевает.
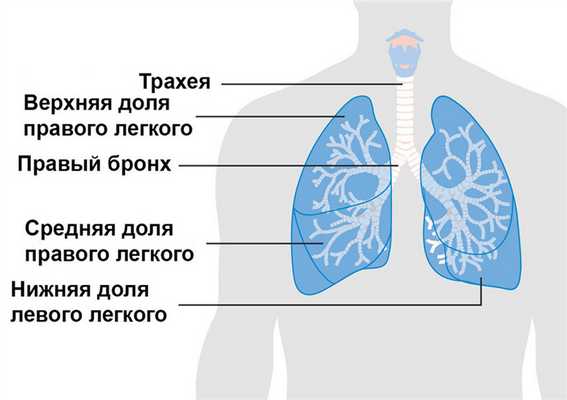
Рисунок 1. Основные органы дыхания. Источник: Cancer Research UK / Wikimedia Commons
Состояние больных с интерстициальной пневмонией быстро ухудшается, что приводит к дыхательной недостаточности и требует скорейшего медицинского вмешательства.
Важно! Двусторонняя пневмония и ИВЛ. Тяжелые пациенты с двусторонним поражением легких могут перевести на искусственную вентиляцию легких. К этой мере прибегают, когда все остальные методы не привели к желаемому результату. Многие ошибочно полагают, что аппараты ИВЛ - причина высокого уровня летальности среди пациентов, находящихся на искусственной вентиляции легких. Однако высокий уровень летальности, прежде всего, связан с тяжестью протекания заболевания. На ИВЛ переводят очень тяжелых больных с изначально высоким риском летального исхода. Вместе с тем, при использовании ИВЛ существуют риски травматизации легких, а также инфицирования внутрибольничными инфекциями.
Причины развития двусторонней пневмонии
Наиболее частая причина двусторонней пневмонии - инфекция, поражающая легкие. Чаще всего это следующие виды инфекционных патогенов:
- Бактерии. Как правило, это пневмонии, вызванные стрептококками, пневмококками, стафилококками и другими видами бактериальных патогенов. В медицинской практике, бактериальные пневмонии встречаются чаще всего. Серьезную проблему составляют внутрибольничные инфекции, поражающие дыхательную систему пациента при аспирации, вентиляции легких, хирургических вмешательствах или приеме цитостатических препаратов.
- Вирусы. Вирусные пневмонии встречаются реже бактериальных. Чаще всего воспаление легких вызывается вирусами гриппа, респираторно-синцитиальным вирусом, а также коронавирусами (SARS-CoV, SARS-CoV-2, MERS-CoV). При вирусной инфекции часто воспаляются интерстициальные ткани легких с образованием инфильтратов в альвеолярных мешочках. Поражение происходит в результате иммунного ответа на инфицирование. При вирусной инфекции белые кровяные тельца (в частности, лимфоциты) активируют цитокины (так называемый цитокиновый шторм), что приводит накоплению жидкости в альвеолах и дальнейшей дыхательной недостаточности.
- Грибки. Грибковые пневмонии встречаются гораздо реже бактериальных или вирусных. Нередко грибковое поражение легких отмечается на фоне интенсивной антибактериальной терапии. Пневмония, вызванная грибками также встречается у людей с ослабленным иммунитетом (например, ВИЧ-инфицированные пациентов), а также больные с хроническими обструктивными болезнями легких (ХОБЛ).
Примечательно, что вероятность развития двусторонней пневмонии у некоторых категорий людей выше, чем у других. Рассмотрим основные факторы риска развития двустороннего воспаления легких:
- Возраст - люди старше 65 и дети младше 5 лет.
- Нехватка витаминов и питательных веществ (люди с болезненной худобой).
- Легочные заболевания, например, астма, ХОБЛ, муковисцидоз, туберкулез и другие.
- Курение.
- Наличие хронических заболеваний. В частности, это болезни сердца и сосудов, патологии легких, сахарный диабет.
- Нарушение работы иммунной системы. Примечательно, что опасность таит в себе как ослабленная иммунная система, так и гипериммунный ответ. В группе риска и люди, страдающие аутоиммунными заболеваниями.
- Пациенты, принимающие иммунодепрессанты - препараты, подавляющие иммунную систему.
- Люди, имеющие проблемы с глотанием.
- Люди, недавно перенесшие вирусную или бактериальную инфекцию дыхательных путей.
Симптомы
По внешним признакам определить у человека одностороннюю или двустороннюю пневмонию невозможно. Например, нередки случаи, когда у пациента с COVID-19 вроде бы нормальное дыхание, имеется лишь высокая температура, однако на компьютерной томографии (КТ) выявляют двустороннее воспаление легких.
Некоторые признаки заболеваний, на фоне которых обычно развивается пневмония, могут указывать на вероятность воспаления легких. К таким симптомам относятся:
- Высокая температура, часто сопровождающаяся ознобом и дрожью. Однако это может быть и субфебрильная температура (не выше 38 градусов по Цельсию). В очень редких случаях при воспалении легких у больного отмечается снижение температуры (как правило, такой симптом редко встречается у пожилых пациентов).
- Сухой кашель, течение которого со временем ухудшается. Со временем могут наблюдаться выделения густой слизи или мокроты.
- Одышка в состоянии покоя или при выполнении физической работы, которая ранее не вызывала одышку. Такой симптом указывает на частичную дыхательную недостаточность.
- Боли в груди при кашле или дыхании.
- Сильное недомогание, слабость.
- Тошнота, рвота - отмечаются в редких случаях.
У людей старше 65 лет пневмония (как односторонняя, так и двусторонняя) может привести к спутанности сознания и изменению мыслительной деятельности.
Когда обращаться к врачу
Специфических симптомов у двусторонней пневмонии нет. Чаще всего симптоматика напоминает простуду или грипп, и при таких признаках люди предпочитают лечиться дома. Однако в настоящее время, когда высока вероятность заражения коронавирусом SARS-CoV-2, при подобных симптомах желательно обратиться к врачу и пройти соответствующую диагностику.
К врачу следует также обращаться в случаях, когда вы испытываете сложности с дыханием, когда отмечается боль в груди при кашле или дыхании. Помните, чем раньше обратиться к врачу, тем выше шансы на успешное лечение пневмоний.
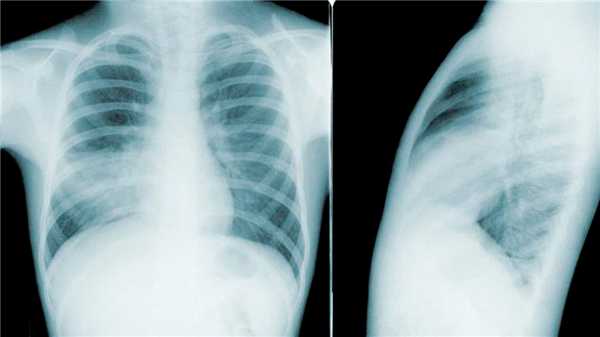
Рисунок 2: Двусторонняя пневмония на рентгеновском снимке в двух проекциях. Источник: PHIL CDC
Диагностика
Диагностический протокол при подозрении на пневмонию, как правило, включает следующие процедуры:
- Анализы крови (общий, биохимический). Определяется формула крови, уровень С-реактивного белка и ряд других маркеров инфекционно-воспалительного процесса.
- Рентгенография легких - позволяет выявить очаг воспаления.
- Компьютерная томография - назначается в случаях, когда рентгенография не показывает поражения легких, однако клиническая картина указывает на обратное. Компьютерная томография позволяет определить поражения легких по типу «матового стекла». Это изменения в легочной ткани на уровне альвеол. Такой характер воспаления часто отмечают при вирусных пневмониях, например, при гриппе или коронавирусной инфекции.
- Пульсоксиметрия - измерение уровня кислорода в крови (сатурация).
- Анализ мокроты. У больного берут образец мокроты и проводят бактериологическое исследование или ПЦР-анализ для определения возбудителя инфекции.
Лечение
Лечение как односторонней, так и двусторонней пневмонии направлено на устранение инфекционного процесса и предотвращение осложнений. Алгоритм лечения зависит как от возбудителя, так и от клинической картины заболевания.
Для облегчения дыхания применяются препараты, расширяющие бронхи. Компенсация дыхательной недостаточности проводится путем кислородотерапии. Для подавления воспаления и цитокинового шторма применяют гормональные противовоспалительные препараты (кортикостероиды). Последние хорошо себя зарекомендовали в лечении пневмонии, вызванной коронавирусной инфекцией.
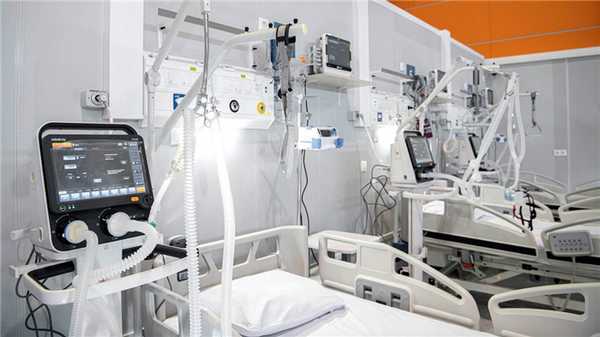
Рисунок 3. Аппарат для искусственной вентиляции легких. Обычно его назначают при тяжелых случаях пневмонии. Источник: Максим Мишин / Правительство Москвы
Что касается противовирусных препаратов при вирусных пневмониях, то они используются не всегда. В данном случае все зависит от типа вируса. В настоящее время медицине доступны лишь несколько противовирусных препаратов с доказанной эффективностью в отношении вирусов гриппа. В остальных случаях применение этих средств лишено смысла.
Отдельно нужно сказать об антибиотиках. Назначает их только врач в случае, если доказано бактериальное происхождение пневмонии. Антибиотики также уместны при высоком риске бактериального осложнения на фоне вирусной инфекции. Все эти риски, а также сроки приема препарата определяет врач после диагностики. Самостоятельный прием антибактериальных препаратов недопустим.
Осложнения двусторонней пневмонии
Двусторонняя пневмония может привести к ряду осложнений, а именно:
- Сепсис - системное заражение крови.
- Поражение плевры (плевральный выпот, плеврит).
- Нарушение деятельности внутренних органов (легких, сердца, почек).
Вероятность развития осложнений увеличивается с возрастом, а также при наличии вышеуказанных факторов риска.
Прогнозы
В большинстве случаев пациенты с двусторонней пневмонией выздоравливают. Прогнозы зависят от возраста больного, сопутствующих заболеваний, а также первопричины инфекционно-воспалительного процесса.
Заключение
Лечение двусторонней пневмонии осуществляется как в амбулаторных условиях, так и в стационаре, в зависимости от степени тяжести заболевания. Алгоритм лечения зависит от причины воспаления легких и ряда других факторов, определяемых во время диагностики.
Помните, что пневмонии (как односторонние, так и двусторонние) могут иметь как краткосрочные, так и долгосрочные последствия. Например, у людей, перенесших двустороннюю пневмонию, повышен риск развития хронических легочных заболеваний.
Читайте также:
