Поражение клубочков почек детей. Патогенез гломерулонефрита
Добавил пользователь Skiper Обновлено: 21.01.2026
Что такое острый пиелонефрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Закуцкого Александра Николаевича, уролога со стажем в 16 лет.
Над статьей доктора Закуцкого Александра Николаевича работали литературный редактор Маргарита Тихонова , научный редактор Александр Комаров
Определение болезни. Причины заболевания
Острый пиелонефрит — это воспалительное заболевание почек бактериальной причины с преимущественным поражением лоханки, чашечек и межуточной ткани паренхимы почек. В Международной классификации болезней отказались от термина «острый пиелонефрит», заменив его на «острый интерстициальный нефрит». [3]
Пиелонефрит следует отличать от гломерулонефрита. Обе формы нефрита характеризуются воспалением паренхимы почек, но при пиелонефрите поражается межуточная ткань, а при гломерулонефрите — клубочки почек. Поэтому пиелонефрит называют «интерстициальным нефритом», от слова «интерстиций» — межуточная ткань, а гломерулонефрит можно назвать «клубочковым нефритом», от слова «гломерула» — почечный клубочек. [2]
Причина пиелонефрита — бактериальная инфекция. Среди возбудителей заболевания лидирует кишечная палочка (Escherichia coli). Реже встречаются другие микробы, такие как протей, энтерококк, синегнойная палочка и стафилококк. [4]
Особую опасность представляют БЛРС+ бактериями. Аббревиатура «БЛРС» расшифровывается как «бета-лактамазы расширенного спектра действия». БЛРС — это группа бактериальных ферментов, которые позволяют бактериям игнорировать антибиотики. Благодаря БЛРС бактерии расщепляют и нейтрализуют несколько групп антибактериальных препаратов, включая пенициллины и цефалоспорины. Продуцировать подобные ферменты могут далеко не все микробы, довольно часто эта способность наблюдалась у кишечной палочки и клебсиеллы пневмонии. Современные микробиологические лаборатории всегда отмечают подобные микробы либо русской аббревиатурой БЛРС+, либо английским аналогом ESBL+. Согласно европейским данным, БЛРС, продуцируемые кишечной палочкой, встречаются в 10% случаев, а клебсиелла пневмонии продуцирует БЛРС в 20% случаев. Таким образом, проблема БЛРС+ бактерий имеет важное клиническое значение. [8]
Острый пиелонефрит может возникнуть в любом возрасте и у любого пола. Чаще всего заболевание возникает у женщин активного репродуктивного возраста, что объясняется особенностями строения женской мочеполовой системы. Однако нередко пиелонефрит выявляют у детей и половозрелых мужчин, поэтому возраст и пол заболевавшего не могут быть использованы в качестве дифференциального признака данного заболевания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острого пиелонефрита
Для острого пиелонефрита типично сочетание высокой температуры с болями в области воспалённой почки. Если почка располагается на своём месте, то боль беспокоит в проекции рёберно-позвоночного угла. При опущении почки боль возникает по фланкам живота. Пиелонефрит может затрагивать как одну почку, так и обе почки, соответственно боль может беспокоить как с одной стороны, так и с обеих сторон одновременно.
Выраженность боли может быть различной — от умеренной до интенсивной. Как правило, боль носит постоянный характер и не зависит от положения тела или движений. Иными словами, невозможно найти такое положение в кровати, когда боль будет беспокоить меньше или пройдет совсем. Также верно и то, что движения туловищем в виде сгибания, разгибания или поворотов не приводят к обострению болей.
В отдельных случаях боль носит приступообразный характер. Это характерно для пиелонефритов, которые возникают на фоне закупорки мочевых путей камнем. Если при классической почечной колике боль между приступами отступает совсем, то при сопутствующем пиелонефрите болевой синдром сохраняется и между приступами.
Развитие острого пиелонефрита может сопровождаться изменения со стороны мочеиспускания, хотя это не является обязательным условием. Можно отметить появление мути в моче и неприятного запаха. Кроме того, воспалённая моча потенциально способна спровоцировать учащённое мочеиспускание. В целом мочевые симптомы выходят на первый план только в том случае, если острый пиелонефрит осложняет уже имеющееся воспаление мочевого пузыря. [1] [4]
Патогенез острого пиелонефрита
Бактерия попадает в почку либо с кровью, либо с мочой. Кровяной занос бактериальной инфекции получил название «гематогенного» пути передачи. Иногда врачи говорят о нисходящем пути развития острого пиелонефрита. Например, тот же нелеченный бронхит может осложниться развитием пиелонефрита за счёт обильного поступления бактерий в кровь. Нужно понимать, что почки фильтруют кровь со всего организма, поэтому пиелонефрит может осложнить любой несвоевременно пролеченный гнойник, даже расположенный в ногах или руках.
Альтернативой кровяному пути попаданию бактерий является мочевой путь распространения микробов. В научной литературе такой путь передачи возбудителя именуется «уриногенным», от слова «урина» — моча. Раньше такой путь заражения называли «восходящим», так как инфекция фактически "карабкается" вверх из мочевого пузыря. Вот почему очень важно своевременно пролечивать воспаление мочевого пузыря в виде цистита, не дожидаясь распространения бактерий вверх в почку.
Уриногенный путь передачи особенно характерен для детей из-за широкого распространения пузырно-мочеточникового рефлюкса. Так называют заброс мочи из мочевого пузыря обратно в почку. Несмотря на широкое распространение рефлюкса именно в детском возрасте, многие взрослые страдают аналогичным заболеванием. Особенно часто рефлюкс, то есть обратный заброс мочи, наблюдается при переполнении мочевого пузыря. Поэтому очень важно своевременно опорожнять мочевой пузырь. [8]
Классификация и стадии развития острого пиелонефрита
Традиционно острый пиелонефрит подразделяют на серозный и гнойный, хотя гнойный пиелонефрит является скорее осложнением острого пиелонефрита.
Существует несколько форм гнойного пиелонефрита:
- апостематозный пиелонефрит;
- абсцесс почки;
- карбункул почки;
- некротический папиллит;
- эмфизематозный пиелонефрит.
Если гнойников много, и они небольшие по размеру, то говорят об апостематозном пиелонефрите. В том случае, если гнойник большой и одиночный, то мы имеем дело с абсцессом почки.
Почечный абсцесс нужно дифференцировать с карбункулом почки. Карбункул — это часть почечной паренхимы, погибшая вследствие закупорки крупного почечного сосуда микробным эмболом. Рано или поздно погибшие от эмболии ткани подвергаются гнойному расплавлению, что приводит к абсцедированию карбункула.
Особой формой острого пиелонефрита является некротический папиллит — это грозное и смертельно опасное заболевание. К счастью, эта болезнь встречается настолько редко, что даже опытные урологи со стажем работы в несколько десятков лет могут вспомнить лишь несколько случаев данной формы острого пиелонефрита. При некротической папиллите происходит некроз, то есть омертвление и гибель почечного сосочка. Это сопровождается почечной недостаточностью и появлением крови в моче. Причина некротического папиллита сходна с причиной карбункула: закупорка почечного сосуда микробным эмболом. Только при папиллите страдает сосуд, питающий почечный сосочек. [4]
Также пиелонефрит можно подразделить на первичную и вторичную форму. Первичный острый пиелонефрит развивается в интактной почке, то есть без аномалий развития, камней и значимых нарушений оттока мочи. Вторичный острый пиелонефрит возникает на фоне заболеваний, которые нарушают пассаж мочи. Между вторичной формой острого пиелонефрита и первичным обострением хронического пиелонефрита очень тонкая грань, поэтому в МКБ-10 введён код № 12 «Тубулоинтерстициальный нефрит, не уточнённый как острый или хронический». [3]
Осложнения острого пиелонефрита
Местные осложнения острого пиелонефрита включают апостематоз, абсцесс почки, эмфизематозный пиелонефрит, а также тромбоз почечных сосудов либо в виде карбункула почки, либо в виде некротизирующего папиллита. [10]
Эмфизематозный пиелонефрит является исключительно редким заболеванием и отличается от прочих гнойных осложнений пиелонефрита появлением пузырьков газа. Воздушные скопления могут быть в почечной паренхиме, полостной системе почек или даже в паранефральной клетчатке. К счастью, эмфизематозный пиелонефрит встречаются существенно реже других гнойных осложнений почки. [7]
Среди системных осложнений нужно отметить острую почечную недостаточность и синдром системной воспалительной реакции (сепсис). Именно поэтому часть пациентов нуждается в госпитализации в урологические стационары. В условиях стационара проводится регулярный контроль анализов и УЗИ для своевременного выявления осложнений острого пиелонефрита. [4]
Некоторые осложнения пиелонефрита в большей степени ассоциированы с хронической формой этого заболевания, но так как острый пиелонефрит может перейти в хронический, то нельзя не упомянуть о таком важном осложнении как мочекаменная болезнь. В некоторых ситуациях воспаление почечной паренхимы вызывают уреаза-продуцирующие микробы. Уреаза — это фермент, который позволяет бактериям расщеплять мочевину из мочи. После срабатывания фермента мочевина расщепляется до углекислоты и аммиака. Именно эти два компонента запускают сложный биохимический каскад, который приводит к образованию инфекционных камней: струвита и гидроксиапатита. К счастью, самый частый возбудитель пиелонефрита — кишечная палочка — не умеет производить уреазу, этой способностью обладают другие более редкие возбудители пиелонефрита — протей, клебсиелла и синегнойная палочка.
Важным осложнением острого пиелонефрита является хроническая форма этого заболевания. Именно поэтому очень важно диспансерное наблюдение после удачного излечения острого пиелонефрита. Словосочетание «диспансерное наблюдение» немного пугает своей бюрократической составляющей, но по сути это означает необходимость контролировать анализы мочи в течение минимум трёх месяцев после перенесённого острого пиелонефрита.
Диагностика острого пиелонефрита
Минимальный объём обследований:
- общий анализ мочи;
- посев мочи на флору с определением чувствительности к антибиотикам;
- клинический анализ крови;
- анализ крови на креатинин;
- УЗИ почек и мочевого пузыря.
Общий анализ мочи
Типичным для пиелонефрита является повышение уровня лейкоцитов и обнаружение бактерий. Могут быть и другие неспецифичные для данного заболевания изменения, включая повышенный уровень белка или положительный тест на нитриты. Обнаружение большого количества эритроцитов требует проведения дифференциальной диагностики с мочекаменной болезнью и гломерулонефритом.
Посев мочи на флору и чувствительность к антибиотикам
Этот анализ имеет смысл сдавать до назначения антибиотиков. Посев мочи позволяет выявить возбудитель пиелонефрита и определить наиболее эффективные антибактериальные препараты.
Клинический анализ крови
Неспецифическим признаком пиелонефрита является повышенный уровень лейкоцитов со сдвигом лейкоцитарной формулы влево. Как правило, больной с острым пиелонефритом повторяет клинический анализ крови два или три раза во время лечения. Данный анализ позволяет оценить эффективность антибактериальной терапии и своевременно сигнализировать о развитии гнойных осложнений в воспаленной почке.
Анализ крови на креатинин
Этот анализ является обязательным для всех пациентов с пиелонефритом прежде всего потому, что в ряде случаев острый пиелонефрит может осложниться развитием острой почечной недостаточности. Кроме того, анализ крови на креатинин необходим для решения вопроса о рентгенологическом исследовании почек с применением контраста.
УЗИ почек и мочевого пузыря
Ультразвуковое исследование позволяет исключить обструктивный пиелонефрит, связанный с нарушением оттока мочи из почки. Кроме того, УЗИ почек необходимо для своевременного выявления апостематоза, абсцесса и карбункула в паренхиме почки. Все вышеперечисленные термины используются для описания осложнений острого пиелонефрита.
Важнейшим преимуществом ультразвукового исследования является возможность повторения этого исследования в динамике без нанесения какого-либо вреда или даже дискомфорта организму. Важно помнить, что нормальные результаты УЗИ не исключают наличие острого пиелонефрита.
Рентгеновское обследование почек: внутривенная урография или компьютерная томография почек с внутривенным контрастированием.
Рентгеновское обследование почек является самым точным и достоверным методом диагностики. Традиционный рентген в виде внутривенной урографии подразумевает обязательное внутривенное введение йодсодержащего контраста. Это не всегда возможно из-за сопутствующих причин: аллергия на йод, приём гормонов щитовидной железы и повышенный уровень креатинина в крови. По сути, в настоящее время внутривенная урография необходима только для установления степени нефроптоза при опущении почек.
Значительно более широко применяется КТ почек (компьютерная томография). КТ относится к рентгеновским методам исследования, однако его информативность значительно выше, чем у обычного рентгена. Вопрос о введении йодсодержащего внутривенного контраста решается лечащим урологом индивидуально с каждым пациентом. [2] [4]
Лечение острого пиелонефрита
Стационарное лечение обычно требуется для беременных, детей, пожилых людей, пациентов с ослабленным иммунитетом, плохо контролируемым диабетом, после трансплантации почек и, конечно же, всех людей с обструкцией мочевых путей. Также желательно госпитализировать людей с острым пиелонефритом единственной существующей или единственно функционирующей почки. Здоровые, молодые, небеременные женщины, которые болеют неосложнённым пиелонефритом, могут лечиться амбулаторно.
Обычно острый пиелонефрит требует исключительно медикаментозного лечения. Показания к хирургическому лечению возникают крайне редко.
Первоначальный выбор антибиотика при остром пиелонефрите является эмпирическим. Через 4-7 дней антибактериальная терапия может быть скорректирована по результатам посева мочи. Эмпирический выбор антибиотика остаётся на усмотрение лечащего врача.
В национальных рекомендациях в качестве средства выбора при остром пиелонефрите указаны фторхинолоны второго и третьего поколения. [4] Тоже самое сказано и в рекомендациях Европейской ассоциации урологов: начиная с 2020 года, она рекомендует использовать фторхинолоны и цефалоспорины в качестве препаратов для эмпирической терапии, т. е. в случаях, когда не готов посев мочи. [11] Между тем, ещё в 2016 году FDA (Управление по контролю качества пищевых продуктов и лекарственных препаратов) рекомендовала отказаться от использования данных антибиотиков из-за большого количества осложнений в отношении связок, суставов и периферических нервов. [6] Поэтому в качестве первой линии терапии рекомендуют использовать цефалоспорины третьего поколения.
Также Европейская ассоциация урологов не рекомендует назначать фосфомицин для приёма внутрь и нитрофурантоин при лечении пиелонефрита, так как у них нет накопительного эффекта [11] .
Наиболее широко используемым цефалоспорином третьего поколения является цефтриаксон. Активно практикуется ступенчатая терапия с плавным переходом от внутривенно вводимого антибиотика к его пероральному аналогу. С внутривенного цефтриаксона можно перейти на пероральный цефиксим, который также относится к цефалоспоринам третьего поколения. Цефиксим больше известен под своими торговыми названиями: «Супракс», «Супракс солютаб» и «Панцеф».
Часто можно встретить комбинацию из двух антибиотиков для лечения острого пиелонефрита. Как правило, комбинируют цефалоспорины с фторхинолонами или аминогликозидами. Аминогликозиды в виде амикацина обладают явным нефротоксическим действием, поэтому их использование для эмпирической терапии оправдано только в тяжёлых случаях.
Если в посеве мочи обнаружили микроорганизмы, устойчивые к большинству антибиотиков, могут назначить альтернативные препараты в виде карбапенемов — антибиотики группы бета-лактамов. [11]
В целом выбор антибиотика — на усмотрение лечащего врача. [9]
Показания к оперативному лечению возникают при гнойной форме воспаления и остром вторичном пиелонефрите. При вторичном пиелонефрите главная цель хирургического вмешательства состоит в дренировании мочи. Это можно сделать как путём установки почечного стента, так и благодаря чрезкожной пункционной нефростомии.
Гнойная форма острого пиелонефрита требует ревизии и декапсуляции почки, вскрытия гнойных очагов или даже нефрэктомии при гнойном разрушении большей части почки. [4]
Прогноз. Профилактика
Прогноз при пиелонефрите благоприятный. Большинство острых пиелонефритов успешно лечатся амбулаторно, и лишь небольшая доля случаев требует госпитализации. Тем не менее сохраняется определённый процент летальный исходов. Причиной неблагоприятного течения заболевания являются возраст старше 65 лет, присоединение острой почечной недостаточности, несвоевременно выявленные гнойные осложнения, требующие хирургического вмешательства либо приводящие к уросеспису, и тяжёлые сопутствующие заболевания наподобие декомпенсированного сахарного диабета. [5]
Составление плана индивидуальной профилактики начинается с изучения истории конкретного заболевания. В частности, необходимо ответить на вопрос, каким образом бактерии попали в почку: с кровью или с мочой? При гематогенном пути заражения необходимо санировать имеющиеся в организме очаги хронической инфекции, исключить переохлаждение и проводить профилактику сезонных простудных заболеваний. При уриногенном пути заражения необходимо заняться профилактикой воспалительных заболеваний мочевого пузыря.
В случае вторичной формы острого пиелонефрита целесообразно восстановить нормальный отток мочи из поражённой почки.
Вне зависимости от пути попадания микробов в почку всем пациентам рекомендуется потреблять достаточное количество жидкости и разнообразные урологические сборы растительного происхождения. [4]
Острый гломерулонефрит
Острый гломерулонефрит - это заболевание иммуновоспалительного характера, характеризующееся вовлечением структурных единиц почек - нефронов и преимущественным поражением клубочкового аппарата. Патология протекает с развитием экстраренальных синдромов (отечного и гипертонического) и ренальных проявлений (мочевого синдрома). В диагностике применяется исследование мочи (общий анализ, проба Реберга, Зимницкого, Нечипоренко), УЗИ почек, биохимическое и иммунологическое исследование крови, биопсия почечной ткани. Лечение требует соблюдения постельного режима и диеты, назначения стероидных гормонов, гипотензивных, диуретических средств.
Общие сведения
Острый гломерулонефрит развивается преимущественно у детей в возрасте 2-12 лет и взрослых до 40 лет. Мужчины заболевают в 15,2 раза чаще, чем женщины. Пик заболеваемости приходится на влажное и холодное время года. При болезни происходит преимущественное поражение клубочков (почечных телец), кроме этого в патологический процесс вовлекаются канальца и межуточная ткань обеих почек. Поражение почек связано со специфической иммунной реакцией, обусловленной инфекционным или аллергическим процессом.
Причины
В большинстве случаев развитие острого гломерулонефрита сопряжено с перенесенной стрептококковой инфекцией - фарингитом, ангиной, обострением тонзиллита, скарлатиной, рожистым воспалением кожи. Этиологическим агентом в этих случаях, как правило, выступает b-гемолитический стрептококк группы А. О стрептококковой этиологии острого гломерулонефрита свидетельствует определение повышенного титра антител к стрептококковой гиалуронидазе и стрептолизину-О, увеличение ЦИК, содержащих антигены к стрептококку.
Иногда развитию болезни предшествует вирусная инфекция - грипп, эпидемический паротит, ветряная оспа, краснуха, инфекционный мононуклеоз, герпес, гепатит. Реже патология возникает после дифтерии, стафилококковых и пневмококковых пневмоний, малярии, бруцеллеза, инфекционного эндокардита, брюшного и сыпного тифа и других инфекций.
Кроме инфекционно-иммунных острых гломерулонефритов встречаются неинфекционно-иммунные формы заболевания, вызванные введением сывороток и вакцин, индивидуальной непереносимостью пыльцы растений, приемом нефротоксичных лекарственных препаратов, укусом насекомых или змей, алкогольной интоксикацией и др. причинами. Предрасполагающими факторами служат переохлаждение, анатомо-физиологическая незавершенность строения нефронов у детей.
Патогенез
Специалисты в сфере современной урологии придерживаются мнения, что острый гломерулонефрит - это иммунокомплексная патология. После инфекционного или аллергического воздействия происходит изменение реактивности организма, что проявляется образованием антител к чужеродным антигенам. Взаимодействуя с комплементом, иммунные комплексы откладываются на поверхностях базальных мембран капилляров клубочков. Изменяется структура капиллярных стенок, увеличивается проницаемость сосудов, создаются условия для тромбообразования.
Расстройство трофики почечной ткани ведет к тому, что в ишемической почке активизируется функция ренин-ангиотензин-альдостероновой системы, что приводит к спазму периферических сосудов и, как следствие, повышению АД. На этом фоне нарушаются процессы фильтрации и реабсорбции, происходит задержка Na и воды, в моче появляются патологические элементы.
Классификация
По вызывающим поражение причинам различают первичный, идиопатический и вторичный гломерулонефрит. Первичный гломерулонефрит связан с инфекционным, аллергическим или токсическим воздействием на почечную ткань; вторичный - служит проявлением системной патологии (геморрагического васкулита, СКВ и др.); идиопатический гломерулонефрит развивается по неопределенным причинам. В зависимости от этиофакторов гломерулонефриты могут быть инфекционно-иммунными и неинфекционно-иммунными.
По клиническому течению заболевание может развиваться в классической развернутой форме (с гипертензивным, отечным и мочевым синдромами), в бисиндромной форме (сочетание мочевого синдрома с отечным или гипертензивным) или моносиндромной форме (только с мочевым синдромом). В МКБ-10 для обозначения острого диффузного гломерулонефрита используется понятие «острый нефритический синдром».
Симптомы острого гломерулонефрита
Классическая картина включает триаду симптомокомплексов: почечный (ренальный) - мочевой синдром и внепочечные (экстраренальные) - отечный и гипертензивный синдромы. Патология обычно манифестирует спустя 1-2 недели после имевшего место этиологического воздействия (инфекции, аллергической реакции и т. д.).
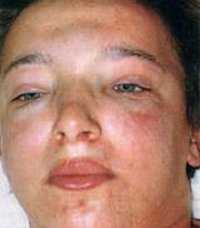
Появление отеков - наиболее ранний и частый признак острого гломерулонефрита, встречается у 70-90% пациентов, у половины из них отеки бывают значительными. Отеки располагаются преимущественно в области лица: наиболее выражены по утрам и спадают днем, сменяясь отечностью лодыжек и голеней. В дальнейшем отечный синдром может прогрессировать до анасарки, гидроперикарда, гидроторакса, асцита. В некоторых случаях видимые отеки могут отсутствовать, однако ежедневное увеличение массы тела пациента свидетельствует о задержке жидкости в тканях.
Артериальная гипертензия обычно выражена умеренно: у 60-70% пациентов АД не превышает 160/100 мм рт. ст. Однако стойкая длительная гипертензия имеет неблагоприятный прогноз. Для острого гломерулонефрита характерно сочетание артериальной гипертензии с брадикардией менее 60 уд. в мин., которая может держаться на протяжении 1-2 недель. При остро развивающейся гиповолемии возможны явления недостаточности левого желудочка, выражающейся сердечной астмой и отеком легких.
Нередко отмечается развитие церебральных нарушений, обусловленных отеком головного мозга - головной боли, тошноты и рвоты, снижения зрения, «пелены» перед глазами, понижения слуха, психо-моторной возбудимости. Крайним проявлением церебрального синдрома может стать развитие ангиоспастической энцефалопатии - эклампсии (тонико-клонических судорог, потери сознания, набухания шейных вен, цианоза шеи и лица, урежения пульса и т. д.).
Течение патологии может сопровождать болевой синдром различной степени выраженности: боли в пояснице чаще симметричны и обусловлены растяжением почечных капсул и нарушением уродинамики. Мочевой синдроме характеризуется ранним развитием олигурии и даже анурии в сочетании с сильной жаждой. При этом отмечается повышение относительной плотности мочи, появление в моче гиалиновых и зернистых цилиндров, эритроцитов, большого количества белка.
Эритроцитурия может протекать в виде микрогематурии (Er- 5 -50 - 100 в поле зрения) или макрогематурии, при которой моча становится цвета «мясных помоев». Протеинурия и гематурияе в большей степени выражены в первые сутки заболевания. Реже острый гломерулонефрит развивается по типу моносиндромной (мочевой) формы без отеков и при нормальном АД. На фоне болезни может формироваться нефротический синдром.
Диагностика
При диагностике острого гломерулонефрита учитывается наличие типичных клинических синдромов, изменений в моче, биохимическом и иммунологическом анализе крови, данные УЗИ и биопсии почки. Общий анализ мочи характеризуется протеинурией, гематурией, цилиндрурией. Для пробы Зимницкого типично уменьшение количества суточной мочи и повышение ее относительной плотности. Проба Реберга отражает снижение фильтрационной способности почек.
Изменения биохимических показателей крови могут включать гипопротеинемию, диспротеинемию (уменьшение альбуминов и увеличение концентрации глобулинов), появление СРБ, и сиаловых кислот, умеренную гиперхолестеринемию и гиперлипидемию, гиперазотемию. При исследовании коагулограммы определяются сдвиги в свертывающей системе - гиперкоагуляционный синдром. Иммунологические анализы позволяют выявить нарастание титра АСЛ-О, антистрептокиназы, антигиалуронидазы, антидезоксирибонуклеазы В; повышение содержания IgG, IgM, реже IgА; гипокомплементемию СЗ и С4.
УЗИ почек обычно показывает неизмененные размеры органов, уменьшение эхогенности, снижение скорости клубочковой фильтрации. Показаниями к проведению биопсии почки служат необходимость дифференциации острого и хронического гломерулонефрита, быстропрогрессирующего нефрита. При острой форме болезни в нефробиоптате определяются признаки клеточной пролиферации, инфильтрация клубочков моноцитами и нейтрофилами, наличие плотных депозитов иммунных комплексов и др. При гипертензивном синдроме необходимо проведение исследования глазного дна и ЭКГ.
Лечение острого гломерулонефрита
Терапия проводится в урологическом стационаре и требует назначения строгого постельного режима, бессолевого диетического питания с ограничением потребления животных белков, жидкости, назначением «сахарных» и разгрузочных дней. Производится строгий учет количества потребляемой жидкости и объема диуреза. Основная терапия заключается в применении стероидных гормонов - преднизолона, дексаметазона курсом до 5-6 недель.
При выраженных отеках и артериальной гипертензии одновременно назначаются диуретические и гипотензивные средства. Антибиотикотерапия проводится при имеющихся признаках инфекции (тонзиллите, пневмонии, эндокардите и др.). При острой почечной недостаточности может потребоваться назначение антикоагулянтов, проведение гемодиализа. Курс стационарного лечения составляет 1-1,5 месяца, после чего пациента выписывают под наблюдение врача-нефролога.
Прогноз и профилактика
В большинстве случаев патология хорошо поддается терапии кортикостероидными гормонами и заканчивается выздоровлением. В 1/3 случаев возможен переход в хроническую форму; смертельные исходы крайне редки. На этапе диспансерного наблюдения пациенту требуется динамическое исследование мочи.
Профилактика развития первичного острого гломерулонефрита и его рецидивов заключается в лечении острых инфекций, санации хронических очагов в носоглотке и полости рта, повышении сопротивляемости организма, недопущении охлаждения и длительного нахождения во влажной среде. Лицам с повышенным аллергическим фоном (крапивницей, бронхиальной астмой, сенной лихорадкой) профилактические вакцинации противопоказаны.
Гломерулонефрит у детей
Гломерулонефрит у детей - острое или хроническое воспаление почечных клубочков инфекционно-аллергической природы. Для острого гломерулонефрита у детей характерна триада синдромов: мочевой (олигурия, анурия, гематурия, протеинурия), отечный и гипертензивный; при хронических формах преобладает один из них или латентное течение. Диагноз гломерулонефрита у детей основан на данных анамнеза, характерной клинической картине, лабораторных показателях, УЗИ и пункционной биопсии почек. В остром периоде гломерулонефрита у детей назначается постельный режим, диета, антибиотикотерапия, кортикостероиды, антикоагулянты, мочегонные, гипотензивные и иммуносупрессивные препараты.
Гломерулонефрит у детей - иммуно-воспалительное поражение клубочкового аппарата почек, приводящее к снижению их функции. В педиатрии гломерулонефрит является одной из самых распространенных приобретенных патологий почек у детей, занимая второе место после инфекций мочевыводящих путей. Большинство случаев гломерулонефрита регистрируется у детей дошкольного и младшего школьного возраста (3-9 лет), редкие эпизоды (менее 5%) - у детей первых 2-х лет жизни. У мальчиков гломерулонефрит возникает в 2 раза чаще, чем у девочек.
В основе развития гломерулонефрита у детей лежит инфекционная аллергия (образование и фиксация в почках циркулирующих иммунных комплексов) или аутоаллергия (выработка аутоантител), а также неиммунное повреждение органа вследствие развивающихся гемодинамических и метаболических нарушений. Помимо почечных клубочков в патологический процесс могут вовлекаться канальца и межуточная (интерстициальная) ткань. Гломерулонефрит у детей опасен риском развития хронической почечной недостаточности и ранней инвалидизации.

Выявить этиологический фактор удается в 80-90% острого гломерулонефрита у детей и в 5-10% случаев хронического. Основными причинами гломерулонефрита у детей являются инфекционные агенты - бактерии (в первую очередь, нефритогенные штаммы β-гемолитического стрептококка группы А, а также стафилококки, пневмококки, энтерококки), вирусы (гепатита В, кори, краснухи, ветряной оспы), паразиты (возбудитель малярии, токсоплазмы), грибы (кандида) и неинфекционные факторы (аллергены - чужеродные белки, вакцины, сыворотки, пыльца растений, токсины, лекарства). Чаще всего развитию острого гломерулонефрита у детей предшествует недавно перенесенная (за 2-3 недели до этого) стрептококковая инфекция в виде ангины, фарингита, скарлатины, пневмонии, стрептодермии, импетиго.
Хронический гломерулонефрит у детей обычно имеет первично хроническое течение, реже может быть следствием недолеченного острого гломерулонефрита. Основную роль в его развитии играет генетически детерминированный иммунный ответ на воздействие антигена, присущий данному индивидууму. Образующиеся при этом специфические иммунные комплексы повреждают капилляры почечных клубочков, что приводит к нарушению микроциркуляции, развитию воспалительных и дистрофических изменений в почках.
Гломерулонефрит может встречаться при различных заболеваниях соединительной ткани у детей (системной красной волчанке, геморрагическом васкулите, ревматизме, эндокардите). Развитие гломерулонефрита у детей возможно при некоторых наследственно обусловленных аномалиях: дисфункции Т-клеток, наследственном дефиците С6 и С7 фракций комплемента и антитромбина.
Предрасполагающими факторами развития гломерулонефрита у детей могут служить: отягощенная наследственность, повышенная чувствительность к стрептококковой инфекции, носительство нефритических штаммов стрептококка группы А или наличие очагов хронической инфекции в носоглотке и на коже. Способствовать активации латентной стрептококковой инфекции и развитию гломерулонефрита у детей могут переохлаждение организма (особенно во влажной среде), излишняя инсоляция, ОРВИ.
На течение гломерулонефрита у детей раннего возраста влияют особенности возрастной физиологии (функциональная незрелость почек), своеобразие реактивности организма ребенка (сенсибилизация с развитием иммунопатологических реакций).
Гломерулонефрит у детей может быть первичным (самостоятельная нозологическая форма) и вторичным (возникающим на фоне другой патологии), с установленной (бактериальной, вирусной, паразитарной) и с неустановленной этиологией, иммунологически обусловленный (иммунокомплексный и антительный) и иммунологически необусловленный. Клиническое течение гломерулонефрита у детей подразделяют на острое, подострое и хроническое.
По распространенности поражения выделяют диффузный и очаговый гломерулонефрит у детей; по локализации патологического процесса - интракапиллярный (в сосудистом клубочке) и экстракапиллярный (в полости капсулы клубочка); по характеру воспаления - экссудативный, пролиферативный и смешанный.
Хронический гломерулонефрит у детей включает несколько морфологических форм: незначительные гломерулярные нарушения; фокально-сегментарный, мембранозный, мезангиопролиферативный и мезангиокапиллярный гломерулонефрит; IgA-нефрит (болезнь болезнь Берже). По ведущим проявлениям различают латентную, гематурическую, нефротическую, гипертоническую и смешанную клинические формы гломерулонефрита у детей.
Симптомы гломерулонефрита у детей
Острый гломерулонефрит у детей обычно развивается через 2-3 недели после перенесенной инфекции, чаще, стрептококкового генеза. При типичном варианте гломерулонефрит у детей имеет циклический характер, характеризуется бурным началом и выраженными проявлениями: повышением температуры, ознобом, плохим самочувствием, головной болью, тошнотой, рвотой, болью в пояснице.
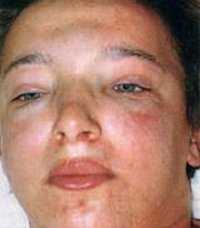
В первые дни заметно уменьшается объем выделяемой мочи, развивается значительная протеинурия, микро- и макрогематурия. Моча приобретает ржавый цвет (цвет «мясных помоев»). Характерны отеки, особенно заметные на лице и веках. Из-за отеков вес ребенка может на несколько килограммов превышать норму. Отмечается повышение АД до 140-160 мм рт. ст, в тяжелых случаях приобретающее длительный характер. При адекватном лечении острого гломерулонефрита у детей функции почек быстро восстанавливаются; полное выздоровление наступает через 4-6 недель (в среднем через 2-3 месяца). Редко (в 1-2% случаев) гломерулонефрит у детей переходит в хроническую форму, имеющую весьма разнообразную клиническую картину.
Гематурический хронический гломерулонефрит является самым распространенным в детском возрасте. Имеет рецидивирующее или персистирующее течение с медленным прогрессированием; характеризуется умеренной гематурией, при обострениях - макрогематурией. Гипертензия не отмечается, отеки отсутствуют или слабо выражены.
У детей нередко обнаруживается склонность к латентному течению гломерулонефрита со скудными мочевыми симптомами, без артериальной гипертензии и отеков; в этом случае заболевание может выявляться только при тщательном обследовании ребенка.
Для нефротического гломерулонефрита у детей типично волнообразное, постоянно рецидивирующее течение. Преобладают мочевые симптомы: олигурия, значительные отеки, асцит, гидроторакс. Артериальное давление в норме, либо немного повышено. Наблюдается массивная протеинурия, незначительная эритроцитурия. Гиперазотемия и снижение клубочковой фильтрации проявляются при развитии ХПН или обострении заболевания.
Гипертонический хронический гломерулонефрит у детей встречается редко. Ребенка беспокоит слабость, головная боль, головокружение. Характерна стойкая, прогрессирующая гипертензия; мочевой синдром выражен слабо, отеки незначительные или отсутствуют.
Диагностика гломерулонефрита у детей
Диагноз острого гломерулонефрита у ребенка верифицируется на основании данных анамнеза о недавно перенесенной инфекции, наличии наследственной и врожденной почечной патологии у кровных родственников и характерной клинической картины, подтвержденных лабораторными и инструментальными исследованиями. Обследование ребенка с подозрением на гломерулонефрит проводится педиатром и детским нефрологом (детским урологом).
В рамках диагностики исследуется общий и биохимический анализ крови и мочи, проба Реберга, анализ мочи по Нечипоренко, проба Зимницкого. При гломерулонефрите у детей выявляются снижение диуреза, скорости клубочковой фильтрации, никтурия, микро- и макрогематурия, протеинурия, цилиндрурия. В крови отмечается небольшой лейкоцитоз и увеличение СОЭ; снижение фракций комплемента СЗ и С5; повышение уровня ЦИК, мочевины, креатинина; гиперазотемия, повышение титра стрептококковых антител (АСГ и АСЛ-О).
УЗИ почек при остром гломерулонефрите у детей показывает незначительное увеличение их объема и повышение эхогенности. Пункционная биопсия почек выполняется для определения морфологического варианта гломерулонефрита у детей, назначения адекватной терапии и оценки прогноза заболевания.
При гломерулонефрите у детей показаны консультация детского офтальмолога (с исследованием глазного дна для исключения ангиопатии сосудов сетчатки), генетика (для исключения наследственной патологии), детского отоларинголога и стоматолога (для выявления и санации очагов хронической инфекции).
Лечение гломерулонефрита у детей
При выраженных проявлениях гломерулонефрита у детей (макрогематурии, протеинурии, отечности, артериальной гипертензии) показано стационарное лечение с назначением постельного режима и специальной диеты (с ограничением соли и белка), проведением этиотропной, симптоматической и патогенетической терапии. Строгая бессолевая диета необходима до исчезновения отеков, а строгая безбелковая диета - до восстановления нормального объема выводимой жидкости.
В остром периоде гломерулонефрита у детей назначается антибиотикотерапия (пенициллин, ампициллин, эритромицин). Коррекцию отечного синдрома проводят с помощью фуросемида, спиронолактона. Из гипотензивных средств у детей используют ингибиторы АПФ пролонгированного действия (эналаприл), блокаторы медленных кальциевых каналов (нифедипин), в подростковом возрасте - блокаторы рецепторов к ангиотензину II (лозартан, валсартан). Применяются глюкокортикостероиды (преднизолон), при тяжелых формах хронического гломерулонефрита - иммуносупрессивные препараты (хлорбутин, циклофосфан, левамизол). Для профилактики тромбозов при выраженном нефротическом синдроме назначаются антикоагулянты (гепарин) и антиагреганты. При значительном повышении уровней мочевой кислоты, мочевины и креатинина в крови, сопровождающихся сильным зудом и иктеричностью кожного покрова, может применяться гемодиализ.
После выписки из стационара дети должны находиться на диспансерном учете у педиатра и детского нефролога в течение 5 лет, а при рецидивах гломерулонефрита - пожизненно. Рекомендуется санаторно-курортное лечение; профилактическая вакцинация противопоказана.
Прогноз и профилактика гломерулонефрита у детей
При адекватном лечении острый гломерулонефрит у детей в большинстве случаев заканчивается выздоровлением. В 1-2% случаев гломерулонефрит у детей переходит в хроническую форму, в редких случаях возможен летальный исход.
При остром гломерулонефрите у детей возможно развитие серьезных осложнений: острой почечной недостаточности, кровоизлияний в головной мозг, нефротической энцефалопатии, уремии и сердечной недостаточности, представляющих угрозу для жизни. Хронический гломерулонефрит у детей сопровождается сморщиванием почек и снижением почечных функций с развитием ХПН.
Профилактика гломерулонефрита у детей заключается в своевременной диагностике и лечении стрептококковой инфекции, аллергических заболеваний, санации хронических очагов в носоглотке и полости рта.
Острый гломерулонефрит (нефритический синдром) - симптомы и лечение
Что такое острый гломерулонефрит (нефритический синдром)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Застело Елены Сергеевны, детского нефролога со стажем в 15 лет.
Над статьей доктора Застело Елены Сергеевны работали литературный редактор Вера Васина , научный редактор Кирилл Лелявин и шеф-редактор Маргарита Тихонова

Острый гломерулонефрит (Acute glomerulonephritis) — это группа заболеваний почек, которые отличаются по своей структуре, подходам к лечению и причинам, но все они в первую очередь приводят к повреждению почечных клубочков. Клубочками, или гломерулами, называют пучки кровеносных сосудов с мелкими порами, через которые в почках фильтруется кровь.
При развитии болезни в моче внезапно появляется кровь и выявляется белок, повышается артериальное давление, возникают отёки и может временно нарушиться работа почек.

Заболевание впервые описал английский врач Р. Брайт в 1827 году. В честь него все нефриты долгое время, вплоть до 1950-х годов, назывались «болезнью Брайта». В начале XX века Ф. Фольгарт и Т. Фар создали первую классификацию гломерулонефритов, выделив острые и хронические формы болезни. Разработанная в 1951 году техника биопсии почек позволила составить алгоритмы лечения для различных видов гломерулонефрита [1] .
Распространённость
Острый гломерулонефрит встречается у пациентов всех возрастов, но выделяют два пика заболеваемости: в 5-12 лет и после 60 лет [3] [4] . Чаще гломерулонефритом болеют мужчины.
Ежегодно выявляют около 470 000 случаев острого гломерулонефрита, уровень заболеваемости колеблется от 9 до 29 случаев на 100 000 населения [3] [4] .
В России гломерулонефрит — это ведущая причина терминальной стадии хронической болезни почек. Эта болезнь несовместима с жизнью и требует дорогостоящей почечной заместительной терапии: диализа и трансплантации донорской почки [19] .
Причины острого гломерулонефрита
Острый гломерулонефрит зачастую возникает после перенесённой инфекции, вызванной бета-гемолитическим стрептококком группы А (БГСА).
К болезням почек могут приводить следующие штаммы:
- 1, 4, 12 (вызывают болезнь после фарингита);
- 2, 49, 55, 57, 60 (после кожных инфекций) [16] .
Такой гломерулонефрит называют острым постстрептококковым гломерулонефритом (ОПСГН) [2] . Риск развития ОПСГН зависит от локализации инфекции: после фарингита он возникает в 5-10 % случаев, после кожной инфекции, например стрептодермии, — в 25 % случаев [5] [6] . В последнее время ОПГСН в развитых странах встречается всё реже.
Стрептококк может также вызывать ангину, тонзиллит и скарлатину, поэтому эти заболевания часто предшествуют острому гломерулонефриту. Однако в большинстве случаев точную причину гломерулонефрита установить не удаётся: в посевах мочи и крови возбудитель отсутствует, в истории болезни нет перенесённых инфекций [1] [3] [11] [15] .
Помимо стрептококка, к развитию острого гломерулонефрита могут приводить:
- токсические факторы — отравление свинцом и ртутью, употребление органических растворителей и алкоголя, приём некоторых лекарств (Амикацина, рентгеноконтрастных препаратов);
- другие инфекции — бактерии (стафилококк, энтерококк, диплококк, бледная трепонема и др.), вирусы (цитомегаловирус, вирусы простого герпеса, гепатита В, Эпштейна — Барр, коронавирус).
Острый гломерулонефрит может около трёх недель протекать без симптомов [2] [4] [10] . Затем развивается характерный острый нефритический синдром, включающий основные проявления болезни:
- отёки;
- гематурию (кровь в моче);
- гипертонию [12][15] .
Отёки возникают у 80-90 % пациентов [16] . Появление отёков при остром гломерулонефрите вызвано задержкой натрия и замедленной фильтрацией крови в клубочках [16] . У детей отёки распространяются по всему телу, у взрослых, как правило, отекают только ноги и лицо. В 10-50 % случаев отёки сопровождаются тупыми болями в пояснице, которые возникают из-за воспаления и растяжения капсулы почки.
Моча приобретает красный оттенок и становится цвета «мясных помоев» у 30-50 % больных [16] . Видимое окрашивание мочи сгустками крови называют макрогематурией. У остальных пациентов развивается микрогематурия — в моче присутствует небольшое количество эритроцитов, но кровь в моче не видна. Гематурия — это самое типичное проявления болезни, она может быть единственным симптомом гломерулонефрита и сохраняться в течение нескольких месяцев после перенесённого заболевания.

Гипертония развивается у 50-90 % пациентов, из них более чем у 75 % больных давление сильно повышено [16] [19] . Гипертония может протекать бессимптомно или проявляться головными болями. Основные причины высокого давления при остром гломерулонефрите — это увеличение объёма циркулирующей крови, связанное с задержкой жидкости и натрия, а также повышение сердечного выброса и периферического сосудистого сопротивления.
С первых дней болезни уменьшается объём выделяемой мочи (диурез). При лечении он восстанавливается через 4-7 дней, после чего исчезают отёки и нормализуется артериальное давление (гипертония обычно наиболее выражена в разгар заболевания [16] ). Однако ещё в течение полугода отдельные симптомы могут сохраняться.
Острый постстрептококковый гломерулонефрит может протекать в двух формах:
- циклически — типичный вариант;
- ациклически — только с одним симптомом, атипичный вариант.
Циклическое течение
Болезнь начинается остро: состояние резко ухудшается, появляется выраженная слабость, тошнота, рвота и повышается температура.
Затем развивается нефритический синдром:
- с почечными симптомами — уменьшается объём выделенной мочи, в ней появляется кровь, белок и цилиндрические тельца;
- с внепочечными симптомами — болит голова, живот или поясница, возникает слабость, астения, снижается или пропадает аппетит.
Пациент, как правило, вспоминает, что этим симптомам предшествовала ангина, тонзиллит, скарлатина или другая бактериальная инфекция. Скрытый период после ангины и обострения хронического тонзиллита составляет 2-4 недели, после стрептодермии — 8-12 недель.
Ациклическое течение
Снижается диурез, появляется гематурия, но внепочечные симптомы не возникают, поэтому заболевание обычно переносится легче. Предугадать, как будет развиваться гломерулонефрит, невозможно — течение болезни зависит от состояния иммунной системы.
Патогенез острого гломерулонефрита
Известно, что гломерулонефрит развивается под действием бактериальных и токсических факторов, однако патогенез заболевания до конца не изучен. Выделяют три основных механизма развития болезни: иммунный, гемодинамический и метаболический. Наибольшее значение имеет первый фактор [16] [18] [19] [21] .
К иммунным механизмам развития гломерулонефрита относятся:
- образование иммунных комплексов в клубочках;
- захват клубочками циркулирующих иммунных комплексов;
- перекрёстная реакция между антигенами;
- прямая активации системы комплемента антигенами в клубочках [7][8][9] .
Рассмотрим эти механизмы более подробно на примере острого постстрептококкового гломерулонефрита (ОПСГН). Антиген нефритогенного, т. е. опасного для почек штамма, откладывается в клубочках, что запускает иммунные реакции.
Иммунная система состоит из гуморального и клеточного иммунитета. Клетки гуморального иммунитета — это B-лимфоциты, которые первыми встречают антигены. К антигенам относятся, например, вещества, которые содержатся в микроорганизмах или выделяются ими. Эти вещества организм рассматривает как чужеродные или потенциально опасные и начинает вырабатывать против них антитела. При остром гломерулонефрите клетки гуморального иммунитета вырабатывают нефритогенные антистрептококковые антитела. Эти антитела связываются с антигенами и образуются иммунные комплексы.

Затем активируется клеточный иммунитет. Его агенты — это макрофаги и Т-лимфоциты: Т-хелперы, Т-киллеры и Т-супрессоры [10] . При этом запускается система комплимента по классическому типу, из-за чего вырабатываются дополнительные медиаторы воспаления и привлекаются провоспалительные клетки. Система комплемента — это комплекс белков, которые защищают организм от действия чужеродных агентов. Из-за активации этой системы почечные клубочки начинают разрушаться [7] .
Повреждённые клетки вырабатывают провоспалительные цитокины: IL-1, IL-6, TNF-a, из-за чего клубочки пропитываются лейкоцитами и моноцитами, а макрофаги вызывают отёк тканей.
Стрептококковые М-белки и пирогенные экзотоксины (токсины, которые вызывают повышение температуры) выступают в качестве суперантигенов, т. е. могут массово активировать Т-лимфоциты, вырабатывающие провоспалительные цитокины. В активный период гломерулонефрита образуются специфические антитела и криоглобулины, что приводит к аутоиммунному воспалению [11] .
Согласно последним исследованиям, гломерулонефрит развивается из-за генетических нарушений Т-клеточного звена иммунитета [19] .
Классификация и стадии развития острого гломерулонефрита
По характеру течения гломерулонефрит бывает:
- острым;
- подострым (с бурным, часто злокачественным течением и развитием острой почечной недостаточности); .
По этиологическому фактору:
- Инфекционный — бактериальный, вирусный и паразитарный.
- Токсический — вызванный действием органических растворителей, лекарств, алкоголя, свинца и ртути.
- Гломерулонефриты при системных заболеваниях:
- Люпус-нефрит — осложнение системной красной волчанки.
- IgA-нефропатия — вид гломерулонефрита, который может длительно проявляться только микрогематурией, артериальное давление при этом не повышается. Макрогематурия развивается при присоединении респираторной инфекции или воспалении других слизистых оболочек.
- Пурпура Шенлейна — Геноха — воспаление мелких сосудов, проявляется геморрагической сыпью, артритом и болью в животе.
По морфологической картине:
- минимальные изменения;
- фокальный сегментарный гломерулосклероз;
- мембранозный гломерулонефрит (нефропатия);
- мезангиопролиферативный гломерулонефрит (IgA-нефропатия);
- мембранопролиферативный гломерулонефрит;
- полулунный гломерулонефрит;
- фибропластический гломерулонефрит (диффузный склероз) [4][10] .
Морфологические данные выявляются при биопсии почек. Их интерпретацией занимаются морфолог и клиницист.
Осложнения острого гломерулонефрита
Заболевание опасно следующими осложнениями:
- Острое почечное повреждение, острая или хроническая почечная недостаточность.
- Острая сердечная недостаточность — нарушается ритм сердца, его способность сокращаться и расслабляться, меняется степень напряжения сердечной мышцы перед и во время сокращения (преднагрузка и постнагрузка). Может возникать как у людей, страдающих болезнями сердца, так и у здоровых пациентов. Осложнение опасно для жизни и требует срочного лечения [13] .
- Энцефалопатия — накопление в головном мозге токсических органических кислот. Сопровождается неврологическими симптомами, уменьшить которые можно при помощи гемодиализа или перитонеального диализа. К ранним признакам уремической энцефалопатии относятся снижение внимания, быстрая утомляемость и апатия. В дальнейшем эти симптомы усиливаются, ухудшается память, возникает дезориентация в пространстве и неустойчивость настроения, нарушается режим сна и бодрствования [16][18] . — может возникать при беременности.
Без своевременной диагностики и лечения острого гломерулонефрита пациент может погибнуть [15] .
Диагностика острого гломерулонефрита
При подозрении на острый гломерулонефрит проводится лабораторная и инструментальная диагностика.
Лабораторная диагностика
- Общий анализ мочи. Для гломерулонефрита характерны:
- Гематурия (наличие крови в моче) — обязательный симптом для постановки диагноза «острый гломерулонефрит». Микрогематурия может сохраняться в течение многих месяцев после перенесённого заболевания.
- Протеинурия (наличие белка в моче) — чаще всего при заболевании возникает протеинурия лёгкой степени тяжести.
- Лейкоцитурия (более шести лейкоцитов в поле зрения) — встречается примерно у половины пациентов, присутствует в течение 10-14 дней [16] .
- Цилиндрурия — в моче выявляются эритроцитарные, гранулярные и лейкоцитарные цилиндры.
- Общий анализ крови — повышается уровень лейкоцитов, нейтрофилов и эозинофилов, наблюдается сдвиг лейкоцитарной формулы влево, увеличивается СОЭ и уменьшается концентрация гемоглобина.
- Биохимия крови — при гломерулонефрите повышен уровень креатинина и мочевины, снижается скорость клубочковой фильтрации (СКФ), т. е. нарушается работа почек. В большинстве случаев эти изменения необратимы, некоторым больным может потребоваться диализная терапия.
- Серологическое исследование крови на антистрептолизин-О — при остром постстрептококковом гломерулонефрите повышен уровень антистрептококковых антител.
- Коагулограмма — при болезни сокращается протромбиновое время, повышается протромбиновый индекс, снижается содержание антитромбина III и угнетается фибринолитическая активность, т. е. способность крови растворять тромбы.
Инструментальная диагностика
- Ультразвуковая диагностика почек — оцениваются размеры почек, структурные нарушения, наличие пороков и аномалий развития. Исследование проводится для дифференциальной диагностики с другими болезнями почек.
- Биопсия почек — показана в тех случаях, когда назначенная терапия оказалась неэффективной. С помощью биопсии можно уточнить тип гломерулонефрита, определить прогноз и тактику лечения [15] . Показания к биопсии: отягощённая наследственность по заболеваниям почек, нетипичные симптомы, высокая концентрация белка в моче и прогрессирующее снижение СКФ.
Основным критерием диагностики гломерулонефритов является морфологическая картина (т. е. состояние клеток и тканей почечных клубочков), так как она индивидуальна для каждого типа заболевания [16] [18] [19] [20] .
Дифференциальная диагностика острого и хронического гломерулонефритов
При лечении острого гломерулонефрита применяют немедикаментозную, антибактериальную, симптоматическую и иммуносупрессивную терапию. В тяжёлых случаях может потребоваться заместительная терапия.
Лечение может проходить как амбулаторно, так и в больнице.
Показания к госпитализации:
- возраст до 18 лет;
- нарушение работы почек (как с уменьшением диуреза, так и без этого симптома);
- сохраняющаяся или нарастающая гипертония;
- признаки острой сердечной недостаточности;
- нефротический синдром.
Немедикаментозная терапия
- При тяжёлом течении болезни показаны покой и постельный режим. К признакам тяжёлого течения относятся кровь в моче, заметная визуально, отёки по всему телу и симптомы сердечной недостаточности.
- Следует потреблять до 1-2 г соли в сутки. Если появились отёки, особенно если они нарастают, нужно сократить потребление соли до 0,2-0,3 г в сутки [16] .
- При снижении функции почек рекомендуется есть менее 0,5 г/кг белка в сутки. Его количество нужно сократить за счёт животных белков, сохранив при этом калорийность рациона и содержание витаминов [15] .
- В острый период болезни следует меньше пить, необходимый объём жидкости рассчитывают с учётом диуреза за предыдущий день + 300 мл.
Диета и постельный режим помогают жидкости не задерживаться в организме. Питание и режим можно скорректировать после того, как исчезнут отёки и давление придёт в норму [16] .
Антибактериальная терапия
Всем пациентам с подтверждённой стрептококковой инфекцией (положительные результаты посевов с кожи, зева и высокие титры антистрептококковых антител в крови) рекомендуется проводить антибактериальную терапию. Её назначают с учётом чувствительности возбудителя. Наиболее часто применяются препараты пенициллинового ряда. Макролиды II и III поколений являются препаратами второй линии терапии [16] .
Симптоматическая терапия
Чтобы уменьшить отёки и предотвратить связанные с ними осложнения, назначаются мочегонные средства (диуретики) [16] . Для снижения артериального давления применяются блокаторы медленных кальциевых каналов. При выраженных изменениях со стороны крови, например повышенной свёртываемости, врач может назначить антикоагулянты. Продолжительность терапии зависит от различных факторов: тяжести заболевания, длительности почечных изменений по данным анализов, возраста и т. д.
Иммуносупрессивная терапия
При быстром развитии заболевания, сильных отёках и артериальном давлении выше 130/90 мм рт. ст. назначаются глюкокортикостероиды.
Заместительная почечная терапия
Заместительная терапия показана при развитии почечной недостаточности [15] .
Основные методы заместительной терапии:
- гемодиализ;
- перитонеальный диализ;
- трансплантация почки.

Прогноз в большинстве случаев благоприятный [7] . Как правило, отёки уменьшаются в течение 10 дней, уровень креатинина в сыворотке нормализуется за 3-4 недели [16] .
Среди детей осложнения встречаются редко. У пожилых пациентов может развиться острая сердечная и почечная недостаточность [14] . Тяжёлая почечная недостаточность возникает менее чем у 1 % больных [16] [18] .
Большинство пациентов полностью выздоравливают в течение 1-2 лет. В это период нужно соблюдать диету, терапия показана только при ухудшении клинических и лабораторных показателей.
Критический период после перенесённого острого гломерулонефрита составляет 1,5-2 месяца. В это время часто возникают рецидивы. Если симптомы сохраняются более полугода, такое течение называется затяжным. Симптомы, которые не проходят более года, указывают на развитие хронического гломерулонефрита.
Профилактика острого гломерулонефрита
Чтобы предотвратить развитие гломерулонефрита, нужно своевременно выявлять и лечить хронические заболевания. Для этого рекомендуется раз в год проходить осмотр у стоматолога, оториноларинголога и гинеколога.
Читайте также:
- Развитие и морфогенез глазного поля
- Головной мозг при болезни Альцгеймера: нарушение функции гиппокампа
- Аллергические реакции, вызванные физическими упражнениями
- Укладка при рентгенограмме плечевого сустава в косой ПЗ проекции (метод Грэши)
- Гидроцефалия после субарахноидального кровоизлияния. Факторы риска
