Пример метахронного рака ЖКТ. Сочетание рака губы и желудка
Добавил пользователь Валентин П. Обновлено: 21.01.2026
Ростовский научно-исследовательский онкологический институт Минздрава РФ
Ростовский научно-исследовательский онкологический институт, Ростов-на-Дону, Россия
ФГБУ «Ростовский научно-исследовательский онкологический институт» Минздрава России, Ростов-на-Дону, Россия
Первично-множественный колоректальный рак: клинические аспекты
Резюме Цель исследования. Определить некоторые клинические особенности синхронного и метахронного колоректального рака (КРР). Материалы и методы. Объектом исследования послужили данные о 150 больных первично-множественным КРР T1-4N0-2M0-1. Проведен анализ клинических, биологических, морфологических особенностей синхронных и метахронных опухолей. Результаты. Первично-множественные опухоли составили 6,01% от всех форм КРР. Преобладал синхронный КРР (63,75%) с локализацией опухоли в сигмовидной и прямой кишке. Синхронные колоректальные опухоли у женщин чаще сочетались с раком молочной железы, метахронные выявлялись после лечения опухолей половых органов. У мужчин синхронные колоректальные опухоли чаще сочетались с раком почки, метахронные выявлялись после лечения рака желудка. Заключение. Выявленные особенности первично-множественных колоректальных опухолей возможно учитывать в программах как первичной диагностики, так и диспансерного наблюдения после лечения больных со злокачественными опухолями, что позволит улучшить раннее выявление и результаты лечения онкологических больных.
КРР - колоректальный рак
МКО - метахронная колоректальная опухоль
Проблема колоректального рака (КРР) на протяжении нескольких десятилетий продолжает оставаться актуальной, что обусловлено как ростом заболеваемости, так и прогрессивными достижениями в лечении [1]. Наряду с увеличением общей онкологической заболеваемости наблюдается увеличение заболеваемости первично-множественными опухолями толстой и прямой кишки [2], которые в настоящее время составляют 17% от всех первично-множественных злокачественных новообразований и являются одной из наиболее частых локализаций первично-множественных злокачественных опухолей после первично-множественного рака кожи [3, 4].
В настоящее время проводится изучение как клинических, так и онкобиологических аспектов первичной множественности опухолей толстой и прямой кишки 6, тем не менее многие аспекты в этой проблеме остаются открытыми, что и побудило нас коснуться некоторых вопросов первично-множественного КРР.
Цель исследования: определить некоторые клинические особенности синхронного и метахронного КРР.
Материалы и методы
Из 2497 больных КРР T1-4N0-M0-1, подвергшихся хирургическому лечению в клинике ФГБУ «РНИОИ» МЗ РФ за последние 5 лет, первично-множественный рак выявлен у 150 (6,01%), данные о которых мы и использовали для анализа. Статистическую обработку результатов выполняли с применением пакетов программ Microsoft Excel 2010 и Statistica 8.0. Оценку различий проводили с использованием критерия χ 2 , статистически значимыми считали различия при р
Результаты
Анализ клинических проявлений первично-множественного КРР показал, что отдельные симптомы многообразны и соответствуют таковым при одиночной опухоли толстой или прямой кишки. Известно, что при локализации опухоли в правой половине ободочной кишки это чаще всего хроническая анемия, нарушение общего состояния (слабость, похудание), кишечный дискомфорт (снижение аппетита, чувство тяжести в верхней половине живота, иногда рвота через несколько часов после еды), боли в животе и наличие пальпируемой опухоли. При локализации опухоли в левой половине ободочной кишки преобладают: кишечные расстройства (запоры, поносы и их чередование), патологические выделения (кровь, слизь) при дефекации. При локализации опухоли в прямой кишке основными симптомами являются тенезмы, выделение крови и слизи при дефекации, боли в прямой кишке.
При синхронных колоректальных опухолях наблюдаются симптомы, соответствующие локализации опухоли в кишке. Так, анемия в течение нескольких лет, пальпируемая опухоль в правой подвздошной области и тенезмы свидетельствуют о синхронной опухоли слепой и прямой кишки. Оценка клинической картины заболевания с обязательным обследованием всех отделов толстой и прямой кишки позволят выявить синхронный КРР и избежать диагностических ошибок. В большинстве случаев нераспознанной синхронная колоректальная опухоль остается в случае, если в связи со стенозирующим характером дистальной опухоли эндоскоп не проходит в проксимальные отделы кишки и не позволяет произвести их осмотр. Об этом следует помнить, и в таких случаях производить дополнительное обследование вышележащих отделов толстой кишки (это может быть исследование пассажа бария по кишке, спиральная рентгеновская компьютерная томография органов брюшной полости и малого таза с пероральным контрастированием).
Следует отметить возможность развития одновременно опухоли колоректальной локализации и других органов. В этом плане важным является наличие в клинической картине симптомов, не характерных для КРР, даже если диагноз уже установлен. При этом следует продолжить обследование больного для исключения опухоли другой локализации. Анализ преимущественного поражения других органов синхронным раком будет произведен далее.
В случае метахронного развития опухолей как толстой и прямой кишки, так и других органов после излечения КРР диагностика не вызывает особых трудностей. Это связано с регулярной диспансеризацией и обследованием излеченных больных, приводящей к своевременной постановке диагноза.
Оценка частоты проявления симптомов заболевания показала, что при одиночном КРР преобладали боли (60%), кровь в кале (56,7%) и запоры (46,7%). При синхронных колоректальных опухолях наиболее частыми симптомами были боль (56,7%), слабость (53,3%) и похудание (40%). При метахронном КРР в клинической картине преобладали слабость (63,6%) и боль (56,7%) (табл. 1).
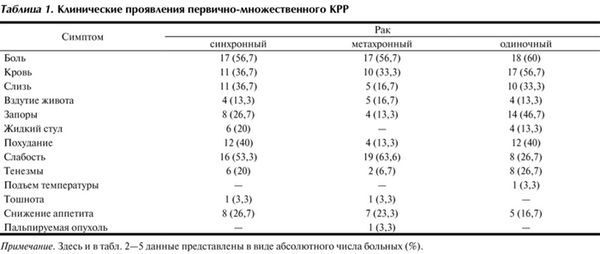
Таблица 1. Клинические проявления первично-множественного КРР Примечание. Здесь и в табл. 2-5 данные представлены в виде абсолютного числа больных (%).
В нашем исследовании время от появления первых клинических симптомов до момента обращения в специализированный онкологический стационар у больных одиночным раком составило преимущественно 6-12 мес (40% больных), а первично-множественным раком - 2-3 мес (48,3% больных).
Среди больных первично-множественным КРР синхронные и метахронные опухоли, локализующиеся только в толстой и прямой кишке, выявлены у 80 (53,3%). В этой группе больных преобладал синхронный КРР - 51 (63,75%) больной. Средний возраст пациентов составил 62,9 года. Преобладали мужчины - 32 (62,75%), средний возраст 63,2 года, женщин 19 (37,25%), средний возраст 62,5 года. Локализация синхронных опухолей в толстой и прямой кишке представлена в табл. 2. Согласно представленным данным синхронные опухоли преимущественно локализовались в сигмовидной (у 32 больных, 62,75%) и прямой кишке (у 29 больных, 56,86%). При этом сочетание опухолей в прямой и сигмовидной кишке выявлено у (35,29%). Половые различия по локализации синхронных опухолей в толстой и прямой кишке отсутствовали.

Таблица 2. Локализация синхронных опухолей в толстой и прямой кишке Примечание. Здесь и в табл. 3-5 * - различия между подгруппами достоверны (р<0,05).
У 34 (66,67%) мужчин и женщин распространение синхронных колоректальных опухолей ограничено только кишкой, без регионарных и отдаленных метастазов. Опухоли с регионарными метастазами имелись у 11 (21,57%) больных, с отдаленными - у 6 (11,76%). Распределение синхронных колоректальных опухолей по гистологической структуре свидетельствует о преобладании синхронных умереннодифференцированных аденокарцином (у 25, 49,02%), в основном у мужчин (у 17, 53,13%). У женщин часто встречались и слизеобразующие аденокарциномы (у 6, 31,58%).
Таким образом, синхронные опухоли составили 34% от всего первично-множественного КРР. Средний возраст больных достигал 62,9 года. Среди заболевших преобладали мужчины (62,75%). Синхронные опухоли преимущественно локализовались в сигмовидной (62,75%) и прямой кишке (56,86%), представлены в основном умереннодифференцированными аденокарциномами (49,02%), без регионарных и отдаленных метастазов (66,67%).
Метахронный КРР среди первично-множественного рака с локализацией опухолей только в толстой и прямой кишке выявлен у 29 (36,25%) больных (средний возраст 64,7 года). В этой группе было 16 (55,17%) женщин (средний возраст 66,9 года). Метахронная колоректальная опухоль (МКО) выявлена у них в среднем через 8,3 года после выявления первой опухоли. Среди больных метахронным первично-множественным КРР было 13 (44,83%) мужчин (средний возраст 62,5 года), метахронная опухоль выявлена у них в среднем через 4,5 года после первой опухоли.
Данные по локализации метахронных опухолей в толстой и прямой кишке отражены в табл. 3, представляющей распределение по локализации опухоли в следующем порядке: прямая кишка (51,72%, 15 больных), сигмовидная и правая половина ободочной кишки (по 48,28%, 14 больных), левая половина ободочной кишки (37,93%, 11 больных). В группе больных метахронным первично-множественным КРР наблюдались половые различия по локализации опухоли. Так, у женщин метахронные опухоли чаще локализовались в правой половине ободочной кишки - у 9 (56,25%) и прямой кишке - у 8 (50%). У мужчин МКО преимущественно локализовались в прямой и сигмовидной кишке - по 7 (53,85%) больных.

Таблица 3. Локализация метахронных опухолей в толстой и прямой кишке
У 14 (48,28%) больных распространение МКО ограничено только кишкой, без регионарных и отдаленных метастазов. Статистически значимых половых различий МКО по стадии TNM мы не наблюдали. Распределение МКО по гистологической структуре свидетельствует о значительном преобладании метахронных умереннодифференцированных аденокарцином - у 22 (75,86%) больных, как у мужчин, так и у женщин.
Итак, метахронный КРР составил 19,33% от всего первично-множественного рака толстой и прямой кишки. Средний возраст больных достигал 69,9 года, женщины были на 4 года старше мужчин. Среди заболевших было одинаковое число мужчин и женщин. Интервал между первой и последующей колоректальной опухолью у женщин в 2 раза больше (8,31 года), чем у мужчин (4,5 года). Метахронные опухоли у женщин преимущественно локализовались в правой половине ободочной кишки (56,25%) и прямой кишке (50%), у мужчин - в прямой и сигмовидной кишке (по 53,85%). МКО представлены в основном умереннодифференцированными аденокарциномами (75,86%), без регионарных и отдаленных метастазов (48,28%).
Среди больных первично-множественным КРР синхронные и метахронные опухоли, локализующиеся помимо толстой или прямой кишки, также в других органах, выявлены у 70 (46,7%). В этой группе синхронный первично-множественный рак наблюдался у 26 (37,14%) больных. Средний возраст пациентов составил 67,1 года. Женщин и мужчин было поровну - по 13 больных. Женщины на 7 лет моложе мужчин (63,6 и 70,5 года соответственно).
Локализация синхронных первично-множественных опухолей представлена в табл. 4, из которой видно, что синхронные колоректальные опухоли у женщин чаще сочетались с опухолями гениталий - у 8 (61,5%), причем у 5 - с раком молочной железы. У половины 7 (53,8%) мужчин синхронный КРР сочетался с опухолями мочевыделительной системы, причем у 6 из них - с раком почки.
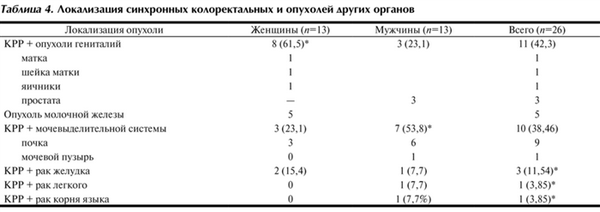
Таблица 4. Локализация синхронных колоректальных и опухолей других органов
У 65,4% больных опухоль была местно-распространенной, с наличием регионарных метастазов у одной из опухолей. Статистически значимых половых различий по стадии TNM синхронных колоректальных опухолей и других локализаций рака мы не наблюдали.
Распределение синхронных колоректальных опухолей при наличии и другой локализации рака по гистологической структуре свидетельствует о значительном преобладании синхронных умереннодифференцированных аденокарцином (80,8%) у мужчин и женщин.
Итак, синхронный КРР с другими локализациями опухолей составил лишь 17,33% от всего первично-множественного рака толстой и прямой кишки. Средний возраст больных достигал 67,1 года, женщины были на 7 лет моложе мужчин. Среди заболевших было одинаковое число женщин и мужчин. Синхронные колоректальные опухоли у женщин чаще сочетались с раком молочной железы. У мужчин синхронный КРР чаще сочетался с раком почки. Синхронные колоректальные опухоли представлены в основном умереннодифференцированными аденокарциномами (80,8%), местно-распространенными, с наличием регионарных метастазов (65,4%).
Метахронный КРР после лечения первой опухоли, локализующейся в других органах, составил 44 (29,33%) случая среди первично-множественных КРР и 62,86% среди первично-множественного КРР, сочетающегося с опухолями других органов. Средний возраст больных достигал 65,1 года. В этой группе больных было 24 (54,55%) женщины (средний возраст 61,3 года) и 20 (45,45%) мужчин (средний возраст 69 лет) на 8 лет старше женщин. Среднее время выявления МКО после лечения опухоли другой локализации у женщин составило 5,7 года, у мужчин - 4,4 года.
Локализация метахронных первично-множественных опухолей показана в табл. 5. Согласно представленным данным МКО у женщин чаще сочетались с опухолями половых органов - у 19 (79,23%), преимущественно матки и молочной железы. У мужчин метахронный КРР чаще сочетался с раком желудка - у 11 (55%).
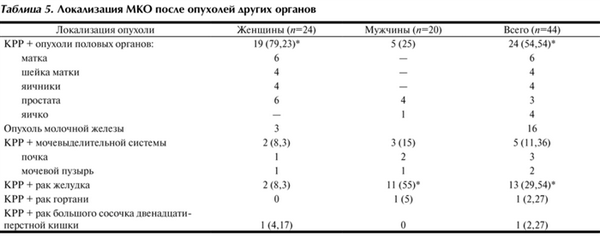
Таблица 5. Локализация МКО после опухолей других органов
28 (63,6%) больных имели местно-распространенную форму МКО и других локализаций рака, без отдаленных метастазов. Половые различия при этом отсутствовали.
Распределение МКО при наличии и другой локализации рака свидетельствует о значительном преобладании метахронных умеренно дифференцированных аденокарцином у мужчин и женщин - 33 (75%) больных.
Итак, метахронный КРР с другими локализациями опухолей составил 29,33% от всего первично-множественного рака толстой и прямой кишки. Средний возраст больных достигал 65,1 года, женщины на 8 лет моложе мужчин. Среди заболевших одинаковое число женщин и мужчин. Среднее время выявления МКО после лечения опухоли другой локализации у женщин составило 5,7 года, у мужчин - 4,4 года. МКО у женщин преимущественно выявлялись после лечения опухолей половых органов (79,23%). У мужчин метахронный КРР чаще наблюдался после лечения рака желудка (55%). МКО представлены в основном умереннодифференцированными аденокарциномами (75%), местно-распространенными, без отдаленных метастазов (63,64%).
Заключение
Клиническая картина первично-множественного КРР характеризуется наличием симптомов, не свойственных только одной локализации рака. Это обусловливает необходимость расширения диагностического поиска для исключения синхронной опухоли. При этом более выраженное клиническое проявление симптомов первично-множественного заболевания приводит к уменьшению до 3 мес сроков от появления клинической картины недуга до обращения за специализированной помощью у большинства больных (50% больных синхронным и 70% больных метахронным раком). В этот срок при одиночном КРР обращаются лишь 30% больных.
Диагностика метахронных опухолей облегчается наличием диспансеризации и регулярного обследования больных после излечения первой опухоли.
Первично-множественный КРР с локализацией опухолей только в толстой и прямой кишке составил 53,33% от всех форм первично-множественного КРР. В этой группе больных преобладал синхронный КРР (63,75%), которым заболевают чаще в 62,9 года, несколько чаще мужчины (62,75%). Синхронные опухоли преимущественно локализовались в сигмовидной (62,75%) и прямой кишке (56,86%). Средний возраст больных при выявлении МКО был старше, чем синхронных - 69,9 года. Интервал между выявлением первой и последующей колоректальной опухоли у женщин был в 2 раза больше, чем у мужчин (8,3 и 4,5 года соответственно). Метахронные опухоли у женщин преимущественно локализовались в правой половине ободочной кишки (56,25%) и прямой кишке (50%), у мужчин - в прямой и сигмовидной кишке (по 53,85%).
Если КРР выявлялся одновременно с опухолями других органов, то средний возраст больных (67,1 года) был на 4,2 года больше, чем при выявлении синхронного КРР, а женщины при выявлении опухолей на 7 лет моложе мужчин. Синхронные колоректальные опухоли у женщин чаще сочетались с раком молочной железы, у мужчин - с раком почки. Выявление колоректальной опухоли после лечения опухоли другой локализации наблюдается примерно в том же возрасте, что и синхронное (65,1 года), но несколько чаще, чем их одновременное выявление (62,86%). МКО у мужчин выявлялась в среднем через 4,4 г, чаще после лечения рака желудка (55%). У женщин колоректальная опухоль выявлялась в среднем через 5,7 года, преимущественно после лечения опухолей половых органов (79,17%).
Все первично-множественные колоректальные опухоли представлены в основном умереннодифференцированными аденокарциномами (как наиболее распространенного гистологического типа колоректальной опухоли), местно-распространенными, без отдаленных метастазов (возможно, в связи с тем что больные отобраны для хирургического лечения). Преобладание при первично-множественном КРР, сочетающемся с опухолями других органов, регионарных метастазов, возможно, свидетельствует о его более агрессивном течении по сравнению с другими видами первично-множественных колоректальных опухолей.
Выявленные особенности первично-множественных колоректальных опухолей можно учитывать в программах как первичной диагностики, так и диспансерного наблюдения после лечения больных со злокачественными опухолями, что позволит улучшить раннее выявление и результаты лечения больных с первично-множественными опухолями.
Рак желудка 4 стадии
Стадию рака желудка определяют по трем показателям, которые обозначаются буквами латинского алфавита:
- T (tumor) — размер первичной опухоли, глубина ее прорастания в стенку желудка и распространение на соседние ткани.
- N (nodes) — распространение раковых клеток в ближайшие (регионарные) лимфатические узлы.
- M (metastasis) — наличие метастазов, вторичных очагов, которые возникли в результате распространения раковых клеток с током крови или лимфы из желудка в другие органы.
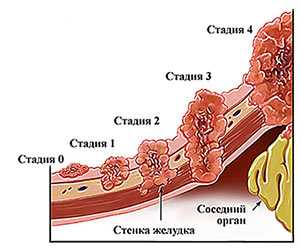
При раке желудка 4 стадии первичная опухоль может иметь любые размеры, прорастать в стенку желудка на любую глубину, распространяться или не распространяться в соседние органы, лимфатические узлы. Но всегда есть отдаленные метастазы. Это ключевой признак. [1,2,7]
В какие органы чаще всего метастазирует рак желудка?
Опухолевые клетки могут распространяться из желудка в другие органы разными способами:
- Рак может непосредственно прорастать в соседние органы. Чаще всего — в поджелудочную железу, реже — в поперечную ободочную кишку, левую долю печени.
- Иногда раковые клетки распространяются по поверхности брюшины — тонкой пленки из соединительной ткани, которая выстилает изнутри стенки брюшной полости и покрывает внутренние органы. При этом у женщин нередко обнаруживаются метастазы в яичниках (опухоль Крукенберга).
- Гематогенным путем (с током крови) рак желудка 4 стадии чаще всего распространяется в печень, реже — в легкие и кости.
- Лимфогенное распространение раковых клеток происходит вдоль печеночно-дуоденальной связки, чревного ствола, сосудов селезенки.
При раке желудка могут возникать специфические метастазы. Для них существуют специальные названия:
- Метастаз Вирхова — в лимфатическом узле, расположенном над ключицей.
- Метастаз сестры Марии Джозеф — в пупок.
- Метастазы Шницлера — в лимфатические узлы, расположенные вокруг прямой кишки.
- Метастазы Айриша — в лимфатические узлы, расположенные в подмышечной области.
Согласно статистике, рак желудка 4 стадии чаще всего метастазирует в печень (у 48% пациентов), брюшину (32%), легкие (15%), кости (12%). [3]
Симптомы
При раке желудка 4 стадии могут беспокоить такие неспецифические симптомы, как плохой аппетит и потеря веса, вплоть до сильного истощения (кахексии), дискомфорт, чувство тяжести, распирания и боль в животе, изжога, тошнота и рвота (иногда с кровью), запоры, примесь крови в стуле.
Специфические симптомы — это желудочное кровотечение при распаде опухоли и анемия из-за кровопотери. Поражение опухолевыми клетками брюшины приводит к асциту (скоплению жидкости в брюшной полости). Также характерны зловонный стул черного цвета и рвота массами, напоминающими кофейную гущу.
Рак желудка длительно не дает о себе знать. На ранних стадиях многие люди не испытывают симптомов и не знают, что больны. У четырех из пяти больных диагноз устанавливают, когда опухоль уже успевает распространиться на другие органы.
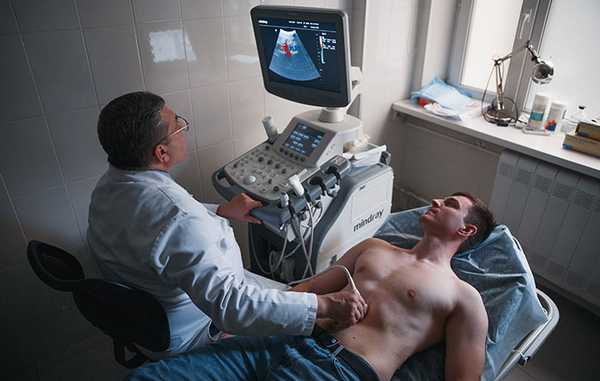
Люди, имеющие повышенный риск рака желудка, должны регулярно проходить скрининг — гастроскопию. Это помогает диагностировать опухоль на ранних стадиях. [4,6]
Методы диагностики
При раке желудка 4 стадии применяют разные методы диагностики, они помогают выявить первичную опухоль и вторичные очаги в других органах:
- Эндоскопическое исследование (гастроскопия, ФГДС) помогает обнаружить патологические изменения на слизистой оболочке желудка.
- Эндоскопическое ультразвуковое исследование — по сути та же ФГДС, но на конце гастроскопа находится ультразвуковой датчик. Он может «просветить» соседние органы и лимфатические узлы через стенку желудка. Зачастую это намного информативнее, чем обычное УЗИ.
- Биопсия. Исследование, во время которого врач получает образец опухолевой ткани и отправляет на анализ в лабораторию. На данный момент биопсию можно назвать самым точным методом диагностики онкозаболеваний. Исследовать можно ткань желудка, лимфатических узлов, других органов.
- Рентгенография с контрастным усилением. Этот метод диагностики используется довольно редко, так как гастроскопия более информативна (к тому же, во время нее можно взять материал для биопсии). Но рентгенография — менее инвазивный метод, во время нее в желудок не вводят никаких инструментов. Иногда это преимущество важно. Суть метода в том, что пациенту дают выпить раствор непроницаемого для рентгеновских лучей сульфата бария, затем делают снимки.
- Компьютерная томография. Более «продвинутая» разновидность рентгенографии, позволяет получить послойные снимки-«срезы» всего тела, на которых будет видна опухоль желудка и очаги в других органах.
- МРТ — в каком-то смысле аналог компьютерной томографии, но во время этого исследования вместо рентгеновских лучей используют мощное магнитное поле. Это безопаснее. МРТ лучше «видит» мягкие ткани. Минус метода в том, что он более сложен, нужен дорогой аппарат, который есть далеко не во всех клиниках.
- Позитронно-эмиссионная томография (ПЭТ). Идеальна для поиска метастазов, которые не могут обнаружить другие методы диагностики. В организм вводят безопасный радиоактивный сахар. Он накапливается в раковых клетках, так как они активно потребляют энергию, и делает их видимыми на специальных снимках.
- Рентгенография грудной клетки. Применяется для поиска метастазов в легких. [1,6]
Современные методы лечения
Лечение при раке желудка четвертой стадии преследует две цели:
- Сократить размеры опухоли, замедлить ее прогрессирование.
- Устранить симптомы: боль, анемию, нарушение проходимости желудка, асцит. [5]

Хирургическое лечение
В случаях, когда операцию выполнить нельзя, можно провести стентирование желудка. В месте его соединения с пищеводом или двенадцатиперстной кишкой (в зависимости от локализации опухоли) с помощью эндоскопа устанавливают стент — полый каркас с металлической сетчатой стенкой. Иногда проводят эндоскопическую абляцию: через эндоскоп подают лазерный луч, который разрушает опухолевую ткань.
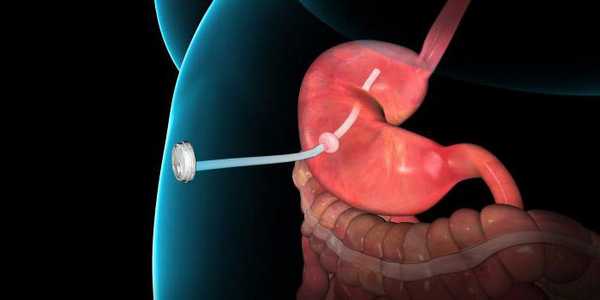
Химиотерапия и лучевая терапия
При раке желудка с метастазами проводят паллиативную химиотерапию и лучевую терапию. Их главная задача — уменьшить размеры опухоли и продлить жизнь пациента. Применяют разные комбинации химиопрепаратов:
- Эпирубицин + цисплатин + 5-фторурацил.
- Доцетаксел + цисплатин + 5-фторурацил.
- Иринотекан + цисплатин.
- Иринотекан + 5-фторурацил.
- Иринотекан + капецитабин.
- Оксалиплатин + 5-фторурацил.
- Оксалиплатин + капецитабин.
Комбинации из трех препаратов, а также химиотерапия в сочетании с лучевой терапией (химиолучевая терапия) более эффективны, но хуже переносятся, несут более высокий риск побочных эффектов. [1,5,10]
Таргетная терапия
Таргетные препараты могут быть эффективны в случаях, когда химиотерапия не помогает. Это современная группа противоопухолевых средств, они атакуют определенные молекулы-мишени, которые важны для роста опухолевой ткани. При раке желудка четвертой стадии применяют два таргетных препарата:
- Трастузумаб блокирует белок-рецептор HER2, который находится на поверхности раковых клеток и заставляет их размножаться. Активность этого белка повышена в каждой пятой злокачественной опухоли желудка (такой рак называют HER2-позитивным).
- Рамуцирумаб блокирует VEGF — белок, который вырабатывается раковыми клетками и стимулирует рост новых сосудов, снабжающих опухоль кислородом и питательными веществами.
Таргетные препараты применяют самостоятельно или в сочетании с химиопрепаратами. Они эффективны, когда раковые клетки обладают определенными молекулярно-генетическими особенностями, когда в них повышена активность соответствующего «вещества-мишени». [2,9]
Иммунотерапия
Иммунитет человека устроен очень сложно. В нем есть множество звеньев и всевозможных механизмов регуляции. Например, для того чтобы сдерживать себя от атаки на собственные здоровые ткани, иммунная система использует особые вещества — контрольные точки. Иногда их используют злокачественные опухоли, чтобы защититься от иммунной атаки. С этим помогают бороться современные лекарства, которые относятся к классу иммунопрепаратов и называются ингибиторами контрольных точек.

При раке желудка 4 стадии иногда эффективен ингибитор контрольных точек под названием пембролизумаб (Китруда). [8,9]
Лечение анемии
Кровотечение при раке желудка может привести к анемии — состоянию, при котором в крови снижается количество эритроцитов и гемоглобина. В результате ухудшается качество жизни, выживаемость. Приходится снижать дозы химиопрепаратов и сокращать продолжительность курсов химиотерапии, лечение становится менее эффективным.
С анемией при раке желудка 4 стадии борются с помощью препаратов железа, фолиевой кислоты, витамина B12, переливаний эритроцитарной массы. Существуют препараты-аналоги гормона эритропоэтина, который вырабатывается почками и активирует образование новых эритроцитов в красном костном мозге. Обеспечить организм дополнительным количеством железа помогают некоторые рекомендации относительно рациона питания. [2,9]
Лечение асцита при раке желудка 4 стадии
Асцит — скопление жидкости в брюшной полости — одно из самых частых осложнений рака желудка четвертой стадии. Это состояние возникает по двум причинам:
- Из-за метастазов рака в брюшину. При этом увеличивается проницаемость стенок кровеносных сосудов, жидкость из них в большем количестве поступает в брюшную полость. Работа лимфатических сосудов нарушается, они не могут выводить жидкость.
- Из-за метастазов в лимфатических узлах. Нарушается отток лимфы, лимфатические сосуды, которые в норме должны выводить жидкость из брюшной полости, больше не могут выполнять свою функцию.
При асците проводят лапароцентез: в стенке брюшной полости делают прокол и выводят через него лишнюю жидкость. Для того чтобы обеспечить постепенное выведение жидкости в течение некоторого времени, применяют специальные перитонеальные порт-системы. Уничтожать метастазы в брюшине помогает внутрибрюшинная химиотерапия, когда химиопрепарат вводят в брюшную полость. При любом из видов лечения необходима специальная диета и приём ряда препаратов, уменьшающих тошноту. [11,12]

Сколько живут с раком желудка 4 стадии?
Главный прогностический показатель при онкологических заболеваниях — пятилетняя выживаемость. Он обозначает процент пациентов, которые остались живы спустя 5 лет с момента диагностики и начала лечения злокачественной опухоли. Для IV стадии рака желудка этот показатель составляет 4%. В течение пяти лет 96 больных из 100 погибают, 4 остаются в живых. Но такая удручающая статистика — не повод сдаваться. Методы лечения совершенствуются, сегодня онкологи могут сделать намного больше, чем десятилетия назад. Пациенты, которым не помогают стандартные методы, могут принять участие в клинических испытаниях новых препаратов. [8,9]
Рак желудка с метастазами
Способность к метастазированию — одна из основных особенностей злокачественных опухолей, которая, собственно, и делает их смертельно опасными. Раковые клетки способны отделяться от первичного очага, проникать в кровеносные или лимфатические сосуды и распространяться в различные части тела, давая начало новым очагам.
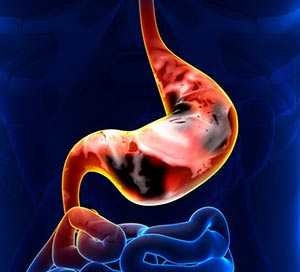
Течение большинства онкологических заболеваний принято делить на пять основных стадий, их обозначают цифрами 0, I, II, III, IV. Рак желудка с метастазами — это рак четвертой стадии. В классификации TNM буква M обозначает отдаленные метастазы. Она может принимать два значения:
- M0 — отдаленных метастазов нет, в таких случаях будет диагностирован рак желудка 0, I, II или III стадии.
- M1 — отдаленные метастазы имеются. В таких случаях диагностируют рак IV стадии.
Как часто диагностируют рак желудка с метастазами?
Так как на ранних стадиях опухоль не имеет симптомов, либо маскируется под другие заболевания (например, гастрит), зачастую она диагностируется на поздних стадиях. Примерно у четырех пациентов из пяти на момент постановки диагноза опухоль уже успела распространиться в организме. Это американская статистика, в России дела обстоят не лучше.
Так как с появлением отдаленных метастазов прогноз резко ухудшается, крайне актуален вопрос ранней диагностики рака желудка. Для этого применяются скрининговые исследования, в частности, гастроскопия. Наиболее удачный пример массового скрининга можно наблюдать в Японии: при высокой распространенности рака желудка в этой стране смертность от него ниже, чем во многих западных странах. Этого удалось добиться благодаря тому, что у многих больных опухоль обнаруживают на ранних стадиях.

Почему рак желудка метастазирует?
В процессе метастазирования принимают участие многие молекулярные механизмы, в современных знаниях о них остается еще немало пробелов. Известно, что злокачественные опухоли желудка развиваются из особых стволовых клеток. Некоторые подтипы стволовых клеток делают рак более склонным к метастазированию.
В общих чертах процесс метастазирования происходит следующим образом:
- Первичная опухоль в желудке постепенно растет и вторгается в окружающие ткани.
- Некоторые раковые клетки отделяются от первичного очага и проникают в кровеносные или лимфатические сосуды.
- С током крови или лимфы опухолевые клетки мигрируют в другие органы, оседают в мелких кровеносных сосудах, проникают через их стенки в окружающие ткани.
- Такое «путешествие» опасно для раковых клеток, многие из них погибают. Но, если условия оказываются благоприятными, раковая клетка закрепляется на новом месте и образует микроскопический вторичный очаг.
- Метастазировавшие клетки могут длительно, годами, оставаться неактивными. В определенный момент времени они могут начать активно размножаться, выделять вещества, которые стимулируют образование новых кровеносных сосудов, необходимых для роста опухолевой ткани.
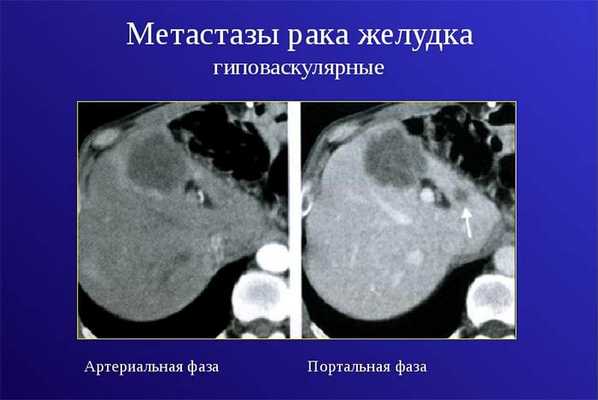
Даже после того как пациент прошел курс лечения, и наступила ремиссия, в организме могут остаться некоторые микроскопические метастазы. Со временем они способны стать причиной рецидива.
В какие органы метастазирует рак желудка?
В 2016 году группой ученых из Германии, Швеции и Финляндии было проведено исследование, по результатам которого были названы наиболее распространенные места локализации метастазов рака желудка:
- Печень — 48%.
- Брюшина — 32%.
- Легкие — 15%.
- Кости — 12%.
Локализация метастазов зависит от типа опухоли. Так, при раке кардии (места перехода пищевода в желудок) у мужчин опухолевые клетки чаще распространяются в легкие, нервную систему и кости. Опухоли в других частях органа склонны метастазировать в брюшину. Перстневидноклеточный рак чаще метастазирует в брюшину, кости и яичники, реже — в легкие и печень. В печени и брюшине обычно обнаруживают одиночные метастазы, в то время как метастазы в легких часто сочетаются с метастазами в печени.
Зачастую первые симптомы рака желудка появляются именно на поздних стадиях, когда уже произошло метастазирование. Симптомы зависят от того, в какой орган распространились раковые клетки:
- В брюшине: боли в животе, увеличение живота за счет скопления внутри жидкости (асцит), потеря аппетита, беспричинное сильное снижение веса.
- В печени: потеря аппетита и снижение веса, окрашивание мочи в темный цвет, увеличение живота, желтуха, боль в верхней части живота справа (под правым ребром), тошнота, рвота, повышенная потливость.
- В легких: боль в грудной клетке, упорный хронический кашель, примесь крови в мокроте, хрипы, одышка, снижение веса.
- В костях: боли, патологические (от небольшого усилия) переломы.
- В головном мозге: головные боли, тошнота, рвота, слабость, онемение в руках и ногах, нарушение координации движений, расстройства личности и поведения, речи, глотания, недержание мочи и стула.
Все эти симптомы могут быть вызваны другими заболеваниями.
Как диагностируют метастазы рака желудка?
Для поиска метастазов при раке желудка прибегают к следующим методам диагностики:
- Компьютерная томография хорошо обнаруживает метастазы в костях, но может также показать очаги и в мягких тканях.
- МРТ — безопасное исследование с применением магнитного поля, которое помогает обнаруживать метастазы в мягких тканях. В этом плане она точнее, чем КТ.
- Позитронно-эмиссионная томография — исследование, во время которого в организм вводят особую метку — безопасный радиоактивный сахар. Так как опухолевые клетки активно размножаются и нуждаются в большом количестве энергии, они накапливают этот сахар, благодаря чему становятся видны на снимках, сделанных специальным аппаратом. Существуют аппараты, с помощью которых можно одновременно выполнять ПЭТ и КТ, это помогает получить более детальную картину.
- Рентгенографию грудной клетки применяют для поиска метастазов в легких.
- Иногда возникает необходимость в диагностической лапароскопии — процедуре, во время которой врач делает прокол в стенке брюшной полости и вводит внутрь инструмент с видеокамерой (лапароскоп). Это помогает оценить степень распространения опухоли, обнаружить вторичные очаги в брюшине, внутренних органах.
Можно провести биопсию метастатического очага. При изучении ткани под микроскопом, в ней обнаруживают опухолевые клетки, характерные для рака желудка. Для того чтобы подобрать оптимальное лечение, проводят молекулярно-генетический анализ на некоторые вещества-маркеры:
- HER2 — рецептор на поверхности клеток, который стимулирует их размножение. При раке активность HER2 может быть повышена. — белок, который может взаимодействовать с иммунными клетками и подавлять их активность. Его относят к классу веществ, называемых контрольными точками.
Методы лечения
Если обнаружены отдаленные метастазы, ремиссия, как правило, становится невозможна. Лечение носит паллиативный характер, оно направлено на сокращение размеров и замедление роста опухоли, продление жизни пациента, борьбу с симптомами. Но рак с метастазами — это еще не приговор. Современные онкологи все чаще говорят о нем как о временно хроническом заболевании. На какой бы период времени ни удалось продлить жизнь пациента — это в любом случае небольшая победа.
Иногда удается удалить часть желудка с опухолью — провести субтотальную резекцию. Если такая операция невозможна, и опухоль создает препятствие для пищи, возможен один из следующих вариантов лечения:
- Шунтирование: верхнюю часть желудка соединяют отверстием с тонкой кишкой.
- Стентирование: в месте сужения устанавливают каркас с сетчатой стенкой, он помогает восстановить просвет желудка.
- Гастростомия или еюностомия: отверстие из желудка или тонкой кишки выводят на кожу, через него можно вводить пищу.
- Разрушение опухолевой ткани лазером с помощью эндоскопа, введенного через рот.
Химиотерапия
При раке желудка применяют препараты: 5-фторурацил, капецитабин, карбоплатин, цисплатин, доцетаксел, эпирубицин, иринотекан, оксалиплатин, паклитаксел. Их назначают в разных комбинациях.

Лучевая терапия
Облучение помогает сократить размеры опухоли, улучшить прохождение пищи, уменьшить боль. Применяются такие современные методы, как трехмерная конформная лучевая терапия, интенсивно-модулированная лучевая терапия. В них используются точные расчеты, которые помогают сконцентрировать излучение в области опухоли, минимально затрагивая здоровые ткани.
Иногда лучевую терапию сочетают с химиотерапией. Это помогает повысить эффективность лечения, но повышает риск серьезных побочных эффектов.
Таргетная терапия и иммунотерапия
При раке желудка с метастазами могут быть назначены некоторые таргетные препараты и иммунопрепараты:
- Если опухоль является HER2-позитивной, назначают трастузумаб (герцептин).
- Рамуцирумаб (цирамза) блокирует VEGF — вещество, которое раковые клетки синтезируют, чтобы стимулировать рост новых сосудов и обеспечить себя кислородом.
- Пембролизумаб (кейтруда) — иммунопрепарат, блокатор контрольной точки PD-L1. Он снимает блок с иммунных клеток, в результате чего те начинают атаковать опухолевую ткань.
Борьба с симптомами
На поздних стадиях онкологических заболеваний многих пациентов беспокоят сильные боли. Адекватное обезболивание помогает улучшить качество жизни. Применяются как ненаркотические, так и наркотические анальгетики. При желудочных кровотечениях развивается анемия. Если уровни эритроцитов и гемоглобина в крови сильно снижаются, приходится прибегать к переливанию эритроцитарной массы.
Важно оценивать нутритивный статус пациента. Если организм не получает нужных веществ, и проблему не удается решить с помощью диеты и гастростомии, назначают парентеральное питание: растворы питательных веществ вводят внутривенно, в обход пищеварительной системы.
Лечение метастазов в печени
Для борьбы с метастазами в печени при раке желудка существуют некоторые специальные методы:
- Интраартериальная химиотерапия, когда химиопрепарат вводят непосредственно в сосуд, питающий опухоль. При этом можно сильно увеличить дозировку и добиться положительного эффекта, не боясь серьезных побочных эффектов.
- Химиоэмболизация. В печеночную артерию вводят эмболизирующий препарат в сочетании с химиопрепаратом. Эмболизирующий препарат состоит из эмболов — микросфер, которые перекрывают просвет мелких сосудов и нарушают поступление к опухоли кислорода, питательных веществ.
- Радиочастотная абляция. В узел в печени вводят тонкий электрод в виде иглы и подают на него радиоволны, которые уничтожают раковые клетки. При необходимости процедуру можно повторять.
Лечение асцита
Асцит — скопление жидкости в брюшной полости — возникает при раке желудка в результате поражения метастазами печени и брюшины. Бороться с этим состоянием можно разными способами:
- Ограничение потребления жидкости и соли, мочегонные препараты.
- Лапароцентез — процедура, во время которой в брюшной стенке делают прокол и выводят избыток жидкости. Можно установить специальный перитонеальный катетер для оттока жидкости.
- Хирургические вмешательства, направленные на профилактику скопления жидкости в брюшной полости: оментогепатофренопексия, перитонеовенозный шунт, деперитонизация стенок брюшной полости.
- Внутрибрюшинная химиотерапия для борьбы с метастазами брюшины.
Прогноз при раке желудка с метастазами
Пятилетняя выживаемость на 4 стадии рака желудка составляет 5%. Это означает, что только пять из ста пациентов, у которых было диагностировано заболевание, останутся живы спустя 5 лет.
В среднем спустя 3 месяца с момента диагностики рака желудка с метастазами в живых остается половина пациентов. Прогноз хуже, если рак распространился в кости и печень: при таких метастазах половина пациентов погибает в течение 2 месяцев.
Карцинома
Один из самых распространенный типов раковых опухолей у людей - карцинома. Этот тип неоплазии, злокачественного роста, который зарождается в тканях, которые покрывают как внешние поверхности тела, так и внутренние полости. Этот вид онкологии относится к опухолям эпителиального происхождения.
Акции

Полное обследование на онкологические заболевания для мужчин и женщин.

Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.

«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!

Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Общие данные
В большинстве случаев эти типы опухолей, которые называют карциномой, происходят их клеток особых зародышевых листков - эктодермального либо энтодермального, образующих ткани тела в период эмбриогенеза (развития зародыша). Карцинома считается опухолью, тканью, которая, по предположению ученых, берет основу из эпителиальных (покровных) тканей, генетический материал которых повреждается или изменяется, в результате клетки подвергаются трансформации, начинают проявлять аномальные свойства и злокачественность.
Кроме того, будут характеризоваться как карцинома и те злокачественные опухоли, которые состоят из клеток, подвергшихся трансформации, которые имеют специфические характеристики на молекулярном, гистологическом и клеточном уровне, типичные для эпителиальной ткани.
По данным ВОЗ на долю карцином приходится ежегодно до 9,5 млн смертей. Лечение этих видов рака (карциномы) достаточно трудная задача, показатели выживаемости очень разнятся. Участки органов, часто поражаемые карциномами, включают:
- легкое;
- грудь;
- простату;
- толстую и прямую кишку;
- поджелудочную железу.
Причины возникновения карцином
Пока точные причины, по которой развиваются разные типы рака, включая карциному, не определены. Но ученые выделили ряд факторов, предрасполагающих к развитию патологии:
- гены (наследование определенных дефектов);
- влияние химических факторов (например, ароматические амины или углеводороды);
- физические влияния (ионизирующие излучения, ультрафиолет);
- биологические факторы (заражение определенными онкогенными вирусами - гепатит, папилломавирус);
- расстройства гормонального статуса - нарушение метаболизма определенных гормонов.
Типы карциномы, классификация
Хотя карциномы могут возникать во многих частях тела, наиболее распространены следующие типы карциномы:
- базальноклеточная карцинома;
- плоскоклеточная карцинома;
- почечно-клеточный рак;
- протоковая карцинома in situ (DCIS);
- инвазивный протоковый рак;
- аденокарцинома.
Основа классификации карцином - тип клеток и их локализация, а также стадии карциномы.
Карциномы могут распространяться на другие части тела или ограничиваться основным местом. Заболевание имеет различные формы, в том числе:
Важно знать также признаки опухоли в разных стадиях развития.
Стадия 1 - опухоль имеет размер не более 20 мм, нет метастазов в лимфатических узлах, в области внутренних органов.
Стадия 2 - опухоль не более 5 см в диаметре, в лимфоузлах определяются единичные метастазы.
Стадия 3 - опухоль превышает 50 мм диаметром, есть массивные метастазы в области лимфоузлов.
Стадия 4 - определяются отдаленные метастазы по всему организму.
Карцинома: симптомы
Врачи дают описание того, как выглядит тот или иной тип карциномы.
- Базально-клеточный рак часто выглядит так:
- открытые язвы;
- красные пятна;
- розовые наросты;
- блестящие шишки или шрамы.
Если выявлена базальноклеточная карцинома, вероятно, она возникла из-за слишком длительного пребывания на солнце. Возможно, было несколько серьезных солнечных ожогов или в течение жизни человек много времени проводил на солнце.
- Плоскоклеточная карцинома. Этот рак также может быть обнаружен на коже и в других частях тела, таких как выстилка клеток:
- определенных органов;
- пищеварительного тракта;
- дыхательных путей.
Когда плоскоклеточный рак развивается в коже, он часто обнаруживается на участках, подверженных воздействию солнца, таких как:
- лицо;
- уши;
- шея;
- губы;
- тыльная сторона ладони.
Плоскоклеточная карцинома, которая развивается на коже, имеет тенденцию к росту и распространению больше, чем рак базальных клеток. В редких случаях он может распространяться на лимфатические узлы.
На фоне карциномы возможен синдром интоксикации с лихорадкой, потерей аппетита и веса, слабостью, локальные изменения в области пораженной кожи, изменение цвета, уплотнение. Если поражен внутренний орган, страдают его функции.
Диагностика
Постановкой диагноза занимаются онкологи, они помимо оценки жалоб и осмотра, назначают целый ряд обследований. К ним относят:
- полное лабораторное обследование крови и мочи, включая анализ на онкомаркеры;
- эндоскопические исследования респираторного тракта и пищеварительной трубки;
- рентгенографию предполагаемого места опухоли для выявления повреждений окружающих тканей;
- КТ и МРТ для уточнения размера опухоли, определения метастазов;
- биопсию подозрительного очага для подтверждения типа рака Источник:
Скрининг и ранняя диагностика гепатоцеллюлярной карциномы. Кириенко В.Т., Зайцев И.А., Грушкевич В.В., Потий В.В. Актуальная инфектология, 2018. с. 70-76 .
Лечение карциномы варьируется в зависимости от типа, местоположения и степени заболевания, но может включать:
- Хирургию. В зависимости от типа рака, карциному можно лечить с помощью хирургического удаления раковой ткани, а также некоторых окружающих тканей. Минимально инвазивные хирургические методы лечения могут помочь сократить время заживления и снизить риск инфицирования после операции.
- Лучевую терапию. Может использоваться в сочетании с хирургическим вмешательством и/или химиотерапией. Передовые методы лучевой терапии используют визуализацию до и во время лечения целевых опухолей и разработаны, чтобы помочь сохранить здоровые ткани и окружающие органы.
- Химиотерапию. Она лечит карциному с помощью лекарств, предназначенных для уничтожения раковых клеток во всем теле или в определенной области. В некоторых случаях химиотерапия может использоваться в сочетании с другими видами лечения, такими как лучевая терапия или хирургическое вмешательство Источник:
Скрининг и ранняя диагностика гепатоцеллюлярной карциномы. Кириенко В.Т., Зайцев И.А., Грушкевич В.В., Потий В.В. Актуальная инфектология, 2018. с. 70-76 .
Карцинома: прогноз
Важно понимать, что означает диагноз. Это злокачественная опухоль, которую нужно лечить как можно раньше. При локальном поражении прогноз наиболее благоприятный, при метастазировании проводят поддерживающее лечение, которое улучшает качество жизни пациента.
Рекомендации
Для рака кожи основные рекомендации - это снизить облучение кожи УФ-лучами и оградить себя от влияния потенциальных канцерогенов. В целом, ведение здорового образа жизни с рациональным питанием, дозированными нагрузками помогает снизить риск онкологии.
Источники статьи:
- Инвазивные методы лечения гепатоцеллюлярной карциномы. Исмаилова Г., Енин Е., Каниев Ш., Таджибаев Т., Байшалова А., Шорманов А., Баймаханов Б. Клиническая медицина Казахстана, 2017. с. 11-13
- Скрининг и ранняя диагностика гепатоцеллюлярной карциномы. Кириенко В.Т., Зайцев И.А., Грушкевич В.В., Потий В.В. Актуальная инфектология, 2018. с. 70-76 Merkel cell carcinoma. Jürgen C. Becker, Andreas Stang, James A. DeCaprio, Lorenzo Cerroni, Celeste Lebbé, Michael Veness, Paul Nghiem Lobular Carcinoma in Situ. Hannah Y Wen, MD, PhD and Edi Brogi, MD, PhD
Михайлов Алексей Геннадьевич оперирующий онколог, врач высшей квалификационной категории, к.м.н. стаж: 21 год
Информация в статье предоставлена в справочных целях и не заменяет консультации квалифицированного специалиста. Не занимайтесь самолечением! При первых признаках заболевания необходимо обратиться к врачу.
Онкологические заболевания органов ЖКТ
Онкологические заболевания пищеварительного тракта - это общий термин для целой группы раковых поражений органов желудочно-кишечного тракта. В структуре заболеваемости онкология ЖКТ занимают лидирующие позиции, одинаково часто болеют как мужчины, так и женщины, преимущественно среднего и преклонного возраста.
- Рак слюнных желез
- Рак фатерова сосочка
- Рак толстой (ободочной) кишки
- Рак желчного пузыря
- Рак желчных протоков
- Рак пищевода
- Рак кишечника
- Рак двенадцатиперстной кишки
- Рак языка
- Рак гортани
- Рак поджелудочной железы
- Рак прямой кишки
- Рак анального канала
- Первичный рак печени
- Метастазы рака в печень
- Гастроинтестинальная стромальная опухоль ЖКТ
- Рак желудка
Рак пищеварительной системы включает в себя опухолевые образования:
- пищевода;
- поражения желудка (одни из самых частых);
- поджелудочной железы;
- тонкой и толстой кишки;
- поражения прямой кишки и области ануса;
- опухоли печени и желчного пузыря.
В эту группу также относятся стромальные и эндокринно-активные (гормональные) опухоли тканей, образующих пищеварительную систему.
Общие сведения
Рак пищеварительной системы - это злокачественные поражения пищеварительной трубки, а также желез, участвующих в процессе переваривания пищи. Этот вид онкологии опасен тем, что длительное время может никак себя не проявлять, повреждает большой объем тканей и способен к метастазированию в соседние и отдаленные органы. Раковые опухоли имеют разные размеры и локализацию, гистологический тип и форму, но приводят к нарушению работы ЖКТ и формированию осложнений.
В сравнении с другими типами рака выживаемость в течение 5 лет при поражениях ЖКТ ниже. Если это опухоли желудка, она составляет до 30%, для поражений кишечника - около 68%. При раке поджелудочной железы после установления диагноза только 9% людей живут более 5 лет. Летальность от рака пищеварительной системы вдвое превышает гибель от рака молочной железы и простаты вместе взятых Источник:
Е.М. Аксель
Статистика злокачественных
новообразований желудочно-кишечного тракта //
Сибирский онкологический журнал, 2017, №16(3), с.5-11 .
Проблема еще и в лечении данного типа рака. Обычно требуется комбинированный подход с удалением опухоли, а также лучевыми и химиотерапевтическими методами. Это достаточно тяжело для организма, поэтому нужно подбирать терапию индивидуально и тщательно, с учетом стадии и локализации рака.
Причины рака ЖКТ
Опухоли пищеварительной системы - достаточно разнородна группа рака. На сегодняшний день не выявлено единой конкретной причины, которая бы провоцировала рост злокачественных онкологических заболеваний желудочно-кишечного тракта. Выделяют влияние негативных внешних факторов в сочетании с генетической предрасположенностью человека к развитию раковых опухолей. Эти сочетания провоцируют трансформацию здоровых клеток пищеварительной системы в неопластические, которые дают начало раковой опухоли.
Общие факторы риска рака ЖКТ актуальны для большинства опухолей. К ним относятся:
- вредные привычки - курение, вейпинг и прием алкоголя в неумеренных дозах;
- старение организма;
- питание с высоким содержанием жиров, красителей, консервантов, химических соединений, канцерогенов;
- хронические воспалительные поражения органов (колиты, панкреатиты, гастрит);
- избыточный вес, ожирение, метаболический синдром;
- длительный и нерациональный прием некоторых лекарственных препаратов.
Для некоторых видов рака типичны и свои дополнительные провоцирующие факторы. Например, для рака желудка типично присутствие в слизистой органа Helicobacter pylori, кислотоустойчивых бактерий, повреждающих клетки. Для рака пищевода одним из провоцирующих факторов становится рефлюксная болезнь - постоянный заброс кислоты из желудка приводит к метаплазии эпителия и инициации рака. Для рака кишечника типичны длительные эпизоды интоксикаций на производстве и в быту. Также провокаторами рака толстой кишки могут стать язвенный колит и полипоз кишечника, пернициозная анемия.
Первые признаки, клинические симптомы
Для многих видов онкологии желудочно-кишечного тракта имеется рад специфичных признаков, отражающий нарушение функции. Общими характеристиками всех видов рака пищеварительных органов является их длительное, бессимптомное течение, на ранних стадиях пациенты не имеют жалоб, или жалобы носят общий характер. Серьезные проявления возникают, когда опухоли достигают больших размеров, разрушают стенку кишки, прорастают в соседние ткани, сдавливают протоки желез. Среди общих признаков выделяют:
- ощущение давления в области грудной клетки, брюшной полости, боль в спине;
- нарушение прохождения пищи по пищеводу, расстройство желчеотделения или выведения панкреатических ферментов;
- нарушения пищеварения с вздутием живота, спазмами, частицами непереваренной пищи в стуле;
- появление крови в стуле или изменения его окраски.
Обычно симптомы онкологических заболеваний ЖКТ возникают при наличии раковых опухолей большого размера, если они давят на кишку, печень или соседние органы брюшной полости. Возникает:
При поражении желудка типична кровавая рвота, анемия, черный стул. При поражении печени - желтуха, кожный зуд, обесцвечивание кала, чередование поносов и запоров, метеоризм.
Виды рака ЖКТ
Раковые опухоли ЖКТ дифференцируют в зависимости от локализации. К ним относятся опухолевые поражения:
- и глотки; ;
- разные виды рака желудка;
- поражения поджелудочной железы; и метастатические поражения печени, желчных протоков;
- тонкокишечный рак;
- поражения толстого кишечника; и анального отверстия;
- разные локализации гастроинтестинальных стромальных опухолей.
По форме раковой опухоли, с учетом ее внешнего вида, роста и состава клеток, выделяют несколько типов поражений:
- Язвенный. Опухоль прорастает в просвет органов, постепенно перекрывая его.
- Полипозный. Образуются узлы разного размера, выпирающие в просвет органа и перекрывающие его.
- Диффузный. Второе название - инфильтративный. Образуется под слизистой оболочкой, поражает все слои органа и растет в стороны от первичного очага. На поверхности пораженного участка могут образовываться язвы Источник:
Nathan M Krah , L Charles Murtaugh
Differentiation and Inflammation: 'Best Enemies' in
Gastrointestinal Carcinogenesis //
Trends Cancer . 2016 Dec;2(12):723-735.
doi: 10.1016/j.trecan.2016.11.005 .
По строению клеток, образующих раковые опухоли, выделяется несколько вариантов онкологии. На основе этих данных врач определяет агрессивность течения и прогнозы заболевания.
- Высокодифференцированная опухоль - раковые клетки очень похожи на здоровые, опухолевый рост медленный, метастазы возможны только в терминальных стадиях.
- Умеренно дифференцированная опухоль - клетки рака отличаются от здоровых, опухоль растет относительно медленно, метастазы возможны уже на 3 стадии процесса.
- Низкодифференцированная опухоль - клетки существенно отличаются от нормальных, типично быстрое увеличение размеров рака, метастазы поражают соседние ткани, лимфоузлы и отдаленные органы.
- Недифференцированная опухоль - клетки незрелые, появляются из слизистой, течение агрессивное со стремительным ростом образования, метастазы возможны на ранних стадиях, прогноз для жизни неблагоприятный.
Для выявления рака пищеварительного тракта используются лабораторные тесты и инструментальная диагностика. Во многом план обследования зависит от локализации, размеров и типа рака. У большинства опухолей ЖКТ не имеется специфических онкомаркеров, выявляющих рак на ранней стадии, поэтому врач учитывает первые признаки у взрослых, типичные жалобы и данные, полученные при визуализации.
Обычно опухоли впервые обнаруживают при эндоскопическом исследовании (фиброгастроскопия, колоноскопия, ректороманоскопия), дополняя исследование забором биопсии подозрительного участка с проведением гистологических, генетических и гистохимических тестов.
Лечение опухолей ЖКТ
Ведущий метод терапии при раке желудочно-кишечного тракта - это хирургическое удаление опухоли или ее части. Если рак выявлен в поздней стадии, определяются метастазы в отдаленные органы или прорастание в соседние ткани, опухоль неоперабельная или состояние пациента не дает возможности на радикальное вмешательство, применяют другие методики, включая паллиативную и симптоматическую терапию.
При операции хирурги удаляют все пораженные раком ткани с захватом некоторых здоровых участков, если есть метастазы, удаляют также близлежащие лимфоузлы. Это важно для предотвращения рецидивов. После операции проводится реабилитация, могут быть назначены дополнительные курсы терапии.
Лучевая терапия может быть дополнительным методом, проводится до операции с целью уменьшения размеров опухоли, или после нее - для подавления роста оставшихся клеток Источник:
В.Ю. Скоропад, Б.А. Бердов, Л.В. Евдокимов, Л.Н. Титова
Интраоперационная лучевая терапия — инновационная
технология в комбинированном лечении опухолей
желудочно-кишечного тракта //
Поволжский онкологический вестник, 2013, №1, с.4-10 .
Может применяться химиотерапия (введение препаратов, подавляющих рост рака) для уничтожения раковых клеток до и после операции, а при неоперабельном раке в качестве паллиативного лечения.
Прогнозы при раке ЖКТ
Во многом прогнозы для жизни и здоровья зависят от типа опухолевых клеток, стадии выявления и особенностей лечения, возраста пациента и имеющихся у него сопутствующих патологий.
Самый неблагоприятный прогноз - при раке поджелудочной железы, самый оптимистичный - для нейроэндокринных опухолей кишечной стенки. Процент выживаемости в течение 5 лет колеблется от 5 до 90% в зависимости от вида рака. На начальных стадиях, когда нет метастазов, шансы на успех достигают 80-90%, в терминальных стадиях не превышают 10%.
Читайте также:
