Принципы гемостаза при операции на ухе - височной кости
Добавил пользователь Владимир З. Обновлено: 01.02.2026
Московский научно-практический центр оториноларингологии Департамента здравоохранения Москвы
Московский научно-практический центр оториноларингологии ДЗ Москвы
Федеральный медико-биологический Центр им. А.И. Бурназяна ФМБА России, Москва, Россия, 123098
Хирургическое лечение холестеатомы пирамиды височной кости
Журнал: Вестник оториноларингологии. 2015;80(3): 57‑60
Кратко представлена эпидемиология, классификация, диагностика и современные тенденции хирургического лечения холестеатомы пирамиды височной кости. Описан клинический случай диагностики и хирургического лечения холестеатомы верхушки пирамиды височной кости.
Из всех заболеваний верхушки пирамиды височной кости холестеатома встречается в 3,4—9% случаев. Наиболее часто (в 60%) в этой зоне выявляется холестероловая гранулема. В то же время имеются случаи диагностики мукоцеле, арахноидальных кист, менингиомы, хордомы, ксантомы, кавернозной гемангиомы, аневризм внутренней сонной артерии, фиброзной дисплазии, хондросаркомы и метастатической карциномы. Может симулировать заболевание верхушки пирамиды и асимметричная пневматизация этой локализации [1—5].
Среди больных с холестеатомой височной кости у 2,9% встречается холестеатома пирамиды височной кости. Холестеатома этой локализации может быть первичной (врожденной), происходящей из остатков эмбриональной или аберрантной эпителиальной ткани, или вторичной вследствие инвазии холестеатомы из среднего уха или сосцевидного отростка. Вторичная холестеатома выявляется у 58%, а первичная — у 12% пациентов [2, 6]. В зависимости от локализации холестеатомы в пирамиде височной кости по классификации M. Sanna [7] выделяют пять ее видов: супралабиринтная, инфралабиринтная, массивная лабиринтная, инфралабиринтная с апикальным распространением и апикальная [7]. Наиболее часто встречается супралабиринтная (26,7—67%), массивная лабиринтная (20—38%) и инфралабиринтная (7—40%) холестеатомы [1, 6, 8].
При холестеатоме пирамиды височной кости часто наблюдается бессимптомное течение при значительном ее объеме. В зависимости от локализации ранними симптомами могут быть выраженное снижение слуха или глухота (у 9—69%), дисфункция лицевого нерва (у 29—53%), оторея (у 66,7%), периферическое головокружение (у 33,3%) или центральные неврологические осложнения вследствие эрозии рядом расположенных важных анатомических структур [1, 2, 6, 8, 9].
Применение в диагностике высокоинформативных методов исследования: мультиспиральной компьютерной томографии (МСКТ) и магнитно-резонансоной томографии (МРТ) с контрастным усилением, в том числе в non- EPY режиме, позволяет определить локализацию, распространение холестеатомы и на дооперационном этапе планировать хирургический подход.
В литературе имеются единичные обзоры, посвященные диагностике и хирургии холестеатомы пирамиды височной кости, освещающие значительное количество клинических случаев [1, 6, 8—11]. Основными задачами операции являются тотальное макроскопическое удаление холестеатомы, сохранение ствола лицевого нерва, предупреждение ликвореи и менингита и сохранение слуховой функции. Поэтому современный алгоритм выбора хирургического подхода строится на локализации холестеатомы, состоянии слуховой функции и лицевого нерва. Большинство авторов отдают предпочтение закрытым вариантам с облитерацией зоны операции и ушиванием наружного слухового прохода по Rambo, учитывая современные средства реабилитации слуха. Так, при супралабиринтной холестеатоме и нормальном слухе используют транстемпоральный супралабиринтный подход через среднюю черепную ямку, а при сенсоневральной тугоухости — выполняют субтотальную петрозэктомию транслабиринтным и транскохлеарным подходом. При инфралабиринтной холестеатоме и нормальном слухе применяют субтотальную петрозэктомию трансмастоидальным и ретролабиринтным подходами, а при сенсоневральной тугоухости — транслабиринтным и транскохлеарным подходами [6, 11, 12]. В то же время стремление сохранить слух после операции в ущерб радикальному удалению холестеатомы может привести к резидуальной патологии и необходимости повторного вмешательства. В тех случаях, когда холестеатома распространяется медиальнее капсулы лабиринта, сохранить слух невозможно, и на выбор хирургического подхода влияет состояние лицевого нерва. При этих локализациях холестеатомы при сохранной функции лицевого нерва применяют транслабиринтный и транскохлеарный или инфратемпоральный доступы, а при дисфункции лицевого нерва — транскохлеарный. Для лечения дисфункции лицевого нерва в зависимости от места компрессии выполняют декомпрессию ствола нерва, нейропластику или VII—XII анастомоз одновременно (или на втором этапе) [1, 6, 10]. Лучшие результаты операции отмечают при длительности дисфункции лицевого нерва менее 12 мес. В результате лечения глухота оперированного уха наблюдается у 18—83%, рецидив холестеатомы в разные сроки — у 2—19% и интракраниальные осложнения у 2—6% больных [6, 8].
В последние годы некоторые авторы выполняют модифицированную субтотальную петрозэктомию различными подходами, в зависимости от локализации холестеатомы, с тимпанооссикулопластикой для сохранения или улучшения функции слуха. По их данным, преимуществами открытой реконструкции являются функциональный результат, ранняя диагностика рецидива холестеатомы и менее сложная ревизионная хирургия в условиях необлитерированной полости. При этой методике после удаления холестеатомы пирамиды височной кости у 90% пациентов выполнялась тимпанопластика и у 52% — оссикулопластика. В результате операции слух улучшился у 38% пациентов, сохранился на прежнем уровне — у 29% и у 33% отмечено его ухудшение [8].
В нашей стране хирургией пирамиды височной кости занимаются преимущественно нейрохирурги. Однако и их возможности ограничены при распространенной холестеатоме пирамиды височной кости.
Представляем случай диагностики и хирургического лечения холестеатомы верхушки пирамиды височной кости.
Пациентка М., 32 года, обратилась в отделение нейрохирургии клиники ФГБУ ФМБЦ им. А.И. Бурназяна с жалобами на отсутствие слуха на правое ухо, периодические выделения из него, асимметрию лица.
Из анамнеза известно, что пациентка с детства страдает хроническим гнойным правосторонним средним отитом с периодическими обострениями в виде выделений из правого уха на фоне ОРВИ или попадания воды в ухо. Регулярно проводилась местная антибактериальная терапия с временным положительным эффектом. С 16-летнего возраста стала отмечать головокружения системного характера. В 2006 г. обратилась в клинику МОНИКИ, где выполнена КТ височных костей, по данным которой выявлено новообразование правой пирамиды височной кости. В той же клинике выполнена санирующая операция на правой височной кости с удалением задней стенки слухового прохода. В послеоперационном периоде головокружения купировались, но сохранялись выделения из этого уха. В 2009 г. стала отмечать подергивание мышц правой половины лица, эпизоды по типу гемифациального спазма до нескольких раз в день. В НИИ нейрохирургии им. Н.Н. Бурденко выполнена ретросигмовидным доступом операция на пирамиде височной кости с удалением холестеатомы правой пирамиды височной кости. После операции у пациентки полностью восстановилась функция лицевого нерва справа. Однако в 2012 г. у пациентки вновь развился парез лицевого нерва справа. Обратилась в отделение нейрохирургии клиники ФМБЦ им. А.И. Бурназяна для обследования и лечения.
При поступлении: общее состояние больной удовлетворительное. Температура тела нормальная. Кожные покровы обычной окраски. В легких дыхание везикулярное, без хрипов. АД — 120/80 мм рт.ст. Пульс 90 в 1 мин, ритмичный, удовлетворительных свойств.
При осмотре имеются спокойные, безболезненные послеоперационные рубцы в правой заушной и ретросигмовидной области. При отомикроскопии справа — наружный слуховой проход широкий, свободный, без отделяемого. Барабанная перепонка сохранена только в передних отделах. Слизистая оболочка в мезогипотимпануме утолщенная, полипозно-измененная. Полость в мастоидальном отделе небольшая, покрыта утолщенной слизистой оболочкой без эпидермиса. Слуховая труба проходима по Вальсальва. Слева наружный слуховой проход широкий, свободный. Барабанная перепонка серого цвета, опознавательные знаки дифференцируются.
В неврологическом статусе: сознание ясное. Контактная. Менингеальных знаков нет. Гипостезия в зоне иннервации V нерва справа (больше по 1—2 ветвям), корнеальный рефлекс снижен справа. Определяется грубый парез правого лицевого нерва справа (V степень по шкале House—Brackmann). Координаторные пробы выполняла удовлетворительно.
При тональной пороговой аудиометрии (ТПА) выявлена правосторонняя глухота. Слух слева в пределах возрастной нормы.
По данным электронейромиографии отмечались признаки умеренного поражения правого лицевого нерва по смешанному типу (аксональному и демиелинизирующему), проводимость по всем ветвям составляла 30—40% от нормы по типу неврита.
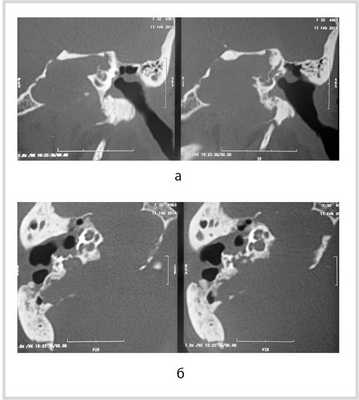
Рис. 1. КТ височных костей пациентки М. а — коронарная проекция: деструктивная полость в пирамиде височной кости, заполненная субстратом неоднородной плотности, капсула лабиринта значительно разрушена на уровне базального и апикального завитков улитки, латерального и верхнего полукружных каналов; б — аксиальная проекция: деструктивная полость с разрушением задней грани пирамиды, передневерхней и нижней поверхности.
По результатам МРТ головного мозга правая пирамида височной кости деформирована, увеличена в объеме, выполнена субстратом размером до 5,5—2,8—3 см, распространяющимся на область внутреннего слухового прохода, заднего полукружного канала, медиальные отделы барабанной полости, сосцевидный отросток. Описанный субстрат изо-гипоинтенсивен в режиме Т1, гиперинтенсивен — в Т2 и non-EPI DWI (рис. 2). Заключение: признаки рецидива холестеатомы с деструктивными изменениями структур внутреннего и среднего уха на фоне хронических воспалительных изменений.
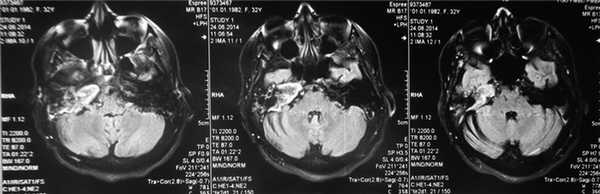
Рис. 2. Магнитно-резонансная томография головного мозга пациентки М. Деформированная, увеличенная в объеме пирамида височной кости выполнена мягкотканым субстратом.
Учитывая анамнез заболевания, ранее выполненные операции, клинические проявления (глухота, явления периферического пареза лицевого нерва) и локализацию процесса по данным КТ височных костей и МРТ, свидетельствующие о массивной лабиринтной холестеатоме, пациентке была выполнена реоперация. Транслабиринтным подходом произведена субтотальная петрозэктомия (частичная лабиринтэктомия) с удалением холестеатомы и пластикой дефекта височной кости жиром. При ревизии определялась послеоперационная неэпидермизированная мастоидальная полость, которая была заполнена утолщенной слизистой оболочкой. В барабанной полости также определялась утолщенная полипозная слизистая оболочка. Барабанная перепонка сохранена только в передних отделах. Цепь слуховых косточек отсутствовала. За счет удаления перилабиринтных клеток, заднего верхнего и латерального полукружных каналов был открыт широкий доступ в сторону верхушки пирамиды, где выявлена большая холестеатома, распространявшаяся от верхушки сосцевидного отростка до верхушки пирамиды височной кости. Выявлено обнажение луковицы яремной вены, мозговых оболочек задней черепной ямки, нисходящей части канала лицевого нерва. Холестеатома удалена с образованием большой полости внутри пирамиды височной кости. При удалении холестеатомы из области внутреннего слухового прохода (который не дифференцировался) отмечалась ликворея. Эпидермальные оболочки оставлены на луковице яремной вены, у верхушки пирамиды височной кости, под улиткой. Произведена герметизация твердой мозговой оболочки двухкомпонентным фибриновым клеем. В область верхушки пирамиды височной кости уложена подкожно-жировая клетчатка, которая была взята с передней брюшной стенки. Выполнена пластика полости свободным миофасциальным лоскутом. В барабанную полость, под остатки барабанной перепонки, уложена аутофасция. Слуховой проход не ушивался для возможности контроля за созданной полостью.
По данным гистологического исследования удаленного образования от 29.07.14: в присланном материале бесструктурные холестеатомные массы и мелкий пласт многослойного плоского эпителия с рыхлой подэпителиальной стромой с кровоизлияниями.
При наблюдении в послеоперационном периоде отмечена длительная эпителизация послеоперационной полости и сохранение пареза правого лицевого нерва (V степень по шкале House—Brackmann). Неврологический статус — без отрицательной динамики.
Представленный случай свидетельствует о возможности успешного применения транслабиринтного подхода для удаления холестеатомы верхушки пирамиды височной совместно с нейрохирургами.
Холестеатома уха
Холестеатома уха — это опухолевидное инкапсулированное образование среднего уха, состоящее преимущественно из клеток слущенного эпителия и кристаллов холестерина. Различают истинную (врожденную) и ложную холестеатому уха. Проявляется заболевание ощущением распирания и болями в ухе, снижением слуха смешанного типа, небольшим количеством имеющих гнилостный запах выделений из уха. Холестеатома уха диагностируется при помощи рентгенографии и КТ черепа, отоскопии, зондирования и промывания барабанной полости, исследований вестибулярного и слухового анализаторов. Лечение холестеатомы уха в большинстве случаев заключается в радикальном хирургическом удалении. Иногда возможно промывание надбарабанной полости с расположенной в ней холестеатомой.
МКБ-10



Общие сведения
Холестеатома - эмбриональное или (чаще) приобретенное псевдоопухолевое образование, происходящее из тканей среднего уха. В 90% случаев она появляется на фоне хронического гнойного среднего отита. В популяции частота гнойный отитов, осложненных холестеатомой, составляет 0,01%. Заболеванием чаще страдают дети старше 10 лет и взрослые 20-30 лет. У детей патология протекает более агрессивно с многократными рецидивами.

Причины
Холестеатома уха может иметь врожденный характер. В таких случаях она носит название истинной. Благодаря гладкой, напоминающей поверхность жемчужины, капсуле истинную холестеатому уха называют еще «жемчужной опухолью». Она возникает вследствие эмбриональных нарушений и располагается в пирамиде височной кости. Истинная холестеатома может также находиться в других костях черепа, в боковой цистерне и желудочках головного мозга.
Ложная холестеатома уха образуется в результате длительно протекающих отитов или как последствие травмы уха. Считается, что образование ложной холестеатомы уха возможно 2 путями. В первом случае происходит врастание плоского эпителия наружного слухового прохода в полость среднего уха через краевой разрыв барабанной перепонки. Второй механизм образования холестеатомы уха реализуется при нарушении проходимости слуховой трубы в связи с евстахиитом. В результате пониженного давления в барабанной полости происходит втяжение в нее части барабанной перепонки. Когда втяжение становится достаточно глубоким, в нем начинает накапливаться кератин и слущенный эпителий, что ведет к развитию холестеатомы уха.
Патогенез
Холестеатома уха не является истинной опухолью уха, хотя по своему внешнему виду и характеру роста напоминает опухолевое образование. Холестеатома уха имеет слоистую структуру. Сверху она покрыта капсулой из соединительной ткани, под которой находится ороговевающий плоский эпителий. Средний слой холестеатомы уха представлен наложенными одна на другую пластинами слущенного эпителия и расположенными между ними кристаллами холестерина. Центральную часть холестеатомы уха или ее ядро занимает имеющий гнилостный запах беловатый детрит.
Холестеатома уха может быть единичным образованием или представляет собой скопление большого количества узелков, имеющих плотную консистенцию и размер от 3 мм. Холестеатома уха выделяет специфические химические вещества, которые приводят к резорбции окружающих холестеатому костных тканей с образованием гладкостенной полости. Кроме того, эти вещества оказывают токсическое воздействие на рецепторный аппарат внутреннего уха, вызывая расстройство звуковосприятия и реактивный лабиринтит.
Симптомы холестеатомы уха
В начальном периоде холестеатома уха может иметь бессимптомное течение. Затем пациент начинает предъявлять жалобы на чувство распирания в ухе, появление тупой, давящей, ноющей или стреляющей ушной боли. Происходит понижение слуха. Возможны головные боли, при развитии лабиринтита — головокружения. Наблюдаются выделения из уха, которые обычно имеют гнилостный запах и носят скудный характер. Отличительной особенностью является обнаружение в отделяемом небольших комочков белого цвета.
При холестеатоме уха тугоухость имеет смешанный характер. С одной стороны она обусловлена нарушением звукопроведения в связи с ограничением подвижности слуховых косточек, а с другой — расстройством звуковосприятия в результате токсического поражения рецепторов лабиринта проникающими в него агрессивными выделениями холестеатомы.
Осложнения
Разрушая рядом расположенные костные образования, холестеатома уха увеличивается в размерах. Так она со временем заполняет ячейки сосцевидного отростка, доходит до капсулы лабиринта и способна разрушить его полукружные канальцы с образованием фистулы лабиринта. При разрушении коркового слоя сосцевидного отростка холестеатома уха выходит под кожу сосцевидной области.
Разрушение стенки косного канала лицевого нерва ведет к развитию пареза лицевого нерва, стенки сигмовидного синуса — к его тромбозу. Зачастую холестеатома уха достигает размера грецкого ореха и имеет расходящиеся в различных направлениях отростки. При этом она образует гигантскую полость, похожую на полость, остающуюся после общеполостной операции на ухе.
Старая холестеатома уха включает содержащие токсическую жидкость кисты, прорыв которых в подпаутинное пространство приводит к развитию асептического менингита, в вещество головного мозга — к появлению менингоэнцефалита. Эти осложнения могут привести к гибели больного от отека головного мозга. Обострение среднего отита часто сопровождается гнойным распадом холестеатомы уха, обуславливающим развитие гнойного лабиринтита и менингита, околосинусового и экстрадурального абсцесса, абсцесса головного мозга, отогенного сепсиса.
Диагностика
К диагностике холестеатомы уха могут привлекаться не только врачи-отоларингологи, но также неврологи и нейрохирурги. В современной отоларингологии используется комплекс визуализирующих и функциональных методик:
- Рентгенография височных костей. На рентгенограммах в проекции по Майеру, Шюллеру или Стенверсу холестеатома определяется как имеющая среднюю плотность однородная тень, которая находится в круглой патологической полости с гладкими и четко визуализирующимися краями. Более точную визуальную картину образования получают при проведении КТ и МСКТ черепа.

КТ височных костей. Деструкция сосцевидного отростка, сосцевидной пещеры, пирамиды и среднего уха правой височной кости, обусловленная холестеатомой
- Эндоскопия уха. При отоскопии возможно обнаружение краевой перфорации барабанной перепонки, признаков деструкции костной части слухового прохода, обусловленных разрастанием холестеатомы. При наличии краевой перфорации производят зондирование полости среднего уха пуговчатым зондом и промывание надбарабанного пространства. О наличии деструктивного процесса свидетельствует шероховатая при прощупывании поверхность кости. В пользу холестеатомы уха говорит присутствие в промывных водах включений и чешуек эпидермиса.
- Исследование слухового анализатора. Дополнительно у пациентов с холестеатомой уха проводят исследование слуха и вестибулярного анализатора. Аудиометрия выявляет снижение слуха, пороговая аудиометрия — смешанный тип тугоухости. Производят также исследование камертоном, определение проходимости слуховой трубы, электрокохлеографию, акустическую импедансометрию, отоакустическую эмиссию, вестибулометрию, электронистагмографию, стабилографию, непрямую отолитометрию.
- Неврологическая диагностика. В диагностике осложнений может применяться неврологический осмотр, МРТ головного мозга, люмбальная пункция и др.

МРТ головы. Гиперинтенсивный сигнал в области сосцевидной пещеры, сосцевидного отростка и пирамиды правой височной кости (холестеатома)
Холестеатому уха необходимо дифференцировать от опухолей и инородных тел уха, кохлеарного неврита, серной пробки, гломусной опухоли, адгезивного среднего отита, специфических гранулем при туберкулезе и сифилисе.
Лечение холестеатомы уха
Консервативная тактика
Консервативное лечение возможно лишь в случае небольшой холестеатомы уха, находящейся в надбарабанном пространстве. Терапия таких холестеатом заключается в промывании надбарабанного пространства растворами протеолитических ферментов и борной кислоты. Начинают и заканчивают процедуру промыванием полости изотоническим раствором. Подобную манипуляцию проводят ежедневно в течение недели.
Хирургическое лечение
При неэффективности консервативного лечения, большом размере холестеатомы уха, наличии осложнений показано радикальное удаление образования. В зависимости от распространенности холестеатомы хирургическое вмешательство может включать:
- санирующую операцию на среднем ухе;
- лабиринтотомию;
- транслабиринтное вскрытие пирамиды височной кости;
- тимпанпластику, мастоидопластику, мирингопластику и пр.
Прогноз и профилактика
В случае своевременного выявления, последовательного консервативного или радикального хирургического лечения холестеатомы прогноз благоприятный. В отдельных случаях возможны рецидивы процесса. В запущенных стадиях возможно развитие тугоухости, жизнеугрожающих внутричерепных осложнений. Профилактика холестеатомы заключается в предупреждении ХГСО, своевременном лечении воспаления среднего уха.
Миринготомия уха - что за операция и как проходит?
Сильная боль при отите часто связана со скоплением в среднем ухе жидкости (слизи, гноя или крови). Эти субстанции обычно не должны там находиться, и когда вдруг там оказываются — это может сильно ухудшить качество жизни. Если прием антибактериальных препаратов не принес нужного эффекта, может помочь миринготомия - прокол барабанной перепонки.
Как устроено ухо
Ухо разделяют на три отдела: наружное ухо, среднее и внутреннее. В состав наружного уха включают ушную раковину, наружный слуховой проход и барабанную перепонку, являющуюся границей между наружным и средним ухом.
Среднее ухо представлено барабанной полостью, пещерой сосцевидного отростка и их содержимым - прежде всего, слуховыми косточками, а также слуховой (евстахиевой) трубой, соединяющей барабанную полость с полостью глотки.
Внутреннее ухо представлено преддверием, улиткой, полукружными каналами и расположено в пирамиде височной кости.
Наиболее мучительным для человека является средний отит - отек и воспаление слизистой барабанной полости.
Что такое миринготомия, пapaцeнтeз, тимпанотомия?
Все это разные названия хирургической операции, суть которой - прокол барабанной перепонки, извлечение вредного содержимого из барабанной полости, образовавшегося там из-за воспаления. Сквозной разрез обеспечивает свободный выход скопившейся в среднем ухе жидкости, после чего человеку становится значительно лучше, а боль отступает.
Вмешательство связано с определенными сложностями. Длительно протекающий воспалительный процесс утолщает перепонку, и в ней бывает трудно сделать маленький сквозной прокол. Операция обычно назначается детям, ведь они болеют отитом чаще взрослых из-за возрастных особенностей анатомии слуховой трубы.
Показания
Прокол барабанной перепонки показан в следующих случаях:
- выраженный болевой синдром при подтвержденном среднем отите;
- жидкость в среднем ухе, выявленная путем специального обследования - тимпанометрии;
- нет положительной динамики при длительном приеме антибиотиков и других лекарств;
- дисфункция евстахиевой трубы у взрослых;
- ухудшение слуха из-за скопления жидкости в барабанной полости;
- необходимость проведения анализа, для выявления возбудителя возможной инфекции и проведения адекватной лекарственной терапии.
Если экссудат из полости среднего уха удалить вовремя, не дожидаясь осложнений, отит не перейдет в хроническую стадию.
Важно! Миринготомия барабанной перепонки не заменяет антибактериальной терапии, не уменьшает частоту развития среднего отита и не снижает число рецидивов.
Противопоказания
Миринготомия может быть противопоказана при любых признаках опухоли среднего уха или сосудистых аномалиях. К относительным противопоказаниям относят предшествующую лучевую терапию области головы и шеи.
Как проходит операция
Методику проведения операции определяет ЛОР-врач на основе данных всестороннего обследования пациента, подтвержденного диагноза и наличия показаний к вмешательству.
Чтобы получить наилучший обзор полости среднего уха, применяют микроскоп. Затем выполняют маленький надрез в барабанной перепонке, а жидкость из среднего уха удаляют. В большинстве случаев, может понадобиться небольшая трубка, которая останется в месте надреза, и позволит дренажу продолжаться.
Для закрытия надреза наложение швов не требуется - он заживет сам.
Острый средний отит определяется по совокупности признаков:
- данные анамнеза;
- показатели отоскопии - исследования наружного уха и барабанной перепонки с помощью специального прибора;
- характерные симптомы наличия жидкости за барабанной перепонкой: сильная боль в ухе, снижение слуха и проявление интоксикации: бледность, слабость, отсутствие аппетита, головная боль и повышенная температура.
В некоторых случаях врач назначает дополнительные диагностические процедуры: бактериальный посев экссудата и рентгенографию височной кости.
Подготовка
Включает ряд обязательных исследований:
- проверка слуха;
- общий анализ крови;
- тимпанография - оценка деформации барабанной перепонки на перепады давления.
За неделю до плановой операции необходимо прекратить прием противовоспалительных препаратов и лекарств, разжижающих кровь.
Под каким наркозом проходит?
Миринготомия относится к малоинвазивным вмешательствам и обычно выполняется в амбулаторных условиях. Взрослым достаточно местного обезболивания, а детям необходим общий наркоз, поэтому ребенку нельзя принимать пищу за 6 часов до операции.
Сколько длится?
При отсутствии технических сложностей - 15-20 минут.
Процесс операции
Прокол барабанной перепонки проводится в несколько этапов:
- удаление серы из слухового прохода;
- промывание уха раствором антисептика;
- введение анестетика;
- линейный разрез барабанной перепонки стерильной парацентезной иглой;
- обработка антисептиком;
- установка плотного марлевого тампона (турунды) с лекарством.
Послеоперационный период и реабилитация
В послеоперационном периоде слуховой проход несколько раз в день промывают фурацилином или борным спиртом для быстрого снятия воспаления и улучшения состояния пациента. Чтобы вредное содержимое барабанной полости вытекало скорее, рекомендуют ложиться прооперированным ухом вниз, на подушку.
Обычно полное восстановление после операции происходит в течение 4-х недель, но уже примерно через 5 дней после операции отверстие в барабанной перепонке заживает. В течение 3-5 дней после операции из места прокола может выделяться гной, это нормально. Восстановительный период требует соблюдения следующих рекомендаций:
- слуховой проход следует ежедневно очищать;
- если врач прописал ушные капли, нужно закапывать их строго в соответствии с назначением;
- необходимо регулярно менять ватные тампоны в ухе;
- уточнить у врача правила проведения водных процедур.
Возможные осложнения
Срочно позвоните врачу или в скорую, если после операции произошло что-то из нижеперечисленного:
- появились признаки инфекции — лихорадка или озноб;
- ухо покраснело, появился отёк, усилилась боль, пошла кровь или другие выделения;
- если боль не проходит после приёма лекарств, назначенных для этого врачом;
- ухудшился слух;
- появился кашель, одышка, боль в груди, сильная тошнота или рвота.
Заключение
Прокалывание барабанной перепонки для удаления скопившегося в полости содержимого - рутинная процедура, которая избавляет от острой боли при воспалении среднего уха. Родители часто опасаются таких радикальных методов лечения отита, особенно у совсем маленьких детей. Но многолетняя успешная практика подтвердила высокую эффективность и безопасность миринготомии.
Принципы гемостаза при операции на ухе - височной кости
Астраханский филиал «Научно-клинический центр оториноларингологии» ФМБА России, Астрахань, Россия, 414056
Научно-клинический центр оториноларингологии» ФМБА России, Москва, Россия, 125310
Отдел заболеваний уха, лаборатория патологической анатомии ЛОР-органов НКЦ оториноларингологии ФМБА России
Мастоидопластика при повторных санирующих операциях на ухе
Журнал: Вестник оториноларингологии. 2016;81(1): 40‑43
Цель исследования — оценка результатов мастоидопластики ортотопической костной тканью с области височной линии. Показали, что область височной линии является оптимальным участком височной кости для забора костного материала для мастоидопластики при повторных санирующих операциях в условиях дефицита ортотопической костной ткани. Мастоидопластика ортотопической костной тканью имеет ряд преимуществ перед другими методами мастоидопластики, в том числе с точки зрения биосовместимости. В отдаленном послеоперационном периоде высокоинформативным и неинвазивным методом исследования и контроля у пациентов, перенесших санирующую реоперацию с мастоидопластикой костной тканью, является мультиспиральная компьютерная томография височных костей.
Мастоидопластика является реконструктивным этапом при санирующих операциях (СО) на ухе. Концепция облитерации мастоидальной полости (МП) впервые введена H. Mosher в 1911 г. [1]. Мастоидопластика чаще проводится при повторных операциях по поводу рецидива хронического гнойного среднего отита (ХГСО) после ранее выполненных открытых методов СО на ухе с образованием МП [2, 3].
Как открытые, так и закрытые методы СО чаще выполняются по поводу форм ХГСО с холестеатомой [4]. Обе методики имеют свои преимущества и недостатки [5]. Закрытые методы характеризуются меньшим риском развития так называемой болезни оперированного уха, но повышенным риском рецидива холестеатомы (30—63%) [6—8]. При открытой методике меньше риск рецидива холестеатомы (2—10%) [9], но более высок риск развития «болезни оперированного уха» (20—60%) [10].
Болезнь оперированного уха возникает чаще после открытых методов СО на ухе, основными факторами ее развития являются неполная эпидермизация МП, высокая шпора, большая послеоперационная полость, нарушенная функция слуховой трубы [4, 11]. Целью облитерации является уменьшение объема МП для сокращения площади эпидермизации, ликвидации карманов, в которых могут скапливаться эпидермальные массы, поддерживающие хроническое воспаление.
Для облитерации МП используют ауто-, алло-, ксеноткани, а также различные биосовместимые материалы (метакрилат, керамика, гидроксиапатит и так далее) [12, 13].
Каждый из предложенных для мастоидопластики материалов имеет свои преимущества и недостатки. Аутоткань обладает преимуществами перед другими материалами благодаря высоким биопластическим свойствам, отсутствию антигенности, доступности и простоте использования, безвредности и переносимости тканями. После пересадки свежие аутотрансплантаты перестраиваются интенсивнее, чем алло- и ксенотрансплантаты [14].
Недостатком мягкотканных пластических материалов является их сморщивание, истончение, что в конечном итоге приводит к атрофии пластического материала с приближением размеров МП к первоначальным [15]. Использование аутоткани отдаленных анатомических областей (подвздошный гребень, гребень большеберцовой кости) связано с дополнительной операционной травмой, что увеличивает длительность послеоперационного периода и время нахождения в стационаре. Недостатками аллогенного материала является риск отторжения и передачи инфекции, а сохранение ценных качеств аллоткани зависит от методов ее консервации и стерилизации, что требует дополнительных специальных условий для забора, консервации и хранения аллоткани. Использование биосовместимых материалов в практике ограничено высокой вероятностью их инфицирования, неполной остеоинтеграцией, возможностью экструзии имплантата [16].
Наиболее подходящим материалом для мастоидопластики как с точки зрения биосовместимости, так и с точки зрения простоты забора материала является ортотопическая костная ткань (ОКТ), которая может быть использована в виде костных чипсов, пластинок, закрученных кусочков, пасты [17]. При использовании ОКТ не требуется дополнительных разрезов для ее получения, консервации и стерилизации. При повторных СО на ухе всегда имеется дефицит ОКТ, так как кортикальная кость с сосцевидного отростка удаляется во время первичной СО.
Все вышесказанное определило цель исследования: поиск наиболее оптимального участка височной кости для взятия ОКТ с целью облитерации МП при повторных СО на ухе и оценка результатов мастоидопластики.
Пациенты и методы
С января 2014 г. по апрель 2015 г. в Астраханском филиале НКЦО ФМБА России было прооперировано 25 больных с рецидивом ХГСО после ранее перенесенной СО по открытому типу. Возраст больных варьировал от 18 до 55 лет (64% мужчин, 36% женщин). Всем больным была выполнена санирующая реоперация с одномоментной мастоидопластикой стружкой ОКТ, взятой из области височной линии (ВЛ). Пациенты имели выраженную симптоматику, характерную для «болезни оперированного уха». Все больные жаловались на снижение слуха на оперированное ухо. Жалобы на отделяемое из оперированного уха предъявляли 76% больных (см. таблицу).

Структура жалоб больных с «болезнью оперированного уха»
Обследование включало переднюю и заднюю риноскопию, отомикроскопию, аку- и вестибулометрию, исследование проходимости слуховых труб, тональную пороговую аудиометрию, мультиспиральную компьютерную томографию (МСКТ) височных костей, эндоскопию полости носа и носоглотки с тщательным осмотром глоточных устьев слуховых труб.
Хирургическое лечение выполнялось заушным доступом под общей анестезией.
Разрез в заушной области проводили по старому послеоперационному рубцу с продолжением его у верхнего конца прикрепления ушной раковины кзади и кверху на 1,5 см, параллельно В.Л. Мягкие ткани заушной области отслаивались до кости, обнажая область В.Л. Далее эпидермальная выстилка послеоперационной полости отслаивалась, визуализировались мастоидальная и барабанная полости вместе с оставшейся частью оссикулярной системы, овальным и круглым окном, барабанным устьем слуховой трубы. Далее проводили санирующий этап операции, ликвидировали карманы, при высокой шпоре она сглаживалась. Перед выполнением тимпано- и мастоидопластики проводили гемостаз, тщательное удаление мягких тканей из М.П. Для выполнения тимпанопластики и отграничения малой тимпанальной полости от мастоидальной в качестве трансплантата использовали хрящ. После выполнения одного из вариантов тимпанопластики и формирования малой тимпанальной полости выполняли мастоидопластику. МП облитерировали стружкой ОКТ, которую укладывали за хрящевым трансплантатом, последний фиксировали в сформированные по границе костного дефекта задней стенки наружного слухового прохода желобки (сверху и снизу). Кожную пластику наружного слухового прохода производили на завершающем этапе операции. Операционную рану послойно ушивали. В слуховой проход укладывались силиконовые полоски и проводили тампонаду гемостатической губкой. Удаление тампонов и силиконовых полосок производили через 3 нед после операции.
Эффективность оперативного лечения оценивалась по клиническим данным и результатам объективных методов исследования (отомикроскопия, МСКТ височных костей). Первичные результаты оценивали через 3 мес, отдаленные — через 12 мес и более.
Результат лечения расценивали как хороший, если в оперированном ухе отсутствовали клинические признаки воспаления, рецидивы ХГСО, неотимпанальный лоскут представлял собой целостную подвижную мембрану, а пациенты отмечали заметное улучшение слуха.
Удовлетворительными считали результаты операции, если в оперированном ухе имелись признаки воспаления послеоперационной полости, которые ликвидировались при помощи консервативной терапии и не требовали реоперации, а неотимпанальный лоскут представлял собой ограниченно подвижную мембрану или имел «сухую» центральную перфорацию.
При возникновении рецидива заболевания и необходимости в реоперации результаты считали неудовлетворительными.
МСКТ височных костей проводили перед операцией и через год после операции на спиральном компьютерном томографе фирмы «Philips» MX-16 в коронарной и аксиальной проекциях с толщиной среза 0,65 мм.
Результаты и обсуждение
Через 3 мес после операции хорошие результаты были достигнуты у 21 (84%) пациента. Удовлетворительные результаты получены у 4 (16%) больных и обусловлены наличием неэпидермизированных участков у 3 (12%) больных и реперфорацией неотимпанальной мембраны в 1 (4%) случае.
Через год после операции у 22 (88%) больных фиксировали хорошие результаты (рис. 1). Удовлетворительные результаты были достигнуты у 1 (4%) больного, что было обусловлено сохраняющейся реперфорацией неотимпанальной мембраны. Больному была выполнена реоперация с закрытием дефекта в неотимпанальной мембране. В 2 (8%) случаях потребовалась санирующая реоперация из-за рецидива отореи. Рецидив был обусловлен резидуальной холестеатомой, оставленной в тимпанальном синусе.
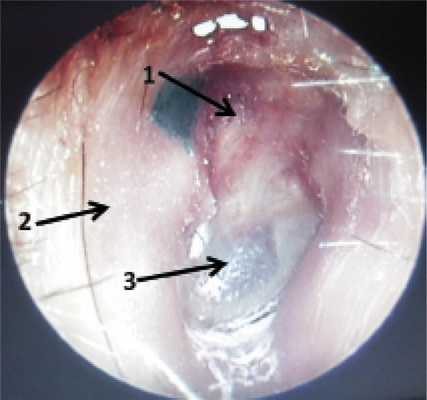
Рис. 1. Правое ухо. Отоэндоскопия отоскопом прямого видения 00 фирмы KARL STORZ. 1 — облитерированный эпитимпанум, 2 — задняя стенка наружного слухового прохода после полной мастоидопластики, 3 — неотимпанальный лоскут.
МСКТ височных костей было выполнено перед операцией с целью определения наиболее оптимального участка височной кости для взятия ОТК для облитерации МП при повторных СО на ухе. Также учитывалось положение данного участка по отношению к важным анатомическим структурам (лицевой нерв, сигмовидный синус, горизонтальный полукружный канал, твердая мозговая оболочка средней и задней черепных ямок).
Результаты исследования 60 компьютерных томограмм височных костей больных с ХГСО показали, что наиболее оптимальным участком для взятия стружки аутокости для мастоидопластики является область ВЛ, так как именно в этом месте наружный кортикальный слой кости имеет наибольшую толщину и меньше риск повреждения важных анатомических структур. В среднем толщина наружного кортикального слоя в области височной линии составила 6,4 мм и варьировала от 3,2 мм до 8,3 мм (рис. 2). При толщине наружного кортикального слоя кости менее 4 мм удавалось получить пластический материал только для закрытия глубоких карманов МП. В 6 случаях полученной стружкой аутокости была выполнена полная облитерация М.П. Облитерация М.П. до уровня горизонтального полукружного канала была выполнена у 12 больных. При этом сформирована значительно меньшая по объему послеоперационная полость, что способствовало ее оптимальной эпидермизации. У двух больных вместе с МП был облитерирован эпитимпанум. В 5 случаях удалось взять пластический материал только для облитерации глубоких карманов МП в области верхушки сосцевидного отростка.
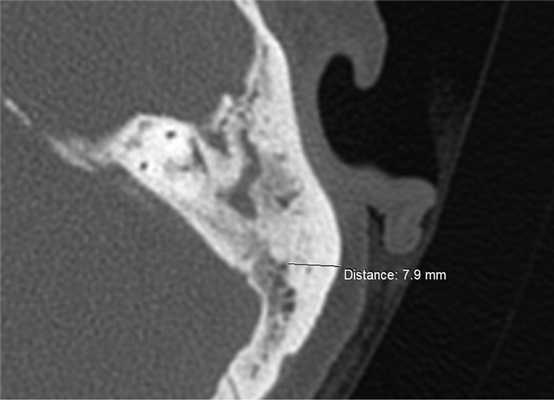
Рис. 2. МСКТ левой височной кости, аксиальная проекция. Проекция области височной линии.
МСКТ височных костей проводилась через год после операции с целью оценки состояния реимплантированной костной ткани.
Анализ данных МСКТ показал, что реимплантрованная костная ткань имеет меньшую плотность, чем наружный кортикальный слой сосцевидного отростка, и варьировала от 350 до 680 едН. В подавляющем большинстве исследований по данным МСКТ не визуализировалась четкая граница между пересаженной костной стружкой и окружающей костной тканью (рис. 3). Лишь в 6 (18%) случаях можно было наблюдать тонкую прослойку низкой плотности между реимплантированной и окружающей костной тканью. По плотности данная прослойка сопоставима с соединительной тканью. Данные МСКТ также позволили в 2 случаях (8%) предположить рецидив холестеатомы. Этим пациентам была выполнена санирующая реоперация по открытому типу (с формированием МП). Интраоперационные находки подтвердили данные МСКТ височных костей и необходимость реоперации.
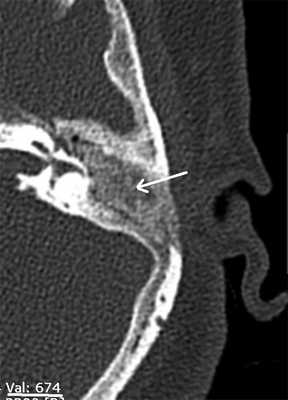
Рис. 3. МСКТ левой височной кости, аксиальная проекция. Стрелка — имплантированная костная стружка.
Выводы
1. Предлагаемый способ мастоидопластики позволяет повысить эффективность хирургического лечения при повторных санирующих операциях на среднем ухе за счет уменьшения частоты рецидивов заболевания.
2. МСКТ височных костей в послеоперационном периоде (через 1 год после операции) является незаменимым методом оценки результатов мастоидопластики у больных после повторных санирующих операций на среднем ухе с использованием костной ткани в качестве пластического материала для мастоидопластики.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России, Москва, Россия
ФГБНУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко», Москва, Россия
Хирургическое лечение неврином слухового нерва (вестибулярных шванном)
Журнал: Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2017;81(3): 66‑76
Клинические рекомендации — это актуальные систематически разработанные положения, созданные для того, чтобы помочь врачу в принятии решений относительно врачебной тактики в определенных клинических ситуациях, они содержат установки по проведению диагностических и скринирующих тестов, по объему медицинской и хирургической помощи и по другим аспектам клинической практики. Вестибулярные шванномы составляют 8% всех внутричерепных образований, до 30% опухолей задней черепной ямки и 85% опухолей мосто-мозжечкового угла. Заболеваемость невриномами слухового нерва составляет примерно 1 случай на 100 000 населения в год. В работе представлены вопросы классификации, диагностики и лечения неврином слухового нерва. В рекомендациях подробно рассмотрены ключевые аспекты формулировки клинического диагноза, классификационные признаки, определение показаний к хирургическому или лучевому лечению, а также принципы выжидательной тактики при вестибулярных шванномах. Особое внимание уделено хирургическому лечению неврином слухового нерва, приведены критерии выбора хирургического доступа, использования современного операционного оснащения, этапы удаления опухоли. В соответствии с принятой клинической классификацией предложены алгоритмы действий в зависимости от стадии заболевания и динамики развития патологического процесса, возраста пациента и клинических проявлений. Ключевые положения клинических рекомендаций основаны на критериях доказательности. Работа предназначена для практической деятельности специалистов нейрохирургов.
Клинические рекомендации (КР) — это актуальные, систематически разработанные положения, созданные для помощи врачу в принятии решений относительно врачебной тактики в определенных клинических ситуациях. Они содержат установки по проведению диагностических и скринирующих тестов, по объему медицинской и хирургической помощи и по другим аспектам клинической практики [1].
Цель составления КР — попытка стандартизации вопросов диагностики и лечения заболеваний по всем разделам медицины, в том числе и по нейрохирургии.
КР включают описание методов диагностики и лечения профильных заболеваний, уровни доказательности основных положений, указатели лекарственных препаратов по Международным непатентованным названиям, оценку информационных ресурсов, использованных для разработки документа. Все основные разделы КР («Общие сведения», «Диагностика», «Лечение») должны содержать уровни доказательности приводимых в данном разделе положений.
В КР могут использоваться различные шкалы уровней доказательности, например, критерии, основанные на шкале уровней (категорий) доказательности Оксфордского центра доказательной медицины. По рекомендации Ассоциации нейрохирургов России в КР нейрохирургического профиля используется шкала «Стандарты—Рекомендации—Опции», в которой «Стандарт» соответствует уровню доказательности класса А, «Рекомендация» — уровням доказательности класса В—С, «Опция» — уровню доказательности класса С.
Стандарты. Это общепризнанные принципы диагностики и лечения, которые могут рассматриваться в качестве обязательной лечебной тактики. Большей частью — это данные, подтвержденные наиболее доказательными исследованиями (1—2 класс) — мультицентровыми проспективными рандомизированными исследованиями, или же данные, подтвержденные результатами независимых крупных нерандомизированных проспективных или ретроспективных исследований, выводы которых совпадают.
Рекомендации. Лечебные и диагностические мероприятия, рекомендованные к использованию большинством экспертов по этим вопросам, которые могут рассматриваться как варианты выбора лечения в конкретных клинических ситуациях. Эффективность рекомендаций определяется в исследованиях 2-го и реже — 3-го класса доказательности, т. е. в проспективных нерандомизированных исследованиях и крупных ретроспективных исследованиях. Для перехода этих положений в разряд стандартов необходимо их подтверждение в проспективных рандомизированных исследованиях.
Опции. Основаны на небольших исследовательских работах 3-го класса доказательности и представляют, главным образом, мнение отдельных авторитетных по тем или иным направлениям экспертов, или экспертных групп.
Общие сведения. Вестибулярные шванномы составляют 8% от всех внутричерепных образований, до 30% опухолей задней черепной ямки и 85% опухолей мосто-мозжечкового угла [2]. Термины «вестибулярная шваннома» и «невринома слухового нерва» являются синонимами, обозначающими доброкачественные опухоли, которые состоят полностью из шванновских клеток и исходят из вестибулярной порции слуховестибулярного нерва (более часто из верхней части вестибулярной порции) [3, 4]. В мировой литературе в основном используется термин «вестибулярная шваннома», а в отечественной — «невринома слухового (VIII) нерва».
Заболеваемость невриномами слухового нерва составляет примерно 1 случай на 100 000 населения в год [5]. Другими словами, каждый год в Российской Федерации появляется 1500 новых случаев неврином слухового нерва. Учитывая постоянное совершенствование методов нейровизуализации, позволяющих устанавливать диагноз на ранних стадиях заболевания, эта цифра может быть еще выше.
Невриномы слухового нерва в 95% случаев является односторонней опухолью. 5% неврином имеют мультицентрический двусторонний характер роста и являются проявлением нейрофиброматоза типа II (НФ-2) — наследственного, аутосомного заболевания, имеющего доминантный характер наследования. Истинные, спорадические невриномы слухового нерва развиваются наиболее часто на четвертом—пятом десятилетии жизни, имея общий возрастной период от 12 до 88 лет [6]. Более часто невриномы встречаются у женщин, чем у мужчин, примерное соотношение 3:2. Двусторонние невриномы, обусловленные НФ-2, проявляются значительно раньше, во втором—третьем десятилетии жизни [7, 8].
Невриномы слухового нерва являются, как правило, плотным, опухолевым образованием, в редких случаях содержат в своей структуре кисты, имеют хорошо выраженную капсулу, четко отграниченную от мозгового вещества. Они возникают во внутреннем слуховом проходе, в зоне Obersteiner-Redlich между миелин-продуцирующими олигодендроцитами и шванновскими клетками, расположенными в 8—10 мм от пиальной оболочки боковой поверхности моста. Рост опухоли происходит в сторону наименьшего сопротивления по корешку нерва в средней части мостомозжечкового угла. Близлежащая часть нерва может быть изолирована при маленькой опухоли, но с увеличением размера последней включается в ее структуру [9]. При более поздних стадиях заболевания и значительно больших размерах опухолевого узла происходит аналогичное воздействие на близлежащие черепные нервы. По частоте вовлечения в этот процесс на первом месте стоит, естественно, вестибуло-кохлеарный нерв, затем в порядке убывания частоты следуют лицевой и тройничный нервы, языкоглоточный нерв и другие [3, 10].
Классификации стадий развития заболевания
В практической деятельности наиболее универсальными являются классификации, предложенные Koos [11] и Samii [12]. Они основаны на оценке размеров невриномы и ее отношении к окружающим мозговым и костным структурам (рис. 1, 2).
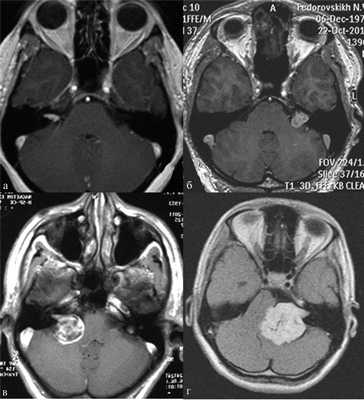
Рис. 1.Иллюстрация классификации неврином слухового нерва по Koos. а — I стадия — опухоль находится в пределах внутреннего слухового прохода, диаметр экстраканальной части составляет 1—10 мм; б — II стадия — опухоль вызывает расширение канала внутреннего слухового прохода и выходит в мостомозжечковый угол, ее диаметр составляет, 11—20 мм; в — III стадия — опухоль распространяется до ствола головного мозга без его компрессии, диаметр составляет 21—30 мм; г — IV стадия — опухоль вызывает компрессию ствола головного мозга, ее диаметр более 30 мм.
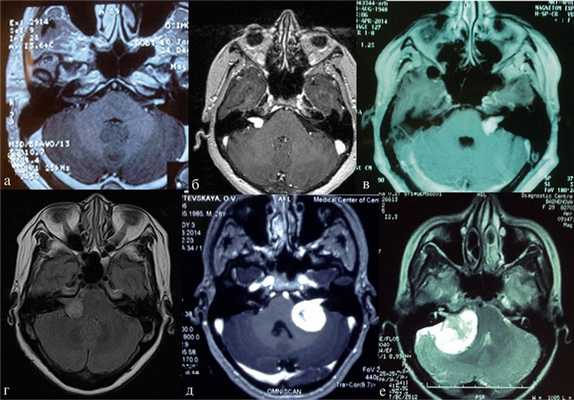
Рис. 2.Классификация неврином слухового нерва по M. Samii. а — Т1 — интрамеатальная опухоль (рис. 2, a); б —Т2 — интра-экстрамеатальная опухоль; в — Т3а — опухоль заполняет мостомозжечковую цистерну; г —Т3b — опухоль распространяется до ствола головного мозга; д —Т4а — опухоль вызывает компрессию ствола; е —Т4b — опухоль грубо деформирует ствол мозга и IV желудочек.
В клинической практике обе эти классификации следует равноценно рассматривать в качестве основных принципов оценки клинической стадии заболевания (опция).
По данным анализа большого массива клинических исследований (663 собственных наблюдения), на сегодняшний день средний размер невриномы слухового нерва составляет 32×30×30 мм. Распределение по стадиям заболевания представлено следующим образом:
Читайте также:
