Торакально-пульмональный комплайнс. Оценка торакально-пульмонального индекса
Добавил пользователь Morpheus Обновлено: 28.01.2026
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Деформация грудной клетки: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Под деформацией грудной клетки понимают различные по степени выраженности изменения формы ее костных структур, в некоторых случаях проявляющиеся не только косметическим дефектом, но и приводящие к функциональным нарушениям со стороны дыхательной и сердечно-сосудистой систем за счет сдавления и смещения органов грудной полости. Грудная клетка - часть туловища, образованная соединенными между собой с помощью суставов грудиной, ребрами, позвонками, а также мышцами.
Иными словами, грудная клетка представляет собой костно-мышечный каркас, защищающий жизненно важные органы от внешних воздействий.
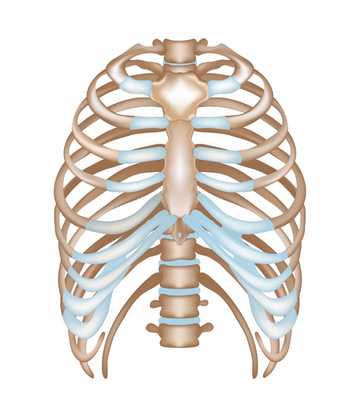
Грудная клетка меняется по мере роста и развития человека, а у взрослых людей ее форма и величина зависят от пола, развития мускулатуры и органов дыхания, рода деятельности, образа жизни. Форма грудной клетки имеет несколько вариантов нормы: плоская, цилиндрическая и коническая.
Разновидности деформаций грудной клетки
Все деформации грудной клетки делят по происхождению на врожденные и приобретенные. К врожденным дефектам относят воронкообразную, килевидную, комбинированную деформации грудной клетки и более редкие дефекты развития. Воронкообразная грудная клетка характеризуется западением грудины и передней грудной стенки. Это самая частая деформация - она составляет около 80% от всех деформаций (встречается в 3 раза чаще у мальчиков) и в 25% случаев носит наследственный характер.
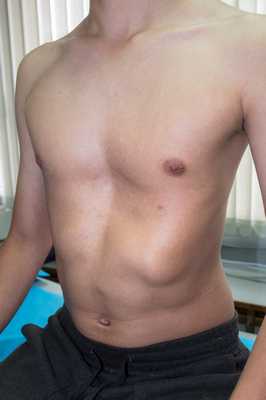
Воронкообразная грудная клетка
Килевидная грудная клетка увеличена в переднезадней своей части, грудина выступает вперед в виде киля. Встречается с частотой от 6 до 20%, чаще у представителей мужского пола.
Приобретенной деформацией грудной клетки может быть ладьевидная, эмфизематозная, или бочкообразная, паралитическая, кифосколиотическая, а также килевидная грудная клетка (рахитическая).
По форме деформации подразделяют на симметричные и асимметричные.
Для определения степени выраженности деформации проводят рентгенографию грудной клетки или компьютерную томографию (КТ).
На рентгенограмме вычисляют отношение наименьшего размера между грудиной и телом позвонка к наибольшему, что является индексом Гижицкой. В зависимости от полученного значения выделяют четыре степени деформации. При проведении компьютерной томографии определяется индекс Галлера (компьютерно-томографический индекс), который равен отношению горизонтального расстояния между внутренней частью ребер к расстоянию между грудиной и телом позвонка в месте наибольшего западения грудины.
По стадии деформации бывают компенсированными, субкомпенсированными и декомпенсированными. При компенсированной деформации косметический дефект незначителен, одышки и учащенного сердцебиения не наблюдается. При субкомпенсированной деформации косметический дефект выраженный, есть одышка и тахикардия при физической нагрузке. При декомпенсированной деформации косметический дефект обезображивающий, одышка и тахикардия присутствуют в покое.
Возможные причины деформации грудной клетки
Врожденные деформации грудной клетки связаны с генетической аномалией развития хрящевой и костной ткани, а также нередко сочетаются с дефектами соединительной ткани (при наследственных заболеваниях: синдромах Марфана, Элерса-Данло и др.). Одни виды деформаций можно диагностировать в грудном или раннем детском возрасте (реберно-мышечный дефект, расщелина грудины). Другие дебютируют и прогрессируют в периоды ускоренного роста организма, в основном такие скачки происходят в возрасте 5-6, 8-10, 13-15 лет.
Приобретенные деформации грудной клетки возникают в результате внешних воздействий (травм, ожогов, оперативных вмешательств, например, по поводу кардиологической патологии) или перенесенных заболеваний (чаще воспалительного характера или инфекционных, связанных с нарушением обмена кальция).
Заболевания, при которых возникает деформация грудной клетки
К заболеваниям, вызывающим деформацию грудной клетки и связанным с нарушением кальциевого обмена, относят рахит.
Рахит - заболевание детского возраста, при котором вследствие различных причин у интенсивно растущего организма возникает полигиповитаминоз с преимущественным снижением уровня витамина D - кости теряют минеральную плотность и деформируются в процессе роста ребенка, грудная клетка приобретает килевидную форму. В настоящее время деформации встречаются реже, т.к. рахит распознается на ранних стадиях.
Для сирингомиелии характерно наличие полости, заполненной жидкостью, расположенной в спинном мозге. Заболевание может возникнуть из-за нарушения развития эмбриона, в связи с родовой травмой, травмой спинного мозга, препятствием оттока спинномозговой жидкости. Стенки полости оттесняют окружающие ткани, которые состоят из нервных клеток и проводящих путей нервной системы. Вследствие этого нарушается иннервация мышц, в том числе образующих каркас грудной клетки. На поздних стадиях это может привести к искривлению позвоночника и формированию ладьевидного вдавления на передней поверхности грудной клетки.
Остеомиелит - инфекционно-воспалительное гнойно-некротическое поражение костной ткани, возбудителями которого могут быть стафилококки, стрептококки, кишечная палочка и др.
Остеомиелит ребер возникает крайне редко, чаще является посттравматическим, реже - бактериальным, когда бактерии попадают в костную ткань с током крови или распространяются контактно (например, при гнойном поражении оболочки легких).
В остром периоде на первый план выступают такие симптомы, как повышение температуры тела до 39-40°C, боль, покраснение, отек в области пораженного ребра.
Среди инфекционных заболеваний особое значение имеет туберкулез. К деформациям грудной клетки может привести не только туберкулез легких (на поздних стадиях), но и туберкулез костей (грудины, ребер, позвонков). Процесс протекает по типу остеомиелита, но вызывает его специфический возбудитель - палочка Коха. При туберкулезе ребер или грудины внешне определяется припухлость и болезненность в области поражения. При туберкулезе позвоночника поражаются и разрушаются тела позвонков, что проявляется болью, на поздних стадиях деформируется позвоночный столб. Заболевание сопровождается повышением температуры тела до 37,2-37,6°С, общим недомоганием, ночной потливостью, отсутствием аппетита, потерей веса.
Эмфизема легких - заболевание, при котором необратимо разрушаются и теряют эластичность стенки альвеол, структурных элементов легочной ткани, нарушается газообмен и возникает повышенная воздушность легких. Эмфизема может возникнуть самостоятельно или на фоне обструктивных болезней легких.
Из-за повышенной воздушности легочной ткани грудная клетка увеличивается в объеме, как бы застывая на вдохе (становится бочкообразной).
При заболеваниях легких и плевры, приводящих к формированию в них соединительной ткани и уменьшению их размеров, грудная клетка деформируется по типу паралитической - уменьшается, уплощается, на стороне поражения втягиваются межреберные промежутки.
К каким врачам обращаться при деформации грудной клетки
Первичную оценку состояния может провести терапевт , врач общей практики, педиатр . При наличии показаний пациента направляют к узким специалистам, таким как хирург, травматолог-ортопед, фтизиатр, онколог, кардиолог , психолог, генетик, эндокринолог , отоларинголог и др.
Диагностика и обследования при деформации грудной клетки
До назначения лечения врачу необходимо оценить вид и форму косметического дефекта, выяснить, когда и при каких обстоятельствах он возник.
Следует обязательно сообщить врачу о других симптомах, если таковые имеются: общей слабости и утомляемости, эпизодах повышения температуры тела, одышке, учащенном сердцебиении.
При необходимости для оценки состояния внутренних органов или уточнения показаний для хирургического лечения специалист назначит дополнительные методы обследования: рентгенографию грудной клетки в двух проекциях с расчетом индексов, общий анализ крови с лейкоцитарной формулой и СОЭ, общий анализ мочи, спирографию, электрокардиографию, эхокардиографию (ЭхоКГ) компьютерную томографию органов грудной клетки и средостения, магнитно-резонансную томографию грудной клетки.
Рентгенологическое исследование структуры легких с целью диагностики различных патологий.
Теоретические и практические аспекты мониторинга торако-пульмонального комплайнса при высокочастотной струйной вентиляции легких
В статье приводятся результаты применения новой версии респиратора для высокочастотной струйной вентиляции легких (ВЧС ИВЛ), позволяющей обеспечить мониторинг статического торако-пульмонального комплайнса ^st) в режиме реального времени. Проведенные исследования на модели легкого и в клинике при проведении ВЧС ИВЛ у 18 больных, перенесших торакальные операции по поводу туберкулеза, опухолей легких и средостения, позволили разработать оригинальные алгоритмы для регистрации auto PEEP и точки на кривой давления, соответствующей нулевому потоку (некое подобие плато), что решило проблему регистрации комплайнса. Клиническая апробация разработанных алгоритмов позволила по-новому оценить физиологическую сущность торако-пульмонального ком-плайнса при ВЧС ИВЛ. В отличие от традиционной вентиляции, при которой снижение Cst указывает на повышение «жесткости» легких (увеличение числа невентилируемых альвеол), снижение Cst при ВЧС ИВЛ, наоборот, свидетельствует о снижении числа невентилируемых альвеол, что сопровождается уменьшением величин дыхательного мертвого пространства, уровня альвеоло-капиллярного шунта и увеличением напряжения кислорода в артериальной крови. Ключевые слова: высокочастотная струйная вентиляция — ВЧС ИВЛ (HFJV), статический торако-пульмо-нальный комплайнс (Cst).
Ключевые слова
Об авторах
Список литературы
2. Jonson B., Lachmann B.Setting and monitoring of high-frequency jet ventilation in severe respiratory distress syndrome. Crit. Care Med. 1989; 17 (10): 1020—1024.
3. Borg U. R., Stoklosa J. C., Siegel J. H. et al.Prospective evaluation of combined high-frequency ventilation in post-traumatic patients with adult respiratory distress syndrome refractory to optimized conventional venti-latory management. Crit. Care Med. 1990; 18 (10): 1187—1190.
5. Ihra G., Gockner G., Kashanipour A., Aloy A.High-frequency jet ventilation in European and North American institutions: developments andclin-ical practice. Eur. J. Anaesth. 2000; 17 (7): 418—430.
6. лярной кинетики газов и использовать ее в коррекции тактических решений при проведении респираторной поддержки у больных с дыхательной недостаточностью.
7. Malarkkan N., Snook N. J., Lumb A. B.New aspects of ventilation in acute lung injury. Anaesthesia, 2003; 58 (7): 647—667.
8. Конторович М. Б., Зислин Б. Д., Чистяков А. В.Устройство для искусственной вентиляции легких. Патент № 60358 от 201.07 //Официальный бюллетень Роспатента №3. 200
9. Конторович М. Б., Зислин Б. Д., Чистяков А. В.Способ искусственной вентиляции лёгких и устройство для его осуществления. Патент № 20000002336859 РФ. // Официальный бюллетень Роспатента №30. 200
11. Терек П., Калит К.Теоретические и клинические основы высокочастотной струйной вентиляции. Екатеринбург: АМБ; 2005.
BTS-British Thoracic Society — руководство по ведению легочных узлов, выявленных вне и во время скрининга.
В данной статье представлены рекомендации Британского торакального общества (BTS) по тактике ведения пациентов с легочными узлами [1] от 2015 года.
Важной информацией из данной рекомендации является:
- Для проведения повторного исследования узел должен составлять в размерах ≥⩾ 5мм или ⩾ 80mm3
- Сокращение периода повторного исследования до одного года для солидных узлов (5-6 мм).
- Данное руководство предусматривает две модели прогнозирования малигнизации при оценке легочных узлов.
- Данная рекомендация подходит, как к случайно выявленным узлам, так и к узлам выявленные в момент скрининга.
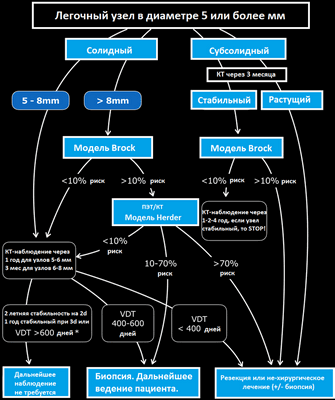
Представлена схема тактики ведения пациента, согласно рекомендациям Британского торакального общества.
Шаг 1
Повторное исследование не требуется, если узел в размерах < 5mm и для узлов, в которых присутствуют паттерн доброкачественной кальцификации и для таких типичных узлов, как гамартомы и перифиссуральные узлы.
Шаг 2
Повторное исследование требуется, если узел в размерах более, чем 5 мм. Принято разделять узлы на солидные и субсолидные (частично солидные и по типу матового стекла).
Шаг 3
Используйте модель Brock для оценки риска малигнизации солидных узлов в размерах более 8 мм и субсолидных узлов, которые стабильны в размерах в течение трех месяцев.
Шаг 4
Используйте модель Herder в случае, если требуется ПЭТ/КТ для оценки узла.
При использовании волюметрии повторные исследования проводятся в течение года, а при оценке узла в 2D режиме повторные исследования проводятся в течении 2 лет согласно рекомендациям BTS.
Узлы, которые в течение повторных исследований в размерах уменьшились более чем на 25%, рассматривают, как стабильные. Относите узлы к стабильным только, если показатель удвоения объема составляет >600 дней, при оценке волюметрии.
Оценка риска развития рака, основана на сравнении полученного и предшествующего исследования, используя (VDT-volume double time) показатель удвоения объема за период времени.
5.3. Мониторинг дыхания (респираторный мониторинг).
Понятие респираторного мониторинга включает мониторинг газообмена, а также мониторинг механики легких и грудной клетки.
5.3.1.Мониторинг газообмена
Мониторинг газообмена подразумевает анализ газового состава артериальной и венозной крови, а также выдыхаемого воздуха. Для оценки адекватности газообмена имеет значение определение рН, концентрации бикарбонатов и величины анионного провала. С дидактической точки зрения, можно разделить мониторинг газообмена на мониторинг оксигенации и мониторинг вентиляции.
Мониторинг оксигенации
При проведении мониторинга оксигенации врач должен получить ответы на три вопроса:
•Сколько кислорода может быть доставлено к тканям?
•Какой ценой достался этот кислород организму?
•Как его усвоили ткани?
Для ответа на первый вопрос оценивают напряжение кислорода (рaО2) и насыщения (сатурации) гемоглобина кислородом в артериальной крови (SaО2). Зная эти величины, по формуле рассчитывают содержание кислорода в артериальной крови (Cа - content arterial)
Cа = (0,00138 × SatО2 × Hb) + (0,003 × рa О2)
Умножая эту величину на величину сердечного выброса (CO - cardiac output), измеренного, например, методом термодилюции, можно рассчитать доставку кислорода (DО2 - delivery of oxygen) к тканям:
Не зная, какую долю сердечного выброса получает каждый отдельный орган (например, мозг), нельзя подсчитать, какое точное количество кислорода ему достается.
Для ответа на второй вопрос сравнивают напряжение кислорода в артериальной крови (рaО2) и в воздухе альвеол (РАО2). Величину РАО2 можно или измерить прямо, или рассчитать из так называемого уравнения альвеолярного газа. Прямое измерение возможно при помощи метода быстрой оксиметрии. При использовании этого метода непрерывно измеряют напряжение кислорода во вдыхаемом и выдыхаемом газе. Приборы, предоставляющие возможность измерения этих показателей, обладают низкой инерционностью, оцениваемой по очень быстрому времени отклика (600 мсек и менее).
Для определения РАО 2 интерес представляют конечные порции выдыхаемого газа, то есть фактически газ, выдыхаемый из альвеол. Эффективность обмена кислорода оценивается на основе расчета альвеолоартериального градиента по кислороду:
Р(А- а)О2
Этот показатель имеет нелинейный характер даже у здорового человека и зависит от содержания кислорода во вдыхаемой смеси (FiО2.): при дыхании воздухом он равен 10, при дыхании 100%-ным кислородом - около 100. Кроме того, он зависит от нарушений вентиляционно-перфузионных отношений и изменений венозной сатурации.
Для оценки эффективности кислородообмена большее практическое значение имеет расчет индексов оксигенации. Один из наиболее часто используемых индексов рассчитывается как частное от деления напряжения кислорода в артериальной крови к процентному содержанию кислорода во вдыхаемой смеси, выраженному в долях единицы:
рaО2 / FiО2
В норме этот показатель превышает 350-400 мм рт.ст. Снижение его ниже 300 мм рт.ст. является признаком острого повреждения легких, ниже 200 мм рт.ст. - острого респираторного дистресс-синдрома.
Расчет РАО 2 возможен с помощью уравнения альвеолярного газа, которое с этой целью используется в упрощенном варианте.
Немного физиологии
Уравнение альвеолярного газа в полной его форме представляет собой следующее математическое выражение:
РАО2 = РIО2 - (PAСО2 /RQ) +(PAСО2 × FiО2 × (1 - RQ)/RQ),
где РАО2 - напряжение кислорода в альвеолярном газе, PAС О2 - напряжение углекислоты в альвеолярном газе, РIО2 - напряжение кислорода во вдыхаемом воздухе, FiО2 - доля кислорода во вдыхаемом воздухе, RQ - респираторный коэффициент (respiratory quotent).
Обычно это уравнение используют для расчета респираторного коэффициента, а не РАО2. Данный коэффициент зависит от сопряжения процессов потребления кислорода и выделения углекислоты периферическими тканями, что определяется характером использующихся нутриентов - белков, жиров или углеводов. Он самый высокий при использовании углеводов (1,0), самый низкий при преимущественном поступлении в организм жиров (0,7).
Напряжение кислорода во вдыхаемом воздухе рассчитывается следующим образом:
РIО2 = (барометрическое давление - 47) × FiО2
Величины РАО2 и PAСО2 измеряют прямо в конечно-выдыхаемых порциях дыхательной смеси (то есть в альвеолярном воздухе) методами капнографии и быстрой оксиметрии.
Используя уравнение альвеолярного газа, можно рассчитать респираторный коэффициент, то есть фактически поглощение кислорода и выделение углекислоты на единицу объема вдыхаемого и выдыхаемого воздуха. Сопоставив эти показатели с величиной минутного объема вентиляции, можно оценить величину потребления организмом энергии и подобрать эффективную нутритивную поддержку.
Если величину респираторного коэффициента считать неизменной в течение коротких промежутков времени, то уравнение альвеолярного газа упрощается:
РАО2 = РIО2 - (1,25 × PAСО2),
Измеряя конечно-выдыхаемые величины PAСО2, можно вычислить РАО2. Из этого уравнения следует, что в норме при дыхании воздухом РАО2 равно 100-110 мм рт.ст., при дыхании чистым кислородом - 550 мм рт.ст.
Для ответа на третий вопрос оценивают потребление кислорода и эффективность его обмена. Потребление кислорода может быть рассчитано при помощи прямого и обратного методов Фика.
При использовании прямого метода Фика необходимо измерение напряжения кислорода в воздухе альвеол (РАО2) с помощью метода быстрой оксиметрии. Зная напряжение кислорода во вдыхаемом воздухе (РIО2) и в выдыхаемом воздухе (РА О2), измерив минутный объем дыхания с помощью спирометрии, можно рассчитать количество поступившего в организм и оставшегося в легких кислорода. Вычитая из первой величины вторую, рассчитывают потребление кислорода.
При использовании непрямого метода Фика потребление организмом кислорода является производным сердечного выброса и разницы в содержании кислорода в артериальной (Cа) и венозной (Сv) крови
Содержание кислорода в венозной крови считают по той же формуле, что и Ca, только используют показатели напряжения кислорода и сатурации гемоглобина не в артериальной, а в венозной крови.
Сv = (0,003 х рvО2) + (0,00138 х SvО2 х Hb)
Напряжение кислорода в артериальной и венозной крови, а также сатурацию гемоглобина измеряют инвазивными и неинвазивными способами. При инвазивных способах возможна дискретная и непрерывная оценка. При дискретной оценке повторно исследуют кровь из артерии или вены в газоанализаторе. Для непрерывной оценки SvО2 используют фиброоптические катетеры. Чтобы определить потребление кислорода для всего организма, этот катетер устанавливают в легочную артерию, то есть в сосуд, содержащий смешанную венозную кровь от всего организма. Необходимо предостеречь от использования для анализа крови, взятой из периферической вены. Эта кровь отражает доставку и потребление кислорода только в том периферическом участке, от которого она оттекает, и не может служить средством оценки оксигенации венозной крови в целом. В отличие от венозной, артериальная кровь практически одинакова в любой артерии, и поэтому нет разницы, что анализировать - кровь из аорты, сонной или лучевой артерии.
Кроме описанных методов, возможно также чрескожное (транскутанное) определение р О2 (как впрочем и рСО2), при помощи специальных датчиков с прогреванием кожи под ними. Показания этих датчиков хорошо согласуются с прямым определением рО2 и рСО2 в артериальной крови у детей. Однако нет единого мнения исследователей в вопросе, можно ли метод применять у взрослых пациентов.
Для неинвазивной оценки сатурации гемоглобина артериальной крови используют пульсоксиметрию. Принцип пульсоксиметрии основан на пропускании через ткани пальца или мочки уха параинфракрасного излучения. Излучение частично проходит через ткани, частично задерживается оксигенированным гемоглобином. Величина поглощенного излучения непрерывно меняется с каждым пульсовым сокращением. Анализ этой изменяющейся величины составляет основу пульсоксиметрической оценки сатурации гемоглобина артериальной крови (рис. 5.16).
Измерение потребления и доставки кислорода позволяет оценить зависимость первого показателя от второго. В норме потребление не зависит от доставки. Однако если доставка снижается, то наступает определенный момент, когда потребление тоже начинает снижаться. В тканях постепенно прекращаются зависимые от кислорода процессы (цикл трикарбоновых кислот) и нарастает накопление лактата из-за незавершенного анаэробного гликолиза. Эти взаимоотношения отображаются характерной кривой (рис. 5.17). Большинство исследователей считает, что при сепсисе эта кривая смещается вправо, отражая нарушение утилизации кислорода тканями.
Для изучения указанных процессов нужны независимые методы оценки потребления кислорода (прямой метод Фика с использованием быстрой оксиметрии и спирометрии) и доставки кислорода (непрямой метод Фика с использованием термодилюции и анализа газового состава крови). В ряде научных исследований авторы пытаются получить информацию о доставке и потреблении, используя для измерения и того, и другого показателя только один непрямой метод. Такой подход является методологически неправильным, так как нельзя изучить зависимость или независимость этих двух показателей, сам процесс измерения которых (одним методом!) делает их зависимыми друг от друга.
Мониторинг вентиляции
Мониторинг вентиляции чаще всего сводится к анализу содержания углекислого газа в выдыхаемом воздухе с помощью капнографии и прямому определению напряжения СО2 в крови с использованием газоанализатора.
При проведении анализа содержания углекислого газа нужно соблюдать ряд методологических условий. Главное из них - необходимость определенного промежутка времени перед проведением анализа после изменения параметров вентиляции легких. В организме существуют большие резервуары углекислоты с различной емкостью и скоростью наполнения и высвобождения СО2. Это приводит к значительной отсрочке стабилизации уровня СО2 - через 10 мин после гипервентиляции и 40 мин после гиповентиляции (J.J. Marini, A.P. Wheeler, 1997).
Прямое определение рСО2 в артериальной крови производят обычно одновременно с определением рО2 при заборе проб артериальной крови. Динамический контроль напряжения углекислого газа можно проводить, используя пробы венозной крови, где рСО2 обычно выше на 3-8 мм рт.ст., чем в артерии. Для анализа берут кровь из центральной вены или легочной артерии, но не из периферической вены.
При анализе выдыхаемого газа концентрация СО2 чаще всего представляют в качестве функции времени, реже - функции объема выдыхаемого газа. Изменения СО 2 во времени менее информативны, однако позволяют оценить степень нарушения вентиляционно-перфузионных отношений по форме кривой, мониторировать ритм дыхания, определить наличие гипо- и гипервентиляции (рис. 5.18). При отсутствии изменений нормальной кривой можно оценить напряжение углекислого газа в артериальной крови (рaСО2) по его напряжению в конечно-выдыхаемых (end tidal) порциях альвеолярного воздуха (рETСО 2 ). В норме величина градиента рaСО 2 - рETСО 2 равна 3-8 мм рт.ст. При развитии грубых нарушений вентиляционно-перфузионных отношений (ТЭЛА, ОРДС, аспирации крови и желудочного содержимого в трахею) этот градиент значительно возрастает. Изменяется также форма кривой напряжения углекислого газа в конечно-выдыхаемом воздухе. Минимизация величины рaСО 2 - рETСО 2 может использоваться как метод подбора оптимального РЕЕР.
Более информативно представление концентрации СО 2 в качестве функции объема выдыхаемого газа. Это позволяет определить, кроме указанных показателей, также среднюю концентрацию СО 2 в выдыхаемом газе и рассчитать величину дыхательного мертвого пространства, соотнесенного с дыхательным объемом (рис. 5.19).
Мониторинг механических свойств легких и грудной клетки
Показатели, имеющие клиническое значение для оценки динамики легочных нарушений - податливость (compliance - С), сопротивление (resistance - R), среднее давление в дыхательных путях (mPaw) и аутоРЕЕР.
Податливость.
Податливость - это изменение объема (volume, V), соотнесенное к изменениям давления (pressure, P):
С = ∆V/ ∆P.
Различают податливость легких (СL), грудной клетки (СW) и респираторной системы (СRS), но на практике оценивают обычно только последний показатель. Для расчета величины ∆V при проведении ИВЛ следует учитывать потери части дыхательного объема (VT) в контуре респиратора. Для приблизительного расчета используют специальную величину - фактор компрессии дыхательного контура (circuit compression factor - Сcf). Для большинства дыхательных контуров она считается равной 3 мл кислородно-воздушной смеси на каждый сантиметр водного столба пикового давления, подаваемого респиратором при вдохе.
Для измерения податливости нужно «выключить» с помощью медикаментов спонтанное дыхание больного и измерить давление в дыхательных путях во время пауз вдоха и выдоха (создать так называемые пассивные условия). Для чего нужны эти паузы? Нас интересует давление во всей респираторной системе, но измерить можно только давление на конце интубационной трубки. Чтобы это измеряемое давление отражало показатели давления в альвеолах, в бронхах, трахее и у конца интубационной трубки, создаются короткие паузы в конце вдоха и выдоха. Вследствие этого величины давления в разных частях респираторной системы временно уравниваются. Податливость респираторной системы определяется следующим образом:
СRS = VT × Сcf / PplatoInsp - PplatoExsp,
где PplatoInsp - давление на плато вдоха (inspiration) в условиях окончания вдоха и остановки потока, PplatoExsp - давление на плато выдоха (expiration) в условиях окончания выдоха и остановки потока (рис. 5.20). Нижняя граница нормы для величины податливости системы грудная клетка-легкие - 120-150 мл/см вод. ст. или 1,5-2 мл/см вод.ст на 1 кг массы тела.
Для раздельной оценки податливости грудной клетки и легких необходимо дополнительное измерение давления в пищеводе, которое отражает внутриплевральное давление. В настоящее время средствами раздельной оценки податливости легких и грудной клетки снабжены некоторые современные аппараты ИВЛ, что позволяет оптимизировать проведение респираторной поддержки при тяжелых дыхательных расстройствах.
Сопротивление
Различают инспираторное сопротивление дыхательных путей и экспираторное. Экспираторное сопротивление всегда больше, чем инспираторное, причем эта разница возрастает при патологии. Однако на практике обычно оценивают только инспираторное сопротивление (рис. 5.21):
RI = PD - PplatoInsp /Flow,
где RI - инспираторное сопротивление, Flow - поток (обычно пиковый поток респиратора), PD - пиковое давление в дыхательных путях, PplatoInsp - давление на плато вдоха (в условиях окончания вдоха и остановки потока). Верхняя граница инспираторного сопротивления - 5 см вод.ст./л∙сек. Увеличение инспираторного сопротивления свидетельствует об ухудшении проходимости трахео-бронхиального дерева из-за бронхоспазма, отека, скопления мокроты.
Среднее давление в дыхательных путях
С некоторой долей упрощения можно считать, что среднее давление в альвеолах (alveolar mean pressure, mPalv) соответствует среднему давлению в дыхательных путях (airways mean pressure, mPaw). Среднее давление в альвеолах - это усредненное давление, которое растягивает альвеолы и грудную клетку. Следовательно, mPalv и mPaw определяют артериальную оксигенацию и сопротивление венозному возврату. Для клинических целей нужно понимать, что mPaw увеличивается при возрастании минутного объема дыхания, положительного давления в дыхательных путях в конце выдоха (positive end-expiratory pressure, РЕЕР) и времени вдоха. Эти факторы, с одной стороны, повышают оксигенацию, с другой - снижают венозный возврат и повышают опасность баро- и волюмотравмы легких.
АутоРЕЕР
АутоРЕЕР представляет собой разницу между общим (тотальным) РЕЕР и установленным врачом на панели респиратора показателем положительного давления в дыхательных путях к концу выдоха. Тотальный РЕЕР определяют по показаниям манометра респиратора в конце вдоха при создании экспираторной паузы. Наличие аутоРЕЕР свидетельствует о затруднении выдоха (рис. 5.22). Имеется две основные причины этого состояния. Первая причина - повышение сопротивления в дыхательных путях во время выдоха, вследствие чего вдох начинается при не полностью законченном выдохе. Такая ситуация вызывает постепенное нарастание количества воздуха, задержанного в легких - так называемую дыхательную гиперинфляцию (рис. 5.23). Вторая причина аутоРЕЕР - появление активности мышц вдоха во время не полностью закончившегося выдоха. Мышечная активность отражает несинхронность работы аппарата ИВЛ и дыхательных попыток больного.
Первую причину аутоРЕЕР можно компенсировать увеличением пикового потока вдоха на панели респиратора. Это приводит к укорочению времени вдоха и удлинению времени выдоха. В результате пациент успевает выдохнуть до того, как наступит новый вдох. Причиной гиперинфляции может быть нерациональное использование паузы вдоха, что вызывает избыточное удлинение фазы вдоха. Это состояние компенсируется при исключении паузы вдоха.
Во втором случае появление аутоРЕЕР свидетельствует о нерациональном подборе режимов вентиляции, причиной чего могут быть недостаточные минутный объем дыхания, чувствительность триггера, содержание кислорода во вдыхаемой смеси, аппаратный РЕЕР. Одним из способов подбора оптимального аппаратного РЕЕР является его постепенное повышение до того уровня, когда исчезает аутоРЕЕР.
Расчет податливости, сопротивления, среднего давления в дыхательных путях и аутоРЕЕР производится на основе анализа обычных кривых, отражающих изменение давления в дыхательных путях, объема и потока газа во времени: кривые «давление в дыхательных путях - время», «поток воздуха - время», «объем воздуха - время» (рис. 5.23) Современные респираторы позволяют получать информацию также в виде петель давление-объем (P-V-петля) и поток-объем (F-V-петля) (рис. 5.24).
Принципиально новой информации они не несут, но делают ее представление более наглядным. Например, появление характерного «клюва» на петле давление-объем свидетельствует о снижении податливости легких и их перерастяжении вдуваемым дыхательным объемом. Разорванность петли поток-объем свидетельствует о наличии утечек в контуре аппарата ИВЛ.
Синдром респираторного расстройства [дистресса] у взрослого (J80)
В 1994 г. на Американо-Европейской согласительной конференции (АЕСК) было предложено следующее определение острого респираторного дистресс-синдрома:
Помимо этого, на AECK было предложено выделять две формы данного заболевания:
1. Острое повреждение легких (ОПЛ) (acute lung injury), которое включает в себя как начальный, более легкий, этап заболевания, так и наиболее тяжелые формы.
2. Собственно ОРДС, являющийся наиболее тяжелым заболеванием.
Таким образом, любой ОРДС можно отнести к ОПЛ, но не все формы ОПЛ являются ОРДС.
В 2012 г. Европейское общество интенсивной терапии (ESICM) иницировало новый подход к проблеме, результатом которого стало так называемое Берлинское соглашение (консенсус) по ОРДС. Согласно этому соглашению, ОРДС получил новое определение:
Острый респираторный дистресс-синдром - это острое, диффузное, воспалительное поражение легких, ведущее к повышению проницаемости сосудов легких, повышению массы легких и уменьшению аэрации легочной ткани.
Основные клинико-физиологические звенья: гипoксемия и двусторонние инфильтраты на рентгенограмме органов грудной клетки, увеличение венозного шунтирования, рост физиологического мертвого пространства, снижение податливости легочной ткани.
Термин "острое повреждение легких" был исключен, ввиду того, что многие клиницисты на практике стали так называть любую нетяжелую гипоксемию.
Примечание. В связи с изменением определения и отсутствием исследований, соответствующих новым критериям, далее в тексте рубрики иногда будет встречаться старый термин ОПЛ (СОПЛ).
Период протекания
Чаще всего почти у всех пациентов между фактором, вызвавшим поражение, и ОРДС, проходит не менее 72 часов и не более 7 дней.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Согласно Берлинскому консенсусу ESICM - 2012, имеются три взаимоисключающие формы острого респираторного дистресс-синдрома:
- легкий;
- средней тяжести;
- тяжелый.
Разделение на указанные выше формы осуществляется по тяжести нарушения оксигенации (гипоксемии):
2. Умеренная: 100 мм рт.ст. < PaO2/FiO2 ≤ 200 при ПДKВ или CPАP ≥ 5 см вод.ст.
3. Тяжелая: PaO2/FiO2 ≤ 100 при ПДKВ или CPАP ≥ 5 см вод.ст.
Этиология и патогенез
Острый респираторный дистресс-синдром (ОРДС) может быть следствием “прямого” или “непрямого” повреждения легких.
“Непрямой” механизм ОПЛ/ОРДС связан с внелегочными заболеваниями, при которых в результате системной воспалительной реакции организма возникает повреждение легких. То есть повреждение легких ассоциировано с повреждающими эффектами цитокинов и других биохимических и клеточных медиаторов.
Примечания:
1 Сепсис с двумя или более факторами из группы "А" + один или более признаков из группы "Б". Наибольшая вероятность развития ОРДС (23% против 8%) возникает при сепсисе вызванном грамнегативной флорой.
Группа признаков "А":
- температура выше 38,5 о или ниже 36 о;
- число лейкоцитов более 12х10 9 /мкл или менее 3х10 9 /мкл;
- установленный гнойный очаг;
- выделение гемокультуры.
Группа признаков "Б":
- артериальная гипотония в течение 2 и более часов, систолическое артериальное давление < 80 мм.рт. ст.;
- необходимость применения ионотропных средств для поддержания среднего АД > 85 мм.рт.ст;
- метаболический ацидоз - ВЕ менее 5 ммоль/л;
| Риск | Fowler, 1983 | Shelling, 1998 | Hudson, 1995 |
| Бактериемия | 3,8 | ||
| Сепсис | 28,8 | 41,2 | |
| Травма | 33,3 | 25,5 | |
| Переломы | 5,3 | 11,1 | |
| Контузия легких | 21,8 | ||
| Ожоги | 2,3 | ||
| Тяжелая пневмония | 11,9 | 27,3 | |
| ДВС-синдром | 22,2 | ||
| Аспирация | 35,6 | 22,0 | |
| Утопление | 33,3 | ||
| Передозировка наркотиков | 8,5 | ||
| Неизвестная причина | 22,7 | 10,6 | 21,1 |
Воспаление при ОРДС проходит следующие патофизиологические стадии:
Механика дыхания
У пациентов с ОРДС наблюдаются выраженные изменения механики дыхания.
Статический комплаенс респираторной системы (Crs), представляющий собой изменение легочного объема на заданное изменение транспульмонального давления, у больных ОРДС практически всегда снижен.
Согласно исследованиям, в которых использовались пищеводные катетеры, легочный комплаенс CL также снижен до 32-72 мл/см H2O (40-60% от нормы), комплаенс грудной клетки Ccw составляет 59-147 мл/см H2O (50-80% от нормы). Ccw снижен вследствие нарушений эластических свойств грудной клетки и стенок брюшной полости (повышение давления в брюшной полости и повышение ригидности стенок).
Поскольку статический комплаенс не дает информации о региональных особенностях легких у больных ОРДС, большое значение приобретает оценка кривой “давление-объем”. Данная кривая обычно строится во время инфляции в дыхательные пути последовательных порций заданных объемов с помощью большого шприца (super-syringe method).
Полученная кривая имеет два “колена”: нижнее “колено” (low inflection point) и верхнее “колено” (upper inflection point). Считается, что альвеолы находятся в спавшемся, коллабированном состоянии при уровне давления менее точки нижнего “колена”; альвеолы перерастянуты при давлении больше точки верхнего “колена”. В идеале во время респираторной поддержки колебания положительного давления в дыхательных путях больного должны происходить между точками верхнего и нижнего “колен”.
При ОРДС также, как правило, значительно повышены все компоненты сопротивления в дыхательных путях. Такие изменения обусловлены накоплением клеточных элементов и жидкости в дыхательных путях, отеком бронхов, бронхиальной гиперреактивностью, уменьшением легочных объемов и количества функционирующих дыхательных путей.
Легочная гемодинамика
Повышение давления в легочной артерии - достаточно типичный признак ОРДС. Среднее давление в легочной артерии обычно составляет около 30 мм рт. ст. Вследствие легочной гипертензии у больных ОРДС возникают нарушение функции правого желудочка, снижение сердечного выброса и снижение транспорта кислорода к тканям. Легочная гипертензия также может выступать дополнительным фактором развития полиорганной недостаточности.
Легочная гипертензия при ОРДС, как правило, имеет мультифакторный генез: гипоксическая вазокoнстрикция, вазоспазм, вызванный вазоактивными медиаторами (тромбоксан, лейкотриены и эндотелин), внутрисосудистая обструкция тромбоцитарными тромбами и периваскулярный отек.
На поздних этапах ОРДС большую роль могут играть такие механизмы, как фиброз и облитерация легочных сосудов (ремоделирование).
Эпидемиология
Заболеваемость острым респираторным дистресс-синдромом (ОРДС) варьирует в широких пределах, частично вследствие того, что при исследованиях использовались различные определения этого заболевания. Статистика из США и статистика, приведенная в международных исследованиях, могут, хотя и не бесспорно, прояснить истинную частоту этого заболевания.
В 1970-х годах, когда Национальный Институт Здоровья (NIH) начал изучение ОРДС, по некоторым оценкам, ежегодная частота составляла 75 случаев на 100000 населения. Данные, полученные в последнее время из NIH-спонсируемых исследований ОРДС, позволяют предположить, что частота ОРДС на самом деле может быть выше первоначальной оценки. В проспективном исследовании с использованием критериев Американо-Европейской согласительной конференции (АЕСК) 1994 года выявлено, что с поправкой на возраст заболеваемость острым повреждением легких (ОПЛ) составляет 86,2 на 100000 человеко-лет. С возрастом заболеваемость увеличивается до 306 случаев на 100000 человеко-лет для людей в возрасте 75-84 лет.
На основании этих статистических данных, по оценкам экспертов, в США ежегодно регистрируется 190 600 случаев ОРДС и что эти случаи связаны с 74500 смертей.
В первом исследовании с использованием критериев AECK 1994 года в Скандинавии, годовой показатель составил 17,9 случаев ОПЛ на 100000 населения и 13,5 случаев ОРДС на 100000 населения.
Российская Федерация
При острой хирургической и соматической патологии синдром ОПЛ развивается в среднем у 15,4±3,6% больных, а ОРДС - у 11,7±4,7%.
В различных регионах Российской Федерации частота ОРДС у взрослых в 2001-2002 годах находилась в пределах 4,8±0,9 - 7,5±0,9 случаев на 100 000 населения в год. На 1000 больных, переводимых в отделения анестезиологии и реанимации клинических медицинских учреждений, в год частота ОРДС достигала 22,7±8,6%.
ОРДС может возникнуть у людей любого возраста. Его частота увеличивается с возрастом, от 16 случаев на 100000 человеко-лет у лиц в возрасте 15-19 лет до 306 случаев на 100000 человеко-лет у лиц в возрасте 75 и 84 лет. Распределение по возрасту отражает заболеваемость в связи с основными причинами развития ОРДС.
Для ОРДС, связанного с сепсисом и большинством других причин, никаких различий в заболеваемости между мужчинами и женщинами по всей видимости, не существуют. Тем не менее, только у травматологических больных , заболеваемость может быть немного выше среди женщин.
Приблизительное распределение по тяжести ОРДС (согласно анализу баз данных при выработке Берлинского соглашения 2012 года):
- легкий ОРДС ((по сути - ОПЛ из старой классификации)) - 22% больных клинической базы данных (95% ДИ 21-24%);
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
диспноэ, дискомфорт в грудной клетке, сухой кашель, цианоз, тахипноэ, тахикардия, участие в дыхании вспомогательных мышц, диффузная крепитация, жесткое, а иногда и бронхиальное “амфорическое” дыхание; расстройство сознания.
Cимптомы, течение
Возникновение острого респираторного дистресс-синдрома (ОРДС) наиболее часто происходит в первые 12-48 часов от начала развития основного заболевания или события. В ряде случаев возможно развитие ОРДС и спустя 5 дней.
Облигатный признак ОРДС - гипоксемия (SpO2 ниже 90%, часто - ниже 75%).
Больные с ОРДС практически всегда рефрактерны к терапии кислородом, что отражает основной механизм нарушения газообмена при ОРДС - развитие внутрилегочного шунта.
Диагностика
Критерии Delphi - 2005
4. Некардиогенный характер определяется по субъективным признакам (отсутствие клиники сердечной недостаточности).
Диагноз ОРДС, согласно критериям Delphi, выставляется при наличии первых четырех признаков + один признак 5а или 5b.
1. Временной интервал: возникновение синдрома (новые симптомы или усугубление симптомов поражения легких) в пределах одной недели от момента действия известного причинного фактора.
3. Механизм отека: дыхательную недостаточность нельзя объяснить сердечной недостаточностью или перегрузкой жидкостью. Если факторов риска сердечной недостаточности нет, необходимы дополнительные исследования, прежде всего эхокардиография.
4. Нарушение оксигенации (гипоксия):
- легкая: 200 мм рт.ст. < PaO2/FiO2 ≤ 300 при ПДКВ или CPAP ≥ 5 см вод.ст.;
- умеренная: 100 мм рт.ст. < PaO2/FiO2 ≤ 200 при ПДКВ или CPAP ≥ 5 см вод.ст.;
- тяжелая: PaO2/FiO2 ≤ 100 при ПДКВ или CPAP ≥ 5 см вод.ст..
Примечания к методам диагностики ОРДС, согласно Берлинским соглашениям - 2012
Визуализация
Рентгенологическое исследование имеет меньшую диагностическую ценность по сравнению с компьютерной томографией (КТ и КТВР КТВР - компьютерная томография высокого разрешения
).
Тяжелый ОРДС предполагает затемнение минимум 3-4 полей.
Характерная рентгенологическая находка - возникновение картины “матового стекла” и диффузных мультифокальных инфильтратов довольно высокой плотности с хорошо очерченными воздушными бронхограммами, то есть развитие обширного поражения паренхимы легких.
Часто может визуализироваться небольшой плевральный выпот.
Определенные трудности возникают при дифференциации рентгенографической картинй ОРДС с кардиогенным отеком легких. В пользу ОРДС свидетельствуют:
- более периферическое расположение инфильтративных теней;
- нормальные размеры сердечной тени;
- отсутствие или небольшое количество линий Керли Линии Керли - горизонтальные линейные тени на рентгенограмме нижних отделов легких, наблюдаемые при уплотнении (отеке) междольковых перегородок, например у больных с легочной гипертензией
типа В (короткие, параллельные, располагающиеся на периферии легких).
На рентгенологическую картину ОРДС могут влиять терапевтические вмешательства. Например, избыточное введение растворов может привести к усилению альвеолярного отека и усилению выраженности рентгенологических изменений; терапия диуретиками, наоборот, может уменьшить рентгенологические изменения. Уменьшение регионарной плотности легких, приводящее к ошибочному впечатлению об улучшении патологического процесса, может быть вызвано искусственной вентиляцией легких (в особенности при использовании РЕЕР), которая повышает среднее давление в дыхательных путях и инфляцию легких.
На поздних этапах развития ОРДС очаги консолидации сменяются интерстициальными изменениями, возможно появление кистозных изменений.
Компьютерная томография (КТ) позволяет получить данные, которые не могут быть получены при обычной рентгенографии. В частности, получить дополнительную информацию о степени и протяженности поражения паренхимы легких, а также выявить наличие баротравмы Баротравма - повреждение воздухсодержащих органов (ухо, придаточные пазухи носа, легкие), вызванное разницей давлений между внешней средой (газ или жидкость) и внутренними полостями
или локализованной инфекции.
Ранние КТ-исследования структуры легких показали, что локализация легочных инфильтратов носит пятнистый, негомогенный характер, причем существует вентрально-дорсальный градиент легочной плотности:
- нормальная аэрация легочной ткани в вентральных (так называемых независимых) отделах;
- картина “матового стекла” в промежуточных зонах;
- плотные очаги консолидации в дорсальных (зависимых) отделах.
Возникновение плотных очагов в дорсальных отделах обусловдено зависимым от силы тяжести распределением отека легких и, в большей степени, развитием “компрессионных ателектазов” зависимых зон вследствие их сдавления вышележащими отечными легкими.
Из критериев диагностики в Берлинских соглашениях - 2012 устранено давление в левом предсердии, поскольку в настоящее время редко используют соответствующий катетер.
Предполагать развитие ОРДС возможно в тех случаях, когда нарастающая дыхательная недостаточность не может быть объяснена сердечной недостаточностью и перегрузкой жидкостью.
В случае отсутствия явной причины ОРДС требуется проведение дополнительных исследований. Например, эхокардиоскопии для исключения застоя в легких.
Оксигенация. Согласно Берлинским соглашениям - 2012, минимальный уровень ПДКВ, при котором замеряется отношение PaO2/FiO2, составляет 5 см вод. ст., для тяжелого ОРДС - 10 см вод.ст.
Дополнительные показатели
Поскольку измеить мертвое пространство в клинике нелегко, специалисты рекомендуют использовать взамен минутную легочную вентиляцию, стандартизированную к PaCO2 40 мм рт.ст. (VECORR = МВЛ * PaCO2/40). Для определения ОРДС предложено использовать высокую VECORR > 10 л/мин. или низкий комплайенс (< 40 мл/см.вод.ст.), или и то, и другое вместе.
Согласно Берлинским соглашениям - 2012, результаты регистрации массы легких по результатам КТ, маркеры воспаления и прочие методы, использовавшиеся ранее для оценки повышенной проницаемости капилляров являются малодоступными и зачастую опасными для больного в критическом состоянии часто опасными, поэтому эксперты пришли к заключению, что особой пользы это не принесет.
Лабораторная диагностика
Лабораторные признаки малоспецифичны для ОРДС. За исключением кислотно-щелочного состояния (КЩС), большинство лабораторных признаков связаны с основным заболеванием, поскольку ОРДС часто сопутствует системной воспалительной реакции организма на инфекцию или другие факторы.
2. Общий анализ крови:
- лейкоцитоз или лейкопения;
- анемия;
- нередко - тромбоцитопения, отражающачя системную воспалительную реакцию или повреждение эндотелия.
3. Биохимия: возможно выявление недостаточности функции печени (цитолитиз, холестаз) или почек (повышение креатинина, мочевины). это связано с тем, что ОРДС часто является проявлением полиорганной недостаточности.
4. Бронхоальвеолярный лаваж. В первые дни заболевания характерной находкой у больных ОРДС является высокое содержание нейтрофилов - более 60% (в норме менее 5%), которое по мере обратного развития заболевания уступает место альвеолярным макрофагам.
Дифференциальный диагноз
Проводят дифференциальную диагностику ОРДС со следующими заболеваниями:
1. Кардиогенный отек легких. Для исключения данного заболевания проводится эхокардиография.
2. Острая интерстициальная пневмония является редкой и быстро прогрессирующей формой поражения легких. Характерные проявления: эозинофилия и нейтрофилия жидкости, полученной при бронхоальвеолярном лаваже (БАЛ). Для подтверждения диагноза проводят патогистологическое исследование.
3. Идиопатическая острая эозинофильная пневмония развивается на фоне полного здоровья и проявляется кашлем, одышкой, лихорадкой, иногда болью в грудной клетке. Содержание эозинофилов (обычно порядка 40%) повышено в крови и в жидкости, полученной при БАЛ. Заболевание имеет место быстрый ответ на кортикостероиды (в течение 48 часов).
4. Диффузное альвеолярное кровоизлияние определяется если у пациента с признаками острой респираторной недостаточности присутствует резкое снижение содержания гемоглобина в крови. При бронхоскопии, как правило, видна кровь, даже при отсутствии кровохарканья. Диагностическое значение имеет появление макрофагов, насыщенных гемосидерином, через 48 часов после начала заболевания.
5. Злокачественное новообразование (в особенности лимфогенный карциноматоз) может симулировать картину ОРДС в случае быстрого диссеминирования в тканях легких. Для дифференциации применяют бронхоскопию с БАЛ и биопсией.
Читайте также:
