Третья неделя острого панкреатита. Панкреатический абсцесс. Чрескожное дренирование.
Добавил пользователь Дмитрий К. Обновлено: 22.01.2026
Острый некротический панкреатит нередко сопровождается образованием жидкостных скоплений в сальниковой сумке, забрюшинной клетчатке и брюшной полости, в лечении которых в настоящее время используют чрескожные вмешательства под контролем УЗИ и КТ [1, 4, 7, 9]. При этом тонкоигольные пункции и дренирование производят на стадии как гнойных осложнений, так и стерильного панкреонекроза, однако общепринятый единый подход к применению этих методов при скоплениях асептической жидкости пока отсутствует. Одни авторы являются сторонниками широкого использования пункций и дренирования таких скоплений [2, 8]. Другие считают, что следует применять только пункции без дренирования [3, 5, 10]. В ряде публикаций рекомендуют строго консервативное лечение при наличии недавно образовавшихся скоплений жидкости и использование пункций только для дифференциальной диагностики стерильного и инфицированного панкреонекроза [11, 12].
В целях определения показаний к пункциям и дренированию ограниченных жидкостных скоплений при остром некротическом панкреатите нами изучено их влияние на течение заболевания и оценены эффективность и возможные осложнения пункционно-дренажного способа лечения.
Материал и методы
Проведен анализ результатов обследования и лечения 82 больных острым некротическим пакреатитом. Возраст больных от 18 до 85 лет (в среднем 45,2±1,9 года). Среди больных мужчин было 60%. Причиной заболевания большинства больных было злоупотребление алкоголем, у 29% больных имелся билиарный и у 13% - алиментарный панкреатит. Ожирение диагностировано у 35% больных. Все пациенты получали стандартную терапию, включающую применение октреотида, антисекреторных препаратов, антибиотиков и инфузионных сред.
По данным УЗИ и КТ у пациентов выявляли наличие и оценивали размеры ограниченных жидкостных скоплений в сальниковой сумке, забрюшинной клетчатке и брюшной полости. С учетом клинических и лабораторных данных оценивали наличие синдрома системной воспалительной реакции (ССВР) и тяжесть полиорганной недостаточности (ПОН) по шкале SOFA. Выполняли бактериологическое исследование полученной при пункции жидкости и определяли в ней уровень амилазы. Через 4-6 мес после выписки из стационара пациентам выполняли УЗИ брюшной полости для оценки динамики размеров жидкостных скоплений.
Ограниченные жидкостные скопления у 21% пациентов отсутствовали, у 13% они были представлены мелкими участками и полосками, у 66% выявлены скопления значимых размеров. Известно, что несостоятельность барьерной функции фасций с распространением жидкости по клетчатке соседних анатомических областей наблюдается обычно при объеме скоплений более 100 см 3 [6]. У 20 пациентов скопления имели объем до 100 см 3 , у 34 - более 100 см 3 . Пункционно-дренажный метод лечения был применен на асептической фазе заболевания у 15% больных со скоплениями объемом до 100 см 3 и у 53% пациентов с большими скоплениями. Общее количество пункций составило 66, в каждом наблюдении выполняли от 1 до 13 пункций. Процедуру осуществляли под контролем ультразвуковых аппаратов Voluson Е8, Aloca SSD 630 и Aloca 4000 иглами типа Хиба 18G длиной 20 см. Для дренирования использовали стилет-катетер Даусена-Мюллера (диаметр дренажа от 8,5 до 12 Fr). Лапароскопию с дренированием брюшной полости выполняли при наличии большого количества свободной жидкости. По поводу гнойных осложнений панкреонекроза 5 больным производили вскрытие и дренирование абсцессов, в остальных наблюдениях был эффективен пункционно-дренажный метод лечения абсцессов.
При статистической обработке данных для сравнения количественных признаков в двух группах использовали t-критерий Стьюдента, для сравнения показателей одной группы в разные моменты времени - парный критерий Стьюдента, при сравнении качественных признаков в двух группах - Z-критерий. Для выявления взаимосвязи признаков вычисляли коэффициент корреляции r по методу Пирсона.
Результаты и обсуждение

Проведенное исследование показало, что на протяжении всего периода заболевания тяжесть ПОН коррелирует только с количеством признаков ССВР (r=0,54). В свою очередь ССВР, кроме ПОН, коррелирует с количеством свободной жидкости в брюшной полости (r=0,56). Максимально выраженный ССВР наблюдался при большом количестве свободной жидкости, при этом тяжесть ПОН была выше на 2,7 балла (р <0,002), летальный исход имел место только у этих больных. Однако корреляции ССВР с наличием ограниченных скоплений асептической жидкости выявлено не было. Количество признаков ССВР было одинаковым у пациентов с ограниченными скоплениями и без таковых, а тяжесть ПОН и летальность при наличии скоплений значимых размеров были даже несколько ниже, чем при их отсутствии (см. таблицу). Образование скоплений жидкости значимых размеров происходило у больных в среднем на 5-6-е сутки заболевания, поэтому при летальном исходе в ранние сроки наличие больших скоплений не характерно.
Таким образом, наличие ограниченных скоплений асептической жидкости в отличие от ферментативного перитонита не влияет на развитие ССВР, ПОН и летальность при панкреонекрозе. Поэтому сам факт наличия ограниченных скоплений асептической жидкости не может служить показанием к пункционно-дренирующему лечению. В то же время образование ограниченных жидкостных скоплений при остром некротическом панкреатите может сопровождаться абсцедированием, сдавлением соседних органов и формированием псевдокист поджелудочной железы в отдаленном периоде. Нами исследовано влияние пункционно-дренажного лечения на развитие данных осложнений.
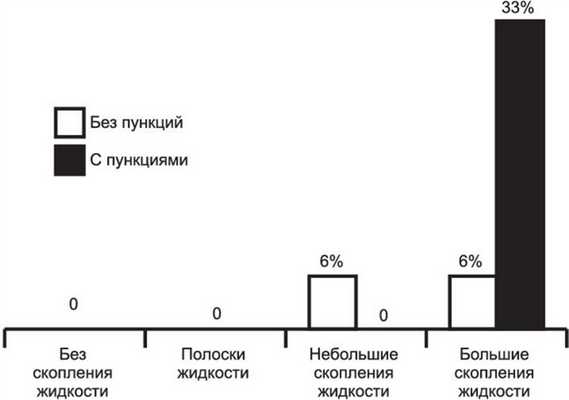
Гнойные осложнения развивались только при наличии ограниченных жидкостных скоплений значимых размеров, что приводило к достоверному (p <0,003) увеличению сроков госпитализации таких больных (см. таблицу). Анализ частоты развития гнойных осложнений у пациентов со скоплениями значимых размеров при различных подходах к лечению показал следующее. При консервативном лечении частота гнойных осложнений составила 6±4% (рис. 1), Рисунок 1. Частота развития гнойных осложнений в зависимости от размеров ограниченных жидкостных скоплений и применения пункций. при использовании пункционно-дренажного метода - 29±10% (p<0,05), в случае наличия больших скоплений - 33%. Результаты существенно зависели от характера манипуляции. При пункциях частота нагноения составляла 22±10%, при дренировании скоплений - 67±33%, т.е. увеличивалась в 3 раза.
Клинические симптомы компрессии желудка с деформацией его просвета и нарушением проходимости, потребовавшие эндоскопической установки назоинтестинального зонда для питания, имели место только при скоплениях жидкости объемом более 100 см 3 (18±6% наблюдений). При объеме скоплений более 1000 см 3 сдавление желудка развивалось у каждого второго больного. Вероятность развития компрессии желудка зависела также от локализации скоплений жидкости, она составила 12% при локализации в сальниковой сумке и/или распространении в левые отделы и 30% при распространении в правые отделы брюшной полости и забрюшинной клетчатки. Расширение желчных протоков с повышением уровня прямого билирубина крови в среднем до 39,9 мкмоль/л при небилиарной этиологии панкреатита отмечено у 7 больных, при этом в большинстве наблюдений происходило купирование билиарной гипертензии в течение 2-3 сут консервативного лечения острого некротического панкреатита. Частота развития длительной билиарной гипертензии при наличии больших жидкостных скоплений составила всего 6±4%, причем у этих пациентов наблюдались и симптомы компрессии желудка.
Таким образом, признаки сдавления соседних органов имели место у 18% больных со скоплениями жидкости объемом более 100 см 3 . Чаще происходило сдавление жидкостными образованиями желудка с нарушением его функции, реже - сдавление желчных протоков с развитием билиарной гипертензии. Пункционно-дренажное лечение применялось у половины пациентов с симптомами компрессии соседних органов и во всех наблюдениях способствовало быстрому их купированию, т.е. развитие сдавления соседних органов может служить показанием к применению пункционного лечения скоплений.
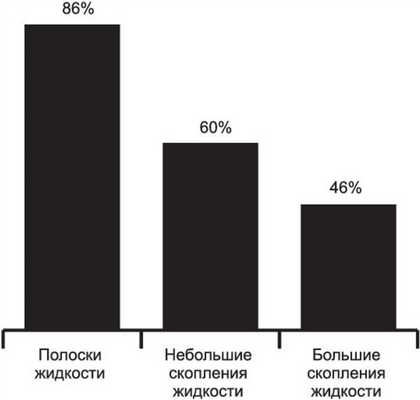
Была изучена динамика уменьшения объема ограниченных жидкостных скоплений под влиянием проводимого лечения. У 26% пациентов со скоплениями первично асептической жидкости, в лечении которых использовали только консервативные методы, за время нахождения в стационаре произошло полное рассасывание и у 34% - значительное уменьшение объема жидкостных скоплений, т.е. у 60±8% пациентов зафиксирована положительная динамика на фоне консервативного лечения. Наблюдалась прямая зависимость уменьшения объема скоплений жидкости от их размеров (рис. 2). Рисунок 2. Частота рассасывания и уменьшения размеров ограниченных скоплений асептической жидкости без применения пункций. Отдельные мелкие жидкостные участки рассасываются за время госпитализации в большинстве наблюдений.
Исследование показало, что на уменьшение размеров скоплений наиболее сильно влияют выраженность системной воспалительной реакции и их локализация. Редукция скоплений под влиянием консервативного лечения наблюдалась только в отсутствие выраженного ССВР. Ни в одном наблюдении в процессе уменьшения объема скопления у больных не было зафиксировано более 2 признаков ССВР, в среднем количество признаков составляло 0,5±0,2. В то же время прогрессирующее увеличение размеров скоплений часто происходило на фоне наличия 3-4 признаков ССВР, в среднем количество признаков составляло при этом 2±0,4 (p<0,001). При локализации скопления в сальниковой сумке и/или распространении в левые отделы брюшной полости и забрюшинной клетчатки его редукция начиналась, а часто и завершалась в течение периода госпитализации в 68±10%, при распространении в правые отделы - только в 22±14% наблюдений (p<0,05).
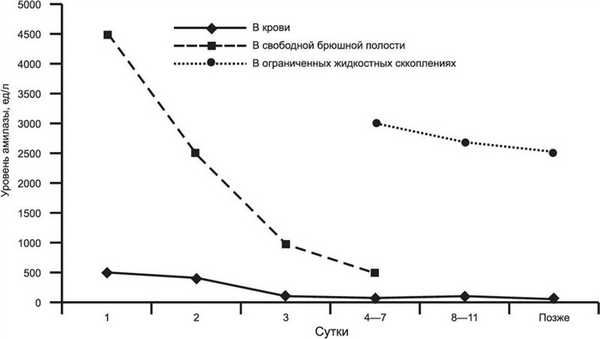
Сравнительное исследование показало, что в асептической жидкости, полученной из ограниченных скоплений, уровень амилазы был высок при полной нормализации содержания амилазы в крови, не демонстрировал тенденции к быстрому снижению во времени, его положительная линейная корреляция с уровнем амилазы крови отсутствовала вовсе. Вместе с тем высокий уровень амилазы жидкости, находящейся в свободной брюшной полости, наблюдался только в период гиперамилаземии, быстро снижаясь параллельно снижению уровня амилазы крови и коррелируя с ним (рис. 3). Рисунок 3. Изменение уровня амилазы в крови, выпоте из свободной брюшной полости и из ограниченных скоплений асептической жидкости при остром некротическом панкреатите. Отсутствие зависимости уровней амилазы в крови и выпоте из ограниченных скоплений асептической жидкости свидетельствует о наличии связи последних непосредственно с протоковой системой поджелудочной железы. Следовательно, образование ограниченных скоплений жидкости, которые в отличие от таковых при ферментативном перитоните не ассоциированы с развитием ССВР, является следствием возникновения дефекта стенки протоков поджелудочной железы с последующим локальным скоплением секрета. Это позволяет объяснить полученные результаты.
Ряд пациентов выписываются из стационара с остаточными жидкостными скоплениями различной величины, хотя при этом отмечается уменьшение размеров поджелудочной железы, отсутствуют свободная жидкость в брюшной полости, признаки ССВР и нарушения лабораторных показателей. Среди пациентов с благоприятным исходом заболевания у 87% в отдаленном периоде после выписки была зафиксирована полная редукция скоплений независимо от их локализации. У остальных больных произошло формирование капсулы, окружающей жидкостные образования. В 67% наблюдений образование псевдокист происходило в области хвоста и только в 33% - в области головки поджелудочной железы. Таким образом, у пациентов с ограниченными жидкостными скоплениями значимых размеров частота развития псевдокист поджелудочной железы в исходе острого некротического панкреатита составила 13±4%. Этот показатель практически не зависел от размеров скоплений, но сильно различался в зависимости от динамики рассасывания скоплений во время госпитализации. У пациентов с положительной динамикой на фоне лечения псевдокисты не возникали, при отсутствии такой динамики частота образования псевдокист составляла 27±8% (p<0,02).
Применение пункций скоплений не снижало частоту развития псевдокист по сравнению с консервативным лечением (21±9% при пункциях и 9±5% при консервативном лечении, разница недостоверна). При отсутствии положительной динамики рассасывания скоплений на фоне консервативного лечения частота образования псевдокист в отдаленном периоде составила 17±9%, тогда как при отсутствии положительной динамики на фоне пункционного лечения она достигла 50±18%. Отсутствие уменьшения размеров скопления после повторных эвакуаций жидкости пункционным методом указывает на сохраняющийся дефект стенки протоков поджелудочной железы, обеспечивающий повторное накопление жидкости, что и определяет высокий риск развития псевдокист в отдаленном периоде.
Показания к пункционному лечению должны ограничиваться ситуациями, при которых скопления жидкости представляют для больного большую угрозу, чем сама дренирующая манипуляция. Как показало настоящее исследование, пункционное лечение имеет преимущество перед консервативным только при наличии признаков сдавления соседних органов. Пункционное лечение эффективно устраняет данное осложнение, но при отсутствии признаков компрессии органов не показано, так как увеличивает частоту гнойных осложнений и не позволяет снизить риск развития псевдокист поджелудочной железы. Развитие компрессии соседних органов у больного с острым некротическим панкреатитом более вероятно при длительном отсутствии уменьшения размеров скоплений, что характерно для локализации скоплений объемом более 100 см 3 в правых отделах брюшной полости и забрюшинной клетчатки и сохранении 3-4 признаков синдрома системной воспалительной реакции.
Таким образом, показанием к пункциям ограниченных скопленияй асептической жидкости при остром некротическом панкреатите является только наличие признаков компрессии соседних органов. Дренирование таких скоплений не показано, так как оно сопровождается значительно более высоким риском гнойных осложнений.
Отсутствие положительной динамики после повторных эвакуаций жидкости пункционным методом указывает на высокий риск развития у больного псевдокисты поджелудочной железы.
Третья неделя острого панкреатита. Панкреатический абсцесс. Чрескожное дренирование.
Кафедра госпитальной хирургии им. В.А. Оппеля ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия
Хирургическое лечение острого панкреатита: возможности чрескожного дренирования
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2017;(8): 91‑94
Острый панкреатит среди острых хирургических заболеваний является причиной 5—10% госпитализаций в хирургические стационары. В США ежегодно госпитализируются около 300 000 пациентов с острым панкреатитом. Общая смертность от острого панкреатита в мире составляет от 5 до 10% [1]. В 40—70% случаев тяжелого панкреатита возникает инфицированный панкреонекроз. Развитие инфицированного некроза у пациентов с продолжающейся органной недостаточностью связано с крайне высокой летальностью (36—50%). На сегодняшний день так и не удалось снизить летальность от гнойно-септических осложнений, уменьшить длительность стационарного лечения, что непосредственно связано с особенностями течения заболевания. Раннее распознавание тяжелого острого панкреатита и выбор адекватного метода лечения являются основными задачами успешного лечения.
Разработка и внедрение методов миниинвазивной хирургии являются одним из перспективных направлений, дающим возможность улучшить результаты лечения больных с воспалительными заболеваниями поджелудочной железы [3]. В настоящее время широкое применение нашли чрескожные пункция и дренирование острых жидкостных образований поджелудочной железы, панкреатических абсцессов, оментобурситов, парапанкреатитов, забрюшинных флегмон, кист поджелудочной железы [5].
Цель исследования — определить целесообразность, сроки и последовательность использования чрескожного дренирования как миниинвазивного метода хирургического лечения пациентов с острым панкреатитом.
Материал и методы
Проведено изучение источников литературы за 2000—2015 гг., в которых анализируется структура летальности и осложнений, исходов в зависимости от выбора хирургического метода лечения больных острым панкреатитом.
Пациенты с тяжелым острым панкреатитом, как определено в пересмотренной классификации Атланты 2012 г. [2], должны проходить лечение в условиях реанимации. Считается, что показания к вмешательству при панкреонекрозе уже достаточно изучены и точно определены. Тем не менее на практике нередко встречаются хирургические вмешательства в раннюю фазу заболевания, когда отсутствует отграничение панкреонекроза, или применяется агрессивная тактика хирургического лечения. Результаты применения чрескожного дренирования у больных острым тяжелым панкреатитом, приводимые в отечественной и зарубежной литературе, довольно противоречивы, что связано с отсутствием объективного анализа эффективности миниинвазивных вмешательств, с объединением в одни группы пациентов с разными фазами течения панкреатита и разнородными жидкостными образованиями поджелудочной железы и парапанкреатической клетчатки. В наилучшем из имеющихся в распоряжении исследований показано, что хирургическая некрэктомия у всех пациентов с осложнениями панкреонекроза в идеале должна быть отложена до тех пор, пока скопления не станут отграниченными, обычно это 4 нед после начала панкреатита. При этом не было выявлено подгрупп, которым бы принесло пользу раннее или отложенное вмешательство [2].
В литературе активно обсуждается вопрос целесообразности применения миниинвазивных навигационных методик у больных с формированием острых жидкостных скоплений при стерильном панкреонекрозе. Стремление к уменьшению риска интраоперационного инфицирования жидкостного скопления, а также возможность абортивного течения привели к тому, что большинство исследователей не считают целесообразным выполнение чрескожных дренирующих вмешательств при объемах образований менее 50 мл [7].
Оптимальной стратегией хирургического вмешательства для пациентов с предполагаемым или подтвержденным инфицированным панкреонекрозом является первичное чрескожное дренирование под ультразвуковым контролем или эндоскопическое транслюминальное дренирование с последующей (если необходимо) эндоскопической или хирургической некрэктомией [2]. Обычная чрескожная тонкоигольная пункция парапанкреатических скоплений для диагностики инфицированного панкреонекроза малоинформативна.
В.А. Пельц и В.И. Подолужный в 2011 г. [9] привели статистически достоверные данные, свидетельствующие о преимуществах чрескожного дренирования острых жидкостных скоплений при стерильном панкреонекрозе перед пункционным методом. Так, частота инфицирования жидкостных образований при чрескожном дренировании составила 1,9%, при пункционном методе — 22,9%, различалась и летальность — 3,8 и 11,4% соответственно.
Чрескожное дренирование представляет собой эффективный метод лечения больных панкреонекрозом. В некоторых наблюдениях чрескожное дренирование может быть использовано как предварительный метод хирургического лечения перед тем или иным методом некрэктомии, например миниинвазивной забрюшинной панкреатнекрэктомией, либо применяться после некрэктомии в послеоперационном периоде для удаления остаточных скоплений жидкости.
Имеются данные из крупных центров и о более агрессивной тактике, например, о сочетании чрескожного дренирования очагов некроза множественными дренажами большого диаметра (12—30 F), агрессивной ирригации очагов (катетеры для орошения, иногда в сочетании с ловушками и корзины для дополнительной санации) и некрэктомии через просвет ретроперитонеостом. Регулярная замена дренажей необходима при многокамерных вязких некротических скоплениях. Большинство скоплений жидкости расположено в малом сальнике, переднем околопочечном и других отделах забрюшинного пространства, что позволяет через забрюшинный подход по боковому флангу выполнить чрескожное дренирование. Этот доступ сводит к минимуму риск занесения кишечного содержимого, бактериального загрязнения и кровотечения.
По мнению ряда авторов, сочетание управляемого чрескожного дренирования некротических очагов и некрэктомии через просвет ретроперитонеостом позволяет избежать открытых операций у 65—86% больных [11].
Проанализировано 11 системных исследований, в которых чрескожное дренирование использовано в качестве первоначального метода лечения панкреонекроза (данные опубликованы в период с 1998 по 2010 г.). У 271 (70,6%) из 384 пациентов был инфицированный парапанкреатический некроз (что определялось по наличию газа при компьютерной томографии или по высеванию микробной культуры после аспирации). 214 (55,7%) пациентов выжили без дополнительной хирургической некрэктомии, 133 (34,6%) пациентам требовалась дополнительная некрэктомия, остальные 37 (9,6%) больных умерли до возможного дополнительного вмешательства. Большинство описанных осложнений — свищи, наблюдавшиеся у 103 (51,5%) больных. Авторы не сообщают о численности пациентов, у которых применили другие методы хирургического лечения, за исключением чрескожного дренирования. Таким образом, остаются неопределенными критерии, по которым чрескожное дренирование было выбрано в качестве первичного метода лечения. Тем не менее эти данные показывают, что чрескожное дренирование может применяться в качестве первоначального хирургического метода лечения у некоторых пациентов.
А.А. Наумов и соавт. [13] представили собственный опыт применения пункционно-дренирующих вмешательств под ультразвуковым контролем у больных тяжелым панкреатитом, осложнившимся флегмоной забрюшинной клетчатки. У 42% больных миниинвазивные вмешательства привели к выздоровлению, в остальных наблюдениях способствовали стабилизации состояния. Д.Ю. Семенов и соавт. [15] отмечают положительные результаты дренирования под ультразвуковым контролем у 82% больных с гнойными осложнениями острого панкреатита. Одним из факторов, определяющих благоприятное течение послеоперационного периода, является минимальное разрушение анатомо-физиологических барьеров вокруг септического очага и, следовательно, меньшее усиление эндогенной интоксикации, чем при открытых операциях. В 2000 г. J. Gmeinwieser и соавт. [17] продемонстрировали возможность успешного удаления секвестров парапанкреатической клетчатки под ультразвуковым контролем с использованием корзинки Дормиа и других эндоскопических инструментов через установленные в забрюшинном пространстве дренажи большого диаметра. В другом небольшом исследовании, в котором чрескожное дренирование было первоначальным методом лечения с последующей видеоассистированной забрюшинной санацией, 40 пациентов зачислены в проспективное исследование с использованием чрескожного дренирования; дренажи менялись каждые 3—4 дня, пока не был достигнут размер катетера 20 °F. В случае уменьшения объема жидкостных скоплений по данным контрольной компьютерной томографии более чем на 75% на 10-й день от начала чрескожного дренирования было продолжено лечение дренированием (что составляет 23% группы больных, в лечении которых использовали дренирование).
M. Dua и соавт. [14] также применяли чрескожное дренирование после лапароскопической трансгастральной некрэктомии, 21 больному была выполнена лапароскопическая трансгастральная некрэктомия, в том числе у 19 была достигнута достаточная санация за одну процедуру, 2 пациентам потребовалось выполнение чрескожного дренирования. Во время наблюдения продолжительностью 11 (7—22) мес ни одному пациенту не потребовалось дополнительного оперативного вмешательства, ни у кого не развились панкреатические или кишечные свищи, а также раневые осложнения.
Существует много вариантов миниинвазивной панкреатнекрэктомии из доступа через забрюшинное пространство. В рандомизированном исследовании PANTER среди 43 пациентов 93% первоначально было выполнено чрескожное дренирование через левое забрюшинное пространство, что улучшило прогноз для миниинвазивной забрюшинной некрэктомии в последующем. Эти методы пригодны для случаев скопления частично жидких выделений в глубине левого забрюшинного пространства. Некоторые пациенты со скоплениями в правой части забрюшинного пространства могут быть оперированы методом видеоассистированной санации, хотя этот подход используется редко. При отграниченном некрозе головки поджелудочной железы или крючковидного отростка или при изолированном некрозе забрюшинной клетчатки в области латеральных каналов брюшной полости чрескожное дренирование забрюшинного пространства непригодно. Таким образом, применение миниинвазивной забрюшинной панкреатнекрэктомии ограничено в данных случаях.
Описанные исследования показывают эффективность использования методики чрескожного дренирования при лечении больных острым панкреатитом и значимость ее для исхода заболевания.
Анализ литературы показал, что традиционные открытые операции у тяжелобольных сопровождаются высоким уровнем осложнений и летальности. Именно поэтому так ценно использование миниинвазивных методик. Чрескожное дренирование при инфицированном панкреонекрозе является наиболее полезным в качестве промежуточного метода при сепсисе, а также перед открытой операцией при раннем формировании некротических скоплений. По этой причине чрескожное дренирование стало популярно как первоначальный метод перед контрольной некрэктомией по типу снизу—вверх. Тем не менее чрескожное дренирование требует частой компьютерной томографии и последующих смен дренажных трубок, а также неэффективно при многокамерных вязких некротических скоплениях. Дренажи, как правило, должны находиться в течение длительного периода, что само по себе препятствует быстрому выздоровлению.
Таким образом, использование миниинвазивных методик в лечении больных панкреонекрозом может снизить уровень летальности, связанной с инфекционными осложнениями. Для эффективного их применения важно понимание разных фаз течения острого панкреатита. Методика чрескожного дренирования является наиболее универсальной: применима и как первоначальный метод лечения, и как дополнительный, что позволяет улучшить общие результаты лечения острого тяжелого панкреатита.
Гнойный панкреатит
Гнойный панкреатит - это флегмонозное воспаление поджелудочной железы с формированием микро- или макроабсцессов в ее паренхиме. Является одной из самых тяжелых форм острого панкреатита. Наблюдаются изнуряющие опоясывающие боли в животе, тошнота, рвота, изжога, диарея, в тяжелых случаях - полиорганная недостаточность. Диагноз ставится на основании клинического осмотра, ультразвукового исследования, РХПГ и лапароскопии. Лечение осуществляется в условиях отделения реанимации, включает в себя инфузионную терапию, введение спазмолитиков и обезболивающих препаратов, ингибиторов протеаз, кардиотоников; при необходимости проводится хирургическое вмешательство.

Общие сведения
Гнойный панкреатит - грозное заболевание, развивающееся при сочетании нескольких этиологических факторов, приводящее к диффузному гнойному воспалительному процессу в ткани поджелудочной железы. Острый панкреатит - третье по частоте хирургическое заболевание, нуждающееся в неотложной оперативной помощи, после острого аппендицита и холецистита.
Среди всех вариантов острого воспаления поджелудочной железы гнойный панкреатит встречается у каждого десятого пациента. В целом патология поражает 0,02-0,08% населения мира ежегодно, подавляющее большинство пациентов - мужчины. Опасность заключается в высоком риске развития полиорганной недостаточности и последующего летального исхода при несвоевременной диагностике и начале лечения.

Причины
Для развития гнойного панкреатита недостаточно только попадания инфекции в паренхиму поджелудочной железы, а требуется сочетание нескольких этиологических факторов. К предрасполагающим факторам гастроэнтерологи и абдоминальные хирурги относят употребление большого количества алкоголя (алкогольный панкреатит), курение, погрешности в питании, злоупотребление некоторыми лекарственными препаратами.
Благоприятным фоном могут служить заболевания гепатобилиарной системы, приводящие к нарушению оттока желчи: холелитиаз, холангиты, кисты, стенозы и опухоли желчевыводящих протоков (билиарный панкреатит); травмы и кисты поджелудочной железы. На фоне воздействия перечисленных факторов происходит повышение давления в желчных путях, что способствует ретроградному забросу панкреатического сока в протоки поджелудочной железы.
Патогенез
В основе патогенеза лежат сосудистые нарушения и преждевременная активация панкреатических ферментов. Собственные ферменты расплавляют ткань поджелудочной железы, вызывая асептическое воспаление. Из-за аррозии стенки мелких сосудов органа возникают множественные кровоизлияния в паренхиму (геморрагический панкреатит). При наличии очага хронической инфекции (холецистит, холангит, аппендицит, тяжелые бактериальные или вирусные заболевания и др.) бактерии по желчным путям, с током крови либо по лимфатическим сосудам попадают в ткань железы, вызывая ее инфицирование.
Чаще всего воспалительный процесс принимает диффузный характер, на его фоне формируется множество микроабсцессов, с течением времени сливающихся в большие гнойные полости. При вскрытии абсцессов гной может попадать в брюшную полость и кровоток, приводя к распространению воспаления на другие органы и системы. Для гнойного панкреатита, в отличие от абсцесса поджелудочной железы, характерно диффузное воспаление, множество гнойных очагов.
Попадание гноя, продуктов распада и ферментов поджелудочной железы в кровоток и брюшную полость приводит к значительной интоксикации, нарушению работы жизненно важных внутренних органов и в итоге к полиорганной недостаточности. Если не распознать гнойный панкреатит до этого этапа, не начать интенсивную патогенетическую терапию, поражение внутренних органов может стать необратимым, что в результате приведет к летальному исходу.
Симптомы гнойного панкреатита
От начала заболевания до появления яркой клинической картины панкреатита может пройти как несколько дней, так и несколько недель. Обычно первым клиническим признаком является панкреатическая колика - возникновение острой опоясывающей боли в верхней половине живота. Боль иррадиирует в спину, лопатки, за грудину. Интенсивность боли может быть настолько сильной, что иногда приводит к потере сознания. Часто боль сопровождается упорной рвотой, которая не приносит облегчения пациенту, возникает даже после глотка воды.
Рвота провоцирует повышение внутрибрюшного давления, вызывая заброс панкреатических соков в поджелудочную железу, из-за чего интенсивность боли после рвоты повышается еще больше. Пациент часто занимает вынужденное положение на боку с подтянутыми к груди коленями. Из-за нарушения деятельности поджелудочной железы развиваются симптомы диспепсии: тошнота, отрыжка, повышенный метеоризм, диарея. Стул жидкий, содержит непереваренные частички пищи и жиры. Сочетание тяжелого диспепсического, болевого и интоксикационного синдромов приводит к возникновению беспокойства, плаксивости, иногда - к развитию панкреатогенного психоза.
При прогрессировании процесса возникает динамическая кишечная непроходимость, проявляющаяся значительным вздутием живота, рвотой застойным содержимым. При пальпации живота в верхней половине отмечается резкая болезненность, возможно появление симптомов раздражения брюшины. На коже передней брюшной стенки выступают цианотичные пятна, заметен отек жировой клетчатки в области поясницы. На первых этапах развития заболевания температура тела субфебрильная, но после присоединения инфекции и диффузного воспалительного процесса отмечается значительная гипертермия.
Осложнения
Токсическое воздействие панкреатических ферментов на костный мозг проявляется выраженной тромбоцитопенией, анемией. В результате гнойного расплавления тканей поджелудочной железы и окружающих органов могут формироваться свищи, ферментативный перитонит, гнойный плеврит; аррозия крупных сосудов приводит к профузным кровотечениям; в результате воспалительного процесса возникают тромбозы и тромбофлебиты вен порто-кавальной системы. Возможно формирование септического процесса, в котором гнойный панкреатит служит первичным очагом.
Выраженная интоксикация приводит к поражению сердца - отмечается постоянная тахикардия, артериальная гипотензия. Токсический миокардит вызывает развитие тяжелой недостаточности кровообращения. Поражение легких может сопровождаться респираторным дистресс-синдромом, дыхательной недостаточностью. Прогрессирующая полиорганная недостаточность в итоге может привести к летальному исходу.
Диагностика
Диагностика может быть затруднена, если пациент обращается за медицинской помощью после развития осложнений. Обследование должно производиться в условиях стационара, при гнойном панкреатите средней тяжести - в отделении гастроэнтерологии или общей хирургии, при тяжелом состоянии больного - в отделении реанимации. При наличии характерного анамнеза (прием алкоголя, погрешности в питании) производится экстренная обзорная рентгенография органов брюшной полости, ультрасонография поджелудочной железы и желчных путей, магнитно-резонансная томография поджелудочной железы.
При проведении перечисленных исследований будет обнаружено увеличение размеров органа за счет отека, формирование множества гнойных полостей, отек и воспалительная инфильтрация забрюшинной клетчатки вокруг железы. В сальниковой сумке может быть виден выпот. К назначению ретроградной холангиопанкреатографии нужно подходить очень осторожно - данная процедура может привести к развитию панкреонекроза. РХПГ выполняется только для исключения закупорки общего желчного протока конкрементами, как причины гнойного панкреатита, либо после стабилизации состояния пациента. По показаниям назначается эзофагогастродуоденоскопия, МСКТ органов брюшной полости.
Обязательно проводятся динамические исследования по определению уровня ферментов поджелудочной железы в крови и моче. При затруднениях в диагностике рекомендуется диагностическая лапароскопия. Показаниями к этой операции являются развитие панкреатита, гипертензия в желчных путях, подозрение на панкреонекроз. Дифференцировать гнойный панкреатит следует с другой острой хирургической патологией: холециститом, аппендицитом, прободной язвой желудка и ДПК, кишечной непроходимостью, тромбоэмболией мезентериальных сосудов.
Лечение гнойного панкреатита
Терапию рекомендуется проводить в условиях отделения абдоминальной хирургии или реанимации. Консервативное лечение требует соблюдения принципа «холод, голод и покой» - именно он гарантирует стихание воспалительного процесса, эффективность консервативной терапии при данном заболевании. Лечебное голодание приводит к угнетению выработки ферментов поджелудочной железы, купированию болевого синдрома. Также для снижения интенсивности боли рекомендуется прикладывание пузыря со льдом к верхней половине живота. Постельный режим обязателен, так как пациенты находятся в состоянии сильной интоксикации.
Проводится высокообъемная инфузионная терапия в сочетании с форсированным диурезом для выведения из кровотока токсинов, снижения уровня ферментов поджелудочной железы, уменьшения отека органа. В состав инфузионной терапии обязательно включаются ингибиторы протеолитических ферментов (апротинин), а при снижении уровня глюкозы на фоне деструкции ткани поджелудочной железы - концентрированные растворы сахаров. Для коррекции водно-электролитных нарушений требуется введение растворов солей, кальция, магния.
Сильные боли при гнойном панкреатите обусловлены не только ферментативным расплавлением тканей органа, но и сдавлением отечной поджелудочной железы ее плотной капсулой. С обезболивающей целью назначаются спазмолитики, наркотические анальгетики. Обязательным в лечении является использование антибиотиков. При развитии полиорганной недостаточности назначаются глюкокортикоиды, кардиотропные препараты, другие средства для коррекции жизненно важных функций организма.
Наличие диффузного воспалительного процесса в поджелудочной железе требует хирургического лечения. По показаниям проводится лапароскопическая холецистэктомия, рассечение капсулы поджелудочной железы с дренированием абсцессов. В тяжелых случаях используется развернутое оперативное вмешательство - некрэктомия поджелудочной железы, дренирование брюшной полости.
Прогноз и профилактика
Прогноз гнойного панкреатита всегда очень серьезен из-за сопутствующих ему тяжелых осложнений. Даже после выздоровления такие пациенты требуют длительного наблюдения гастроэнтеролога, серьезного восстановительного лечения. Профилактика заключается в полном отказе от алкоголя и курения, соблюдении режима питания, своевременном лечении хронических заболеваний гепатобилиарной системы (холелитиаз, холецистит и др.).
Острый панкреатит
Острый панкреатит - воспаление поджелудочной железы. Симптомы острого панкреатита: острая, нестерпимая боль в области живота. В зависимости от того, какая часть железы воспалена, локализация боли возможна в правом или в левом подреберье, в подложечной области, боль может быть опоясывающей. Хронический панкреатит сопровождается потерей аппетита, нарушением пищеварения, острыми болями (как при острой форме), возникающими после употребления жирной, острой пищи или алкоголя.
МКБ-10


Панкреатит - заболевание, характеризующееся развитием воспаления в ткани поджелудочной железы. По характеру течения панкреатит разделяют на острый и хронический. Острый панкреатит занимает третье место среди заболеваний брюшной полости острого течения, требующих лечения в хирургическом стационаре. Первое и второе место занимают острые аппендицит и холецистит.
Согласно данным мировой статистики, в год острым панкреатитом заболевает от 200 до 800 человек из миллиона. Это заболевание чаще встречается у мужчин. Возраст больных колеблется в широких пределах и зависит от причин развития панкреатита. Острый панкреатит на фоне злоупотребления алкоголем возникает в среднем в возрасте около 39 лет, а при панкреатите, ассоциированном с желчекаменной болезнью, средний возраст пациентов - 69 лет.

Факторы, способствующие возникновению острого панкреатита:
- злоупотребление алкоголем, вредные пищевые привычки (жирная, острая пища);
- желчекаменная болезнь;
- инфицирование вирусом (свинка, вирус Коксаки) или бактериальное заражение (микоплазма, кампилобактерии);
- травмы поджелудочной железы;
- хирургические вмешательства по поводу других патологий поджелудочной железы и желчевыводящих путей;
- прием эстрогенов, кортикостероидов, тиазидных диуретиков, азатиоприна, других лекарственных средств с выраженным патологическим действием на поджелудочную железу (медикаментозный панкреатит);
- врожденные аномалии развития железы, генетическая предрасположенность, муковисцидоз;
- воспалительные заболевании органов пищеварения (холецистит, гепатит, гастродуоденит).
В развитии острого воспаления поджелудочной железы согласно самой распространенной теории основным фактором выступает повреждение клеток преждевременно активированными ферментами. В нормальных условиях пищеварительные ферменты вырабатываются поджелудочной железой в неактивной форме и активизируются уже в пищеварительном тракте. Под воздействием внешних и внутренних патологических факторов механизм выработки нарушается, ферменты активизируются в поджелудочной железе и начинают переваривание ее ткани. Результатом становится воспаление, развивается отек ткани, поражаются сосуды паренхимы железы.
Патологический процесс при остром панкреатите может распространяться на близлежащие ткани: забрюшинную клетчатку, сальниковую сумку, брюшину, сальник, брыжейку кишечника и связки печении ДПК. Тяжелая форма острого панкреатита способствует резкому повышению уровня различных биологически активных веществ в крови, что ведет к выраженным общим нарушениям жизнедеятельности: вторичные воспаления и дистрофические расстройства в тканях и органах - легких, печени, почках, сердце.
Классификация
Острый панкреатит классифицируется по степени тяжести:
- легкая форма протекает с минимальным поражением органов и систем, выражается в основном интерстициальным отеком железы, легко поддается терапии и имеет благоприятный прогноз к быстрому выздоровлению;
- тяжелая форма острого панкреатита характеризуется развитием выраженных нарушений в органах и тканях, либо местными осложнениями (некроз тканей, инфицирование, кисты, абсцессы).
Тяжелая форма острого панкреатита может сопровождаться:
- острым скоплением жидкости внутри железы либо в околопанкреатическом пространстве, которые могут не иметь грануляционных или фиброзных стенок;
- панкреатическим некрозом с возможным инфицированием тканей (возникает ограниченная или разлитая зона отмирающей паренхимы и перипанкреатических тканей, при присоединении инфекции и развитием гнойного панкреатита повышается вероятность летального исхода);
- острой ложной кистой (скоплением панкреатического сока, окруженным фиброзными стенками, либо грануляциями, которое возникает после приступа острого панкреатита, формируется в течение 4 и более недель);
- панкреатическим абсцессом (скопление гноя в поджелудочной железе или близлежащих тканях).
Симптомы острого панкреатита
Характерные симптомы острого панкреатита.
- Болевой синдром. Боль может локализоваться в эпигастрии, левом подреберье, носить опоясывающий характер, иррадиировать под левую лопатку. Боль носит выраженный постоянный характер, в положении лежа на спине усиливается. Усиление боли происходит и после приема пищи, особенно - жирной, острой, жареной, алкоголя.
- Тошнота, рвота. Рвота может быть неукротимой, содержит желчь, не приносит облегчения.
- Повышение температуры тела.
- Умеренно выраженная желтушность склер. Редко - легкая желтуха кожных покровов.
Кроме того, острый панкреатит может сопровождаться диспепсическими симптомами (метеоризм, изжога), кожными проявлениями (синюшные пятна на теле, кровоизлияния в области пупка).
Опасность острого панкреатита заключается в высокой вероятности развития тяжелых осложнений. При инфицировании воспаленной ткани железы бактериями, обитающими в тонком кишечнике, возможен некроз участков железы и возникновение абсцессов. Это состояние без своевременного лечения (вплоть до хирургического вмешательства) может закончится летальным исходом.
При тяжелом течении панкреатита может развиться шоковое состояние и, как следствие, полиорганная недостаточность. После развития острого панкреатита в ткани железы могут начать формироваться псевдокисты (скопления жидкости в паренхиме), которые разрушают структуру железы и желчных протоков. При разрушении псевдокисты и истечении ее содержимого возникает асцит.
Диагностику панкреатита гастроэнтерологи осуществляют на основании жалоб, физикального осмотра, выявления характерных симптомов. При измерении артериального давления и пульса зачастую отмечают гипотонию и тахикардию. Для подтверждения диагноза служат лабораторные исследования крови и мочи, МСКТ и УЗИ органов брюшной полости, МРТ поджелудочной железы.
- Биохимия крови. При исследовании крови в общем анализе отмечаются признаки воспаления (ускорена СОЭ, повышено содержание лейкоцитов), в биохимическом анализе крови обнаруживают повышение активности панкреатических ферментов (амилаза, липаза), возможна гипергликемия и гипокальциемия. Может отмечаться билирубинемия и повышения активности печеночных ферментов.
- Биохимия мочи. Проводят определение концентрации ферментов в моче. При диагностировании острого панкреатита берут биохимический анализ мочи и определяют активность амилазы мочи.
- Инструментальные методы. Визуальное исследование поджелудочной железы и близлежащих органов (УЗИ, КТ, МРТ) позволяет выявить патологические изменения паренхимы, увеличение органа в объеме, обнаружить абсцессы, кисты, наличие камней в желчных протоках.

Дифференциальную диагностику острого панкреатита проводят с:
- острым аппендицитом и острым холециститом;
- перфорациями полых органов (прободные язвы желудка и кишечника);
- острой кишечной непроходимостью;
- острым желудочно-кишечным кровотечением (кровоточащая язва желудка и 12п. кишки, кровотечение из варикозных вен пищевода, кишечное кровотечение);
- острый ишемический абдоминальный синдром.
Лечение острого панкреатита
При остром панкреатите показана госпитализация. Всем пациентам предписан постельный режим. Основными целями терапии является снятие болевого синдрома, снижение нагрузки на поджелудочную железу, стимуляция механизмов ее самовосстановления.
Терапевтические меры:
- новокаиновая блокада и спазмолитики для снятия выраженного болевого синдрома;
- голод, лед на область проекции железы (создание локальной гипотермии для снижения ее функциональной активности), питание осуществляют парентеральное, желудочное содержимое аспирируют, назначают антациды и ингибиторы протонной помпы;
- дезактиваторы панкреатических ферментов (ингибиторы протеолиза);
- необходимая коррекция гомеостаза (водно-электролитного, кислотно-основного, белкового баланса) с помощью инфузии солевых и белковых растворов;
- дезинтоксикационная терапия;
- антибиотикотерапия (препараты широкого спектра действия в больших дозировках) в качестве профилактики инфекционных осложнений.
Хирургическое лечение
Хирургическая тактика показана в случае выявления:
- камней в желчных протоках;
- скоплений жидкости в железе или вокруг нее;
- участков панкреатического некроза, кист, абсцессов.
К операциям, проводимым при остром панкреатите с образованием кист или абсцессов, относятся: эндоскопическое дренирование, марсупиализация кисты, цистогастростомия и др. При образовании участков некроза, в зависимости от их размера, проводят некрэктомию или резекцию поджелудочной железы. Наличие камней является показанием к операциям на протоке поджелудочной железы.
К хирургическому вмешательству могут прибегать и в случае сомнений в диагностики и вероятности пропустить другое хирургическое заболевание, требующее хирургического лечения. Послеоперационный период подразумевает интенсивные меры профилактики гнойно-септических осложнений и восстановительную терапию.
Лечение легкой формы панкреатита, как правило, не представляет трудностей, и положительная динамика отмечается уже в течение недели. Для излечения от тяжелой формы панкреатита требуется заметно больше времени.
Прогноз при остром панкреатите зависит от его формы, адекватности терапии и наличия осложнений. Легкая форма панкреатита обычно дает благоприятный прогноз, а при некротических и геморрагических панкреатитах высока вероятность летального исхода. Недостаточное лечение и несоблюдение врачебных рекомендаций по диете и режиму могут привести к рецидивам заболевания и развитию хронического панкреатита.
Первичной профилактикой является рациональное здоровое питание, исключение алкоголя, острой, жирной обильной пищи, отказ от курения. Острый панкреатит может развиться не только у лиц, регулярно злоупотребляющих алкоголем, но и как следствие однократного приема спиртосодержащих напитков под жирную, жареную и острую закуску в больших количествах.
Абсцесс поджелудочной железы
Абсцесс поджелудочной железы - это полость, заполненная гноем и некротическими массами в ткани железы. В подавляющем большинстве случаев развивается после острого алкогольного панкреатита. Характеризуется появлением лихорадки, опоясывающих болей, лейкоцитоза, опухолевидного образования в брюшной полости примерно через две недели после приступа панкреатита. Диагноз устанавливается после проведения УЗИ, МРТ или КТ брюшной полости, анализа биохимических и общеклинических параметров крови. Единственный эффективный метод лечения - хирургическая санация абсцесса с последующей антибактериальной терапией.




Абсцесс поджелудочной железы - тяжелейшее заболевание, которое развивается у пациентов, перенесших панкреатит (остро или повторное обострение) или панкреонекроз с формированием в железе отграниченной гнойной полости. Заболевание опасно для жизни пациента, а коварство его кроется в стёртости клиники на фоне антибиотикотерапии. Именно поэтому в современной гастроэнтерологии принято назначать антибиотики при панкреатите только при сопутствующем поражении желчных путей или доказанных бактериальных осложнениях. Все случаи повышения температуры и появления болей в животе в течение двух недель после панкреатита должны рассматриваться как вероятный панкреатический абсцесс. Единственный метод лечения, приводящий к выздоровлению - хирургическая операция по дренированию гнойника. Без операции летальность при данной патологии достигает 100%.

Абсцесс поджелудочной железы развивается на фоне острого панкреатита, может образовываться при любой форме патологии, кроме отёчной; 3-4% случаев этого заболевания заканчиваются образованием абсцесса. Наиболее часто выявляется на фоне алкогольного панкреатита. Причины формирования гнойной полости в поджелудочной железе до конца не ясны. Предполагается, что инфекция может быть занесена током крови, при проколе псевдокист (если не соблюдается асептика), при формировании свища кисты с кишечником. Развитию абсцесса способствуют:
- тяжёлый панкреатит с более чем тремя факторами риска;
- послеоперационный панкреатит;
- ранняя лапаротомия;
- раннее начало энтерального питания;
- нерациональная антибиотикотерапия.
В подавляющем большинстве случаев при аспирации и посеве содержимого гнойника выделяется кишечная палочка либо энтеробактерии. Согласно исследованиям в области гастроэнтерологии, присоединение вторичной инфекции наблюдается практически в 60% случаев панкреонекроза, поэтому при лечении этого заболевания следует учитывать вероятность образования полости с гнойным содержимым.
При возникновении острого панкреатита ткань железы повреждается, из-за чего ферменты попадают и на саму железу, и на окружающие ткани, разрушая их. Из-за этого может начаться панкреонекроз, образуются псевдокисты - полости, заполненные жидким содержимым и некротизированными тканями. При попадании в область патологического процесса инфекции развивается либо флегмона поджелудочной железы - тотальное гнойное расплавление, либо формируется абсцесс. Следует отметить, что флегмона является более тяжёлым и прогностически неблагоприятным состоянием, по клинике практически не отличающимся от единичного абсцесса. Кроме того, при флегмоне в тканях могут формироваться множественные абсцессы.
Симптомы абсцесса
Абсцесс поджелудочной железы формируется длительно - обычно не менее 10-15 дней. Таким образом, в течение двух-четырёх недель от начала панкреатита повышается температура до фебрильных цифр, появляются озноб, тахикардия, усиливаются боли в верхней половине живота. Боли носят опоясывающий характер, достаточно сильные. Больной обращает внимание на слабость, утомляемость, отсутствие аппетита, повышенное потоотделение. Беспокоит тошнота, рвота, после которой во рту долго ощущается горечь. Налицо все признаки интоксикации. При пальпации живота обращает на себя внимание наличие опухолевидного образования, напряжение мышц передней брюшной стенки.
Абсцесс поджелудочной железы часто осложняется дальнейшим распространением инфекции, образованием множественных гнойников в самой железе и окружающих органах. Гной может затекать забрюшинно, прорываться в полые органы (кишечник, желудок), поддиафрагмально и в околокишечную клетчатку, плевральную и перикардиальную полости, в связи с чем могут сформироваться абсцесс кишечника, поддиафрагмальный абсцесс, гнойный плеврит и перикардит. Также гнойник изредка может прорываться наружу через кожу с образованием свища. При разрушении ферментами стенки сосуда может возникнуть сильное кровотечение, иногда с летальным исходом.
Диагноз абсцесс поджелудочной железы устанавливается специалистом в сфере общей хирургии после тщательного обследования больного. Дифференциальный диагноз проводится с псевдокистой поджелудочной железы, панкреонекрозом. Применяются следующие методы:
- Лабораторные исследования. В общем анализе крови отмечается высокий лейкоцитоз, сдвиг формулы лейкоцитов влево, повышение СОЭ, анемия. В биохимическом анализе крови обращает на себя внимание повышение уровня панкреатических ферментов, гипергликемия. Повышен уровень амилазы мочи, хотя при формировании абсцесса её количество может постепенно снижаться.
- Визуализирующие методики. УЗИ поджелудочной железы, КТ органов брюшной полости позволит определиться с локализацией и размерами очага, количеством абсцессов. При необходимости возможно одновременное проведение чрескожной пункции с аспирацией, исследованием и посевом содержимого.

УЗИ поджелудочной железы. На фоне резкого увеличения размеров железы (обведена пунктиром) в ее головке определяется крупный (до 3 см в диаметре) абсцесс (показан стрелками).
Рентгенологическое исследование панкреатического абсцесса имеет некоторые особенности. Так как железа расположена за желудком, то тень полости гнойника может накладываться на газовый пузырь желудка. Поэтому экспозиция должна быть дольше, а при подозрении на абсцесс в полость желудка вводят контрастное вещество и делают вертикальный снимок в боковой проекции - при этом округлая тень с границей жидкости (абсцесс) будет находиться за желудком. При попадании контраста в полость абсцесса можно говорить о наличии свища. Также на снимках можно увидеть признаки сдавления кишечника, смещения органов. Левый диафрагмальный купол высокий, подвижность его ограничена, может быть выпот в плевральную полость.

КТ органов брюшной полости. Диффузно увеличенная поджелудочная железа. Большая стрелка указывает на тело поджелудочной железы, маленькие стрелки - на абсцесс, расположенный в хвосте поджелудочной железы.
Лечение абсцесса поджелудочной железы
Лечение осуществляет абдоминальный хирург. Абсцесс является абсолютным показанием к санации и дренированию. Практика показывает, что чрескожное дренирование гнойников приводит к излечению только в 40% случаев, к тому же при такой тактике можно пропустить флегмону, множественные абсцессы, распространение инфекции на окружающие панкреас ткани. Именно поэтому эндоскопическое или классическое лапаротомное иссечение и дренирование абсцесса будет наилучшим выходом.
Во время операции производится внимательный осмотр окружающих органов, забрюшинной клетчатки на предмет вторичных абсцессов. Параллельно пациенту назначается антибиотикотерапия согласно полученным посевам, обезболивающие препараты, спазмолитики, ингибиторы ферментов. Проводится инфузионная терапия с целью дезинтоксикации.

Поскольку причины образования абсцессов поджелудочной железы до конца не выяснены, на сегодняшний день не существует и мер профилактики развития этой патологии после панкреатита и панкреонекроза. Таким образом, профилактикой абсцедирования является предупреждение панкреатита - ведь абсцесс может сформироваться только на его фоне.
Прогноз при формировании абсцессов серьёзный: без хирургического лечения смертность составляет 100%, после проведения операции выживаемость достигает 40-60%. Исход заболевания зависит от своевременности обращения, быстрой диагностики и оперативного лечения. Чем раньше поставлен диагноз и проведена операция, тем лучше отдалённые результаты.
Читайте также:
- Гуморальные ( гормональные ) влияния на сердце. Гормональная функция сердца.
- Причины опухолевидных образований и обследование при них
- Сердечный цикл при легочной гипертензии. Методика исследования сердечного цикла
- Анатомия: Правый лимфатический проток, ductus lymphaticus dexter. Топография, строение правого лимфатического протока
- Идиотия
