УЗИ при отторжении трансплантата почки
Добавил пользователь Владимир З. Обновлено: 22.01.2026
М.Г. ТУХБАТУЛЛИН 1,2 , Р.Х. ГАЛЕЕВ 2 , Л.И. ГАРИФУЛЛИНА 1 , Ш.Р. ГАЛЕЕВ 1
1 Казанская государственная медицинская академия , 420012, г. Казань, ул. Бутлерова, д. 36
2 Республиканская клиническая больница МЗ РТ, 420064, г. Казань, Оренбургский тракт, д. 138
В статье представлены результаты 205 ультразвуковых исследований почечных трансплантатов у 85 больных за период с 02.11.2015 г. по 25.04.2016 г. Установлена диагностическая значимость ультразвуковой эластографии сдвиговой волны в оценке состояния трансплантированной почки в ранние и отдаленные сроки наблюдения.
Ключевые слова: ультразвуковое исследование, компресссионная эластография, эластография сдвиговой волны, допплерографическое исследование.
M.G. TUKHBATULLIN 1,2 , R.Kh. GALEEV 2 , L.I. GARIFULLINA 1 , Sh.R. GALEEV 1
1 Kazan State Medical Academy, 36 Butlerov Str., Kazan, Russian Federation, 420012
2 Republican Clinical Hospital of the MH of RT, 138 Orenburgskiy Trakt, Kazan, Russian Federation, 420064
Modern ultrasound diagnostics in the assessment of renal transplant
The article presents the results of 205 ultrasound examinations of kidney transplants in 85 patients from 02.11.2015 till 25.04.2016. The diagnostic value of the shear wave ultrasound elastography is discussed for the evaluation of the transplanted kidney at various stages after transplantation.
Key words: ultrasound examination, compression elastography, shear wave elastography, Doppler examination.
В настоящее время ультразвуковая эластография ― метод качественного и количественного анализа упругих свойств тканей, приобретает все большее клиническое значение. Термин «эластография» (от лат. еlasticus ― «упругий») впервые предложили в 1991 г. врачи-исследователи из Хьюстона (США). Физической составляющей эластографии является модуль упругости Юнга, который характеризует свойства мягких тканей сопротивляться растяжению/сжатию при упругой деформации. В зависимости от способа расчета модуля упругости Юнга эластографию подразделяют на компрессионную и эластографию сдвиговой волны [1, 2].
Компрессионная эластография (real time elastography-RTE) ― метод качественной оценки упругих свойств тканей, основанный на уравнении Е=σ/ɛ, где Е ― модуль упругости Юнга, σ ― величина компрессии, ɛ ― относительная деформация столбика ткани (стрейн-напряжение). Данный метод используется для исследования поверхностно и глубоко расположенных органов, таких как молочные железы, щитовидная железа, предстательная железа, матка, мочевой пузырь и т.д. [1]. Более упругий, твердый объект (например, опухоль) уменьшается в объеме меньше, чем здоровая ткань. Компрессионная эластография дает возможность сравнить упругости различных участков ткани. Отношение показателей упругости называется относительным показателем или коэффициентым деформации SR (strain ratio). Относительно новым является применение компрессионной эластографии в определении эластических свойств глубоко расположенных органов ― печени, почек, поджелудочной железы [3].
Ультразвуковая эластография сдвиговой волны (УЭСВ). С точки зрения физики, сдвиговая волна ― упругая поперечная волна (в отличие от продольной ультразвуковой), которая вызывает смещение частиц среды перепендикулярно направлению распространения волны. Методика базируется на уравнении Е=3*р*С 2 , где Е ― модуль упругости Юнга (Ра), С ― скорость сдвиговой волны (м/сек.), р ― плотность вещества (кг/м 3 ). Скоростные показатели прямо пропорциональны показателям упругости (жесткости) ткани. Следовательно, чем выше жесткость, тем выше скорость [4]. Жесткость тканей определяется в килопаскалях (кПА).
Электронный способ генерации волн используется в ультразвуковых сканерах производителей Aixplorer (SuperSonic Imaging S.A., Aixen-Provens, Франция), Ultima PA Expert (Радмир, Украина) и Acuson S3000 (Siemens, Германия). Причем генерация волн электронным способом также различна. В ультразвуковых сканерах Acuson S3000 (Siemens, Германия) для создания сдвиговой волны используется мощный ульразвуковой импульс, который приобретает максимальную величину в определенной точке-источнике сдвиговых волн, распространяющихся в перпендикулярном направлении. В ультразвуковых системах Aixplorer (SuperSonic Imagine, Франция) и Ultima (Радмир, Украина) с определенной временной задержкой создается не одна, а несколько точек давления по глубине с последующим формированием фронта сдвиговых волн [1, 4].
В таблице приведены экспериментально полученные количественные данные оценки модуля Юнга и, следовательно, жесткости различных тканей [Sarvazyan A.P., 2001] 5. Полученные результаты выражаются в килопаскалях (kPa).
Таблица.
Данные оценки модуля Юнга (экспериментальные данные)
Нормальная гранулированная (normal grandular)
Фиброзная ткань (fibroustissue)
Нормальная ткань задней поверхности (normal posterior)
Доброкачественная гиперплазия предстательной железы (BPH)
Клиническое применение ультразвуковой эластографии:
― диагностика и классификация злокачественных образований молочной железы, печени, простаты, щитовидной железы и др.;
― интервенционный ультразвук: контроль за правильностью наведения биопсийной иглы; терапевтических процедур типа радиочастотной абляции и высокоинтенсивного сфокусированного ультразвука (high intensity focusing ultrasound ― HIFU);
― мониторинг изменений при лечении злокачественных образований;
― трансплантология (мониторинг возможного отторжения трансплантированной почки);
― кардиология (Myocardial Elastography ― ME);
― ангиология ― в частности, исследование характера и жесткости бляшек (Endovascular elastography ― EVE) 8.
Роль трансплантации почки (ТП) на сегодняшний день трудно переоценить. Данный метод относится к наиболее радикальным способам лечения терминальных заболеваний почек. Являясь одним из видов заместительной почечной терапии, трансплантация позволяет не только обеспечить высокий уровень качества жизни, снизить стоимость лечения, уменьшить риски кардиоваскулярной летальности, но и достоверно увеличить продолжительность жизни данной категории пациентов. Допплерографическое исследование и ультразвуковая эластография сдвиговой волны в комплексе, оказались весьма перспективными методами для исследования почечного трансплантата, определения осложнений и морфологических изменений.
Цель исследования ― изучить диагностическую значимость ультразвуковой эластографии сдвиговой волны (УЭСВ) в оценке состоянии почечного трансплантата на разных сроках.
Материал и методы
За период с 02.11.2015 г. по 25.04.2016 г. было выполнено 205 УЗИ почечных трансплантатов у 85 пациентов, средний возраст которых составил 38,2±2,1 года. Сроки проведения УЗИ от 0 суток до 10 лет после трансплантации почки. УЗИ проводилось на аппарате Aixplorer (SuperSonic Imagine S.A., Aixen-Provence, Франция), с применением конвексного датчика 1-6 МГц. Исследование проводилось в РКБ МЗ РТ. При оценке состояния трансплантата нами определялись контуры почки, однородность и эхогенность паренхимы, состояние почечного синуса, чашечно-лоханочной системы и мочеточника. При топометрии устанавливались размеры (длина, ширина и толщина) почечного трансплантата. Оценка состояния околопочечного пространства сводилась к поиску свободной жидкости вокруг трансплантата, которая может наблюдаться при образовании гематом, урином и лимфоцеле. В режимах цветовой и спектральной допплерографии был оценен кровоток в сосудах почечного трансплантата, включая сосудистый анастомоз. Определялись систолическая, диастолическая скорости кровотока и индексы резистентности в сегментарных, дуговых и междольковых артериях. При режиме УЭСВ оценивалась жесткость паренхимы на верхнем, нижнем полюсе, латеральном и медиальном крае почечного трансплантата. Для сравнительного анализа, все результаты исследования были разделены на две группы: первая группа ― пациенты на сроках от 0-30 суток после пересадки почки, вторая ― пациенты на сроках более 30 суток после операции. Основной причиной, приведшей к хронической почечной недостаточности (ХПН), у пациентов, перенесших трансплантацию почки, являлся хронический гломерулонефрит.
Результаты и обсуждение
Клинический пример из первой группы. Пациент М., с хронической почечной недостаточностью. Трансплантация почки произведена от живого родственного донора. Трансплантат находится в правой подвздошной области. При нормальном функциональном состоянии трансплантата, показатели цветовой и спектральной допплерографии оценивались как удовлетворительные, с индексом резистентности не более 0,60 (рис. 1); показатели жесткости паренхимы почечного трансплантата при УЭСВ на различных участках составили от 20,05 до 29,18 кПа (рис. 2-4).
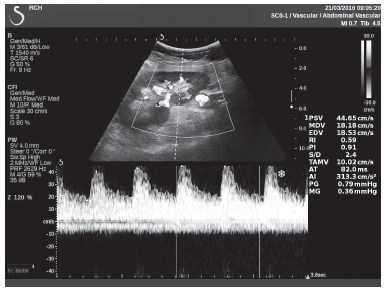
Рисунок 1. Ультразвуковое исследование в режиме цветовой и спектральной допплерографии в междольковых и сегментарных артериях у пациента М. Показатели кровотока в данном случае не изменены
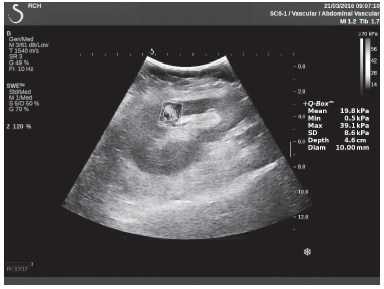
Рисунок 2. Исследование в режиме ультразвуковой эластографии сдвиговой волны у пациента М.: жесткость паренхимы в зоне медиального края трансплантата 19,8 кПа
Рисунок 3. Исследование в режиме ультразвуковой эластографии сдвиговой волны у пациента М.: жесткость паренхимы в зоне верхнего полюса почечного трансплантата 21,4 кПа
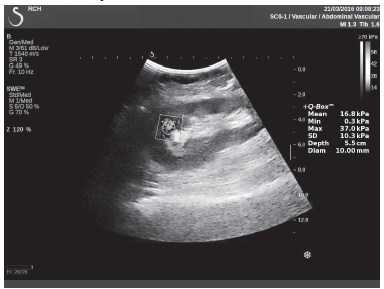
Рисунок 4. Исследование в режиме ультразвуковой эластографии сдвиговой волны у пациента М.: жесткость паренхимы в зоне нижнего полюса почечного трансплантата 16,8 кПа
У пациентов второй группы, при нормальных показателях клинико-лабораторных и допплерографических исследований, показатели жесткости почечного трансплантата составили 17,00-26,06 кПа.
Клинический пример из второй группы. Пациент К. перенес операцию пересадки почки от живого родственного донора. Трансплантат в левой подвздошной области. Индекс резистентности в междольковых артериях составил 0,70 (рис. 5). В сегментарных артериях индекс резистентности составил 0,66 (рис. 6). Показатели жесткости паренхимы почечного трансплантата при режиме УЭСВ составили от 31,6 до 36,9 кПа (рис. 7-9).
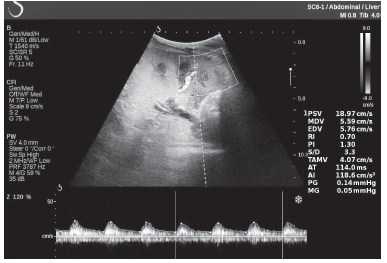
Рисунок 5. Исследование у пациента К. в режиме цветовой и спектральной допплерографии. Индекс резистентности в междольковых артериях почечного трансплантата составил 0,70
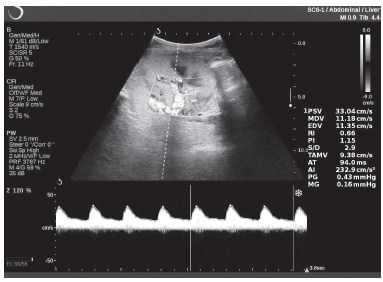
Рисунок 6. Эхограмма пациента К. Кровоток в сегментарных артериях неизменен
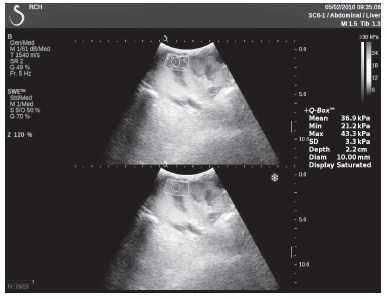
Рисунок 7. Исследование в режиме ультразвуковой эластографии сдвиговой волны у пациента К.: жесткость паренхимы в зоне медиального края почечного трансплантата 36,9 кПа
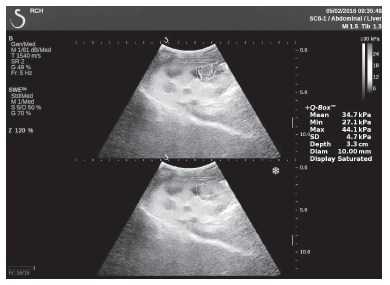
Рисунок 8. Исследование в режиме ультразвуковой эластографии сдвиговой волны у пациента К.: жесткость паренхимы в зоне нижнего полюса почечного трансплантата 34,7 кПа
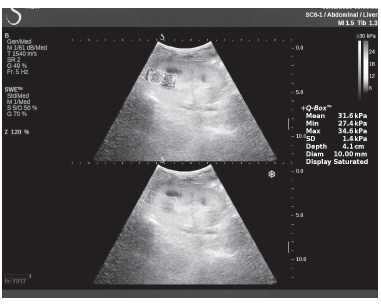
Рисунок 9. Исследование в режиме ультразвуковой эластографии сдвиговой волны у пациента К.: жесткость паренхимы у верхнего полюса почечного трансплантата 31,6 кПа
Заключение
При снижении скорости кровотока и повышении индекса резистентности до 0,70 и более, как в первой, так и во второй группах, показатели УЭСВ составили от 28,00 до 39,45 кПа. Повышение жесткости паренхимы почечного трансплантата, на наш взгляд, связано с начавшимися изменениями (фиброза) в паренхиме почки. При повышении индекса резистентности более 0,70 показатели жесткости паренхимы при УЭСВ является дополнительным критерием, позволяющим оценить функциональное состояние почечного трансплантата. Ультразвуковая эластография ― новая развивающаяся методика, чувствительность, специфичность и точность которой увеличиваются при комплексном использовании с другими методами исследования. Анализ результатов проведенных исследований выявил значительные клинические возможности и перспективы применения метода ультразвуковой эластографии сдвиговой волны в оценке состояния почечного трансплантата. Полученные данные о диагностической точности метода позволяют использовать результаты в целях принятия решения о дальнейшем ведении пациента и тактике лечения [4].
1. Зыкин Б.И., Постнова Н.А., Медведев М.Е. Эластография: анатомия метода // Променева диагностика, променева терапия. ― 2012. ― 2-3.
2. Зубарев А.Р., Федорова В.Н., Демидова А.К. и соавт. Ультразвуковая эластография как новая ступень в дифференциальной диагностике узловых образований щитовидной железы: обзор литературы и предварительные клинические данные // Медицинская визуализация. ― 2010. ― №1. ― С. 11-16.
3. Тухбатуллин М.Г., Алиева И.М. Современные ультразвуковые технологии в клинической практике // Практическая медицина. ― 2012. ― №5.
4. Тухбатуллин М.Г., Галеева З.М., Бастракова А.Е. Ультразвуковая эластография // Эхография в диагностике заболеваний внутренних и поверхностно расположенных органов. ― Казань: Медицинская книга, 2016. ― С. 119-130.
5. Bamber J. et al. EFSUMB* Guidiness and recommendations on the clinical use of ultrasoundelastography. Part 1: Basic principles and technology // Ultrashall in Med. ― 2013. ― 34. ― P. 164-168.
6. Bamber J. et al. EFSUMB* Guidelines and Recommendations on the Clinical Use of Ultrasound Elastography. Part 2: Basic Principles and Technology // Ultrashall in Med. ― 2013. ― 34. ― P. 169-184.
7. Осипов Л.В. Ультразвуковые диагностические приборы: Режимы, методы и технологии —М.: Изомед, 2011. ― 312 с.
8. Ophir J. et al. Elastography: Imaging the Elastic Properties of Soft Tissues with Ultrasound // J. Med. Ultrasonics. ― 2002. ― P. 155-171.
9. Ophir J., Cespedes I., Ponnekanti H., Yazdi Y., Li X. Elastography: a quantita-tive method for imaging the elasticity of biological tissues // Ultrason Imaging. ― 1991. ― Vol. 13. ― P. 111-134.
1. Zykin B.I., Postnova N.A., Medvedev M.E. Elastografiya: anatomiya metoda [Elastography: anatomy method]. Promeneva diagnostika, promeneva terapiya, 2012, 2-3.
2. Zubarev A.R., Fedorova V.N., Demidova A.K. et al. Ultrasound elastography as a new stage in the differential diagnosis of thyroid nodules: a literature review and preliminary clinical data. Meditsinskaya vizualizatsiya, 2010, no. 1, pp. 11-16 (in Russ.).
3. Tukhbatullin M.G., Alieva I.M. Modern ultrasound technology in clinical practice. Prakticheskaya meditsina, 2012, no. 5 (in Russ.).
4. Tukhbatullin M.G., Galeeva Z.M., Bastrakova A.E. Ul’trazvukovaya elastografiya [Ultrasound elastography]. Ekhografiya v diagnostike zabolevaniy vnutrennikh i poverkhnostno raspolozhennykh organov. Kazan: Meditsinskaya kniga, 2016. Pp. 119-130.
5. Bamber J. et al. EFSUMB* Guidiness and recommendations on the clinical use of ultrasoundelastography. Part 1: Basic principles and technology. Ultrashall in Med, 2013, 34, pp. 164-168.
6. Bamber J. et al. EFSUMB* Guidelines and Recommendations on the Clinical Use of Ultrasound Elastography. Part 2: Basic Principles and Technology. Ultrashall in Med, 2013, 34, pp. 169-184.
7. Osipov L.V. Ul’trazvukovye diagnosticheskie pribory: Rezhimy, metody i tekhnologii [Ultrasonic diagnostic equipment: Modes, methods and technologies]. Moscow: Izomed, 2011. 312 p.
8. Ophir J. et al. Elastography: Imaging the Elastic Properties of Soft Tissues with Ultrasound. J. Med. Ultrasonics, 2002, pp. 155-171.
9. Ophir J., Cespedes I., Ponnekanti H., Yazdi Y., Li X. Elastography: a quantita-tive method for imaging the elasticity of biological tissues. Ultrason Imaging, 1991, vol. 13, pp. 111-134.
УЗИ почки трансплантата (лекция на Диагностере)
Статья находится в разработке.
УЗИ трансплантата почки проводили методом УЭСВ, а также использовали стандартные режимы сканирования:
1) серошкальное сканирование: оценка состояния и топометрия трансплантата (размеры трансплантата, толщина коркового слоя, величина чашечно-лоханочной системы и т.д.), оценка состояния околопочечного пространства;
2) цветовое доплеровское картирование скорости и энергии кровотока;
3) спектральное доплеровское исследование.
При пересадке почки методом УЗИ оценивают возможные осложнения в пересаженной почке.
Обычно первое УЗИ проводят через 24-48 часов после трансплантации.
Часто выполняемый с помощью радионуклидной визуализации (йод-131 ортойодогиппурат, Tc-99m MAG3).
Важно знание хирургической техники, отчета об операции часто улучшает интерпретацию исследования.
Трансплантированная почка обычно располагается забрюшинно в подвздошной ямке, чаще справа.
При трансплантации трупной почки основную почечную артерию забирают с прикрепленной частью донорской аорты.
Затем анастомозируется из стороны в сторону к наружной подвздошной артерии реципиента.
Трансплантация живых доноров включает прямой сквозной трансплантат почечной артерии к наружной подвздошной артерии или сквозной анастомоз с внутренней подвздошной артерией.
Основная почечная вена почти всегда пересаживается реципиентной наружной подвздошной вене сквозным образом.
Мочевой дренаж обычно восстанавливается путем имплантации донорского мочеточника в купол мочевого пузыря (уретеронеоцистостомия).
Хотя он также может быть имплантирован в нативный мочеточник или почечную лоханку.
Структурная оценка
Общая структурная оценка включает: эхогенность, кортикомедуллярная дифференциация должна быть сохранена, размер почек.
Увеличение может указывать на отек, который неспецифичен, но изменение размера между исследованиями является признаком основного заболевания.
Хирургические осложнения: Обструктивная уропатия, гидронефроз,проксимальный гидроуретер
Коллекции жидкостей
Характер сбора жидкости после трансплантации не может быть надежно определен только по внешнему виду ультразвука, так как большинство из них безэховые с различными внутренними акустическими характеристиками.
Лучше всего это делать на основе шкалы времени, поскольку разные сборы жидкости имеют тенденцию представлять в разное время в послеоперационном периоде:
сразу после операции: гематома
1-2 недели после операции: уринома
3-4 недели после операции: перинефритический абсцесс
2-й месяц и далее: лимфоцеле
Оценка сосудов
тромбоз почечной вены или стеноз
изменение диастолического кровотока в почечной артерии
тромбоз почечной артерии или стеноз
высокие скорости потока в месте стеноза
пиковая систолическая скорость ≥2 м / с
разница скоростей между пре- и постстенотическими сегментами 2:1
постстенотическое расширение спектра
Форма волны Парвуса и Тардуса дистальнее стеноза
обычно развивается через месяцы или недели
псевдоаневризма: обычно после биопсии или другой почечной пункции
внутрипочечный артериовенозный свищ
Медицинские осложнения
Существует ряд медицинских причин дисфункции или отказа почечного трансплантата:
острый тубулярный некроз
отказ
сверхострый: сразу после операции
острый: 1-3 недели после пересадки
хронический:> 3 месяца после пересадки
лекарственная нефротоксичность
рецидивирующее заболевание, например рецидивирующая IgA нефропатия
пиелонефрит
встречается у 80% получателей в первый год
Ультразвуковое исследование при медицинских осложнениях трансплантата неспецифично и может включать:
повышенный резистивный индекс (RI)> 0,8
очаговый или диффузный паренхиматозный отек
В конечном счете, пациенты с подозреваемыми медицинскими причинами дисфункции трансплантата подвергаются биопсии для окончательного диагноза.
Главная » Методы диагностики заболеваний » Ультразвуковая диагностика »
Дергачев А.И., Котляров П.М., Абдоминальная эхография .Справочник, 2003
« предыдущая
к содержанию
следущая »
Трансплантация почки Ультразвуковое исследование трансплантированной почки
Трансплантированная почка обычно располагается вдоль поверхности подвздошнопоясничной мышцы, ее эхогенность совпадает с эхо- генностью обычной почки. Эхографические признаки отторжения трансплантата включают: патологическое увеличение размеров почки, гидронефроз, паранефральное скопление жидкости, гематомы, абсцессы и экстраренальные накопления мочи. При допплерографии почечного кровотока обычно определяется увеличение сосудистого сопротивления или полное прекращение кровотока в главной почечной артерии, междолевых артериях, дугообразных артериях (для исключения отторжения), почечной вене (для исключения перегиба почечной вены).
Способ диагностики острого отторжения пересаженной почки
Способ диагностики острого отторжения пересаженной почки путем определения в послеоперационном периоде индекса периферического сопротивления сосудистого русла трансплантата при допплеросонографии и, дополнительно, эхосканировании, определяют объем трансплантата, толщину его паренхимы, индекс примамид мозгового вещества,а индекс периферического сопротивления сосудистого русла пересаженной почки определяют по отношению разницы максимального пикового систолического допплеровского частотного сдвига в конце диастолы к максимальному пиковому систолическому допплеровскому частотному сдвигу и при индексе периферического сопротивления сосудистого русла пересаженной почки более 0,79, или объеме почки более 300 см3, или толщине паренхимы более 2 см и индексе пирамид мозгового вещества более 2,1, или толщине паренхимы меньше или равной 2,0 см и индексе пирамид мозгового вещества более 2,8 диагностируют острое отторжение пересаженной почки (Арутюнян С. М. и соавт., 1990).
Осложнения трансплантации почки
Осложнения трансплантации почки — это расстройства, этиологически связанные с пересадкой нефротрансплантата. В раннем периоде проявляются гипертермией, олигоанурией, артериальной гипертензией, болью в области трансплантата. Поздние осложнения длительно протекают бессимптомно, в последующем превалируют признаки почечной недостаточности и нарушений в работе других органов. Патология диагностируется с помощью исследований крови и мочи, УЗИ, УЗДГ, МРТ почек, пункционной биопсии. Для лечения применяют иммуносупрессоры, антибиотики, антиагреганты, антикоагулянты, проводят хирургическую ревизию раны, оперативные вмешательства на мочеточниках, нефротрансплантатэктомию.
МКБ-10

Общие сведения
Выживаемость пациентов, перенесших трансплантацию почки, на протяжении первого послеоперационного года достигает 94-98%, однако развитие осложнений существенно влияет на функциональность пересаженного органа и качество жизни реципиентов. В раннем и позднем посттрансплантационном периоде могут возникать как урологические заболевания, так и повреждения других органов, способные спровоцировать гибель пациента.
По результатам наблюдений, 33,2% смертей после трансплантации почек вызваны кардиальными причинами, из них 11,3% — острым инфарктом миокарда, 17,8% — инфекционными заболеваниями, 11,9% — опухолевым процессом, 6,9% — нарушением мозгового кровообращения, 30,3% — другими факторами. В течение первых 12 месяцев после вмешательства отторгается от 6 до 12% нефротрансплантатов, что требует возобновления заместительной почечной терапии и проведения повторной пересадки. До 36% реципиентов переносят инфекционные заболевания мочевыделительных органов и оппортунистические инфекции.

Причины
Несмотря на накопленный опыт и внедрение эффективных стандартов проведения операции, техническая сложность ее выполнения и использование аллотрансплантата повышают риск осложненного течения послеоперационного периода. Специалисты в сфере современной урологии, нефрологии и трансплантологии выделяют следующие группы причин, провоцирующих возникновение осложнений после нефротрансплантации:
- Возраст и состояние здоровья реципиента. Кроме абсолютных противопоказаний, при которых проведение трансплантации в большинстве случаев завершается неблагоприятным исходом, существуют относительные, существенно повышающие вероятность осложнений. В группу риска входят пациенты старше 65-70 лет, а также страдающие рядом сопутствующих заболеваний — активным гепатитом, циррозом печени, СКВ, васкулитом, гемолитико-уремическим синдромом, системными заболеваниями в активной фазе, сахарным диабетом, острыми инфекционными процессами, ХСН IIБ ст.
- Особенности трансплантируемой почки. Осложнения чаще возникают при AB0 и HLA-несовместимости тканей, пресенсибилизации реципиента. Приживление органа ухудшается при длительной (более 24 ч) холодовой ишемии почки, по результатам некоторых наблюдений этот фактор оказывается более значимым, чем гистосовместимость. Функциональность трупной почки зависит от причин смерти донора, электролитных нарушений, степени и длительности гипотонии, других особенностей агонального периода. На течение посттрансплантационного периода также влияет техника забора органа.
- Медицинские факторы. Исход трансплантации зависит от полноты предоперационного обследования реципиента и прижизненного донора, правильности оценки выявленных противопоказаний, проведения предтрансплантационной подготовки при обнаружении гистологической несовместимости тканей. На качество приживления почки оказывают влияние техническая точность пересадки, соблюдение требований асептики и антисептики, профилактика ишемического повреждения органа, качество наблюдения за пациентом, выбор оптимального режима иммуносупрессии (ИСТ).
- Иммунодефицит. Ряд постнефротрансплантационных осложнений связан с медикаментозным угнетением иммунитета реципиента. Назначение иммуносупрессивных препаратов — важное условие профилактики отторжения трансплантата. Однако на фоне иммунодефицита повышается вероятность возникновения ранних и отдаленных инфекционных заболеваний. Кроме того, иммуносупрессия является фактором риска онкогенеза. У части пациентов нарушения гуморального и клеточного иммунитета стимулируют возникновение аллергических и аутоиммунных реакций.
Патогенез
Механизм развития осложнений трансплантации почек зависит от этиологических факторов, спровоцировавших патологическое состояние. Зачастую в основе расстройства лежит иммунное или инфекционное воспаление. В первом случае наблюдается отторжение нефротрансплантата вследствие Т-клеточного ответа или гуморальной реакции типа антиген-антитело. При попадании в рану инфекционных агентов воспалительная деструкция тканей происходит под действием бактериальных эндо- и экзотоксинов.
Ситуация часто усугубляется ишемическими нарушениями, возникшими на фоне расстройств микроциркуляции, артериальной окклюзии, венозного тромбоза. Отдельную роль в патогенезе постнефротрансплантационных осложнений играет иммуносупрессия, снижающая или извращающая нормальную защитную реакцию организма на действие повреждающих факторов. В отдаленные сроки преобладают процессы склерозирования почечной паренхимы.
Классификация
Систематизация вариантов осложнений после трансплантации почки создана с учетом времени возникновения, причин, механизма развития и клинической симптоматики расстройства. Такой подход соответствует принципам своевременной диагностики и адекватной этиопатогенетической терапии постнефротрансплантационных нарушений. Осложнения при нефротрансплантации могут быть ранними, возникшими остро в ходе операции или в первые месяцы после пересадки, и поздними, с постепенным нарастанием симптомов. Различают следующие формы патологии:
Симптомы
Ранние острые нарушения обычно отличаются бурной клинической картиной. Вскоре после трансплантации у пациента возникает ярко выраженный интоксикационный синдром с высокой температурой, ознобом, суставными и мышечными болями, тошнотой, рвотой, кожным зудом, резкой слабостью. При внутреннем кровотечении наблюдается головокружение, бледность кожных покровов, возможна потеря сознания.
У большинства реципиентов о появлении осложнений свидетельствует значительное уменьшение мочеотделения вплоть до его полного прекращения в сочетании с высоким артериальным давлением. В области трансплантированной почки может пальпироваться болезненное уплотнение. Распространенным признаком инфекционного воспаления является наличие обильного раневого отделяемого. При вовлечении в воспалительный процесс брюшины и развитии перитонита возникает резкая боль в брюшной полости, живот становится напряженным, доскообразным, отмечается учащение пульса, резкое падение АД, часто отсутствует стул.
Проявлением поздних осложнений обычно становится прогрессирующее снижение фильтрационной способности почек. Клиническая симптоматика длительное время отсутствует. В последующем пациент начинает предъявлять жалобы на быструю утомляемость, снижение работоспособности. Уменьшается суточный диурез. Утром на лице преимущественно в области век появляются отеки, которые по мере развития почечной недостаточности сохраняются в течение дня и распространяются на другие части тела. Часто повышается артериальное давление.
Возникают и нарастают симптомы уремии — заторможенность, апатичность, бледность и сероватый оттенок кожи, интенсивный кожный зуд, жажда, нарушения сна, низкая температура тела, отсутствие аппетита, тошнота, рвота, диарея. При сочетанном поражении других органов и систем отмечается соответствующая симптоматика. Из-за угнетения иммунитета реципиенты часто болеют ОРВИ, у них развиваются тяжелые длительные бронхиты, пневмонии. Возможны различные формы пиодермий.
Нарушение всасывания кальция приводит к остеопорозу, гиперплазии паращитовидных желез. Из-за недостаточного синтеза эритропоэтинов часто формируется анемия. У пациентов, длительно принимающих иммуносупрессоры, могут диагностироваться онкологические заболевания. При этом преобладают новообразования предположительно вирусного происхождения — плоскоклеточная (сквамозная) и базальноклеточная карциномы, лимфопролиферативная болезнь (преимущественно В-клеточная неходжкинская лимфома), аногенитальные неоплазии, в том числе рак шейки матки, саркома Капоши.
Диагностика
Диагностический поиск при подозрении на осложнение трансплантации почки направлен на уточнение характера расстройства, оценку жизнеспособности и функциональной состоятельности почечного трансплантата, выявление критических органных и метаболических нарушений, угрожающих жизни реципиента. Наиболее информативными методами обследования являются:
- Общий анализ крови. Вероятное развитие острых осложнений подтверждается значительным повышением уровня лейкоцитов, падением содержания тромбоцитов, ускорением СОЭ. В отдаленном периоде часто наблюдается снижение концентрации эритроцитов, гемоглобина, на фоне иммуносупрессии возможно возникновение лейкопении.
- УЗИ почечного трансплантата. Эхография почки является безопасным скрининговым методом, позволяющим выявить изменение размеров пересаженного органа, деструкцию паренхимы, наличие патологических изменений в паранефральном пространстве. Исследование дополняют УЗДГ почечных сосудов для комплексной оценки состояния кровотока.
- Биохимический анализ крови. О нарушении фильтрационной функции клубочков свидетельствует нарастание уровней креатинина, остаточного азота, мочевины, калия. Поражение гломерулярного аппарата подтверждается данными пробы Реберга, нефрологического комплекса. Характерен высокий уровень ЛДГ, С-реактивного белка.
В зависимости от типа осложнения в общем анализе мочи может обнаруживаться повышение или снижение удельной плотности, наличие эритроцитов, лейкоцитов, цилиндров, бактерий. Для исключения отторжения нефротрансплантата рекомендовано проведение расширенного комплексного иммунологического исследования, пункционной биопсии с последующим гистологическим анализом полученного материала. Исследования с введением рентгеновского контраста (экскреторная урография, КТ, МСКТ почек) производятся с осторожностью из-за возможного усугубления клинической ситуации за счет развития контраст-индуцированной нефропатии.
В качестве дополнительных методов может назначаться МРТ для выявления возможных структурных нарушений в тканях трансплантата и нефросцинтиграфия, позволяющая уточнить функциональность пересаженной почки. Для мониторинга состояния пациента в раннем посттрансплантационном периоде оценивают волемический статус (гемогидробаланс, уровень ЦВД), электролитное состояние (уровни калия, натрия, кислотно-щелочного равновесия), коагулограмму, обеспечивают контроль диуреза, суточное мониторирование АД, регулярно выполняют ЭКГ.
Дифференциальную диагностику обычно проводят между различными видами осложнений. При поздних урологических последствиях трансплантации исключают развитие возвратного гломерулонефрита, рецидивирующей волчаночной нефропатии, пиелонефрита, гидронефроза. По назначению врача-нефролога или уролога пациента консультирует трансплантолог, анестезиолог-реаниматолог, абдоминальный хирург, инфекционист, ревматолог, иммунолог, онколог.
Лечение осложнений трансплантации почки
Основными врачебными задачами являются скорейшая коррекция возникших расстройств и поддержание основных жизненных функций реципиента. При отсутствии острых хирургических осложнений лечение обычно представлено комплексной медикаментозной терапией. С учетом выявленных нарушений пациентам, перенесшим трансплантацию почки, назначаются:
- Коррекция иммуносупрессорной терапии. Применение пульс-методов, изменение дозировки ингибиторов кальциневрина, антиметаболитов, глюкокортикоидов, ингибиторов интерлейкинов, биологических антилимфоцитарных агентов, замена одних препаратов другими зачастую позволяет купировать эпизод отторжения. Коррекция назначений также может потребоваться при связи осложнений с принимаемыми иммунодепрессантами.
- Лечение ишемии пересаженной почки. При возникновении сосудистых и тромботических нарушений используются дезагреганты, антикоагулянты, антигипоксанты, цитопротекторы, синтетические простагландины. С их помощью удается эффективно улучшить почечный кровоток, микроциркуляцию, перфузию тканей. Для увеличения кислородной емкости крови может назначаться гипербарическая оксигенация.
- Антибактериальные препараты. Показанием к проведению активной антибиотикотерапии служит наличие инфекционно-воспалительных осложнений. Предпочтительны противобактериальные средства с минимальным риском нефротоксического эффекта — хинолоны, комбинации диаминопиримидинов с синтетическими сульфаниламидами. При лечении оппортунистических инфекций учитывается чувствительность микроорганизмов.
Инфузионная терапия под контролем диуреза проводится при возникновении острых, угрожающих жизни состояний, метаболических расстройств. С учетом клинической картины реципиенту почки могут вливаться коллоидные и кристаллоидные растворы, отдельные электролиты, цельная кровь и ее компоненты. При нарастании признаков почечной недостаточности возобновляется заместительная терапия (гемодиализ, перитонеальный диализ, гемофильтрация, гемодиафильтрация). Лечение заболеваний, спровоцированных трансплантацией почки, осуществляется согласно протоколам для соответствующей патологии.
Оперативные методы лечения требуются при выявлении хирургических осложнений, деструкции мочеточника или почечного трансплантата. Объем вмешательств зависит от особенностей осложнения. Может выполняться ревизия и дренирование раны, ушивание поврежденных сосудов, лапароскопическая марсупиализация лимфоцеле. При повреждении мочеточника возможно проведение эндоскопического рассечения уретероцеле, уретеропластики, уретерокутанеостомии, наложение неоуретероцистоанастомоза. Необратимая деструкция трансплантированной почки служит показанием для нефротрансплантатэктомии с последующим назначением ЗПТ и возможной повторной пересадкой органа.
Прогноз и профилактика
Возникновение осложнений ощутимо ухудшает показатели выживаемости пациентов, однако своевременное выявление и грамотная коррекция расстройств делают прогноз более благоприятным. Профилактика возможных осложнений начинается с комплексного обследования больного перед операцией для определения всех абсолютных и относительных противопоказаний, оценки гистосовместимости с донором. При предстоящей AB0-несовместимой трансплантации требуется проведение предоперационной десенсибилизации. По показаниям на предтрансплантационном этапе может назначаться превентивная антибиотикотерапия.
С учетом вероятной компрометации заживления раны на фоне иммуносупрессивной терапии важна прецизионная хирургическая техника, повышенное внимание к деталям, строгое соблюдение правил асептики, тщательный гемостаз. После трансплантации ключевую роль играет правильный выбор индукционной и поддерживающей ИСТ, послеоперационный мониторинг состояния реципиента.
2. Инфекции после трансплантации почки (Обзор литературы)/ Кабулбаев К.А.// Нефрология и диализ. - 2009 - Т.11, №4.
3. Инфекционные осложнения раннего послеоперационного периода у пациентов после трансплантации почки/ Барканова О.Н., Перлин Д.В., Шепелева Ю.Б., Реброва Е.В., Ильченко О.В. // Вестник Волгоградского государственного медицинского университета. - 2016.
4. Этиология возбудителей инфекционных осложнений после трансплантации печени и почек и их резистентность к антибиотикам/ Габриэлян Н.И.// Российский медицинский журнал. - 2016.
Реакция отторжения трансплантата
Реакция отторжения трансплантата (РОТ) - иммунологический процесс, направленный против чужеродных для организма тканей, пересаженных в ходе операции трансплантации. Сопровождается комплексом местных (отек, воспаление) и общих (явления интоксикации, повышение температуры, слабость) проявлений, выраженность и скорость развития которых зависят от варианта реакции. Диагностика производится посредством изучения клинической картины, гистологического исследования пересаженных тканей, ряда лабораторных и инструментальных методов в зависимости от типа трансплантата. Лечение сводится к проведению иммуносупрессивной терапии, использованию цитотоксических средств, некоторые препараты назначают пожизненно.
Иммунологические реакции отторжения трансплантата возникают при использовании аллогенных (пересаженных от человека человеку) или ксеногенных (от животных человеку) тканей и органов. Аутотрансплантаты, например кожа, пересаженная с бедра на лицо, имеют такую же антигенную структуру, как и другие ткани организма, поэтому реакции не вызывают. Отторжение крайне редко возникает при пересадке бессосудистых структур - роговицы, некоторых хрящей - поскольку в этом случае отсутствует контакт чужеродных тканей с иммунокомпетентными клетками. Состояние было самым распространенным осложнением на заре трансплантологии, но в последние годы встречается все реже, несмотря на увеличение количества хирургических операций такого типа. Это связано с успехами в определении гистосовместимости тканей донора и реципиента, разработкой более действенных методов иммуносупрессивной терапии.
Причины реакции отторжения трансплантата
Антигенная совместимость тканей обусловлена сочетанием ряда антигенов - в первую очередь, главного комплекса гистосовместимости (шесть главных антигенов и ряд второстепенных или минорных). Кроме того, влияние могут оказывать и другие белковые антигенные комплексы (АВ0, белки соединительных тканей). Во многом реакции отторжения аналогичны обычному иммунному ответу при попадании в организм чужеродных антигенов или (в некоторых случаях) реакциям гиперчувствительности 2-го и 3-го типов. В их развитии принимают участие гуморальные и клеточные механизмы иммунитета. Скорость возникновения патологических изменений трансплантата зависит от вида реакции, активности иммунитета реципиента, величины антигенного различия тканей.
Причиной молниеносных разновидностей отторжения трансплантата служит сенсибилизация организма реципиента, в результате которой при пересадке возникают процессы, аналогичные реакциям непереносимости с образованием иммунных комплексов и активацией системы комплемента. Более распространенные острые виды иммунологической реакции на пересаженные ткани обычно развиваются из-за несовместимости по антигенам ГКГС, в патогенезе участвует преимущественно клеточный иммунный ответ. Хронические формы РОТ обусловлены как клеточными, так и гуморальными реакциями, их причиной часто становится некорректная иммуносупрессивная терапия, назначенная после операции.
Процессы патогенеза реакции отторжения трансплантата отличаются при разных формах этого состояния. Сверхострые или молниеносные реакции обусловлены сенсибилизацией организма к антигенам пересаженного органа, поэтому протекают по типу непереносимости или аллергии. При контакте тканей аллотрансплантата с кровью реципиента стимулируется образование иммунокомплексов, оседающих на внутренней поверхности сосудов. Они провоцируют активацию системы комплемента, сильно повреждая эндометрий сосудистой сети трансплантата, из-за чего происходит образование множественных микротромбов и эмболизация сосудов. Это ведет к ишемии пересаженных тканей, их отеку, а при отсутствии терапевтических мер - к некрозу. Скорость развития патологических процессов составляет всего несколько часов или суток.
В основе острых и хронических видов РОТ лежат процессы клеточного иммунного ответа, поэтому такие реакции развиваются несколько медленнее - на протяжении нескольких недель. При антигенной несовместимости тканей трансплантата и реципиента на фоне адекватной или повышенной активности иммунитета происходит распознавание чужеродных клеток макрофагами и Т-лимфоцитами (хелперами или индукторами). Последние активируют Т-киллеры, которые выделяют протеолитические ферменты, разрушающие клеточные мембраны структур аллотрансплантата. Итогом является развитие воспалительной реакции в пересаженном органе, выраженность которой зависит от уровня активности иммунной системы. При длительно протекающем процессе возможно подключение гуморальных факторов иммунитета с синтезом специфических антител, направленных против антигенов трансплантата.
Выделяют несколько форм реакции отторжения, различающихся между собой по скорости развития и ряду клинических проявлений. Причиной такой разницы являются разные виды РОТ, обладающие неодинаковой скоростью возникновения, а также преимущественным поражением тех или иных структур трансплантата. Зная примерные сроки формирования того или иного типа иммунного ответа, специалист может определить его характер и назначить оптимальное лечение. Всего существует три основных клинических формы реакций непереносимости тканей трансплантата:
- Молниеносная или сверхострая. Возникает в первые минуты или часы после «подключения» пересаженного органа к системному кровотоку реципиента, обусловлена сенсибилизацией организма последнего к антигенам трансплантата. Характеризуется массивными микроциркуляторными нарушениями с ишемическими явлениями в аллотрансплантате и развитием некроза, воспаление при этом имеет вторичный характер.
- Острая. Регистрируется в течение первых трех недель после пересадки, патогенез основан на клеточном иммунном ответе при несовместимости донора и реципиента. Основным проявлением становится развитие воспалительных процессов в пересаженных тканях, их выраженность зависит от активности иммунитета.
- Хроническая. Возникает через несколько месяцев после трансплантации, может иметь рецидивирующий характер, сильно зависит от режима иммуносупрессивной терапии. Развивается посредством как клеточных, так и гуморальных механизмов иммунного ответа.
Симптомы реакции отторжения трансплантата
Все проявления отторжения аллотрансплантата разделяют на системные, зависящие только от патогенеза процесса и реактивности иммунитета, и локальные, связанные непосредственно с трансплантированным органом или тканью. Среди общих симптомов всегда наблюдается повышение температуры, озноб, лихорадка большей или меньшей степени выраженности. Регистрируются проявления общей интоксикации - головная боль, тошнота, рвота, снижение артериального давления. Симптомы интоксикации организма резко усиливаются при развитии процессов некроза в трансплантате, в тяжелых случаях на этом фоне возможно возникновение токсигенного шока.
Локальные проявления РОТ связаны с пересаженным органом, поэтому могут различаться у разных больных. При трансплантации целого органа на первый план выступают симптомы, обусловленные нарушением его функции - например, кардиалгии, нарушения ритма, сердечная недостаточность при пересадке сердца. Острая почечная недостаточность может быть связана с реакцией отторжения трансплантированной почки, печеночная - печени. При аллотрансплантации кожного лоскута возникает его отек, покраснение вплоть до багрового оттенка, возможно присоединение вторичной бактериальной инфекции. Сроки появления местных и общих симптомов отторжения зависят от его формы - молниеносный тип характеризуется тяжелой реакцией уже через 2-3 часа после трансплантации, тогда как острые и хронические виды могут проявляться через несколько недель или даже месяцев.
Осложнения
Наиболее ранним и тяжелым осложнением реакции отторжения пересаженных тканей является развитие шока, связанного с иммунологическими процессами или обусловленного интоксикацией организма. Некроз и поражение тканей трансплантированного органа, работа которого является жизненно важной для организма (например, сердца), часто приводит к летальному исходу. К осложнениям РОТ некоторые специалисты относят и инфекционные болезни, вызванные усиленной иммуносупрессивной терапией. В отдаленной перспективе на фоне искусственного понижения активности клеточного иммунитета возможно развитие онкологических заболеваний.
Особенностью диагностики реакции отторжения трансплантата является необходимость ее максимально быстрого проведения, позволяющего не только улучшить состояние больного, но и сохранить пересаженный орган. Некоторые исследователи относят к диагностике РОТ ряд иммунологических исследований, выполняемых перед операцией на этапе подбора донора - типирование спектра трансплантационных антигенов, определение биологической совместимости тканей. Качественное выполнение данных анализов позволяет избежать развития сверхострой реакции и значительно снизить вероятность возникновения других форм отторжения. Среди диагностических процедур, выполняемых после трансплантации, наиболее информативными являются следующие:
- Лабораторные исследования. При процессе отторжения в общем анализе крови будут выявляться признаки неспецифического воспаления - лимфоцитоз, увеличение СОЭ. Исследование иммунного статуса позволяет обнаружить иммунные комплексы, увеличение уровня компонентов комплемента (при молниеносных формах), иммуноглобулинов. Под действием иммуносупрессивной терапии результаты анализов могут искажаться, что необходимо учитывать при их интерпретации.
- Инструментальные исследования. Инструментальные методы диагностики (рентгенография, УЗИ, УЗДГ, КТ, МРТ) используют для оценки функциональной активности и структуры трансплантата - почки, печени, сердца, легкого. В общем плане РОТ проявляется отеком органа, нарушением его работы, наличием циркуляторных нарушений (ишемии, инфарктов, некроза). При хронических и рецидивирующих типах реакции в структуре трансплантата могут определяться участки склероза.
- Гистологические исследования. Биопсия тканей аллотрансплантата, их последующее гистологическое и гистохимическое изучение является золотым стандартом в определении РОТ. При молниеносном типе реакции в биоптате выявляются поврежденны е капилляры, периваскулярный отек, признаки ишемии и некроза тканей, биохимические исследования определяют иммунные комплексы на поверхности эндометрия. При хронических или острых типах отторжения обнаруживается лимфоцитарная инфильтрация тканей трансплантата, наличие участков ишемии и склероза.
Подходы к диагностике реакций отторжения могут меняться с учетом конкретного пересаженного органа. Например, при трансплантации почки показаны общий и биохимический анализ мочи, УЗДГ и другие ультразвуковые исследования органа, с осторожностью - экскреторная урография. В случае пересадки сердца необходимо проведение электрокардиографии, ЭхоКГ, коронарной ангиографии.
Лечение реакции отторжения трансплантата
Лечение РОТ заключается в уменьшении активности иммунного ответа, до сих пор продолжается разработка наиболее эффективных методов. Составлением схемы терапии занимается врач-иммунолог в кооперации с трансплантологом. Перспективной техникой считается выработка иммунологической толерантности к антигенам аллотрансплантата, однако ее механизмы довольно сложны и пока недостаточно изучены. Поэтому практически единственным методом лечения и профилактики отторжения является неспецифическая иммуносупрессивная терапия, проводимая несколькими группами лекарственных средств:
- Стероидные препараты. К этой группе относят преднизолон и его производные, дексаметазон и другие средства. Они снижают скорость пролиферации лимфоцитов, являются антагонистами многих факторов воспаления, эффективно уменьшают выраженность иммунного ответа. В ряде случаев курсовое применение этих препаратов после проведения трансплантации назначают пожизненно.
- Аналоги азотистых оснований. Данные препараты способны встраиваться в процесс синтеза нуклеиновых кислот и тормозить его на определенном этапе, снижая скорость образования иммунокомпетентных клеток и выраженность процессов отторжения. В целях профилактики их используют вскоре после пересадки органа.
- Алкилирующие средства. Группа препаратов, способных присоединяться к ДНК клеток и блокировать их деление. Медикаменты применяют при острых формах данного состояния по причине быстрого и надежного цитотоксического эффекта.
- Антагонисты фолиевой кислоты. Витамин В9 участвует в синтезе некоторых азотистых оснований и пролиферации лимфоцитов, его антагонисты замедляют процесс развития иммунного ответа при РОТ. Средства используют при хронических формах реакции в составе комплексной терапии.
- Антибиотики. Отдельные препараты данной группы (циклоспорин, хлорамфеникол) блокируют синтез РНК, тормозя как клеточные, так и гуморальные иммунные реакции. Иногда применяются пожизненно после трансплантации для профилактики отторжения.
По показаниям могут быть назначены и другие медикаменты для улучшения состояния больного - детоксикационные препараты, диуретики, стимуляторы сердечной деятельности, противовоспалительные и жаропонижающие средства. При тяжелых осложнениях (шок, острая сердечная или почечная недостаточность) необходимы реанимационные мероприятия, гемодиализ. При присоединении инфекции на фоне иммуносупрессии требуется своевременное назначение антибиотиков, противогрибковых или противовирусных (с учетом характера возбудителя) средств.
Прогноз при молниеносных видах реакции отторжения трансплантата практически в 100% случаев неблагоприятный - требуется операция по удалению пересаженного органа, подбор нового донора и повторная трансплантация. В то же время, риск развития РОТ при вторичной пересадке повышается в несколько раз. Своевременно начатая иммуносупрессия при острых или хронических вариантах состояния нередко позволяет сохранить аллотрансплантат, но повышает риск инфекционных осложнений и вероятность возникновения рака в будущем. Эффективной профилактикой отторжения является тщательный подбор донора для пересадки, проверка совместимости по всем возможным антигенным системам - особенно по ГКГС, совместимы должны быть не менее 4-х из 6-ти главных аллелей. Резко снижает вероятность развития патологии наличие прямой кровной родственной связи между донором и реципиентом.
Читайте также:
