Вторичное повреждение мозга при черепно-мозговой травме. Механизмы
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Категории МКБ: Внутричерепная травма с продолжительным коматозным состоянием (S06.7), Диффузная травма головного мозга (S06.2), Очаговая травма головного мозга (S06.3), Травматический отек головного мозга (S06.1), Травматическое субарахноидальное кровоизлияние (S06.6), Травматическое субдуральное кровоизлияние (S06.5), Эпидуральное кровоизлияние (S06.4)
Общая информация
Краткое описание
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: S06.1 S06.2 S06.3 S06.4 S06.5 S06.6 S06.7
Черепно-мозговая травма (ЧМТ)- повреждения черепа, головного мозга, мозговых оболочек, сосудов и черепно-мозговых нервов сопровождающиеся клинической симптоматикой и в большинстве случаев морфологическими изменениями. Крайне важным является наличие четкого травматического анамнеза.
Тяжелая черепно-мозговая травма - остро развившееся нарушение функции мозга, вследствие воздействия механической энергии, при котором пострадавший при поступлении в стационар находится в тяжелом или крайне тяжелом состоянии со снижением уровня бодрствования от 8 до 3 баллов по шкале комы Глазго и/или с выраженными повреждениями головного мозга очагового, диффузного или смешанного характера.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической классификации болезней и проблем, связанных со здоровьем

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Классификация ЧМТ основана на ее биомеханике, виде, типе, характере, форме, тяжести повреждений, клинической фазе, периоде течения, а также исходе травмы [41].
По клиническим формам : 1) сотрясение мозга, 2) ушиб мозга легкой степени, 3) ушиб мозга средней степени, 4) ушиб мозга тяжелой степени, 5) диффузное аксональное повреждение, 6) сдавление мозга, 7) сдавление головы.
По генезу повреждения мозга при ЧМТ дифференцируют: 1) первичные повреждения которые возникают в результате непосредственного воздействия травмирующих факторов - очаговые ушибы и размозжения мозга, диффузные аксональные повреждения, первичные внутричерепные гематомы, их сочетания; 2) вторичные интракраниальные повреждения являются результатом воздействия таких факторов, как нарушение проницаемости ГЭБ, увеличения объема мозга или его набухания вследствие отека, гиперемии или венозного полнокровия, повышения интракраниального давления, смещений и деформаций мозга, отсроченных гематом (эпи-субдуральных, внутримозговых), нарушения гемо- и ликвороциркуляции в результате субарахноидального или внутрижелудочкового кровоизлияния, внутричерепной инфекции и др. б) вторичные экстракраниальные факторы: артериальная гипотензия, гипоксемия, гиперкапния, анемия и др. Вторичные факторы могут быть предупреждены или излечены, что зависит от своевременной и правильной диагностики, организации и качества нейрохирургической помощи.
По течению травматической болезни головного мозга [21,23] 1) острый, 2) промежуточный, 3) отдаленный.
Примечание. Острый период - это промежуток времени от момента повреждающего воздействия механической энергии на головной мозг с внезапным расстройством его интегративно-регуляторных и локальных функций до стабилизации на том или ином уровне нарушенных общемозговых и общеорганизменных функций, либо смерти пострадавшего. Временная протяженность острого периода от 2 до 10 недель в зависимости от клинической формы ЧМТ. Примерные сроки острого периода ЧМТ при сотрясении мозга - до 2 недели легком ушибе мозга - до 3 недели, средне- тяжелом ушибе мозга - до 4 - 5 неделей, тяжелом ушибе мозга - до 6 - 8 неделей6 диффузном аксональном повреждении - до 8 -10 неделей, сдавлении мозга - от 3 до 10 неделей (в зависимости от фона).
Промежуточный период - это промежуток времени от стабилизации нарушенных травмой общеорганизменных, общемозговых, очаговых функций до их полного или частичного восстановления или устойчивой компенсации. Временная протяженность промежуточного периода: при легкой ЧМТ - до 2 месяцев, при среднетяжелой ЧМТ - до 4 месяцев, при тяжелой ЧМТ - до 6 месяцев.
Отдаленный период - это период клинического выздоровления, либо максимально достижимой реабилитации нарушенных функций, либо возникновения и/или прогрессирования обусловленных перенесенной ЧМТ новых патологических состояний. Временная протяженность отдаленного периода: при клиническом выздоровлении - до 2 лет, при проградиентном течении - не ограничена [21,23].
По характеру ЧМТ (закрытая/открытая; проникающая/непроникающая; изолированная/сочетанная/комбинированная)
По субстрату повреждения: (ДАП/очаги ушибов/оболочечные гематомы; повреждения костных структур; наличие или отсутствие субарахноидального кровоизлияния; а также подробно описать повреждение мягких тканей и экстракраниальных структур (грудная/брюшная полость; шейный отдел позвоночника; скелетная травма, таз).
По наличию повреждений мягких тканей выделяют закрытую тяжелую ЧМТ (с повреждением мягких тканей до апоневроза) и открытую (с повреждением мягких тканей глубже апоневроза).
По наличию повреждений ТМО выделяют проникающую (ТМО повреждена) и непроникающую (ТМО не повреждена) тяжелую ЧМТ.
По типу ЧМТ различают: изолированную (если отсутствуют какие-либо внечерепные повреждения), сочетанную (если механическая энергия одновременно вызывает внечерепные повреждения) и комбинированную (если одновременно воздействуют различные виды энергии — механическая и термическая или лучевая, или химическая) травмы
Комментарий. Используемые шкалы для оценки состояния пациентов с исходами ЧМТ: шкала исходов Глазго (в том числе расширенная, модифицированная) (приложения Г6, Г7)
Этиология и патогенез
Черепно-мозговая травма (ЧМТ) — одна из главных проблем современного здравоохранения. По данным Всемирной организации здравоохранения, травма, в том числе ЧМТ, является одной из 3 основных факторов (наряду с сердечно-сосудистыми и онкологическими заболеваниями) смертности населения в мире. Для трудоспособного населения травматизм — ведущая причина летальных исходов [50]. По данным Всемирной организации здравоохранения дорожно-транспортный травматизм в настоящее время является ведущей причиной смертности у детей и молодых людей в возрасте от 5 до 29 лет, а также является одной из ведущих причинсмертности для людей всех возрастов. Более 1,35 млн. человек в мире погибли в 2016 году только в результате ДТП [11,1].
В основе развития заболевания лежит концепция первичных и вторичных повреждений. Первичные повреждения возникают результате непосредственного воздействия механической энергии. Вторичные повреждения - возникают вследствие сложных и многообразных механизмов, которые «включаются» в момент травмы. При воздействии внешнего травмирующего фактора возникают контактные повреждения черепа, его оболочек, сосудов головного мозга и его вещества. При травме высоких скоростей (автоаварии, падение с высоты и др.) возникают линейные и угловые ускорения головы, происходят смещение и ротация мозга в полости черепа, полушарий мозга относительно его оси, кавитационные процессы, что также приводит к первичному повреждению головного мозга [13,23].
В зависимости от особенностей биомеханики травмы выделяют локальные и диффузные повреждения мозга. Локальные повреждения , как правило, возникают в результате прямого воздействия травмирующей силы или в результате контрудара. Диффузные повреждения мозга , среди которых выделяют диффузное аксональное и диффузное сосудистое повреждения, возникают в результате ускорения/торможения и ротационных механизмов. Чаще всего при ЧМТ наблюдают сочетание как локальных, так и диффузных повреждений головного мозга [10].
Патогенез ЧМТ. При первичном повреждении происходит нарушение структуры нейронов и глиальных клеток, образуются синаптические разрывы, возникает тромбоз сосудов и нарушается целостность сосудистой стенки. Вокруг очага первичного повреждения формируется перифокальная зона, в которой клетки сохраняют свою жизнеспособность, но становятся крайне чувствительными к малейшим изменениям доставки кислорода и питательных веществ (зона пенумбры).
Вследствие сложных и многообразных патофизиологических механизмов, которые индуцируются в момент травмы и развиваются с течением времени, возникают вторичные повреждения мозга. В ответ на первичное механическое повреждение в веществе мозга возникает патологический процесс, являющийся эволюционно выработанной воспалительной реакцией. Действие первичного травмирующего агента инициирует биохимические и иммунологические деструктивные процессы. Нарушаются процессы окислительного фосфорилирования в митохондриях, увеличивается концентрация внутриклеточного кальция, освобождаются свободные радикалы кислорода и вазоактивные метаболиты арахидоновой кислоты, активируются механизмы комплементного каскада и перекисного окисления липидов. Происходит накопление «возбуждающих» аминокислот, таких как глутамат и аспартат, что приводит к повреждению мембран нейронов и эндотелия мозговых капилляров (эксайтотоксичность). Нарушаются церебральная микроциркуляция и метаболизм клеток, развивается отек мозга [13,23]..
Вследствие повреждения мозга происходит активация метаболизма нейронов, что сопровождается истощением АТФ и нарушением функции кальциевого насоса. В результате увеличивается проницаемость клеточных мембран для ионов кальция и выход кальция из внутриклеточных депо, что вызывает деполяризацию нервных окончаний и выброс из них «возбуждающих» нейротрансмиттеров (глутамата). Глутамат, активируя постсинаптические комплексы, вызывает приток в клетку ионов натрия, деполяризацию, и еще большее поступление ионов кальция через ионные каналы. Следствием перегрузки клетки кальцием является ее повреждение, обусловленное активацией фосфолипаз, протеаз и нуклеаз, ведущее к нарушению целостности клеточных мембран, фосфорилирования и синтеза белков и экспрессии генома, лизису структурных белков клетки. Гибель нейронов при ЧМТ также возникает вследствие процессов апоптоза. Апоптоз может запускаться как прямым воздействием травмирующего агента на геном клетки, так и опосредованно - путем повреждающего действия медиаторов воспаления. Следствием действия факторов вторичного повреждения мозга являются нарушение доставки кислорода и питательных веществ к клеткам головного мозга и недостаточная их утилизация. Особенно страдают клетки, близко расположенные к очагу первичного повреждения мозга (зона пенумбры). Возникают нарушения церебральной микроциркуляции, оксигенации и метаболизма нейронов, развивается отек мозга и его ишемия. Вторичные ишемические повреждения мозга возникают у 36-42,6% пострадавших с ЧМТ средней степени тяжести и у 81-86,4% больных с тяжелой ЧМТ. Развитие вторичных повреждений мозга существенно усугубляет тяжесть состояния пострадавших с ЧМТ, ухудшает восстановление психической и моторной деятельности больных и повышает риск развития неблагоприятного исхода. В связи с этим предупреждение и своевременная коррекция факторов вторичного повреждения мозга являются важнейшей задачей лечения пострадавших с тяжелой ЧМТ [13].
Эпидемиология
По данным НИИ скорой помощи им. Склифосовского число госпитализированных с ЧМТ пациентов в г. Москве составляет от 10000 до 13000 в год. Преимущественно страдают мужчины, средний возраст до 43 лет, при этом от 15 до 25% пациентов имеют сочетанные повреждения [13].
Наиболее сложной группой являются пострадавшие с угнетением сознания до уровня комы (8 баллов и менее по шкале комы Глазго, что свидетельствует о тяжелой ЧМТ. Адекватная диагностика первичных повреждений мозга, своевременное предупреждение и лечение вторичных патофизиологических реакций и механизмов повреждения во многом определяют возможность снижения летальности и тяжелых инвалидизирующих последствий [1]. В большинстве исследований отмечено, что черепно- мозговая травма чаще встречается среди детей, молодых людей до 30 лет и среди пожилых пациентов. Преимущественно ЧМТ получают мужчины. В различных исследованиях посвященных ЧМТ доля мужчин колеблется от 70 до 81%. Доля мужчин и женщин в разных странах составляет от 1.2:1 в Швеции до 2.7:1 в Испании. В развивающихся странах это соотношение составляет- 4.8:1.
Клиническая картина
Cимптомы, течение
Клиническая картина ЧМТ обусловлена сложным симтомокомплексом, включающим общемозговую, менигеальную, очаговую симптоматику. Для клиники внутричерепных гематом характерно трехфазное течение - первичная утрата сознания, далее светлый промежуток и повторное ухудшение состояния с развитием снижения уровня сознания до сопора или комы [11,1]. Следует иметь ввиду, что помимо классического «светлого» промежутка после первичной утраты сознания может отмечаться редуцированный «светлый» промежуток или его отсутствие. Острая субдуральная гематома может быть как изолированной, так и сочетаться с контузионными очагами повреждения головного мозга. Ушиб головного мозга тяжелой степени характеризуется утратой сознания на срок от нескольких часов до нескольких суток, развивается снижение бодрствования до сопора или комы, может отмечаться психомоторное возбуждение, стволовые симптомы, горметония, менингеальные знаки, эпилептические приступы, нарушение витальных функций.
Появление брадикардии при ЧМТ обусловлено рефлекторным раздражением ядер блуждающего нерва вследствие ВЧГ и дислокации. Анизокория чаще развивается на стороне гематомы при начальной фазе височно-тенториальной дислокации, чаще при острых субдуральных гематомах, однако не во всех случаях (до 30% по данным НИИ СП им. Склифосовского, 2019). При наличии анизокории в 82% случаев она отмечалась на стороне гематомы, в 18% на противоположной стороне [1]
Клиническая картина острой эпидуральной гематомы зависит от темпа ее развития и локализации, при быстром развитии дислокационного синдрома пациенты могут поступать в стационар в тяжелом состоянии, при этом частота сопора и комы доходит до 60% [11,1]. Часто при данном виде гематом отмечается отсутствие светлого промежутка до 40% случаев. При прогрессировании дислокационного синдрома развивается общемозговая, гипертензионная, менингеальная симптоматика, сонливость, психомоторное возбуждение, брадикардия и последующее снижение уровня бодрствования. У 7% пациентов возможны судороги [1]. Особенностью клинического течения ОЭГ является возможность их отсроченного нарастания в динамике, в связи с этим всем пострадавшим с тяжелой ЧМТ при ухудшении состояния или при выявлении ОЭГ небольшого объема необходимо проведение повторной СКТ головного мозга. До 90% пациентов с ОЭГ имеет перелом костей черепа.
В отличие от эпидуральных, субдуральные гематомы не ограничены в своем распространении и могут располагаться над 2 долями мозга и более, при этом переломы костей черепа при ОСГ встречаются реже, чем при ОЭГ - до 45% [11,1]. В отличие от ОЭГ при ОСГ дислокационный синдром развивается медленнее, в клинической картине преобладают общемозговые симптомы и психические нарушения, несколько чаще встречаются эпилептические приступы (до 12%). Трехфазное течение при ОСГ встречается редко, однако чаще выражена анизокория (до 56%) и брадикардия (50%), до 28% пациентов имеет контралатеральную пирамидную недостаточность. Тяжесть состояния пациента с ОСГ обусловлена ее объемом, так при объеме гематомы до 50 см3 пациенты не имеют грубого нарушения уровня бодрствования.
Диффузное аксональное повреждение головного мозга характеризуется длительным (до 2—3 нед.) коматозным состоянием, выраженными стволовыми симптомами (парез взора вверх, разностояние глаз по вертикальной оси, двустороннее угнетение или выпадение световой реакции зрачков, нарушение или отсутствие окулоцефалического рефлекса и др.). Часто наблюдаются нарушения частоты и ритма дыхания, нестабильность гемодинамики. Характерной особенностью клинического течения диффузного аксонального повреждения является переход из длительной комы в стойкое или транзиторное вегетативное состояние, о наступлении которого свидетельствует появление ранее отсутствовавшего открывания глаз спонтанно либо в ответ на различные раздражения. При этом нет признаков слежения, фиксации взора или выполнения хотя бы элементарных инструкций (данное состояние называют апаллическим синдромом). Вегетативное состояние у таких больных длится от нескольких суток до нескольких месяцев и характеризуется функциональным и/или анатомическим разобщением больших полушарий и ствола мозга. По мере выхода из вегетативного состояния неврологические симптомы разобщения сменяются преимущественно симптомами выпадения. Среди них доминирует экстрапирамидный синдром с выраженной мышечной скованностью, дискоординацией, брадикинезией, олигофазией, гипомимией, мелкими гиперкинезами, атаксией. Одновременно четко проявляются нарушения психики: резко выраженная аспонтанность (безразличие к окружающему, неопрятность в постели, отсутствие любых побуждений к какой-либо деятельности), амнестическая спутанность, слабоумие и др. Вместе с тем наблюдаются грубые аффективные расстройства в виде гневливости, агрессивности [11,1].
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Механизмы вторичного повреждения нейронов при тяжелой черепно-мозговой травме (часть 1)
Обзор посвящен механизмам вторичного гипоксически-ишемического повреждения головного мозга при тяжелой черепно-мозговой травме. Приводятся новые данные по механизмам глутамат-кальциевого повреждения нейронов и ок-сидантного стресса. Ключевые слова: центральная нервная система, черепно-мозговая травма, гипоксия, ишемия, глутамат-кальциевый каскад, оксидантный стресс.
Об авторах
Список литературы
2. Balestreri M., Czosnyka M., Steiner L. A. et al.Intracranial hypertension: what additional information can be derived from ICP waveform after head injury? Acta Neurochir. (Wien) 2004; 146 (2): 131 — 141.
4. Park E., Bell J. D., Siddiq I. P., Baker A. J.An analysis of regional microvascular loss and recovery following two grades of fluid percussion trauma: a role for hypoxia-inducible factors in traumatic brain injury. J. Cereb. Blood Flow Metab. 2009; 29 (3): 575—58
5. Armstead W. M., Kiessling J. W., Kofke W. A, Vavilala M. S.SNP improves cerebral hemodynamics during normotension but fails to prevent sex dependent impaired cerebral autoregulation during hypotension after brain injury. Brain Res. 2010; 1330: 142—150.
6. Lo E. H.A new penumbra: transitioning from injury into repair after stroke. Nat. Med. 2009; 14 (5): 497—500.
7. Candelario-Jalil E.Injury and repair mechanisms in ischemic stroke: considerations for the development of novel neurotherapeutics. Cur. Opin. Investig. Drugs 2009; 10 (7): 644—654.
8. Greve M. W., Zink B. J.Pathophysiology of traumatic brain injury. Mt. Sinai J. Med. 2009; 76 (2): 97—104.
9. Wang Q., van Hoecke M., Tang X. N. et al.Pyruvate protects against experimental stroke via an anti-inflammatory mechanism. Neurobiol. Dis. 2009; 36 (1): 223—231.
12. Gibbs M. E., Hertz L.Inhibition of astrocytic energy metabolism by D-lac-tate exposure impairs memory. Neurochem. Int. 2008; 52 (6): 1012—1018.
13. Mangia S., Simpson I. A., Vannucci S. J., Carruthers A.Thein vivoneu-ron-to-astrocyte lactate shuttle in human brain: evidence from modeling of measured lactate levels during visual stimulation. J. Neurochem. 2009; 109 (Suppl 1): 55—62.
14. Yamagata K., Tagami M., Yamori Y.Nitric oxide reduces astrocytic lac-tate production and induces neuronal vulnerability in stroke-prone spontaneously hypertensive rats. Glia 2008; 56 (4): 387—393.
15. Lewerenz J., Dargusch R., Maher P.Lactacidosis modulates glu-tathione metabolism and oxidative glutamate toxicity. J. Neurochem. 2010; 113 (2): 502—514.
16. Li Y., Li Q., Wang Z. et al.15-HETE suppresses K (+) channel activity and inhibits apoptosis in pulmonary artery smooth muscle cells. Apoptosis 2009; 14 (1): 42—51.
17. Кармен Н. Б.К механизму нейропротекторного действия клониди-на. Анестезиология и реаниматология 2005; 3: 53—57.
18. Siesjo B. K., Siesjo P.Mechanisms of secondary brain injury. Eur. J. Anaesthesiol. 1996; 13 (3): 247—268.
19. Маевский Е. И., Розенфельд А. С., Гришина Е. В., Кондрашова М. Н.Коррекция метаболического ацидоза путем поддержания функций митохондрий. Пущино; 2001.
20. Иванов К. П., Мельникова Н. Н.Роль лейкоцитов в микрососудах мозга в норме и ее нарушения при гипоксии. Гематология и транс-фузиология 2003; 48 (3): 21—27.
21. Lao F., Chen L., Li W. et al.Fullerene nanoparticles selectively enter oxidation-damaged cerebral microvessel endothelial cells and inhibit JNK-related apoptosis. ACS Nano 2009; 3 (11): 3358—3368.
23. Rothman S. M., Olney J. W.Glutamate and the pathophysiology of hypoxic-ischemic brain damage. Ann. Neurol. 1986; 19 (2): 105—111.
24. Capela J.P., Carmo H., Remiao F. et al.Molecular and cellular mechanisms of ecstasy-induced neurotoxicity: an overview. Mol. Neurobiol. 2009; 39 (3): 210—271.
25. Pivovarova N. B., Hongpaisan J., Andrews S. B., Friel D. D.Depolarization-induced mitochondrial Ca accumulation in sympathetic neurons: spatial and temporal characteristics. J. Neurosci. 1999; 19 (15): 6372—6384.
26. Orrenius S., Zhivotovsky B., Nicotera P.Regulation of cell death: the cal-cium-apoptosis link. Nat. Rev. Mol. Cell Biol. 2005; 4 (7): 552—565.
27. Zablocka B., Domanka-Janik K.Enhancement of 3[H] D-aspartate release during ischemia like conditions in rat hippocampal slices: source of excitatory amino acids. Acta Neurobiol. Exp. (Wars.) 1996; 56 (1); 63—70.
28. ГусевЕ. И., СкворцоваВ. И.Ишемия головного мозга. М.: Медицина; 2001.
29. Monnerie H., Hsu F. C., Coulter D. A., Le Roux P. D.Role of the NR2A/2B subunits of the N-methyl-D-aspartate receptor in gluta-mate-induced glutamic acid decarboxylase alteration in cortical GABAergic neurons in vitro. Neuroscience 2010; 171 (4): 1075—1090.
30. Blackburn D., Sargsyan S., Monk P. N., Shaw P. J.Astrocyte function and role in motor neuron disease: a future therapeutic target? Glia 2009; 57 (12): 1251—1264.
31. Hur J, Lee P., Kim M.J. et al.Ischemia-activated microglia induces neu-ronal injury via activation of gp91phox NADPH oxidase. Biochem. Biophys. Res. Commun. 2010; 391 (3): 1526—1530.
32. Barros L. F., Deitmer J. W.Glucose and lactate supply to the synapse. Brain Res. Rev. 2010: 63 (1—2): 149—159.
34. Halim N. D., Mcfate T., Mohyeldin A. et al.Phosphorylation status of pyruvate dehydrogenase distinguishes metabolic phenotypes of cultured rat brain astrocytes and neurons. Glia 2010; 58 (10): 1168—1176.
35. Nakashima K., Todd M. M.Effects of hypothermia, pentobarbital, and isoflurane on postdepolarization amino acid release during complete global cerebral ischemia. Anesthesiology 1996; 85 (1): 161—168.
36. MacDonald J. W., Bhattacharyya T., Sensi S. L. et al.Extracellular acidity potentiates AMPA receptor-mediated cortical neuronal death. J. Neurosci. 1998; 18 (16): 6290—6299.
37. Pertusa M., Garcia-Matas S., Rodriguez-Farri E. et al.Astrocytes agedin vitroshow a decreased neuroprotective capacity. J. Neurochem. 2007; 101 (3): 794—805.
38. WillmoreL.J., Ueda Y.Posttraumatic epilepsy: hemorrhage, free radicals and the molecular regulation of glutamate. Neurochem. Res. 2009; 34 (4): 688—697.
39. Brahma M. K., Dohare P., Varma S. et al.The neuronal apoptotic death in global cerebral ischemia in gerbil: important role for sodium channel modulator. J. Neurosci. Res. 2009; 87 (6): 1400—1411.
40. Петров В. И., Пиотровский Л. Б., Григорьев И. А.Возбуждающие аминокислоты (нейрохимия, фармакология и терапевтический потенциал ВАКергических средств). Волгоград; 1997.
41. Heja L., Barabas P., Nyitrai G. et al.Glutamate uptake triggers transporter-mediated GABA release from astrocytes. PloS. One 2009; 4 (9): e7153.
42. Hardingham G. E.Coupling of the NMDA receptor to neuroprotective and neurodestructive events. Biochem. Soc. Trans. 2009; 37 (Pt 6): 1147—1160.
43. Matute C.Calcium dyshomeostasis in white matter pathology. Cell Calcium. 2010; 47 (2): 150—157.
44. Su W., Song X., Ji J. J.Functional expression of a large-conductance Ca2+-activated K+channel in mouse substantia nigra pars compacta dopaminergic neurons. Neurosci. Lett. 2010; 471 (1): 1—5.
45. Chinopoulos C., Connor J. A., Shuttleworth C. W.Emergence of a sper-mine-sensitive, non-inactivating conductance in mature hippocampal CA1 pyramidal neurons upon reduction of extracellular Ca2+: dependence on intracellular Mg2+ and ATP. Neurochem. Int. 2007; 50 (1): 148—158.
46. Bano D., Munarriz E., Chen H. L. et al.The plasma membrane Na+/Ca2+ exchanger is cleaved by distinct protease families in neuronal cell death. Ann. N.-Y. Acad. Sci. 2007; 1099: 451—455.
47. Brustovetsky T., Bolshakov A., Brustovetsky N.Calpain activation and Na (+)/Ca (2+) exchanger degradation occur downstream of calcium deregulation in hippocampal neurons exposed to excitotoxic glutamate. J. Neurosci. Res. 2010; 88 (6): 1317—1328.
48. Linde R., Laursen H., Hansen A. J.Is calcium accumulation post-injury an indicator of cell damage. Acta Neurochir. Suppl. 1996; 66: 15—20.
49. Ralay Ranaivo H., Wainwright M. S.Albumin activates astrocytes and microglia through mitogen-activated protein kinase pathways. Brain Res. 2010; 1313: 222—231.
50. Yao H., Shu Y., Wang J. et al.Factors influencing cell fate in the infarct rim. J. Neurochem. 2007; 100 (5): 1224—1233.
51. Tekkok S. B., Ye Z., Ransom B. R.Excitotoxic mechanisms of ischemic injury in myelinated white matter. J. Cereb. Blood Flow Metab. 2007; 27 (9): 1540—1552.
52. Phillips J. M., Nicholson C.Anion permeability in spreading depression investigated with ion-sensitive microelectrodes. Brain Res. 1979; 173 (3): 567—571.
53. Branston N. M., Strong A. J., Symon L.Extracellular potassium activity, evoked potential and tissue blood flow. Relationships during progressive ischaemia in baboon cerebral cortex. J. Neurol. Sci. 1977; 32 (3): 305—321.
56. Back T., Kohno K., Hossmann K. A.Cortical negative DC deflections following middle cerebral artery occlusion and KCl-induced spreading depression: effect on blood flow, tissue oxygenation, and electroencephalogram. J. Cereb. Blood Flow Metab. 1994; 14 (1): 12—19.
57. Mies G., Ishimaru S., Xie Y. et al.Ischemic thresholds of cerebral protein synthesis and energy state following middle cerebral artery occlusion in rat. J. Cereb. Blood Flow Metab. 1991; 11 (5): 753—761.
58. Sukhotinsky I., Yaseen M. A., Sakadzio S. et al.Perfusion pressure-dependent recovery of cortical spreading depression is independent of tissue oxygenation over a wide physiologic range. J. Cereb. Blood Flow Metab. 2010; 30 (6): 1168—1177.
59. Spiotta A. M., Stiefel M. F., Gracias V. H. et al.Brain tissue oxygen-directed management and outcome in patients with severe traumatic brain injury. J. Neurosurg. 2010; 113 (3): 571—580.
60. Dietrich W. D., Feng Z. C., Leistra H. et al.Photothrombotic infarction triggers multiple episodes of cortical spreading depression in distant brain regions. J. Cereb. Blood Flow Metab. 1994; 14 (1): 20—28.
Гематома головного мозга - симптомы и лечение
Что такое гематома головного мозга? Причины возникновения, диагностику и методы лечения разберем в статье доктора Яковлева Дмитрия Вячеславовича, нейрохирурга со стажем в 11 лет.
Над статьей доктора Яковлева Дмитрия Вячеславовича работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Гематома головного мозга — это грозное патологическое состояние, при котором кровь изливается из повреждённого сосуда внутрь черепной коробки. Скапливаясь во внутричерепном пространстве или в веществе головного мозга, кровь сдавливает мозг и повреждает его. Стремительно появляются и прогрессируют неврологические симптомы, столь же быстро, а иногда и молниеносно, гематома приводит к угнетению сознания, вплоть до комы. Данное состояние является тяжёлым и зачастую угрожает жизни, поэтому требует своевременной диагностики и лечения [1] .
Согласно зарубежным источникам:
- ежегодно инсульт головного мозга с формированием гематомы случается у 2400 человек из 1 млн жителей западных развитых стран ;
- из них более 700 человек ежегодно погибает;
- менее половины из этих 2400 человек восстанавливаются и способны полноценно обслуживать себя [11] .
Причины развития гематомы головного мозга:
- Основная — артериальная гипертензия и атеросклеротическая болезнь[2] . Риск инсульта с формированием гематомы среди пациентов с артериальной гипертензией составляет 60 %;
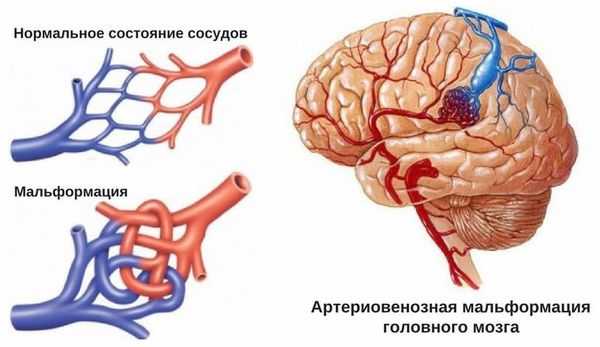
- Пороки развития сосудов головного мозга. К ним относят аневризму (выпячивание стенок мозговых артерий) и артериовенозную мальформацию (патологическое переплетение артерий и вен).
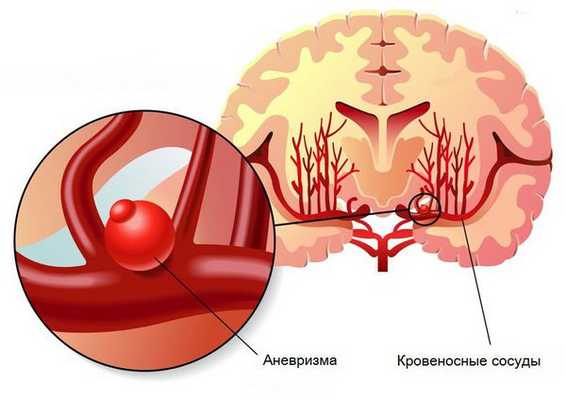
- Опухоли головного мозга, воспалительные заболевания сосудов, нарушения свёртывающей системы крови с повышением кровоточивости.
- Препараты, повышающие кровоточивость: антикоагулянты, антиагреганты и фибринолитики. Эти медикаменты назначают пациентам со склонностью к образованию тромбов и после тяжёлых шунтирующих операций. Приём лекарств необходим, но риск развития гематомы головного мозга при этом возрастает.
- Черепно-мозговые травмы. Гематомы возникают в 55 % всех случаев черепно-мозговых травм и являются причиной 2/3 смертей при данных повреждениях [12] . Травмы мозга — одна из самых частых причин смерти в развитых странах. По статистике они находятся на третьем месте после летальных исходов от сердечно-сосудистых заболеваний и онкологии [7] .
Причины развития гематом головного мозга зависят от возраста пациента:
- у детей — пороки развития сосудов головного мозга и болезни системы крови [3] ;
- у молодых взрослых — артериальная гипертензия, алкогольная и наркотическая интоксикации;
- у лиц среднего и пожилого возраста — артериальная гипертензия, опухоли головного мозга, артериовенозные мальформации и аневризмы.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гематомы головного мозга
Гематома головного мозга проявляется различными способами. Симптомы делятся на две группы:
1. Общемозговые — головная боль, головокружение, тошнота или рвота. Вызваны значительным повышением внутричерепного давления.
2. Очаговые — слабость в руке или ноге, нарушение зрения или движений глаз и др. Напрямую зависят от расположения гематомы.
Симптомы острой нетравматической гематомы:
- интенсивная головная боль, вызванная физической нагрузкой, эмоциональным перенапряжением, повышенным артериальным давлением [3] ;
- тошнота, рвота;
- нарушение речи;
- слабость в руке или ноге;
- асимметрия лица;
- крайне важные и тяжёлые признаки — судороги, кратковременная потеря или стойкое угнетение сознания, кома;
- пульсирующий шум в голове, нарушение координации или зрения, икота.
Патогенез гематомы головного мозга
К кровоизлиянию могут приводить травмы и различные заболевания. Однако при патологии всегда повреждается кровеносный сосуд и внутри или снаружи от вещества головного мозга скапливается кровь, для которой в норме нет места. Она сдавливает головной мозг и повреждает его отделы.
При внутримозговом кровоизлиянии гематома может формироваться в больших полушариях головного мозга и мозжечке. Расположение влияет на клиническую картину и косвенно указывает на причину кровоизлияния:
- гематомы, вызванные повышенным артериальным давлением, располагаются в глубоких отделах полушарий головного мозга вблизи таламуса или в мозжечке;
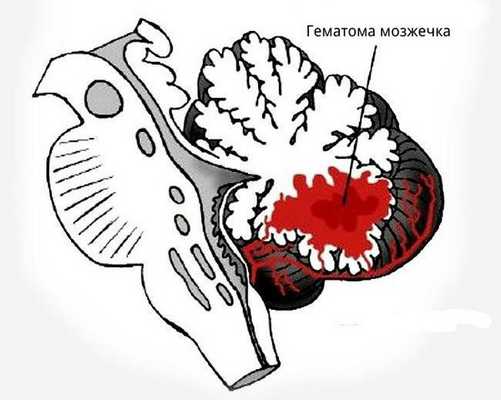
- более поверхностно локализованы гематомы, связанные с разрывом аневризм головного мозга, амилоидной ангиопатией (заболеванием мелких сосудов мозга), длительным приёмом препаратов, влияющих на свёртываемость крови, кавернозной ангиомой (сосудистой опухолью) или кровоизлиянием в опухоль;
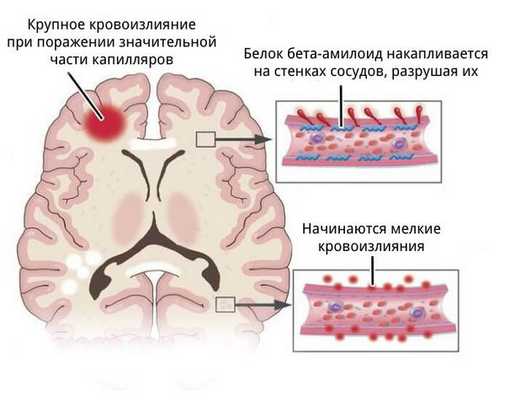
- для артериовенозных мальформаций характерно расположение гематомы под корой головного мозга, а также прорыв крови в полость между мозговыми оболочками.
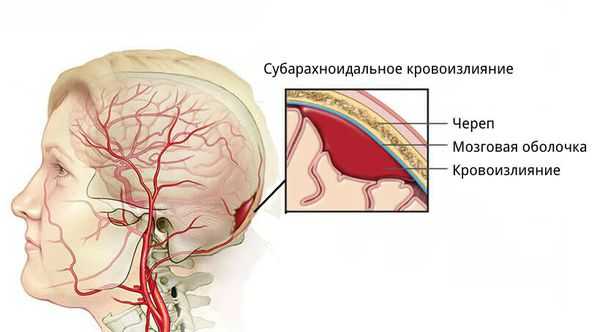
Классификация и стадии развития гематомы головного мозга
Все гематомы головного мозга подразделяются на две группы:
- нетравматические, или спонтанные;
- травматические, возникшие при травме.
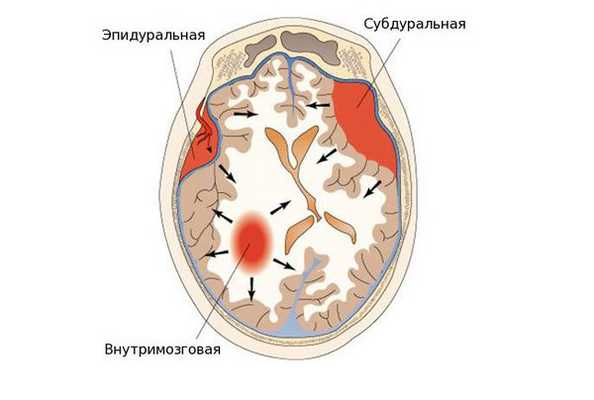
По локализации во внутричерепном пространстве выделяют:
- эпидуральные гематомы — располагаются между внутренней поверхностью костей черепа и твёрдой мозговой оболочкой;
- субдуральные — локализованы между твёрдой мозговой оболочкой и веществом головного мозга;
- внутримозговые гематомы — залегают в веществе головного мозга.
По срокам давности гематомы головного мозга подразделяются на три типа:
- острые — обнаружены в течение трёх суток после возникновения;
- подострые — выявлены через 3-21 день после травмы;
- хронические — после травмы и появления гематомы прошло более 21 дня.
Врач может определить приблизительный возраст гематомы по снимкам компьютерной и магнитно-резонансной томографии (КТ и МРТ). От срока давности зависит выбор методов лечения.
По глубине расположения гематомы делятся на два вида:
- поверхностные (подкорковые);
- глубокие (в центральных отделах полушария).
Внутримозговые кровоизлияния, приводящие к гематомам, разделяют на две группы:
- первичные, вызванные артериальной гипертензией (70-90 % всех внутримозговых гематом) [9] ;
- вторичные, связанные с нарушениями свёртываемости крови, сосудистой патологией и кровоизлиянием в опухоль.
Существует два механизма развития кровоизлияния:
- излившаяся кровь расслаивает вещество головного мозга и формирует полость с жидкой средой и кровяными свёртками;
- кровь пропитывает вещество мозга, перемешиваясь с ним.
Осложнения гематомы головного мозга
Внутричерепная гематома как частое последствие черепно-мозговых травм вызывает ряд нарушений, связанных с работой мозга. Так как череп является замкнутой жёсткой костной структурой, он не способен растягиваться и увеличиваться в объёме. Поэтому образовавшееся внутри черепной коробки скопление крови давит на головной мозг, спинномозговую жидкость и сосуды головного мозга, вытесняя и занимая их место. Именно из-за этого состояние пациента осложняется ещё сильнее [4] [5] .
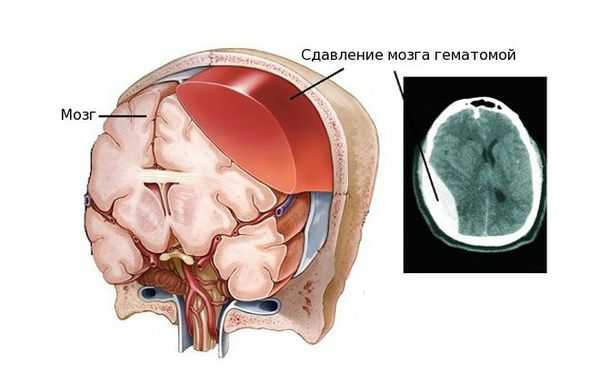
Вне зависимости от того, вызвана гематома травмой или заболеванием, проявление патологии схожее. Гематома вызывает следующие нарушения:
- Двигательные и чувствительные нарушения, например в ногах и руках. Возникают вследствие ограниченного проведения нервных импульсов.
- Гибель клеток мозга и отёк в результате сдавления сосудов головного мозга, ухудшения кровоснабжения и оттока крови.
- Смещение участков головного мозга.
- Повышение внутричерепного давления.
- Нарушение движения спинномозговой жидкости внутри черепа.
- Самое опасное последствие — вклинение ствола головного мозга в большое затылочное отверстие. Это приводит к остановке дыхания и сердечно-сосудистой деятельности.
Все вышеперечисленные процессы взаимосвязаны и влияют друг на друга. Последствия различаются в зависимости от объёма гематомы, расположения, наличия прорыва крови в желудочковую систему, нарушения циркуляции спинномозговой жидкости и других факторов. В самом худшем варианте — это смерть.
Часто после травмы головы с повреждением сосудов гематома развивается в течение трёх часов. Однако известны случаи отсроченных гематом, возникших через 72 часа. Невозможно точно указать время, когда гематома начнёт ухудшать состояние пациента, так как это зависит от её объёма. Малые гематомы, расположенные вне зон, регулирующих деятельность мышц и органов чувств, могут остаться незамеченными без проведения КТ и МРТ исследований.
Диагностика гематомы головного мозга
Как правило, пациенты или их родственники (если пациент находится в бессознательном состоянии) сперва сталкиваются не с неврологом или нейрохирургом, а с врачом скорой помощи, общей практики или терапевтом. Врач предполагает наличие внутричерепного кровоизлияния на основании состояния пациента, жалоб и сведений, полученных от него и сопровождающих лиц. В некоторых случаях определить гематому оказывается сложной задачей, и дальнейшую диагностику проводят врач-невролог или нейрохирург.
Для определения степени поражения головного мозга невролог и нейрохирург проводят оценку неврологического статуса (осмотр, проверка рефлексов). После этого подбирается тактика лечения.
Для подтверждения или опровержения гематомы, определения её расположения, сроков появления, размеров, степени сдавления головного мозга применяют методы нейровизуализации:
- Бесконтрастная компьютерная томография (КТ) — достоверный способ диагностики острых гематом головного мозга. КТ позволяет распознать гематому, её объём, воздействие на различные структуры головного мозга. На основании снимков КТ нейрохирург определяет тактику и объём оперативного вмешательства. Большинство стационаров, особенно оказывающих экстренную помощь, оснащены КТ аппаратами. Однако в хронической стадии и при пороках сосудов головного мозга без кровоизлияния КТ может не предоставить врачу нужной информации. В этих случаях применяют МРТ [8] .
- Магнитно-резонансная томография (МРТ) позволяет более подробно рассмотреть мягкотканные структуры. Поэтому в случае затруднений при диагностике, несмотря на проведённое КТ исследование, врач может назначить МРТ.
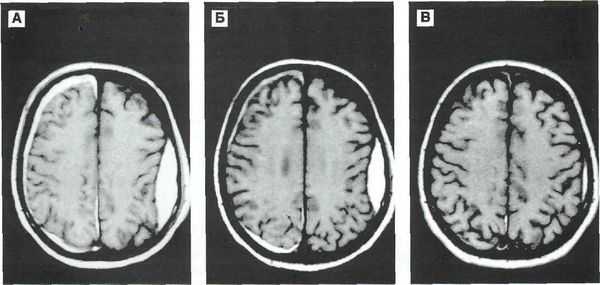
- Церебральная ангиография (золотой стандарт визуализации аневризм головного мозга [10] ), магнитно-резонансная ангиография (МРА) или КТ-ангиография дополняют МРТ исследования для определения патологии сосудов головного мозга. Преимущество КТ-ангиографии — возможность получить 3D-модель сосудов головного мозга и определить расположение относительно сосудистых или костных структур.
Ранее для диагностики широко применяли люмбальную пункцию. Однако этот метод имеет существенные недостатки и постепенно вытесняется вышеперечисленными, хотя в лечебных учреждениях, не оснащённых КТ и МРТ аппаратурой, применяется до сих пор.
Лечение гематомы головного мозга
Выделяют два вида лечения: консервативное и хирургическое.
Консервативное лечение
Методы консервативного (медикаментозного) лечения нормализуют жизненные функции организма:
- поддерживают артериальное давление на необходимом уровне: так, чтобы кровоснабжение головного мозга сохранялось, но объём гематомы при этом не увеличивался;
- воздействуют на свёртывающую систему крови;
- предотвращают и устраняют отёки;
- укрепляют сосудистую стенку.
Это крайне важный и ответственный этап лечения. Все мероприятия проводит врач, глубоко анализируя патогенетические процессы в организме человека. Многие методы основаны на лабораторных данных. Консервативную терапию ни в коей мере не могут контролировать или регулировать родственники либо сочувствующие лица из-за отсутствия у них этих знаний. Например снижение давления при гипотензивной терапии не должно быть резким. Его понижают до уровня, который не совпадает с показателями нормы для здорового человека. Давление поддерживают в определённых пределах: оно не должно быть слишком высоким, но и слишком низким. Это позволяет снизить риск продолжения кровоизлияния и сохранить адекватное кровенаполнение головного мозга для его защиты от вторичного повреждения из-за кислородного голодания.
Консервативные методы применяют для лечения в следующих случаях:
- гематомы небольших размеров и не оказывают значительного давления на мозг;
- гематомы не вызывают смещение структур головного мозга, грубого угнетения сознания, сопровождаются умеренными неврологическими нарушениями.
Хирургическое лечение
Хирургическое лечение заключается в механическом удалении гематомы. В результате прекращается давление гематомы на мозг.
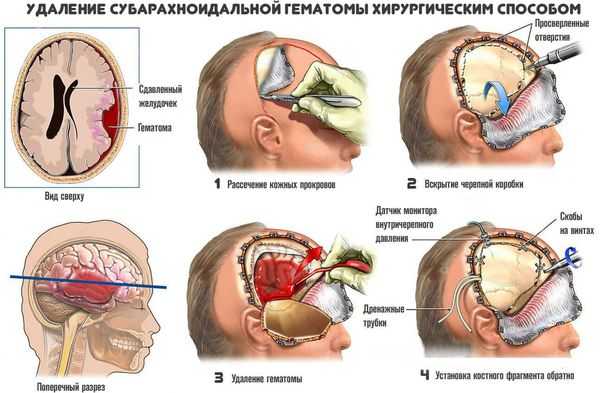
Применяют несколько методов хирургичекого удаления внутримозговых гематом:
- Пункционный метод — выкачивание жидкой части гематомы (аспирация) через отверстие. Однако удалить всю гематому таким способом невозможно, так как обычно она на 80 % состоит из кровяных сгустков, а жидкий компонент составляет 20 % и меньше. Метод применяют только при тяжёлой форме заболевания для спасения жизни. Если после операции состояние пациента не улучшается, то используют радикальные методы удаления.
- Открытый метод — традиционный способ удаления гематомы путем создания отверстия в костной ткани черепа (трепанации), рассечения участка мозга (энцефалотомии) и аспирации отсосом как жидкой крови, так и её сгустков. Метод позволяет полностью удалить гематому. Однако сопровождается дополнительной хирургической травмой мозга, что приводит к нарастанию отёка, усилению смещения и деформации структур мозга и нередко вызывает повторное кровоизлияние.
- Эндоскопический метод — перспективная технология удаления внутримозговых гематом. Совмещает низкую травматичность пункционного метода с возможностью полного удаления гематомы. Но метод можно применять только при условии прозрачности среды в зоне операции. Например, при кровотечении проведение операции затруднено, а часто и невозможно.
- Стереотаксический метод — проводят при помощи специальных инструментов, погружённых в головной мозг через отверстие диаметром 5-10 мм. Особенность метода — перенос координат гематомы с помощью компьютерной томографии или рентгенографии. Технология уменьшила летальность глубоких гематом на 22 % в сравнении с консервативными методами лечения. Однако в 10-16 % случаев возможны повторные кровоизлияния в первые несколько суток после операции.
- Нейронавигационный метод — применяют нейронавигационные системы: ОртiсаI Тracking System «Radionics Inc» Compass Cygnus PFS System, «Compass» Vectorvision ВrаinLАВ. Метод с высокой точностью определяет расположение гематомы. Технология особенно эффективна при очагах в функционально значимых зонах мозга. Её широкое применение пока невозможно из-за высокой стоимости оборудования и ограниченного опыта операций у врачей [13] .
Тактика оперативного вмешательства, его объём, меры для устранения сдавления головного мозга, сроки проведения операции и многое другое зависят от конкретной ситуации. Решение принимает врач-нейрохирург на основании состояния пациента, лабораторных данных и КТ/МРТ снимков.
Прогноз. Профилактика
Гематома головного мозга — это результат патологических изменений в организме, которые формируются постепенно под влияние различных причин. Поэтому прогноз в каждом конкретном случае будет различаться [3] .
Исход во многом зависит от объёма и расположения гематомы. Быстрое ухудшение состояния с угнетением сознания является негативным признаком. Согласно зарубежным источникам, гематомы головного мозга в 55 % случаев приводят к значительному ухудшению состояния пациента и смерти [6] . Поэтому очень важно незамедлительно доставить пациента в специализированный стационар и оказать медицинскую помощь.
После выздоровления могут остаться последствия повреждения мозговой ткани: слабость в руке или ноге, когнитивные расстройства (нарушение мышления, памяти, снижение критики к своему состоянию и поведению).
Профилактика заболевания заключается в здоровом образе жизни в любом возрасте и внимательном отношении к своему состоянию в случае уже имеющихся болезней. Нередко пациенты с артериальной гипертензией не посещают кардиолога и терапевта, не контролируют уровень давления и показатели крови. Пациенты с сахарным диабетом зачастую игнорируют рекомендации эндокринолога, способствуя ухудшению своего состояния. Конечно, длительный приём препаратов и соблюдение диеты могут быть психологическим испытанием для человека, но это важный шаг к сохранению своего здоровья.
Сотрясение головного мозга - симптомы и лечение
Что такое сотрясение головного мозга? Причины возникновения, диагностику и методы лечения разберем в статье доктора Попович Анны Мироновны, невролога со стажем в 34 года.
Над статьей доктора Попович Анны Мироновны работали литературный редактор Елизавета Цыганок , научный редактор Роман Люкманов и шеф-редактор Маргарита Тихонова
Сотрясение головного мозга (Brain concussion) — это закрытая травма головы, которая проявляется головными болями, головокружением, тошнотой и рвотой.

Мозг — это главный орган нервной системы, контролирующий работу всего организма. Его защищает оболочка черепа, а также твёрдая и мягкая оболочки, между которыми находится цереброспинальная жидкость (ликвор). Она смягчает повреждение мозга при ударе головы [6] .
Несмотря на такую защиту, процент травм головного мозга остаётся достаточно высоким. Лидирующую позицию среди них занимает сотрясение [6] .
Сотрясение головного мозга не очень опасно по сравнению с другими травмами черепа, так как через 2-3 недели симптомы проходят.
Причины сотрясения мозга
Причиной такой травмы может стать падение, уличная драка, дорожно-транспортное происшествие, занятие определёнными видами спорта (боксом, хоккеем, футболом, фигурным катанием и т. д.).
Также к факторам риска можно отнести пренебрежение правилами безопасности, пожилой и детский возраст.
Симптомы сотрясения головного мозга
Ведущим симптомом сотрясения головного мозга является потеря сознания. Причём чем дольше пациент находится без сознания, тем тяжелее сотрясение. Обычно человек приходит в себя в течение 10 минут [1] .
Ещё один важный признак, который помогает определить тяжесть полученной травмы, — потеря памяти. Выделяют три вида так называемой амнезии:
- ретроградная — пострадавший не помнит, что произошло за несколько минут или месяцев до травмы;
- конградная — пострадавший не помнит часть или все события, которые происходили во время острого периода болезни;
- антероградная — после травмы пациент теряет способность запоминать события.
После лечения память восстанавливается. Сначала возвращаются самые яркие эмоциональные впечатления, со временем восстанавливаются и более мелкие детали. Время и объём восстановления памяти зависит от тяжести травмы, а также от некоторых других факторов, например от состояния памяти до травмы [3] .
После того как пациент приходит в себя, появляются следующие симптомы:
- давящие боли в голове;
- головокружение, которое усиливается при смене положения тела;
- спутанность сознания, снижение внимания, растерянность, быстрая смена настроения (может возникнуть позже), иногда дезориентация во времени и пространстве;
- затуманивание зрения, расплывчатость, диплопия (раздвоение предметов); (ритмичные движения глаз);
- звон в ушах;
- невнятная речь;
- заторможенность действий;
- тошнота, рвота;
- фото- и фонофобия (повышенная свето- и звукочувствительность);
- быстрая смена цвета кожи от ярко-красного до бледного, слабость, потливость;
- колебание частоты пульса и артериального давления;
- подъём температуры до 37,5 °С [2] .

Через несколько дней после травмы или раньше возникают отложенные симптомы:
- сонливость, повышенная утомляемость;
- раздражительность, тревожность с возможным развитием эпизода депрессии (постоянная усталость, апатия и тоска) [2] ;
- плохой сон.
Симптомы могут проявляться вместе и по отдельности.
Часто клиническая картина сотрясения головного мозга зависит от возраста пострадавшего. Например, младенцы с черепно-мозговой травмой обычно не теряют сознание. В таких случаях следует обращать внимание на бледность кожи лица, заторможенность, беспокойный сон, рвоту и/или срыгивание после еды. Состояние улучшается через 2-3 дня. У детей дошкольного возраста, а также у пожилых людей симптомы смазаны, поэтому иногда потеря сознания может пройти незаметно.
Любая черепно-мозговая травма нуждается в лечении, поэтому после сотрясения, независимо от тяжести симптомов, необходимо проконсультироваться с травматологом.
Патогенез сотрясения головного мозга
В механизме развития черепно-мозговой травмы играют роль сразу несколько теорий. Например, есть теория, в которой основное значение придаётся расстройству обмена веществ, из-за чего нарушается деятельность нейрональных мембран. Это приводит к повреждению нервных волокон и в конечном итоге нарушает работу центральной нервной системы, после чего развиваются симптомы сотрясения.
Эту теорию подтвердило экспериментальное моделирование черепно-мозговой травмы у лабораторных животных.
Однако самыми распространёнными можно считать следующие: теория градиента давления и ротационная теория.
Теория градиента давления
При ударе или ушибе головы развивается деформация черепа, после чего повышается внутричерепное давление, мозг смещается и движение внутри черепа ускоряется. При этом давление повышается на стороне удара, а на противоположной, наоборот, понижается. Это приводит к тому, что в ткани мозга образуются полости и небольшие газовые пузыри.

Отрицательное давление длится тысячную долю секунды, пузыри также быстро регрессируют. Нарушенное равновесие между давлением в сосудах и в окружающей их мозговой ткани повреждает капилляры и мозговые структуры. Происходит так называемый процесс кавитации, который обуславливает появление симптомов при сотрясении головного мозга.
Эта теория является наиболее распространённой.
Ротационная теория
Получила подтверждение в эксперименте. Было установлено, что при ударе или ушибе головы одновременно в 2-3 плоскостях подвижные отделы мозга начинают вращаться, а зафиксированные стволовые отделы — перекручиваются. При этом некоторые участки мозга смещаются относительно друг друга. Всё это повреждает синапсы, нервные волокна и сосуды головного мозга, что приводит к развитию симптомов сотрясения, в том числе отложенных [8] [11] .

Классификация и стадии развития сотрясения головного мозга
Лёгкая черепно-мозговая травма делится на несколько степеней:
- лёгкая степень — протекает без потери сознания и памяти, с незначительной тошнотой, симптомы проходят в течение получаса;
- средняя степень — проявляется умеренной тошнотой, периодическими головными болями, головокружением, пошатыванием при ходьбе и фотофобией (неприятным ощущением при взгляде на яркий свет);
- тяжёлая степень — характерна утрата сознания до 10 минут, ярко выраженная потеря памяти, сильные головные боли, головокружение, фотофобия, шаткость походки, тошнота, многократная рвота и заторможенность [5] .
Осложнения сотрясения головного мозга
Все последствия черепно-мозговой травмы можно разделить на преходящие (краткосрочные) и отдалённые расстройства.
К преходящим можно отнести все симптомы, которые не прошли через месяц после получения травмы головы. Это головные боли, головокружение, пошатывание при ходьбе, слабость, утомляемость, повышенная потливость, снижение настроения или его перепады, плаксивость, раздражительность, плохой сон [10] .
К отдалённым последствиям, которые могу развиться через несколько месяцев и даже лет после перенесённой черепно-мозговой травмы, можно отнести:
- Посттравматическую эпилепсию — проявляется потерей сознания, судорогами, прикусом языка, пеной изо рта и упусканием мочи. Риск развития посттравматической эпилепсии зависит от тяжести перенесённой черепно-мозговой травмы и наличия повторных сотрясений головного мозга [13] .
- Посткоммоционный синдром — сопровождается утомляемостью, раздражительностью, головокружением, головной болью и апатией. Симптомы усиливаются на фоне психоэмоционального перенапряжения и неправильного режима дня.
- Синдром второго удара — отёк головного мозга. Появляется после повторной черепно-мозговой травмы, когда явления первой ещё не прошли. Проявляется головными болями, головокружением, нарушением речи, тошнотой и рвотой, не приносящими облегчения, снижением остроты зрения, судорогами и потерей сознания разной степени, вплоть до глубокой комы. Отёк головного мозга является неотложным состоянием и требует экстренной госпитализации.
- Синдром внутричерепной гипертензии — проявляется давящими головными болями, тошнотой и рвотой. Эти симптомы возникают ежедневно, могут по несколько раз в день. Иногда усиливаются из-за смены погоды и переутомления.
- Изменения личности — плаксивость, раздражительность, быстрая смена настроения. Обычно такие изменения замечают окружающие, но в тяжёлых случаях пациент также может обратить на это внимание.
Обычно память восстанавливается в течение нескольких недель или месяцев в зависимости от травмы. Однако в некоторых случаях проблемы с памятью остаются. Такие пациенты нуждаются в повторном лечении. В конечном счёте 80 % из них в течение полугода выходят на свой прежний уровень, остальным приходится менять вид деятельности или уменьшить количество рабочих часов [12] .
Диагностика сотрясения головного мозга
Сотрясение головного мозга диагностируют на основе жалоб и данных неврологического осмотра.
При обращении к врачу следует подробно объяснить обстоятельства травмы, механизм её получения, а также описать жалобы. Это поможет врачу быстрее поставить верный диагноз и раньше начать лечение.
В первые часы после сотрясения зрачки сильно сужаются или расширяются, также ухудшается реакция на свет. Полное отсутствие реакции говорит о тяжёлом повреждении мозга.
При осмотре зрачков обращают внимание на анизокорию (разницу в диаметре), которая также может указать на сторону поражения. Например, если повреждён левый зрачок, то нарушена работа правого полушария, и наоборот.

Дифференциальная диагностика
Дифференциальная диагностика основывается на жалобах пациента, истории болезни, данных осмотра, лабораторных и инструментальных исследований.
При сотрясении головного мозга важно исключить другие, более тяжёлые травмы черепа:

При подозрении на сотрясение головного мозга необходимо провести следующие исследования:
- общий анализ крови и мочи — проводят, если поднялась температура, чтобы исключить другие причины её возникновения;
- краниографию (рентгенографию черепа) в двух проекциях — исключает костно-травматические изменения.
Дополнительно может потребоваться:
- эхоэнцефалоскопия — позволяет заподозрить внутримозговую гематому;
- компьютерная томография (КТ) головного мозга — проводят по показаниям при тяжёлой степени сотрясения головного мозга, по её результатам исключают перелом костей черепа, внутримозговые гематомы и посттравматические кровоизлияния в головной мозг [4][9] ;
- консультация окулиста — проводит осмотр глазного дна.
При необходимости пациента консультируют другие специалисты: терапевт осматривает пострадавшего с гипертонией или ишемической болезнью сердца, хирург или травматолог — при подозрении на травму внутренних органов и переломы [5] [10] .
Лечение сотрясения головного мозга
Даже при лёгком сотрясении головного мозга необходима госпитализация в травматологическое отделение. Это позволяет повысить эффективность лечения и улучшить прогноз. Стационарное лечение длится пять суток, после чего пациент проходит амбулаторное лечение у невролога.
Немедикаментозное лечение
В стационаре пациент соблюдает постельный режим. Пострадавший может переворачиваться в постели, сидеть на кровати со свешенными ногами, совершать утренний и вечерний туалет, принимать пищу в постели, однако ему нельзя читать книги, пользоваться мобильным телефоном и компьютером, слушать громкую музыку и смотреть телевизор. Если пациент не соблюдает запрет, симптомы усиливаются и период выздоровления затягивается.
На время лечения пациенту необходимо отказаться от употребления алкоголя, кофе, крепкого чая и энергетиков. При этом в рационе обязательно должны быть гречка, фасоль, яйца, печень, т. е. продукты, содержащие витамины группы В. Также желательно заменить хлеб из муки высшего сорта на хлеб из цельнозерновой муки. Необходимо соблюдать строгий баланс между углеводами, жирами и белками. Усреднённая формула соотношения белков, жиров, углеводов выглядит так:
- белки — 15-20 %;
- жиры — 30 %;
- углеводы — 55-60 %.
Медикаментозное лечение
Лекарства, которые назначают при лечении сотрясения головного мозга, делятся на основные и дополнительные.
К основным относятся:
- обезболивающие — нестероидные противовоспалительные препараты, другие ненаркотические анальгетики;
- препараты, стимулирующие микроциркуляцию и проницаемость капилляров внутреннего уха, а также препараты, которые стабилизируют давление эндолимфы в улитке и лабиринте уха — назначают при головокружении;
- дегидратирующие препараты — против отёков, применяют в течение трёх дней.
Дополнительные:
- сосудистые и метаболические препараты — способ введения зависит от тяжести состояния пострадавшего;
- противорвотные [3][5] .
Если соблюдать все рекомендации лечащего врача, вероятность благоприятного прогноза составляет 90 % [10] . В остальных случаях сохраняются проблемы с памятью и резкая смена настроения, которые со временем также сходят на нет [10] .
Прогноз также зависит от тяжести травмы и других факторов, в том числе от длительности потери сознания.
При черепно-мозговой травме важно сразу обратиться к врачу, пройти назначенный курс лечения и в течение года наблюдаться у невролога, чтобы снизить риск возможных осложнений.
Профилактика сотрясения мозга
Чтобы предупредить сотрясение головного мозга, необходимо соблюдать следующие правила:
Читайте также:
- Влияние ацетилхолина на нервную систему. Эффекты стимуляции холинорецепторов нервной системы
- Значение фотосинтеза. Строение листа.
- Иммунная нейтропения детей и новорожденных
- Фрукты: вкус и польза. Чем полезны фрукты, и когда какие фрукты следует употреблять?
- Статьи по отравлению лекарствами от аритмии (антиаритмиками)
