Операция на бедре антикоагулянты
Ранее считалось, что ожирение, ишемическая болезнь сердца, сердечная недостаточность и хроническая венозная недостаточность повышают риски при эндопротезировании крупных суставов. Однако последние научные исследования доказали обратное. Оказывается, нет четкой взаимосвязи между частотой развития тромбозов и наличием у пациентов сопутствующей патологии.
Это значит, что тромбоэмболические осложнения возникают отнюдь не потому, что человек страдает варикозом или имеет лишний вес.
Основным фактором риска является нарушение свертываемости крови, которое возникает в ходе операции. При этом адекватная своевременная профилактика позволяет предупредить развитие тромбоэмболических осложнений (ВТЭО).
В чем опасность операции при варикозе
Операции по замене крупных суставов (коленного, тазобедренного) сопряжены с высоким риском тромбозов. По данным разных авторов, вероятность развития тромбоэмболических осложнений у разных пациентов колеблется в пределах 3,4-50%. Причем в 0,7-30% случаев тромбоз сопровождается тромбоэмболией легочной артерии (ТЭЛА), которая в 1-3% случаев приводит к летальному исходу.
Основной причиной тромбоза являются функциональные изменения в системе гемостаза, а именно — преобладание свертываемости крови над процессами фибринолиза. Гиперкоагуляция развивается в результате массивного повреждения костных и мягких тканей в ходе хирургического вмешательства. Причем у пациентов с варикозом и хронической венозной недостаточностью она более выражена, чем у мужчин и женщин без сопутствующей сосудистой патологии.
В связи с этим пациенты с варикозом и ХВН относятся к группе высокого риска тромбоэмболических осложнений. По данным некоторых авторов, вероятность возникновения тромбоза у них составляет 40-70%. Однако причиной этого являются не сами болезни, а сопутствующие изменения в системе гемостаза, которые имеются у таких пациентов.
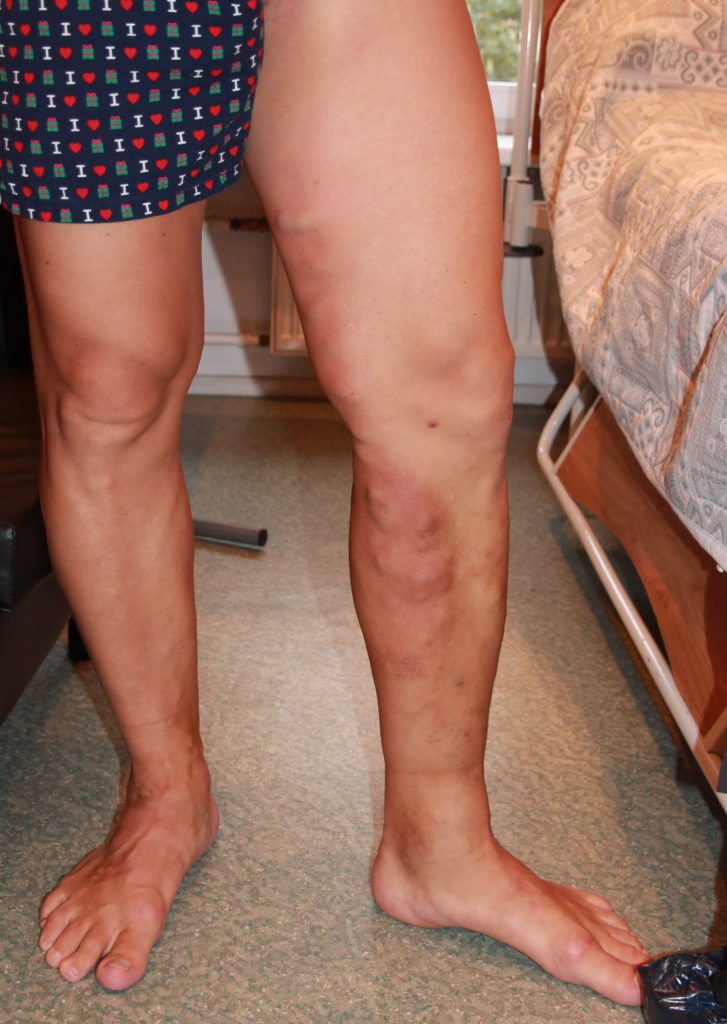
Фото ноги с тромбозом.
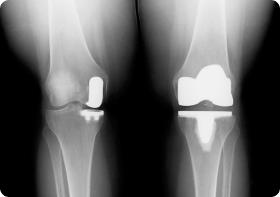
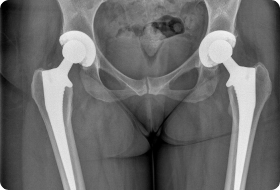
Можно ли делать эндопротезирование с варикозом
Варикоз и хроническая венозная недостаточность не являются противопоказаниями к эндопротезированию. Однако при их наличии могут возникнуть определенные сложности во время и после операции. Ведь пациенты с сосудистой патологией больше остальных рискуют получить тромбоэмболические осложнения в раннем послеоперационном периоде.
И тем не менее при варикозе и ХВН оперироваться можно. Главное — делать это в хорошей клинике, где используются адекватные алгоритмы обследования и тактики ведения данной категории пациентов.
Что делать, если отказали врачи
Перед операцией врачи обязательно обследуют каждого пациента и оценивают риски. При высокой вероятности осложнений в операции могут отказать. В таком случае следует искать клинику и специалиста, который согласится выполнить эндопротезирование. Но нужно быть готовым к тому, что перед операцией придется пройти курс лечения. А в послеоперационном периоде — курс сосудистой терапии и тромбопрофилактики по схеме высокого риска.
При индивидуальном подходе и адекватной профилактике риск тромбоэмболических осложнений будет сведен к минимуму. А послеоперационный период и восстановление пройдут максимально успешно.
Как исключить тромбоз
Чтобы провести эффективную профилактику тромбоза, врачам необходимо сначала оценить риск его развития. Как мы уже сказали, сопутствующие заболевания не являются факторами, определяющими появление осложнений. Так как же оценить возможные риски?
Большую роль в прогнозировании играют такие показатели:
- фибринолитическая активность крови;
- скорость оседания эритроцитов (СОЭ);
- количество эритроцитов в периферической крови;
- показатель гематокрита;
- этаноловый тест.
Большое значение в оценке рисков также имеет обследование ангиохирурга и ультразвуковое ангиосканирование (УЗАС) сосудов нижних конечностей. На основании результатов этих исследований можно с высокой вероятностью спрогнозировать послеоперационные осложнения еще на этапе подготовки к операции. После этого специалисты могут с большей эффективностью подобрать схему профилактики и тактику ведения больного.
Пациентам с патологией вен нижних конечностей требует особенно тщательная подготовка к эндопротезированию. Более того, в связи с высоким риском им необходим индивидуальный подход. Им подбирают оптимальную схему тромбопрофилактики (парентеральные + пероральные антикоагулянты), а также назначают курс сосудистой терапии. В некоторых случаях больным выполняют санирующую флебэктомию, что позволяет значительно снизить вероятность тромбоэмболии.
Отметим, что эндопротезирование коленных суставов сопряжено с большим риском, чем замена ТБС. И в этом случае требуются еще более тщательное планирование и подготовка.
Меры предосторожности после
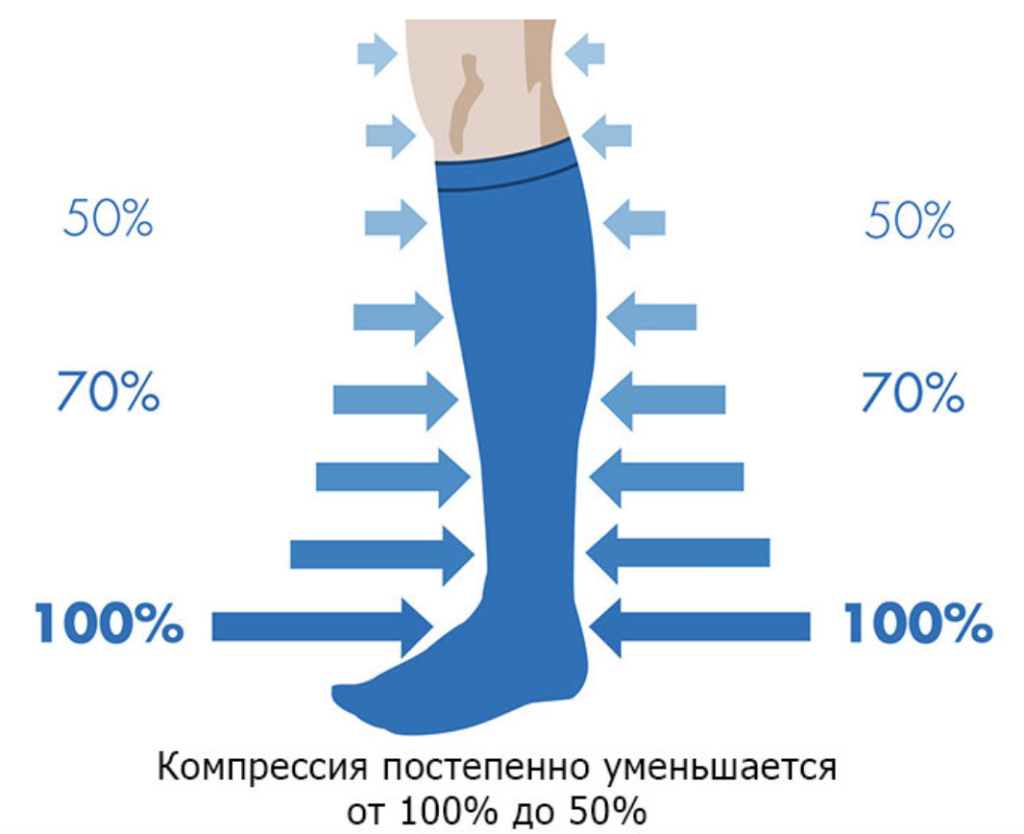
Для профилактики тромбозов крайне важно ношение компрессионного белья подходящего класса компрессии. Чулки всегда подбирает специалист, учитывая степень варикоза и стадию венозной недостаточности. Компрессионное белье требуется носить в течение как минимум 30 дней после операции.
Итоги
Наличие варикоза и ХВН не должно быть поводом для отказа от эндопротезирования. Ведь операция является единственным способом, который позволяет избавиться от хронических болей и вернуться к привычному образу жизни. Так что оперироваться в любом случае необходимо.
Но, поскольку операция может быть сопряжена с рисками, делать ее следует только в хорошей клинике. При выборе учреждения следует поинтересоваться, как там оценивают возможные риски и какие схемы профилактики используют. Очень важно, чтобы в раннем послеоперационном периоде там проводилась адекватная тромбопрофилактика.
Не менее важно и ношение подходящего компрессионного белья после хирургического вмешательства.
Эндопротезированию крупных суставов нижних конечностей в основном подвергаются люди пожилого и старческого возраста. Новые оральные антикоагулянты обладают удобным способом введения, они безопасны, эффективны и не требуют лабораторного мониторинга. В стат
Generally total hip and knee replacement are performed in elderly and very elderly patients. New oral anticoagulants have comfort level of using, a high level of safety and efficacy; laboratory monitoring is not required for these anticoagulants. The article contains an algorithm for selecting new oral anticoagulants, there are guidelines for the perioperative management of patients with atrial fibrillation and for transition between anticoagulants.
Венозный тромбоз и тромбоэмболия легочной артерии (ТЭЛА) остаются важнейшей проблемой клинической медицины и затрагивают профессиональную сферу врачей разных специальностей, начиная от гинекологии, онкологии, сердечно-сосудистой хирургии и заканчивая травматологией и ортопедией. По данным статистических отчетов Министерства здравоохранения Российской Федерации ежегодно регистрируются около 80 000 новых случаев тромбоза глубоких вен (ТГВ), легочную эмболию регистрируют ежегодно с частотой 35–40 на 100 000 человек [1].
В группу высокого риска развития венозного тромбоза, наряду с прочими категориями лиц, входят пациенты ортопедического профиля, перенесшие эндопротезирование крупных суставов нижних конечностей, у которых риск ТГВ в отсутствие медикаментозной тромбопрофилактики может достигать 60% [2]. Фатальная ТЭЛА может развиться примерно у 1 из 500 пациентов после планового эндопротезирования тазобедренного сустава (ЭТБС) [3].
Количество проводимых в РФ плановых эндопротезирований тазобедренного сустава растет с каждым годом, и в настоящее время ежегодно выполняется около 25 ЭТБС на 100 000 населения [4]. Следует отметить, что среди этих пациентов большой процент лиц пожилого и старческого возраста. Согласно Глобальному ортопедическому регистру среди пациентов, перенесших эндопротезирование крупных суставов нижних конечностей, средний возраст составляет около 70 лет [5]. На 2017 г. по данным Росстата численность населения старше трудоспособного возраста в РФ составляет 38 935 300 человек, а по среднему варианту прогноза к 2022 г. увеличится еще примерно на 2,25 млн человек. По мере увеличения средней продолжительности жизни и старения населения возрастет и потребность в эндопротезировании суставов. Так, в США c 2005 до 2030 г. прогнозируется увеличение потребности в первичном ЭТБС на 174%, а в эндопротезировании коленного сустава (ЭКС) — на 673% [6].
Таким образом, старение населения в целом, увеличение потребности в эндопротезировании крупных суставов нижних конечностей и более высокий риск ТГВ в пожилом и старческом возрасте определяют важность проблемы рационального медикаментозного сопровождения с целью тромбопрофилактики и выбора оптимального антикоагулянта, в том числе с учетом возрастных особенностей пациентов, состояния функции почек, наличия и характера коморбидных состояний и сопутствующей лекарственной терапии.
В РФ в настоящее время для профилактики венозных тромбозов и тромбоэмболий могут применяться следующие антикоагулянты:
- нефракционированный гепарин (НФГ);
- низкомолекулярные гепарины (НМГ): далтепарин натрия, надропарин кальция, эноксапарин натрия;
- фондапаринукс натрия;
- новые оральные антикоагулянты (НОАК): дабигатрана этексилат, ривароксабан, апиксабан;
- антагонисты витамика К (АВК): варфарин.
Данные лекарственные средства являются эффективными антикоагулянтами, однако обладают различной степенью безопасности.
Согласно Российским клиническим рекомендациям по диагностике, лечению и профилактике венозных тромбоэмболических осложнений (ВТЭО) 2015 г. у больных ортопедического профиля при плановом протезировании тазобедренного или коленного суставов могут использоваться практически все из перечисленных выше антикоагулянтов, за исключением варфарина, который для тромбопрофилактики после эндопротезирования крупных суставов не рекомендуется [1].
В клинической практике могут использоваться различные схемы профилактики ВТЭО. Так, НМГ назначают в профилактической дозе, рекомендуемой для больных высокого риска. Особенности применения каждого конкретного препарата изложены в рекомендациях производителя. Целесообразно введение препаратов не позже чем за 12 ч до начала вмешательства и не ранее чем через 12 ч после его завершения.
Фондапаринукс натрия вводят подкожно по 2,5 мг 1 раз в сутки. Первое введение рекомендуется через 6–24 ч после окончания операции.
Апиксабан по 2,5 мг 2 раза в сутки. Первый прием через 12–24 ч после окончания операции.
Дабигатрана этексилат назначают перорально 1 раз в сутки по 220 мг. Первый прием через 1–4 ч после окончания операции и по достижении гемостаза в половинной суточной дозе.
Ривароксабан назначают перорально по 10 мг 1 раз в сутки, первый прием через 6–10 ч после окончания операции.
НФГ характеризуется меньшей эффективностью и безопасностью и может применяться только в случаях, когда использование вышеуказанных препаратов невозможно. Обычная суточная доза НФГ составляет 15 000 ЕД за три введения, первая инъекция за 4–6 ч до или через 6–8 ч после операции. Имеются данные о большей эффективности индивидуально подобранных доз НФГ.
Начинать антикоагулянтную профилактику после операции можно не ранее, чем будет обеспечен первичный гемостаз. Решение о выборе одного из указанных вариантов профилактики ВТЭО должно основываться на планируемой продолжительности профилактики, опасности возникновения геморрагий.
По данным многочисленных исследований среди пациентов после ЭТБС или ЭКС НОАК оказались более эффективны и не хуже в плане безопасности по сравнению с эноксапарином. К тому же они не требуют титрования дозы и лабораторного контроля, как варфарин, и подкожных инъекций, как НФГ, НМГ, фондапаринукс. При длительном применении они не вызывают развития тромбоцитопении, как гепарины [7].
Ривароксабан и апиксабан являются прямыми ингибиторами фактора свертывания Xa. Ривароксабан достигает максимальной концентрации через 2–4 ч, период полувыведения: 5–9 часов у молодых, 11–13 часов у пожилых [8]. Апиксабан максимальной концентрации достигает через 3–4 ч, период полувыведения — около 12 ч [9]. Для определения противосвертывающей активности ривароксабана и апиксабана надежным способом является определение анти-Xа-активности.
Дабигатрана этексилат является пролекарством, которое после приема внутрь превращается в активную форму дабигатран — прямой ингибитор тромбина. На 80% выводится почками, средний период полувыведения после однократного приема составляет 8 ч, с увеличением его до 12–14 ч после многократного приема [10]. Для оценки уровня активности дабигатрана в настоящее время стандартизированный тест отсутствует, но активированное частичное тромбопластиновое время более чувствительно, чем протромбиновое время [10].
Лица пожилого и старческого возраста в большинстве случаев могут иметь различные сопутствующие заболевания, такие как артериальная гипертензия, сахарный диабет, хроническая болезнь почек, фибрилляция предсердий (ФП) или другие, по поводу которых назначена лекарственная терапия. В анамнезе у них может быть недавно перенесенный инсульт головного мозга или инфаркт миокарда. Таким пациентам требуется персонализированный подход в подборе НОАК и их дозировании. Учитывая разнообразные факторы, К. Руффом из Гарвардской школы медицины был предложен алгоритм выбора НОАК для тромбопрофилактики (рис.) [12].
У пациентов с ишемической болезнью сердца или инфарктом миокарда в анамнезе предпочтительнее назначать ривароксабан, так как дабигатрана этексилат, по данным метаанализа, может быть связан с небольшим увеличением риска развития острого коронарного синдрома и инфаркта миокарда [13].
Начиная с 30-летнего возраста каждые 10 лет скорость клубочковой фильтрации в среднем снижается на 10 мл/мин [14]. По данным III Национальной программы проверки здоровья и питания в США (III NHANES) у пожилых людей распространенность хронической болезни почек намного выше, чем у лиц более молодого возраста: 39,4% (≥ 60 лет) по сравнению с 12,6% (40–59 лет) и 8,5% (20–39 лет) [15]. В связи с тем что повышение экспозиции лекарственных средств у пациентов пожилого возраста и у пациентов с сахарным диабетом часто обусловлено снижением функции почек, перед назначением антикоагулянтов требуется оценивать ренальную функцию.
НОАК в разной степени выводятся из организма с помощью почек (дабигатрана этексилат на 80%, ривароксабан на 36%, апиксабан на 27%), поэтому функциональное состояние почек имеет определяющее значение для концентрации антикоагулянтов в крови. При умеренном нарушении функции почек (клиренс креатинина 30–50 мл/мин) препаратом выбора должен быть апиксабан в силу его более хорошего профиля безопасности; ривароксабан можно использовать с осторожностью; назначая дабигатрана этексилат, требуется уменьшить дозу до 150 мг 1 раз/сут (2 капсулы по 75 мг).
Важное значение в клинической практике имеют вопросы лекарственных взаимодействий НОАК с препаратами, которые пациенты принимают по поводу прочих сопутствующих заболеваний, что во многом определяется тем, что НОАК метаболизируются с участием различных ферментов, на активность которых могут оказывать влияние принимаемые одновременно лекарственные средства. Так, все НОАК являются субстратами P-гликопротеина (P-gp), мембранного белка, локализующегося в тонком кишечнике, гематоэнцефалическом барьере, печени и почках. Данный белок транспортирует из клеток различные вещества, в том числе лекарственные средства и их метаболиты [17]. Ривароксабан на 18% метаболизируется с помощью CYP3A4 и на 14% — с помощью CYP2J2 [8]. Апиксабан на 25% метаболизируется с помощью CYP3A4. Дабигатрана этексилат не является субстратом для CYP3A4 [17].
Соответственно, лекарственные средства, которые индуцируют P-gp и/или CYP3A4, могут снижать концентрацию НОАК в плазме крови, повышая риск развития тромбоэмболических осложнений, в то время как ингибиторы P-gp и/или CYP3A4 могут увеличивать концентрацию НОАК, тем самым повышая риск развития кровотечения. С учетом этого рекомендуется избегать совместного применения НОАК с ЛС, являющимися ингибиторами или индукторами P-gp и/или CYP3A4. В табл. 2 представлена информация о влиянии сопутствующих лекарственных средств на экспозицию НОАК.
В среднем продолжительность госпитального этапа послеоперационного периода у пациентов, перенесших эндопротезирование крупных суставов нижних конечностей, составляет около 7 дней. Далее пациент переводится на амбулаторный этап. Участковому терапевту необходимо помнить о том, что такие пациенты должны продолжать медикаментозную тромбопрофилактику с учетом международных рекомендаций: для ЭТБС продолжительность медикаментозной тромбопрофилактики составляет 35 дней, а для ЭКС — 14 дней [18].
Зачастую в многопрофильных стационарах закупка лекарственных средств (ЛС) осуществляется централизованно и в рамках экономической целесообразности может быть не учтено удобство применения НОАК, в связи с чем НМГ используются как в отделении реанимации и интенсивной терапии, так и в хирургических отделениях стационара. В последующем на амбулаторном этапе послеоперационного периода у поликлинического терапевта может возникнуть необходимость в переводе пациента с парентерального антикоагулянта на НОАК, чтобы повысить приверженность к медикаментозной тромбопрофилактике. При переходе с парентерального антикоагулянта на новый оральный применение НОАК следует начать за 0–2 часа перед очередным введением исходного антикоагулянта, который в последующем отменяется [17].
Нами был проведен ретроспективный анализ историй болезней пациентов (n = 111) травматолого-ортопедического отделения № 1 УКБ № 1 Первого МГМУ им. И. М. Сеченова, перенесших ЭКС (n = 63; 56,8%) или ЭТС (n = 48; 43,2%) за период май–июль 2016 г., с анализом структуры назначения антикоагулянтов, режима дозирования, соответствия инструкциям по применению ЛС и клиническим рекомендациям по профилактике венозных тромбоэмболических осложнений, наличия межлекарственных взаимодействий, потенциально неблагоприятных в плане развития кровотечений, а также с расчетом стоимости курсов антикоагулянтной терапии.
Результаты показали, что среди пациентов преобладали лица старших возрастных групп, средний возраст которых составил 65 ± 9,2 года. Из антикоагулянтов в послеоперационном периоде с целью тромбопрофилактики по частоте назначения преобладал дабигатрана этексилат, который получали 90 пациентов (81,1%) в суточной дозе 220 мг (79,3% — 110 мг 2 раза/сут, 1,8% — 220 мг 1 раз/сут), ривароксабан принимали 11 пациентов (9,9%) в дозе 10 мг 1 раз/сут, эноксапарин натрия — 10 пациентов (8,1% — 0,4 мл п/к 1 раз/сут, 0,9% — 0,2 мл п/к 1 раз/сут). У 14 пациентов (12,6%) с нарушением функции почек (КК = 30–50 мл/мин) дозы НОАК были уменьшены в соответствии с инструкцией. Анализ межлекарственных взаимодействий показал, что наиболее часто встречались комбинации дабигатрана этексилат + кетопрофен (n = 81; 73%), ривароксабан + кетопрофен (n = 11; 9,9%) и эноксапарин натрия + кетопрофен (n = 11; 9,9%), повышающие потенциальный риск развития кровотечения.
Фармакоэкономический анализ показал, что суммарные расходы на тромбопрофилактику у пациентов после ЭТС в случае применения дабигатрана этексилата составляют 2816,0 руб., ривароксабана — 3010,0 руб. и эноксапарина натрия — 8209,5 руб. После ЭКС общие затраты на тромбопрофилактику в случае применения дабигатрана этексилата составляют 894,0 руб., ривароксабана — 1204,0 руб. и эноксапарина натрия — 8209,5 руб. Это свидетельствует о том, что оральные антикоагулянты, назначаемые с целью тромбопрофилактики у пациентов после ЭТС или ЭКС, имеют экономические преимущества по сравнению с эноксапарином натрия.
Таким образом, при назначении новых оральных антикоагулянтов с целью тромбопрофилактики у пациентов после эндопротезирования крупных суставов нижних конечностей врачам необходимо учитывать, что в основном это пожилые пациенты, которые могут иметь различные коморбидные состояния и нарушения функционального состояния почек, по поводу которых получают лекарственную терапию. Необходимо избегать клинически значимых лекарственных взаимодействий, которые могут повлиять на эффективность или безопасность медикаментозной тромбопрофилактики. Также требуется соблюдать продолжительность курса тромбопрофилактики, поскольку раннее прекращение приема антикоагулянтов может привести к развитию тромбоза глубоких вен с последующими более серьезными осложнениями.
Литература
Т. Е. Морозова 1 , доктор медицинских наук, профессор
Р. М. Миннигулов
И. Ю. Юдина, кандидат медицинских наук
ФГБОУ ВО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Аннотация научной статьи по клинической медицине, автор научной работы — Божкова Светлана Анатольевна
Проблема развития венозных тромбозов и эмболии (ВТЭ) до настоящего времени остается серьезной проблемой в области травматологии и ортопедии. Для сохранения равновесия между эффективностью тромбопрофилактики и риском серьезных кровотечений у особых групп пациентов предлагается проводить выбор конкретного антикоагулянта на индивидуальной основе с учетом массы тела пациента, функции его печени и почек, длительности курса профилактики, возможность проведения лабораторного мониторирования показателей свертываемости крови после выписки из стационара. Анализируется возможность использования новых пероральных антикоагулянтов у пациентов после эндопротезирования тазобедренного или коленного сустава.
Похожие темы научных работ по клинической медицине , автор научной работы — Божкова Светлана Анатольевна
Specificity of anticoagulant choice for VTE prophylaxes after major orthopedic surgery - the view of clinical pharmacologists
The issue of development of venous thrombosis and embolism still remains a serious problem in the traumatology and orthopedics. To maintain a balance between efficacy of thromboprophylaxis and the risk of serious bleeding in special patient groups the authors encourage to undertake the choice of anticoagulant on an individual basis taking into account the patient's weight, as his liver and kidneys, the duration of prophylaxis course, the possibility of laboratory monitoring of coagulation parameters after discharge from hospital. The authors analyze the possibility of the use of new oral anticoagulants in patients after hip or knee arthroplasty.
ОСОБЕННОСТИ ВЫБОРА АНТИКОАГУЛЯНТОВ ДЛЯ ПРОФИЛАКТИКИ ВЕНОЗНЫХ ТРОМБОЗОВ И ЭМБОЛИЙ ПОСЛЕ КРУПНЫХ ОРТОПЕДИЧЕСКИХ ОПЕРАЦИЙ: ВЗГЛЯД КЛИНИЧЕСКОГО ФАРМАКОЛОГА
Проблема развития венозных тромбозов и эмболий (ВТЭ) до настоящего времени остается серьезной проблемой в области травматологии и ортопедии. Для сохранения равновесия между эффективностью тромбопрофилактики и риском серьезных кровотечений у особых групп пациентов предлагается проводить выбор конкретного антикоагулянта на индивидуальной основе с учетом массы тела пациента, функции его печени и почек, длительности курса профилактики, возможность проведения лабораторного мониторирования показателей свертываемости крови после выписки из стационара. Анализируется возможность использования новых пероральных антикоагулянтов у пациентов после эндопроте-зирования тазобедренного или коленного сустава.
Ключевые слова: тромбоэмболические осложнения, тромбопрофилактика, парентеральные антикоагулянты, перо-ральные антикоагулянты.
SPECIFICITY OF ANTICOAGULANT CHOICE FOR VTE PROPHYLAXES AFTER MAJOR ORTHOPEDIC SURGERY- THE VIEW OF CLINICAL PHARMACOLOGISTS
The issue of development of venous thrombosis and embolism still remains a serious problem in the traumatology and orthopedics. To maintain a balance between efficacy of thromboprophylaxis and the risk of serious bleeding in special patient groups the authors encourage to undertake the choice of anticoagulant on an individual basis taking into account the patient's weight, as his liver and kidneys, the duration of prophylaxis course, the possibility of laboratory monitoring of coagulation parameters after discharge from hospital. The authors analyze the possibility of the use of new oral anticoagulants in patients after hip or knee arthroplasty.
Keywords: thromboembolic complications, thromboprophylaxis, parenteral anticoagulants, oral anticoagulants.
Проблема развития венозных тромбозов и эмболий (ВТЭ) до настоящего времени остается серьезной проблемой в области травматологии и ортопедии, несмотря на существующие стандарты и рекомендации. Впервые использование тромбопрофилактики было рекомендовано для пациентов травматолого-ортопедического профиля в 1986 году [13]. В многочисленных зарубежных клинических исследованиях убедительно показано, что первичная рутинная профилактика развития венозных тромбозов и эмболий (ВТЭ) высокоэффективна и позволяет существенно снизить частоту тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА) [6, 12]. В таблице 1 представлены данные об эффективности проведения тромбопрофилактики низкомолеку-
лярными гепаринами при некоторых травмах и крупных ортопедических вмешательствах. Большие ортопедические операции - эндопро-тезирование коленного или тазобедренного сустава - относят к оперативным вмешательствам высокого риска развития ВТЭ, после которых без назначения антикоагулянтной профилактики тромбоэмболические осложнения (ТЭО) могут развиваться в 42-57% и 41-87% случаев соответственно. При этом использование антикоагулянтов приводит к снижению частоты данных осложнений в десятки раз [6, 14, 18]. У пациентов с дополнительными факторами риска развития ВТЭ тромбозы глубоких вен могут осложнять послеоперационный период даже при таком малоинвазивном вмешательстве, как артроскопия коленного сустава [3, 19].
Частота развития ВТЭ в зависимости от проведения тромбопрофилактики низкомолекулярными гепаринами (НМГ), %
Операция/ травма Без НМГ С НМГ Исследование
ЭПТБС 42-57 1,3-1,7 Оее^в ШИ. е1 а!, 2004; Батата С.М. е1 а1, 2007; Шагшюк й. е1 а1, 2007
Изолированные переломы костей голени (гипс) 4-17 0-5 КфШ Р. е1 а1, 1993; Коек И.и. е1 а1, 1995
Изолированные переломы костей голени (операция) 2 1 Бе!Ьу Я. е1 а1., 2007
Артроскопия КС 3,2-4,1 0,85-0,9 ШПЬ Т. е1 а1., 2001; Сатрогеве О. е1 а. 2008
Однако до настоящего времени любого травматолога-ортопеда при выборе антикоагулянта для тромбопрофилактики волнует проблема равновесия между тем, чтобы максимально снизить риск развития тромбоза глубоких вен (ТГВ) и при этом не увеличить риск развития тяжелых кровотечений. В настоящее время в Российской Федерации зарегистрированы и могут использоваться к клинической практике для профилактики ВТЭ после больших ортопедических операций следующие антикоагулянты:
• нефракционированный гепарин (НФГ),
• низкомолекулярные гепарины (НМГ): дальтепарин, надропарин, эноксапарин,
• дабигатрана этексилат (дабигатран),
• антагонисты витамина К (варфарин) в РФ у пациентов травматолого-ортопедическо-го профиля применяют для продления курса тромбопрофилактики после парентеральных антикоагулянтов [1], доза подбирается индивидуально каждому пациенту под контролем уровня МНО.
Все эти лекарственные препараты являются высокоэффективными антикоагулянтами, однако именно это их свойство и может приводить к развитию нежелательных эффектов при их применении, которые крайне опасны в послеопера-
ционном периоде - больших кровотечений.
Цель данной статьи - ознакомить травматологов-ортопедов с принципами выбора антикоагулянта и дозами для профилактики ВТЭ в зависимости от особенностей пациента и фар-макокинетики препаратов.
Выбор времени начала тромбопрофилактики
При назначении профилактического курса антикоагулянтов врач должен определиться со сроком начала профилактики. В настоящее время, согласно российским и американским рекомендациям [2, 7], существуют несколько вариантов старта тромбопрофилактики:
- первое введение НМГ за 12 часов до начала операции;
- первое введение НМГ в половинной дозе за 2 часа до начала операции;
- первое введение НФГ, НМГ, фондапари-нукса, дабигатрана, ривароксабана после окончания операции.
Результаты исследований показывают, что не получено достоверной разницы в эффективности и безопасности тромбопрофилактики в зависимости от времени старта антикоагулянта. Как видно из таблицы 2, при введении первой дозы за 12 часов до операции не выявлено достоверных различий в частоте развития ТЭО и больших кровотечений. Большая величина интраоперационных кровопотерь отмечается при введении НМГ за 2 часа до начала операции [17]. Вышедшие в 2010 году рекомендации Британского национального института повышения качества медицинской помощи [8] предлагают начинать курс антикоагулянтов только после операции, при этом время начала зависит от используемого препарата.
Эффективности и безопасность тромбопрофилактики в зависимости от времени
первого введения НМГ [17]
Частота, % Старт до операции за 12 часов Старт после операции
Тромбоз глубоких вен 14,4 19,2
Серьезные 2,5 1,4
Как видно из таблицы 3, большинство антикоагулянтов можно назначать только через 6 и более часов после окончания операции. Исключением является дабигатран, который можно принимать уже через 1-4 часа после хирургического вмешательства.
Рекомендуемое время введения первой дозы антикоагулянтов в послеоперационном периоде
Антикоагулянты Сроки введения препаратов после операции
Фондапаринукс 6 часов
Ривароксабан 6-10 часов
Дабигатран 1-4 часа
Зависимость дозы антикоагулянта от массы тела пациента
В Российских клинических рекомендациях по диагностике, лечению и профилактике венозных ТЭО [2] и в инструкциях по применению препаратов имеются указания на необходимость учета массы тела пациентов при назначении антикоагулянтов. Особенности выбора дозы препаратов представлены в таблице 4.
Таблица 4 Зависимость дозы антикоагулянтов от массы тела пациента
Международное непатентованное наименование Масса тела пациента
менее 50 кг 120 кг и более
Надропарин Всегда рассчитывается на кг массы тела
Дальтепарин Снижение1дозы на 50% Увеличение1 дозы на 25%
Фондапаринукс Не требует коррекции1,2 . У пациентов с массой тела менее 50 кг имеется риск развития кровотечения2
Дабигатрана этексилат Не требует коррекции2
Ривароксабан Не требует коррекции2
1 - Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэм-болических осложнений [2];
2 - инструкция по медицинскому применению препарата.
Применение НМГ и фондапаринукса у особых групп пациентов
В рекомендациях АССР 2008 года [7] существует специальный раздел, в котором оговариваются отдельные группы пациентов, требующие нестандартного подхода. С самым высоким уровнем доказательности (1А) рекомендовано учитывать функцию почек при назначении и выбора дозы НМГ, фондапаринукса и других антитромбических препаратов, которые
выводятся почками у пациентов следующих категорий:
• пожилого возраста (старше 75 лет);
• с сахарным диабетом;
• с высоким риском кровотечений.
Для данных категорий пациентов рекомендовано применение (1В) одного из следующих вариантов:
• избегать применения антикоагулянтов, кумулирующих при почечной недостаточности;
• использовать сниженные дозы антикоагулянтов;
• проводить мониторинг антикоагулянт-ной активности.
В настоящее время в РФ только некоторые клиники могут проводить мониторинг антико-агулянтной активности большинства современных антикоагулянтов, например, определять активность фактора Ха для оценки эффекта НМГ, фондапаринукса. При этом, например, при проведении эндопротезирования тазобедренного или коленного сустава врач обязан проводить антикоагулянтную профилактику ТЭО [1]. Таким образом, остается третий вариант - корректировать дозы антикоагулянтов
Таблица 5 Зависимость дозы антикоагулянтов от массы тела пациента
Международное непатентованное название Путь выведения
Надропарин в основном почками
Дальтепарин в основном почками
Эноксапарин около 40% почками
Фондапаринукс 64-77% почками
Как видно из таблицы 5, все указанные препараты в той или иной степени выводятся почками. В настоящее время появились данные о различной степени кумулирования низкомолекулярных гепаринов. В обзоре литературы Р. 8еЬш1ёа с соавторами показано, что дальте-парин возможно применять в течение 10 суток в профилактических дозах у пациентов даже с выраженной ХПН (клиренс креатинина 75 лет), у которых, как правило, существенно снижена выделительная функция почек, рекомендуют для проведения профилактики ВТЭ
низкомолекулярными гепаринами выбирать дальтепарин или использовать сниженные дозы эноксапарина [16].
При назначении фондапаринукса пациентам с умеренной ХПН коррекции дозы не требуется, при выраженной ХПН (20 мл/мин Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
В виду имеющихся особенностей дизайна каждого из исследований, пациенты со сниженной фильтрационной функцией почек и больные старческого возраста были из них исключены. Таким образом, общие выводы, сделанные исходя из результатов этих исследований, имеют отношение к популяции пациентов, отобранной согласно жестким критериям включения, и надо осторожно экстраполировать полученные результаты на популяцию в целом.
В настоящее время опубликованы результаты исследования эффективности и безопасности дабигатрана у пациентов старше 75 лет [4] и у пациентов с хронической почечной недостаточности (ХПН) [5]. При назначении дабигатрана в дозе 150 мг один раз в сутки после эндопротезирования ТБС или КС в группе пациентов старше 75 лет была показана сходная эффективность по сравнению с эноксапарином при меньшей частоте тяжелых кровотечений (рис. 1). В группе пациентов со среднетяжелой почечной недостаточностью (рис. 2) дабигатран продемонстрировал эффективность, сопоставимую с энокса-парином при значительно более низкой частоте развития серьёзных кровотечений (Р 75 лет) или при наличии умеренной степени почечной недостаточности.
Публикаций с аналогичными исследованиями по ривароксабану найти не удалось. В инструкции к препарату есть указания о том, что коррекции дозы при легкой и умеренной ХПН не требуется, необходимо соблюдать осторожность при среднетяжелой почечной недостаточности (30 > клиренс креатинина > 15 мл/ мин). Кроме того, в связи с тем, что риварокса-бан метаболизируется в основном в печени посредством изоферментов системы цитохромов, его рекомендуется применять с осторожностью при умеренной почечной недостаточности (50 > клиренс креатинина > 30 мл/мин) у пациентов, получающих одновременно препараты, повышающие концентрацию ривароксабана в плазме крови (эритромицин, кларитромицин). Назначение данного антикоагулянта противопоказано при заболеваниях печени, протекающих с коагулопатией, обуславливающей клинически значимый риск кровотечений, а также пациентам, получающих системное лечение противогрибковыми препаратами азоловой группы (кетоконазол) или ингибиторами про-теазы ВИЧ (ритонавир).
Дабигатрана этексилат не метаболизируется с участием системы цитохрома, в связи с чем не отмечается значимого межлекарственного взаимодействия при совместном приеме с дру-
гими препаратами. Рекомендуется соблюдать осторожность во время назначения дабигатрана с активными ингибиторами Р-гликопротеина (транспортного белка): верапамил, кларитро-мицин. Этот эффект может быть снижен при назначении дабигатрана как минимум за два часа до приема указанных лекарственных препаратов. Кроме того, при совместном применении дабигатрана и амиодарона необходимо использовать специальную дозу антикоагулянта - 150 мг в сутки. Одновременный прием дабигатрана с хинидином противопоказан.
Таким образом, несмотря на стандартизированные подходы к профилактике тромбоэмбо-лических осложнений, хирурги, выполняющие ортопедические операции, ежедневно должны выбирать конкретный метод профилактики на индивидуальной основе, сопоставляя риск развития венозных тромбозов и эмболий с риском тяжелых кровотечений. Как правило, при этом необходимо учитывать массу тела пациента, функцию его печени и почек, длительность курса профилактики, возможность проведения лабораторного мониторирования показателей свертываемости крови после выписки из стационара. Поскольку дабигатрана этексилат и ривароксабан по эффективности сопоставимы с низкомолекулярными гепаринами, по удобству применения превосходят все парентеральные антикоагулянты, а по безопасности - варфарин, особенно при лечении пациентов на амбулаторном этапе, то новые антикоагулянты представляют собой заманчивую альтернативу для использования у пациентов, перенесших эндо-протезирование коленного или тазобедренного сустава.
10 9 8 7 6 5 4 3 2 1 0
P Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
— 2004. — Vol. 126. — Р. 338 — 400.
7. Geerts, W.H. Prevention of venous thromboembolism: Evidence-Based Clinical Practice Guidelines (8th ed.) / W.H. Geerts [et al.] // Chest. — 2008. — Vol. 133. — Р. 381—453.
8. Hill, J. Reducing the risk of venous thromboembolism in patients admitted to hospital: summary of the NICE guideline / J. Hill, T. Treasure // Heart. 2010. — Vol. 96, N 11. — P. 879 — 882.
9. Huisman, M.V. Enoxaparin versus dabigatran or rivaroxaban for thromboprophylaxis after hip or knee arthroplasty results of separate pooled analyses of phase III multicenter randomized trials / M.V. Huisman, D. J. Quinlan, O. E. Dahl, S. Schulman // Cardiovasc. Qual. Outcomes. — 2010. — Vol. 3, N 6. — P. 652 — 660.
10. Kujath, P. Incidence and prophylaxis of deep venous
thrombosis in outpatients with injury of the lower limb/ P. Kujath, U. Spannagel, W. Habscheid // Haemostasis.
- 1993. - Vol. 23, Suppl. 1. - P. 20-26.
11. Kock, H.J. Thromboprophylaxis with low-molecular-weight heparin in outpatients with plaster-cast immobilisation of the leg / H.J. Kock [et al.] // Lancet.
- 1995. - N 346. - P.459-461
12. Koch, A. Low molecular weight heparin and unfractionated heparin in thrombosis prophylaxis: meta-analysis based on original patient data / A. Koch, S. Ziegler, H. Breitschwerdt, N. Victor // Thromb. Res.
- 2001. - Vol. 102. - P. 295 -309.
13. Nurmohamed, M.T. Low-molecular-weight heparin versus standard heparin in general and orthopaedic surgery: a meta-analysis / M.T. Nurmohamed [et al.] // Lancet. - 1992. - Vol. 340. - P. 152-156.
14. Samama, C.M. Epidemiology of venous thromboembolism after lower limb arthroplasty: the FOTO study / C.M. Samama [et al.] // J. Thromb. Haemost. 2007. - Vol. 5, N 12. - P.2360 -2367.
15. Selby, R. A prospective cohort study of the epidemiology of symptomatic thromboembolism (VTE) after isolated leg fractures distal to the knee without thromboprophylaxis / R. Selby [et al.] // Blood. -2005. - Vol. 106. - P. 583.
16. Schmida, P. Low-molecular-weight heparin in patients with renal insufficiency / P. Schmida, A. G. Fischerb, W. A. Wuillemina // Swiss. Med. Weekly. - 2009. -Vol. 139, N 31-32. - P. 438-452.
17. Strebel, N. Preoperative or postoperative start of prophylaxis for venous thromboembolism with low-molecular-weight heparin in elective hip surgery? / N. Strebel [et al.] // Arch. Intern. Med. - 2002. - Vol. 162. - P.1451-1456.
18. Warwick, D. Insufficient duration of venous thromboembolism prophylaxis after total hip or knee replacement when compared with the time course of thromboembolic events: findings from the Global Orthopaedic Registry / D. Warwick [et al.] / J. Bone Joint. Surg. - 2007. - Vol. 89-B. - P. 799 -807.
19. Wirth, T. Prevention of venous thromboembolism after knee arthroscopy with low-molecular weight heparin (reviparin): results of a randomized controlled trial / T. Wirth [et al.] // Arthroscopy. - 2001. - Vol. 17. - P. 393-399.
Читайте также:


