Выращивание хрящей тазобедренного сустава

Тазобедренный сустав, как наиболее сложно устроенный подвижный костный участок организма, ежедневно претерпевает большое количество нагрузок. Чтобы опорно-двигательная система функционировала исправно, костная бедренная область устлана хрящевой тканью. Она обеспечивает амортизацию тазобедренному сочленению, защищая костный участок от повреждений.
Тем не менее, тазобедренный хрящ, как и любая область тела, на которую ежедневно влияют внешние факторы, способен изнашиваться. Повреждения хрящевой ткани могут быть вызваны механически или определенными болезнями, такими как коксартроз.

В результате, поврежденные хрящи делают костную ткань тазобедренного сустава уязвимой и более восприимчивой к внешним воздействиям. При этом в упомянутой области возникают боли, деформации, а ее движения ограничиваются. Как следствие, повреждения хрящевой ткани неизбежно ведут к эндопротезированию – операции по замене тазобедренного сустава имплантатом.
Однако современная медицина шагнула далеко вперед, и сегодня пациенты, страдающие от болезней хрящей, могут выбрать инновационный метод операции — трансплантацию хрящевой ткани тазобедренного сустава. Такая технология предполагает выращивание необходимого количества хрящевой массы из небольшой части здоровой ткани.
Эффективность
Трансплантация хрящевой ткани тазобедренного сустава способна устранить болевые ощущения, присутствующие в организме пациента, полностью или практически полностью (в зависимости от стадии повреждения тканей). К тому же, такое оперативное вмешательство может значительно оттянуть сроки установки эндопротеза, вернув пациента к привычному для него образу жизни и улучшив двигательную активность организма. Эффективность метода трансплантации хрящевой ткани тазобедренного сустава научно проверена и доказана. Оперативное вмешательство позволяет добиться таких результатов:
Еще одним преимуществом трансплантации бедренного хряща является практически полная неинвазивность хирургического вмешательства, что позволяет организму быстрее регенерировать.
Кому показана операция
Важным моментом при назначении лечащим врачом операции по хрящевой трансплантации бедренной области является возраст больного. Так, хирургическое вмешательство можно проводить у больных, достигших возраста 15 лет. Крайний порог для проведения трансплантации – 55 лет.
Однако специалист может назначать процедуру и в более раннем, а также, позднем возрасте пациентов. Решающую роль при назначении играет физическое состояние организма больного.
Трансплантацию тазобедренной зоны назначают только в том случае, если:
- Дефекты хрящевой ткани составляют не менее 2,5-10 квадратных сантиметров в диаметре;
- Диагностировано ненормальное смещение физиологических осей сустава;
- Связки и мышечные ткани бедренной области не имеют повреждений.
Как происходит

Прежде, чем назначить соответствующую операцию, лечащий врач должен провести полную диагностику организма при помощи таких действенных методик, как рентгенография, магнитно-резонансная терапия и ультразвук. Определившись, что в конкретном случае операция по трансплантации хрящевой ткани необходима, проводится практически неинвазивная хирургическая процедура по изъятию здорового хрящевого участка, на который не оказывалось серьезное внешнее воздействие.
Помимо хрящевой ткани, у пациента необходимо произвести забор крови в небольших количествах. При помощи крови в дальнейшем будет обеспечена выработка сыворотки – так хрящевая ткань сможет разрастаться в привычных условиях. После забора образцов ткани пациенту показано двухдневное пребывание в больнице. При этом нагрузки на прооперированную ногу должны быть минимальными.

Новые хрящевые клетки выращиваются в лабораторных условиях, такой процесс происходит в разы быстрее, нежели в человеческом организме. Поле того, как достаточное количество хрящевой ткани будет произведено, ее замораживают и транспортируют в больницу, где будет проходить второй этап хирургического вмешательства. Зачастую, временной отрезок между забором образцов и трансплантацией составляет не более 8 недель.
Спустя 2 суток после операции, пациента выписывают из больницы. В течение 6 недель прооперированный сустав не должен подвергаться нагрузкам, чтобы обеспечить хрящевым клеткам возможность быстро разрастаться. Уже спустя 12 месяцев после проведения трансплантации, имплантированную хрящевую ткань невозможно будет отличить от природной структуры, а пациент вернется к привычному для него образу жизни.
2017. Шведские ученые научились распечатывать биосовместимые хрящи
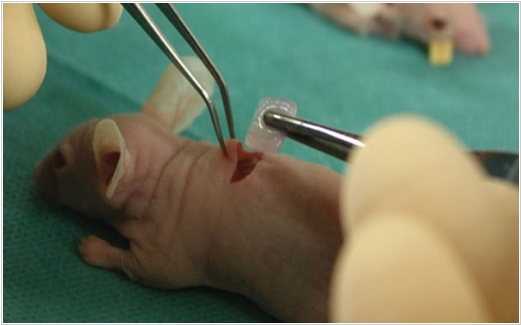
На сегодняшний день, чтобы восстановить поврежденный нос, ухо или хрящ сустава, пациенту имплантируют силиконовые протезы, что часто вызывает иммунные реакции и болевые ощущения. А что если создать гель из собственных хрящевых клеток пациента и распечатывать из него живые хрящи на 3D-биопринтере? Так и поступили шведские ученые из Сальгренской Академии. Распечатанные хрящи они имплантировали в мышку и через некоторое время в них проросли кровеносные сосуды, а хрящевые клетки стали размножаться и занимать больше объема распечатанной структуры.
2016. Новый искусственный хрящ самостоятельно борется с артритом

Обычно врачи не делают операции по замене тазобедренного сустава пациентам моложе пятидесяти, потому что искусственные суставы, как правило, служат меньше двадцати лет. Повторная операция, в ходе которой доктора удаляют износившийся эндопротез, увеличивает риск проникновения инфекции и может привести к артриту разрушению кости. Учёные из университета Вашингтона в Сент-Луисе вырастили из стволовых клеток суставной хрящ и с помощью генной инженерии заставили его вырабатывать противовоспалительные вещества. Исследователи полагают, что хрящ из живой ткани можно будет использовать для поверхностного эндопротезирования - операции, в ходе которой протезом заменяют только поверхность головки тазобедренного сустава. Если всё пройдёт хорошо, через три-пять лет начнутся клинические испытания этих био-протезов на людях.
2016. В США создали технологию выращивания человеческих костей и мышц
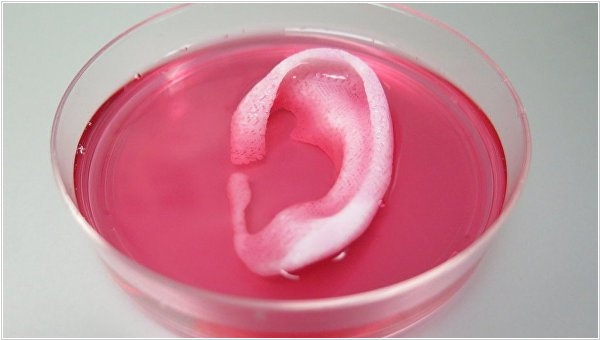
Биоинженеры из Института регенеративной медицины в Уэйк-Форесте (США) разработали необычную технологию трехмерной печати, которая позволяет создавать полноценные копии отдельных костей, мышц и хрящей из стволовых клеток. До сих пор ученым удавалось распечатывать только очень тонкие слои живой ткани (до 200 мкм) - иначе ткань начинала гибнуть, так как питательные вещества и кислород не могут проникнуть на такую глубину без наличия кровеносных сосудов. В данном случае биоинженеры использовали особый полимер, позволявший укладывать клетки слоями и при этом сохранять небольшой просвет между ними. А после печати, ученые помещают органоид в организм мыши, где он постепенно "зарастает" кровеносными сосудами, а полимер постепенно разлагается, уступая им место. В конечном итоге на месте заготовки возникает полноценный орган, обладающий нужной трехмерной формой и всеми необходимыми видами ткани.
2014. Врачи научились распечатывать мениск коленного сустава на 3D-принтере

В коленном суставе находится два хрящевых образования – мениски, которые служат для амортизации при движении и защиты суставного хряща. Колени испытывают огромную нагрузку в течение всей жизни, и именно мениски чаще всего травмируются. На сегодняшний день поломанный мениск просто удаляют, чтобы убрать боль. Однако, это снижает качество жизни человека и значительно увеличивает последующий риск развития остеоартрита. Американские врачи из медицинского центра Колумбийского университет научились распечатывать мениск на 3D-биопринтере. Причем, материал, из которого они печатают - это не просто мертвый пластик. Он содержит живые протеины, которые позволят имплантанту притягивать стволовые клетки организма для дальнейшего развития сустава.
2013. Ручка-биопринтер позволяет хирургу печатать ткани прямо во время операции
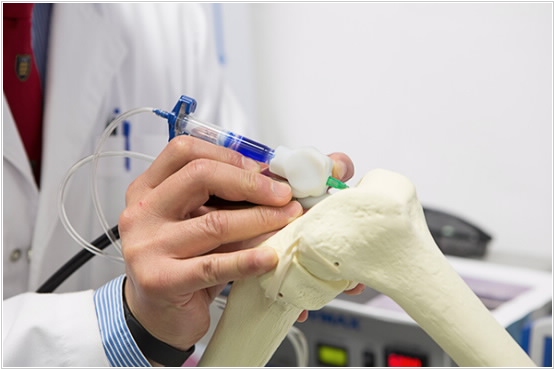
Уже, наверное, никто не сомневается, что 3D-биопринтеры скоро станут неотъемлемой частью медицины и будут использовать для создания искусственных органов и тканей. Но до сих пор речь шла об использовании больших биопринтеров в лабораториях. А вот австралийские ученые из университета Вуллонгонг подумали, почему бы не сделать портативный биопринтер, с помощью которого можно формировать нужные ткани и прямо на живом человек. И вот результат - BioPen - биопринтер в форме ручки, на которую по трубочкам подаются материалы: стволовые клетки и полимер (который обеспечивает нужную структуру, а потом растворяется через некоторое время). Ультрафиолетовый излучатель на кончике ручки обеспечивает быстрое застывание био-чернил. Использовать BioPen сначала собираются для ортопедических операций по эндопротезированию суставов, в которых нужно восстанавливать поврежденные хрящи и кости.
2013. Искусственный суставный хрящ позволит избавиться от артрита
При артрите, который не лечится лекарствами, изношенный сустав заменяют на пластиковый или металлический протез. Однако, такие имплантанты далеки от идеала. Специалисты по ортопедии из университета Дьюка (США) смогли создать синтетический сустав, который имплантировать пациенту будет гораздо проще, чем “железяку”. То есть, замене в таком случае подлежит только, собственно, изношенная часть сустава - его не надо безжалостно удалять, превращая человека в киборга с металлом в конечностях. Материал для синтетических хрящей состоит из переплетенных меж собой пучков волокон, каждое из которых не толще человеческого волоса. В итоге получается крепкое, гибкое и не пересыхающее чудо медицинской инженерной мысли. Затем в волокно оное вживляются стволовые клетки пациента. Из них вырастает живой хрящ толщиной примерно в один миллиметр. Полученную ткань пересаживают больному в суставы. Выращенная из стволовых клеток прочная белковая субстанция срастается с естественной хрящевой тканью пациента без отторжения.
2013. Новая технология имплантации искусственных межпозвоночных дисков
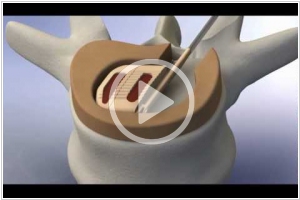
Межпозвоночный диск - это хрящевая пластинка между позвонками, которая играет роль амортизатора при ходьбе, прыжках, беге, наклонах, поворотах. В результате дегенеративных заболеваний эти пластинки могут разрушаться, при этом ограничивается подвижность, а из-за защемления нервных корешков, появляется сильная боль в спине. Если не удается вылечить эту боль лекарственными методами и лечебной физкультурой - прибегают к оперативной замене межпозвонкового диска на искусственный имплантант. Это довольно сложная операция, в ходе которой хирургу приходится разрезать мышцы и нервные волокна для доступа к позвоночнику. Американская компания Vertebral Technologies придумала способ, как свести эти повреждения к минимуму. Их технология InferFuse L позволяет имплантировать искусственный межпозвоночный диск по частям (в виде конструктора) и собирать его уже на месте. При этом разрез можно делать в разы меньше, а имплантируемый диск можно собрать любого размера - под индивидуальные особенности пациента. Технология InferFuse L на днях была сертифицирована для использования в американских клиниках.
2013. Японские ученые вырастили хрящевую ткань из клеток кожи

Японским ученым из университета Киото удалось воссоздать хрящевую ткань за счет перепрограммирования клеток эпидермиса кожи. Для этого в клетки кожи (с помощью специального вируса) был пересажен ген SOX9, который отвечает за образование хрящевой ткани. В результате через две недели ученые смогли получить ее подобие. Преимуществом данного метода является быстрота: использование стволовых клеток дает подобный результат только через месяц. Ученые отмечают, что выращенный хрящ был успешно пересажен лабораторным мышам. Ученые отмечают, что новый метод имеет еще одно преимущество - онкобезопасность. Старые методы преобразования обладают существенным минусом: довольно часто на пересаженных участках возникает онкологический процесс, который по тяжести может превосходить основное заболевания. Новый метод лишен столь серьезного недостатка.
2012. Видео: 3D биопринтер распечатывает человеческие органы

Лоуренс Бонассар, профессор отделения биотехнологий американского университета Cornell University рассказывает и показывает современные технологии 3D-печати человеческих тканей и органов. Его лаборатория специализируется на клонировании хрящей, например, ушных раковин. Процесс начинается с 3D-сканирования человека. Затем создается точная компьютерная модель. Затем создаются чернила - живые чернила из клеток и связующего геля. Затем 3D-биопринтер распечатывает хрящ слой за слоем.
Отделение ортопедии Клиники Фридрихсхафен получило сертификат Немецкой ассоциации травматологической медицины, принимает более 25 000 пациентов и проводит более 3 тысяч операций в год.
Его глава — профессор, доктор Ойген Винтер, является признанным специалистом в области ортопедической хирургии и не только проводит операции, но и обучает других врачей. Отделение ортопедии занимается лечением травм и заболеваний позвоночника, бедренных, коленных, плечевых и локтевых суставов, стоп, рук, хронических болей, сдавливания нерва и т.д.
Основная специализация отделения ортопедии — эндопротезирование бедренных и коленных суставов, включая полную замену сустава и восстановление хрящевой ткани путем ее трансплантации.
При повреждении или заболевании сустава могут страдать не только кости, но и покрывающие их ткани. В некоторых случаях нарушение целостности хряща предшествует разрушению кости.
Повреждение хрящевой ткани
Повреждение хрящевой ткани может быть вызвано несколькими причинами, в том числе:
- травмой,
- постоянным износом из-за чрезмерного веса или тяжелых физических нагрузок,
- нарушением обмена веществ,
- неправильным расположением элементов сустава (например коленного),
- возрастными изменениями,
- воспалением
Хрящевая ткань сама почти не восстанавливается. До недавнего времени считалось, что единственным решением при сильном повреждении была замена сустава.
Однако современная медицина предлагает иной способ: трансплантацию (пересадку) хрящевой ткани, хотя здесь имеются некоторые ограничения. Подобный способ лечения рекомендуется в основном для молодых пациентов со средним и обширным повреждением хрящевой ткани и не подходит для пожилых людей с остеоартритом.
Трансплантация хрящевой ткани проводится в случае, если размер пораженного участка не более 3-х квадратных сантиметров.
Для трансплантации может использоваться несколько видов хрящевой ткани:
- образец ткани с надкостницы (соединительной пленки, покрывающей кость там, где нет суставных хрящей)
- костно-хрящевой (трансплантация части хрящевой ткани вместе с кусочками костной, образующая своего рода мозаику на кости сустава)
- образец пасты стволовых клеток суставного хряща ( часть хрящевой ткани из углубления в центре коленного сустава извлекается и измельчается в специальном растворе, после чего им заполняют место удаленного поврежденного хряща).
- Трансплантация выращенных из собственного образца клеток хрящевой ткани
Трансплантация выращенных из собственного образца клеток хрящевой ткани - последная разработка медицины.
Во время минимально инвазивной операции у пациента берут небольшой образец здоровых клеток хряща и в лаборатории выращивают из них подходящий материал для трансплантации, а из пораженной части сустава извлекают разрушившиеся области. В некоторых случаях для компенсации нагрузки взятые здоровые клетки хряща заменяют своими же больными. Сама процедура занимает от половины до целого часа.
Для того, чтобы новая хрящевая ткань достигла необходимых размеров требуется в среднем три-четыре недели.
По истечении этого срока готовые к трансплантации клетки на специальной подложке пересаживают в место повреждения хряща.
После операции по трансплантации хрящевой ткани требуется восстановительный период длительностью от 6 до 12 недель, в некоторых случаях прописывают курс физиотерапии. Занятия спортом можно возобновлять только через 12- 16 недель. В зависимости от рода занятий, человеку, перенесшему операцию по трансплантации хрящевой ткани, может понадобиться отпуск с отрывом от производства.
Клинические испытания коллагенового геля (CaReS)
Клинические испытания модернизированного объемного коллагенового геля (CaReS) при лечении фокальных хрящевых дефектов коленного сустава.
Результаты: Пациентам вводят коллагеновый гель в область пораженного хряща. Во всех случаях гелеобразный матрикс беспрепятственно соединяется с фибрином в месте дефекта, чем укрепляет межтканевое взаимодействие. В среднем время хирургического вмешательства составляет 69 минут, а длина разреза для операционного доступа - 8,2 см. Специфические осложнения после операции не зафиксированы. В послеоперационном периоде со стороны объективных/субъективных IKDC-показателей, а также со стороны функциональных показателей и успешности процесса в целом, отмечаются значительные улучшения через 3-6 месяцев и до завершения наблюдения через 2 года. Метод очень прост в применении и демонстрирует, спустя незначительное время, превосходные клинические результаты.
Для подтверждения успешности конвенциональной АСТ по сравнению с классическими старыми методами было проведено долгосрочное исследование, в котором принимали участие множество пациентов, и в которое были включены гистологические и биомеханические методы диагностики регенеративной способности ткани.
Трансплантация хряща
Конвенциональная трансплантация хряща была разработана и введена в городе Бриттберг более 15 лет назад. Она получила признание в качестве действующего метода при лечении хондральных и остеохондральных дефектов. Успеху трансплантация хряща обязана многолетнему опыту ее использования в прошлом. Методика, которую врачи проводят в 2 этапа, по сей день считается стандартом лечения хряща сустава во всем мире и проводится после подтверждения показаний к операции.
- В первом этапе проводится артроскопия, во время которой в малонагруженном локусе медиально и латерильно надколенной поверхности бедренной кости или углубления, проводится изъятие хрящевых клеток (биологические пробы).
- После культивирования хрящевых клеток в специальной суспензии, на втором этапе оперативного вмешательства, суспензия вводится в биоактивную камеру. Последняя плотно вшивается в ткань периоста (высокая герметичность), расположенным по краям хрящевого дефекта. Защитная поверхность должна быть не только гидрофобной и устойчивой к механическим факторам, но и должна обладать хондрогенным эффектом (продуцировать рост новых дифференцированных клеток периоста).
Результаты: данного 2-хэтапного метода клинически определялись, как успешные и очень успешные (более 70%). И в сравнении с другими хирургическими методами лечения хрящевых дефектов, например таким, как классическая трансплантация (ACT) с его обширными дефектами и длительным временем курации, явно видно, на чьей стороне преимущества.
Недостатки классической трансплантации хрящя
Воодушевляющие результаты конвенциональной трансплантации хрящя не обходятся без недостатков на клеточном и техническом уровне. В результате непосредственного использования периоста появляется угроза кальцификации и расщепления. Использование жидкой клеточной суспензии может привести к потере герметичности.
При потере стабильности и целостности хрящевой основы становится сложно сшить концы ткани периоста, что негативно влияет на результат операции. Получение ткани периоста возможно при массивной артротомии или при многочисленных надрезах. Обе манипуляции требуют много времени, как и процесс фиксации трансплантата.
Кроме того, из-за обширного оперативного доступа травматизация сустава усугубляется, послеоперационный период удлиняется и появляются осложнения, например: артрофиброз. Низкое качество культивированных хондроцитов или уменьшение ширины ткани периоста может привести к плохому заполнению дефекта или к отказу от проведения операции.
Матрикссвязывающее лечение хряща, при помощи CaReS технологии
Чтобы избежать вышеописанной проблемы, были созданы разнообразные биоматериалы для матрикссвязывающей трансплантации(ATC). Некоторые варианты биоматериала находятся в лаборатории на стадии испытаний или в мультицентрическом клиническом введении. К используемому биоматериалу относится коллагеновый гель и мембраны, синтетические полимеры и структуры с гиалуроновой кислотой.
Используемая нами объемная матрикс-конструкция основана на коллагеновом геле 1 типа, который получают из крысиных хвостов. Процесс культивирования и заливка аутохондроцитов происходит после извлечения их из экстрацеллюлярного матрикса первичного хряща без каких-либо других действий.
Благодаря этому, обычно сводится к нулю возможность неверной дифференциации клеток при множественной заливке. Трансплантация возможна только при гомогенизации клеточной суспензии. Матрикс CaReS ведет к дальнейшей пролиферации клеток без возможности возникновения неверной дифференциации. Оперирующий врач может задать трансплантату желаемую консистенцию и точный размер.
Оперативная техника лечение хряща
После клинических исследований и готовности рентгенологических и МРТ-снимков, проводится артроскопия для определения размера и локализации хрящевого дефекта.
Инновационное оборудование для биопсии
Здесь важно повторно проверить консистенцию и прочность основания хряща, состояние необходимой суставной поверхности, а также менисков и связок. Биопсия выполняется по предписанию: от медиального до латерального края надколенной поверхности бедренной кости.
Для данной манипуляции мы используем специальное оснащение для изъятия хрящевой ткани. С помощью современной аппаратуры для биопсии становится возможным изъятие любого количества материала. Под визуальным контролем при помощи инструментов захватывается верхний конец от медиального до латерального края надколенной поверхности бедренной кости. С помощью инструментов проводится изъятие внутренних структур хряща, которые врач-лаборант осторожно вытягивает наружу, чтобы сделать срез ткани для биопсии. Последним этапом биопсии является перемещении образца ткани в пробирку со средой. Для культивирования клеток необходимы пробы, размером от 1 до 5 см, массой от 200 до 300 мг. Биоптат заливают веществом (не содержащим серы), добавляя 120-150 мл цельной крови и отправляют для дальнейшей обработки и культивирования, которое выполняет фирма “Ars Arthro”, город Эсслинген. Хрящевой биоптат смешивается с коллагеназой, из которого путем центрифугирования получают хондроциты. После оценки жизнеспособности к хрящевым клеткам добавляется коллаген-1 типа до образования гелеобразной суспензии.
Диаметр и плотность трансплантата может меняться в зависимости от состояния дефекта. После образования желеподобной изолированной субстанции и двухнедельной подготовки в серосодержащей среде, процесс завершается рассеиванием клеток хондроцитов в коллагеновом геле, который используется непосредственно для трансплантации.
На втором этапе оперативного вмешательства, после введения антибиотиков и наложения кровоостанавливающего жома, коленный сустав, в зависимости от локализации дефекта, медиально или латерально осуществляется парапателярный доступ. Проводится эта манипуляция, когда речь идет только о повреждении хряща, в прочих случаях при помощи кюретки проводится освобождение хряща до субхондральной зоны от омертвевшей ткани. Краевая часть срезается скальпелем таким образом, чтобы здоровая ткань слегка выступала. Следующим этапом является создание субхондральной кости. Здесь мы используем, при глубоком дефекте кости, один или несколько костных цилиндров, которые извлекаются из дистального бедренного метафиза или из головки большеберцовой кости при помощи костной дрели, после чего материал помещается в специальный вакутейнер для забора материала. Все выступающие неровности заполняются губчатым веществом. Следующие оперативные действия применяются при обоих видах повреждений. Дефект измеряется в соответствии с шаблоном, после чего заранее подготовленная конструкция клеточного матрикса вырезается строго по его размеру. Края дефекта смазываются тонким слоем фибринового клеящего вещества (Tissucol, компания Baxter), после чего в центр дефекта укладывается матрикс. Благодаря своей плотной структуре коллагеновый гель затвердевает в центре, а в остальных зонах его можно моделировать. Перед послойным заполнением повреждения проводится проверка сустава на подвижность, что позволяет максимально точно определить верную позицию для установки трансплантата.
Прочная, желатинообразная консистенция материала делает трансплантат гладким и однородным (нет разделения на отдельные волокна). Подготовленный коллагеновый гель после обработки фибрином основания трансплантата и краев, аккуратно укладывается в зону повреждения. Сразу после укладки коллагенового геля создается желаемая форма, которая полностью заполняет дефект, обволакивая рядом расположенные ткани. Средняя длина разреза для создания оперативного доступа составляет 8,2 см.
Реабилитация, после лечение хряща
Для изолированного бедренного дефекта мы накладываем временную шину на 48 часов, которая обеспечивает полное обездвиживание конечности. Также рекомендуется активная вспомогательная гимнастика, эргометрия и комплексные упражнения на мышцы после 12 недель. Спортивная нагрузка возможна через год после операции.
Результаты
Субъективное состояние пациентов в общем до проведения оперативного лечение оценивается, как плохое или очень плохое. Но уже спустя 3 месяца после проведения операции не остается ни одного негативного отзыва со стороны пациентов, касающегося состояния здоровья. Большое количество пациентов через 12 недель после хирургического вмешательства, а если быть точнее - 18,2% пациентов оценивают свое состояние, как очень хорошее, 54,5% оценивают свое состояние, как хорошее, и 27,3% чувствуют себя удовлетворительно. Через 6 месяцев повышается количество пациентов, оценивающих свое состояние, как очень хорошее и хорошее - 31,8 % и 50%, а количество пациентов, чувствующих себя удовлетворительно сокращается до до 18,2%. Через 2 года после операции 38,5% пациентов чувствуют себя очень хорошо, 46,1% - хорошо и всего 15,4% - удовлетворительно.
Послеоперационные осложнения после применения данного метода в практике не наблюдались.
Классическая трансплантация до настоящего момента является самым приемлемым методом для лечения массивных хондральных и остеохондральных дефектов в коленном суставе. Конвенциональная трансплантация показывает блестящие результаты, как в процессе многочисленных исследований, так и в клинической практике. Также показательными являются и интерпретации гистологических и биомеханических результатов. Результаты наших исследований демонстрируют значительное клиническое улучшение состояния больных после операции на бедре (повреждение хряща) с использованием объемного коллагенового геля. Через 12 месяцев после операции 86,4% пациентов (ICRS функциональный показатель) не имеют никаких ограничений. В процессе наблюдения отмечается значительное улучшение общего состояния среди пациентов: через 12 месяцев 90,9%, через 24 месяца 92,3%.
Также стоит отметить, что трансплантат прост в изготовлении, а операция по имплантации считается несложной. Продолжительность операции недолгая, разрез при операции незначительный. Послеоперационные трансплантационные осложнения, которые наблюдаются только при классической трансплантация, до сих пор не наблюдались, зато сразу дают о себе знать преимущества. Метод демонстрирует хорошие клинические результаты, что является основанием для его частого использования.
Резюме
Обобщив всю информацию, можно утверждать, что жидкие хондрофиллеры - оптимальный и надежный продукт для трансплантации. Любые дефекты хрящевой ткани можно заполнить при помощи представленных филлеров. Их надежность проявляется в отсутствии необходимости ревизии и дополнительного введения филлера, так как невозможно частичное вытекание или дислокация. При проведении МРТ (магнитно-резонансной томографии) у пациентов, зафиксированных в нашей базе, визуализируется четкое заполнение дефекта гелем, что подтверждает превосходный результат лечения суставного повреждения.
Читайте также:


