Что обозначает рнк вируса
Открытие вирусов, вызывающих злокачественные опухоли у животных, произошло еще на рубеже XIX и XX веков. В 1910 г. Пейтон Рауш обнаружил, что бесклеточный фильтрат из тканей птичьей саркомы может вызывать развитие аналогичной саркомы у цыплят. Примерно в это же время была доказана вирусная природа птичьего миелобластоза. Позднее было обнаружено, что часто проходит весьма значительный латентный период между инфицированием вирусом и развитием рака.
Тем не менее вплоть до 1960-х годов не существовало четких доказательств того, что инкорпорация вирусной ДНК в геном клетки является необходимым условием развития злокачественной трансформации, как не было и случаев выделения вирусной ДНК из раковых клеток.
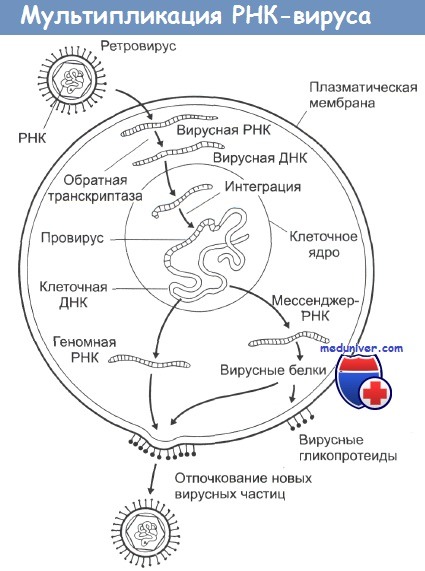
РНК-содержащие вирусы вызывают развитие целого ряда различных опухолей у животных, при этом наиболее распространена индукция этими вирусами лимфом, лейкемий и сарком. Типичная структура таких вирусов - это две идентичные цепочки молекул РНК в сочетании с ферментом обратная транскриптаза, одетых в гликопротеиновую оболочку. При инфицировании вирусом его обратная транскриптаза заставляет клетки синтезировать ДНК, комплементарную вирусной РНК.
Эта ДНК затем встраивается в клеточные хромосомы, и на ее основе клетка уже сама начинает синтез новых вирусных белков, вирусных обратных транскриптаз и элементов гликопротеиновой оболочки. Из-за механизма их действия этот тип вирусов получил название ретровирусы. Все они имеют весьма схожий внешний вид на электронных микрофотографиях и являются самыми маленькими из известных вирусов.
Некоторые из ретровирусов (например, вирусы птичьего лейкоза, кошачьей и мышиной лейкемии) содержат в себе только три гена и обладают очень длительным инкубационным периодом с момента заражения до возникновения опухоли. Другие вирусы (например, вирус саркомы Рауса (ВСР)) вызывают очень быструю злокачественную трансформацию и могут быть выделены из культуры опухолевых клеток.
Показано, что вирус ВСР содержит особый ген (v-src), способный вызывать трансформацию фибробластов in vitro. Этот ген кодирует наработку протеинкиназы, которая фосфорилирует тирозин. К сожалению, действие этой протеинкиназы запускает целый каскад различных метаболических процессов, и очень сложно оценить, какой именно из них ведет к злокачественной трансформации.
В настоящее время известно, что и нормальные, и злокачественные клетки содержат в своем генотипе участки ДНК, сходные или идентичные ряду последовательностей онкогенных РНК-содержащих вирусов. Такие участки получили название клеточных прото-онкогенов (чтобы отличать их от вирусных онкогенов). Постулируется, что активация этих участков, возникающая в результате канцерогенного воздействия, запускает целую цепочку событий, ведущую в итоге к злокачественной трансформации клетки. Считается также, что ретровирусы инкорпорировали эти клеточные участки в свой геном в процессе эволюции.
В настоящее время мы лучше понимаем механизмы действия продуктов вирусной активации. Примером такого продукта является протеинкиназа, активируемая геном sre, а также целый ряд других вирус-индуцированных канцерогенов. Это и рецепторы к эпидермальному фактору роста, продуцируемые геном v-erb, и тромбоцитарный фактор роста (ТФР), кодируемый фрагментами гена v-sis, и целый ряд связывающихся с ядром клетки белков, продукцию которых вызывает вирус птичьей лейкемии.
Как нормальные, так и раковые клетки содержат в себе участки последовательностей ДНК, гомологичные РНК онкогенных вирусов. Если происходит экспрессия или активация под действием канцерогенов этих клеточных онкогенов, это ведет к злокачественной трансформации клеток.
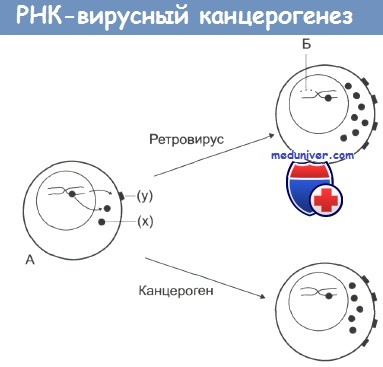
Онкогенная и злокачественная трансформация.
На стадии А нормальная клетка, которая характеризуется низкой протоонкогенной активностью, продуцирует фактор роста (х) или белки дифференцировки или рецепторы (у).
Канцерогены повышают активность протоонкогенов, что дает начало неопластической трансформации.
По другому механизму: при заражении ретровирусом происходит внедрение в ДНК клетки вирусных промоторов или онкогенов (Б), что также ведет к увеличению онкогенной активности и последующей злокачественной трансформации.
Первым ретровирусом, для которого была однозначно доказана связь со злокачественными новообразованиями, был вирус Т-клеточной лейкемии человека (ВТКЛ-1), выделенный из клеток хронической кожной Т-лимфомы. Этот вирус довольно широко распространен, может передаваться половым путем, через кровь, особенно в среде наркоманов, и от беременной женщины к плоду. Первоначально эндемический ареал циркуляции данного вируса был в основном представлен тропическими странами, однако в настоящее время в США серопозитивная реакция на вирус обнаруживается у каждого из 4000 человек населения. Кроме Т-клеточной лейкемии вирус вызывает тропический спастический паралич.
После 20 лет наблюдения за серопозитивными пациентами оценено, что риск развития последнего заболевания составляет около 5%. Один из вирусных генов, а именно tax-ген, вызывает увеличение продукции клеточного интерлейкина-2 (ИЛ-2) и его рецепторов, что является основным фактором, стимулирующим деление Т-клеток.
Ретровирусы могут вызывать опухолевые заболевания не напрямую, а опосредованно, как это было показано для вируса иммунодефицита человека (ВИЧ-1), вызывающего развитие СПИДа. Случаи развития рака у ВИЧ-инфицированных рассмотрены в одном из обзоров. Отмечается, что у ВИЧ-инфицированных наиболее часто развиваются три типа опухолей: мгновенная или высокозлокачественная В-клеточная лимфома; саркома Капоши (СК, которую вызывает другой вирус — герпесвирус ГСК, или герпесвирус 8); карцинома шейки матки.
До разработки эффективных методов терапии ВИЧ-инфицированных более 40% из них заболевали тем или иным видом рака. Тем не менее связь этого вируса с развитием онкологических заболеваний скорее всего косвенная и опосредована развитием общей хронической иммунодепрессии организма, которая и позволяет другим канцерогенным вирусам вызывать рак. В-клеточные лимфомы также характеризуются довольно сложным патогенезом. Хотя В-клетки не поражаются вирусом ВИЧ-1, они могут быть мишенью для других типов вирусов, например для вируса Эпштейна-Барра (ВЭБ). Рак шейки матки у женщин также развивается на основе вторичной вирусной инфекции — вируса папилломы человека (ВПЧ), на фоне общей иммунодепрессии, вызванной ВИЧ-1. По причине общего снижения иммунных реакций организма все эти опухоли развиваются особенно быстро и агрессивно.
Показано, что РНК-содержащий вирус гепатита С значительно увеличивает риск заболевания гепатоклеточной карциномой. У больных, инфицированных этим вирусом, риск развития раковой опухоли возрастает в 100 раз, но механизмы его канцерогенного действия в настоящее время почти не изучены. Если больной заражен еще и вирусом гепатита В, риск развития рака печени возрастает многократно. На земном шаре одним или обоими из этих вирусов заражено около миллиарда человек.

РНК гепатита С – это молекула, содержащая наследственную информацию вируса. Именно ее определяет анализ методом ПЦР (полимеразной цепной реакции). Это ключевой этап диагностики, подтверждающий инфицирование гепатитом. Также по строению РНК определяют генотип HCV. Эти данные нужны для выбора терапии, поскольку некоторые подтипы (3а, 3б) не поддаются традиционному лечению интерфероном. Для достоверного результата потребуется соблюдать правила подготовки к исследованию.
Что такое РНК вируса
РНК, или рибонуклеиновая кислота, – это уникальный генетический материал организма. У вирусных гепатитов С от конструкции РНК зависит устойчивость вируса к разным типам лечения и особенности протекания болезни. Появление в крови фрагментов вирусной РНК значит, что болезнь вступила в острую фазу.
У хронических больных в состоянии ремиссии кровь также содержит РНК гепатита С и антитела к ней, но в меньшем объеме, чем при обострениях. Тем не менее, этого количества вируса все равно достаточно для заражения здоровых людей.
Кому назначают диагностику
Обследование крови на РНК HCV нужно в таких случаях:
- При обнаружении антител или повышения печеночных ферментов у человека, считающегося здоровым. Анализы на разные виды гепатита проводят для выявления болезни или ее исключения из списка возможных причин разрушения клеток печени.
- Когда лечат уже обнаруженный гепатит для отслеживания эффективности терапии. Контроль за уровнем вирусной РНК в крови своевременно выявит резистентность (устойчивость) к принимаемым лекарствам.
- После выздоровления на протяжении года – чтобы вовремя заметить рецидив.
Техника проведения анализа
Методом ПЦР обнаруживают нуклеиновые элементы, входящие в состав белковой оболочки вируса. Полимеразная цепная реакция выявляет:
- присутствие фрагментов HCV в крови;
- уровень вирусной нагрузки – количество частиц в миллилитре крови;
- генотип гепатита.
Важно правильно подготовиться к забору крови из вены для полимеразной реакции, чтобы не было искажений в результате теста. Для этого:
- Не употреблять алкоголь, энергетики, жирную и жареную пищу в течение 3 дней до сдачи теста.
- Избегать физических и нервных нагрузок за 2-3 дня до анализа.
- Отказаться от приема лекарств, а если это невозможно – уведомить врача о принимаемых препаратах.
- Не сдавать анализ во время обострения хронических вирусных болезней, а также при ОРВИ.
- При беременности и во время менструации предупредить врача о своем состоянии, поскольку гормональные нарушения в этот период вызывают искажения результатов.
Расшифровка
Обработка крови состоит из трех этапов:
- Определение РНК вируса гепатита в крови (качественный анализ).
- Оценка вирусной нагрузки (количественный анализ). Применяется только при положительном результате первого (когда в материале обнаружено присутствие вируса).
- Генотипирование. Его проводят при первом обращении по подозрению на гепатит, а также при низкой эффективности терапии – чтобы выявить мутацию вируса.
При подозрении на ложный результат потребуется повторно пройти обследование через 2 недели.
На оборудовании большинства лабораторий гепатит С будет выявлен, если количество частиц больше 50 МЕ/мл (международных единиц на миллилитр крови). Редкие диагностические аппараты способны выявить гепатит при уровне 10 МЕ/мл. При меньшем количестве частиц вируса будет получен ложноотрицательный результат (гепатита C не обнаружено).
Присутствие в крови антител с одновременным отрицательным результатом на тестирование по вирусу – причина пройти повторное обследование через 2 недели. Также можно обратиться в другую лабораторию с более современным оборудованием для диагностики.
По результатам количественного теста можно определить, насколько эффективно организм борется с гепатитом С. Этим тестом определяют прогресс болезни, а также действенность терапевтической программы. Уровень вируса в крови определяют в МЕ/мл. В зависимости от результатов пациента относят к одной из пяти групп:
- Здоров (вируса не обнаружено).
- Минимальный уровень вируса в крови (меньше 180 МЕ/мл. Условно здоров. Иногда может означать ложноположительный результат или скрытое носительство без болезни.
- Болен с низкой вирусной нагрузкой (менее 800 тыс. МЕ/мл)
- Болен с высокой вирусной нагрузкой (от 800 тыс. до 2.5 млн. МЕ/мл)
- Терминальная вирусная нагрузка (более 2,5 млн. МЕ/мл).
От регресса вирусной нагрузки зависит длительность терапии. При слишком медленном падении активности вируса (плохой эффективности терапии) лечение растягивается на полгода и более. Если вирус удастся уничтожить быстрей, срок лечения не превышает 3 месяцев.
Существует 11 генотипов вируса с различными подтипами. Некоторые из них вводят больных в группу риска по онкологии и фиброзу сильней остальных, другие не поддаются стандартной терапии интерфероном. В идеале генотипирование нужно провести при первичном обнаружении гепатита. Но из-за ограниченности ресурсов к этому анализу прибегают только при отсутствии результатов терапии.
Если есть возможность сделать генотипирование платно, обязательно нужно ею воспользоваться. Этот анализ предотвратит потерю времени на терапию, которая может быть неэффективна при редком субтипе гепатита С.
Как часто нужно сдавать кровь на диагностику
Регулярное обследование на гепатит показано:
- Людям, которые входят в группу риска из-за профессии или вредных привычек. К первым относятся врачи, ко вторым – наркоманы и люди, практикующие беспорядочные половые связи без использования презервативов.
- Проходящим терапию – для отслеживания эффективности лечения.
- Излечившимся от гепатита с целью предотвращения рецидивов.
Кровь на профилактическое обследование у группы риска берут раз 3-6 месяцев. Во время лечения потребуется сдавать анализы чаще – раз в 4-6 недель. При сомнениях в эффективности оборудования той лаборатории, где проводятся анализы, лучше сдать тест в нескольких клиниках одновременно.
Интересуетесь, что такое ДНК? Это важная молекула в организме человека, которая выполняет определенную функцию. Именно благодаря ДНК устанавливается родство, а также определяются внешние данные человека. Подробнее о молекуле прочтете в статье.

Внимание! Материал носит лишь ознакомительный характер. Не следует прибегать к описанным в нем методам лечения без предварительной консультации с врачом.
Что такое ДНК человека простыми словами
О ДНК не понаслышке знает каждый человек, который учил в школе биологию или смотрел какие-либо фильмы и сериалы, в которых главные герои часто проходят генетический тест. Однако многие так и не могут понять, что же на самом деле собой представляет загадочное вещество ДНК.
ДНК — это сокращенная аббревиатура названия кислоты, которая находится в хромосомной клетке человека. Научное название выглядит так —дезоксирибонуклеиновая кислота. Сокращение пошло от трех составляющих этого вещества: Дезоксирибо Нуклеиновая Кислота.
Казалось бы, что важного в обычной кислоте и почему о ней так много говорят? Дело в том, что в веществе хранится генетическая информация (код), в которой заложены данные человека. Именно благодаря ДНК у каждого индивида определенное телосложение, цвет глаз и волос, а также характеристика. Во время деления клеток кислота обеспечивает правильную подачу и считывание информации.

Фото: В чем разница
Интересует строение ДНК? Если посмотрите на кислоту под микроскопом, увидите длинную волнообразную кривую с перекрытиями. Она состоит из нескольких нуклеотидов, которые соединяются цепями, а затем закручиваются в спирали. Если одну такую волну раскрутить, ее длина будет такой же, как и рост среднестатистического мужчины — приблизительно 1 м 80 см.
ДНК содержится в ядре абсолютно каждой клетки человека, причем по своему составу она идентичная. Она структурируется в 46 хромосомах, которые несут генетический код.
ДНК каждого человека уникальна. Абсолютно идентичной по составу она может быть только у однояйцевых близнецов.

Фото: Популярная механика
Молекула ДНК может повреждаться. Зачастую это случается из-за воздействия агрессивных веществ:
РНК: что это такое
РНК расшифровывается как рибонуклеиновая кислота. Эта молекула состоит из остатков фосфорных кислот и азотистых оснований.
Структура ДНК и РНК практически аналогична, да и по внешнему виду у молекул есть сходство, только РНК состоит из одной волнообразной цепи.

ДНК и РНК — это нуклеиновые кислоты, которые похожи по своему составу, однако отличаются функциями. О пользе первой вы уже знаете. Поэтому пришло время выяснить, что же делает РНК.
РНК содержится в каждых клетках живых организмов, даже в вирусах, и разделяется на такие подвиды:
- информационная — отвечает за хранение информации (иРНК);
- транспортная — доставляет аминокислоты к рибосомам (тРНК);
- рибосомная — содержится в рибосомах (рРНК).
В некоторых источниках классификация РНК расширяется: можно встретить еще вирусную, рибозиму и минорную кислоты.

В отличие от ДНК, в которой информация лишь хранится, РНК отвечает за транскрипцию и трансляцию генетической информации, а также участвует в синтезе белка.
Вы узнали, что такое ДНК и РНК, в чем их разница и схожесть. Разобраться в сложных биологических терминах бывает непросто, однако важно запомнить одно: ДНК отвечает за хранение информации, а РНК — за ее перенос.
Рецензент: кандидат медицинских наук, профессор Иван Георгиевич Максаков

Вирусный гепатит С является заболеванием, передающимся через кровь. Это означает, что основными методами диагностики данного заболевания являются аналитические исследования данной биологической жидкости.
РНК вируса гепатита С не обнаружено
Для первичной диагностики гепатита С используются данные, полученные в процессе качественного анализа. Этот диагностический метод относится к наиболее точным и в настоящее время считается одним из лучших способов определения наличия в крови пациента возбудителя вирусного воспаления печени. Результаты анализа могут быть следующими:
- РНК гепатита С не обнаружено. Что это значит? Это означает, что фрагментов патогенной рибонуклеиновой кислоты в исследуемом образце крови нет. Такой результат может говорить о том, что обследуемый здоров.
- РНК гепатовируса обнаружено. Такой результат может говорить о наличии патогена в организме человека. Но болезнь не обязательно находится в активной форме (возможно, что вы являетесь носителем вируса или на данный момент инкубационный период).
Таким образом, если РНК не обнаружено, гепатита С в организме обследуемого, скорее всего, нет. Однако рекомендуется пройти дополнительную диагностику, так как возможны и ложные результаты.
Особенности анализа
Вирусный гепатит С относится к типу заболеваний с осложненной диагностикой. Проблема в том, что в большинстве случаев заболевание проявляется бессистемно, ярких симптомов не наблюдается, и пациент может попросту не подозревать о своем недуге. Таким образом, помочь определить заболевание на ранних стадиях и выявить РНК вируса гепатита С можно только на основании качественного анализа крови.
Обследование основывается на полимеразной цепной реакции (ПЦР). Суть его заключается в эксплуатации специфических ферментов, имитирующих РНК ВГС. В процессе исследования изучается реакция образцов крови пациента на эти ферменты. Это позволяет выявить наличие и концентрацию патогена.
Преимуществами анализа на выявление элементов вирусного РНК являются:
- Точность метода. Погрешность в результатах, в случае соблюдения лабораторными работниками самим обследуемым всех необходимых мер, сведена к минимуму.
- Оперативное получение результатов диагностики. Результат анализа предоставляется в течение 6-7 часов после явки пациента в лабораторию. Даже с учетом очередей на сдачу крови, обследуемый очень быстро узнает, найдены ли в его крови фрагменты вирусной РНК.
- Высокая чувствительность. Это означает, что даже при небольшой концентрации искомого материала в крови больного РНК без труда обнаруживается.
- Невысокая стоимость. Данный анализ по цене не отличается от других, менее информативных методов. В совокупности с надежностью и скоростью реакции, качественный метод ПЦР остается наиболее востребованным вариантом определения гепатовируса.
Однако некоторые нюансы необходимо принимать в расчет. В первую очередь, пациенту рекомендуется обращаться только в те медицинские учреждения, в штате которых трудятся специалисты высокого уровня. Из-за чувствительности реагентов малейшая неточность в работе лаборанта приводит к ложноположительным или ложноотрицательным результатам.
Также необходимо понимать, что у каждого аппаратного оборудования есть нижний предел чувствительности к реагентам. Это означает, что если возбудитель вирусного воспаления печени пребывает в крови больного в чрезвычайно низкой концентрации, даже такой точный метод, как ПЦР, может не выявить его РНК. Если у пациента или лечащего врача сохраняется подозрение на заражение ВГС, рекомендуется через некоторое время пройти повторную диагностику.
Принципы проведения анализа

Для того чтобы наверняка выявить наличие или отсутствие РНК вируса гепатита С в образцах крови пациента, материал должен быть максимально пригодным для обследования. Это невозможно без соблюдения пациентом следующих норм:
- Отказ от жирной и тяжелой пищи накануне сдачи крови
- Отказ от курения и распития алкогольных напитков
- Отказ от любой пищи в течение последних 8 часов и сдача образца биологической жидкости натощак
- Явка в лабораторию в раннее время суток
Следует отметить, что качественный анализ на обнаружение РНК гепатита С назначается не во всех случаях. Врач может порекомендовать его проведение, если:
- Обнаружены иммуноглобулины ВГС в крови больного
- Вирус гепатита С обнаружен, но иммуноглобулины не выявлены
- Проводилась противовирусная терапия, и требуется выявить уровень РНК ВГС для мониторинга ее эффективности
В первых двух случаях анализ на проверку РНК HCV качественный предписывается только после сероконверсии. В случае, если антитела к антигенам ВГС не обнаруживаются, можно понять, что вирус в организме присутствует, но по каким-либо причинам не получает иммунологического отклика.
При наличии иммуноглобулинов анализ позволяет установить, необходимо ли медикаментозное лечение, или организм может справиться сам.
В случае мониторинга противовирусного лечения, ПЦР проводится строго для проверки его эффективности. Результаты позволяют понять, насколько действенна подобранная лекарственная схема. Если эффект незначительный, гепатолог может переосмыслить терапевтический подход и назначить более подходящее лечение. Если же РНК не обнаружено, гепатит С с большой долей вероятности побежден.
Заключение
Итак, чтобы уметь расшифровывать качественный анализ ПЦР до прибытия к лечащему врачу, необходимо запомнить, что может быть 2 варианта результата:
- РНК гепатита С не обнаружено. Что это значит? Патогена в крови исследуемого не обнаружено. Либо он полностью отсутствует, либо его концентрация ничтожно мала. РНК не обнаружено — что это значит? Скорее всего, пациент здоров. В любом случае, лечение не требуется.
- Фрагменты РНК обнаружены. Положительный результат, вирус присутствует в крови исследуемого. Для точного определения патогенной нагрузки рекомендуется пройти количественный ПЦР-тест. Если уровень заражения не снизился в процессе противовирусной терапии, лечащий врач должен переосмыслить схему лечения и внести в нее коррективы.
Важно помнить: если инфицирование подтверждено, следует незамедлительно приступить к терапевтическим мерам.
Промедление в лечении ВГС грозит тяжелыми последствиями. Самолечением заниматься не следует. Определить подходящую терапию может только лечащий врач.
Из нескольких сотен известных в настоящее время вирусов человека и животных РНК-геном содержит около 80% вирусов. Способность РНК хранить наследственную информацию является уникальной особенностью вируса.
У просто организованных и некоторых сложно организованных вирусов вирусная РНК в отсутствие белка может вызвать инфекционный процесс. Впервые инфекционная активность РНК вируса табачной мозаики была продемонстрирована X. Френкель-Конратом и соавт. в 1957 г. и А. Гирером и Г. Шраммом в 1958 г. Впоследствии положение об инфекционной активности РНК было перенесено на все РНК-содержащие вирусы, однако долголетние усилия доказать это для таких вирусов, как вирусы гриппа, парамиксовирусы, рабдовирусы (так называемые минус-нитевые вирусы), оказались бесплодными: у этих вирусов инфекционной структурой являются не РНК, а комплекс РНК с внутренними белками. Таким образом, геномная РНК может обладать инфекционной активностью в зависимости от своей структуры.
Структура вирусных РНК чрезвычайно разнообразна. У вирусов обнаружены однонитчатые и двунитчатые, линейные, фрагментированные и кольцевые РНК. РНК-геном в основном является гаплоидным, геном ретровирусов — диплоидный, т. е. состоит из двух идентичных молекул РНК.
В основном однонитчатые РНК являются линейными молекулами, однако РНК-фрагменты буньявирусов обнаружены в виде кольцевой формы. Кольцевая форма возникает за счет образования водородных связей между концами молекул.
Двунитчатые РНК.Этот необычный для клетки тип нуклеиновой кислоты, впервые обнаруженный у реовирусов, широко распространен среди вирусов животных, растений и бактерий. Вирусы, содержащие подобный геном, называют диплорнавирусы.
Общей особенностью диплорнавирусов является фрагментированное состояние генома. Так, геном реовирусов состоит из 10 фрагментов, ротавирусов — из 11 фрагментов.
Молекулярная масса РНК таких вирусов варьирует в широких пределах.
БЕЛКИ
В зараженной клетке вирусный геном кодирует синтез двух групп белков: 1) структурных, которые входят в состав вирусных частиц потомства, и 2) неструктурных, которые обслуживают процесс внутриклеточной репродукции вируса на разных его этапах, но в состав вирусных частиц не входят.
Структурные белки. Количество структурных белков в составе вирусной частицы варьирует в широких пределах в зависимости от сложности организации вириона. Наиболее просто организованный вирус табачной мозаики содержит всего один небольшой белок с молекулярной массой 17—18- 10 3 , некоторые фаги содержат 2—3 белка, просто организованные вирусы животных — 3—4 белка. Сложно устроенные вирусы, такие как вирусы оспы, содержат более 30 структурных белков.
Структурные белки делятся на 2 группы:
1) капсидные белки, образующие капсид, т. е. футляр для нуклеиновой кислоты вируса (от лат. capsa — вместилище), и входящие в состав капсида геномные белки, и ферменты;
2) суперкапсидные белки, входящие в состав суперкапсида, т. е. наружной вирусной оболочки.
Просто организованные вирусы, представляющие собой нуклеокапсид, содержат только капсидные белки. Сложно организованные вирусы содержат капсидные и суперкапслдные белки.
В составе капсида некоторых вирусов (пикорнавирусы, паповавирусы, аденовирусы) содержатся белки, ковалентно связанные с вирусным геномом (геномные белки). Эти белки являются терминальными, т. е. соединенными с концом вирусной нуклеиновой кислоты. Функции их неразрывно связаны с функциями генома и их регуляцией.
У ряда сложно организованных вирусов в составе капсида имеются ферменты, осуществляющие транскрипцию и репликацию вирусного генома — РНК и ДНК (РНК-и ДНК-полимеразы), а также ферменты, модифицирующие концы иРНК. Если ферменты и геномные белки представлены единичными молекулами, то капсидные белки представлены множественными молекулами. Эти белки и формируют капсидную оболочку, в которую у сложно организованных вирусов вставлены молекулы белков с другими функциями.
Основным принципом строения капсидной оболочки вирусов является принцип субьединичности, т. е. построение капсидной оболочки из субъединиц-капсомеров, образованных идентичными полипептидными цепями. Правильно построенные белковые субъединицы — капсомеры возникают благодаря способности вирусных капсидных белков к самосборке. Самосборка объясняется тем, что упорядоченная структура — капсид имеет наименьшую свободную энергию по сравнению с неупорядоченными белковыми молекулами. Сборка капсидной оболочки из субъединиц запрограммирована в первичной структуре белка и происходит самопроизвольно или при взаимодействии с нуклеиновой кислотой.
Принцип субъединичности в строении вирусного капсида является универсальным свойством капсидных белков и имеет огромное значение для вирусов. Благодаря этому свойству достигается огромная экономия генетического материала. Если бы капсидная оболочка была построена из разных белков, то на кодирование ее потребовалась бы основная часть генетической информации, заложенной в вирусном геноме. В действительности на кодирование, например, одной полипептидной цепи вируса табачной мозаики, расходуется менее 10% генома. Далее, в механизме самосборки заложена возможность контроля за полноценностью вирусных полипептидов: дефектные и чужеродные полипептидные цепи при таком способе сборки вирионов будут автоматически отбрасываться.
Описанная способность к самосборке в пробирке и в зараженной клетке характерна только для простых вирусов. Сборка сложно организованных вирусов является гораздо более сложным многоступенчатым процессом, хотя отдельные ее этапы, например формирование капсидов и нуклеокапсидов, также основаны на самосборке.
Суперкапсидные белки. Гликопротеиды. Суперкапсидные белки, или пепломеры, располагаются в липопротеидной оболочке (суперкапсиде или пеплосе) сложно устроенных вирусов. Они либо пронизывают насквозь липидный бислой как, например, гликопротеиды альфа-вирусов (вируса леса Семлики), либо не доходят до внутренней поверхности. Эти белки являются типичными внутримембранными белками и имеют много общего с клеточными мембранными белками. Как и последние, суперкапсидные белки обычно гликозилированы. Углеводные цепочки прикреплены к молекуле полипептида в определенных участках. Гликозилирование осуществляют клеточные ферменты, поэтому один и тот же вирус, продуцируемый разными видами клеток, может иметь разные у углеводные остатки: может варьировать как состав углеводов, так и длина углеводной цепочки и место прикрепления ее к полипептидному остову.
Основной функцией гликопротеидов является взаимодействие со специфическими рецепторами клеточной поверхности. Благодаря этим белкам осуществляется распознавание специфических клеточных рецепторов и прикрепление к ним вирусной частицы, т. е. адсорбция вируса на клетке. Поэтому гликопротеиды, выполняющие эту функцию, называют вирусными прикрепительными белками.
Другой функцией гликопротеидов является участие в слиянии вирусной и клеточной мембран, т. е. в событии, ведущем к проникновению вирусных частиц в клетку. Вирусные белки слияния ответственны за такие процессы, как гемолиз и слияние плазматических мембран соседних клеток, приводящие к образованию гигантских клеток, синцитиев и симпластов.
Неструктурные белки. Неструктурные белки изучены гораздо хуже, чем структурные, поскольку их выделяют не из очищенных препаратов вирусов, а из зараженных клеток, и возникают трудности в их идентификации и очистке от клеточных белков.
К неструктурным белкам относятся:
1) предшественники вирусных белков, которые отличаются от других неструктурных белков нестабильностью в зараженной клетке в результате быстрого нарезания на структурные белки;
2) ферменты синтеза РНК и ДНК (РНК- и ДНК- полимеразы), обеспечивающие транскрипцию и репликацию вирусного генома;
4) ферменты, модифицирующие вирусные белки, например протеиназы и протеинкиназы.
Однако многие неструктурные белки при ряде вирусных инфекций еще не идентифицированы и функции их не определены.
Читайте также:


