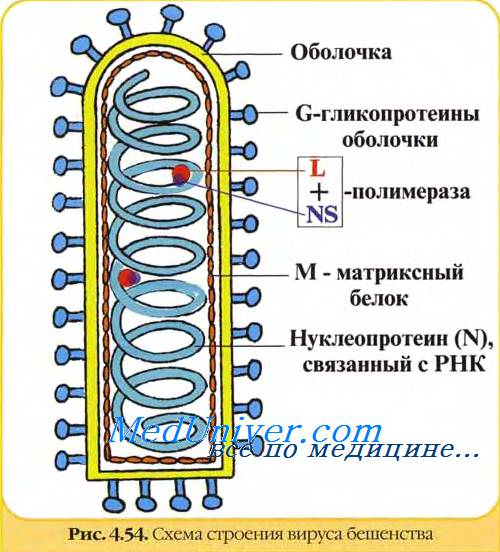
Что такое фиксированный вирус бешенства
Бешенство (синонимы: rabies, lyssa, hydrophobia – водобоязнь) – особо опасная инфекционная болезнь человека и теплокровных животных, передающаяся при контакте с инфицированным животным (укус, ослюнение микроповреждений), характеризующаяся поражением ЦНС и смертельным исходом. Вирусная этиология бешенства доказана в 1903 г. П. Рем-ленже.
Таксономия. Возбудитель бешенства – РНК-содержащий вирус, относится к семейству Rhabdoviridae (от греч. rhabdos – прут), роду Lyssavirus.
Морфология и химический состав. Вирионы пулевидной формы, размером 170x70 нм, состоят из сердцевины, окруженной липопротеидной оболочкой с шипиками гликопро-теидной природы. РНК – однонитчатая, минус-нитевая.
Культивирование. Вирус бешенства культивируют в мозговой ткани белых мышей, сирийских хомячков, кроликов, крыс, морских свинок, овец и др. У зараженных животных развиваются параличи конечностей, затем они погибают. Вирус бешенства может быть адаптирован к первичным и перевиваемым культурам клеток и куриным эмбрионам. В цитоплазме пораженных вирусом клеток головного мозга животных или культур ткани образуются специфические включения, впервые описанные В. Ба-бешем (1892) и А. Негри (1903) и поэтому названные тельцами Бабеша.Негри. Включения сферической или овальной формы, величиной от 0,5 до 20 мкм, хорошо окрашиваются кислыми красителями, содержат вирусный антиген, имеют диагностическое значение.
Антигенная структура. В составе вируса бешенства обнаружены сердцевинные и поверхностные антигены. Гликопротеидный антиген (белок шипиков) обладает выраженными иммуногенными свойствами. Существуют два вируса бешенства, идентичных по антигенным свойствам: дикий, циркулирующий среди животных, патогенный для человека, названный уличным вирусом, и фиксированный вирус (virus fixe), полученный Л. Пастером в лабораторных условиях путем длительных пассажей уличного вируса через мозг кроликов. В связи с утратой последним вирулентности для человека Л. Пастер использовал этот вирус в качестве антирабической вакцины.
Резистентность. Вирус бешенства малоустойчив в окружающей среде: быстро погибает под действием солнечных и УФ-лучей, дезинфицирующих средств (фенол, хлорамин, формалин), чувствителен к жирорастворителям и щелочным растворам. Длительно сохраняется при низкой температуре (-20ºС).
Эпидемиология. Бешенство известно с древних времен. Это типичная зоонозная инфекция, которая широко распространена на земном шаре. Все теплокровные животные могут болеть бешенством. Однако в силу особенностей механизма передачи (через укус) циркуляцию вируса в природе обеспечивают дикие и домашние плотоядные животные, главным образом собаки, волки, лисицы, енотовидные собаки, шакалы, кошки. Природные очаги бешенства имеются повсеместно. Человек является случайным звеном в эпидемическом процессе и не принимает участия в циркуляции вируса в природе. Вирус бешенства накапливается и выделяется через слюнные железы животного во время болезни и в последние дни инкубационного периода. Механизм передачи возбудителя – прямой контактный, в основном при укусах, в меньшей степени при обильном ослюнении кожи, имеющей царапины и ссадины. Роль больного человека как источника инфекции минимальна, хотя слюна его и содержит вирус бешенства. Имеются лишь единичные случаи заражения человека человеком.
Патогенез и клиническая картина. Вирус бешенства обладает выраженными нейротропными свойствами. Из места внедрения вирусы поступают в ЦНС по периферическим нервным волокнам, размножаются в ней, а затем распространяются центробеж-но, поражая всю нервную систему, в том числе нервные узлы некоторых железистых органов, особенно слюнных желез. В последних вирусы размножаются и выделяются со слюной в окружающую среду. Инкубационный период при бешенстве у человека варьирует от 7 дней до 1 года и более в зависимости от локализации и характера повреждения, а также вирулентности штамма. Наиболее короткая инкубация наблюдается при обширных укусах головы.В клинической картине бешенства у человека различают следующие периоды: предвестников (продромальный), возбуждения и параличей. Заболевание начинается с появления чувства страха, беспокойства, раздражительности, бессонницы, общего недомогания, воспалительной реакции на месте укуса. Во второй период болезни резко повышается рефлекторная возбудимость, появляются гидрофобия (водобоязнь), спазматические сокращения мышц глотки и дыхательной мускулатуры, затрудняющие дыхание; усиливается слюноотделение, больные возбуждены, иногда агрессивны. Через несколько дней возникают параличи мышц конечностей, лица, дыхательной мускулатуры. Продолжительность заболевания 3-7 дней. Летальность 100 %.
Иммунитет. Естественно приобретенный иммунитет не изучен, так как обычно заболевание заканчивается смертью. Искусственно приобретенный иммунитет возникает после проведения вакцинации людям, укушенным бешеными животными. Он обусловлен выработкой антител, сохраняющихся в течение года, образованием интерферона, а также клеточными факторами иммунитета.
Лабораторная диагностика. Лабораторные исследования проводят посмертно. В качестве исследуемого материала используют кусочки головного и спинного мозга, подчелюстные слюнные железы согласно правилам, предусмотренным для работы с особо опасным инфекционным материалом.
Экспресс-диагностика основана на обнаружении специфического антигена с помощью РИФ и ИФА и телец Бабеша.Нефи. Выделяют вирус с помощью биопробы на белых мышах.
Специфическая профилактика и лечение. Вакцины против бешенства были разработаны и предложены Л.Пастером. Вакцины, полученные из мозга зараженных животных – кроликов, овец, могут вызывать осложнения, поэтому их используют редко. В нашей стране применяют антирабическую культуральную концентрированную вакцину, полученную из штамма Внуково-32 (происходит от фиксированного вируса Пастера), инактивированную УФ- или гамма-лучами. Лечебно-профилактической вакцинации подвергают лиц, укушенных или ослюненных больными или подозрительными на бешенство животными. Прививки необходимо начинать как можно раньше после укуса. В тяжелых случаях применяют комбинированное введение антирабического иммуноглобулина и вакцины. Разрабатываются генно-инженерные антирабические вакцины. Лечение симптоматическое.
В классических опытах Пастера штамм уличного вируса бешенства, выделенный из мозга коровы 19 ноября 1881 г., в дальнейшем поддерживался путем субдурального заражения кроликов. При первых пассажах кролики заболевали с инкубационным периодом 14—17 дней, на 12-м пассаже инкубационный период сократился до 12 дней и после 90 пассажей — до 7 дней (Pasteur е. а.). При последующих пассажах в лаборатории Пастера 7-дневный инкубационный период оставался постоянным, фиксированным. Одновременно было отмечено изменение патогенных свойств вируса для собак при подкожном введении: если исходный вирус вызывал заболевание бешенством у 6 из 7 собак, то после 90 пассажей он убивал только одну из 7 собак.
Выжившие после подкожного введения фиксированного вируса собаки оказались иммунными к заражению уличным вирусом бешенства.
Таким образом, разработанная Пастером методика культивирования вируса бешенства in vivo и выведенный им частично аттенуированный фиксированный вирус бешенства до сих пор используются в производственной и лабораторной практике. Штамм Пастера был передан для производства антирабической вакцины почти всем странам мира. В многочисленных институтах различных стран он до сих пор поддерживается путем субдурального или интрацеребрального заражения кроликов.
В литературе есть сведения о фиксации вируса бешенства путем интрацеребральных пассажей на собаках (Jonnesco), лошадях или телятах (Jacott, Roux), морских свинках, овцах, мышах и других животных. В 20-х годах в связи с ошибочным мнением об антигенных различиях между штаммами вируса бешенства наблюдалось увлечение штаммами фиксированного вируса, выведенными из местных штаммов уличного вируса. Такого рода штаммы были выведены как за рубежом, так и в нашей стране. Большинство из них было оставлено, по отдельные местные штаммы фиксированного вируса бешенства до сих пор применяются для производства нервно-тканевых аптирабических вакцин: штамм Пекин, выделенный от собаки и фиксированный на кроликах, штамм Бабеш, выделенный от волка и фиксированный по методике Пастера (Babes).
За многие годы фиксированный вирус Пастера в различных производственных институтах прошел на кроликах тысячи интрацеребральных пассажей: в Московском институте вакцин и сывороток (ИВС) имени Мечникова с 1886 по 1956 г. — 3420 пассажей, в Сайгонском институте Пастера с 1896 по 1953 г.— 3080, в Институте Пастера в Париже с 1881 по 1956 г.— 1946 пассажей. Несмотря на строгое соблюдение условий культивирования (пассажи на кроликах 1,5 кг и др.), поддерживаемые в различных институтах мира штаммы Пастера изменились в самых различных направлениях.
Изменения коснулись инкубационного периода болезни кроликов, минимальной заражающей дозы, степени накопления вируса в мозге кроликов, патогенной активности для различных лабораторных животных при подкожном или внутримышечном введении, характера цитоплазматических включений, устойчивости к воздействию физических или химических факторов. Так, в Московском ИВС имени Мечникова этот вирус на 150-м кроличьем пассаже имел инкубацию 7 дней, на 1825-м — 5 дней, на 1889-м —4—5 дней, на 1950-м — 4 дня и на 3422-м пассаже — 3,5 дня. DLM и предельные инфекционные титры у кроликов были соответственно на 1889-м пассаже 1 : 1000 и 1:20 000, на 2799-м — 1 : 1000 и 1 : 3000 и на 3422-м пассаже — 1 : 8000 и 1 : 64 000.
По мере увеличения числа пассажей на блюдалось повышение патогенной активности для белых мышей, морских свинок при подкожном и внутримышечном введениях, на 3422-м пассаже он оказался патогенным для щенков собак при подкожном введении, но апатогенным для кроликов (А. В. Жуковский, В. А. Сура и В. П. Порай-Кошиц, Л. А. Еремина и др., Л. Т. Болтуций и др.). Штамм, поддерживаемый в Одесском институте имени Мечникова, приобрел высокую патогенную активность для кроликов при подкожном введении (Г. Б. Палавандов, Б. Г. Вайнберг).
В течение долгого времени считалось общепризнанным, что фиксированный вирус не вызывает образования телец Бабеша — Негри. Этот признак имеет большое значение для дифференциации штаммов уличного и фиксированного вирусов. Некоторые авторы сообщали о повышении негригенной активности штаммов фиксированного вируса для ряда животных. Парижский и тунисский варианты штамма Пастера образовывали тельца Негри у мышей, по их не было у собак (Levaditi, Schoen, Bequignon et al.). О негригенной активности различных вариантов фиксированного вируса Пастера сообщали многие авторы (Б. Фурсенко, А. Муратова, Г. Палавандов и др., Levaditi, Schoen, Lepine, Pasquelle).
Б. Фурсенко подчеркивал, что обнаружение телец Негри при фиксированном вирусе зависит от выбора методики окраски и фиксации препаратов.
В настоящее время эталонным вакцинным вирусом все еще остается оригинальный вирус, поддерживаемый в Институте Пастера в Париже. Комитет экспертов ВОЗ (Женева) для производства инактивированных нервно-тканевых антирабических вакцин в качестве эталонного штамма рекомендовал вирус Пастера (PV-11).
В связи с изменчивостью фиксированного вируса давно возникла необходимость в систематическом наблюдении за его свойствами. В нашей стране еще на XI Пироговском съезде была рекомендована программа изучения фиксированного вируса бешенства. Позже надзор за свойствами фиксированного вируса бешенства осуществлялся согласно инструкции Государственного института стандартизации и контроля медицинских и биологических препаратов имени Л. А. Тарасевича (ГИСК). В нашей стране с 1954 г. в качестве единого производственного вируса введен штамм Московского ИВС имени Мечникова (3420-й кроличий пассаж). С целью стабилизации и ограничения числа пассажей при ГИСК имени Л. А. Тарасевича он сохраняется в лиофилизированном виде и подвергается ежегодно не более чем 3 пассажам. Вирус рассылается производственным лабораториям и на месте может пройти не более 10 пассажей.
Фиксированный вирус бешенства имеет следующую характеристику: как правило, вызывает паралитическую форму заболевания, инкубационный период заболевания длится от 4 до 6 дней, накапливается в ЦНС мышей до 6,0—7,0 lg LD50/0,03 мл, у незаболевших животных не проникает в слюнные железы и не выделяется вместе со слюной, имеет высокую тропность к ЦНС и низкую тропность к внутренним органам.
|