Что такое штамм и изолят вируса
В биологии для описания определенного организма, который относится к царствам животных, грибов или растений, разработана своя номенклатура. Она отражает принадлежность к одному виду в зависимости от особенностей морфологии и внешнего вида. К животным применительны критерии отнесения к виду в зависимости от возможности давать плодовитое потомство при оплодотворении. Однако указанные закономерности применительны только к этим организмам, тогда как микробы не могут быть классифицированы подобным образом.
Понятие штамма в микробиологии
Вследствие наличия огромного количества организмов, имеющих морфологические свойства, но различные биохимические и иммунологические особенности, для присвоения имени невозможно применять стандартную номенклатуру. В результате этого введено такое понятие, как штамм. Это чистая культура микробов, которую удалось выделить и изолировать в определенном месте в определенный час.
Каждый микроб, который принадлежит к одному штамму, аналогичен другому такому представителю по биохимическим, морфологическим, иммунологическим и генетическим критериям. Но в пределах одного бактериального вида такой аналогии не наблюдается. Потому штамм - это более гибкое название микробной культуры. Поскольку быстрый обмен генетическим материалом (мутация) приводит к появлению новых организмов в пределах вида, но с другими свойствами, именно это определение позволяет более точно характеризовать патогенность и факторы вирулентности.
Бактериальные штаммы
Существующая номенклатура бактерий позволяет классифицировать виды организмов, однако не характеризует их новые свойства. Последние появляются вследствие быстрой мутации, приобретая новые свойства, в том числе и патогенные для человека, хозяйственных животных и растений, а также других микробов. Пример номенклатуры на примере кишечной палочки выглядит так: царство - бактерий, тип - протеобактерий, класс гамма-протеобактерий, порядок - Enterobacteriales, семейство энтеробактерий. Род - Escherichia, а вид - Escherichia colli. Однако существует множество культур бактерий вида Escherichia colli, проявляющих различные свойства. Они выделены в отдельные штаммы бактерий и имеют дополнительное название. Например, Escherichia colli O157:H7.
Сама кишечная палочка присутствует в кишечнике человека и не вызывает заболеваний, но штамм O157:H7 - исключительно патогенный за счет наличия большего количества факторов вирулентности. Она отметилась эпидемией энтеротоксигенных заболеваний в последние 5 лет.
Вирусные штаммы
Понятие штамм - это гибкое название организмов с одинаковыми свойствами, которые были выделены, а затем идентифицированы и описаны в определенной местности в определенное время. С его течением вирус может приобрести новые свойства за счет антигенного дрейфа. Это создаст новый вирусный штамм, возможно, более патогенный, чем его прародитель.
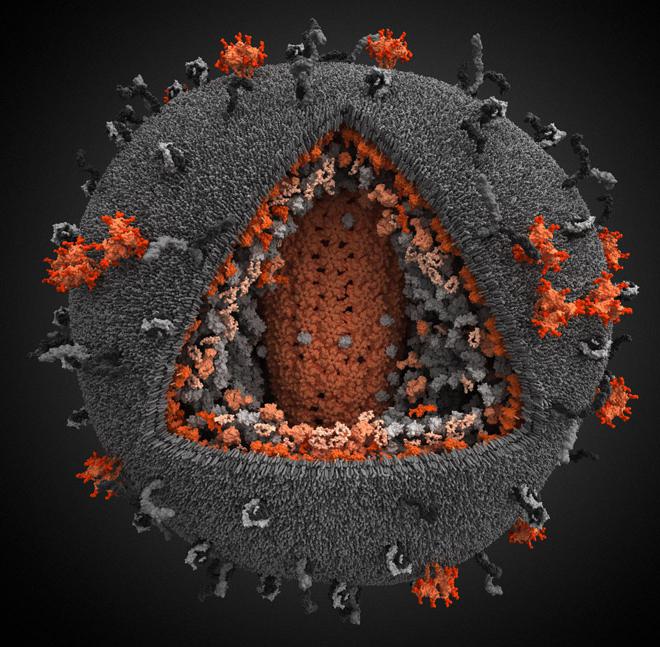
Наглядно показать появление новых штаммов можно на примере вируса гриппа. Он относится к семейству Ортомиксовирусов и называется в зависимости от антигенов (гемаглютининов и нейраминидазы) HxNy. Х и У - это числовые значения, отражающие наличие антигенов. Пример - H5N1, известный недавней эпидемией свиного гриппа с быстропрогрессирующими геморрагическими пневмониями. По теории, из данного штамма за счет того же антигенного дрейфа может развиваться новый и более опасный штамм.
Грибковые штаммы и штаммы протистов
Из всех микробов плесневые грибки являются наименее изменяемыми, хотя их биохимия также сложна. За счет более сложной структуры, чем у бактерий и вирусов, а также из-за отсутствия механизмов быстрой передачи генов количество новых грибковых штаммов увеличивается незначительно. Существует также мнение, что любой новый недавно найденный грибковый штамм - это существовавший ранее организм, который попросту не попадался исследователям.
Аналогичная ситуация обстоит и в царстве протистов. Их способность к мутации невелика, потому вероятность того, что новые штаммы появятся быстро, предельно мала. Однако новые варианты организмов одного вида все равно появляются. Потому, видимо, они также существовали ранее, но не были обнаружены.

Особенно актуальной проблема ИББ стала в 90-х годах ХХ столетия в связи с появлением в Европе и Азии высоковирулентных штаммов вируса ИББ, инфицирование которыми приводит к высокой смертности птицы. В странах Америки превалируют вариантные штаммы, которые самостоятельно не способны вызывать клиническое проявление заболевания, при этом приводят к выраженному иммуносупрессивному состоянию организма. 1
Благодаря наличию молекулярных диагностических инструментов сегодня существует возможность анализировать последовательности геномов разных полевых штаммов вируса ИББ, что позволяет выбирать наиболее подобные вакцинные штаммы для профилактики заболевания у птицы.
С 2000-х годов мы проводим скрининговые исследования для изучения молекулярно-эпизоотической ситуации с вирусом ИББ на территории Украины и стран СНГ.
Изоляты, выделенные в разное время и в разных регионах Украины, Российской Федерации, Республики Беларусь, были охарактеризованы и проанализированы. Характеристику изолятов проводили по двум основным критериям:
- Оценка генетического родства выделенных изолятов путем определения последовательности вариабельной области гена VP2.
- Оценка вирулентности каждого изолята путем заражения SPF-цыплят.
Основой антигенной изменчивости вируса ИББ являются мутации вариабельного участка гена VP2, который кодирует основной белок капсида. Изменения последовательностей этого участка гена VP2 приводят к антигенному шифту штаммов, а отдельные, так называемые, точечные мутации приводят к антигенному дрейфу с образованием новых субтипов вируса. 2
Белок VP2 является основным протективным антигеном, индуцирующим вирус-нейтрализующие антитела, которые и обеспечивают иммунитет против болезни Гамборо. 3 Следовательно, знание кода аминокислотной последовательности в вариабельной области участка VP2 украинских изолятов является ключом к оценке их генетического родства как между собой, так и с вирусными штаммами вакцинных препаратов, применяемых в Украине.
Данные рестрикционного анализа изолятов, выделенных на территории Украины, позволяют классифицировать украинские изоляты ИББ, патогенные для цыплят, на две основные группы – высоковирулентные (vv IBDV) и классические вирулентные (cv IBDV) группы штаммов вируса ИББ.
Необходимо отметить, что зафиксированные вспышки заболевания Гамборо на птицеводческих предприятиях с выраженной клинической картиной и высоким процентом смертности всегда были связаны с инфицированием птицы высоковирулентными штаммами вируса ИББ. При этом инфицирование поголовья проходило на фоне проведенных профилактических обработок птицы против ИББ, что указывает на неспособность отдельных используемых вакцинных препаратов обеспечить полноценную защиту птицы против давления высоковирулентных вирусов ИББ (vv IBDV).
Cеквенирование выделенных изолятов (определение последовательности нуклеотидов в вариабельной области гена VP2) позволило провести оценку гомологии участков VP2 между различными вирусами ИББ и установить высокую степень генетического родства среди выделенных изолятов вируса ИББ.
Полученные таким образом данные оценки молекулярно-эпизоотической ситуации по ИББ в Украине были положены в концепцию создания линейки вакцинных препаратов против болезни Гамборо на основе выделенных украинских изолятов. Так, начальный вирус для получения штамма МВ/5 (вакцинный препарат POLIMUN IBD) был выделен из фабрициевых сумок больных бройлеров птицефабрики в Донецкой области. Эффективность данных вакцин достигнута за счет максимальной степени гомологии участков гена VP2 полевых украинских изолятов по отношению к антигенному профилю вакцинных штаммов POLIMUN. За счет чего и формируется специфический поствакцинальный иммунный ответ к циркулирующим штаммам вируса ИББ.
По мнению ведущего исследователя вируса ИББ в мире D.J. Jackwood, установление степени гомологии гена VP2 полевых изолятов вируса, выделенных из бурс зараженных птиц, к различным вакцинным штаммам является необходимым, поскольку лишь максимально подобные штаммы могут защитить птицу от вируса, который циркулирует в хозяйстве. 4
В качестве примера могут служить данные филогенетического родства отдельно взятых изолятов вируса ИББ к вакцинным препаратам POLIMUN Гамборо. Топология ветвей филогенетического дерева отображает степень сходства штаммов, которые анализировались, и указывает на аминокислотные различия в вариабельном антигенно важном участке капсидного белка различных вакцинных штаммов вируса.
Пример 1.Филогенетический анализ полевого изолята, выделенного на одном из предприятий Украины (Isolate1517, 2015 г.)

Уровень гомологии разных штаммов вируса ИББ к выявленному изоляту (Isolate 1517) по результатам секвенирования.

Статистика вещь упрямая – она говорит о том, что в течение года каждый человек на планете 1-2 раза переносит инфекционное заболевание, вызванное вирусом гриппа. Уж сколько про эту болезнь, пути заражения и профилактику написано, а угрозы пандемий висят над человечеством как дамоклов меч. Под общим названием грипп мы понимаем довольно широкий спектр симптомов инфекции, связанных в первую очередь с поражением верхних дыхательных путей. Сколько вирусов гриппа выделяют сегодня эпидемиологи, чем отличаются разные штаммы возбудителя и есть ли пути эффективной борьбы с этой заразой – об этом данная статья.
Отдельное царство
Вирусы – это настолько удивительные создания, что выделены в системе органического мира в отдельное царство Vira (от лат. virus, яд). Вне клетки они представлены жизненной формой, которая носит название вирион, и только когда они попадают внутрь живой клетки, мы говорим о вирусном инфицировании. Находясь на границе живой и неживой материи, эти внутриклеточные паразиты на молекулярном, генетическом уровне включают механизмы самовоспроизведения.
Не многие знают, но вирусы открыл наш соотечественник Дмитрий Иосифович Ивановский в 1892 году. Хотя саму болезнь описал Этьен Паскье в 1403 году, назвав ее инфлюэнца, вирусы гриппа были обнаружены в 1931 году американским вирусологом Ричардом Шоупом.
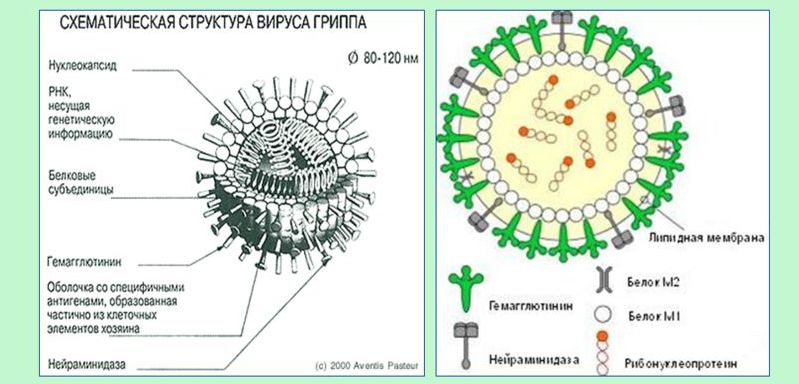
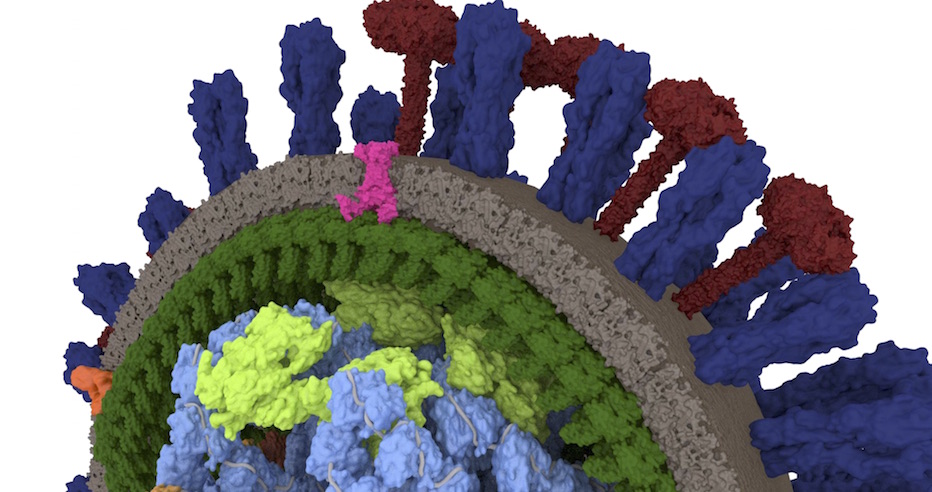
Этиология патогена
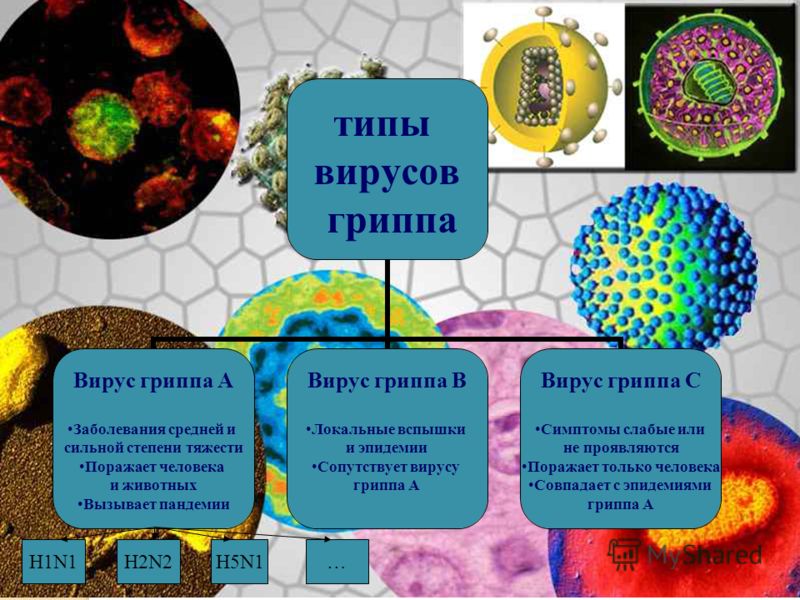
Все известные сегодня серотипы (штаммы) вируса гриппа относятся к семейству РНК-содержащих вирусов Orthomyxoviridae. Это группа ортомиксовирусов, нуклеопротеид (цепочка РНК), в их сердцевине состоит из 8 фрагментов, которые кодируют порядка 10 вирусных протеинов. Нуклеопротеид имеет постоянную структуру, и по специфичности белков выделяют типы (серотипы) вируса гриппа – А, В и С.
Специфика серотипов
Подтипов вируса гриппа типа А известно множество, и все они отличаются по поверхностным гликопротеидам. Вирусы этой группы поражают человека и многих животных (млекопитающих и птиц). При этом грипп А строго специфичен. Именно этот тип патогена вызывает болезнь средней и сильной тяжести и ответственен за возникновение пандемий и эпидемий.
Вирус гриппа B циркулирует исключительно в популяции людей. Чаще этот подтип приводит к локальным вспышкам заболеваемости, при этом болезнь протекает в легкой форме.
Самый малоизученный подтип возбудителя гриппа – это С. Инфицированию подвержены только люди, при этом симптоматика выражена слабо или отсутствует полностью. Чаще этот вирус курсирует в популяции вместе с подтипами А и В на фоне общей эпидемии.
Грипп – сложнейшая проблема медицины
И проблемы инфицирования данным патогеном становятся все более масштабными. К гриппу восприимчивы все возрастные категории и люди любого социального статуса. Влияние возбудителя гриппа на организм человека непредсказуемо, а социальный и экономический ущерб от эпидемий гриппа огромен. Все большая урбанизация, множественные трудовые и общественные контакты, общественный транспорт способствуют быстрому распространению инфекции. Способствующими этому факторами является и то, что основным источником болезни является больной с самых первых этапов инфицирования, и высокая контагиозность возбудителя.
К потенциальной пандемичности приводит и характерная особенность вируса к полному (шифт) или частичному (дрейф) мутированию. Это приводит к возникновению новых штаммов гриппа, к которым у человека нет иммунитета. Если у переболевшего гриппом типа А иммунитет сохраняется до 3 лет, к вирусу В - до 6 лет, то к его мутировавшим формам иммунитета нет. Именно такие новые вирусы гриппа и приводят к появлению эпидемий и пандемий заболевания.
Самые крупные пандемии
Грипп быстро распространяется и протекает в виде эпидемий – от локальных вспышек до пандемий, когда эпидемия охватывает несколько государств. История знает порядка 20 таких масштабных эпидемий.
Самые давние достоверные сведения о пандемии гриппа относятся к 1580 году. Начавшись на территории России, эпидемия гриппа распространилась в Европу и Африку. В Риме от гриппа умерло порядка 8 тысяч человек, а некоторые испанские города полностью исчезли.
Другая пандемия относится к 1889-1891 годам. Она унесла жизни более 750 тысяч человек и проделала путь из Средней Азии через Россию, Европу, попала в Африку и Австралию, затем перекинулась в Северную Америку и завершила свое шествие в Мексике.
Угрозы нашего века
В наше время специалисты здравоохранения бьют тревогу по поводу вируса птичьего гриппа, которых существует три главных подтипа гриппа А – Н5, Н7 и Н9. Первые два могут приводить к летальному исходу для человека. Вирус H5N1 способен переходить от диких к домашним птицам, а от них и на людей. Распространение инфекции от человека к человеку не подтверждено, но полученный при контакте с зараженными птицами он приводит к летальному исходу в 50 % случаев. Эпидемия этого вируса 2003-2008 года унесла жизни 360 человек. Сегодня случаи данного заболевания регистрируются в странах Азии среди людей, которые работают на птицефермах. Заражение происходит воздушно-капельным и контактным путем, возможно, при употреблении в пищу мяса птицы, не прошедшего должной термической обработки.
Другой подтип вируса А – свиной грипп (H1N1). Считается, что этот штамм является продуктом эволюционирования генов человека, свиней и птиц. Он передается от животных, от человека к человеку воздушно-капельным путем и при употреблении не прожаренного мяса. В 2009 году только в Москве было зарегистрировано 55 инфицирований вирусом свиного гриппа. Вспышку пандемии Всемирная организация здравоохранения объявила 11 июня 2009 года. За два года в мире от этого вируса умерло порядка 1900 человек.
Вирусологи ВОЗ постоянно проводят мониторинг циркуляции различных штаммов патогена и на основании этих данных могут предсказать вероятность потенциальных эпидемий. Так, по прогнозам в 2018 году для северного полушария повышена вероятность активности таких штаммов вируса, вызывающих грипп, как A/California/7/2009 (H1N1)pdm09 (один из подтипов свиного гриппа), A/Switzerland/9715293/2013 (H3N2) и B/Phuket/3073/2013 (линия Yamagata).

Специфика возбудителя и иммунитет человека
У большинства людей с рождения имеется иммунитет к определенным штаммам гриппа. Кроме того, особенность нашей иммунной системы – способность учиться. У людей с высоким ее статусом инфекция может быть уничтожена на ранних этапах или приведет к развитию легких форм заболевания. Но люди с низким статусом иммунитета имеют большую вероятность заболеть в период сезонных эпидемий.
Постоянная способность к мутациям возбудителя гриппа приводит к тому, что вирус может обмануть нашу иммунную систему. При инфицировании вирусом определенного штамма в организме человека вырабатываются специфические антитела, которые уже не работают на мутировавших штаммах. Именно поэтому так трудно бороться с этими коварными патогенами и так важно в случае болезни ограничить контакты для минимизации повторных заражений.
Грипп или ОРВИ
Среди всех инфекционных болезней именно эти два диагноза составляют в 95 % случаев. Все, кто болел гриппом, знают его симптоматику, которая начинается с острых респираторных проявлений. Для точной диагностики именно гриппа необходимы дополнительные лабораторные исследования, а именно смывы с носоглотки с последующим инфицированием куриных эмбрионов. Это сложный и дорогостоящий анализ. В экспресс-анализе часто применяют иммунофлюоресцентый метод (метка пораженных клеток антителами) и серологические методы диагностики (измерение изменений титра антител).
Так как же уберечься
Самый большой прорыв в вопросе изобретения лекарств от вируса гриппа – это разработки специфических вакцин. И прививки пока наилучший способ обезопасить себя от заражения, ведь в мире нет сертифицированного противовирусного препарата.
Современные вакцины трехкомпонентны – включают антигены трех вирусов, наиболее распространенных в данный период времени и на данной территории. В зависимости от технологий изготовления вакцины бывают живые и инактивированные.
Антигриппозную вакцинацию можно начинать с 6-месячного возраста, с сентября по декабрь. Эффективность прививания составляет до 90 %. И если заражение все же происходит, болезнь протекает в легкой форме. Важно помнить, что иммунитет развивается в течение 7-28 дней после прививки и сохраняется до 1 года.
И хотя с последней пандемии гриппа прошло более 30 лет, чем лечить вирус гриппа, лучше его предупредить. По крайней мере, пока ученые не нашли действенные препараты для уничтожения этого патогена.
Если все же заболели
Вероятность подхватить возбудителя из группы ОРВИ гораздо больше, чем заразиться именно гриппом. При повышении температуры тела выше 38 градусов вызывайте врача на дом. Грипп опасен своей токсичностью, и именно она приводит к развитию тяжелого течения болезни. Поэтому до прихода врача и после важным условием снижения проявлений инфекции будет постельный режим и обильное теплое питье.
Все лекарственные препараты должен назначать исключительно врач. Обычно используется терапия, включающая этиотропные (только для гриппа имеются специфические противовирусные препараты – "Тамифлу" и "Ремантадин"), иммуномодулирующие и симптоматические (жаропонижающие, противовоспалительные) препараты. Помните, антибиотики абсолютно бесполезны в борьбе с вирусами, их назначают только в случае наличия сопутствующих бактериальных инфекций.
Справиться с инфекцией в кратчайшие сроки помогут сбалансированная диета, прием витаминов (особенно С), обильное питье (способствует выводу токсинов) и постельный режим.
У данного вируса есть определенные слабые места, зная о которых можно разрабатывать индивидуальную стратегию борьбы и профилактики.
- Боязнь чистоты. Вирус гриппа чувствителен к чистоте в окружающей среде. Именно поэтому соблюдение правил личной гигиены – хорошая тактика в борьбе с инфекцией. Кроме того, вирус теряет вирулентность при химической дезинфекции. Различного рода средства такой защиты очень эффективны, даже простая обработка уксусом приводит к гибели патогена.
- Боязнь ультрафиолета. Солнечный свет убивает вирусы.
- Узкая температурная толерантность. Вирус погибает под действием высоких температур, но устойчив при низких. Так, при +4 °С он погибнет через неделю, а при -76 °С он сохранит патогенность даже через полгода. При нагревании до 50 °С вирус погибает через 3 минуты, а при кипячении он гибнет в течение 1 минуты.
- Сухость и свежесть воздуха смертельны для малоустойчивого во внешней среде возбудителя гриппа. Вентиляция и проветривание помещения – хорошие методы по борьбе с этим возбудителем.
Но главное в борьбе с данным возбудителем - все же вакцинация и правильные модели поведения в период эпидемии и не только. А это и здоровый образ жизни, достаточные физические нагрузки, личная гигиена и забота об иммунном статусе своего организма.
Прорыв есть?
Фармацевтическая компания Shionogi & Co (Япония) заявила о создании лекарства, которое уничтожает вирусы гриппа А и В в организме человека за 24 часа. Препарат Baloxavir Marboxil уже прошел клинические испытания на добровольцах, и с 2019 года его уже планируют использовать в Японии. По заявлениям фармацевтов, лишь однократный прием одной таблетки купирует выход новых вирусов из клетки и сокращает время болезни.
Раньше или позже, но ученые найдут способ эффективной борьбы с возбудителями гриппа. Но не стоит забывать и о высоких мутагенных характеристиках вирусов. В отличие от нас, людей, эти организмы существовали на нашей планете задолго до появления высших форм жизни. Поэтому пока мы ищем панацею от этой болезни, не стоит забывать и о личной гигиене. Берегите себя и своих любимых. Будьте здоровы!

Одна из самых страшных инфекций — это самый обычный грипп. Ежегодно он уносит около 250 тысяч жизней, а в отдельные годы гораздо больше. Самая масштабная из известных эпидемий гриппа — знаменитая испанка 1918 года, погубившая несколько процентов населения Земли.
Из-за накапливающихся мутаций свойства вируса гриппа постепенно изменяются. Самый заметный для нас результат мутаций — это изменения антигенных свойств вируса, то есть способности клеток нашей иммунной системы узнавать данный штамм. Такие постепенные изменения называются антигенным дрейфом. Сейчас считается, что бо́льшая часть антигенного дрейфа идет в тропических широтах, где у гриппа нет выраженных сезонных эпидемий и он держится на одном уровне в популяции человека круглый год. А вот в Северном и Южном полушариях — соответственно, в декабре–марте и в июне–октябре — каждый год возникают новые эпидемии. Обычно ВОЗ рекомендует новый состав вакцины за полгода до того, как эта вакцина реально начинает использоваться — по той причине, что ее производственный цикл довольно длинный.

Помимо постепенного антигенного дрейфа, эволюция вируса гриппа характеризуется также антигенными сдвигами — радикальными изменениями свойств вируса, которые обычно связаны с реассортацией. У вируса гриппа геном записан на восьми отдельных сегментах, немного напоминающих человеческие хромосомы. Когда клетка хозяина заражается одновременно двумя вирусными частицами двух разных штаммов, эти сегменты могут перемешаться, и может возникнуть новая вирусная частица с новыми свойствами, состоящая отчасти из сегментов одного родительского штамма и отчасти — другого. Такие реассортантные штаммы часто отличаются по свойствам от родительских штаммов и иногда приводят к большим эпидемиям. Все крупнейшие пандемии ХХ века, о которых мы знаем, — пандемии 50–70-х годов, а также, скорее всего, испанка 1918 года — вызывались, видимо, такими реассортациями, когда штаммы, приходящие из разных видов организмов, например из птиц, свиней, лошадей, перемешивались и давали что-то новое, с чем человеческая иммунная система раньше не сталкивалась.
Предсказуема ли эволюция гриппа? В краткосрочной перспективе — да. Недавние научные работы показывают, что можно отчасти предсказать будущую эволюцию вируса, если знаешь о его предыдущей эволюции. Можно, как любят эволюционисты, построить эволюционное дерево. Причем у обычного вируса гриппа А оно имеет очень характерную форму: это отдельный ствол, от которого отходят коротенькие веточки. Когда вы видите дерево такой формы, вы почти всегда можете быть уверены, что имеете дело с патогеном. Есть одна-единственная линия, которая оказывается эволюционно успешной, и она характеризуется быстрыми изменениями, так что коллективной иммунной системе человечества приходится все время стрелять по движущейся мишени. От нее ответвляются другие линии, которые в конце концов вымирают. Тем не менее некое разнообразие существует постоянно.
Эпидемии могут вызывать штаммы, присутствовавшие в популяции раньше. Например, текущая эпидемия 2016 года вызвана вирусом гриппа, впервые замеченным у людей в 2009 году. Однако обычно самые серьезные эпидемии вызываются штаммами, новыми для человека. Чтобы случилась такая эпидемия, должно произойти несколько событий. В каком-то виде животных, с которыми взаимодействует человек, должен возникнуть вариант патогена, способный заражать людей; этот вариант должен передаться человеку; наконец, как правило, он должен приобрести дополнительные мутации, позволяющие ему заражать людей эффективно. Вероятность каждого из этих событий оценить очень сложно, поэтому заранее предсказывать эпидемии мы не умеем.
От гриппа существует довольно эффективная вакцина. Но проблема в том, что она все время устаревает, поскольку каждый год вирус эволюционирует, изменяя свои антигенные свойства и становясь снова незнакомым для нашей иммунной системы. Вакцину в результате приходится постоянно обновлять. Каждый год специалисты из Всемирной организации здравоохранения (ВОЗ) рекомендуют всем производителям новый состав так называемой трехвалентной вакцины, перечисляя те три штамма, которые должны быть в нее заложены. Лучше всего трехвалентная вакцина защищает именно от них. Хотя, конечно, существует перекрестный иммунитет, и от штаммов, похожих по антигенным свойствам на эти три штамма, она будет защищать тоже неплохо. Тем не менее прививаться от гриппа нам рекомендуют каждый год, и это правильно. Трехвалентная вакцина этого года включает в себя H1N1/09, так что те, кто прививался осенью, сейчас, скорее всего, в выигрыше. Прививка не гарантирует, что вы не заболеете, но снижает вероятность этого.
При лицензировании новых живых вакцин для животных во многих странах (ЕС, США, Япония) их проверяют на отсутствие горизонтальной передачи вакцинного штамма. Проверку проводят на естественно восприимчивых животных (10 вакцинированных и 10 контактных). При совместном содержании в течение 2—4 недель о наличии или отсутствии горизонтальной передачи судят по результатам тщательного лабораторного обследования этих животных. Однако при отрицательном результате таких исследований не исключается принципиальная возможность контактной передачи вакцинного штамма при массовой вакцинации в условиях влияния множества эндогенных и экзогенных факторов.
Редкие случаи такой передачи некоторых вакцинных штаммов известны, но они не ведут к повышению вирулентности вакцинного вируса и не сопровождаются снижением эффективности вакцинации. Исключением из этого правила является живая вакцина против полиомиелита. Вакцинный штамм Сэбина полиовируса типа 1 и 3 в редких случаях оказался способным вновь обрести нейровирулент-ность и вызывать заболевание у вакцинированных или у контактировавших с ними людей. Однако это происходит с исключительно низкой частотой (около одного случая на 106—107 иммунизации) и в общем не влияет на выраженную эпидемиологическую эффективность данного препарата.
Выяснена генетическая основа этого довольно редкого повышения вирулентности полиовирусных вакцинных штаммов при репликации в кишечнике привитых.
Другое исключение состоит в том, что некоторые аттенуированные вакцинные штаммы могут довольно легко передаваться горизонтальным путем, не вызывая при этом нежелательных последствий. Однако из-за их высокой эффективности приходится мириться с циркуляцией вакцинного вируса в популяции. Таким примером могут служить некоторые вакцинные штаммы вируса ньюкаслской болезни, которые бессимптомно иммунизируют кур, находящихся в контакте с привитыми в полевых условиях. Способность некоторых аттенуированных штаммов выделяться из организма вакцинированных животных и иммунизировать контактирующих индивидуумов данной популяции считалась положительным явлением, так как облегчала формирование группового иммунитета. Вероятно, данное положение может быть приемлемым только в случае применения нереверсибельных вакцин.
Другая потенциальная опасность живых вакцин состоит в том, что вакцинные штаммы могут длительно персистировать в организме привитых. Например, известны случаи, когда вирус краснухи выделяли из лимфоцитов лиц с артритами через 6 лет после иммунизации. Известны также случаи длительной персистенции (19 мес) вакцинного штамма вируса ветряной оспы в организме привитых детей с последующей реактивацией и восстановлением вирулентности. Однако, в общем, вероятность такой ситуации очень низкая, а широкое применение живой вакцины против кори устраняет редкое, но длительное носительство полевого вируса кори.
Живые вакцины, применяемые в ветеринарии, должны использоваться только для тех видов животных, для которых они предназначены. Например, живая вакцина против чумы собак может вызывать летальную инфекцию у некоторых видов пушных зверей. Живая вакцина против болезни Ауески безопасна для свиней, но высоко вирулентна для пушных зверей.
Противоположным явлением недостаточной аттенуации является чрезмерная аттенуация вируса, при которой могут утрачиваться полезные свойства аттенуированных штаммов и практический смысл их получения. Чрезмерная аттенуация вируса кори при длительном пассировании в различных культурах клеток могла быть возможной причиной ослабления иммуногенной активности вакцины Эдмонстон-Загреб и Ленинград-16. Однако такого не произошло в опытах с вирусом осповакцины. После продолжительной персистентной инфекции выделены аттенуированные для мышей мутанты, имеющие большую делению размером 8 МД на левом конце генома и изменение нуклеотидной последовательности в другой части генома, что сопровождалось значительным изменением структуры белков оболочки (14 и 21 кД) и нуклеоида (39 кД).
Несмотря на такие изменения, аттенуированные мутанты сохраняли иммуногенность и защищали мышей от заражения летальными дозами вирулентного штамма вируса. Таким образом, глубокая аттенуация вируса осповакцины сохранялась в процессе персистенции и, несмотря на значительные изменения генома и поверхностных белков, не сопровождалась потерей иммуногенных свойств. Создается впечатление, что вирус осповакцины является исключением из правил.
Во избежание потери полезных свойств при изготовлении живых вакцин используют вакцинные штаммы только в том диапазоне пассажей, который определен для каждого из них в предварительных опытах и является гарантией безвредности и активности вакцины (обычно в течение не более 20 пассажей от матричной расплодки вируса).
Теоретически одновременное введение двух или более живых вакцин может вызывать снижение иммунного ответа за счет гетерологической интерференции вакцинных штаммов вирусов. На практике оказалось, что это зависит от конкретных вакцин. Так, одновременное применение комбинированной вакцины против кори, краснухи и паротита безопасно и эффективно. Аналогичный результат получен при одновременной иммунизации кур против болезни Марека, ларинготрахеита, ньюкаслской болезни и оспы. Однако пероральная вакцина против полиомиелита и вакцина против ротавирусной инфекции не сочеталась между собой. Также не рекомендуется использовать комбинацию живых вакцин против инфекционного бронхита, ларинготрахеита и ньюкаслской болезни.
Вероятно, все зависит от места репликации вакцинных вирусов в организме. Если места репликации вакцинных штаммов совпадают, значит будет гетероинтерференция, и такие вакцины нельзя применять одновременно.
Читайте также:


