К какому роду относятся аденовирусы
Аденовирусы (греч. aden — железа + вирусы) — группа возбудителей респираторных и других заболеваний, включающая около 50 разновидностей (серотипов), выделенных от людей, обезьян, собак, рогатого скота, грызунов и птиц. Резистентны к действию эфира и кислот, обладают общим групповым комплементсвязывающим антигеном, эпителиотропны.
Вызывая по преимуществу заболевания дыхательных путей, аденовирусы, в отличие от других респираторных вирусов, значительно чаще поражают другие системы организма: конъюнктиву, лимфатические узлы, желудочно-кишечный тракт (см. Аденовирусные болезни). Легко преодолевая желудочный барьер в связи с резистентностью к кислотам, аденовирусы интенсивно размножаются в кишечнике.
Независимо от первых исследователей Хиллеман и Вернер (1954), изучая этиологию заболеваний органов дыхания у военнослужащих, нашли, что часть заболеваний, протекающих по типу острых катаров дыхательных путей и атипичных пневмоний, связана с новым, ранее неизвестным вирусом, названным R1-67. Этот вирус удалось выделить от больных и вырастить в культуре ткани, в частности в клетках HeLa. В дальнейшем обе группы исследователей показали сходство изучаемых вирусов и нашли, что они могут быть выделены как от здоровых людей, так и от больных различными заболеваниями с преимущественным пораженцем дыхательных путей.


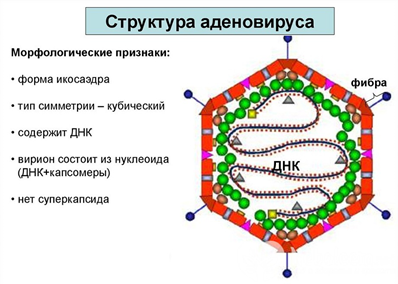
Аденовирусы имеют величину от 70 до 90 нм. Внутренняя структура вирусной частицы — вириона — состоит из наружной белковой мембраны и внутренних субъединиц величиной около 7 нм (рис. 1 и 2). Число субъединиц, называемых капсомерами, у всех исследованных аденовирус имеет постоянную величину и равно 252. Вирионы имеют кубическую исосаэдральную структуру. Аденовирусы содержат двунитчатую ДНК с молекулярным весом 20—25 млн. дальтон, составляющую 12—14% массы вириона с меньшим содержанием аденина и тимидина (43%), чем гуанина и цитозина (57%). В случае выраженной онкогенной активности (12-й и 18-й серотипы) соотношение гуанина к цитозину падает до 48—49% против 50—60% у неонкогенных аденовирусов. Белок составляет 87% массы очищенного вириона с молекулярным весом менее 35 000. Липиды, углеводы, собственные энзимы отсутствуют.
Содержание
Действие физических и химических факторов
Адновирусы инактивируются прогреванием и t° 56° в течение 5 мин. или 20— мин. при t° 50°; сохраняют активность в течение 7 дней при t°36°, 14 дней — при t° 22—23°, 70 дней — при t° 4°. Устойчивы в кислой зоне pH от 6,5 до 3,0; при pH 1,5—2,5 частично инактивируются в течение 30 мин. при t° 36 . При комнатной температуре хорошо сохраняются в зоне pH от 6,0 до 9,5, более чувствительны к повышению щелочной, чем кислой, границы pH. Резистентны к органическим растворителям (эфиру, хлороформу, флуорокарбону), а также к трипсину, папаину, рибонуклеазе, дезоксирибонуклеазе и к желчи.
Антигенная структура
С помощью хроматографии и электрофореза выделены три различных растворимых антигена, отличающихся по иммунологическим свойствам и связанных с различными морфологическими субъединицами вируса.
1. А-антиген, гексон,— групповой, общий для всех серотипов вируса антиген, локализованный в 240 капсомерах капсида, каждый из которых граничит с шестью соседними капсомерами, что определило название антигена (hexon). Антитела против очищенного гексонного антигена нейтрализуют инфекционные свойства только гомологичного серотипа. В то же время эта сыворотка реагирует в реакции связывания комплемента с любыми гетерологичными серотипами, так как в составе гексонного антигена имеются две реактивные группы, одна из которых стимулирует образование группоспецифических, а другая — типоспецифических антител.
2. В-антиген, пентон,— токсический антиген, вызывающий округление и скучивание (агрегация) чувствительных клеток однослойной культуры и отделение клеток с поверхности стекла. Локализован в капсомерах, расположенных на вершине двенадцати угловых участков вириона, каждый из которых граничит с пятью соседними капсомерами (pepton). Чувствителен к действию трипсина. Ингибирует активность интерферона (см.) и повышает тяжесть ассоциированных респираторных инфекций.
3. С-антиген — нитевой (fiber) антиген, имеет морфологически форму нити с узловым утолщением, прикрепленной к пентонному антигену. Представляет собой типоспецифический антиген, устойчив к действию трипсина, способствует адсорбции аденовирусов на эритроцитах обезьяны или крысы и их агглютинации.
Цикл размножения
Адсорбция аденовирусов на чувствительных клетках тканевой культуры занимает 4—6 час., после чего вирус проникает в цитоплазму с помощью пиноцитоза. Освобождение нуклеоида (депротеинизация) осуществляется в пиноцитарных вакуолях в течение 60—90 мин., вслед за чем вирусная ДНК транспортируется к ядру клетки. Латентный период репродукции продолжается от 13 до 15 час., когда в ядре синтезируется ДНК, а на цитоплазматических рибосомах — вирусные белки. Через 16 час. после заражения возникают зрелые структурные частицы, сборка которых происходит в ядрах клеток. Но более 10—15% вирусных ДНК и белков тканевой культуры используется для синтеза вирионов, вся остальная масса стимулирует поражения ядер клетки и нарушения синтеза клеточных ДНК и белков, с прекращением деления клеток через 10—11 час. после заражения культуры.
Максимальный выход вируса обеспечивается в случае массивного заражения и инкубации культуры до полного развития цитопатических поражений. Для получения максимального выхода вируса из достаточно сохранившихся клеток их разрушают повторным 3—6-кратным замораживанием и оттаиванием, гомогенизируют ультразвуком или механическим размалыванием. При этом концентрация вируса колеблется в зависимости от серотипа от тысяч до миллиардов частиц в 1 мл тканевой жидкости.
Клеточные поражения
Зараженные аденовирусами клетки округляются и формируют гроздевидные скопления различной величины, облегчающие распознавание агентов данной группы. Цитопатические изменения сопровождаются повышением гликолиза и скоплением органических кислот, подкисляющих тканевую жидкость.
Клеточный лизис отсутствует и зараженные клетки длительное время сохраняют жизнеспособность.


В процессе дегенерации клеток под действием аденовирусов различают две фазы (рис. 3): первая связана с токсическим эффектом, вторая — с истинным размножением вирусов, которое происходит внутри ядер и в цитоплазме. При этом аденовирусы образуют внутриядерные включения из вирусных частиц, которые составляют агломераты кристаллоподобного строения (рис. 4).
Электронномикроскопические исследования Перейры и Валентина (Н. G. Pereira, R. С. Valentine, 1958) показали, что одна цитопатогенная доза вируса содержит от 10 до 103 вирусных частиц.
Размножение в перевиваемых линиях клеток КВ, HeLa, а также в почечных культурах обезьян под агаровым покрытием сопровождается формированием видимых глазом колоний (бляшек) в районе пораженных клеток.
Гемагглютинирующие свойства
Все серотипы аденовируса человека, кроме типа 18, способны агглютинировать эритроциты обезьян резус или крыс. По этому признаку аденовирусы можно классифицировать на следующие четыре подгруппы: первая включает девять серотипов (3, 7, 11, 14, 16, 20, 21, 25, 28), агглютинирующих только эритроциты обезьян; вторая включает двенадцать серотипов (8, 9, 10, 13, 15, 17, 19, 22, 23, 24, 26, 27), агглютинирующих эритроциты крыс; третья — шесть серотипов (1, 2, 4, 5, 6, 12), агглютинирующих эритроциты крыс после взаимодействия с иммунной аденовирусной сывороткой против других типов (например, 6 типа); четвертая включает серотип 18, не способный к гемагглютинации.
Патогенность для человека и животных
В отличие от других респираторных вирусов, аденовирусы размножаются не только в цилиндрическом мерцательном эпителии верхних дыхательных путей, трахеи и бронхов, но и в под слизистой оболочке. С участием аденовирусов наиболее часто связано развитие острой респираторной инфекции, протекающей с явлениями ангины, фарингита, кашля, озноба, боли в мышцах, головной боли, при непостоянном насморке и повышении температуры (см. Аденовирусные болезни, Респираторные вирусные болезни).
Наиболее частыми возбудителями оказались первые семь серотипов, а также типы 14 и 21. У грудных детей часто развиваются тяжелые пневмонии, изредка с детальным исходом, вызванные серотипами 1, 2, 3, 7 и 7а.
Еще недавно считалось общепризнанным положение об отсутствии у аденовирусов человека патогенности для животных.
Многочисленные опыты заражения многих видов млекопитающих, включая обезьян, давали либо отрицательные, либо сомнительные результаты. Это остается справедливым для обычных условий получения экспериментальной инфекции, однако при изменении методов исследования получены новые данные. Дженнингс и Беттс (A. R. Jennings, А. О. Betts, 1962) адаптировали аденовирусы 1, 2, 4 и 6 серотипов к культуре ткани свиной почки. Затем интратрахеально заражали поросят, рожденных и выращенных в стерильных условиях в безмикробной внешней среде. На 4-й день после заражения у большинства животных развилась бронхопневмония с выраженной лимфоидной гиперплазией.
Интраназальное или подкожное заражение взрослых сирийских хомяков, собак, кроликов, а также новорожденных мышей и крыс вирусами 3, 4, 5, 7, 12, 18 типов приводило к развитию бессимптомных инфекций.
Заражение новорожденных хомяков серотипом 5 вызывало, по данным Перейры, смерть животных через 4 дня с типичными поражениями легких и выделением вируса. Патогенность для обезьян выделяющихся от них аденовирус не доказана.
В ряде лабораторий нередко выделяются аденовирусы от больных вирусным гепатитом как из кала, так и из крови. Возможно, аденовирусы являются спутниками истинного возбудителя, но нельзя исключить и наличие у некоторых штаммов определенного гепатотропизма. Заслуживает внимания работа Л. Г. Руденко и др. (1972), где показана восприимчивость новорожденных хомяков в возрасте до 5 суток к аденовирусу 1 типа (штамм 1237) при подкожном заражении. У зараженных хомяков развивается гепатит и происходит избирательная репродукция вируса в печени.
Онкогенные свойства
Способность аденовирусов человека вызывать развитие злокачественных опухолей (сарком) у новорожденных сирийских хомяков, зараженных подкожно массивной дозой активного вируса, впервые выявлена у серотипа 12. Онкогенные свойства подтверждены сейчас у семи других типов аденовирусов человека, а также у шести типов от обезьян и у одного от птиц. Наибольшую активность проявили серотипы 12, 18 и 31; тип 12 вызывал опухолевый рост, помимо хомяков, также у новорожденных крыс, диких африканских грызунов Mastomys и некоторых линий мышей. В образовавшихся опухолях инфекционные частицы аденовирусов отсутствовали.
Злокачественная трансформация клеток наблюдалась также в опытах in vitro при заражении типом 12 нормальных эпителиальных клеток культуры почек новорожденных сирийских хомяков, а также фибробластов зародыша крысы. Через 3—10 нед. после инокуляции культур массивной дозой вируса развивался рост опухолевых клеток, свободных от инфекционного вируса. Клетки, трансформированные in vivo или in vitro, содержали два новых антигена: Т-антиген (неоантиген) и трансплантационный (TSTA) антиген. Их продукция индуцируется частью ДНК опухолеродного А. Весьма большой мол. вес ДНК аденовируса (более 20 млн. дальтон) обеспечивает возможность кодирования синтеза более 50 различных белков. Т-антиген, обнаруживаемый нерегулярно в ранние этапы обычной цитолитической инфекции, постоянно присутствует в опухолевых клетках и стойко передается при их культивировании in vitro. Обнаруживается в реакции связывания комплемента и по иммунофлуоресценции с сыворотками хомяков с развивающейся опухолью, которые не взаимодействуют со структурными белками вирусов. Т-антиген малоустойчив к нагреванию, воздействию кислоты и щелочи, не содержит РНК или ДНК, имеет мол. вес 78 000 дальтон.
По антигенным свойствам различают Т-антиген группы А (высокоонкогенные аденовирусы 12, 18 и 31 серотипов) и группы В (слабоонкогенные аденовирусы 3, 7, 11, 14, 16 и 21 серотипов). Попытки обнаружить Т-антиген групп А и В в опухолевых клетках и гомологичные для них антитела в сыворотках людей, болеющих раком различной локализации, дали отрицательный результат. В опухолевой ткани хомяков этот антиген присутствует в весьма высокой концентрации и легко обнаруживается с помощью флуоресцирующих антител в каждой опухолевой клетке.
Выделение аденовирусов осуществляется заражением чувствительных тканевых культур отделяемым из полости носа, зева, конъюнктивы, а также кишечным содержимым. Аденовирусы лучше размножаются (с развитием характерных цитопатических изменений) в перевиваемых эпителиальных культурах (HeLa, КВ, НЕр-2), а также в первичной культуре эмбриональной почки человека; слабее размножаются в первичных эпителиальных культурах человеческой трахеи, амниона, почечной ткани обезьян и кроликов. Оптимальный метод выделения — заражение первичной клеточной культуры эмбриональной почки человека с пассажами на перевиваемых линиях после адаптации вируса.
Серологическая идентификация выделенных штаммов
Для отнесения к группе аденовирусов выделенные агенты дифференцируются иммунологически путем установления общего группового антигена в РСК или в реакции преципитация (по методу диффузия в агаровом геле). Определение серотипа проводится с помощью реакции торможения гемагглютинации или нейтрализации. Для идентификации серотипа выделенного штамма определяют его принадлежность к одной из четырех подгрупп по гемагглютинации, после чего ставят реакцию торможения гемагглютинации (РТГА) с иммунными сыворотками кроликов или лошадей, обработанными каолином и истощенными чувствительными для данной подгруппы эритроцитами. Результаты РТГА проверяют в реакция нейтрализация на тканевых культурах с гомологичной иммунной сывороткой (см. Вирусологические исследования).
В современной классификации вирусов человека аденовирусы занимают самостоятельное положение среди ДНК-содержащих вирусов, четко дифференцируясь от других сочленов этой группы по свойствам вирионов.
Библиография
Руденко Л. Г. и др. Динамика репродукции аденовируса в печени новорожденных хомяков и изменение гуморальных факторов иммунитета при экспериментальном аденовирусном гепатите, Вопр. вирусол., № 3, с. 269, 1972; Смородинцев А. А. и Коровин А. А. Грипп, с. 73, Л., 1961, библиогр.; Шубладзе А. К. и др. Некоторые итоги изучения штаммов вирусов, выделенных от больных эпидемическим гепатитом, Всстн. АМН СССР, № 6, с. 49, 1963; Buescher Е. L. Respiratory disease and adenoviruses, Med. Clin. N. Amer., v. 51, p. 779,1967; Enderb J. P. a. o. Adenoviruses, Science, v. 124, p. 119, 1956; Ginsberg H. S. Identification and classification of adenoviruses, Virology, v. 18, p. 312, 1962, bibliogr.; Hilleman M. R. a. Werner J. H. Recovery of a new agent from patients with acute respiratory illness, Proc. Soc. exp. Biol. (N. Y.), v. 85, p. 183, 1954, bibliogr.; HuebnerR. J., Rowe W. P. a. Сhanосk R. M. Newly recognized respiratory tract viruses, Ann. Rev. Microbiol., v. 12, p. 49. 1958, bibliogr.; Pereira H. G. a. Valentine R. C. Infectivity titrations and particle counts of adenovirus type 5, J. Gen. Microbiol., v. 19, p. 178, 1958, bibliogr.; Rose H. M. Adenoviruses, в кн.: Diagnostic rocedures for viral a. ricket. infections, ed. у E. H. Lennette a. N. J. Schmidt, p. 205, N. Y., 1969;Rosen L. Hemagglutination-inhibition techniques for typing adenoviruses, Amer. J. Hyg., v. 71, p. 120, 1960; Sohier R., C hard onnet Y. a. Prunieras M. Adenoviruses. Progr. med. Virol., v. 7, p. 253, 1965, bibliogr.
Что такое аденовирусы?
Аденовирусы — это вирусы, геном которых состоит из двухцепочечной ДНК. Они принадлежат к роду Мастаденовирусов (лат. Mastadenovirus). Аденовирусы показывают высокую устойчивость к факторам окружающей среды. На сегодняшний день идентифицировано 51 серотипов аденовирусов, но только треть из них являются патогенными для человека. Доказано, что некоторые серотипы являются онкогенными у грызунов, но пока не было продемонстрировано никакой связи между аденовирусами и трансформацией их в опухоли у человека.
В настоящее время ведутся исследования по использованию аденовирусов в качестве ДНК-вектора в генной терапии. Аденовирусные инфекции поражают дыхательную, пищеварительную и зрительную системы. Они могут быть особенно опасны для новорожденных и людей с ослабленным иммунитетом. Заражение обычно происходит капельным или фекально-оральным путем. Резервуаром вируса является человек.
Распространению инфекции способствует такие места, как детские сады, ясли, интернаты, больницы и военные казармы.
В результате контакта с полотенцами больных людей, использования контактных линз или плавательных бассейнов может возникнуть конъюнктивальная инфекция (конъюнктивит). Оставление инфекции на определенном серотипе вируса создает постоянную устойчивость к этому конкретному серотипу (но не к другим).
Инфицирование происходит через слизистые оболочки дыхательных путей, желудочно-кишечного тракта, конъюнктивы и роговицы.
Аденовирусы также обладают особым сродством к лимфоидной ткани, и в инфицированных тканях и органах образуются инфильтраты лимфоцитов.
Как часто встречаются аденовирусные инфекции?
Аденовирусные инфекции распространены и заражают людей во всем мире. Человек заражается ими в первые годы жизни — обычно от 6 месяцев до 5 лет. Специфические антитела к различным серотипам аденовируса можно обнаружить практически у всех взрослых, что указывает на наличие инфекции в детском возрасте.
В странах с умеренным климатом аденовирусная инфекция наблюдается в течение всего года. Эпидемии инфекций дыхательных путей чаще всего происходят зимой, весной и в начале лета. Около 5% инфекций верхних дыхательных путей и 10% пневмоний у детей раннего возраста обусловлен аденовирусами.
Как проявляются аденовирусные инфекции (симптомы и признаки)?
Инкубационный период аденовирусных инфекций обычно составляет 2—14 дней, а их течение обычно умеренное. Чаще всего они относятся к дыхательной, пищеварительной и зрительной системам.
Повреждения кожи также являются типичным симптомом аденовирусных инфекций. В зависимости от серотипа вируса и возраста пациента наблюдаются различные клинические синдромы, подробно описанные ниже.
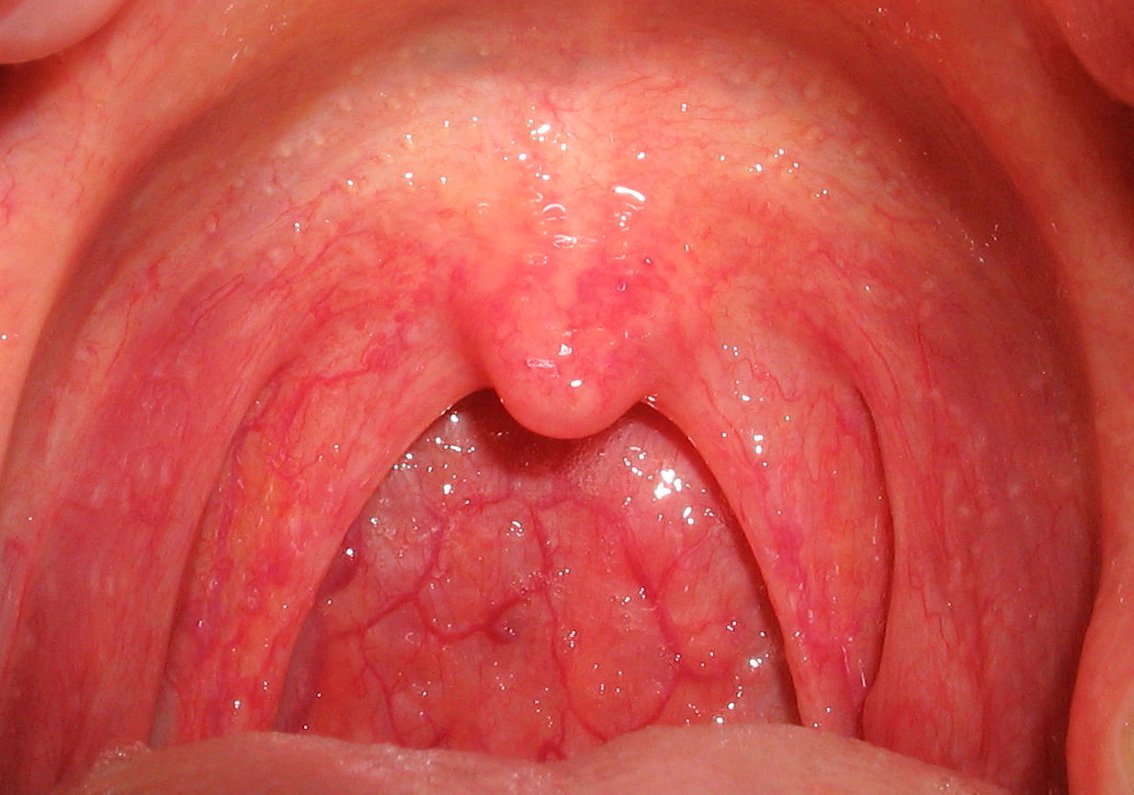
Наиболее распространенной клинической формой является острая инфекция верхних дыхательных путей, включая фарингит, ринит и лихорадку. Отдельным синдромом заболевания является лихорадка с фарингитом и конъюнктивитом. Этот синдром может возникать в виде единичных случаев, но часто наблюдается как эпидемия среди детей, проживающих в колониях, лагерях и пользующихся бассейнами. Инкубационный период составляет 6-9 дней.
Заболевание протекает с симптомами фарингита, ринита, лихорадки, опухшей шейной лимфаденопатии и неуправляемого конъюнктивита, сначала одностороннего, а затем двустороннего. Симптомы длятся 3—5 дней и обычно исчезают без осложнений. Возможен вторичный бактериальный конъюнктивит. Заражение аденовирусами может происходить в виде псевдобластического синдрома с пароксизмальным кашлем. Инфекция нижних дыхательных путей у младенцев и детей младшего возраста происходит в виде бронхита и пневмонии.
Аденовирусная инфекция у взрослых (особенно у новобранцев в армии) может вызывать острый респираторный синдром с высокой температурой, ознобом, головной болью и мышечными болями, опухшими лимфатическими узлами на шее, сухим кашлем, фарингитом, ларингитом, бронхитом и пневмонией.
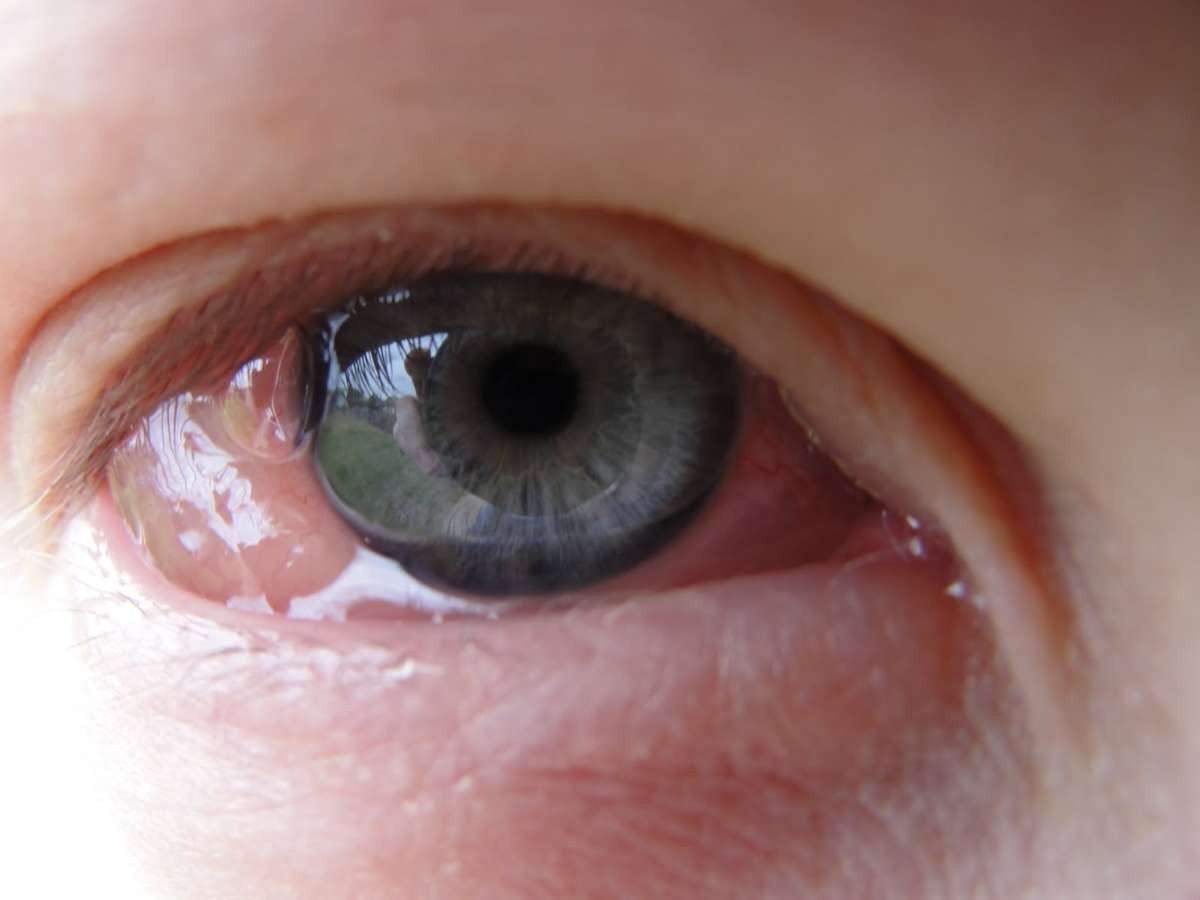
Аденовирусы являются одной из основных причин конъюнктивита и кератита (включая эпидемический конъюнктивит). Инкубационный период составляет 8-10 дней. Инфекция передается в офтальмологических отделениях, при использование контактных линз, общих полотенец, использование бассейнов или зон для купания. Течение болезни одностороннее, а затем двустороннее.
Конъюнктивит может быть геморрагическим. Кератит может привести к помутнению роговицы. Заболевание сопровождается:
- опухшими веками;
- светобоязнью;
- слезотечением и болезненностью глазного яблока.
Также распространены воспаление околоушных лимфатических узлов и лихорадка.
Геморрагический цистит, вызванный аденовирусами, встречается в основном у детей в возрасте 6–15 лет. Заболевание имеет внезапное начало, возникает при гематурии. Однако бактерии в моче, лихорадки или проблем с почками не наблюдаются.

Острый гастроэнтерит у детей имеет аденовирусную этиологию в 5–9% случаев. Аденовирусы являются частой причиной внутрибольничных пищевых инфекций. Желудочно-кишечные симптомы могут сопровождаться респираторными жалобами. По оценкам, половина детей в возрасте до 5 лет имеют антитела против типов вируса, вызывающего желудочно-кишечный дискомфорт. Бессимптомный носитель аденовирусов в желудочно-кишечном тракте также часто обнаруживается.
В редких случаях (в основном у людей с нарушенным иммунитетом) аденовирусные инфекции могут вызывать менингит и энцефалит, миокардит, воспаление печени и почек.
Что делать, если вы испытываете симптомы аденовирусной инфекции?
Если вы испытываете какие либо вышеописанные симптомы, пожалуйста, обратитесь к врачу.
Как врач определяет диагноз аденовирусной инфекции?
Большинство аденовирусных инфекций — это легкие инфекции, диагностируемые на основании клинических симптомов.
Лечения аденовируса
Лечение аденовирусных инфекций предполагает использование симптоматических и поддерживающих препаратов.
В настоящее время вопрос о специфической терапии аденовирусной инфекции, кроме поддерживающего и симптоматического лечения, остается предметом дискуссий. К счастью, большинство инфекций самоограничены в условиях нормального иммунного ответа и не требуют специальной терапии.
Пациентам с ослабленным иммунитетом для лечения аденовирусных инфекций назначают несколько препаратов, таких как:
Большинство из этих агентов являются виростатическими, могут вызывать лекарственную устойчивость и иметь значительный риск токсичности.
Можно ли полностью вылечить аденовирусную инфекцию?
Аденовирусные инфекции, как правило, легкие и полностью излечиваются. Аденовирусные инфекции могут быть опасны у людей с ослабленным иммунитетом и после пересадки органов. У этих пациентов могут быть полиорганные инфекции, пневмония, гепатит, менингит и энцефалит, а также диарея.
Что делать после прекращения лечения аденовирусной инфекции?
В большинстве случаев пациенты не требуют последующего наблюдения после лечения. Только людям с кератоконъюнктивитом и тяжелой пневмонией требуется контроль после лечения.
Что делать, чтобы избежать аденовирусной инфекции?
Во избежание заражения соблюдайте стандартные правила гигиены. Доступных прививок или других методов для снижения риска аденовирусной инфекции нет.
Семейство Adenoviridae (от греч. Adenos — железа) — большая группа вирусов, поражающая млекопитающих и птиц. Впервые аденовирусы были выделены в 1953 г. из миндалин и аденоидов детей.
Вирионы аденовирусов имеют икосаэдрическую (двадцатигранную) структуру и состоят из капсида и сердцевины, суперкапсидной оболочки нет. Капсид вирионов имеет диаметр 70—90 нм и состоит из 252 капсомеров, из которых 240 — гексоны (они образуют 20 поверхностей) и 12 пентоны. Пептоны расположены на вершинах икосаэдра и состоят из основания и длинного отростка (нити). Каждый пентон окружен пятью капсомерами, гексон — шестью соседними капсомерами. Сердцевина вирионов аденовирусов состоит из ДНК и четырех внутренних белков.
Геном аденовирусов содержит одну линейную двуспиральную молекулу ДНК с молекулярной массой 20—25 МД (35 000—36 500 пар нуклеотидов). Каждый 5′-конец молекулы ДНК ковалентно связан с терминальным белком (55 кД). Вероятно, он кодируется геномом вируса и играет важную роль в репликации ДНК. ДНК вируса инфекционна.
В вирионах аденовирусов содержится 13—14 полипептидов с молекулярными массами от 5 до 120 кД. В состав капсида входит 7 полипептидов: II, III, IIIa, IV, VI, VIII и IX.
Полипептид II содержится в гексонах, которые составляют основную массу белка вирионов (53 %) и имеют сложную антигенную структуру. В составе гексонов обнаружены две антигенные детерминанты, одна из которых индуцирует синтез группоспецифических, а другая — типоспецифических антител, нейтрализующих инфекционную активность вируса. Пентоны токсически действуют на клеточные культуры. Цитоплазматическая активность связана с основанием пентона (полипептид III). Нити пентонов (полипептид IV) отвечают за адсорбцию вирионов на клеточной поверхности и образование антител, обладающих вируснейтрализующей активностью.
В сердцевине вирионов содержатся четыре изученных белка: V, VII, X и 55 кД. Кроме этого, в вирионах в незначительных количествах содержатся полипептиды XI и XII, локализация и функции которых пока не ясны.
В состав вирионов аденовирусов входит 86—88 % белка и 12—14 % ДНК. Основная масса белков вириона приходится на капсид, на долю сердцевины — около 20 %. Молекулярная масса вирионов 170—175 МД, плавучая плотность в CsCl 1,328—1,390 г/см 3 , коэффициент седиментации около 560S.
Подразделение аденовирусов на серотипы основано на результатах реакции нейтрализации и торможения гемагглютинации (если вирус обладает гемагглютинируюгцей активностью).
Различные штаммы аденовирусов крупного рогатого скота обладают неодинаковой гемагглютинирующей активностью, которая зависит от вида и концентрации эритроцитов, температуры и pH среды.
По гемагглютинирующему признаку аденовирусы человека разделены на три подгруппы (А, В, С). Пока нет доказательств роли аденовирусов в возникновении опухолей у людей и домашних животных. В то же время доказано, что некоторые аденовирусы онкогенны для различных грызунов. Аденовирусы человека по онкогенным свойствам Хюбнер разделил на три группы: высокоонкогенные — А, слабоонкогенные — В и неонкогенные — С, соответственно их способности индуцировать злокачественные опухоли при инокуляции новорожденным хомякам.
В клетках аденовирусы размножаются с участием ядра клетки. Нити пентона отвечают за адсорбцию на клетку вируса, который проникает внутрь клетки путем виропексиса (эндоцитоза). После проникновения вирионы теряют пентоны с отростками и быстро достигают околоядерной зоны, где они освобождаются от капсида, и дезоксирибонуклеопротеид проникает в ядро через поры ядерной мембраны. Транскрипция и трансляция ДНК происходят в ядрах инфицированных клеток с участием клеточных полимераз. Структурные белки аденовирусов, синтезированные в цитоплазме (на рибосомах) клетки, мигрируют в ядра, где осуществляется сборка вирионов. Аденовирусы выходят из клеток в незначительном количестве. Даже при полном разрушении монослоя в культуральной жидкости находят около 10% синтезированного вируса. В зараженных клетках наряду с полными вирионами синтезируются и дефектные частицы, ДНК которых оказалась на 3 % короче стандартной вирусной ДНК. Аденовирусы индуцируют образование внутриядерных телец-включений.
Семейство Adenoviridae включает два рода: Mastadenovirus и Aviadenovirus.
Род Mastadenovirus (от греч. mastos — молочная железа). В состав рода входят аденовирусы млекопитающих: человека — 51 серотип; обезьян — 27; крупного рогатого скота — 10; свиней — 5; овец — 6; коз — 1; лошадей — 2; собак — 2; мышей — 2; землеройки — 1 серотип. Прототипный вирус — аденовирус С человека.
Род Aviadenovirus (от лат. avis — птица). В состав рода входят аденовирусы птиц: кур — 12 серотипов; индеек — 3; уток — 2, фазанов — 1 серотип. Прототипный вирус — аденовирус I (CELO) кур.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Читайте также:
|


