Как увидеть тело вируса
" title="Рисунки Владимира Орехова"/>
Все сейчас говорят о вирусах: коронавирус, грипп, ВИЧ, гепатит, ВПЧ, оспа и т.д. В мире существует более тысячи видов вирусов, способных поражать различные живые клетки, да практически все виды клеток. А что же такое вирусы и с чем их едят (в прямом и переносном смысле)? Где они живут, как попадают к нам в организм, что там делают и есть ли лекарства против них? Статей и постов в интернете много, в том числе, антинаучных и дилетантских. Поэтому ТИА обратилось за информацией в Тверской медуниверситет, к профессору кафедры микробиологии и вирусологии, доктору медицинских наук, декану фармацевтического факультета Юлии Червинец.
Что такое вирус и в чём отличие от бактерий?

Название "вирус" произошло от латинского слово virus и переводится как "яд". По сути, это мельчайшие внутриклеточные микробы-паразиты, потому что живут и размножаются они только внутри хозяина - практически во всех живых организмах (бактериях, грибах, растениях, животных и человеке). Несмотря на своё "коварство", все вирусы имеют примитивное строение: одна нуклеиновая кислота (ДНК или РНК), окруженная одной или несколькими оболочками. Различают просто устроенные вирусы (безоболочечные) и сложно устроенные вирусы (оболочечные). К простым вирусам относят: вирусы полиомиелита, гепатита А, аденовирусы. Примеры сложных вирусов: гепатит В, грипп, парагрипп, корь, ВИЧ, герпес. Различаются вирусы и по форме:
- палочковидная (вирус табачной мозаики)
- пулевидная (вирус бешенства)
- сферическая (вирусы полиомиелита, ВИЧ)
- нитевидная (филовирусы)
- в виде сперматозоида (многие бактериофаги).
Размеры вирусов настолько малы (18-400 нм), что увидеть их можно только с помощью электронного микроскопа. Единицы измерения - нанометры, в отличие от бактерий (микрометры, мкм). Кстати, вирусы приблизительно в 100 раз меньше бактерий. Наиболее мелкими вирусами являются вирус полиомиелита (20 нм), гепатита А (30 нм), гепатита С (50 нм), вирус бешенства (170 нм), наиболее крупным — вирус натуральной оспы (350 нм).
От бактерий вирусы отличаются не только размерами, но и количеством генов (минимальное у вирусов от 4 до сотни, у бактерий – от 3000); нуклеиновыми кислотами (вирусы содержат только одну - ДНК или РНК, а бактерии – обе); количеством ферментов и, конечно же, самой формой жизни: вирусы размножаются только внутри живых существ, а бактерии – свободноживущие.
Интересный факт: первооткрыватель вирусов и основоположник вирусологии - русский ученый Д.И. Ивановский. В 1892 году описал необычные свойства возбудителей болезни табака (табачной мозаики), которые проходили через бактериальные фильтры и были названы "фильтрующимися частицами".
Жизненный цикл вирусов состоит из нескольких этапов:

1. Вирус прикрепляется к поверхности чувствительной клетки. Для каждого вируса есть свои чувствительные клетки, например, для гепатита – клетки печени, для гриппа – клетки дыхательных путей и т.д.
2. Проникновение вируса в клетку: либо его оболочка сливается с мембраной клетки или клетка сама его захватывает и поглощает.
3. Далее в клетке идёт процесс как бы “раздевания” вируса от всех его оболочек и активация его нуклеиновой кислоты.
4. Начинается синтез нуклеиновых кислот и белков вируса, т.е. вирус подчиняет системы клетки хозяина и заставляет их работать на своё воспроизводство.
5. Сборка вируса — многоступенчатый процесс, включающий в себя соединение всех компонентов.
6. Последний этап - выход вирусных частиц из клетки взрывным путем или почкованием. Полный цикл размножения вирусов завершается через 5-6 ч (вирус гриппа) или через несколько суток (вирус кори). Из погибающей клетки, которая длительное время может сохранять жизнеспособность, одновременно выходит большое количество вирусов. В результате пораженные вирусом клетки в основном погибают от истощения, а новые вирусы завоевывают и разрушают другие клетки. Но возможна и так называемая онкогенная трансформация клетки: тогда в организме появляется и начинает расти из мутированных клеток раковая опухоль.
Сколько вирус может жить вне организма хозяина и где?
Как правило, большинство вирусов малоустойчивы во внешней среде: они становятся инертны и погибают от многих причин, если снова не попадут в чувствительную клетку. Некоторые вирусы во внешней среде могут образовывать кристаллы, что свойственно только неживой материи.
Вирусы быстро погибают под действием солнечных лучей, ультрафиолета, стандартных веществ для дезинфекции. В воздухе помещений вирусы могут сохраняться несколько часов. При кипячении полностью инактивируются в течение нескольких минут.
Однако вирусы устойчивы к низким температурам: сохраняют свою жизнеспособность при t +4°С в течение нескольких недель, а при замораживании - в течение нескольких месяцев, а иногда и лет (особенно супернизких температурах).
Устойчивость вируса на различных поверхностях различна и зависит от температуры. На бумаге вирус разрушается за 3 часа, на банкнотах - за 4 дня, на дереве и одежде - за 2 дня, на стекле - за 4 дня, на металле и пластике - за 7 дней. Кстати, на внутреннем слое использованной маски они могут жить 7 дней, а на внешней поверхности маски – даже более недели (данные соответствуют условиям при температуре +22 °С и влажности 65 %).
Есть и исключения. Некоторые вирусы обладают значительной устойчивостью при комнатной температуре: вирус гепатита В сохраняет жизнеспособность в течение трех месяцев, гепатита А – в течение нескольких недель. ВИЧ сохраняется в высохшей крови до двух недель, в донорской крови вирус остается жизнеспособным в течение нескольких лет.
Что такое штаммы и почему вирусы мутируют?
Штамм (от нем. Stamm - "ствол,род") — чистая культура вирусов, изолированная в определённое время и в определённом месте. Один и тот же штамм не может быть выделен второй раз из того же источника в другое время. В зависимости от среды обитания – почва, вода, воздух, время года, чувствительный организм (человек, животные, птицы) - вирусы подразделяют на штаммы. Например, водный штамм, весенний, птичий, свиной и т.п. Во внешней среде геном вируса подвержен различным воздействиям, например, ультрафиолетовое облучение, солнечная радиация, химические вещества, что приводит к различного рода мутациям, т.е. изменениям в структуре нуклеиновой кислоты. В зависимости от характера мутаций вирусы могут изменять свои свойства, скажем, сменить хозяина. Так, вирус гриппа, который поражал только птиц, стал поражать и людей.
Как часто происходит в мировом научном сообществе открытие нового вируса?
Ученые каждый год открывают новые вирусы. Так, в 1972 г. открыт вирус Эбола, 1980-1989 гг. - вирусы иммунодефицита человека, гепатита Е и С, коронавирус человека впервые был выделен в 1965 году от больных ОРВИ. В Китае 2002—2003 годах была зафиксирована вспышка атипичной пневмонии или тяжелого острого респираторного синдрома (ТОРС, SARS). Заболевание было вызвано штаммом коронавируса SARS-CoV. В результате болезнь распространилась на другие страны, всего заболело 8273 человека, 775 умерло (летальность 9,6 %). И вот в 2019 году появился новый штамм коронавируса CoViD 19, который вызвал пандемию.
Так откуда берутся вирусы?
Вопрос риторический. Пока ответа у науки нет. Может быть, они были привнесены из космоса на космических телах. Ведь при низких температурах они могут сохраняться неопределенно долгое время.
Как они попадают в организм человека/животного и т.д.?
Разными путями: воздушно-капельным (корь, грипп, ветряная оспа), половым (ВИЧ, вирус простого герпеса 2 типа), через кровь (гепатит В,С, ВИЧ), через инфицированные продукты (гепатит А, Е) или через членистоногих (скажем, клещей). Различают вирусы, вызывающие инфекции с преимущественным поражением органов дыхания (респираторные), кишечника (ротавирусы), печени (вирус гепатита), иммунной (ВИЧ) или нервной системы (бешенство, энцефалит).
Как организм реагирует на вирус?

Частицы самого вируса, а также биологически активные вещества, выделяющиеся при разрушении наших клеток, могут вызвать повышение температуры тела, тошноту, рвоту, сильную слабость, головокружение вплоть до потери сознания, нарушение работы сердечно-сосудистой системы и др. На фоне нарушения функционирования различных органов и систем к вирусной инфекции может присоединиться бактериальная (стафилококки, стрептококки, кишечные бактерии) и грибковая (дрожжевые грибы), усугубив воспалительный процесс с тяжелыми последствиями вплоть до летального исхода.
Как наш организм борется?
Однако организм человека не простая мишень для атаки болезнетворных микроорганизмов, он активно борется, и в этом нам помогает иммунная система. Вырабатываются специфические, нейтрализующие данный вирус антитела, формируются клетки-"убийцы" или Т-лимфоциты, которые уничтожают как поражённые, инфицированные клетки, так и сам вирус. Но иммунной системе нужно время, чтобы вычислить "чужака", "вирусного преступника", который не просто прячется внутри наших клеток, но и старается обмануть иммунную систему. Например, новое или мутировавшее поколение вируса наша иммунная система поначалу не видит. Конечно же, со временем все вирусные клетки распознаются, но к сожалению, с потерей драгоценного времени для нашего организма.
Возможно ли повторное заражение одним и тем же вирусом?
Наше здоровье зависит напрямую от активности и лабильности иммунной системы. Если она работает со сбоями и не справляется с негативным воздействием патогенов, заболевание может перейти в хроническую форму вплоть до смертельного исхода. Поэтому повторное заражение этим же вирусом возможно. Другая причина появления рецидива заболевания - мутации вируса. Если вирус стабилен, то наша иммунная система запоминает его и, как правило, повторных случаев инфицирования не бывает. Но если вирус подвергается изменчивости, то попав в организм человека, он воспринимается уже как новый вирус.
Есть ли лекарственные препараты для лечения вируса? Что может убить вирус?
Да есть, но не против всех вирусов. Антибиотики, применяемые при лечении бактериальных инфекций, здесь совершенно не работают, т.к. они воздействуют на структуры клетки только бактерий. В случае вирусной инфекции нужны препараты, которые блокируют различные этапы размножения вируса в клетке. Таким неспецифическим веществом является интерферон, который вырабатывается клетками организма человека (кишечника, печени).
Если выработка интерферона недостаточна, то можно применить индукторы интерферона, например: ламовакс, курантил, дибазол, адаптогены растительного (элиутерококк, оралия) и животного происхождения (вытяжка из мидий). Активно действуют при респираторных вирусных заболеваниях препараты интерферона - виферон, амиксин и др. Подавляют активность вируса гриппа на ранних стадиях ремантадин, амантадин, арбидол. Герпес подавляет ацикловир (зовиракс) и т.п. Однако пока точно неизвестны препараты, подавляющие репродукцию коронавируса. К специфическому лечению от коронавируса относится введение плазмы от переболевших людей, которая содержит антитела, но этот метод находит ограниченное применение.

Зачем нужна вакцинация? Как и из чего делают вакцины?
По сути, вакцины - это препараты для создания искусственного активного иммунитета. Термин "вакцина" произошел от французского vacca – "корова". Его ввел Л. Пастер в честь Дженнера, применившего вирус коровьей оспы для иммунизации людей против натуральной оспы человека. Вакцины – это препараты, содержащие сами микроорганизмы (убитые или живые ослабленные), части микроорганизмов, а также анатоксины (токсин, лишенный своих ядовитых свойств, но сохранивший свойства активировать иммунный ответ). После введения вакцины вырабатываются специфические антитела, которые нейтрализуют, прежде всего, поверхностные рецепторы вируса, с помощью которых он проникает в клетку. Таким образом блокируется основной механизм проникновения вируса в клетку. Многие вакцины создают пожизненный иммунитет у человека, например, вакцина от гепатита В, кори, краснухи, полиомиелита, эпидемического паротита.
Сколько времени уходит на создание вакцины?
На создание вакцины уходит 1-2 года, в течение которого должны пройти многочисленные проверки на эффективность и безопасность препарата, испытания на животных, потом на людях-добровольцах, а после – наладить массовое фармацевтическое производство.
Что представляют собой тесты на вирус? Как в лабораториях выявляют положительные результаты анализов?
Диагностика вируса основана на определении структуры вируса (специфических рецепторов и нуклеиновой кислоты), а также противовирусных антител у переболевших людей. Используются различные реакции: иммуноферментный анализ (ИФА), полимеразная цепная реакция (ПЦР). Время диагностики зависит от производителя тестов - от нескольких часов до 1 суток.
Несколько примеров самых массовых с убийственных с точки зрения эпидемий вирусов в истории человечества
Вирусы гриппа постоянно циркулируют среди населения, вызывая сезонные подъемы заболевания, периодически приобретающие характер эпидемий и даже пандемий. Эпидемии гриппа наносят огромный экономический ущерб, приводят к людским потерям. Это, прежде всего, относится к вирусам типа А, который каждые 2-3 года вызывает эпидемии, а несколько раз в столетие - пандемии с числом заболевших 1-2 млрд. человек. Эпидемии, вызываемые вирусом типа В, повторяются через 3-6 лет.
Пандемии гриппа, вызванные мутированными вирусами, против которых у людей нет иммунитета, возникают 2-3 раза в 100 лет. Пандемия гриппа 1918—1919 ("испанка", штамм H1N1) унесла жизни 40-50 миллионов человек. Предполагают, что вирус "испанки" возник в результате рекомбинации генов вирусов гриппа птиц и человека. В 1957—1958 была пандемия "азиатского гриппа", вызванная штаммом H2N2; в 1968—1969 - пандемия "гонконгского гриппа" (H3N2).
С 2009 появилось новое заболевание людей и животных, вызываемое штаммами вируса гриппа А/H1N1, А/H1N2, А/H3N1, А/H3N2 и А/H2N3, известных под общим названием "вирус свиного гриппа". Он распространён среди домашних свиней, а также может циркулировать в среде людей, птиц и др. видов; этот процесс сопровождается его мутациями.

Как уберечься от вирусов? Существуют ли действенные меры профилактики и гигиены?
Выделяют специфические и неспецифические способы профилактики вирусных инфекций. Специфические заключаются в использовании вакцин, при их наличии. При их введении у человека формируется как правило пожизненный иммунитет (вакцина от кори, краснухи, эпидемического паротита, ветряной оспы, гепатита В). Существует также экстренная профилактика. Ее проводят во время эпидемического подъема заболеваемости. Для экстренной профилактики, например, гриппа применяют противовирусные химиопрепараты: ремантадин (активен только против вирусов типа А), арбидол, амиксин, оксалиновую мазь и др. Используют также интерферон, дибазол, различные индукторы интерферона (например, элеутерококк, продигиозан).
Против многих вирусных инфекций вакцин не существует. В этом случае помогает неспецифическая профилактика. Существуют ряд общих правил:
- соблюдать личную гигиену (мойте руки перед приемом пищи, после использования туалета; не трогайте грязными, немытыми руками нос, глаза, рот).
- обязательно поддерживать здоровый образ жизни с помощью сбалансированного питания, занятий физкультурой, прогулок на свежем воздухе и многое другое.
Но для каждого вируса неспецифическая профилактика своя. Если речь идет о вирусах, передающихся воздушно-капельным путем, то необходимо придерживаться следующих правил:
- надевать маски, причем на больного человека, чтобы исключить попадание в пространство крупных частиц слюны при кашле и чихании, мелкие же частицы она не задерживает;
- тщательно убирать помещения, так как вирус любит теплые и пыльные помещения, поэтому стоит уделить время влажной уборке и проветриванию;
- избегать массовых скоплений людей и воздержаться от походов в общественные места.
Если вирус передается с помощью фекально-орального механизма, например, вирус гепатита А, то необходимо соблюдать следующее:
- употреблять чистую или кипяченую воду;
- мыть фрукты, ягоды, овощи кипяченой водой:
- поливать свой сад и огород проточной водой.
Если вирус передается через кровь, например, вирус гепатита В,С, ВИЧ, то необходимы:
- дезинфекция, стерилизация медицинских изделий;
- обследование доноров крови;
- не употреблять наркотики;
- использовать индивидуальные предметы личной гигиены;
- быть осторожными с маникюром, пирсингом и татуировками, делать это только в профессиональном салоне.
Если вирус передается половым путем, например, ВИЧ, то нужно:
- исключить незащищенные половые контакты, если вы не уверены в своём партнёре;
- использовать барьерные средства контрацепции, если вы не знаете статус своего партнера.
Как выглядят вирусы под микроскопом?
Сегодня описано больше 5 тысяч вирусов, и каждый из них питается и размножается за счет других клеток, то есть паразитирует внутри организма. По мнению ученых, вирус способен выживать в экстремальных условиях, обладает разумом и хитростью. Сам по себе вирус не представляет никакой опасности, но, попадая в организм, начинает активно размножаться. Выбрав нужные клетки, он словно ввинчивает в них свой код ДНК. Это происходит настолько быстро, что с момента вторжения до первых признаков заболевания проходит менее суток.
Многие вирусы считаются смертельными. При этом даже самые безобидные могут при определенных обстоятельствах настолько мутировать, что, попав в организм, вызовут тяжелые заболевания.
Эбола — вирус, вызывающий геморрагическую лихорадку, сопровождающуюся резким повышением проницаемости сосудов. Болезнь развивается очень быстро. Человек погибает за несколько дней от массивных кровотечений.
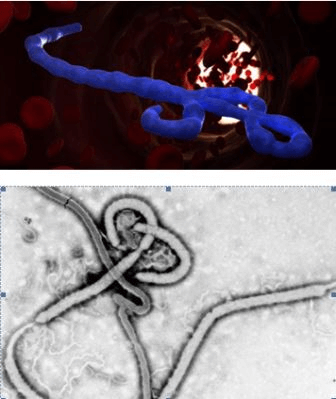
Бешенство — болезнь, вызываемая смертельным для человека вирусом. Передается от больных животных контактным путем или через укус. Вирус в организме продвигается со скоростью 3 мм/ч и поражает, в первую очередь, нервную систему.
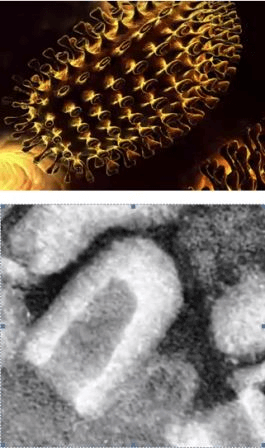
ВИЧ — медленное и прогрессирующее заболевание, вызванное вирусом, поражающим иммунные клетки. За несколько лет заболевание перерастает в СПИД.
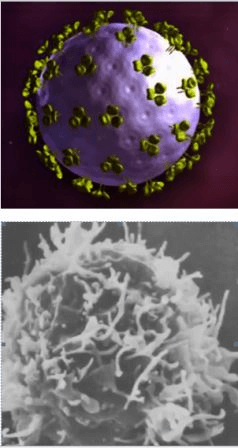
Вирус полиомиелита вызывает детский спинномозговой паралич, который может развиться за 2 дня. В группу высокого риска входят дети до 7 лет. Вакцинация — лучший способ избежать заболевания.

Вирус папилломы размножается в верхних слоях кожи и является очень заразным заболеванием, вызывающим рак. Особенно опасен для людей со сниженным иммунитетом.
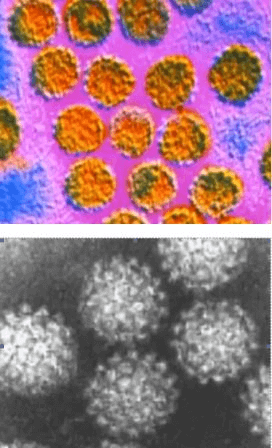
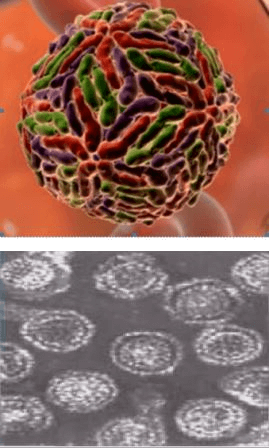
Оспа — высокозаразное и опасное заболевание, которое также вызывает вирус. Поражает в основном детей, вызывая различные осложнения.
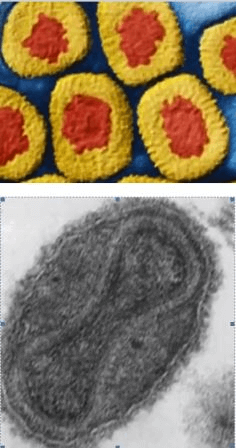
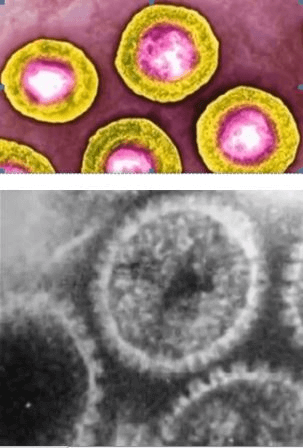
Вирусы гриппа вызывают острое инфекционное респираторное заболевание верхних дыхательных путей, которое без отсутствия лечения может протекать в тяжелой форме и вызывать осложнения. Сегодня описано более 2000 видов данного вируса.
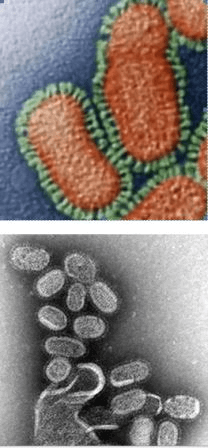
Ротавирус вызывает кишечные инфекции. Попадая в пищеварительный тракт, начинает активно размножаться в тонком кишечнике. Главная опасность — обезвоживание организма, которое может привести к печальным последствиям.
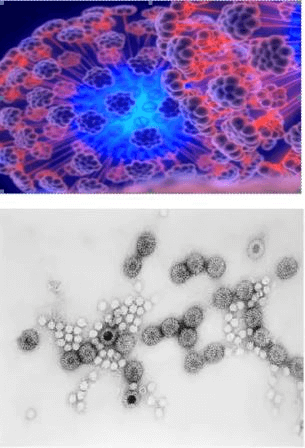
По мнению ученых, вирусы являются самым загадочным явлением на Земле. Только современные электронные микроскопы способны максимально увеличивать такие микроскопические объекты и позволяют человеку изучать их разновидности, правильно ставить диагнозы, лечить, а, самое главное, находить способы профилактики и защиты.
Многие вирусы могут очень долго присутствовать в организме и циркулировать в крови, до поры до времени не вызывая никаких неприятностей. Однако это вовсе не значит, что они безопасны. Лабораторные анализы на вирусы позволяют выявить наличие последних, даже если никаких симптомов нет.
Анализы на вирусы: какие инфекции они выявляют
Для выявления вирусов лаборатории проводят исследования крови несколькими методами. Наибольшее распространение на сегодня получили ПЦР и иммуноферментный (ИФА) анализы.
Иммуноферментный анализ крови определяет наличие антител к вирусам (или антигенов к ним) в крови — иммуноглобулины (lgA, lgG, lgM) вырабатываются при заражении вирусами и являются своеобразными маркёрами инфекции.
Анализ на ДНК вируса, или ПЦР-исследование, позволяет выявить тип инфицирующего агента.
В качестве биоматериала для исследования обычно берут кровь. Анализ крови может подтвердить гепатит, герпес и вирус Эпштейна-Барра, аденовирус, различные половые инфекции (в том числе и сифилис), вирус иммунодефицита человека (ВИЧ) и другие инфекции. Однако кровь не единственный биоматериал, пригодный для выявления вирусных поражений. В зависимости от заболевания и симптомов, для анализа на вирусы сдают соскоб слизистой оболочки, кал, мочу, мазок, слюну.
Как мы уже отмечали, исследование крови на вирусы можно проводить двумя разными способами. Расскажем о них подробнее.
Иммуноферментный метод анализа на вирусы позволяет установить форму болезни, вызванной вирусом (хроническая, острая или бессимптомная), а также оценить эффективность противовирусной терапии. Это один из самых распространенных и точных методов для выявления половых инфекций, в частности ВИЧ и ВПЧ, гепатита В.
Для анализа на вирусы чаще всего сдается кровь. Обязательно предупредите врача, если вы недавно проводили вакцинацию, — этот факт может отразиться на точности анализов. Рекомендуется не принимать пищу на протяжении 8-ми часов перед забором биоматериала, а также воздержаться от употребления алкоголя и от курения.
Время ожидания результатов зависит от типа вируса, на который проводится анализ, и от методики работы лаборатории. Обычно результаты готовы через 1–3 дня, но иногда приходится ждать и 2 недели.
Рассказать о том, каким образом следует трактовать результаты анализов на все виды вирусов, в рамках одной статьи невозможно. Далее мы поговорим лишь о наиболее известных заболеваниях и о часто назначаемых исследованиях.
В случае проведения анализа методом ИФА наличие IgG в крови на гепатит говорит о том, что этот вирус в организме присутствовал, но иммунная система выработала к нему антитела. Присутствие одновременно антител класса IgM и IgG говорит о заболевании в острой форме. Иммуноглобулины только класса IgM — признак первичного инфицирования.
При проведении исследования методом ПЦР определяется РНК вируса. Результаты могут быть приведены в следующем формате:
- РНК вируса не выявлена.
- РНК вируса выявлена в концентрации ниже предела количественного определения (менее15 МЕ/мл). Сомнительный результат.
- РНК вируса гепатита С выявлена (от 15 и выше 100000000 МЕ/мл).
Для выявления этого вируса гепатита чаще всего назначается ИФА. Если в крови присутствуют антитела IgG и IgM, это значит, что вирус очень активен или же заражение произошло недавно.
В случае проведения ПЦР-анализа определяется концентрация фрагментов ДНК вируса гепатита В. Пациент получает результат с одной из приведенных трактовок:
- Не обнаружено.
- Сомнительный результат (результат положительный с концентрацией ДНК вируса гепатита В на границе точности метода).
- Обнаружено.
Если говорить о трактовке ИФА, то наличие антител, обозначаемых как Anti-HSV-IgG, говорит не об иммунитете к вирусу, а о том, что вы уже были когда-то инфицированы. Этот маркёр наблюдается у большинства пациентов. Если показатель anti-HSV-IgG в пробах, взятых в динамике за 2-недельный период, заметно растет, это значит, что заражение произошло недавно. О рецидиве говорит высокий показатель IgG.
Расшифровка анализа крови на ВИЧ очень проста — если результат отрицательный, это значит, что вирус не обнаружен, если положительный — увы, вирус в крови есть. Но следует знать, что сегодня даже самые надежные методы точны лишь на 98–99%, то есть всегда остается шанс, что результат будет, например, ложноположительным.
При анализе на аденовирус, вызывающий респираторные заболевания, применяется в основном ИФА. В ходе анализа подсчитываются IgG-антитела. Если показатель менее 0,8 условных единиц — результат отрицательный, более 0,8 — положительный.

Не пренебрегайте профилактическими анализами на вирусы. Раннее выявление инфекции позволяет отсрочить или подавить развитие заболевания. В случае же беременности сдача биоматериала на анализ с целью выявления вирусных инфекций является обязательной процедурой. Поводом для прохождения исследования также может стать повышенный уровень лейкоцитов в крови, сдвиг лейкоцитарной формулы, увеличение количества нейтрофилов (палочкоядерных), миелоцитов и метамиелоцитов, снижение числа лимфоцитов при высокой СОЭ в результатах клинического анализа крови.
Относящийся к данному классу атомно-силовой микроскоп оказался инструментом, подходящим для исследования биологических объектов и позволил не только визуализировать наноразмерные структуры, но и манипулировать ими. В частности, принципиально возможной оказалась манипуляция одиночными вирионами и прямое измерение сил, возникающих при их контакте с поверхностью клетки. Такие эксперименты позволяют получать подробные данные о самом первом и во многих случаях еще недостаточно исследованном этапе заражения клетки – адгезии вируса к ее поверхности. Данные исследования представляют и значительный практический интерес, т.к. могут дать ключ к созданию эффективных противовирусных препаратов, защищающих клетки от проникновения вирусов.
Вирусы являются чрезвычайно малыми объектами – их размеры лежат в диапазоне от нескольких десятков до нескольких сотен нанометров. Первым и на долгое время единственным методом прямой визуализации наноразмерных частиц стала электронная микроскопия (ЭМ), которая начала развиваться в 1930-е гг. Метод, оказавшийся очень информативным, позволил не только детально охарактеризовать структуру различных вирусов, но и исследовать процессы, происходящие в зараженной клетке.
Оказалось, что форма вирусных частиц отличается большим разнообразием: от правильных сфер до сложных структур, напоминающих кирпичи, обклеенные трубочками (вирус натуральной оспы), или щетинистых червей (вирус геморрагической лихорадки Эбола).
Вне клетки любой вирус является всего лишь молекулярным контейнером с генетическим материалом (ДНК или РНК) и вряд ли может считаться полноценным живым организмом, хотя по этому вопросу в научной среде до сих пор нет окончательной терминологической определенности.
Так, исследование репликации вируса методом просвечивающей электронной микроскопии на ультратонких срезах выглядит следующим образом: зараженные клетки обрабатывают фиксирующим раствором, обезвоживают спиртом и заливают специальной смолой. После отвердевания смолы с помощью специального прибора – ультратома – делают ультратонкие (≈ 50 нм) срезы, которые затем наносят на специальную сетку и обрабатывают растворами солей тяжелых металлов. Во время самого микроскопического исследования образец находится в вакуумной камере и подвергается действию пучка электронов с энергией в несколько десятков кэВ. Очевидно, что прижизненная визуализация в данном случае принципиально невозможна.
В течение почти полувека электронная микроскопия оставалась единственным методом визуализации наноразмерных объектов. Однако в начале 1980-х гг. эта монополия была нарушена появлением сканирующей зондовой микроскопии (СЗМ). Основным принципом СЗМ является сканирование – прецизионное (с высокой точностью) перемещение зонда вблизи исследуемой поверхности, сопряженное с отслеживанием определенного параметра, характеризующего взаимодействие между зондом и образцом. Результатом такого сканирования является топографическая карта рельефа поверхности образца.
Первым прибором СЗМ стал сканирующий туннельный микроскоп (СТМ), который мог лишь весьма ограниченно использоваться для визуализации биологических объектов, так как для его работы требовалась высокая электрическая проводимость исследуемой поверхности.
В 1986 г. швейцарский физик Г. Бинниг и его коллеги создали новый прибор семейства СЗМ – атомно-силовой микроскоп (АСМ). В основе его работы лежит силовое (Ван-дер-Ваальсово) взаимодействие атомов зонда и поверхности. АСМ не требуется электрическая проводимость поверхности образца, и он может осуществлять съемку в жидкой среде. Поэтому этот прибор оказался удобным инструментом для исследования биологических объектов.

С момента появления атомно-силового микроскопа было опубликовано огромное число работ, посвященных АСМ-визуализации самых разнообразных биологических образцов. Следует все же признать, что в большинстве случаев в плане визуализации АСМ не дает ничего принципиально нового в сравнении с обычной электронной микроскопией, поэтому зачастую данный метод воспринимается биологами как техническая экзотика, а не как полноценный исследовательский инструмент.
Однако важнейшим, пусть и почти единственным преимуществом визуализации биологических объектов при помощи АСМ по сравнению с электронной микроскопией является возможность выполнения исследований нативных, природных образцов без какой-либо фиксации и специальной пробоподготовки, при физиологических параметрах среды.
Помимо визуализации рельефа поверхности с субнанометровым разрешением АСМ позволяет осуществлять прямое измерение сил, возникающих при взаимо¬действии одиночных наноразмерных объектов.
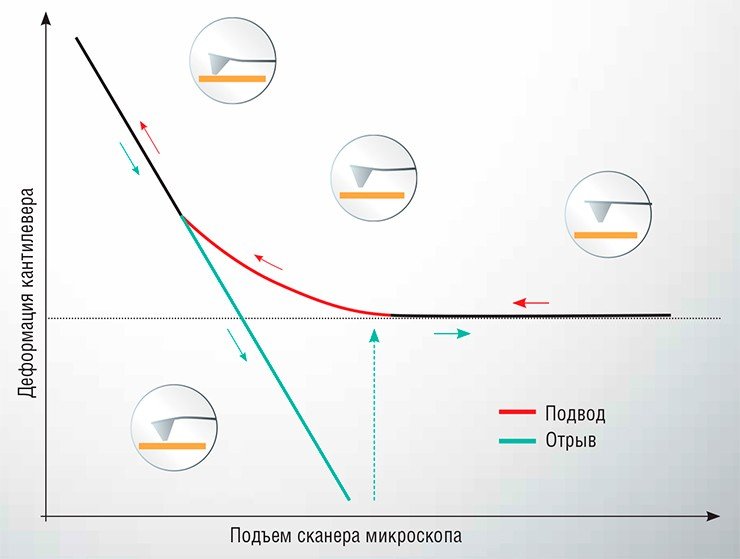
Проводятся такие измерения следующим образом: один объект закрепляется на острие зонда АСМ, а второй фиксируется на подложке, после чего зонд подводится к поверхности подложки до достижения механического контакта, а затем возвращается обратно. В ходе этого перемещения отслеживается деформация упругой консоли (кантилевера). Зависимость этого параметра от расстояния между зондом и подложкой называется силовой кривой. С ее помощью можно определить величину силы, действующей между исследуемыми объектами. Этот метод, названный атомно-силовой спектроскопией (АСС), может использоваться для исследования силовых характеристик взаимодействия самых разнообразных малых объектов: от неорганических наночастиц до вирусов и живых клеток.
Начальным этапом заражения клетки вирусом является адгезия (прилипание) вирусной частицы (вириона) к клеточной поверхности с последующим проникновением генетического материала вируса внутрь клетки. Этот процесс, определяемый взаимодействием белковых рецепторов, расположенных на поверхности клетки, с поверхностными белками вириона, является критически важным для размножения вируса. И, надо отметить, в большинстве случаев изучен недостаточно.

Однако фиксация одиночной вирусной частицы на острие зонда атомно-силового микроскопа является весьма непростой задачей. Для успешного проведения эксперимента требуется большая подготовительная работа:
- получить как можно более чистый и концентрированный препарат вируса;
- подготовить на острие зонда площадку подходящего размера для посадки вириона;
- химически активировать поверхность зонда для образования ковалентных связей при контакте с белками вируса;
- убедиться в том, что на зонде закрепился действительно вирион, а не молекулы свободного белка или мелкие фрагменты клеток, всегда присутствующие в препаратах вирусов.
Оценка концентрации и степени чистоты препарата вируса обычно проводится методом просвечивающей электронной микроскопии. Площадку на острие АСМ-зонда, которое обычно изготавливают из кремния или его нитрида, формируют путем длительного сканирования кремниевой или сапфировой подложки при больших значениях развертки и силы прижатия зонда к поверхности. Наиболее наглядной иллюстрацией для этого процесса служит изменение формы острия карандаша в ходе интенсивного рисования.
По меркам микроскопии, клетка высших организмов является относительно крупным (≈ 10 мкм) объектом, поэтому хорошо видна в световом микроскопе, при помощи которого на нее наводится кантилевер атомно-силового микроскопа. Но как быть с самим зондом, на острие которого предполагается наличие вириона? Строго говоря, вместо вириона там может оказаться все, что угодно: монослой белковых молекул, фрагмент клетки или вириона, агрегат из нескольких вирионов, случайное загрязнение и т. д. Кроме того, в процессе измерения вирион может разрушиться или оторваться от зонда. Визуализация же зонда с вирусной частицей методом электронной микроскопии до силовых измерений недопустима, так как под воздействием высушивания, вакуума и пучка электронов вирион приобретет необратимые изменения.
Наиболее эффективным методом решения данной проблемы оказалась визуализация острия зонда АСМ с помощью электронной микроскопии, осуществляемая непосредственно после силовых измерений. Если на острие будет обнаружена вирусная частица, уцелевшая в ходе эксперимента, то все сомнения развеются.
В течение последних пятидесяти лет в результате поистине титанической работы, проделанной электронными микроскопистами всего мира, накоплен огромный багаж знаний в области ультраструктурных аспектов репликации различных вирусов. Создание атомно-силового микроскопа и техники силовой спектроскопии позволило вплотную приблизиться к произвольной механической манипуляции одиночными вирусными частицами. Это выводит изучение взаимодействия вируса с клеткой на принципиально другой уровень – от структурных исследований к функциональным.
При этом атомно-силовая спектроскопия не является конкурентом для электронной микроскопии, а открывает новое самостоятельное направление исследований – наномеханику взаимодействия вирусной частицы с поверхностью клетки. Весьма вероятно, что в самом ближайшем будущем в данном направлении будут совершены фундаментальные открытия, соизмеримые по значимости с достижениями электронной микроскопии в середине прошлого века.
Изучение механизмов связывания вирусных частиц с поверхностью клетки вызывает значительный интерес не только с позиции фундаментальной науки, но и в контексте практических приложений. Более детальное понимание этих механизмов на молекулярном уровне может дать человечеству ключ к созданию эффективных противовирусных препаратов, защищающих клетки от проникновения вирусов.
*Просвечивающая электронная микроскопия с использованием специальной жидкостной ячейки и сканирующая электронная микроскопия при атмосферном давлении позволяют исследовать биологические объекты без фиксации, но из-за ряда технических трудностей и относительно низкого пространственного разрешения эти методы не получили широкого распространения
Корнеев Д. В., Бессуднова Е. В., Зайцев Б. Н. Изучение взаимодействия наночастиц TiO2 и поверхности эритроцитов человека методом атомно-силовой спектроскопии // УНЖ. 2012. № 4. С. 73—77.
Миронов В. Л. Основы сканирующей зондовой микроскопии. Нижний Новгород: ИФМ РАН, 2004. 182 с.
Alsteens D., Pesavent E., Cheuvart G. et al. Controlled manipulation of bacteriophages using single-virus force spectroscopy // ACSNANO. 2009. V. 3(10). P. 3063—3068.
Alsteens D., Trabelsi H., Soumillion P., Dufrene Y. F., Multiparametric atomic force microscopy imaging of single bacteriophages extruding from living bacteria // Nature Communications. V. 4. Article number: 2926.
Binnig G., Quate C. F., Gerber Ch. Atomic force microscope // Phys. Rev. Lett. 1986. V. 56(9). P. 930—933.
Cappella B., Dietler G. Force-distance curves by atomic force microscopy // Surf. Sci. Rep. 1999. V. 34. P. 1—104.
Malkin A.J., Plomp M., McPherson A. Unraveling the architecture of viruses by high-resolution atomic force microscopy // Methods Mol. Biol. 2005. V. 292. P. 85—108.
В публикации использованы фото автора
Читайте также:


