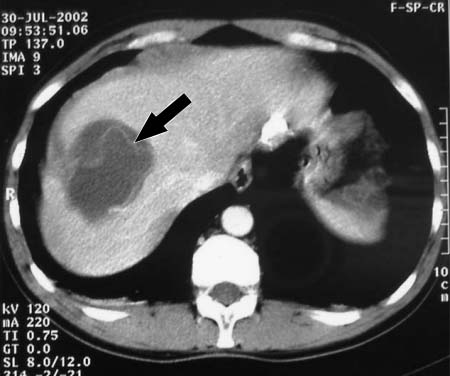
Некроз печени при вирусных гепатитах
Болезни печени: гепатозы, гепатиты, цирроз печени. Осложнения и причины смерти при циррозах печени. Алкогольная болезнь: ее виды и патоморфологические проявления.
Уровень современной медицины требует от врача максимально точной диагностики заболеваний с указанием (там, где это возможно) их этиологии. Это полностью относится к диагностике заболеваний печени, поскольку метод биопсийного исследования открывает большие возможности в раскрытии этиологии болезней печени и назначении высокоэффективного этиотропного лечения. В настоящее время одним из основных методов прижизненной диагностики заболеваний печени является гистологическое исследование печеночного биоптата. Широкое применение этого метода в клинике сформировало новое направление в медицине - клиническую гепатологию.
Классификация болезней печени.
4. Опухолевые поражения
5. Врожденные аномалии строения (кистозная печень)
ГЕПАТОЗЫ - группа острых и хронических заболеваний печени, преобладающими при которых являются дегенеративные изменения паренхимы. Среди гепатозов выделяют наследственные формы, которые не так редки: наследственные липидозы, наследственные гликогенозы, наследственный пигментный гепатоз (болезнь Вильсона-Коновалова). Многие из этих болезней заканчиваются циррозом печени. Приобретенные гепатозы делятся на острые и хронические.
ОСТРЫЙ ГЕПАТОЗ: токсическая дистрофия печени (прогрессирующий массивный некроз печени; острая желтая дистрофия печени). Развивается при экзогенных отравлениях гепатотропными ядами (ядовитые грибы, гелиотроп, соединения фосфора, мышьяка), а также при эндогенных интоксикациях (сепсис, тиреотоксикоз, токсикоз беременных). Токсическая дистрофия печени может иногда развиваться при острых вирусных гепатитах - т.н. острый вирусный гепатит с массивными некрозами печени. Токсическая дистирофия печени не всегда является острым процессом - она может быть подострой или даже хронической, растягиваясь на месяцы до одного года и более.
Патологическая анатомия. Выделяют начальную стадию желтой дистрофии, когда происходит жировая дистрофия гепатоцитов в центрах долек, далее развивается их некроз с аутолитическим распадом и резорбцией, печень имеет желтый цвет, вначале может несколько увеличиваться в размерах, затем, с 3-4 дня, ее размеры быстро уменьшаются (почти вдвое), цвет становится серовато-глинистым. Данная стадия продолжается в течение 2 недель. Нередко развивается асцит. С 3-й недели цвет печени меняется и она становится красной (стадия красной дистрофии). Это связано с тем, что некротический детрит в центре долек резорбируется, а освободившиеся от давления клеток капиллярные синусоиды переполняются
кровью. При большом объеме поражения печени больные умирают от острой печеночной недостаточности. Если смерть не наступает, в дальнейшем формируется постнекротический мультилобулярный цирроз печени. ХРОНИЧЕСКИЙ ГЕПАТОЗ: жировая дистрофия печени (жировой стеатоз печени). Развивается при хроническом токсическом воздействии на печень (алкоголь, инсектициды, хлороформ, некоторые лекарственные препараты), при сахарном диабете и общем ожирении, при кишечных инфекциях (дизентерия, сальмонеллезы, кишечная колиинфекция, кишечная стафилококковая инфекция).
Алкогольный стеатоз печени (ожирение печени) развивается под воздействием на гепатоциты этанола. Этанол вызывает гиперлипидемию и одновременно стимулирует синтез в гепатоцитах жирных кислот и их эстерификацию с образованием триглицеридов. Отложение несгораемых жиров в гепатоцитах облегчается также и низким потреблением алкоголиками липотропных веществ (белковая пища). Основным морфогенетическим механизмом алкогольного стеатоза является инфильтрация. Макроскопически печень увеличена, часто неравномерно, преимущественно за счет правой доли. Цвет ткани от коричневатого до желтого. Липиды при алкогольном стеатозе накапливаются преимущественно в центральных и промежуточных отделах дольки, при выраженном стеатозе липиды распределяются повсеместно. Жировая дистрофия гепатоцитов при алкогольной болезни обычно сочетается с различными видами белковой дистрофии - гидропической, баллонной, зернистой. Иногда несколько рядом расположенных гепатоцитиов с крупными жировыми вакуолями сливаются и образуют жировую кисту; вокруг нее развивается воспалительная реакция, иногда с наличием гигантских клеток.
Жировая дистрофия печени при алкогольной болезни процесс обратимый и через 2-4 недели после полного прекращения приема алкоголя жир из печени исчезает. Исчезновение жира начинается с центральных отделов
долек. Для алкогольного стеатоза характерно развитие перивенулярного фиброза (склероз вокруг центральных вен) - начальной стадии цирроза печени. Этим признаком алкогольный стеатоз отличается от жировой дистрофии печени при сахарном диабете и ожирении. Другой особенностью алкогольного стеатоза является сидероз купферовых клеток печени.
Гепатиты - группа острых и хронических заболеваний печени, преобладающими при которых являются очаговые или диффузные воспалительные изменения печеночной ткани. Различают первичные и вторичные гепатиты. Первичные инфекционные гепатиты в основном представлены вирусными и лептоспирозными. К первичным неинфекционным гепатитам можно отнести токсические гепатиты - алкогольный, медикаментозный. Вторичные инфекционные гепатиты развиваются при многих тяжелых инфекционных заболеваниях - пневмонии, перитониты, сепсис, малярия и др.
В настоящее время насчитывают 7 типов вирусных гепатитов: А,B,C,D,E,F,G. Из них 3 типа - А, Е и F передаются алиментарным путем (эпидемический гепатит, болезнь Боткина), все же остальные - это сывороточные гепатиты, передающиесчя парентерально. Среди сывороточных гепатитов наибольшую актуальность имеют 2 типа - В и С, которые часто ассоциируются друг с другом, вызывая тяжелые прогрессирующие поражения печени, плохо поддающиеся лечению, и имеющие высокую вероятность трансформации в цирроз и рак.
Различают следующие формы острого вирусного гепатита (эпидемического и сывороточного): классическая циклическая с желтухой, безжелтушная, холестатическая и гепатит с массивными некрозами печени (см. острую токсическую дистрофию печени).
Маркеры вирусного поражения печени: наличие частиц вируса (при электронной микроскопии); присутствие вирусных антигенов (обычно HBs-Ag), выявляемое гистологически и иммуногистохимически; белковая дистрофия гепатоцитов (гидропическая и баллонная), коагуляционный некроз гепатоцитов с появлением телец Каунсильмена, воспалительный инфильтрат из макрофагов и лимфоцитов, появление матово-стекловидных гепатоцитов, "песочные" ядра, мультилобулярный цирроз печени в финале.
Хронические вирусные гепатиты делятся на хронические активные (агрессивные) и хронические неактивные (персистирующие). Хронический активный (агрессивный) гепатит (ХАГ) обычно связан с вирусами гепатита В и С - отмечается белковая дистрофия гепатоцитов, некроз гепатоцитов на периферии долек, воспалительная инфильтрация проникает в центр долек, окружая и разрушая гепатоциты. В исходе формирование цирроза печени.
Хронический неактивный гепатит (ХНГ) - дистрофические изменения гепатоцитов имеются, но некрозы отсутствуют, воспалительная инфильтрация сосредоточена только в перипортальных трактах, отмечаются склеротические изменения долек. Вероятность трансформации в цирроз мала.
Считается доказанным, что развитие алкогольного гепатита начинается с появления в гепатоцитах алкогольного гиалина (тельца Мэллори). Алкогольный гиалин представляет собой результат извращенного синтеза гепатоцитами фибриллярных цитоплазматических белков (возможно, имеющих отношение к цитоскелету клетки). Алкогольный гиалин обладает антигенными и хемотаксическими свойствами, стимулирует лимфоциты и макрофаги, активирует коллагенообразование фибробластами, вызывает хемотаксис ПМЯЛ. Появление большого количества алкогольного гиалина в гепатоцитах является плохим прогностическим признаком. Помимо этого для алкогольного гепатита характерны гидропическая и жировая дистрофия гепатоцитов, некрозы групп гепатоцитов, в дальнейшем центролобулярные некрозы, наличие среди клеток воспалительных инфильтратов большого количество ПМЯЛ, сидероз купферовых клеток. При длительном течении алкогольного гепатита может сформироваться монолобулярный септальный цирроз печени. Однако есть данные, согласно которым цирроз при алкогольном поражении печени возникает лишь при наличии сопутствующего хронического вирусного гепатита В (или С).
Маркеры алкогольного поражения печени: жировая дистрофия гепатоцитов, очаги колликвационного некроза гепатоцитов, воспалительный инфильтрат, содержащий большую примесь ПМЯЛ, гемосидероз купферовых клеток, перивенулярный фиброз, монолобулярный септальный цирроз печени.
Развиваются при длительном употреблении гепатотоксических медикаментов: тетрациклин, пуромицин, анаболические стероиды, противозачаточные стероидные гормоны, изониазид, ипрониазид. Установлено, что среди всех больных с желтухами у 2-5% имеется медикаментозное поражение печени.
Морфологические маркеры лекарственного поражения печени: жировая дистрофия гепатоцитов, очаги колликвационного некроза вокруг центральных вен, наличие большого количества эозинофилов в воспалительных инфильтратах, образование неспецифических гранулем, поражение желчных капилляров с развитием холестаза в периферических отделах долек, монолобулярный цирроз печени.
Хроническое заболевание печени, основой которого является извращенная регенерация печеной ткани в ответ на ее острые или хронические повреждения. В зависимости от этиологических факторов циррозы делят на инфекционные (в первую очередь вирусные), токсические (в первую очередь алкоголь и его суррогаты, а также лекарственные препараты), обменно-алиментарный (недостаточность белков, витаминов, липотропных факторов,
циррозы при тезаурисмозах), холестатический, застойный (кардиогенный) цирроз. Могут быть врожденные циррозы у детей, связанные с внутриутробной инфекцией вирусами гепатита В, цитомегалии или герпеса. Среди наших больных наиболее часто встречаются вирусные и алкогольные циррозы печени.
Общая патоморфология циррозов печени.
Независимо от вида цирроза и стадии заболевания печень с поверхности и на разрезе всегда бугриста, узловата или зерниста, а на ощупь
плотная. В начале процесса печень может быть увеличена в размерах, в дальнейшем она может уменьшаться из-за нарастания атрофических процессов. Наиболее крупная по размерам цирротическая печень - при алкогольном циррозе, атрофические формы цирроза более характерны для постнекротических его форм. Величина узловатых разрастаний в печени при циррозе зависит от его вида, соответственно чему различают 2 основных морфологических вида циррозов - мелкоузловой и крупноузловой. Данные узловатые разрастания представляют собой узлы-регенераты, которые построены преимущественно из ложных долек и соединительной ткани. Образование при циррозе печени ложных долек является основным морфогенетическим событием.
Что такое ложная долька и чем она отличается от истинной печеночной дольки ? Ложная долька представляет собой продукт извращенной регенерации печеночной ткани и в отличие от истинной дольки лишена нормальной архитектоники своего строения (нет радиального расположения печеночных балок, центральные вены могут отсутствовать или располагаться эксцентрично, триады неполные и могут также отсутствовать). Ввиду нарушенного строения ложные дольки не могут нормально функционировать: из-за нарушения притока крови нет полноценной конъюгации гепатоцитами токсичного первичного билирубина и нет качественной детоксикации кишечных метаболитов (отсюда печеночноклеточная недостаточность при циррозах с клинической картиной прогрессирующей хронической токсической энцефалопатии), из-за нарушения архитектоники желчных капилляров образующаяся желчь не выводится полностью из дольки в кровь и развивается паренхиматозная (печеночная) желтуха. Недостаточное поступление в кишечник желчи приводит к нарушению эмульгирования и всасывания жиров, развивается вторичная мальабсорбция с потерей веса, гиповитаминозами А,Д,Е, К, замедлением свертывания крови, появлением сосудистых "звездочек" на коже.
Существует 2 основных морфогенетических механизма образования ложных долек при циррозе печени. Первый - при хронических активных гепатитах, когда воспалительная инфильтрация проникает в глубину долек, соединительная ткань по стихании воспаления также врастает вглубь дольки и как бы отхватывает, "откусывает" часть дольки. Из этого отделившегося фрагмента формируется в дальнейшем ложная долька, которая лишена собственных сосудов и желчных капилляров. Таким же путем формируются ложные дольки при хроническим венозном застое в печени (застойный кардиогенный цирроз печени через стадию "мускатной" печени). Разрастающаяся в печени соединительная ткань имеет вид тонких прослоек. Данный морфогенетический механизм лежит в основе формирования монолобулярного мелкоузлового (микронодулярного) цирроза печени (септальный цирроз печени), который является сравнительно доброкачественным по своему течению.
Второй механизм реализуется при развитии в печени массивных некрозов паренхимы (т.н. постнекротический цирроз печени). При этом происходит гибель обширных участков печеночной паренхимы, и источником ее последующей регенерации (если больной не умирает в стадию острой печеночной недостаточности) являются сохранившиеся небольшие островки из уцелевших гепатоцитов, часто расположенных друг от друга на значительном расстоянии. Сохранившиеся гепатоциты, лишенные стромального каркаса (который управляет регенерацией гепатоцитов), начинают регенерировать хаотично, что приводит к формированию ложных долек (мультилобулярный цирроз). Отличием данной формы цирроза от предыдущей является образование крупных узлов-регенератов (макронодуляный цирроз) с грубыми прослойками соединительной ткани. Разрастающаяся при циррозах печени соединительная ткань резко нарушает внутрипеченочную гемодинамику и выведение желчи по желчным протокам (кровеносные сосуды и желчные протоки сдавливаются и склерозируются). В результате возникают печеночная желтуха и что особенно важно - портальная гипертензия. Последняя сопровождается компенсаторным расширением коллатеральных венозных сосудов - портокавальные и кавакавальные анастомозы (вены передней стенки живота, вены слизистой желудка и нижней трети пищевода, вены париетальной брюшины, геморроидальные вены) и образованием асцита. Расширенные вены пищевода и слизистой желудка могут быть источником тяжелых пищеводно-желудочных кровотечений, скапливающаяся в полости брюшины асцитическая жидкость может инфицироваться из кишечника и приводить к развитию асцит-перитонита. Таким образом, при циррозах печени в стадию декомпенсации процесса развиваются: печеночная недостаточность, желтуха, портальная гипертензия с асцитом и асцит-перитонитом, пищеводно-желудочные кровотечения. Возможна также трансформация узлов-регенератов в гепатому - рак печени.
Хронический алкоголизм - понятие больше социальное и социально-юридическое. Медицинским эквивалентом этому является термин "алкогольная болезнь".
Клинико-морфологические формы алкогольной болезни.
1. Алкогольные поражения печени (гепатическая - стеатоз, гепатит, цирроз);
2. Алкогольная кардиомиопатия (кардиальная - жировая дистрофия миокарда с его умеренной гипертрофией и дилатация полостей сердца и сердечной недостаточностью);
3. Алкогольная энцефалопатия (мозговая) и нейропатия (алкогольные полиневриты).
4. Алкогольная нефропатия (ренальная - хронические гломерулонефриты и гломерулопатии, острый и хронический тубуло-интерстициальный нефрит, острая почечная недостаточность при отравлении суррогатами алкоголя - "токсическая почка");
5. Поражения поджелудочной железы и ЖКТ (гастро-панкреатическая - хронический атрофический гастрит, хронический калькулезный панкреатит);
Этиологическими факторами гепатитов являются многие из тех, которые вызывают гепатозы: алкоголь, лекарственные препараты. Вместе с тем имеется большое количество инфекционных гепатитов, среди которых основное значение имеют вирусные гепатиты.
Некроз печени – гибель гепатоцитов под действием механических, химических, температурных либо токсических факторов, а также в результате прекращения кровоснабжения ткани печени. Проявляется болью в правом подреберье, тошнотой, рвотой, повышенной температурой, умеренным увеличением печени, признаками печеночной и сердечной недостаточности. Для постановки диагноза требуется проведение печеночных проб, УЗИ, МРТ, ОФЭКТ печени, пункционной биопсии с морфологическим исследованием биоптатов. Основные направление лечения некроза печени: устранение печеночной недостаточности, коррекция витальных функций, дезинтоксикационная терапия, при неблагоприятном прогнозе для жизни – пересадка печени.
Общие сведения
Некроз печени – серьезнейшее осложнение некоторых заболеваний печени, отравлений, травм, нарушений печеночного кровоснабжения. Характеризуется быстрым нарастанием и прогрессированием явлений полиорганной недостаточности, приводящих к печеночной энцефалопатии и коме. Современные исследования в области гастроэнтерологии позволили выделить несколько форм этого заболевания: сверхострый некроз диагностируют при выявлении симптомов энцефалопатии в течение 7 суток после появления желтухи, острый – если этот период составляет 8-28 суток, подострый – если энцефалопатия развивается между 4 и 12 неделей заболевания. Патология встречается достаточно редко – в США ежегодно регистрируется около 2000 случаев. Острые формы некроза печени характерны для молодых людей (средний возраст 25 лет), подострая – для лиц более старшего возраста (
Причины некроза печени
Некроз печени является полиэтиологичным заболеванием. Острый некроз печени чаще всего встречается при различных гепатитах, из них в 75% случаев - вирусной этиологии. Примерно 1% пациентов с вирусным гепатитом В перенес данную патологию, а сочетание гепатита В и D приводит к острому некрозу печени в 30-40% случаев. Также частой причиной острого некроза печени является отравление лекарственными средствами либо токсическими веществами.
Некроз печени часто сопровождает тяжелую патологию сердечно-сосудистой системы с развитием ишемии печеночной ткани. Длительное нарушение кровоснабжения печени ведет к развитию центролобулярного некроза, либо к тотальному поражению паренхимы с быстрым развитием печеночной недостаточности.
Кроме того, приводить к массивной гибели гепатоцитов могут радиационные и термические воздействия на организм, тяжелые травмы печени. Более редкой причиной являются гемобластозы (опухолевые клетки инфильтрируют ткань печени, приводя к гибели паренхимы), прием препаратов для лечения СПИДа (диданозин), острая жировая инфильтрация гепатоцитов при некоторых заболеваниях обмена веществ.
По степени распространенности процесса некроз может быть фокальным (поражение нескольких рядом расположенных гепатоцитов – при вирусных гепатитах), центролобулярным или зональным (гибнут гепатоциты определенных зон печеночной дольки - при хронических гепатитах, приеме гепатотоксичных веществ), субмассивными и массивными (поражается вся печеночная долька).
Симптомы некроза печени
Проявления некроза печени зависят от объема поражения паренхимы. Чаще всего клиника характеризуется постепенным нарастанием печеночной недостаточности, развитием печеночной энцефалопатии и комы. Первыми проявлениями некроза печени могут быть боль в правом подреберье, незначительное увеличение органа, желтуха, тошнота и рвота. При гибели большого количества гепатоцитов происходит активация иммунной системы для отграничения очага поражения от здоровых тканей, в результате чего возникает отек тканей, увеличение объема печени и растяжение ее капсулы. Из-за этого и возникает боль в подреберье, которая может иррадиировать в правую лопатку, поясницу справа. Последующее уменьшение размеров печени и исчезновение болевого синдрома может говорить о гибели значительного объема паренхимы и плохом прогнозе для жизни пациента.
При некрозе печени теряется достаточно важная функция этого органа – дезинтоксикационная. Токсические вещества начинают накапливаться в организме, вызывая повреждение всех органов. В первую очередь страдает головной мозг – накопившиеся токсины и аммиак раздражают клетки головного мозга, вызывая печеночную энцефалопатию. Проявляется это состояние повышенной сонливостью, забывчивость, тремором конечностей, неадекватным поведением, агрессией. Коматозному состоянию обычно предшествуют дезориентация в пространстве и времени, потеря памяти, повышение мышечного тонуса с развитием спазмов мускулатуры. Нарастание отека мозга может привести к расстройству витальных функций – нарушению дыхания, артериальной гипотензии, брадикардии.
Попадание продуктов распада гепатоцитов в почечные канальцы ведет к поражению почек. Гепаторенальный синдром развивается примерно у половины пациентов с некрозом печени. Угнетение функции почек приводит к выраженным электролитным нарушениям, еще большему накоплению азотистых шлаков в кровотоке. Повышение уровня токсинов в крови приводит к прогрессированию печеночной энцефалопатии и отека мозга.
При некрозе печени значительно угнетается и ее белково-синтезирующая функция, что приводит к развитию ДВС-синдрома из-за нарушения синтеза фибринолитических ферментов и белков системы свертывания. Остановить массивные кровотечения путем простого переливания факторов свертывания обычно не удается, так как для их активации также требуется участие печени. Циркуляция в крови большого количества токсинов приводит к образованию в желудке и кишечнике острых язв, а недостаточность свертывающей системы - к развитию массивных желудочно-кишечных кровотечений. Большую роль в этом процессе играет и гиперпродукция соляной кислоты при некрозе печени, поэтому предупредить ЖКК можно с помощью профилактического назначения ингибиторов протонной помпы.
Частым осложнением некроза печени является генерализованная инфекция. Развитие полиорганной недостаточности приводит к повышению проницаемости кишечной стенки (бактерии из кишечника легко проникают в кровоток), нарушению механизмов местного и общего иммунитета. Настороженность в плане развития сепсиса должна иметь место в отношении всех пациентов с некрозом печени.
Диагностика некроза печени
Пациенты с некрозом печени требуют немедленной консультации гастроэнтеролога, реаниматолога, хирурга. При подозрении на данную патологию необходимо провести УЗИ печени и желчного пузыря, магнитно-резонансную томографию печени и желчевыводящих путей, однофотонную эмиссионную компьютерную томографию печени (ОФЭКТ печени). Все эти исследования позволят выявить очаг поражения в паренхиме печени, однако точное описание патологического процесса сможет предоставить только пункционная биопсия печени с морфологическим исследованием биоптатов.
Для уточнения степени тяжести процесса проводят биохимические пробы печени, исследование уровня азотистых шлаков, ЭКГ, ЭЭГ. Если есть подозрение на вирусный гепатит – необходимо определить уровень антител к основным антигенам (В, С, D).
Лечение некроза печени
Лечение больных с острым некрозом печени проводится в отделении интенсивной терапии. Мероприятия должны быть направлены на устранение печеночной недостаточности. В условиях отделения реанимации производится постоянный контроль за витальными функциями, уровнем глюкозы и азотистых шлаков, электролитов. Для профилактики кровотечений ежедневно внутривенно вводится витамин К. Переливание факторов свертывания в профилактических целях не показано. Обязательно назначаются препараты, угнетающие секрецию соляной кислоты в желудке. При развитии судорог вводится диазепам. При тяжелом течении некроза печени может потребоваться перевод на полное парентеральное питание.
Улучшение функции почек возможно только на фоне улучшения работы печени. Диализ или гемосорбция при данной патологии практически всегда осложняются массивными кровотечениями, генерализацией инфекционного процесса, поэтому лечение должно быть направлено на восстановление функций печени.
Прогрессирование печеночной энцефалопатии при некрозе печени может быть вызвано поступлением азотсодержащих веществ в пищеварительный тракт. Данные соединения расщепляются кишечной флорой, а их метаболиты поступают в кровоток и оказывают повреждающее действие на головной мозг. Для лечения печеночной энцефалопатии пациента переводят на парентеральное питание аминокислотными растворами, назначают внутрь антибактериальные препараты (неомицин, метронидазол) для подавления кишечной флоры, лактулозу.
На сегодняшний день ни один из методов, призванных заместить функцию печени, не является достаточно эффективным. Среди данных методик (заменное переливание крови, плазмаферез, диализ, гемосорбция) эффективной в некоторых случаях считается гемосорбция на активированном угле с поддержкой простациклином (вводится для подавления агрегации тромбоцитов).
При быстром появлении энцефалопатии, отека мозга и отсутствии эффекта от лечения в течение 24 часов единственным методом спасения жизни пациента может являться трансплантация печени. Трансплантацию достаточно сложно осуществить в столь краткие сроки, а выживаемость после проведенной операции у пациентов со сверхострым некрозом печени не превышает 65% в течение года.
Прогноз и профилактика некроза печени
Прогноз при некрозе печени зависит от очень многих факторов: возраста, причины патологии, длительности энцефалопатии и комы, выраженности полиорганной недостаточности, наличия инфекционных осложнений и др. Плохой прогноз при некрозе печени отмечается при наличии следующих условий: возраст до 10 и после 40 лет; выраженный метаболический ацидоз; длительная желтуха до появления энцефалопатии (более недели); уровень общего билирубина более 300 мкмоль/л. Причиной смерти при некрозе печени могут служить неврологические расстройства, кровотечения (в основном желудочно-кишечные), сепсис, нарушения витальных функций (дыхания и кровообращения), почечная недостаточность. У выживших пациентов функция печени может восстановиться полностью или частично (в этом случае развивается постнекротический цирроз).
Профилактика некроза печени заключается в своевременном выявлении и лечении заболеваний, которые могут привести к развитию этого патологического состояния.
Что такое некроз печени
Некроз печени – это опасное патологическое состояние, которое возникает на фоне заболеваний органа, сильной интоксикации организма, нарушения кровообращения или травмы и сопровождается гибелью печеночных клеток – гепатоцитов. Недуг быстро прогрессирует, что приводит к развитию полиорганной недостаточности или коме.
В зависимости от скорости течения некроз печени классифицируется на несколько форм:
- Сверхострая – диагностируется в течение 7 суток после развития желтухи.
- Острый – период проявления симптомов составляет 8-28 суток.
- Подострый – энцефалопатия возникает на 2-3 месяце течения болезни.
Диагностируется некроз печени достаточно редко. Выявляется заболевание преимущественно у людей молодого и среднего возраста. У более старшего поколения, как правило, диагностируется подострая форма патологии.
В зависимости от степени распространенности некроза по органу выделяют:
- Фокальный некроз – поражает несколько близ расположенных гепатоцитов (часто выявляется при вирусных гепатитах).
- Центролобулярный (зональный) – погибают гепатоциты на определенных долях печени.
- Массивный некроз печени – поражается вся доля органа.
![]()
Причины некроза печени
Некроз печени – это не самостоятельное заболевание, а результат патологических процессов, протекающих в организме. Причиной острой формы болезни чаще всего является гепатит, как правило, вирусной этиологии. Провоцирующим фактором может выступать прием некоторых медикаментозных препаратов или токсических веществ.
Некроз печени может развиваться на фоне патологий сердечно-сосудистой системы, которые связаны с нарушением процесса кровообращения. Недостаточность кровообращения провоцирует развитие некроза, вызывает тотальное поражение паренхимы, что ведет к печеночной недостаточности.
Стать причиной гибели гапетоцитов может радиационное воздействие на организм, сильные травмы органа или влияние на тело высоких/низких температур.
Реже провоцирующим фактором развития некроза печени выступают гемобластозы – это опухолевые клетки, которые инфильтрируют ткань печени и приводят к гибели паренхимы. Повышает риск возникновения патологи прием медикаментозных препаратов, направленных на лечение СПИДа, например, Диданозин, а также острое нарушение метаболических процессов в организме.
Симптомы некроза печени
Клиническая картина заболевания зависит от формы некроза и степени поражения органа. Основной признак патологии – постепенно нарастающая печеночная недостаточность, которая провоцирует развитие печеночной энцефалопатии и приводит к коме.
Первоначальный симптом некроза печени – болезненные ощущения в правом подреберье, появление желтухи (желтизна кожных покровов и глаз) и увеличение органа, что ощущается во время пальпации. Пациента беспокоит тошнота и рвота, значительно ухудшается аппетит, что приводит к резкой потери веса.
По мере прогрессирования заболевания происходит активизация иммунной системы, которая ограничивает очаг повреждения, не допуская распространения патологического процесса на другие органы. Результатом таких изменений является появление отечности, значительное увеличение печени в размере и растяжение ее капсулы. Больного мучают сильные боли, которые локализуются не только в правом подреберье, но распространяются на лопатку, грудину и живот. Если после появления таких симптомов у пациента уменьшается печень и проходить боль – это первый признак гибели значительной части паренхимы, что является крайне неблагоприятным прогнозом.
В результате отмирания гепатоцитов, печень не способна полноценно выполнять свои функции, в частности, проводить дезинтоксикацию. Это приводит к накоплению токсических веществ в организме, что негативно сказывается на работе других внутренних органов. В первую очередь это неблагоприятно влияет на головной мозг, что провоцирует развитие печеночной энцефалопатии. Такое состояние характеризуется повышенной сонливость и постоянной слабостью, чрезмерной агрессией и неадекватным поведением, забывчивостью и тремором конечностей.
В предкоматозном состоянии пациент плохо ориентируется в пространстве и во времени, наблюдается потеря памяти, повышение тонуса мышц и спазмов. Постепенное нарастание отека головного мозга может спровоцировать нарушение дыхание, развитие брадикардии и артериальной гипотензии.
При поражении токсинами почек возникает некроз органов. При этом они не справляются со своей работой, следствием чего является накопление азотистых шлаков в крови. Это ведет к еще большей интоксикации организма и ускоряет развитие энцефалопатии.
Некроз печени провоцирует развитие ДВС-синдрома, который возникает в результате нарушение синтеза белков и ферментов, отвечающих за свертываемость крови. При этом переливание факторов свертывания не дает положительного результата, поскольку для их активизации требуется работа печени.
Высокая концентрация токсинов в крови провоцирует развитие язвы желудка и двенадцатиперстной кишки, а плохая свертываемость провоцирует желудочно-кишечное кровотечение.
Диагностика некроза печени
При первом подозрении на некроз печени следует незамедлительно обратиться за консультацией к гастроэнтерологу. Своевременная диагностика и вовремя начатое лечение позволит избежать развития осложнений (энцефалопатии и комы).
Во время первой консультации врач собирает анамнез и изучает историю болезни пациента, чтобы установить возможные причины гибели гепатоцитов. Специалист выполняет визуальный осмотр, выявляя наличие желтухи и пальпирует печень для оценки размеров органа.
С целью получения полной картины о состоянии печени и других внутренних органов выполняется ряд лабораторных тестов и инструментальных видов исследования:
- Ультразвуковое исследование и МРТ печени и желчного пузыря. Однофотонная эмиссионная КТ печени. Данные исследования позволяют оценить поражения паренхимы.
- Пункция печени с дальнейшим морфологическим исследованием биоптатов, что позволяет оценить общее состояние органа и степень повреждения гепатоцитов.
- Биохимические пробы печени, во время которых исследуется уровень азотистых шлаков.
- ЭЭГ для выявления энцефалопатии.
- Определение уровня антител к основным антигенам гепатитов В, С и D.
![]()
Лечение некроза печени
Лечение некроза печени проводится в отделении интенсивной терапии. Главная цель – устранение печеночной недостаточности, нормализация функционирования органа и предотвращение развития осложнений. Во время лечения регулярно исследуется уровень азотистых шлаков и электролитов в крови. Это дает возможность оценивать динамику терапии и при необходимости корректировать его.
Лечение некроза печени включает следующие мероприятия:
![]()
Регулярное внутривенное введение витамина К, который позволяет избежать кровотечений. При этом переливание факторов крови не приносит должного эффекта, поэтому не применяется в лечебных целях.- Прием препаратов, подавляющих выработку соляной кислоты, что позволяет снизить риск возникновения язвы желудка и 12-перстной кишки.
- Для снятия спазмов назначается Диазепам.
- В особо сложных случая применяется парентеральное питание с применением аминокислотных растворов.
Нормализовать работу почек можно только путем восстановления здоровья печени. При этом диализ может привести к сильным кровотечениям или генерализации инфекционного процесса, поэтому он не проводится.
Для борьбы с печеночной энцефалопатией применяются антибактериальные препараты – Метронидахол или Неомицин, а для восстановления кишечной микрофлоры используется Лактулоза. При прогрессировании патологии спасти жизнь пациенту поможет только трансплантация органа в течение 24 часов. Но даже проведение экстренной операции не дает 100% гарантии. После оперативного вмешательства выживаемость пациентов составляет 65%.
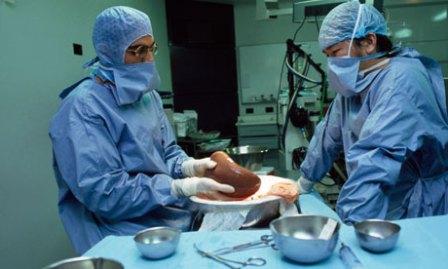
Симптоматическое лечение включает прием жаропонижающих препаратов, противорвотных и обезболивающих медикаментов, а также иммуномодуляторов.
Прогноз при некрозе печени зависит от множества факторов. Прежде всего это возраст пациента и его общее состояние здоровья; причины, спровоцировавшие патологию; запущенность болезни; наличие осложнений и др. Крайне неблагоприятный прогноз при развитии некроза печени у пациентов младше 10 лет или старше 45, наличие метаболического ацидоза, длительной желтухи и повышении билирубина свыше 300 мкмоль/л.
Снижают шансы на выздоровление неврологические расстройства, сильные кровотечения, сепсис и нарушение витальных функций. У выживших пациентов возможно полное или частичное восстановление печени, при этом часто развивается постнекротический цирроз.
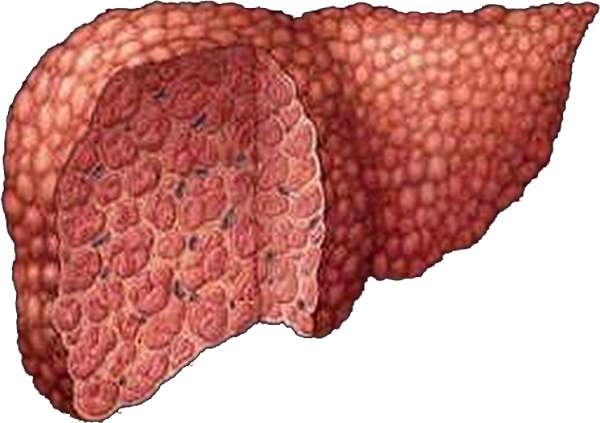
Профилактика некроза печени
Предотвратить развитие некроза печени поможет своевременное лечение заболеваний и патологий, которые его провоцирует (прежде всего гепатитов).
Читайте также: