Противовирусный белок в организме
Что такое противовирусный иммунитет? Это механизм защиты организма, который обеспечивает бесперебойную работу внутренней среды и вступает во взаимодействие с патогенным инфекционным агентом. В современной иммунологии этот раздел занимает преимущественную часть теоретического курса. Его изучение имеет первостепенное значение для будущих иммунологов.
Что такое вирус и как на него реагирует иммунитет
В природе инфекционных микроорганизмов вирусам отводится уникальный статус: все возбудители различных заболеваний, известные современной науке, имеют молекулярную неклеточную организацию. Вирус – это своего рода внутриклеточный паразит, который обладает специфическим механизмом репродукции и взаимодействия с клетками организма. Благодаря многообразию вирусных инфекций ученым удалось определить тип патогенеза заболеваний, вызываемых ими, и характер иммунологической реакции.
Основной задачей микробиологии противовирусного иммунитета является создание эффективных лекарственных препаратов, которые должны помогать организму бороться с инфекцией и наладить эффективный защитный механизм в случае повторной вирусной атаки. Для этого важно определить степень устойчивости патогена к воздействию естественных и искусственных противовирусных комплексов, которые формируются после излечения от инфекции.
Сформированный организмом противовирусный иммунитет может иметь разную напряженность и продолжительность. Также стоит уточнить, что иммунологическая реакция в ответ на инфицирование возникает не во всех случаях. Невосприимчивость к болезнетворным агентам отдельных видов заложена на генетическом уровне. Главным условием формирования таких механизмов противовирусного иммунитета является отсутствие в клетках специфических субстратов. Без них не происходит взаимодействия с инфекцией и блокируется ее размножение. Из-за невозможности репродукции вируса в организме заболевание не развивается.
Общие физиологические факторы формирования иммунной защиты
Врожденный противовирусный иммунитет есть у каждого человека. Главным условием его выработки является наличие неспецифических факторов, которые обеспечивают защиту клеток и молекул от воздействия инфекции. Чтобы спровоцировать развитие заболевания, патоген должен пройти несколько естественных барьеров в организме человека. Каждый из них и является тем самым неспецифическим фактором противовирусного иммунитета.

Первый этап – это кожно-слизистые ткани. На них приходится первая атака патогенных микроорганизмов. Крепким противовирусным иммунитетом обладают неповрежденные кожные покровы и слизистые оболочки, служащие не только механическим, но и стерилизующим препятствием. В противном случае вирус проникает далее вглубь организма. К инфицированному участку начинают активно прибывать фагоциты, которые ограничивают пораженную область от остальных здоровых тканей и ограничивают распространение инфекции.
К особенностям противовирусного иммунитета относится повышение температуры тела. При умеренной лихорадке (до 40 °С), с которой многие активно борются, активизируется иммуногенез, запускается метаболизм и увеличивается продуцирование интерферона – естественного противовирусного вещества. При высокой температуре тела возникает непосредственная инактивация внеклеточного агента, а его репродукция подавляется за счет снижения рН внеклеточной и внутриклеточной среды. В кислой среде инфекция погибает быстрее.
В отличие от бактерий, большинство вирусов легко проходят почечную систему, нисколько не отражаясь на функциональности органов. Буквально через час после заражения вирусы появляются в моче, что способствует скорейшему восстановлению относительного постоянства внутренней среды организма. Именно поэтому при вирусной инфекции пациенту рекомендуется пить как можно больше жидкости. При этом возбудители выделяются не только почками, но и слюнными железами, кишечником.
Вирус в крови: роль иммуноглобулинов, макрофагов, гормонов
К неспецифическим факторам противовирусного иммунитета относится гамма-глобулин, который содержится в сыворотке крови и участвует в процессе естественной нейтрализации вирусов. Похожую функцию выполняют и ингибиторы – неспецифические противовирусные белки, присутствующие в секрете эпителия слизистой органов дыхания и желудочно-кишечного тракта. Все эти элементы противовирусного иммунитета в микробиологии считаются основными факторами, подавляющими активность патогенов. Вирусы находятся вне чувствительной клетки, а именно в крови и других жидких тканях.

Защитные функции ингибиторов такие же, как и у антител, что зависит от типа вирусной инфекции и его количественной нагрузки на организм. На активность ингибиторов и гамма-глобулина влияют индивидуальные и возрастные особенности. Противовирусный иммунитет выше при низком содержании ингибиторов, поскольку они имеют свойство освобождаться и восстанавливать свою активность. У людей зрелого возраста ингибиторов становится больше, но нейтрализованный ими вирус впоследствии становится объектом влияния других иммунологических факторов.
На резистентности к вирусной инфекции сказывается баланс гормонального фона. Так, например, увеличение концентрации кортизона в организме снижает защитные функции, а в малых дозах – повышает. Отдельного внимания среди факторов противовирусного иммунитета заслуживают макрофаги – клетки, фагоцитирующие чужеродные частицы при попадании последних в кровоток. Защищают организм от вирусов такие макрофаги:
- моноциты крови;
- клетки костного мозга;
- клетки печени;
- макрофаги селезенки;
- лимфоциты.
Все эти элементы участвуют в процессах образования антител, кооперируясь с Т- и В-лимфоцитами. Вирусный агент адсорбируется и поглощается лейкоцитами, но в дальнейшем его разрушение не происходит и процесс приостанавливается на этапе фагоцитоза. В завершении этого процесса нет явной необходимости. Макрофаги не способны переваривать вирусы, а это главный принцип защиты, поэтому фагоцитозу отведена второстепенная роль в иммунологии. Противовирусный иммунитет в данном случае больше зависит от интерференции организма.
Интерферон лейкоцитарный человеческий
Если инфекция преодолевает вышеуказанные общие физиологические и гуморальные факторы, ей удается проникнуть в чувствительную клетку. После этого запускается процесс внутриклеточного развития вируса, но в некоторых случаях проникновение инфекции не всегда сопровождается внутриклеточным поражением. Морфологически клетка не меняется, никаких деструктивных процессов в ней не происходит, поэтому в дальнейшем она становится устойчивой к штаммам этого вируса.

Противовирусный иммунитет, выработанный в результате вирусной интерференции, считается самым сильным. В его материальной основе лежит продуцирование особого вещества – интерферона. Этот белок образуется как ответная реакция на проникновение патогена в клетку. Интерферон обладает противовирусными, антипролиферативными и иммуномодулирующими свойствами и теряет свою активность, но не погибает при низких температурах. Разрушить его можно воздействием ультрафиолета и высоких температур (выше 60 °С).
В крови интерферон появляется спустя 1-2 часа после проникновения вируса и максимальной концентрации достигает через 4-8 ч. Белок возникает как реакция в ответ не только на проникновение вирусов, но и бактерий, продуктов их жизнедеятельности, являясь основным элементом противовирусного иммунитета.
Интерферон присутствует в крови, моче, спинномозговой жидкости, секрете носоглотки, в почках, легких и в соединительной ткани организма. Его вырабатывают практически все клетки, но в большей степени этот белок продуцируется селезенкой и лейкоцитами. Принцип действия интерферона состоит в подавлении функции размножения вируса при полном сохранении жизнедеятельности клетки.
Отличие приобретенного иммунитета от врожденного
Иммунная система защиты организма от патогенных микроорганизмов бывает двух видов – врожденной и приобретенной. С точки зрения иммунологии предназначение приобретенного иммунитета, который появляется у человека в течение жизни, заключается в поддержке врожденного. В отличие от врожденного иммунитета, который имеется от рождения и активизируется при вторжении чужеродного микроорганизма, приобретенный иммунитет формируется только после контакта с инфекцией и активизируется в случае ее повторной атаки.
Один из способов получить приобретенный иммунитет к тому или иному вирусу – пройти вакцинацию. При первоначальном контакте с чужеродным агентом запускается несколько действий, которые приводят к запуску работы лимфоцитов и синтезу белков, обладающих повышенной реактивностью против чужеродных частиц. В результате этого процесса организм приобретает защитную систему, которая уверенно противостоит последующим атакам.

Люди, которым удалось выжить при течении смертельно опасных эпидемий бубонной чумы и оспы, в последующем проявляли большую устойчивость к инфекции, чем те, кто ни разу не встречался с болезнью. Открывателем приобретенного противовирусного иммунитета считают англичанина Э. Дженнера.
В конце XVIII века этот врач провел научно-практический эксперимент, за который сегодня был бы лишен лицензии и попал под суд. Дженнер ввел ребенку ничтожную дозу гноя, изъятого из очага поражения у женщины, болевшей коровьей оспой. Таким образом, он попытался намеренно заразить ребенка, но эксперимент прошел успешно: заболевание так и не возникло, несмотря на контакт с возбудителем.
История вакцинации
После проведенного эксперимента по выработке у ребенка приобретенного иммунитета к коровьей оспе многие ученые озадачились созданием теории иммунизации. Но о вакцинации в широких массах стало известно лишь через сотню лет после эксперимента Дженнера. Кроме того, исследователи смогли установить, что иммунитет формируется не только к вирусам и бактериям, но и к продуктам их жизнедеятельности.
Сегодня доказанным фактом является то, что иммунная защита возникает в отношении бесчисленного множества естественных и искусственных элементов, включая металлы, химические соединения с низкой молекулярной массой, белки, углеводы, нуклеотиды и другие антигены, в ответ на которые возникает иммунная реакция.
Основные средства для укрепления иммунитета
Для усиления свойств противовирусного иммунитета, необходимых для борьбы с различными инфекциями, фармакологическая отрасль занимается разработкой лекарственных препаратов, относящихся к категории противовирусных и иммуностимулирующих. Вне зависимости от причины ослабления иммунитета, выбор такого медикамента следует доверять врачу-иммунологу. На сегодняшний день выпускаются иммуномодулирующие средства в различных лекарственных формах для взрослых и детей.
Классифицируют их следующим образом:
- стимуляторы натурального происхождения;
- препараты на бактериальной основе;
- биогенные стимуляторы;
- индукторы выработки интерферонов человека;
- лекарства животного происхождения (из вилочковой железы крупного рогатого скота);
- адаптогенные иммуномодуляторы;
- синтетические препараты.
В раннем возрасте
Лекарства, укрепляющие противовирусный иммунитет и повышающие защитные свойства организма у детей, важно выбирать с учетом индивидуальных особенностей развития ребенка. Необходимости в назначении иммуномодуляторов детям младше шестимесячного возраста, как правило, не возникает, потому что с самого рождения надежную защиту детскому организму обеспечивает материнский иммунитет. После полугода наступает период перехода иммунной защиты на продуцирование собственных иммуноглобулинов.

Детям, не достигшим трех лет, для повышения иммунного статуса врачи назначают препараты из серии интерферонов. В более старшем возрасте эффективнее применять растительные средства либо медикаменты с нуклеиновой кислотой.
Иммуномодуляторы на натуральной основе
Помимо эхинацеи, используются и другие средства для повышения иммунитета. Противовирусными свойствами обладают не менее эффективные:
- Настойка элеутерококка – курс прием для взрослых составляет 30 дней. Лекарство не просто укрепляет организм, но и придает жизненных сил, бодрости.
- Настойка корня женьшеня. Производит аналогичный терапевтический эффект, но в отличие от экстракта элеутерококка, имеет ряд ограничений к применению.
- Настойка лимонника китайского. Повышает стрессоустойчивость и укрепляет иммунитет, делая организм устойчивым к ОРВИ в период массовой заболеваемости.
Препараты с бактериями, повышающие иммунитет
Чтобы повысить устойчивость к заражению, применяются особые стимуляторы для иммунитета. Противовирусные средства такого типа содержат ничтожное количество микробов, частицы их структур. В результате попадания веществ в организм возникает ответная реакция. К бактериальным препаратам с иммуностимулирующими свойствами, относятся:
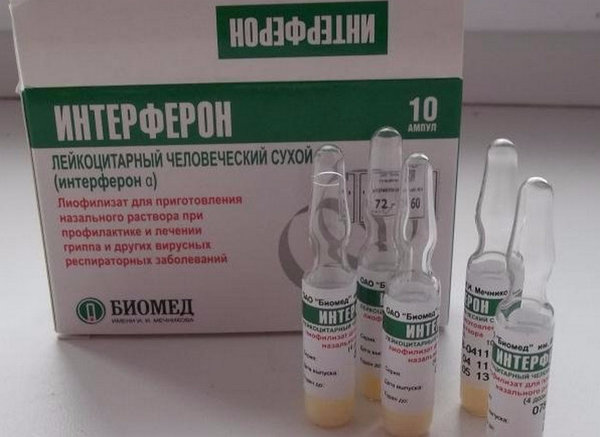
Лекарства с интерфероном
Сомнений в том, насколько высока эффективность интерферонов, у врачей нет. Препараты этой группы назначают при первых симптомах простудных заболеваний, а также в период обострения хронических вирусных инфекций. Противовирусные препараты для иммунитета позволяют остановить развитие симптомов болезни, повысить общую сопротивляемость организма. Однако в профилактических целях интерферон не используется.
Другие иммуностимуляторы
В категорию искусственных стимуляторов неспецифического действия включены витаминно-минеральные комплексы, содержащие коферменты – низкомолекулярные соединения белков со структурами небелкового типа.

Важно понимать, что любое средство, обладающее иммуностимулирующими свойствами, неправильно воспринимать как панацею против всех вирусных болезней. Большинство вирусов, попав в организм человека, остаются в нем до конца жизни. И хотя полностью избавиться от инфекции не удастся, нужно постоянно укреплять противовирусный иммунитет, чтобы держать под контролем заболевание и не допускать развития осложнений.

Для лечения гриппа и других ОРВИ АМИКСИН ® может применяться у взрослых и детей с 7 лет.
Узнать подробнее про АМИКСИН ® …

Противовирусный препарат АМИКСИН ® направлен на борьбу с большинством распространенных респираторных вирусов, включая вирусы гриппа.
Узнать больше…

Современные противовирусные препараты, такие как АМИКСИН ® , могут способствовать снижению риска развития осложнений на фоне гриппа и других ОРВИ.
Подробнее…


Для лечения гриппа и других ОРВИ у детей старше 7 лет АМИКСИН ® выпускается в дозировке 60 мг.
Узнать подробнее о детском "Амиксине"…

АМИКСИН ® обладает не только иммуностимулирующим, но и противовирусным действием за счет подавления трансляции вирус-специфических белков.
Узнать подробнее…

Вирусы гриппа и других ОРВИ способны формировать устойчивость к некоторым противовирусным препаратам. АМИКСИН ® способствует стимулированию собственных ресурсов организма на борьбу с инфекцией…
Читать подробнее…

Механизм действия противовирусных средств
Иммунная система умеет распознавать зараженные клетки, поэтому многие противовирусные лекарственные средства направлены на стимулирование собственного иммунитета. Они называются иммуностимуляторами (иммуномодуляторами).
Вообще, создание эффективного противовирусного средства — задача нетривиальная, поскольку вирусы паразитируют внутри клеток, и как в этом случае уничтожить пришельца, не нанеся вреда организму хозяина?
На сегодня в России чаще всего применяется клинико-фармакологическая классификация, означающая, что разделение препаратов на группы производится в зависимости от того, на какие именно виды вирусов они воздействуют [2] . Внутри каждой узкоспециализированной группы препаратов обычно приводится классификация противовирусных средств по механизмам их действия. Давайте изучим вопрос на конкретном примере:
Как можно убедиться, спектр противовирусных лекарственных средств весьма широк. Большую его часть составляют препараты прямого противовирусного действия (ПППД), что означает их специфичность, направленность на конкретные виды вирусов. Однако эти лекарства зачастую оказывают разрушающее воздействие не только на геном вируса и его способность к репликации (размножению), но и на здоровые клетки хозяина. В общем случае можно констатировать, что чем мощнее противовирусный препарат, тем больше у него побочных эффектов. Это обязательно следует учитывать.
В то же время существует категория противовирусных средств неспецифичного (широкого) спектра действия. Преимущественно, это иммуностимуляторы (иммуномодуляторы), призванные активизировать резервные силы организма для борьбы с самыми разнообразными вирусами и другими микроорганизмами.
Итак, вот пример некоторых противовирусных препаратов, разрешенных детям:
Ограничения по возрасту могут быть вызваны не только составом средства, но и его формой выпуска. Например, таблетки не рекомендуются для приема детям до 3 лет, а капсулы — до 7 лет.
- прикрепление вирусов к клеткам;
- проникновение их в клетки;
- размножение;
- выход из клеток.

В условиях пандемии многие государства приступили к созданию лекарств и вакцин от нового коронавируса. Сообщается, что в России разработка прошла первую фазу — так ли это? Значит ли, что скоро можно ждать появления препарата? Чтобы разработать новое лекарство от неизвестного заболевания по всем правилам научного поиска нужно от 5 до 15 лет. Разобрали весь процесс на примере COVID-19 вместе с Равилем Ниязовым, специалистом по регуляторным вопросам и разработке лекарств Центра научного консультирования.
COVID-19 — инфекционное заболевание, вызываемое коронавирусом SARS-CoV-2. В тяжелых формах оно поражает легкие, иногда — сердце и другие органы. Особенно тяжело заболевание протекает, если у больного есть другие нарушения со стороны дыхательной или сердечно-сосудистой систем. Молниеносно возникшая пандемия COVID-19 поставила вопрос разработки лекарств и вакцин от новой инфекции. Это долгий процесс с множеством стадий, на каждой из которых исключают вещества-кандидатов. Только одно или небольшая группа таких веществ в итоге сможет стать безопасным и эффективным лекарством.
Шаг 1: понять, как развивается новое заболевание
Любая болезнь нарушает естественные физиологические и биохимические процессы в организме. Причины заболеваний могут быть разными, в том числе — инфекционными. Инфекционный агент (в случае COVID-19 это коронавирус SARS-CoV-2) заимствует и эксплуатирует биохимический аппарат клеток, перехватывая управление им, в результате чего клетки перестают выполнять свою физиологическую функцию. Для вируса SARS-CoV-2 основной мишенью являются клетки дыхательного эпителия, отвечающие за газообмен, то есть за дыхание.
Лекарством для лечения COVID-19 будет считаться любое вещество или комбинация веществ, которое будет способно (1) инактивировать вирус еще до того, как он успеет поразить клетку, или (2) нарушать жизненный цикл вируса внутри зараженной клетки, или (3) защищать новые непораженные здоровые клетки от инфицирования.
Чтобы создать лекарство от SARS-CoV-2, нужно хорошо знать, каков жизненный цикл вируса в организме человека:
- с какими клетками человека и через какие рецепторы на поверхности клеток он связывается, какой собственный вирусный аппарат для этого он использует;
- как вирус проникает в клетку;
- как вирус эксплуатирует биохимический аппарат клетки, чтобы воспроизводить собственный генетический материал и белки, нужные для сборки новых вирусных частиц;
- как вирус покидает инфицированную клетку, чтобы инфицировать новые клетки;
- как формируется иммунитет против вируса и какой вклад иммунитет вносит в тяжесть заболевания (чрезмерная иммунная реакция может вызывать тяжелое поражение внутренних органов).

Всё перечисленное — это совокупность фундаментальных знаний, необходимых для перехода к следующему этапу разработки лекарства — синтезу или биосинтезу веществ, которые могут нарушать свойства вирусных частиц, убивая вирус и при этом не вредя человеку. Например, так работают лекарства от ВИЧ-инфекции или гепатита C. Но при этих заболеваниях важно применять сразу несколько веществ из разных классов, чтобы вирус не становился устойчивым к терапии. Об этом нужно будет помнить и при разработке лекарств против SARS-CoV-2.
Для лечения вирусных заболеваний также могут использоваться иммуносыворотки, содержащие антитела, способные инактивировать вирус. Такие сыворотки можно получать от животных, например, лошадей или кроликов, но также и от человека, уже переболевшего заболеванием.
Однако самый эффективный подход — профилактика заболевания. Для этого используют вакцины — естественные или генетически модифицированные белки вируса, а иногда и живой, но ослабленный вирус. Вакцина имитирует инфекционное заболевание и стимулирует организм к формированию иммунитета. В последнее время также разрабатываются РНК- и ДНК-вакцины, но пока одобренных препаратов нет.
В отличие от традиционных вакцин, РНК-/ДНК-вакцины содержат не вирусные белки, а гены, кодирующие основные вирусные белки. Введение такой вакцины приводит к синтезу клетками белков вируса, на которые должна реагировать иммунная система и вырабатывать иммунитет против этих белков вируса. Гипотетически это должно препятствовать началу инфекционного процесса при заражении настоящим патогенным вирусом. Важно отметить, такие РНК- и ДНК-вакцины не должны кодировать те белки вируса, которые способны были бы привести к настоящей вирусной инфекции.
Шаг 2: поиск хитов
На ранней стадии разработки синтезируют и тестируют множество веществ — библиотеку. Основная цель этого этапа — найти группу хитов (hit — попадание в цель), которые бы связывались с нужной вирусной мишенью. Обычно это один из белков вируса. Иногда отбор идет из библиотек, состоящих из миллиардов низкомолекулярных веществ. Сейчас активно используют компьютерные алгоритмы — машинное и глубокое обучение — чтобы искать новые потенциально активные молекулы. Одна из компаний, успешно работающая в этом направлении, — InSilico Medicine, создана российскими математиками.
Другой источник потенциальных лекарств — выздоровевшие люди: в их крови содержатся антитела, часть из которых способны связываться с вирусом и, возможно, нейтрализовать его.
Шаг 3: поиск и тестирование лидов
Когда находят группу хитов, способную связываться с вирусным белком, переходят к следующему этапу скрининга. На этом шаге исключаются вещества, которые:
- нестабильны и быстро разлагаются;
- тяжелы/затратны в синтезе;
- токсичны для различных клеток человека в условиях лабораторных экспериментов на культуре клеток. Вещества не должны быть токсичны сами, токсичностью также не должны обладать продукты их метаболизма в организме, продукты их разложения и примеси, возникающие в процессе производства; вместе с тем если процесс производства способен с помощью очистки удалять продукты разложения или примеси, то такой хит может и не будет выведен из разработки;
- плохо растворимы в воде — лекарство должно в достаточном количестве растворяться в биологических жидкостях, чтобы распределиться по организму;
- быстро разлагаются в живом организме;
- плохо проникают через слизистые оболочки, клеточные мембраны или внутрь клетки, в зависимости от пути введения лекарства и расположения вирусной мишени.
Хиты, которые выдерживают эти испытания и проходят все фильтры, переводят в категорию лидов (lead — ведущий).
Лиды тестируют в еще более широкой серии экспериментов для принятия так называемых решений Go/No-Go о продолжении или остановке разработки. На этой стадии инициируются испытания на животных. Такая схема отбора нужна чтобы как можно раньше вывести из разработки бесперспективные молекулы, потратив на них минимальные время и ресурсы, поскольку каждый последующий этап является еще более затратным.
Те несколько лидов, которые успешно проходят очередные испытания, становятся кандидатами. К этому моменту разработка может длиться уже от трех до семи лет.
Шаг 4: испытания кандидатов и клинические исследования

Прежде чем перейти к испытаниям на людях, нужно выполнить исследования на животных и подтвердить отсутствие неприемлемой для человека токсичности, подобрать первоначальную безопасную дозу. На этом этапе кандидаты тоже могут отсеиваться — например, из-за генотоксичности (токсичности для генетического аппарата клетки) или канцерогенности (способности вызывать рак). Еще они могут оказаться небезопасными для беременных женщин или женщин детородного возраста, вызывать поражение головного мозга, печени, почек, сердца или легких. В зависимости от природы молекулы исследования проводят на грызунах, собаках, обезьянах, минипигах, кроликах и т.д.
В зависимости от природы заболевания, особенностей его терапии и свойств лекарства, какие-то исследования могут не проводиться или быть не значимы. Например, оценка канцерогенности лекарства не потребуется, если оно будет применяться в лечении краткосрочных заболеваний, как в случае COVID-19. Генотоксичность не оценивают для биопрепаратов или если лекарство предназначено для лечения метастатического рака и т. д. Суммарно доклинические исследования могут занимать 3–5 лет. Часть из них проводится параллельно с клиническими исследованиями.
Если доклинические исследования успешны, начинается клиническая разработка, которая условно делится на фазы. Это нужно, чтобы постепенно и контролируемо тестировать лекарство на все большем количестве людей. И снова стадийность процесса позволяет прекратить разработку на любом этапе, не подвергая риску многих людей.
- Первая фаза: здесь подтверждают первичную безопасность для людей в принципе, изучают поведение лекарства в организме человека, его биодоступность (способность достигать места действия в достаточных концентрациях), его взаимодействие с другими лекарствами, влияние пищи, половых и возрастных различий на свойства лекарства, а также безопасность для людей с сопутствующими заболеваниями (особенно важны заболевания печени и почек — эти органы отвечают за метаболизм и выведение лекарств), проверяют, не вызывает ли лекарство нарушение ритма сердца. Кроме того, на I фазе оценивают безопасный диапазон доз: эффективные дозы не должны быть неприемлемо токсичными.
- Вторая фаза: здесь начинают проверять эффективность лекарства на пациентах с заболеванием. На ранней II фазе оценивают, работает ли кандидатная молекула на людях с изучаемым заболеванием в принципе, а на поздней II фазе подбирают режим дозирования, если кандидатное лекарство было эффективным. При этом вещество, эффективное в лабораторных экспериментах, на животных моделях заболевания и даже в ранних клинических исследованиях на людях, вполне может не быть таким же рабочим в реальной медицинской практике. Поэтому и нужен длительный процесс поэтапной исключающей разработки, чтобы на выходе получить эффективное и безопасное лекарство.
- Третья фаза: здесь подтверждают эффективность и безопасность лекарства, а также доказывают, что его польза компенсирует те нежелательные реакции, которые неминуемо будет вызывать лекарство. Иными словами, в исследованиях третьей фазы надо понять, что баланс пользы и рисков положителен. Это всегда индивидуально. Например, у людей с ВИЧ в целом допустимо, если противовирусные лекарства вызывают некоторые нежелательные реакции, а в случае онкологических заболеваний приемлемы и более выраженные токсические реакции.
В случае вакцин, которые рассчитаны на здоровых людей, и особенно детей, приемлемы лишь легкие нежелательные реакции. Поэтому найти баланс трудно: вакцина должна быть высоко эффективной, и при этом вызывать минимальное число тяжелых реакций, например реже, чем 1 случай на 1000, 10 000 или даже 100 000 вакцинированных людей. Клиническая разработка может длиться до 5–7 лет, однако низкомолекулярные противовирусные лекарства для краткосрочного применения, как в случае COVID-19, можно протестировать быстрее — за 1–2 года.
Разработка многих отечественных противовирусных и иммуномодулирующих препаратов не соответствует такому научно выверенному процессу разработки.
Шаг 5: производство
Важный этап — наладить производство лекарства. Разработка процессов синтеза начинается в самом начале отбора лидов и постепенно дорабатывается, оптимизируется и доводится до промышленного масштаба.
В настоящее время против SARS-CoV-2 разрабатывается много разных методов лечения:
- низкомолекулярные соединения, которые нарушают жизненный цикл вируса. Трудность в том, что может быть нужно применять сразу несколько противовирусных лекарств. Сейчас надежды возлагают на ремдесивир. Есть данные, что может быть эффективен давно известный гидроксихлорохин, действующий не на сам вирус, а влияющий на иммунитет. Информацию, что комбинация лопинавира и ритонавира оказалась неэффективной у тяжелобольных пациентов, стоит интерпретировать с осторожностью: она может быть эффективна при более легких формах, или для профилактики, или у каких-то определенных подгрупп;
- противовирусные, в том числе моноклональные, антитела, которые связываются с ним на поверхности и блокируют его проникновение в клетку, а также помечают вирус для клеток иммунной системы. Антитела можно получать как биотехнологически, так и выделять из крови переболевших людей. Сейчас тестируются препараты, получаемые с помощью обоих методов;
- вакцины. Они могут представлять собой естественные или модифицированные белки вируса (модификации вводят для усиления выработки иммунитета), живой ослабленный вирус, вирусоподобные наночастицы, синтетический генетический материал вируса (РНК-вакцины) для того, чтобы сам организм человека синтезировал некоторые белки вируса и смог выработать антитела к нему. Одна из проблем в случае вакцин — простое введение белков вируса, пусть и модифицированных, не всегда позволяет сформировать иммунитет, способный защитить от реального заболевания — так называемый стерильный иммунитет. Даже образование антител в ответ на введение вакцины не гарантирует защиты: хорошим примером являются те же ВИЧ и гепатит C, хотя вакцина против гепатита B достаточно проста и при этом высокоэффективна. Хочется надеяться, что отечественные разработчики следуют рекомендациям Всемирной организации здравоохранения по проведению доклинических и клинических исследований вакцин, включая исследования провокации и изучение адъювантов;
- препараты для РНК-интерференции. Так называемые малые интерферирующие рибонуклеиновые кислоты (РНК) — это небольшие отрезки синтетически получаемой РНК, которые способны связываться с генетическим аппаратом вируса и блокировать его считывание, мешая синтезу вирусных белков или воспроизведению генетического материала вируса.
Процесс разработки лекарства — это научный поиск с неизвестным исходом. Он занимает много времени и требует участия большой команды профессионалов разных специальностей. Однако только реальный клинический опыт позволит оценить, удалось ли получить не только эффективное, но и безопасное лекарство, поэтому любое точное определение сроков получения лекарства — спекуляция. Получить эффективную и безопасную вакцину к концу года, если следовать всем правилам научного поиска, вряд ли удастся.
Детальные обсуждения процессов разработки новых лекарств и возникающих в связи с этим проблем — на YouTube-канале PhED.
Читайте также:


