Современные проблемы вирусных гепатитов
В апреле 2016 г. на Ассамблее Всемирной организации здравоохранения (ВОЗ) было принято решение о глобальной ликвидации вирусных гепатитов как проблемы общественного здравоохранения к 2030 г. Необходимость программы определяется значимостью для человечества этих инфекций, а также разработкой современных вакцинных и лечебных препаратов, которые могут защитить и вылечить больных вирусными гепатитами.
В послании Президента РФ В.В. Путина Федеральному собранию 1 марта 2018 г. (далее – Послание Президента РФ) были поставлены задачи, в аспекте которых может быть рассмотрена проблема борьбы с вирусными гепатитами. Задачу по контролю и искоренению вирусных гепатитов прежде всего необходимо рассматривать как амбициозную, которая может и должна быть решена российским здравоохранением. Послание Президента РФ уделено значительное внимание демографическим проблемам России и увеличению продолжительности жизни граждан.
Как известно, вирусные гепатиты являются существенным бременем для экономики России, поражая в основном трудоспособное население. Доля смертей от вирусных гепатитов в трудоспособном возрасте составляет почти 70%, причем смертность от этой патологии с 2012 по 2016 г. возросла среди всего населения на 40%, а среди трудоспособного – на 60%. К тому же вирусные гепатиты приводят к увеличению летальных исходов от цирроза, рака печени и ряда других заболеваний.
По подсчетам ВОЗ, число смертей, ассоциированных с гепатитами, сопоставимо с уровнем смертей от вируса иммунодефицита человека (ВИЧ). Исходя из этого расчета в РФ вирусные гепатиты ежегодно являются причиной гибели не менее 20 тыс. человек, жизни которых можно было бы сохранить.
Для разработки Стратегии на первом этапе требуется объективно оценить распространенность этой патологии среди различных возрастных групп населения, для того чтобы в последующем определить специфические меры по профилактике и лечению гепатитов среди них. Для этого необходимо проведение эпидемиологического исследования (выявление маркеров гепатитов В, D, С, А и Е) на территории как минимум трех субъектов РФ. Для исследований предлагаются Республика Татарстан, Республика Саха (Якутия) и Калининградская область.
Вирусные гепатиты: ситуация в РФ
Значимость всех форм вирусных гепатитов (гепатиты А, В, С, D и Е) для страны очевидна. Сохраняются относительно высокие показатели заболеваемости вирусными гепатитами, особенно хроническими гепатитами С и В. При этом каждый гепатит имеет свои особенности: по распространению (регионам, возрастным группам и группам риска), тяжести течения (включая такую форму, как фульминантный, или молниеносный, гепатит, который в большинстве случаев заканчивается смертью пациента), исходам (развитие хронического гепатита, цирроза и первичного рака печени), поражению разных возрастных групп, экономическим потерям.
Сегодня эпидемиология вирусных гепатитов изменилась: она определяется как динамикой эпидемического процесса, так и проводимыми мероприятиями по их профилактике.
Гепатит А (ГА). Интенсивность циркуляции вируса гепатита А (ВГА) среди населения РФ уменьшилась, что привело к увеличению числа людей без наличия антител к ВГА и, как следствие, повышению риска возникновения вспышек этой инфекции (в 2017 г. зарегистрированы вспышки в Европе и США), смещению заболеваемости на старшие возрастные группы и, как следствие, увеличению числа среднетяжелых и тяжелых форм заболевания. Многолетние циклы заболеваемости ГА в различных регионах РФ переходят в стадию подъема заболеваемости, что отражает рост заболеваемости в 2017 г. по сравнению с 2016 г. – более чем в 1,5 раза. Незначительное количество лиц, ежегодно вакцинируемых в России, не может обеспечить контроль ГА.
Гепатит С (ГС) сегодня занимает центральное место в программах по ликвидации вирусных гепатитов. Это определяется важностью проблемы и появлением высокоэффективных методов лечения. Как и при ОГВ, заболеваемость острым ГС находится на самом низком уровне с начала официальной регистрации (2017 г. – 1,22 на 100 тыс. населения). Несмотря на отсутствие вакцины против ГС, снижение заболеваемости произошло за счет уменьшения количества лиц, вновь вовлекаемых в группы повышенного риска (принимающих наркотические препараты, гомосексуалистов и др.) инфицирования ГС. который чаще всего проходит бессимптомно, формируется хронический гепатит (60–70%). Показатель хронического ГС (ХГС) в 2017 г. – 34,68 на 100 тыс. населения (50 777 заболевших). Суммарно количество больных ХГС, проживающих в РФ, варьирует от 1,5 до 2,5 млн человек. Как и при ХГВ, больные ХГС служат резервуаром для последующего развития цирроза и первичного рака печени, асcоциированного с вирусным ГС.
Гепатит D (ГD). На территории РФ существуют регионы, гиперэндемичные по ГD (Республика Якутия, Республика Тыва). ГD обычно протекает значительно тяжелее, чем другие вирусные гепатиты. Более частое и быстрое по сравнению с ГВ и ГС развитие цирроза и первичного рака печени определяет его важность для гиперэндемичных регионов. Пробема усугубляется отсутствием эффективных методов терапии. Однако необходимость репликации ВГВ для существования D-инфекции определяет вакцинопрофилактику против ГВ как основной инструмент профилактики ГD.
Гепатит Е (ГЕ). Официальная регистрация заболеваемости ГЕ в РФ была начата лишь в 2013 г. На протяжении прошедших лет она имеет низкие показатели. Так, в 2017 г. она составила всего 0,11 на 100 тыс. населения (158 заболевших). В то же время в этом году в Великобритании и Германии число заболевших, по данным литературы, достигало около 50 тыс. человек в каждой из стран. Высокий уровень антител к вирусу ГЕ среди здорового населения РФ (1,5–5%), а также частое обнаружение вируса ГЕ среди поросят (патогенного штамма вируса и для человека) свидетельствует о скрытой интенсивной циркуляции ГЕ в РФ. Вероятнее всего, диагностика этой инфекции недостаточно внедрена в практику отечественного здравоохранения.
Таким образом, вирусные гепатиты остаются важной проблемой отечественного здравоохранения, что определяет необходимость разработки российской программы по контролю и ликвидации вирусных гепатитов в развитии решений, принятых ВОЗ.
Формирование российской программы по контролю и искоренению вирусных гепатитов
На этапе создания данной программы планируется проведение работ в трех регионах РФ, различающихся по уровню распространения вирусных гепатитов: Республика Татарстан, Республика Саха (Якутия) и Калининградская область.
Обобщение фактических данных позволит разработать программу, учитывающую особенности современного эпидемического процесса.
На основе полученных результатов будут даны рекомендации по улучшению качества проведения лабораторных исследований по вирусным гепатитам, оптимальному и необходимому перечню определения их маркеров, оптимизации системы обеспечения лабораторных исследований.
- Анализ вакцинопрофилактики вирусных гепатитов. Для оценки эффективности вакцинопрофилактики гепатитов В и А на основе рекомендаций ВОЗ и данных медицинских служб мира (например, Великобритании) будет проведен вакцинный аудит. Проведенный анализ позволит улучшить вакцинацию против вирусных гепатитов В и А. Оценка вакцинопрофилактики, проводимая в регионе, позволит предложить оптимальную стратегию, необходимую для реализации программы. Реализация данного стратегического направления позволит получить объективную информацию по вирусным гепатитам, их лечению и профилактике.
- Разработка информационных материалов (на основе полученных данных) для представителей государственных структур в целях проведения информационно- разъяснительной работы.
- Разработка плана мероприятий для повышения знаний о вирусных гепатитах среди медицинских сотрудников различного профиля. Включение тематических циклов по вирусным гепатитам в программы непрерывного медицинского образования.
- Организация семинаров и совещаний при проведении программы по контролю и искоренению вирусных гепатитов на территории РФ с акцентом на регион, где проводится работа.
- Разработка плана мероприятий для населения по информационно-разъяснительной работе, направленной на создание общественного мнения о необходимости и реальности проведения работы по контролю и дальнейшей ликвидации вирусных гепатитов. Эта работа должна включать выступления специалистов на радио и телевидении, создание информационного интернет-портала для региона, в котором проводится реализация программы, публикации в местной прессе статей о вирусных гепатитах, современных методах их лечения и профилактики. Реализация данного стратегического направления позволит создать информационное поле для понимания проблемы вирусных гепатитов и необходимости проведения работ по программе.
В качестве основных блоков программы могут быть следующие направления:
Будет предложена схема оптимизации лабораторных исследований для скрининга населения по выявлению больных ХГС, лабораторного и клинического наблюдения эффективности применяемой терапии.
Перечисленный список узловых блоков, наиболее важных для проведения программы по контролю и искоренению вирусных гепатитов, не является окончательным. В процессе решения стратегического направления № 3 будут выявлены дополнительные направления работ, важные для конкретного региона.
- Определение групп населения и районов, которые нуждаются в первоочередной помощи по профилактике и лечению вирусных гепатитов.
- Оценка работы существующих структур для профилактики (прививочные кабинеты) и лечения (государственные и частные лечебно-профилактические учреждения, работающие в регионе). Предложения по созданию новых структур.
- Рекомендация по созданию (выбору существующего) координационного центра для реализации программы.
- Оценка и рекомендации по предоставлению медицинской помощи больным вирусными гепатитами в местах лишения свободы.
- Государственное финансирование.
- Частное финансирование.
- Страховая медицина.
- Определение необходимого объема финансирования для создания и реализации программы.
Заключение
Целями публикации проекта представленной программы являются:
- привлечение внимания медицинской общественности к проблемам вирусных гепатитов;
- представление плана возможных действий для разработки эффективной программы по контролю и искоренению вирусных гепатитов в РФ;
- приглашение широкого круга медицинской общественности и наших читателей к обсуждению данной проблемы.

Перинатальная передача вкусного гепатита А, В, С от матери к ребенку может реализоваться пренатально (трансплацетарно), интранатально (во время родов) или постнатадьно - во время ухода за новорожденным.
По данным ряда исследователей (Фарбер Н.А., Мартынов К.А.) вирусный гепатит протекает значительно тяжелее во время беременности. ГА существенного влияния на развитие плода не оказывает. ГВ протекает значительно тяжелее и представляет опасность для плода.
Заражение детей может происходить от матерей, больных как острым, так и хроническим гепатитом В, а также вирусоносителей (Шехтман М. М.). В настоящее время считается признанным положение о возможном пренатальном заражении плода гепатитом В.
Трансплацентарное заражение происходит у детей, родившихся от матерей-носителей HBsHg. Вместе с тем существует гипотеза о более частом внутриутробном заражении плода. При этом вирус ГВ инфицирует плод, однако активной рекминации вируса гепатита В в гепатоцитах не происходит (Андриуца К. А., Вязов С. Д, Блохина Н. П.). Во время родов заражение происходит через родовые пути, когда кожа ребенка значительно мацерирована водами (Шехтман М. М., Мартынов К. А.). Высказывается предположение о возможном заражений новорожденных детей в результате заглатывания или аспирации околоплодных вод, в которых имеется ВГ.
Резкое сжатие матки во время родов может привести к попаданию вируса из материнской крови в кровеносную систему плода.
Заражение после родов происходит редко, это прежде всего связано с тем, что большинство детей уже инфицированы во время родов.
Постнатальное заражение после родов при тесном контакте с матерью-носителем вируса гепатита В происходит реже, чем интранатальное; это прежде всего связано с тем, что большинство детей уже инфицированы в родах. Представляет интерес, что грудное молоко матерей-вирусоносителей не играет большой роли в инфицировании их детей.
При гепатите С роль перинатального инфицирования в распространении этой инфекции до конца не определена. Появление антител к вирусу гепатита С через 6-12 месяцев после рождения у детей, чьи матери имели антитела, может косвенно свидетельствовать о перинатальном инфицировании. Младенческая смертность зависит от степени доношенности плода. Недоношенные дети, родившиеся от матерей, больных острым вирусным ГВ, С погибают в два раза чаще.
Цель: изучение клинических проявлений и исходов перинатальной инфекции, вирусного гепатита, передачи ее младенцам и длительность циркуляции у них специфических антител.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Диагноз выставлен на основании данных анамнеза, эпидемиологических анализов, биохимических исследований крови матери и плода.
Исследование крови на маркер вирусных гепатитов, УЗИ печени, селезенки. Нами обследовано 25 детей до 1 года жизни и их матери во время беременности.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Женщины во время беременности находились в РЦИБ г. Махачкала с диагнозом вирусный гепатит. Дети от этих матерей наблюдались до одного года.
Гепатит возникает в I и II триместрах беременности, вероятность заболевания новорожденных была невелика, но в III триместре - риск заболевания для потомства составлял 25-76%. рождались чаще всего недоношенными в состоянии гипоксии. У 25% детей в дальнейшем наблюдалось отставание в общем развитии и предрасположенность к различным заболеваниям Характерным осложнением беременности явилась угроза ее прерывания (у 53%), преждевременные роды происходили у 36% рожениц. Послеродовые гнойно-септические заболевания учащены в связи с угнетением иммунного статуса не только за счет беременности, но и за счет гепатита, и активизации на этом фоне бактериальной микрофлоры.
Помимо изменений в печени при ВГ возникли в 2% - крапивница; у одного ребенка - гломерунефрит.
Предполагаем, что причина этих синдромов - циркуляция в крови иммунных компонентов.
У 12% детей был диагностирован Г. С., у 14% - Г. В., 10% - гепатиты А; D, Е не выявлены. Риск передачи НСУ от матери к плоду ниже, чем при НВУ и составляет 0,9%, особенно при высоком уровне виремии у матери.
Среди пациентов гепатит В диагностирован у 10 детей, матери б из них перенесли во время беременности острый вирусный гепатит В с исходом выздоровления, у 8 диагностированных хронический НВV, 1 ребенок, мама которого болела в III триместр беременности, был госпитализирован в реанимационное отделение РИЦ с клиникой фульминантного гепатита В с летальным исходом. Поводом направления в стационар 7% новорожденных был гепатолиенальный синдром, явления интоксикации, отставание в физическом развитии, изменения функции печени, почек, обнаружении HBsHg при обследовании в связи с наличием НВV-антигена у матери во время беременности. Желтуха выявлена у 7%, нарушение функции почек у 5%. Функциональные пробы печени изменены у 7%. При проведении УЗИ печени: у всех больных отмечено увеличение размеров, повышение эхогенности перенхимы.
Течение болезни было тяжелым у 15% новорожденных, среднетяжелым у 12%. Все новорожденные при рождении и на 5 день были обследованы биохимически и иммунологически на наличие антител НСV-вирус, НВV. 100% случаях на 5 день жизни у всех новорожденных от матерей с НСV -вирусной инфекция сохранилась. Способ родоразрешения (через естественные родовые пути или кесарево сечение) не влиял на частоту перинатального инфицирования. Сразу после родов у 14% новорожденных от инфицированных НСV матерей в сыворотке крови обнаружены материнские антитела к НСV, проникающие через плаценту. У неинфицированных детей антитела исчезли в течение 1 года жизни.
Профилактику перинатального гепатита В рекомендовали проводить с помощью вакцинации новорожденных, чьи матери имеют вирус гепатита В. Для повышения эффективности проводимой вакцинации рекомендовали вводить вакцину в сочетании с гиперимунным гаммаглобулином против гепатита В.
С целью профилактики ВГ у новорожденных им в первые часы жизни был введен гипериммунный Т-глобулин или вакцина, при распространенности вирусоносительства в популяции 2% и более. Если у матери обнаружены HBsHg. и HBеHg. нужна сочетанная активная и пассивная иммунизация, поскольку риск инфицирования ребенка значительно возрастает. В районах с низким уровнем носительства HBsHg. и HBеHg при наличии у большинства женщин носителей HBsHg. антител HBеHg применение средств специфической профилактики ВГ у новорожденных нецелесообразно в связи с редким формированием у них персистирующей Нbs-антигенемии. Отечественная плазменная вакцина против ВГ вызывает при 3-кратной аппликации образование антиHbs у 80% детей, при этом результаты исследования свидетельствуют об эффективности вакцины в отношении профилактики Hbs-антигеноносительства. Грудное вскармливание не прекращалось, поскольку практически крайне редко инфекция передается с молоком матери.
- Андриуца К. А., Вязов С. Д., Блохина Н. П. Вирусный гепатит дельта. Кишинев: Штиинца, 1993.
- Закриров И. Г., Маннанова Д. Р., Хаертынова И.М. Иммунологические показатели при хронических гепатитах, обусловленных вирусами гепатитов В и С // Тез. Докл. Пятого Российского съезда врачей инфекционистов. - М., 1998. С. 106-107
- Фарбер Н. А., Мартынов К. А., Гуртовой Б. Л. Вирусные гепатиты у беременных. М.: Медицина, 1990.
- Шехтман М. М., Мартынов К. А. Принципы ведения беременности у женщин с сами гепатита. (Пособие для врачей). М., МЗ РФ, 1998.
- Hoffman Н. Кnuuz Ch.. // International Congress of Viroky 8-th: abstracts. - Berlin 1990- P. 134
Из всех форм вирусных гепатитов гепатит А является наиболее распространенным. От момента заражения до появления первых признаков болезни проходит от 7 до 50 дней. Чаще всего начало заболевания сопровождается подъемом температуры и может напоминать грипп. Большинство случаев завершается спонтанным выздоровлением и не требует активного лечения. При тяжелом течении назначают капельницы, устраняющие токсическое действие вируса на печень.
Вирус гепатита В передается половым путем, при инъекциях нестерильными шприцами у наркоманов, от матери — плоду. В типичных случаях заболевание начинается с повышения температуры, слабости, болей в суставах, тошноты и рвоты. Иногда появляются высыпания. Происходит увеличение печени и селезенки. Также может быть потемнение мочи и обесцвечивание кала.
Гепатит С — наиболее тяжелая форма вирусного гепатита, которую называют еще посттрансфузионным гепатитом. Это значит, что заболевали им после переливания крови. Это связано с тем, что тестировать донорскую кровь на вирус гепатита С стали всего несколько лет назад. Достаточно часто происходит заражение через шприцы у наркоманов. Возможен половой путь передачи и от матери — плоду. Наибольшую опасность представляет собой хроническая форма этой болезни, которая нередко переходит в цирроз и рак печени.
Хроническое течение развивается примерно у 70-80% больных. Сочетание гепатита С с другими формами вирусного гепатита резко утяжеляет заболевание и грозит летальным исходом.
Гепатит E похож на гепатит A, но начинается постепенно и опаснее для беременных.
Последний в семействе гепатитов, гепатит G, похож на C, но менее опасен.
Пути заражения
Вирусы гепатита попадают в организм человека двумя основными способами. Больной человек может выделять вирус с фекалиями, после чего тот с водой или пищей попадает в кишечник других людей. Врачи называют такой механизм заражения фекально‑оральным. Он характерен для вирусов гепатита А и Е. Таким образом, гепатит А и гепатит Е возникают в основном из‑за несоблюдения личной гигиены, а также при несовершенстве системы водоснабжения. Этим объясняется наибольшая распространенность этих вирусов в малоразвитых странах.
Второй путь заражения — контакт человека с инфицированной кровью. Он характерен для вирусов гепатитов В, С, D, G. Наибольшую опасность, ввиду распространенности и тяжелых последствий заражения, представляют вирусы гепатитов В и С.
Ситуации, при которых чаще всего происходит заражение:
— переливание донорской крови. Во всем мире в среднем 0,01-2% доноров являются носителями вирусов гепатита, поэтому в настоящее время донорская кровь перед переливанием реципиенту исследуется на наличие вирусов гепатита В и С. Риск инфицирования повышается у лиц, нуждающихся в повторных переливаниях крови или ее препаратов
— использование одной иглы разными людьми во много раз увеличивает риск заражения гепатитами В, С, D, G. Это самый распространенный путь заражения среди наркоманов;
— вирусы B, С, D, G могут передаваться при половом контакте. Чаще всего половым путем передается гепатит В. Считается, что вероятность заражения гепатитом С у супругов мала.
Симптомы
От момента заражения до появления первых признаков болезни проходит разное время: от 2-4 недель при гепатите А, до 2-4 и даже 6 месяцев при гепатите В. По истечении этого периода, во время которого вирус размножается и адаптируется в организме, болезнь начинает проявлять себя.
Сначала, до появления желтухи, гепатит напоминает грипп и начинается с повышения температуры, головной боли, общего недомогания, ломоты в теле, как при гепатите А. При гепатитах B и С начало, как правило, более постепенное, без резкого подъема температуры. Так, вирус гепатита В проявляет себя незначительной температурой, болью в суставах, иногда высыпаниями.
Начальные проявления гепатита С могут ограничиться слабостью и снижением аппетита. Через несколько дней картина начинает меняться: пропадает аппетит, появляются боли в правом подреберье, тошнота, рвота, темнеет моча и обесцвечивается кал. Врачи фиксируют увеличение печени и реже — селезенки. В крови обнаруживаются характерные для гепатитов изменения: специфические маркеры вирусов, увеличивается билирубин, печеночные пробы увеличиваются в 8-10 раз.
Обычно после появления желтухи состояние больных улучшается. Однако этого не происходит при гепатите С, а также у хронических алкоголиков и наркоманов, независимо от вида вируса, вызывающего заболевание, из‑за интоксикации организма. У остальных же больных постепенно, в течение нескольких недель, происходит обратное развитие симптомов. Так протекают острые формы вирусных гепатитов.
Клиническое течение гепатитов может быть разной степени тяжести: легкая, среднетяжелая и тяжелая формы. Есть еще и четвертая, фульминантная, то есть молниеносная форма. Это самая тяжелая разновидность гепатита, при которой развивается массивный некроз печени, заканчивается обычно смертью больного.
Наибольшую опасность представляет хроническое течение гепатитов. Хронизация характерна только для гепатитов B, C, D. Наиболее характерными признаками хронических гепатитов являются недомогание и усиливающаяся к концу дня повышенная утомляемость, невозможность выполнять прежние физические нагрузки. На далеко зашедшей стадии хронического вирусного гепатита обнаруживаются желтуха, потемнение мочи, кожный зуд, кровоточивость, похудание, увеличение печени и селезенки, сосудистые звездочки.
Лечение
Длительность гепатита А составляет в среднем 1 месяц.
Специального противовирусного лечения при этом заболевании не требуется. Лечение включает в себя: базисную терапию, постельный режим, соблюдение диеты. При наличии показаний назначается дезинтоксикационная терапия (внутривенно или перорально), симптоматическая терапия. Обычно рекомендуют избегать употребления алкоголя, который, как ядовитое вещество, может ослабить и без того поврежденную печень.
Острый вирусный гепатит В с выраженными клиническими симптомами заканчивается выздоровлением более чем в 80% случаев. У больных, перенесших безжелтушную и субклиническую формы, гепатит В часто хронизируется. Хронический гепатит приводит со временем к развитию цирроза и рака печени. Полного излечения хронического гепатита В практически не наступает, но можно добиться благоприятного течения заболевания при условии выполнения определенных рекомендаций, касающихся режима труда и отдыха, питания, психоэмоциональных нагрузок, а также при приеме препаратов, улучшающих обменные процессы в клетках печени.
В обязательном порядке проводится базисная терапия. Противовирусное лечение назначается и проводится под строгим контролем врача и в тех случаях, когда имеются показания. К противовирусному лечению относятся препараты группы интерферонов. Лечение проводится длительно. Иногда бывают необходимы повторные курсы терапии.
Гепатит C — наиболее серьезный вид гепатита. Развитие хронической формы наблюдается как минимум у каждого седьмого заболевшего. У этих больных высок риск развития цирроза и рака печени. Основой всех схем лечения является интерферон‑альфа. Механизм действия этого препарата заключается в предотвращении инфицирования новых клеток печени (гепатоцитов). Применение интерферона не может гарантировать полного выздоровления, однако, лечение им предотвращает развитие цирроза или рака печени.
Гепатит D протекает только на фоне гепатита B. Лечение гепатита D должно проводиться в стационаре. Требуется как базисная, так и противовирусная терапия.
Гепатит E не лечат, так как организм человека достаточно силен, чтобы избавиться от вируса без помощи лечения. Через месяц‑полтора наступает полное выздоровление. Иногда доктора назначают симптоматическую терапию для устранения головной боли, тошноты и других неприятных симптомов.
Осложнения
Осложнениями вирусных гепатитов могут стать функциональные и воспалительные заболевания желчных путей и печеночная кома, и если нарушение в работе желчевыводящих путей поддается терапии, то печеночная кома является грозным признаком молниеносной формы гепатита, заканчивающейся летальным исходом практически в 90% случаях. В 80% случаев молниеносное течение обусловлено сочетанным действием вирусов гепатитов В и D. Печеночная кома наступает из‑за массивного омертвения (некроза) клеток печени. Продукты распада печеночной ткани попадают в кровь, вызывая поражение центральной нервной системы и угасание всех жизненных функций.
Хронический гепатит опасен тем, что отсутствие адекватного лечения нередко приводит к циррозу, а иногда и раку печени.
Самое тяжелое течение гепатита вызывает сочетание двух и более вирусов, например В и D или B и С. Встречается даже B+D+C. В этом случае прогноз крайне неблагоприятный.
Профилактика
Чтобы уберечься от заражения гепатитами, необходимо соблюдать несложные правила.
Не следует употреблять некипяченую воду, всегда мыть фрукты и овощи, не пренебрегать термической обработкой продуктов. Так можно предотвратить заражение гепатитом А.
В целом, необходимо избегать контакта с биологическим жидкостями других людей. Для предохранения от гепатитов В и С — в первую очередь с кровью. В микроскопических количествах кровь может остаться на бритвах, зубных щетках, ножницах для ногтей. Не стоит делить эти предметы с другими людьми. Нельзя делать пирсинг и татуировки нестерильными приборами. Необходимо принимать меры предосторожности при сексе.
Материал подготовлен на основе информации открытых источников
Получение новых знаний по вышеперечисленным проблемам необходимо для успешной реализации программы по контролю за вирусными гепатитами.
Гепатиты с фекально-оральным механизмом передачи возбудителя
ГА. Его всегда рассматривали как инфекцию, которая в подавляющем большинстве случаев протекает в средне-легкой форме и заканчивается выздоровлением. Прежнее повышенное внимание к этой инфекции определялось высоким уровнем заболеваемости, наличием крупных вспышек с вовлечением сотен и даже тысяч заболевших. Разработка и внедрение в широкую практику здравоохранения вакцины против ГА позволило уже в 90-е годы ХХ века поставить вопрос о глобальном контроле за этой инфекцией. Казалось, еще немного, и будет достигнут успех в этом направлении. Кроме того, создалось мнение, что в изучении ГА не могут быть обнаружены новые фундаментальные данные о возбудителе и эпидемиологии инфекции.
Сегодня произошло изменение в характере эпидемического процесса ГА. Общие показатели заболеваемости ГА, прежде всего среди детей и подростков, снизились. Заболеваемость переместилась на старшие возрастные группы, что привело к развитию более тяжелых форм ГА и увеличению числа смертельных случаев. Наличие большой группы лиц, не имеющих антител к ВГА, определило возможность возникновения крупных вспышек инфекции.
В конце 2017 г. и в 2018 г. в некоторых штатах США зарегистрированы крупные вспышки ГА [2], что стало абсолютно неожиданным для общественного здравоохранения страны. Все началось в г. Сан-Диего (Калифорния), где заболели более 500 человек, из которых 19 (3,7%) умерли. Основной контингент заболевших составили бездомные и лица, употребляющие наркотические средства. В дальнейшем подобная ситуация была зарегистрирована в других штатах: Кентукки, Западной Виржинии, Огайо, Индиане и Миссури. Число заболевших составило более 10 000 человек. Предполагают, что интенсивное распространение ВГА среди заболевших происходит при тесном контакте (водный и пищевой пути реализации фекального механизма передачи вируса исключены) на фоне сопутствующих хронических заболеваний печени (ГВ и ГС), иммунодефицитных состояний, употребления алкоголя при отсутствии ранее проведённой вакцинации среди этой группы населения.
Эта ситуация привлекла пристальное внимание специалистов и общества как в США, так и в других странах мира [3]. Основными причинами возникновения данных вспышек являются рост экономического неравенства различных групп населения и неспособность здравоохранения быстро локализовать распространение инфекции.
Исходя из этого, необходима программа по профилактике ГА в России с учетом научных междисциплинарных исследований, направленных на изучение ситуации с ГА и социальных факторов (старение населения, миграционные процессы, бездомные и лица, принимающие наркотики).
ГЕ. В странах с умеренным климатом его часто рассматривают как возникающее или эмергентное заболевание. Этиологическим агентом ГE является вирус гепатита Е (ВГЕ), принадлежащий к роду Orthohepevirus А семейства Hepeviridae [4]. К настоящему времени идентифицировано 8 генотипов ВГЕ, причем генотипы 3, 4, 7 и 8 способны передаваться человеку от животных [5]. Генотипы 3 и 4 встречаются у нескольких видов животных (диких и домашних свиней, кроликов, оленей), при этом считается, что домашние свиньи являются основным резервуаром инфекции в промышленно развитых странах [6]. В настоящее время накоплен массив последовательностей ВГЕ, выделенных от человека и животных на территории РФ, требующий углубленного анализа для понимания эпидемиологии ГЕ. Авторами изучено генетическое разнообразие ВГЕ на территории РФ для установления взаимосвязи между вариантами вируса, выделенными от разных видов хозяев, и реконструирована история заносов ВГЕ на территорию РФ.
Результаты филогенетического анализа продемонстрировали, что подавляющее число последовательностей, выделенных на территории РФ, относится к подгруппе II ВГЕ-3, к которой относится большинство европейских штаммов ВГЕ. По данным филогенетического анализа с временной шкалой, разделение ВГЕ-3 на группы I и II произошло примерно 88 лет назад (95% ДИ 71–106 лет). Большинство российских штаммов ВГЕ-3 образуют группы, характерные для каждого из обследованных регионов (Архангельская, Белгородская, Владимирская, Калининградская, Саратовская, Свердловская области, Хабаровский край) и являющиеся результатом неоднократного заноса вируса как из Европы, так и из Азии. Средний возраст отделения от общего предка для российских региональных кластеров последовательней ВГЕ-3 составляет не менее 25 лет. Последовательности ВГЕ-3, выделенные в одном и том же регионе от людей и от свиней, группируются вместе, что подтверждает зоонозную природу инфекции у человека. Многолетний мониторинг ВГЕ на одной свиноферме продемонстрировал устойчивую циркуляцию одного варианта ВГЕ-3 в течение 5 лет. Последовательности ВГЕ-3, выявленные в сточных водах свиноферм, оказались идентичными последовательностям, выделенным от животных на этих же фермах, и близкими к геноизолятам ВГЕ-3 от заболевших людей в том же регионе РФ. Заражение человека, по-видимому, может происходить не только при алиментарном пути передачи, но и в результате контаминации окружающей среды сточными водами свиноферм. ВГЕ кроликов широко распространен и устойчиво циркулирует на территории РФ [8], однако до настоящего времени в стране не зарегистрировано ни одного случая заражения человека этим вариантом вируса. Последовательности ВГЕ кроликов не группируются с последовательностями ВГЕ-3 от людей и свиней, хотя генетически близки этому генотипу. По расчетным данным, разделение ВГЕ-3 и ВГЕ кроликов произошло в ХIХ веке (95% ДИ 115–184 года назад). Последовательности ВГЕ кроликов, выявленные в одном регионе РФ, демонстрируют значительную степень различия между группами последовательностей [отделение от общего предка более 60 лет назад (95% ДИ 45–78 лет)] при относительно небольшой гетерогенности внутри групп, что свидетельствует о неоднократном завозе разных штаммов ВГЕ кроликов в регион.
Степень гетерогенности и возраст группы последовательностей ВГЕ-4, впервые выделенных от обезьян, составляющий 5,18 лет (95% ДИ 3,47–10,15 лет), свидетельствуют о том, что инфекция у этих животных не является результатом однократного заражения обезьян от одного источника, а отражает циркуляцию вируса среди этих животных. Полученные данные являются первым свидетельством того, что приматы могут выступать в качестве естественного резервуара ВГЕ-4.
Таким образом, современные штаммы ВГЕ-3, выявляемые на территории РФ, являются результатом неоднократных заносов как из Европы, так и из Азии, и их последующей длительной циркуляции среди поголовья свиней в регионах страны. Выделяемые от заболевших людей штаммы ВГЕ-3 не группируются вместе, но имеют общих предков со штаммами, выделенными от свиней, максимум за 20 лет до выделения, что указывает на регулярную передачу вируса от свиней человеку.
Гепатиты с парентеральной передачей возбудителя ГВ
За более чем 50-летний период, прошедший после открытия вируса ГВ (ВГВ), получены фундаментальные знания о вирусе и инфекции, которую он вызывает. Изучены структура вируса, тонкие механизмы репликации, патогенетические основы, разработаны и широко применяются вакцины против ГВ. Однако, несмотря на впечатляющие успехи в борьбе с ГВ, возникли новые проблемы, определяемые как природой заболевания, так и организационными вопросами при реализации программ профилактики. Сегодня очевидно, что при любой инфекции, вызванной ВГВ, даже при наличии всех показателей выздоровления (элиминация ДНК ВГВ, исчезновение HBsAg и появление анти-НВs) в организме человека остаётся ковалентно замкнутая кольцевая ДНК (кзкДНК) ВГВ. Это определяет возможность последующей реактивации ГВ, возникающей в случаях иммунодефицитных состояний (например, при ВИЧ-инфекции или онкологических заболеваниях), под воздействием лекарственной терапии, в том числе при массовом использовании препаратов прямого действия для лечения ГС. Отсутствие доступных методов удаления кзкДНК ВГВ из организма человека не позволяют в ближайшее время надеяться на полную элиминацию ВГВ из человеческой популяции.
В 2018 г. тенденция к снижению показателей заболеваемости ГВ сохранилась.
О необходимости проведения такой работы могут свидетельствовать данные, полученные нами ранее. Были проанализированы результаты выявления протективных уровней поствакцинальных анти-HBs среди взрослого населения четырех регионов страны (Республики Тыва, Хабаровского края, Саратовской и Свердловской областей), получивших полный курс вакцинации препаратом одного и того же производителя. Частота обнаружения анти-HBs в защитном титре (более 10 МЕ/л) колебалась от 67,2 до 88,1% [9].
ГD. В Российской Федерации изучению ГD уделяется предельно мало внимания. Для этого есть ряд причин: отсутствие официальной регистрации заболевания, неравномерная циркуляция вируса на территории страны (ВГD относительно редко встречается в Европейской части РФ, где сосредоточено большинство научных и клинических центров). Данные о современной эпидемиологии ВГD, генетическом разнообразии, времени циркуляции вируса и истории его распространения на отдельных территориях, молекулярной эпидемиологии в России ограничены. Авторы провели анализ современного эпидемиологического профиля ГD и генетического разнообразия ВГD в эндемичных регионах РФ, а также реконструировали историю распространения ВГD на этих территориях.
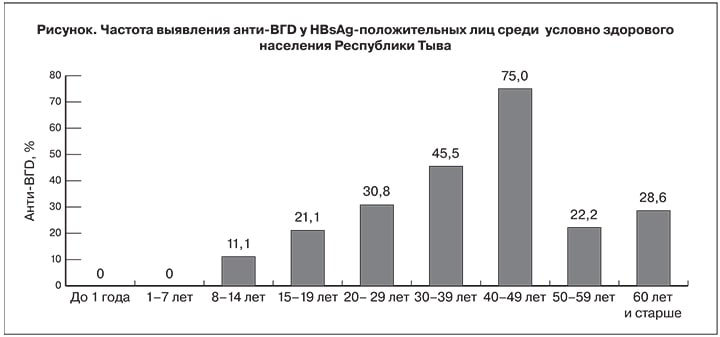
При обследовании 1154 представителей условно здорового населения HBsAg определен в 95 (8,2%) случаях, анти-HBc – в 531 (46,2%) и анти-ВГD – в 27 (2,3%). Наибольшая частота выявления HBsAg (17,6%) отмечена в группе подростков 15–19 лет, наименьшая (2,3%) – в группе младенцев до 1 года; максимальная частота выявления анти-НВс (81,3%) – в группе 60 лет и старше, минимальная (3,7%) – у детей от 1 года до 7 лет. Распространенность анти-ВГD среди HBsAg-положительных лиц составила в среднем 28,4% (у 27 из 95 обследованных), достигая пика (75%) в возрастной группе 40–49 лет (см. рисунок). Среди детей до 7 лет, рожденных после внедрения массовой вакцинации новорожденных против ГВ, не было отмечено ни одного случая выявления анти-ВГD. Эти данные являются первым свидетельством предотвращения распространения ВГD на популяционном уровне в эндемичном регионе в результате массовой вакцинация против ГВ.
Результаты филогенетического анализа продемонстрировали, что все выделенные в Республике Тыва изоляты ВГD относятся к генотипу 1 и образуют несколько кластеров, группируясь с последовательностями из РФ, Турции, Китая и Монголии. Для 12 представителей четырех основных тывинских кластеров ВГD и 9 штаммов из Республики Саха (Якутия) были получены полногеномные последовательности (GenBank MH791027-MH791030). Из 9 последовательностей ВГD из Якутии 4 относились к генотипу 1, 5 – к генотипу 2. Все якутские последовательности генотипа 2 образуют отдельный кластер, значительно отличающийся от остальных штаммов этого генотипа.
Филогенетический анализ с временной шкалой продемонстрировал, что отделение современных тывинских штаммов ВГD от общего предка произошло в 60-е годы ХХ века (95% ДИ 40–66 лет назад), в то время как возраст современных штаммов ВГВ, циркулирующих в Тыве, составляет несколько сотен лет. Предположительно, распространение ВГD в середине прошлого века в этом регионе, где изначально был широко распространен ВГВ, было связано с началом массовых медицинских парентеральных вмешательств.
Анализ последовательностей ВГD из семейных очагов инфекции показал наличие вариантов вируса как близкородственных, так и значительно различающихся между собой, что указывает на гетерогенные источники инфицирования.
Таким образом, массовая вакцинация против ГВ предотвращает распространение ВГD даже в эндемичном регионе и является единственным действенным инструментом управления этой инфекцией. На территории Якутии встречается ВГD генотипов 1 и 2, тогда как в Тыве циркулирует вирус только генотипа 1. Его широкое распространение в регионе произошло в середине ХХ века, в отличие от ВГВ, распространение которого на этой территории имеет значительно более длительную историю. Полученные данные могут послужить материалом для дальнейших исследований по изучению широкого распространения ВГD на отдельных территориях Российской Федерации.
ГС. Одним из важнейших успехов последних лет в борьбе с вирусными гепатитами является разработка и внедрение в клиническую практику безинтерфероновых схем лечения хронического ГС (ХГС). Применение препаратов прямого противовирусного действия (ПППД) – ингибиторов вирусных белков протеазы NS3, белка NS5A и полимеразы NS5B позволяет достигать устойчивого вирусологического ответа (УВО) более чем у 95% пациентов [10]. Несмотря на относительно небольшой (не более 5 лет) мировой опыт применения ПППД, уже накоплены данные о влиянии полиморфизмов в геноме ВГС на эффективность терапии с применением ПППД. Неудачи терапии, по-видимому, обусловлены сочетанием нескольких неблагоприятных факторов, одним из которых является феномен лекарственной резистентности ВГС. Анализ Европейской базы данных по резистентности к ПППД продемонстрировал, что в 83% случаев отсутствия УВО в участках генома вируса, кодирующих белки мишени для ПППД, обнаруживали 1 или несколько аминокислотных замен, ассоциированных с лекарственной резистентностью (Resistance Associated Substitution – RAS) [11]. Наибольшее клиническое значение имеют RAS ВГС, связанные с резистентностью к ингибиторам белка NS5А (даклатасвир, ледипасвир, омбитасвир, пибрентасвир и элбасвир), являющимся препаратами первой линии [12]. По-видимому, это связано с тем, что белок NS5А не является ферментом, в отличие от других мишеней ПППД – белков ВГС NS3 и NS5B, и, вероятно, имеет более высокую степень изменчивости при сохранении функции белка и, соответственно, фитнесса вируса. Для RAS NS5А возможно длительное сохранение в квазивиде ВГС после прекращения неудачной терапии [13], и описаны случаи передачи таких вариантов ВГС в группах риска [14].
Авторами проведен анализ 202 последовательностей NS5А ВГС, выделенных в 2008–2014 гг. в Москве от пациентов из групп повышенного риска инфицирования (инъекционные наркоманы, n = 67) и лиц без установленных факторов риска (n = 135). В исследование были включены последовательности наиболее распространенных в РФ генотипов ВГС: 1b (n = 93), 3а (n = 90) и 1а (n = 19). Процентное соотношение последовательностей ВГС генотипов 1а, 1b и 3а в исследованной выборке составило 9,4, 46,0 и 44,6% соответственно, что соответствует распределению этих генотипов на территории нашей стораны [16].
Фрагмент NS5A величиной 1292 нт для генотипа 1 и 1296 нт – для генотипа 3 амплифицировали с генотип-специфичными праймерами и определяли его нуклеотидную последовательность на автоматическом секвенаторе 3500 Genetic Analyzer (ABI, Foster City, США) с использованием набора BigDye Terminator v 3.1 Cycle Sequencing Kit (Applied Biosystems, США) [17]. Для выравнивания последовательностей и определения порядка аминокислотных позиций использовали референсный штамм H77 субтипа ВГС 1а (GenBank AF011753). Анализ всех нуклеотидных и предсказанных аминокислотных последовательностей ВГС выполняли с помощью программного обеспечения MEGA 7.0.18. Перечень клинически значимых RAS NS5A формировали на основании последних рекомендаций Европейской ассоциации по изучению печени (EASL) [10] и обзора данных литературы [12, 18, 19]. Оценку частоты встречаемости в аа позициях NS5а 28, 29, 30, 31, 32, 58, 62, 92 и 93 проводили с помощью программного обеспечения Microsoft Office Excel.
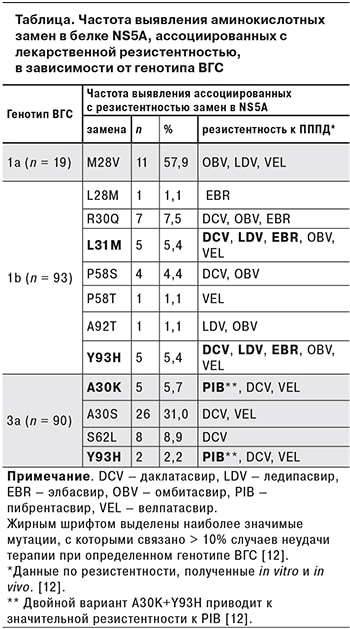
Доля штаммов, несущих в NS5A те или иные полиморфизмы, связанные с лекарственной устойчивостью, составила 30,2% (61 из 202), при этом доля таких штаммов составила 57,9% (11из 19) для генотипа 1а, 22,6% (21 из 93) – для генотипа 1b и 43,3% (39 из 90) – для генотипа 3а. Показатели частоты выявления каждого полиморфизма в NS5A ВГС приведены в таблице.
Среди последовательностей генотипа 1b были выявлены связанные с устойчивостью к большинству ингибиторов NS5A замены L31M и Y93H, каждая с частотой 5,4%, а также менее значимые с клинической точки зрения замены L28M, R30Q, P58S/T и A92T.
Замена A30S, связанная с устойчивостью к даклатасвиру и велпатасвиру и характерная исключительно для штаммов генотипа 3а, была выявлена среди 31% последовательностей этого генотипа. Другой вариант в этой позиции, А30К, тоже связанный с устойчивостью к даклатасвиру и велпатасвиру, был выявлен в 5,7% случаев. Полиморфизм Y93H, характерный для разных генотипов ВГС, был представлен в 2,2% последовательностей ВГС 3а.
Большинство штаммов ВГС содержали только одну замену в NS5A, однако 5 последовательностей несли одновременно по 2 замены: R30Q + Y93H, P58T + Y93H и A92T + Y93H при генотипе 1b; A30K + S62L и S62L + Y93H при генотипе 3a (номера GenBank MH373296, MH373314, MH373334, MH432639 и MH432554 соответственно).
Сложно оценить клиническую значимость широкой распространенностью RAS NS5A среди российских пациентов, инфицированных ВГС генотипа 1a, и угрозу, которую они представляют для применения ингибиторов NS5A. Эти препараты применяются в сочетании с ингибиторами NS3 или NS5B, что должно обеспечивать успех противовирусной терапии, несмотря на наличие RAS в NS5A. В настоящее время тестирование на наличие RAS в NS5A до начала терапии рекомендовано только в следующих случаях: для пациентов с ВГС генотипа 1a (независимо от опыта терапии и степени фиброза) при назначении схемы элбасвир/гразопревир; для ранее получавших терапию пациентов с ВГС генотипа 1a при назначении схемы ледипасвир/софосбувир; для ранее получавших терапию пациентов (а также не получавших терапию пациентов с циррозом) с ВГС генотипа 3a при назначении схемы софосбувир/велпатасвир или даклатасвир/софосбувир [20]. Широкая распространенность полиморфизма M28V среди российских последовательностей ВГС генотипа 1a указывает на целесообразность тестирования на наличие этого варианта отечественных пациентов, инфицированных ВГС генотипа 1а, перед назначением схем терапии, включающих ингибиторы NS5A. Умеренная распространенность наиболее клинически значимых RAS среди российских штаммов ВГС генотипов 1b и 3a указывает на отсутствие в настоящее время необходимости тестировать на наличие генетических детерминант резистентности перед началом терапии пациентов, инфицированных этими генотипами.
Михайлов М.И., Кюрегян К.К., Малинникова Е.Ю., Исаева О.В., Карлсен А.А., Потемкин И.А., Кичатова В.С., Аль-Шараби Шукри А.С., Догадов Д.И., Корзая Л.И., Игнатьева М.Е., Поляков А.Д.
Читайте также:


