В чем цель вирусов и бактерий
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
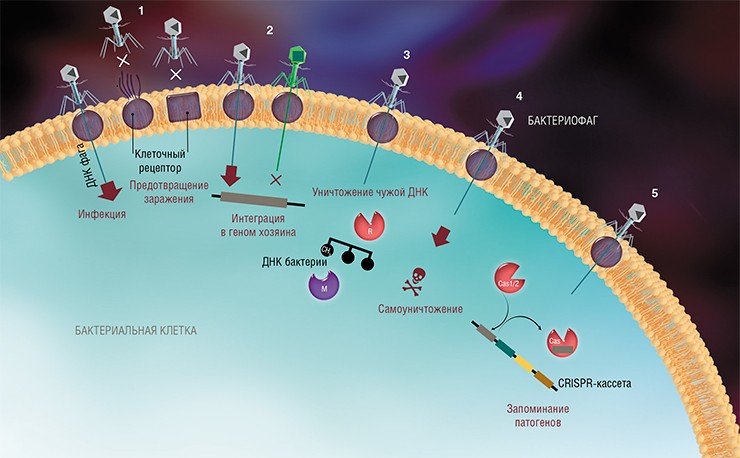
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
Врага нужно знать в лицо
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
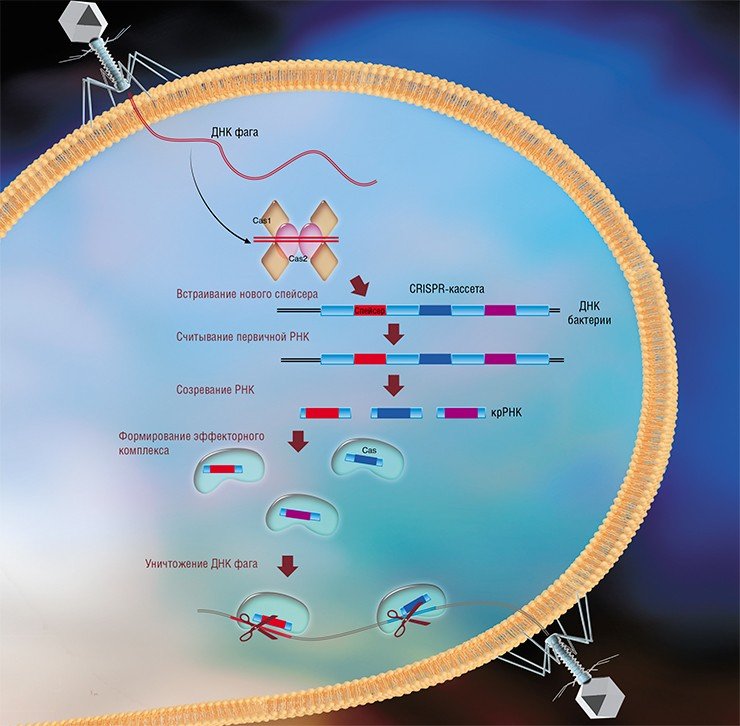
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
Гонка вооружений
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
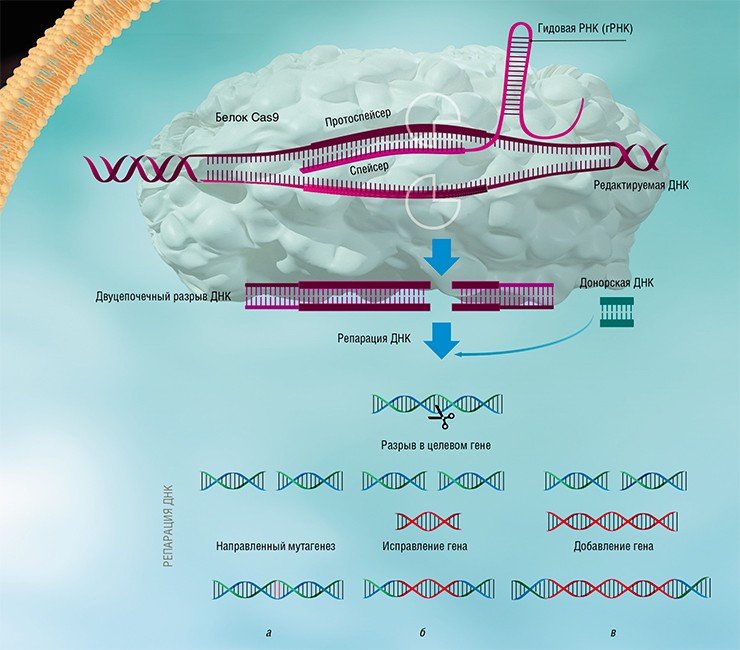
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)
- 16168
- 9,3
- 2
- 4
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Рисунок 5. Схема развития феномена ADE при вирусных инфекциях. а — Взаимодействие между антителом и рецептором FcR на поверхности макрофага. б — Фрагмент С3 комплемента (компонент комплемента, после присоединения которого весь этот комплекс приобретает способность прилипать к различным частицам и клеткам) и рецептор комплемента (complement receptor, CR) способствуют присоединению вируса к клетке. в — Белки комплемента С1q и С1qR способствуют присоединению вируса к клетке (в составе молекулы C1q имеется рецептор для связывания с Fc-фрагментом молекулы антитела). г — Антитела взаимодействуют с рецептор-связывающим сайтом вирусного белка и индуцируют его конформационные изменения, облегчающие слияние вируса с мембраной. д — Вирусы, получившие возможность реплицироваться в данной клетке посредством ADE, супрессируют противовирусные ответы со стороны антивирусных генов клетки. Рисунок с сайта supotnitskiy.ru.
Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
Муниципальный конкурс научно-исследовательских работ
и творческих проектов учащихся
Исследовательская работа на тему:
имени Адмирала Ушакова
Руководитель: Яламова Е.В.
учитель МБОУ СОШ №2
имени Адмирала Ушакова
Геленджик 2016 г
Изучение вредных микроорганизмов:
в) сравнительный анализ.
Основные подходы к лечению.
Список использованной литературы.
Исследовать главные возбудители инфекционных заболеваний, их сходство, различие и главные подходы к их лечению.
Изучить вирусы и бактерии.
Исследовать различия методов лечения вирусных и бактериальных заболеваний.
Выяснить, в чем опасность для человеческого организма при неправильном лечении.
Определить методы профилактики.
Предположим, что человечество можно спасти от вымирания (т.е. от развития устойчивости к антибиотикам) грамотной диагностикой и правильным назначением лечения.
Объект исследования: вирусы и бактерии.
Подбор информации в интернете и в литературе.
Изучение собранных данных.
Анализ собранных данных.
Изучение вредных микроорганизмов.
Для того, чтобы мы начали разговор о главных возбудителях инфекционных заболеваний, стоит вначале сказать о том, что представляют из себя сами инфекционные заболевания. Итак, инфекционные болезни – это болезни, вызванные проникновением в организм вредных микроорганизмов, т.е. заражением . Вот об этих микроорганизмах и пойдет речь.
Начнем с вирусов. Вирусы – это неклеточные формы жизни, которые оживают только при контакте с живой клеткой. В переводе с латинского virus означает "яд, ядовитое начало". Вирус представляет собой микроскопическую частицу, состоящую из генетического вещества (молекул ДНК или РНК), которое окружено защитным слоем белка .
Так выглядит вирус под микроскопом.

Вне живого организма, вне клетки вирусы совершенно безобидны. Они не проявляют никаких признаков жизни: не питаются, не размножаются и не двигаются.
Его нельзя увидеть не только простым глазом, но и в очень сильный микроскоп. Некоторые под микроскопом выглядят как пауки, другие – как колючие мячики .
Попадая в здоровую клетку, вирус начинает быстро размножаться внутри нее и разрушает ее, а выброс вирусов из поврежденных клеток вызывает заболевание. Организм превращается в своеобразный завод по производству вирусов.
Вирусы поражают все типы организмов: человека, животных, растения. По предположениям учёных, существуют миллионы их видов. Вирусы являются самой многочисленной биологической формой. Изучением вирусов занимается наука вирусология , раздел микробиологии. Вирусы по своей сути – это паразиты , они могут жить и размножаться только в живых клетках. В чистом виде они существуют в форме кристаллов. По размеру вирусы гораздо меньше клеток и проще их по строению.
Бактерия — это самостоятельный, живой микроорганизм, состоящий из одной клетки. В среднем размер бактерии составляет около 0,001 мм в диаметре. Некоторые из них настолько малы, что их даже невозможно разглядеть в обычный микроскоп. Большинство бактерий бесцветно. Только немногие окрашены в пурпурный или в зелёный цвет.
Так выглядит бактерия под микроскопом.

Бактерии переносят низкие и высокие температуры и могут жить в самых экстремальных условиях. Например, единственные организмы, обнаруженные в Мертвом море, — это именно бактерии. В помещении в каждом кубометре воздуха содержится до 1 млн. бактерий.
Первые бактерии появились, вероятно, более 3,5 млрд лет назад и на протяжении почти миллиарда лет были единственными живыми существами на нашей планете.



Изогнутая в виде запятой


Бактерии отличаются по форме, в таблице мы привели основные
Размножение бактерий совершается путем деления ; каждая клетка получает поперечную перегородку и затем распадается на две новые. При благоприятных условиях это происходит очень быстро. И если ничего этому не мешает, одна бактерия может заполнить своим потомством громаднейшие пространства. Размножение продолжается до тех пор, пока есть питание.

Бактерии обитают везде: в почве, воздухе и даже в нашем организме. Большинство из них не причиняет вреда.
Полезные свойства бактерий:
Бактерии защищают наш организм.
Бактерии, вызывающие гниение мертвых растений и животных, разлагают мертвые ткани на простые соединения, без них земля покрылась бы бесполезным мертвым веществом, и не осталось бы места для живого.
Другие бактерии вызывают ферментацию. Сюда можно отнести скисание молока (кефир, йогурт и т.д.), брожение сладких фруктовых соков (вино), созревание сливок (сливочное масло), изготовление сыров.
Растения не могут жить без бактерий, которые соединяют азот с другими элементами, чтобы получать нитраты, используемые растениями.
Но есть и такие бактерии, которые могут вызывать болезни, их называют патогенами . Патогены проникают в организм с капельками влаги в воздухе, который мы вдыхаем, через порезы и царапины на коже, с пищей и питьевой водой. В теле болезнетворные бактерии питаются, размножаются и выделяют токсины, разрушающие клетки. Именно токсины вызывают у больного болезненные симптомы.
Определим сходства и различия наших микроорганизмов, а также болезней, которые они вызывают.

И вирусы, и бактерии не видны невооруженным глазом, хотя бактерии во много раз больше вирусов.
Бактерии иногда могут быть как полезными, а вирусы всегда вредные.
Бактерии могут размножаться самостоятельно, а вирусы – нет.
Бактерии имеют собственную клеточную структуру, а вирусы – нет.
Распространяются вирусы и бактерии примерно одинаково:
— воздушно-капельным путем: при кашле или чихании,
— с кожи на кожу: при прикосновениях и рукопожатиях,
— с кожи на продукты: при прикосновениях к пище грязными руками вирусы и бактерии могут попасть в кишечник ,
— через жидкости организма: кровь и слюну.
Некоторые болезни, вызываемые вирусами и бактериями, имеют схожие симптомы. А вот лечение бактериальных и вирусных заболеваний разное .
Основные подходы к лечению.
Вирусы и антибиотики? Антибиотики не действуют на вирусные инфекции . Эти лекарственные препараты можно использовать только для борьбы с вредными бактериями. Если болезнь, вызванную вирусом, лечить антибиотиком, т.е. применять его не по делу, то в человеческом организме возникнет привыкание к этому виду лекарств . А когда случится болезнь, требующая лечения этим самым антибиотиком, то он не поможет, потому что бактерии, живущие в организме человека, уже привыкли к этому лекарству и не боятся его. Лекарство не подействует, болезнь станет неизлечимой, и человек может погибнуть. Вот об этом и говорил ученый. Сейчас очень часто люди, схватив обычную простуду, глотают таблетки, не разбираясь в них. Антибиотики – очень сильное лекарство, мощное оружие. Только применять их надо грамотно.
Вывод. В ходе исследований я теоретически подтвердила свою гипотезу, что при грамотной диагностике и правильном лечении риск вымирания людей при развитии устойчивости к антибиотикам можно свести к минимуму.
Мастерок.жж.рф
Бывает, заболев ОРВИ или гриппом, люди спешат в аптеку за антибиотиком, не отдавая себе отчета в том, что вирусное заболевание им вылечить невозможно. Ведь антибиотик — лекарство, направленное на подавление болезнетворных бактерий, но никак не вирусов. От последних могут помочь только противовирусные препараты.
Бактерии и вирусы — это микроскопические организмы, которые могут вызывать заболевания, как у людей, так и у животных или растений. Хотя бактерии и вирусы могут иметь некоторые общие характеристики, они также очень разные. Бактерии обычно намного больше, чем вирусы, и их можно рассмотреть при помощи обычного микроскопа. Вирусы примерно в 1000 раз меньше бактерий и видны только под электронным микроскопом. Бактерии являются одноклеточными организмами, которые размножаются независимо от других организмов. Вирусы нуждаются в помощи живой клетки для воспроизведения.
Примечательно, что вирус имеет гораздо меньшие размеры, чем бактерии. Потому они и способны проходить через антибактериальный фильтр. Размер вируса варьирует от нескольких десятков до трёхсот нанометров. Они недоступны для микроскопического исследования через световое оборудование. Именно это долгое время не позволяло их обнаружить даже при исследовании тканей заражённых организмов.
Проникая в клетки вирусы, начинают свою пагубную деятельность. Иммунная система человека вырабатывает антитела, которые отправляются на поиски злобного паразита. Только вот ни антитела, ни лейкоциты из-за своих огромных размеров не могут проникать сквозь мембрану оболочек человеческих клеток. Обычно соединительная ткань, где находятся микробы, хорошо омывается кровью, а присутствие в организме ее насыщенной антибиотиком помогает мгновенно справляться с ними.
Вирусы проникают в клетку живого организма или бактерию и заставляют органоиды (рибосомы) клетки синтезировать вирусные белки, из которых потом собираются множественные копии вируса. При выходе вирусов из клетки чаще всего происходит её гибель. Новые вирусы с большой скоростью захватывают другие клетки. Так вирус заставляет организм работать на себя. Так, собственно, и прогрессирует инфекция.
Вирус либо разрушает клетку хозяина, либо провоцируют ответ иммунной системы, который проявляется такими симптомами, как чувство усталости, повышение температуры и даже тяжелое повреждение тканей.
Если визуально представить себе огромный дом в 20-25 этажей, то маленькая, упавшая с подоконника коробка спичек это соотношение размеров микроба и вируса. Потому им легко паразитировать, функционировать, питаясь цитоплазмой, при этом, не повреждая внешние ее клетки. Некоторые даже используют в свою пищу микробов, подобные вирусы еще называют фагоцитами.
Иммунная система, как и многие другие физиологические системы, состоит из молекул, клеток, тканей и органов. Главный орган иммунной системы — это вилочковая железа, или тимус — орган, который находится за грудиной и производит особые клетки, самые главные клетки иммунной системы.
— По сути это клетки-регуляторы и клетки-солдаты, и эта армия стоит на защите нашего организма. Но к встрече с вирусом ее нужно готовить. На формирование иммунитета уходит от двух недель до трёх месяцев после прививки. Поэтому ее лучше делать не накануне, а до предположительного времени эпидемии.
Клетки вакцинированного человека подготовлены и научены бороться с вирусом в отличие от клеток невакцинированного. Они выделяют антитела, которые блокируют вирус. Профилированная клетка знает, какие частички нужно выработать, чтобы заблокировать конкретный вирус. Поэтому организм нужно готовить к возможной встрече с вирусом — иммунизировать вакциной, содержащей антигены.
Таким образом, строение вируса предполагает паразитический образ жизни, который необходим микроорганизмам для защиты от окружающей среды. Хотя вирусы достаточно свободно передвигаются в пространстве от одного хозяина к другому. Поэтому они создают высокий риск эпидемий тех заболеваний, где вирусы выступают возбудителем.
Вирус табачной мозаики поражает не только растения табака, но и плодовую мушку, которая им питается. Таким образом, продлевая жизнь мушки и её плодовитость (принося пользу), вирус вредит растениям;
Вирус, поражающий грибок, который размножается в траве возле геотермальных источников, позволяет растению выживать в условиях повышенной температуры. Это выгодно вирусному организму для сохранения хозяина в труднодоступных для истребления местах, где температура достигает 50 градусов по Цельсию;
Некоторые вирусы защищают организм хозяина от проникновения и размножения в организме других вирусных агентов. Вирус охраняет свою территорию и в некоторых случаях не приносит значительного вреда хозяину для сохранения места проживания.
Интересно, что с течением времени такие вирусы становятся не столько паразитами, сколько частью самого организма. Поэтому он начинает передаваться из поколения в поколение и определяется генетическим кодом, как полезное свойство, которое подлежит передаче. Таким образом, вирус сохраняет свое место и наделяет организм хозяина новыми свойствами для выживания.
Передаваться вирусы могут также от больных животных. Часто причиной становится употребление заражённого мяса или тесный контакт с заражёнными особями. Хотя существуют и вирусы, которые не способны передаваться между видами. Такие микроорганизмы для человека и других животных относительно безопасны. Чаще всего человек заражается, употребляя мясо крупного рогатого скота и домашней птицы. Но известны вирусы, которые разносятся дикими животными, например, голубями. Кроме того, при укусах заражённых млекопитающих передаётся вирус бешенства и другие.
Человек может передавать вирусную инфекцию разными путями. В зависимости от локализации возбудителя и особенностей заболевания выделяются следующие пути передачи от человека к человеку:
Воздушно-капельный. Такой вариант передачи присущ в основном вирусам, поражающим дыхательную систему. Вирус витает в воздухе и передаётся потенциальному хозяину в момент вдыхания заражённых воздушных масс;
Половой. Многие вирусы локализуются на слизистых оболочках, затем поражая весь организм. Нередко такие паразиты попадают в организм здорового человека при половом контакте. При этом даже использование презерватива не всегда может защитить от заражения. Влажные поцелуи также могут стать причиной заражения;
Гематогенный. Это происходит в процессе переливания заражённой крови. Чаще всего такое бывает при экстренном переливании, когда кровь не проходит должной проверки с обязательным периодом хранения;
Бытовой. В некоторых случаях вирус может передаваться через личные вещи или попадание на повреждённую кожу заражённых выделений организма больного. Таким путём может передаваться ряд вирусных гепатитов и СПИД, хотя и считается, что вероятность заражения в этом случае относительно низкая.
Некоторые вирусы требуют также хирургического вмешательства для устранения очага инфекции. В частности, представителей контагиозного моллюска или папилломатозные образования (ВПЧ) необходимо удалять хирургическим путём. После удаления проводят иммуномодулирующую терапию, которая направлена на восстановление защитных функций организма. Любой вирус опасен тем, что вызывает подавление иммунной системы, подвергая организм опасности заражения любыми заболеваниями. Особенно этим отличается ВИЧ. Поэтому с ним так сложно бороться и поддерживать жизнеспособность пациента.
Вирусы окружают нас и могут проникать в наш организм. Становясь паразитами, они начинают отбирать ресурсы человеческого организма и медленно убивать нас. Поэтому важно соблюдать меры предосторожности и своевременно проходить вакцинацию. Особенно это важно для тех, кто по профессии много контактирует с людьми, которые могут быть заражены какими-либо вирусами.
В связи с возможностью передачи вируса даже по воздуху или через слизистые оболочки следует укреплять свое здоровье и избегать сомнительных контактов. Беспорядочные половые связи и тесное взаимодействие с больным человеком может привести к заражению. При этом человек может даже не знать о том, что имеет заболевание, и вести самый обычный образ жизни. Поэтому лучше всегда быть осторожными в общении, а также заботиться о себе и своих близких.
Вирус быстро размножается, поедая цитоплазму клеток, вскоре ему становится мало полученного, и он пробивает оболочку клетки, сразу атаковывается антителами. Но если иммунитет упал, то медикаментозное воздействие может рекомендовать врач, например использование иммуноглобулина. Тогда кровью с активными веществами вирус убивать проще, тем более, когда ни уже остались незащищенными и вышли из человеческих клеток. С успехом используются в антивирусной терапии ацикловир, вирамун, эпивир, ремантадин и другие препараты. Именно по этой причини вирусы бесполезно лечить антибактериальной терапией.
Но вся сложность состоит в том, что более девяноста процентов вирусов в человеческом организме находится именно в клетках, а там их не убить и не достать. То есть, по сути, лекарствами их не убить, а пока синтезируются антитела и глобулины внутри организма, особенно если у человека слабый иммунитет пройдет много времени. А за этот период вирус может нанести достаточно вреда организму. Ученых тревожит незащищенность нашего тела от вирусной природы заболеваний.
Бактерии: бактерии являются прокариотическими клетками, которые показывают все характеристики живых организмов. Бактериальные клетки содержат органеллы и ДНК, которые погружены в цитоплазму и окружены клеточной стенкой. Эти органеллы выполняют жизненно важные функции, позволяющие бактериям получать энергию из окружающей среды и воспроизводится.
Вирусы: Вирусы не считаются клетками, а существуют как частицы нуклеиновой кислоты (ДНК или РНК), заключенные в оболочку белка. Также известные как вирионы, вирусные частицы существуют где-то между живыми и неживыми организмами. Хотя они содержат генетический материал, они не имеют клеточной стенки или органелл, необходимых для производства и воспроизводства энергии. Вирусы полагаются исключительно на клетку-хозяина для репликации.
В то время как большинство бактерий безвредны, а некоторые даже полезны для людей, другие бактерии способны вызывать заболевания. Патогенные бактерии, которые вызывают заболевание, продуцируют токсины, разрушающие клетки организма. Они могут вызывать пищевое отравление и другие серьезные заболевания, включая менингит, пневмонию и туберкулез.
Бактериальные инфекции можно лечить антибиотиками, которые очень эффективны при уничтожении бактерий. Однако из-за чрезмерного использования антибиотиков бактерии получили сопротивление к ним. Некоторые из них даже стали известны как супербактерии, поскольку получили устойчивость к множеству современных антибиотиков. Вакцины также полезны для предотвращения распространения бактериальных заболеваний. Лучший способ защитить себя от бактерий и других микробов — это правильно и часто мыть руки.
Вирусы являются патогенами, которые вызывают ряд заболеваний, включая ветрянку, грипп, бешенство, Эбола, болезнь Зика и ВИЧ/СПИД. Вирусы способны вызывать постоянные инфекции, в которых они находятся в состоянии покоя, и могут быть повторно активированы позднее. Некоторые вирусы вызывают изменения в клетках-хозяевах, которые приводят к развитию рака. Известно, что эти вирусы вызывают раковые заболевания, такие как рак печени, рак шейки матки и лимфома Беркитта. Антибиотики не работают против вирусов. Лечение вирусных инфекций обычно связано с лекарствами, которые лечат симптомы инфекции, а не сам вирус. Как правило, иммунная система самостоятельно борется с вирусами. Вакцины также могут использоваться для предотвращения некоторых вирусных инфекций.
Лекарств от вирусной инфекции не существует? На самом деле, они есть. Большинство противовирусных препаратов действуют по одному из трех механизмов.
Второй – нарушение структуры новых вирусных частиц. Подобного рода лекарственные препараты представляют собой измененные аналоги азотистых оснований, служащих материалом для синтеза нуклеиновых кислот. Из-за структурного сходства они встраиваются в ДНК или РНК размножающегося в клетках вируса, делая новые вирусные частицы дефектными, неспособными к поражению новых клеток. Пример такого препарата – ацикловир, применяющийся для лечения герпетических инфекций.
Третий механизм – не допустить попадание вируса в клетку. Лекарство препятствуют отсоединению вирусной ДНК или РНК от белковой оболочки, из-за чего генетический материал вируса теряет способность проникать сквозь клеточную мембрану. Так действует, например, ремантадин.
Все вышеперечисленные препараты действуют только на активно размножающиеся вирусы.
Читайте также:


